R, И.
-бромкетоном общей формуль; В С-СИ-Еf
il
...
в среде органичесаого раствоэитгз,,я, в йрисутстзии акцептора нротона, с зыдепе, нием целевого продукта в свободпэм ЗИДР или S ввде соли.
В качестве органического раст.зопито- ля предпочтительно применяю х.чсвг(Ьс1ргЛг клористый метилен и ацетои ггрил,
В качестве акцепторов протона цп; связывания бромистого водарода тлзЕплекк--ют триатиламин или берут ивбытои; ijcjfo.ru-,кого амииа формулы f 2f AMmio-&, 2, -тиаэолин моясно ьвсдкть в в виде свобод 1ого основания или
в БВДе СОЛЛ с хлористоводородной И.Но. 6pO--j
мкстоводородной 1Шспотами,
Цепевые продукты выделяют в свобод поы Виде или в анде солей с кислотамИ; например, с хлористоводородной кжяотой.
Пример 1. 2s3«flHriiu.po -3s6™( бис. П- метоксвфенил) цмидазо 2,1- tl азол
В колб с магнитной мешалкой и бар-ботйжем азота помегцают 69.7 гСОЛ.) к Л -броьддезоксианкзоина к Ю WK ,,„ хлороформа. К полученному растз;-:ру пии-. .швают нагретый до 2, ™30®С отц;и;гьгро« ванный 46f5 г (0,356 мг.леп) 2«-ймино-, иааолииа в 90 мл хлоооформа. Реакцию проводят нрпк.ом1атнсн теиггерат ре в токе ааста Ё течение Б, о час. Нерастворимый остаток бром.:г-и/1рата -амянз- .42. - Тиазол1ш0. отфильтрсвывают н прз.гывают кдороформом. Хлорафорыны5( растЕср кр&мыБШОт 6 X 50 MIL аодыс ЗО мл ,.яод&2 с Н-)ч;.к.олькими каплями уксус;ипй кнслоты., 2х5О Ш1 водьь -50 мл воды с :;лым натрием и 2 х SO KJJ; БОДЫ до йейт зальной реакху н
Хлсроф р;4нь е растворы высушцвгжп- . над беааодкк « сернок}шль5м натрносл фкньр- руют, расувяритвль отгоняют и колу скнс е масло вкдержизают в течение аочи прг: комнатной температуре.
Частично закристаллйэйровааше)еся яо растворяют npi-s кипении в ISO мл кола и выдерживают в течение чаевд ртго. ,няют лшикий cnsipT и после начала 1фкстал«. лизаций продукт помещают на 4 часа в
HOJia о iJpoc:Ti:iM Ефкпп...; 50 мл/БО мп. AipLiyvj.- Jib;c vjiiHBaioi ь fia,;;:vyivio зйтс;-д aacv .-: ..( (;;Т;:.ПМ),,.;. : liODBDOW
l/i;p.j--.:.;
ггф--ей ф;-.1: грО М1Т1то,, V,;i.-r;j ;. :; ifr/jE Х.О..ЛИПС i ;1::lTG i ( ; MjJ vjvbOrjyiOT.
upDiv:;biBt O DjjiaHvaefJrifciM aii roirujpJrnoM, зысущи&тю E a ирнсутствтгк калий tipn ко1 -|-штн1Л1 температуре; a ззтег
ори. .
Пап;у а о- 1..1 г телейого i;ir,T; ;-;v,
Т v-nr 1 --V/.
Калдепо. %; Г; (37..в4: П о.И/г К1 3, Сг9,Ба, C..jO.,, ft Выгислеяо, %° С в7.-о-;-° И 5i36j
li ;J и м е jj 2. -V-Мс; -11Л-2;3-ч ИГйД ро- о б-лбис- ;-1 ХЛОр|ШНтш)-41кгт :дазо i liJTpHasoji
В ,1солбу} снабженг ую магнитцой меидад кой и барботироватшетл азотя зигру: --а:от г (0,02 моля) хлоргл цр лй У.-омк;10 5™мет5Уь Л2 « Тиоаола в 10 мл ;слапо форма и ирлбгг&ляют мл. {0,04 моля) н 6:38 г ( молг-:} сзС/ .--бро 1-пис.-,п-хлордслигсскСеи ола л 20 мл хлороформа.
; Получешый растьор кмеет желтозать к .цйет,. G iyi:;TH 5 мни наблюдают образова- шю 5ек.ч: осадка.. Размеилизанко продо..же ют .5 твивцйе часа, 0-::ап к фк-пьтрутот,: премыве-хз-- v оргфор:-,-0у:. ыс гиисагот в эакууме.
Из Ma:v;;4j ii :p чо янлэгпжм эфира янде ияют aonojiyiKieJibHDe количество депевого Тродуктр его -отмывают водой от содей трият и1 гли; а, BbicyiuimaiOT п вакяАПчае.сме nijiBSiOT о ратшЭ вь1Д;;лeuIlь;.{И кристалдамк :ii растворяют в 3.60 мл: этсиола. Спирт 1апа:тойпну отгоняют и .фнстая.гаоуюг прО дуКл онв-гкл а ири медлзниом охлаждении а в течение 0ыдер;;швают в холодильнике, Крксталяы отфкльтрозывают тфпмывают этанолом jv сушат Б saKj yivtev,
в-ыкод 2,35 1% Т. шг„
Ка:йдоки. % С 00,88;: К 3,77л N .«и S fis64| С 19s,27,.
ShnKoncHo, %: С он,а38| К З.ЭОбг М 7,754; Я 8,87:5| C:i .
П р и ы е р о., 2 -Ме7ил- ;1гЗ-длгвдро-6г6--( метоксифенил) имкдазо l,2 -ЬЗтиазпл ,
В колбе с Магниткой ме яалквй смешива .ют 3,05 г (0,02 моля) :-лпргидрета 5.ме тил а «мико« д2«гиааолнг 10 мл хяорО
(|юрма, 5,6 .4 (0,04 моля) тркэтиламина и добаБЛ51 от раствор 6,7 г (0,О2 моля) 0.--бром.дезок.сиаьйзол.ина в 20 мл хлороформа .
Реакционную .ассу размешивают в те- чение 5 час при ког.шатиой температуре, промываю 4x3 мл воды. Хлороформную фазу cyiiiar над сернокислым натром от,фильтровыЕ-ают осушнтель и отгоняют раст ворктель. Полученное масло растворяют в
4О мл этанола ноловину спирта отгоняют и полученный раствор выдерживают в холодильнике в течение ночи. Выпавшие кристаллы филгг,тр)тот5 промывают, в 5 мл этанола и сушат в вакууме. Д/ш очистки кркс таллы подвергают повторной перекристал- лизащп из 11 мл ацетонитр}ша. Выход 3,3 г. То пл. (в тр,убке) 147 148°С. Найдено, %: С 68,671 Н 5,59j .
М 7,83| S 8,89.
Вычислено, %: С 68,155j Н 5,7-20jN 7,948j S 9,097.
П р и hi е р 4 3 -метил 2,3 дигвдро 5j 6(бис-VI метоксифенил)Имндазо 2,1- 1)1гиазол .
В колбу с магнитной мешалкой и барботажем азота помещают 10 мл хлороформа, 5,6 мл (0,04 моля) триэтиламйна, SjOSr (0,О2 моля) хлорпвдрата 2 ам1ШО 4-метил- Д2 -тказолина и добавляют раствор 6,7 г (0,02 моля) Ы -бромдезоксианизоина в 25 мл хлороформа. Реайшонную массу
размешивают 5 час- под током азота при комнатн о и те мп ерат лз е.
Далее раствор промывают 5x6 мл во ды, органическую фазу высушивают над сернокислым натром и полностью отгоняют растворитель. -Полученное масло в течение ночи выдерживают в токе азота. Затрем его ра.ст.вор51ют при нагревании вбОмл этилацетата, нерастворимый осадок отде- ляют горячим фильтрованием и oTroj-шют растворитель до 20 мл. Продукт, кристаллизуют Б течение 3 час при комнатной температуре, фильтруют промывают мини-мальным количеством этилацетата и высушивают в вакууме в течение ночи. Вы- ход 1,7. Т. пл, (в трубке) 150-160°С.
Найдено, %: С 68,42; Н 5,72}. N .7,98; S 9,15.
Вычислено, %: С 68,155j Н 5,720; N 7,948; S 9,097.
Пример 5. 3-Метил-.2,3-дигидро 5,6(бис--П Хлорфешш)-им$щазо 2,1 t)
Реакцшо проводят аналогачно примеру
4. Т. ил. 218 219°С.
Пример 6, 2,3-Дигидро-6-дифенилнмидазо 2,1 Ь}1назол Реакцию проводят алалогищю npiR-iepy 1, Т. нл. 215-21бс.
При -м е р 7, 2,3 Диметил 2, пщро-5, П -метоксифеш1л)имидазо12,1.-Ь17казоп,
В колбу померцают 1,8 г хлоргидрата 2---а .ет-ил-д 2-атиа золина растворенного в 7,6% (0,010 молей) соды, 18 мл хлороформа и мл .0,02 моля -триэтиламйна. К ползче1щому раствору добавляют 3;35 г 0,О10 молей oL . дезоксианизоина.
PeaKUHOtjirjio массу размешивают 6 час при комнатной темпоратуре в токе ааота. Хлороформенну-о 4-- зу промывают 5x6 кш воды, высушивают и но.шюстью отгоняютрастворитель. Оставшееся масло раство-
tj
при нагревании в 13 мл этаиола- в течение часа. Так как продукт net кристаллизуется, спирт отгоняют, продукт растворяют-Б хлорис-.гом метилене. Очищают на колонке заполненной 50 г флоризила, элюнруя хлористым метиленом. Первые 75 М1 целевого ггродугета не содержа-г., затем из след пощлх: 12 фракщп отгоняют растворитель и масло, кото- рое затем кристаллизуют. Крис-галлы промывают простым э(риром и выдерживают npii -комьатной температуре -4 час и сушат в вакууме в прп :; тствии апгидрвда фосфорной кислоты при 50°С. Выход 0,7 5 г, Т. пл. ,
НаЯдено., %: С 68,75| Н 5,84j N 7,72; S8.62.
Вычислено: %: С 68,82} Н 6,05;
M7,64j S8,75.
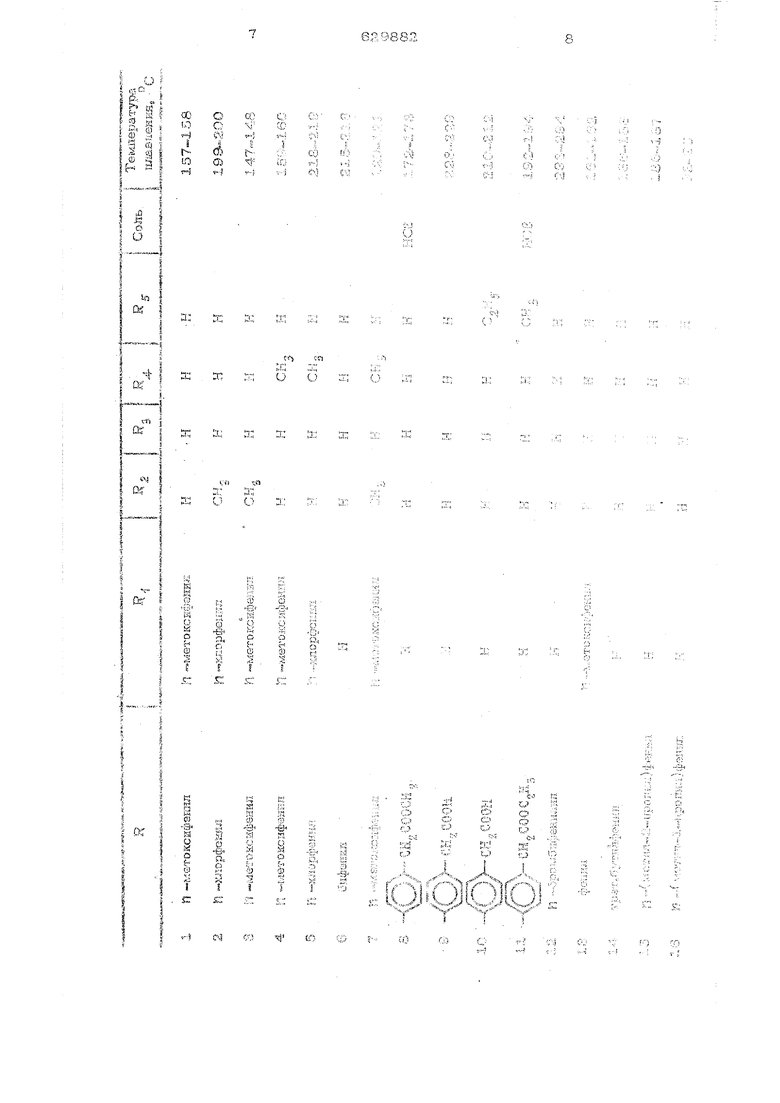
В таблице йряведелы характерзютикн сшдтеаированных с оединенийо о
W
6
h(
0.1
,.|




| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения 5-фенил-5-окси-2,3дигидро-5н-имидазо-/2,1-а/-изоиндолов | 1971 |
|
SU442598A1 |
| Способ получения хелатных макроциклических соединений металлов | 1973 |
|
SU450816A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 3-ОКСО-2,3-ДИГИДРОБЕНЗОКСАЗИНА-1,4 | 1971 |
|
SU321004A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 2,3-ДИГИДРО-5Н- ИМИДАЗО-[2,1-а]-ИЗОИНДОЛА | 1971 |
|
SU294333A1 |
| СПОСОБ ПОЛУЧЕНИЯ ТРИЦИКЛИЧЕСКИХ ПРОИЗВОДНЫХ | 1972 |
|
SU328586A1 |
| Способ получения (+) - ( )-энантиомера 3-12-/4-(8-фтор-10,11-дигидро-2метилдибензо тиепин-10-ил)-1-пиперазинил/-этил-2-оксазолидинова или его солей | 1977 |
|
SU633480A3 |
| ПРОИЗВОДНЫЕ ПИРАНОБЕНЗОКСАДИАЗОЛА ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ. | 1989 |
|
RU2054007C1 |
| Способ получения производных бициклических карбоновых кислот или их аддативных солей с кислотами | 1973 |
|
SU583749A3 |
| Способ получения производных аминокислоты | 1985 |
|
SU1468411A3 |
| Способ получения производных тиенодиазепина | 1971 |
|
SU492088A3 |

о
-Sfisi
м
о
о
а,
S-о
S
о
О г.-;
К 1Л,„. 11 и 3 о б р Формул а т 9 П Е 1, Способ получения производных 2аЗч -дигидроим1здазО 2,1- |з}тиазола обшей формулы J .в где А водород, галоген, алкоксигруп ш С. -Сд фенй тьнаПэ незамешенная ИХЕИ эамещенная группа, галогеном или китро группой; или радикал формулы Kg CR-C008,i где - водород ияй меткльная irpynna R-y - водород или ашшльная па с 1«.б атомагуш углерода| водород или группа, формулы галоген или алкоксигр птита 9 % 5 %™ одинако 5Ь или разгЕИчны могут быть водородом, алкйльныы радй« калом или фенилышгм радикалом; 629882 Я ве могут быть од Rgi 4 нэвр-емеико водородом, еспя R - фенил swiH гапоидфйнил или их сопей о т л и ч а ю ш. и и с я тем, что производные 2--«ам.ино--IB - гиазолина обшей формулы подвергают взаимодействию с оС « porviKeтоном общей формулы , в среде органического растворителя в прИ сут ;твии акцептора протонов, с выделением целевого продукта в свободлом виде или1 в виде солио 2. Способ по п. 1,-о т л и ч а ю - щ и и с а TeMj что в качестве орГаничес кого растворителя применяют .хлороформ, июристый метилен или ацет-онитр ш. Источники ш-хформации принятые во внимание при ежспертязе; 1, Мазур И. А. и др. Синтезы 2,3 дигвдро и 2s3,5s& TerpaiTtapo ipOK3BDflHfcw: кмидазо| 2Д |} j тиазала «. Хикй Фарм журн. 3(8), 1968, 11«Х5,
Авторы
Даты
1978-10-25—Публикация
1977-03-10—Подача