(Н2§В21 Н, Нз(-7 CH BiNHg етг где В, и В имеют указанные значен Пример. Тройной хлоргидраг N - 2(4-метил-5-имйдазолипмегилтио) -этил - N-{2-(4 метил-5-имидазолилметилтио)пропил гуанйдина. А. Раствор 14,8 г хлоргидрата 4-оксиметил-5 метилимидазола я 12,8 г хлоргидрата 2-.меркаптопропиламина в 1ОО мл 48%-ной водной бромистоводородной кислоты нагревают при температуре кипения с обратным холодильником в течение 6 ч, концентрируют и перекрис таллизовывают из смеси этанола и эфира для получения 30,0 г двойного бромгийрата 2(4 метил-5-.имидазолилметилтио) пропиламина, т, пл. 177-178 С. Б. Раствор 2,29 г N (5-метил-4-имидазолилметилтио)этил тиомочевины и 1,56 г Йодистого метила в 5 мл мета нола выдерживают при комнатной температуре в течение 18 ч, получая при BTO 2,3 г S -метил-М- 2-(5-метил-4-имид золнлметилтио) этил тйурониййодида, т. пл. 128-131 С, одид превращают в соответствующий сульфат ионным обменом на ионообменной смоле 1R А 4О1 в сульфатной форме. В, Раствор 4,0 г 2-(4-метил-4-имидазолилметилтио) пропиламина (из дигидробромида) и 3,35 г S -метил- N-J2 (4-метил-5-имидазолил)метилтио этил -тиуронийсульфата в 25 мл воды нагревают при температуре кипения с об ратным холодильником в течение 4 ч. Концентрированием, за которым следует очистка на ионообменной смоле Q50(H с эгаоированием 0,02 н- соляной кислотой, обработкой гидроокисью натния и пикролоновой кислотой получают 1,75 г тройного пикролоната N - 2- (4-метил 5-имидазолилметилтно)пропил} гуанйдин т. пл, 173-175 С, из водного диметилформамида. Найдено,%: С 46,9; Н 4,5; N21,9; &5,1. 8,60 имидазол - 2Н : синглет, и 3,94 имидазол - СНр : синглет. C,,H,,N,S, . еычислено,%: С 47,1; Н 4.4; N22,7S 5,5. Тройной пикролокаТ суспендируют в водном этаноле и обрабатывают соляной ислотой до образования соответствук ей тройной хлористоводородной соли, Найдено,%: СЕ 22,1; сЛг а-знсе. Еычислено,%: СЕ 21,7. П р и м е р 2, Тройной хлоргидрат Н , N-биc f2-.(4мeтил-5-имидaзoлилмeтилтиo)пpoпил}гyaнид raa. А. Раствор 13,0 г, 2-(4-метил-5-имидазолилметилтио) пропиламина (из дигидробромйда) в 50 мл этанола охлаждают до О С и перемешивают во время постепенного прикапывания 3,78 г бензоилиминодшслорметана. После прикапывания реакционную смесь оставляют стоять при комнатной температуре в течение 2 ч и нагревают на паровой бане в течение ЗО мин. Затем смесь сливают в воду и фильтрацией удаляют не рас творившееся вешество, рН фильтрата доводят до 9. Полученный сырой продукт очищают хроматографией на колонке с окисью алюминия, за которой следует хроматографическая очистка на колонке с скликагелем (хлороформ/метанол)и получают N -бензоил- N S N -бис- 2- {4-метил-5-имидазолилметилтио)пропил -гуанидин. Б. 3,2 г бензоильного соединения гндролизуют в 40 мл концентрированной соляной кислоты при температуре паровой бани в течение 5 ч. После охлаждения, разбавления водой и экстракции эфиром для удаления бензойной кислоты продукт очищают так же, как и в примере 1, и концентрируют до получения 1,35 г пикролоната т, пл. 230 С (разлагается ). Пикролонат растворяют в водном метаноле, очищают ионообменной смолой IF А 401 (С6 ) и подкисляют, соляной кислотой, чтобы получить тройной хлоргидрат N,N-бис- 2- (4 метил-5-имидазолилметилтио)пропйл гуанидина. ЯМР-спектр раствора в Л. О снят при 1ОО МГЦ и содержит следующие химические сдвиги: (2,0 протона на интегральной кривой, вычислено для 2,0 протонов), (4,4 протона на интегральной кривой,, вычислено для 4,0 протоноБ), , со
где В и Bg представляют собой шие алкипеновые группы, так что ил является (СН )2, а В- является
СНз -СН2-СН- м -(jH-dH -,
CHj
или В и B.g оба %1бирают из
-СНл-СН- ы СН-СНл-,. II
сн,
СН,
5
отличающийся тем, что динение обшей формулы
HjC-77Г H2$BiUH-
SA UffU
СН2$В,ЖН-(С .
HF.
v
где В и Bg имеют указанные значения;
А является низшим алкнпом, подвергают взаимодействию с соответ ствуюшим амином обшей фо лугал
Н,(-7
3 ЩУК нн ж
или
fijtJ-7 Y 5Н2 $BiKH2 3®НК К
где В и В имеют указанные зваченвя.
Источники ввформаовн, принятые во внимание при экспертизе:
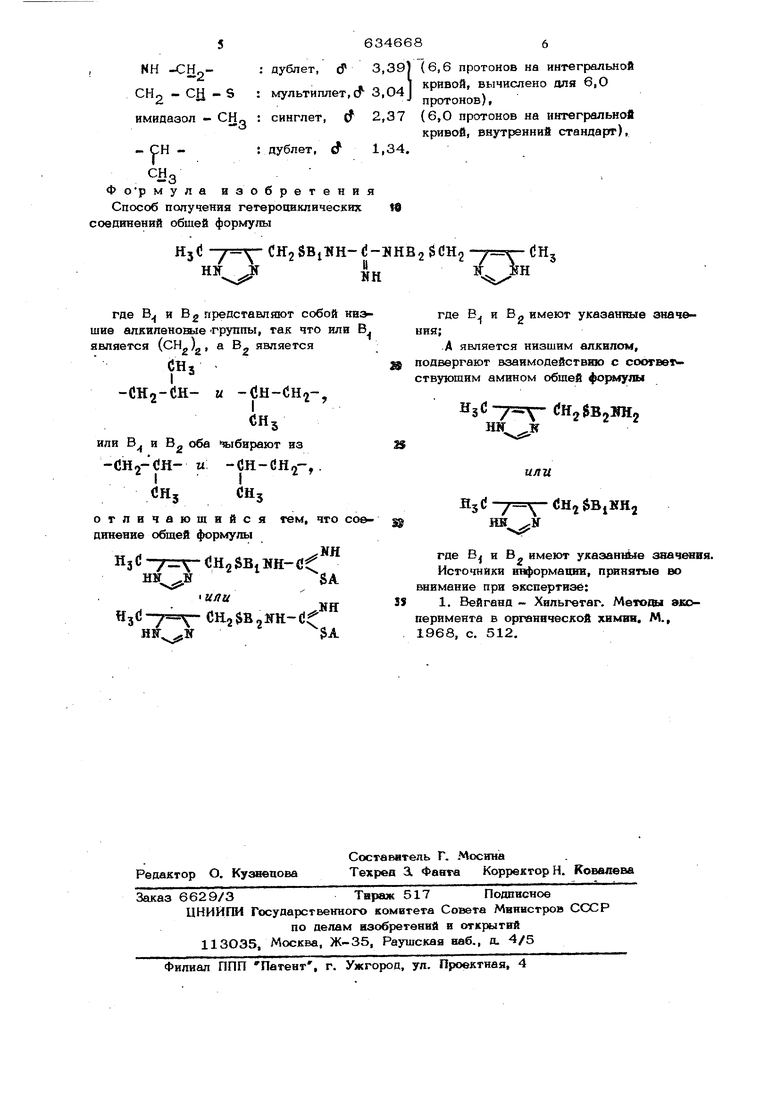
38 1, Вейганд - Хильгетаг. Метопы эксперимента в органической хнмвн. М., 1968, с. 512. NH -СНр-: дублет, (f 3,39 (6,6 протонов на интегральной ои /-и ел. о г-.1 кривой, вычислено апя 6,0 СНо - СН - S : мультиплет,сг 3,04 , J протонов), имидазол - СН„ : синглет, cf 2,37 {6,0 протонов на интегральной - СН -: дублет, d 1,34. СНо ор мула изобретения Способ получения гетероциклических t§ динений обшей формулы Hjd /- СНзSBi:NH-(-HHB2 сщ у- йн, -ь --V -11f ш кривой, внутренний стандаргг), Тн



Авторы
Даты
1978-11-25—Публикация
1976-11-11—Подача