Целевые продукты выделяют в свободном виде или в виде солей с металлами, такими как натрий, калий или кальций.
Исходные соедииеиия формулы И получают взаимодействием соответствующего беизоина с тиомочевиной в днметилформамиде или нагреванием 4,5-диарилимидазолов с серой.
Пример 1. 4,5-Днфенил-2-(2,2,2-трифторэтилтио)-нмидазол.
Смесь 4,5-днфенил-2-меркаптоимидазола 71,9 г (0,285 моль), 2,2,2-трифторэтилтрихлорметансульфовата 80,3 г (0,285 моль), триэтиламина 28,8 г (0,285 моль) и толуола (700 мл) нагревают с обратным холодильником в течение 4 ч в атмосфере азота. По охлажденин до комнатной температуры фильтрованием регенерируют 13,4 г 4,5-дифеиил - 2 - меркаитоимидазола. Фильтрат дважды промывают водой, охлаждают и получениые бесцветные кристаллы фильтруют. Выход 46,2 г (49%); т. пл. 185,5- 187°С.
Пайдено, %: С 61,28; Н 3,97; N 8,49.
С.уП.зРзМгЗ.
Вычислено, %: С 61,06; Н 3,92; N 8,38.
Пример 2. 4,5-Дифенил-2- (2,2,2-трифторэтилсульфонил) -имидазол.
К охлажденной в ледяной бане смеси 13,9 г (0,0416 моль) 4,5-дифеиил-2-(2,2,2трифторэтилтио)-имндазола и 75 мл хлороформа но каилям добавляют 85 мл 86,4%-ной .н-хлорнадбензойной кислоты. Смесь размешивают в теченне суток, нромывают насыщенным бикарбонатом иатрия, сушат сульфатом магния, растворитель отгоняют и получают 12,3 г сырого продукта. Перекристаллизацией из толуола выделяют 10,1 г (69%) соединения в форме бесцветных призм; т. пл. 198°С (с разложением).
Найдено, %: С 58,27; Н 3,76; N 8,10.
CiyHiaFsNsOS.
Вычислено, %: С 58,28; Н 3,74; N 8,00.
Пример 3. 4,5-Дифенил-2-(2,2,2-трифторэтилсульфонил) -имидазол.
В смесь 15,7 г (0,0470 моль) 4,5-дифеиил2 - (2,2,2 - трифторэтилтио) - имидазола и 100 мл хлороформа охлаждают па ледяной бане и но каплям добавляют 19,0 г (0,0952 моль) 86,4%-ной ж-хлорнадбеизойпой кислоты в 200 мл хлороформа. После размешивания реакционной массы в течеиие 4 дией при комиатной температуре добавляют тетрагидрофуран, промывают иасыщенным бикарбонатом натрия, сушат сульфатом магния. После отгонки растворителя иолучают 16,9 г сырого нродукта. После двух перекристаллизации из ацетонитрила выделяют 8,8 г соединения в виде бесцветных игл; т. ил. 228°С (с разложением).
Найдеио, %: С 56,18; Н 3,94; N7,45; F 15,44.
C,7H,3F3N202S.
Вычислено, %: С 56,18; П 3,94; N 7,45; F 15,44.
П р и м е р 4. 4,5-Бис- (4-метоксифенил) 2- (2,2,2-трифтор9тилтио) -имидазол.
Смесь 31,2 г (0,100 моль) 2-меркапто-1,5бис - (4 - метоксифеиил) - имидазола, 31,0 г (0,110 моль) 2,2,2-трифторэтилтрихлорметансульфоната, 11,1 г (0,110 моль) триэтиламнна и 300 мл толуола 6 ч нагревают с обратным холодильником в атмосфере азота. Смесь охлаждают, трижды промывают водой, сущат сульфатом магния и отгоияют растворитель. Выход 43,4 г сырого продукта. Очистку проводят хроматографированием на колонке, заполненную силикагелем, элюируют хлороформом. Полученные кристаллы перекристаллизовывают из метилциклогексаиа. Выход 21,5 г (55%) бесцветных кристаллов; т. нл. 119-120°С. Полиморфный вариант имеет т. пл. 150- 15ГС. Найдеио, %: С 57,96; Н 4,01; N 7,09.
CisH.yFsNzOzS.
Вычислено, %: С 57,86; Н 4,34; N 7,10.
Пример 5. 4,5-Бис-(4-метоксифенил)2 - (2,2,2 - трифторэтилсульфонил) - имидазол.
Аналогично оннсанному в иримере 4 нз 4,5-бис-(4-метоксифеиил)-2-(2,2,2 - трифторэтнлтио) - имидазола иолучакгг продукт. После пе)екристаллизации из водиого этанола выход (83%); т. пл. 193,5°С (с разложсиием).
Найдеио, %: С 55,52; Н 3,80; N 6,77.
Cl9Hi7F3N-:03S.
Вычислено, %; С 55,60; Н 4,18; N 6,83. Пример 6. 4,5-Бис-(4-метоксифенил)2-(2,2,2 - трифторэтилсульфоиил)-имидазол. В смесь 6,0 г (0,015 моль) 4,5-бис-(4-метоксифенил) - 2 - (2,2,2 - трифторэтилтио) имндазола в 75 мл хлороформа охлаждают в ледяной бане и по каплям добавляют раетвор 6,1 г (0,031 моль) 86,4%-пой .1 -хло 1иадбензойной кислоты в 75 мл хлороформа.
Реакцпоииую массу размешивают в течеине иочи, промывают насыщеиным бикарбоиатом натрия, сугиат над сульфатом магпия и отгоияют растворитель. Выход 7,1 г сырого продукта. Перекристаллизацией из 1-хлорбутана иолучают чистый продукт в виде бесцветных игл; т. нл. 173-174°С. Найдено, %: С 53,47; Н 4,06; N 6,55.
Ci9Hi7F3N2O4S.
Вычислено, %: С 53,51; Н 4,02; N 6,57. Пример 7. 4,5-Бис-(4-хлорфенил)-2(2,2,2-трифторэтилтио) -имидазол.
Смесь 32,1 г (0,Ш моль) 4,5-бис-(4хлорфенил)-2 - меркаптоимидазола, 28,1 г
(0,100 моль) 2,2,2-трифторэтилтрихлорметансульфоната, 5,9 г (0,109 моль) метилата
натрия и 300 мл этанола 3 ч нагревают с
обратным холодильником. Реакционную смесь выливают в воду, выиавший осадок фильтруют, иромывают водой и сушат. К иолучеииому твердому иродукту (43,9 г) добавляют 400 мл этилаиетата и ири размеш1тваиии выдерживают в течение суток. Полученный раствор отделяют от нерастворившихся иримесей фильтрованием, отгоияют растворитель и иолучают 15,1 г (37%) чистого соединения в виде бесиветных кристаллов; т. ил. 212-213°С.
Найдено, %: С 50,87; Н 3.05; N 6,69.
CivHi CbFsN S.
Вычислено, %: С 50,63; Н 2,75; N 6,95.
Пример 8. 4,5-Бис-(4-хлорфенил)-2(2,2,2-трифторэтилсульфонил)-имидазол.
Диалогично описаииому в иримере 2 из 4,5 - бис- (4 - хлопфенил) -2- (2,2,2 - трифторэтилтт1о)-имидазола. иолучают иазваииое соединение. Перекристаллизаштей сырого иродукта из аиетонитрила иолучают чистый нродукт (77%); т. ил. 214°С (с разложением) .
Найдено, %: С 48,97; Н 2.89; N 6,47.
Ci7H,,Cl,F,N,OS.
Вычислено, %: С 48,70; Н 2,64; N 6,68.
Пример 9. 4,5-Бис-(4-хлорфеиил)-2(2,2,2-тпифтооэтилсульфоиил)-нмидазол.
В смесь 5,3 г (0,013 моль) 4,5-бис(4-хлорфеиил) - 2-(2,2,2 - трифторэтилтио)имидазола и 50 мл хлороформа охлаждают на ледягтой бане и но каплям добавляют 5,3 г (0,027 моль) 86,4%-ной д/-хлориадбензойной кислоты в 60 мл хлороформа. После размешивания в течение ночи ирн комнатиой темиературе реакиионную массу 15 мин нагревают с обратным холодильииком, охлаждают, образовавшийся осадок фильтруют, нромывают холодным хлороформом, затем растворяют в смеси иростого эфира с тетрагидрофураном, нромывают иолучеиный раствор иасышенным бикарбонатом натрия. Органическую фазу сушат сульфатом магния и отгоняют растворитель с получением 5,8 г бесиветиого осадка, который нерекристаллизовывают из 125 мл нитрометана. Выход 4,1 г (72%) в виде бесиветных игл; т. пл. 24ГС (с разложением) .
Найдено, %: С 47,13; Н 2,67; N 6,56.
CyvHuCbFsNaOoS.
Вычислено, %: С 46,91; Н 2,55; N 6,44.
Пример 10. 2-Этилтио-4,5-бнс-(4-метоксифеннл) -имидазол.
Во взвесь 31,2 г (0,100 моль) 2-меркаито4,5 - бис - (4 - метоксифенил) - имидазола в 200 мл метанола добавляют метилат натрия 6,5 г (0,12 моль), смесь размешивают 15 мин и ио каилям добавляют раствор 17,1 г (0,11 моль) йодистого этила в 50 мл метанола. Реакционную массу нагревают с обратным холодильником 4,5 ч, размешивают в течение ночи ирн комнатиой температуре и выливают в воду. Выпавший твердый продукт фильтруют, промывают водой
Н сушат. Выход 33,0 г сырого продукта. Перекрнсталлизаиией из разбавленного этаиола иолучают 28-,8 г (85%) чистого названного иродукта; т. нл. 108-109°С. Найдено, %: С 66,96; Н 6,10; N 7,85.
CisHaoN.OoS.
Вычислеио, %: С 67,03; Н 5,92; N 8,23.
Пример 11. 2-Аллилтио-4,5-бис- (4-метоксифенил)-имидазол.
Смесь 31,2 г (0,100 моль) 2-меркаито4,5-бнс-(4-метокснфеннл)- имидазола, 13,1 г (0,108 моль) аллилбромида, 20,2 г (0,200 моль) триэтиламииа и 500 мл хлороформа нагревают в теченне суток с обратиым холодильником. Затем добавляют еше 4,8 г (0,040 моль) аллнлбромида, продолжая нагрев с обратным холодильником в течение 2 ч. Онерацию добавления аллнлбромида и нагревание в течение 2 ч повторяют дважды. Прозрачный раствор охлаждают, трижды нромывают водой, сушат сульфатом магния и отгоняют растворитель. Остаток растирают с простым эфиром, твердый продукт собирают. Выход 31,5 г сырого . Перекристаллизацией из разбавленного этанола получают 26,7 г (76%) чнстого соединения; т. пл. 167-167,.
Найдено, %: С 67,22; Н 5,87; N 7,81. CsoH-r.NsO.S.
Вычислено, %: С 68,16; П 5,72; N 7,95.
Пример 12. 4,5-Бие-(4-метоксифеннл)2- (метнлтнометт лтно) -имидазол.
Диалогично описанному в примере 9, прнмеияя хлорметнлметилсульфид, нолучают продукт: т. пл. 171 - 172°С.
Найдено, %: С 61,32; Н 5,57; N 7,32.
CigHooNgOoSo.
Выч1 слено. %: С 61,26; Н 5.41; N 7,52.
Пример 13. 2-Этилсульфииил-4,5-бис(4-метоксифеиил)-нмидазол.
В раствор 10,2 г (0,0300 моль) 4,5-бнс(4-метоксифеннл)-имидазола в 200 мл дихлорметана охлаждают в ледяной бане и
ио каплям добавляют раствор 6,0 г (0,030 моль) 86,4%-ной лг-хлорнадбензойной кнслоты в 100 мл днхлорметана. После размешивания в течение суток ири комнатной темнературе реакционную смесь промьшают тремя порциями (75 мл) насыщенного бикарбоната натрия. Органическую фазу сушат сульфатом магния, растворитель отгоняют на роторном испарителе, оставшееся масло растирают с простым
эфиром, образовавшийся твердый продукт собирают и иерекристаллнзовывают из 500 мл 1-хлорбутана. Выход 7,5 г (70%); т. ил. 161 -162°С.
Найдено, %; С 63,98; Н 5,59; N 7,97.
CigHooNoOsS.
Вычислено, %: С 64,02; Н 5,66; N 7,86, Пример 14. 2-Этилсульфонил-4,5-бис(4-метоксифеннл) чмидазол.
Дналогнчно описанному в примере И, увеличивая количество 86,4%-ной л-хлор4,5-Диарил-2-(замеш,ейнь1е Тйо)-имидазолы
Y
8 Т а б .4 и ц а 1






| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производныхиМидАзОлА | 1978 |
|
SU803858A3 |
| Способ получения 1-замещенных-4,5-диарил-2/замещенный тио/ имидазолов,их сульфоксидов или сульфонов | 1978 |
|
SU867301A3 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ИМИДАЗОЛА1Изобретение относится к области получе- }!ия новых соединений, которые могут найти широкое применение в фармацевтической промышленности и обладают улучшенными свой- ства.ми но сравнению с соединениями нодоб- ного действия.Предложен способ получения новых производных имидазола общей формулы— Со <io—RI— Сн—гги-К. | 1973 |
|
SU392625A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ИМИДАЗОЛА | 1970 |
|
SU413677A3 |
| НNЗиг"'—"—-ы -1015где R2 и RS имеют указанные выше значения, конденсируют в присутствии окислителя, пр<едпочтительно органической соли меди, с избытком аммиака и альдегида общей формулыр с-^ ''"%!' | 1973 |
|
SU398040A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ИМИДАЗОЛА | 1973 |
|
SU404245A1 |
| СПОСОБ ПОЛУЧЕНИЯ БЕНЗОИЛФТОРАЛКИЛСУЛЬФОНАНИЛИДОВ | 1970 |
|
SU264253A1 |
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ ГУАНИДИНА | 1973 |
|
SU382280A1 |
| Диалкиламиды фталоцианинокта-4,5карбоновых кислот для получения оптических фильтров с поглощением в красной области спектра | 1977 |
|
SU740802A1 |
| Способ получения производных 1,1,2-трифенилпропена или их стереоизомеров,или смеси стереоизомеров,или их кислотно-аддитивных солей | 1980 |
|
SU1253426A3 |

надбензойной кислоты до 12,0 г (0,060 моль) получают после перекристаллизации из 125 мл 1-хлорбутана 6,0 г (54%) соединения; т. пл. 136-137°С. Найдено %: С 61,47; Н 5,47; N 7,35.
Cl9H2oN204S.
Вычислено, %: С 61,27; Н 5,41; N 7,52.
Пример 15. 4,5-Бис-(4Метоксифенил)2-метилтиоимидазол.
Заменяя в примере 8 йодистый этил на йодистый метил получают соединение; т. пл. 157-158,5°С.
Найдено, %: С 65,84; Н 5,53; N 8,46.
CigHisNsOsS.
Вычислено, %: С 66,23; Н 5,56; N 8,58.
Пример 16. 2-Ацетонилтио-4,5-бис- (4метоксифенил) -имидазол.
В размешиваемую смесь 31,2 г (0,100 моль) 2-меркапто-4,5-бис-(4 - метоксифенил)-имидазола, 11,0 г (0,11 моль) триэтиламина и 500 мл хлороформа по каплям добавляют 10,2 г хлорацетона в 50 мл хлороформа. Реакционную массу размешивают в течение суток при кипении, трижды промывают водой, сушат сульфатом магния и отгоняют растворитель. Выход 32,0 г сырого продукта. После хроматографической очистки (силикагель, хлороформ) получают 27,0 г (73%) чистого продукта; т. пл. 115-117,5°С.
Найдено, %: С 65,14; Н 5,42; N 7,36.
СгоНго гОзЗ,
Вычислено, %: С 65,20; Н 5,47; N 7,60.
Пример 17. 4,5-Бис-(4-метоксифенил)2-(метилтиометилсзльфонил) -имидазол и 4,5-бис-(4 - метоксифенил) - 2 - (метилсульфинилметилтио)-имидазол.
В раствор 7,4 г (0,020 моль) 4,5-бис-(4метоксифенил) - 2 - (метилтиометилтио) имидазола в 100 мл дихлорметана охлаждают на ледяной бане и добавляют 4,0 г (0,020 моль) 86,4%-ной ж-хлорнадбензойной кислоты в 100 мл дихлорметана. После размешивания в течение суток при комнатной температуре реакционную смесь трижды промывают насышенным раствором бикарбоната натрия, сушат сульфатом магния и отгоняют растворитель. Остаток (7,5 г) хроматографируют на колонке, заполненную силикагелем, элюируя смесью толуола с этилацетатом.
Первое элюируемое соединение (чистое) представляет собой 4,5-бис-(4-метоксифенил)-2 - (метилтиометилсульфинил)-имидазол, т. пл. 142,5-143,5°С.
Найдено, %; С 59,00; Н 5,13; N 6,93.
Cjg zo zOs zВычислено, %: С 58,74; Н 5,19; N 7,21.
Дополнительным элюированием получают чисты; 4,5-бис-(4-мстоксифенил)-2-(метилсульфипилметилтио) - имидазол; т. пл. 84,5-86,5°С.
Найдено, %.: С 58,85; Н 5,36; N 6,94.
CigHzoNgOsSa. 4,5-Диарил-2-(Г1олйгалогеналкилтио)-имидазолы
Вычислено, %: С 58,74; Н 5,19; N 7,21.
Пример 18. 4,5-Дифенил-2-(1,1,2,2-тетрафторэтилтио) -имидазол.
В трубку из нержавеющей стали помещают 0,5 мл 40%-1юго раствора гидроокиси бензилтриметиламмония в метаноле и прибавляют 5,0 г (0,020 моль) 2-меркаптоимидазола в 50 мл диметилформамида. После многократной продувки трубки сухим азотом вводят 2,2 г (0,022 моль) тетрафторэтилена и размещивают реакционную массу в течение 7 ч, затем выливают в воду, осадок фильтруют и промывают водой. Выход 5,7 г сырого продукта. Хроматографией на колонке (силикагель, хлороформ) получают 3,5 г чистого соединения; т. пл. 212-213°С.
Найдено, %: С 57,71; Н 3,70; N 7,89.
C,7Hi2F4N2S.
Вычислено, %: С 57,95; Н 3,43; N 7,95.
Пример 19. 4,5-Бис-(4-метоксифенил)Я-винилтиоимидазол.
В трубку из нержавеющей стали добавляют 15,0 г (0,05 моль) 4,5-бис-(метоксифенил)-меркаптоимидазола, 0,75 г хлористой
640662
10
Т а б л II ц п 2
г
,гсди и 100 мл диметилформамида. Трубку охлаждают, откачивают воздух и нагнетают 1,3 г ацетилена. Затем реакционную массу нагревают до 150°С и при встряхиваНИИ выдерживают 8 ч, охлаждают и удаляют газ. Содержимое трубки разбавляют 500 мл воды, добавляют 25 мл концентрированной гидроокиси аммония и водную смесь экстрагируют простым эфиром (4 раза по 300 мл). Соединенные эфирные экстракты еще раз промывают водой (ЗХ ХЗОО мл), сущат и отгоняют растворитель па роторном испарителе. Остаток хроматографируют на колонке, содержащей 600 г
силикагеля. Продукт элюируют хлороформом. Выход 2,9 г. После перекристаллизации пз 1-хлорбутана - гексана получают 2,8 г чистого продукта; т. пл. 114-115°С. Найдено, %: С 67,17; Н 5,40; N 8,42.
CioHiijNsOaS.
Вычислено. %: С 67,43; Н 5,36; N 8,28.
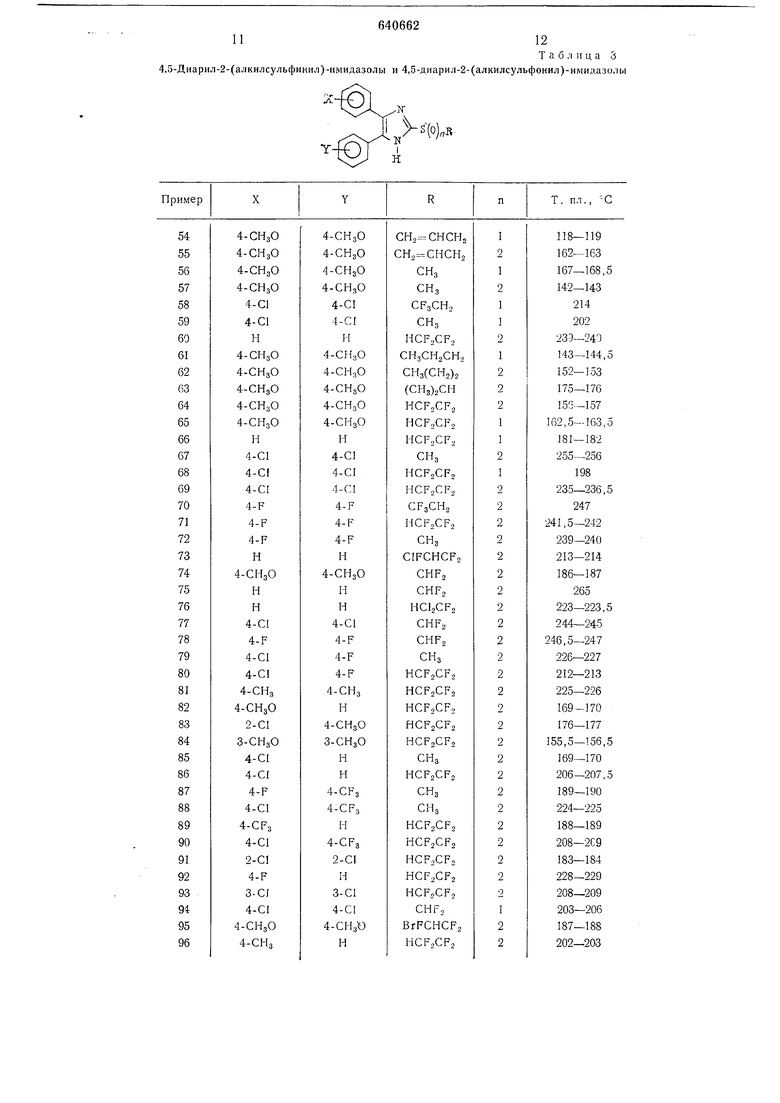
Пример 20. Натриевая соль 4,5-бис(4 - фторфенил)-2 - (1,1,2,2 - тетрафторэтилсульфонил) -имидазола. 4.5-Диарил-2-(алкилсульфинил)-имидазолы таблица 3 и 4,5-диарил-2-(алкилсульфонил)-имидазолы
1Л
Смесь 5,0 (0,0119 моль) 4,5-бис-(4-фторфенил) -2- (1,1,2,2 - тетрафторэтилсульфонил)-имидазола, 0,6 г (0,0111 моль) метилата натрия и 300 мл простого эфира сутки размешивают при комнатной температуре. Выделившийся осадок промывают простым эфпром. Выход 4,1 г натриевой соли; т. пл. 290-292°С.
Майдеио, %: С 45,98; Н 2,19; N 6,07.
CiyHgFgNaOsSNa.
Вычислено, %: С 46,16; Н 2,05; N 6,33.
Пример 21. Натриевая соль 4,5-дифеиил-2 - (1,1,2,2 - тетрафторэтилсульфонил) 1мидазола.
Применяя описанный в примере 22 способ, из 4,5-дифенил-2-(1,1,2,2-тетрафторэтилсульфонил)-имидазола получают соединение; т. пл. 296-302°С (с разложением) .
П р и м е р 22. 4,5 - Бис- (4-оксифенил) -2(1,1,2,2 - тетрафторэтилсульфонил) - имидазол.
Смесь 4,5-бис-(4-трет - бутоксифенил) - 2(1,1,2,2 - тетрафторэтилсульфонил) - имидазола и трифторуксусной кислоты переме14
Продолжение
в течение суток при комнатной температуре. Реакщюнную смесь выливают в воду и после обработки получают названное соединение.
Пример 23. 4,5 - Бис - (4 - ацетоксифен11л)-2-(1,1,2.2 - тетрафторэтплсульфонил) мндазол.
Смесь 4,5 - бис-(4 - оксифенил) - 2-(1,1,2,2тетрафторэтилсульфонил) - имндазола
(0,1 моль), ангидрида уксусной кислоты (0,2 моль) и 500 мл ниридина 2 ч нагревают Н. водяной кипящей бане. Смесь выливают в воду и иолучают соединение.
Применяя соответствующие исходные
продукты и используя способ, описанный в примере 10, иолучают соединения, приведенные в табл. 1, или соответствующие исходные иродукты и способ примера 18 получают соединения, приведенные в табл. 2.
Типичнымн пригодными катализаторами являются диизопропиламин или гидроокись бензилтриметиламмония. Используя соответствующие исходные материалы и способ примеров 13 и 14, получают соединения,
данные в табл. 3, другие соединения сведены в табл. 4.
15
Y
16 Таблица
Авторы
Даты
1978-12-30—Публикация
1976-08-10—Подача