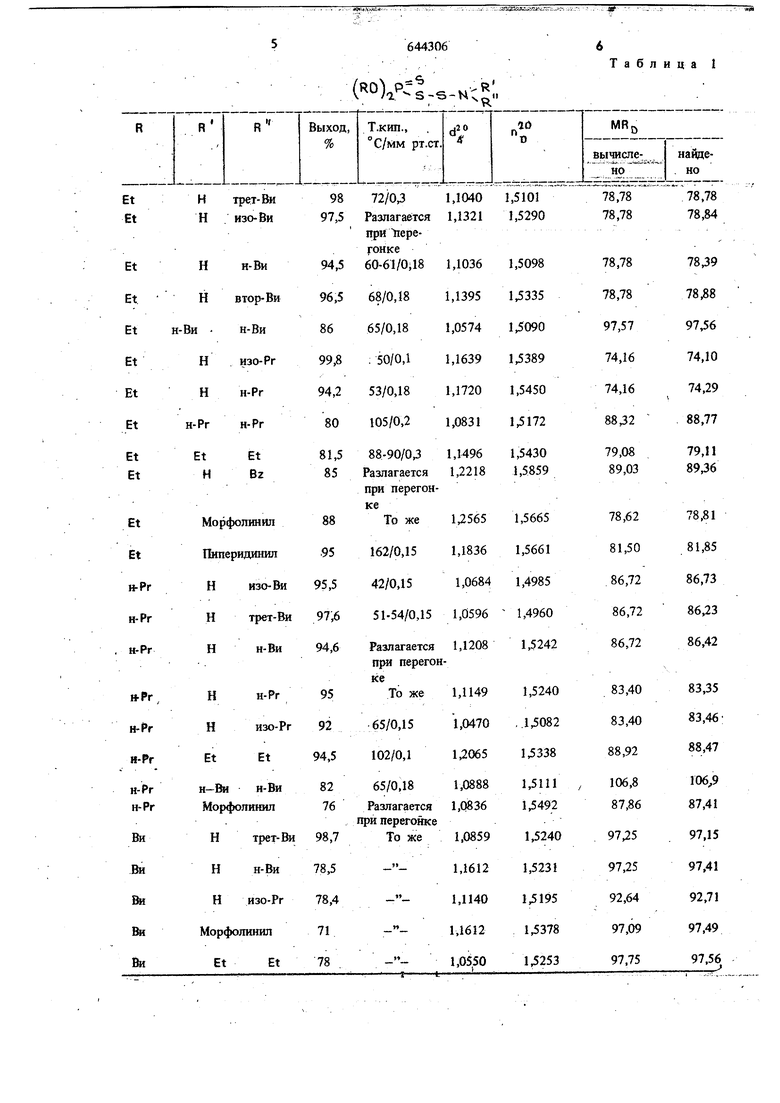
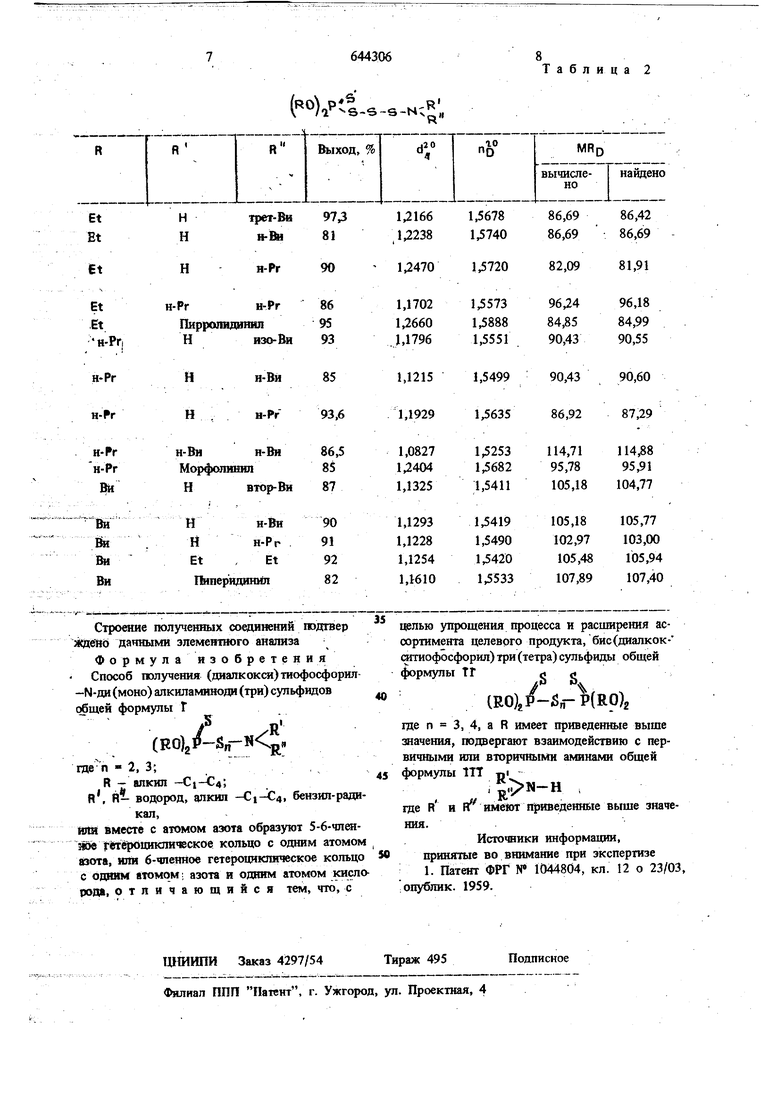
Изобретение относится к новому способу шлучения (даалкокси) тиофосфорил-М-ди(моно алкиламиноди (три)сульфидов общей формза1ы (RO)j,P-Sn-N L« где п 2, R - алкнл -Ci-C4; R, водород, алкил -Ci-t4, бензил-радикал, шш вместе с атомом азота 0.6 разуют 5-6-членное гетерощислическов кольцо с одним атомом азота, или 6-членное гетероциклическое кольцо с одним атомом азота и одним атом кислорода, которые могут использованы в качестве полупродукто для синтеза биологически активных BeiqecTB. Известен способ получения соединений общ формулы (Та)«, ( где Л 1, 2; R - апкил -С2-Сз, фенил; R- циклогексил, R - алкил -Cj , взаимодействием щёлошой или аммонийной соли соответствующей дитиофосфорной кислоты с Ы-диалкш1-8-галоидаминосульфидом в органическом растворителе 1. Выход целевого про-; дутста (60-80%) у Недостатком известного способа является использование в качестве исходного продукта диалкил-8-галоидаминосульфидов, которые получают либо хлорированием бис(диалкш амино) дисульфидов, либо взаимодействием бис(диалкиламино) сульфида с хлорангидридом бензойной кислоты, что усложняет процесс получения целевого гфодукта. К тому же зтот метод исключает синтез соединений общей формулы (f б) Sр(RO) где п 2; Я - апкил -€2-04; в - алкил так как М-моноалкил-З-галоидаминосульфиды, необходимые для этого синтеза в качестве исходного (ялрья, не выделены вследствие их нестабильности. Целью изобретения является упрощение процесса получения (даалкокси) тиофосфорил N-да (моно) алкипаминоди (три) сульфидов и расширение ассортимента целевого продукта. Поставленная цель достигается fr/тем использования дан получения (диалкокси) тиофосфо, реет- N- ди (моно) алкиламиноди (три) сульфидов новых, легко доступньтх исходггых соединений. Прздаагается новый способ получения (диалкокси) тиофосфорил- N-ди (моно) алкиламиноди (три) сульфидов общей формулы 1, который заключается во взаимодействии бис (диалкокси1Иофосфорил)три(тетра) сульфидов общей формулы ТГ //SОд (1го)гР-VPfRO), где п 3, 4, а R имеет приведенные выше зшчения, с йерйич11ыми или вторичными аминами общей формулы ТП N-H « ,,« где Нин имеют приведенные выше значения, гфи гсомнатной температуре. Выхот целевого продукта по описываемому способу 80-98%. Продукты по данным тонкослойной хроматографии не содержат примесей. В указанном способ исходаые бис (диалкокситиофосфорил) три(тетра) (удьфиды доступные соединения, их получают с колнчествеНнь1м выходом при взаимодейсгеии щелочных солей дитиофосфорных кислот с ди (моно) хлоридами серы. По данному способу получены, как известны (диаякркси) тиофосфорил-N-диалкиламино дисуль фиды общей формулы Т, где п 2; R, R , R Имеют прйвёденньте вьш1е значения, так и ранее неизвестнь1е (диалкокси) тиофосфорил-N-ди (моно алкиламинотрисульфиды общей формулы Г, где п 3, а также неизвестные (диалкокси)тиофос форил-М-моноалкнламинодисульфйды общей формулы (Г б), где п, R, R имеют приведенные выще значения. Пример 1. К раствору 4,02 г (0,01 М) бис(дизтокситиофосфорил)трисульфида S смеси абсолютный эфир:петролейный э4тр (1:1) при перемешивашш по каплям прибавляю раствор 1,5 г (0,02 М) третбутиламина в 5 мл петролейюго эфира. Выпавший осадок аммони еяой соли диэтоксидитиофосфорной кислотьГ отфильтровывают. Фильтрат промывают водой, сушат над MgSO4, эфир отгсдаяют. Получают 2,83 г (выход 95% от теоретического) бледно-желтого масла. Т. кип. 72°/0,3 ммрт.ст Найдено,%: Р 9,92; 10,18; S 32,72; 32,94; N5,15; 5,13; CgHjoOjfSsN 6 4 Вычислено,%: Р 10,65; S 33,24; N 4,84. Пример 2. Аналогично примеру 1 з 5,15 г (0,01 М) бис(дибугокситиофосфорил) рисульфида и 1,3 г (0,02 М) изопрошшамина олучают 2,6 г (78,4% от теоретического) (дибугокси)тиофосфорил-М-изопропнламино дисульфида. Разлагается при перегонке. Найдено,%; Р 9,19; S 29,01; 29,26; N 4,52; 4,30. СпНзбОгРЗзЫ Еычислено,%: Р 9,35; S 29,02; N4,23. П Р и М е Р 3. Аналогично примеру 1 из 4,02 г (0,01 М) бис(диэтокситнофосфорил) трисульфида II 3,2 т (0,02 М) дибутипамина получают 3,07 г (86% от теоретического) (диэтокси) гаофосфорил- N-дибутиламинодисульфида. Т. кип. 65°С/0,18 мм рт.ст. Найдено,%; Р 8,38; 8,74; S 27,27; 26,97; N 4,16; 4,19., CizHagOaPSaN. Вычислеио,%: Р 8,96; S 27,84; N 4,05. Пример 4. Аналогично примеру 1 из 4,5 г (0,01М) бис (диизопропокситиофосфорт) трисульфида и 1,9 г (0,02 М) морфолина получают 2,5 г (86% от теоретического) динзог юп6кситиофосфорил-М-морфоли«шдисульфида. Разлагается при перегонке. Найдено,%: Р 9,75; 9,74; S 30,69; N 4,15; 4,14. CioKjOsPSjN Вычисл гно,%: Р 9,35: S 29,02; N 4,23. Пример 5. Аналогично примеру 1 из 4,39 г (0,01 М) бис(диэтокситиофосфорил) тетрасульфида и 1,5 г (0,02 М) третбутиламина получают 2,4 г (97,8% от теоретического) (диэтокси) шофосфорнл- N- третбутнламинотрисулъфиДа. Разлагается при перегонке. Хроматогра фия дает одно пягно на силуфоле в системе ацетон: гексан (1:3). Найдено,%: Р 9,60; 9,50; 540,15; 39,92; N4,62; 4,44 CaH2o02PS4N Вычислено,%: Р 9,63; S 39,90; N 4,36. П Р и М е Р 6. Аналогично примеру 1 из 5,47 г (0,01 М) бис(дибутоксктиофосфорил) тетрасульфида и 1,78 г (0,02 М) пиперидина получают 3,3 г (85% от теоретического (дибутокси) тиофосфорилшперидиннлтрисульфида. Разлагается при перегонке. Хроматография дает одно пятно на снлуфоле в системе ацетон; гексан (1:3). Найдено,%: Р 8,18; 8,05; S 32,74; 32,75; N 3,68; 3,70. , С,зН280з84М Вычислено,%: Р 7,95; S 32,92; N 3,60. Аналогично полученные диалкокситиофосфорил- N-дн (моно) а} 1кяламнноди (три) сульфиды формулы Т приведены в табл. 1 н 2.
Ь
(.R
s-s-u
(.Ptle-e-N.S:
гЧ

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения фосфорсодержащих соединений | 1978 |
|
SU717059A1 |
| СПОСОБ ПОЛУЧЕНИЯ 1,4-БИС-[ДИАМИДО(ГИДРАЗИДО) ТИОФОСФОРИЛ]-БЕНЗОЛОВ | 1969 |
|
SU245769A1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,2-БИС-(ДИАЛКОКСИДИТИОФОСФОРИЛ-ЭТИЛ)-КЕТОНОВ | 1969 |
|
SU241435A1 |
| Способ получения S-этинильных эфиров тио- или дитиофосфорных кислот | 1981 |
|
SU992518A1 |
| О,О-Диалкил-S-дигалометилдитиофосфаты, обладающие фунгицидной активностью, и способ их получения | 1981 |
|
SU944314A1 |
| СПОСОБ ПОЛУЧЕНИЯ Ы,8-БИС-(ТИОФОСФОРИЛ)- р-МЕРКАПТОЭТИЛАМИНОВ | 1972 |
|
SU435245A1 |
| Способ получения S-триалкилстанниловых эфиров 0,0-диалкилдитиофосфорных кислот | 1990 |
|
SU1735299A1 |
| СПОСОБ ПОЛУЧЕНИЯ СОЛЕЙ 1,3-ДИМЕТИЛ-4,8-ДИАЛКОКСИ-6-R-ПИРРОЛО-(ТИЕНО)-[C] ТРОПИЛИЯ | 1997 |
|
RU2131871C1 |
| Способ получения производных моноили диацетиленовых арсинов дигидропирана, или -тиопирана, или -пиперидина | 1977 |
|
SU702028A1 |
| МОНО -3- (3,5-ДИ-ТРЕТ-БУТИЛФЕНИЛ) -ТИОПРОПИОНАТ -2,2-МЕТИЛЕН -БИС- (6-ТРЕТ-БУТИЛ-4-МЕТИЛФЕНОЛ) В КАЧЕСТВЕ СТАБИЛИЗАТОРА ДЛЯ КАУЧУКОВ СКИ-3 | 1993 |
|
RU2039738C1 |


Авторы
Даты
1980-06-15—Публикация
1976-11-01—Подача