Поставленная цель .достигается описываемым способом получения d-замешенных производных бензгидрола или их солей,состоящим в том, что бенэофенон обшей формулы II COCsHj П где имеют вышеприведенные значения, подвергают взаимодействию с этилили винилмагнийгалогенидом при температуре от -10 до в среде органического растворителя с последующим выделением соединений формулы I в свободном виде или в виде их солей. Технология способа состоит в следующем, Вензофенон общей формулы II подвергают взаимодействию с этилили винилмагнийгалогенидом, преимущественно с этилмагнийбромидом или этилмагнийиодидом соответств.енно винилмагнийбромидом или винилмагнийхлоридом, в присутствии безводного органического растворителя. Реактив Гриньяра используют ми-нимум в эквимолярном количестве. Реакцию целесообразно проводить в апротонном органическом растворителе, например в алициклических простых эфирах, таких как тетрагидрофуран или диоксан, в алифатических простых эфирах, таких как диметйловый эфир этиленгликоля, диэтиловый эфир, ди-н-бутиловый эфи D алифатических или ароматических углеводородах, таких как лигроин, бензол, толуол, ксилол, или в смесях перечисленных растворителей. Темпера тура реакции лежит между -10 и +100 По окончании реакции комплекс Гринья ра разлагают разбавленными минеральными кислотами, например, серной кис лотой или соляной кислотой, но более целесообразно водным раствором хлори да аммония, и Образующееся соединение обшей формулы I выделяют. Продук очищают дистилляцией или перекристал лизацией. Соединения общей формулы I в случае Необходимости превращают в соли с кислотами в четвертичные аммониевы соли. Реакцию выполняют в среде раст ворителя, например в ацетоне, этано ле или ацетонитриле, при температур кипения растворителя. Пример 1. 2-Амино-5-хлор- Л -этилбензгидрол. Из 9,7 г опилок магния и 38,15 г этилбромида в 115 мл безводного эфи ра готовят этилмагнийбромид. К охла денному раствору соединения Гриньяр прикапывают 23,2 г 2-амино-5-хлорбензофенона в 350 мл безводного эфи ра, причем следует следить за тем, 6 чтобы температура не превышала -5°С. Реакционную смесь при 0°С еще переешивают в течение 30 мин. По окончании реакции (контроль с помощью тонкослойной хроматографии) реакционную смесь выливают в раствор хлорида аммония в, ледяной воде. Эфирную фазу промывают сначала раствором хлорида натрия, затем водой до нейтральной реакции и после этого сушат над сульфатом натрия. После отгонки эфира олучают 18,3 г 2-амино-5-хлор-d- -этилбензгидрола. Продукт перекристаллизовывают из н-гептана; т.пл. 91,5-92С; Вычислено, %: С 68,83; Н 6,16; се 13,55; N 5,35. C-isH gCENO. Найдено, %: С 68.70; Н се 13,52; N 5,18. Пример 2. 4-( р-диэтиламиноэтокси)- оС-этилбензгидрол. К охлажденному до -10°С реактиву Гриньяра, полученному из 3,88 г магниевых опилок и 17,44 г этилбромида в 60 мл безводного эфира, прибавляют по каплям раствор 24 г 4-( р-диэтиламиноэтокси)-бензофенона в 120 мл безводного эфира. Реакционную смесь интенсивно перемешивают. Температуре смеси позволяют повыситься до 0°С. Затем реакционную смесь кипятят в течение 15 мин. По окончании реакции реакционную смесь выливают в охлажденный льдом водный раствор хлорида аммония, эфирную фазу отделяют. Водную фазу дважды встряхивают в делительной воронке с эфиром с общим количеством 60 мл. Эфирные фазы объединяют, промывают, сушат над безводньм сульфатом магния и эфир отгоняют. Твердый остаток перёкристаллизовывают из этанола. Получают 18,1 го продукта, который плавится при 5859°С. Вычислено, %: С 77,02; Н 8,93; N 4,29. Co HjgNOg. Найдено, %: С 77,04; Н 9,17; N 4,11. Этанольный раствор 4-( Ь-диэтиламиноэтокси)-оС.-этилбензгидрола обрабатывают этанольным раствором эквивалентного количества фумаровой кислоты, К охлажденному до -15с раствору добавляют эфир, после чего выпадает в осадок гидрофумарат продукта. Соль отфильтровывают, промывают эфиром и затем сушат. Гидрофумарат 4-( (5-диэтиламиноэтокси) - cL-этилбензгидрола плавится при 108,5- 109,. Пример 3. 4-{ р-Диэтиламиноэтокси)-{ -этилбензгидрол, этилбромид. 16,3 г 4-{ р-диэтиламиноэтокси)- оС-этилбензгидрола растворяют в 250 мл ацетонитрила и к раствору добавляют 14 мл этилбромида. Смесь
кипятят с обратным холодильником в течение 2 ч и затем оставляют на ночь. На другой Авнь раствор упаривают при пониженном давлении. Твердый остаток перекристаллизовывают из ацетона. Получают 17,4 г кристаллического четвертичного соединения; т.пл. .
Пример 4. 2-(N-Бензоиламино-5-хлор- ct-этилбензгидрол.
5,2 г 2-амино-5-хлор-оС-этилбензгидрола растворяют в 100 мл безводного ацетона и в присутствии 3,4 г безводного бикарбоната натрия апилируют с 2,82 г бензоилхлорида. По окочании реакции неорганическую соль удаляют путем фильтрации, растворитель отгоняют при пониженном давлении. Остаток перекристаллизовываютиз спирта. Получают 5 г продукта; т.пл. 188-189с.
Вычислено, %: С 72,22; Н 5,51; С€ 9,69; N 3,83.
C52«2oC N02.
Найдено, %: С 72,18; Н 5,68; се 9,49; М 3,91.
Пример 5. 4-Гидрокси-оС-винилбензгидрол.
К 184 мл 3,4 молярного раствора винилмагнийхлорида в тетрагидрофуране при в течение примерно 30 мин добавляют 20 г 4-гидроксибензфенона в 180 мл безводного эфира. Реакционную смесь при перемешивают еше в течение 1 ч и оставляют на ночь при комнатной температуре. На другой день реакционную смесь выливают в охлажденный льдом водный раствор хлорида аммония. Эфирную фазу промывают водой и затем сушат над безводным сульфатом магния. После отгонки эфира получают 22,6 г винилсоединения. Продукт перекристаллизовывают из смеси этилацетата и н-гексана.
Вычислено, %: С 79,62; Н 6,24.
-(5 М 2
Найдено, %: С 79,55; Н 6,18.
Пример 6. 4- р-Диэтиламиноэтокси-ci-этилбензгидрол.
В эфире из 3,65 г магния и 16,35 этилбромида готовят этилмагнийбромид и к этому раствору добавляют раствор 29,74 г 4- р-диэтиламиноэтоксибензофенона в бензоле. Смесь кипятят в течение 2ч. После охлаждения смесь выливают в охлажденную смесь хлорида аммония и льда, органическую фазу отделяют и водную фазу экстрагируют эфиром. Органические фазы объединяют промывают.и сушат над безводным сульфатом .натрия. Растворитель упаривают при пониженном давлении. Путем перекристаллизации сырого продукта из этнола получают 28,16 г 4-диэтиламиноэтоксизтилбензгидрола. Физические костанты продукта идентичны с константами продукта, полученного согласно примеру 2. .
.Пример 7.4- р-Диэтиламиноэтокси-ci-этилбензгидрол.
Из 7,3 г магния и 32,7 г этилбромида в безводном тетрагидрофуране готовят этилмагнийбромид,к этому раствору добавляют раствор 59,48 г 4- (3-диэтиламиноэтоксибензофенона в диоксане. Смесь кипятят в течение 90 мин, затем выливают в смесь хлорида аммония и льда и путем разбавления водой выделяют твердый 4- р-диэтиламиноэтокси-ci-этилбензгидрол. Получают 61,13 г продукта/ физические характеристики которого согласуются с таковыми для продукта, полученного согласно примеру 2.
Пример 8. 3- Трифторметил- оС-этилбензгидрол.
Из 36,5 г магнии и. 163,5 г этилбромида в тетрагидрофуране получают этилмагнийбромид. При температуре кипения раствора к нему добавляют раствор 250,2 г 3-трифторметилбензофенона в тетрагидрофуране и смесь кипятят в 2 ч. Охлажденную реакционную смесь выливают в смесь ледяной уксусной кислоты и льда. Продукт экстрагируют эфиром, органическую фазу промывают водой и затем сушат над безводным сульфатом . Растворитель упаривают при пониженном давлении, полученный сырой продукт фракционируют в вакууме. Получают 224,2 г 3-трифторметил-сС-этилбензгидрола; т. кип. 106-108 С/О , 03 мм рт.ст.
Вычислено, %: С 68,56; Н 5,39; F 20,34.
C sHtjFs Найдено, %: С 68,55; Н 5,42;
F 20,18.
Пример 9. 2,5-Диметил- d-этилбензгидрол.
Из 3,65 г магния и 16,35 г этилбромида в тетрагидрофуране получают этилмагнийбромид. К раствору добавляют 21,03 г 2,5-диметилбензофенона в диметиловом эфире этиленгликоля, реакционную смесь кипятят в течение 1 Ч. После охлаждения реакционную смесь выливают в смесь ледяной уксусной кислоты и льда. Из органической фазы путем добавления воды осаждают целевой . продукт. Получают 21,75 г 2,5-диметил-сС-этилбензгидрола; т.пл. 38-39 С.
Вычислено, %: С 84,95; Н 8,39. .
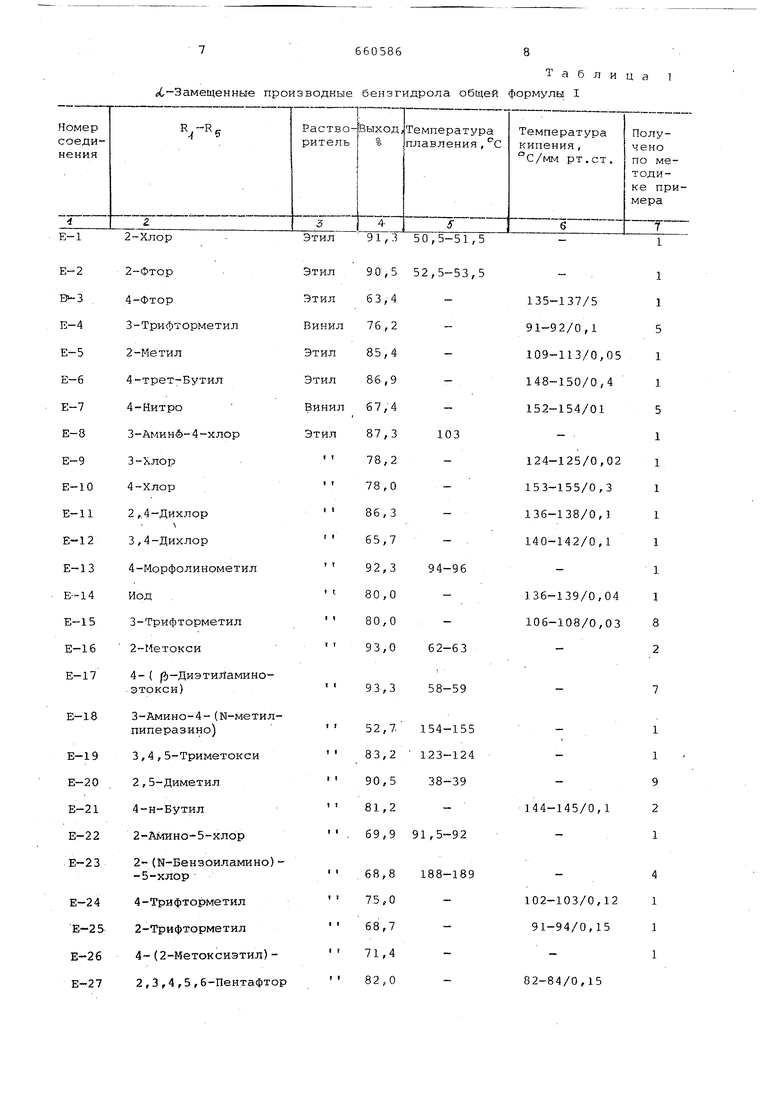
найдено, %: С 85,10; И 8,59. Аналогично получают другие aL--3aмешенные производные бечзгидрола, приведенные в табл. 1.
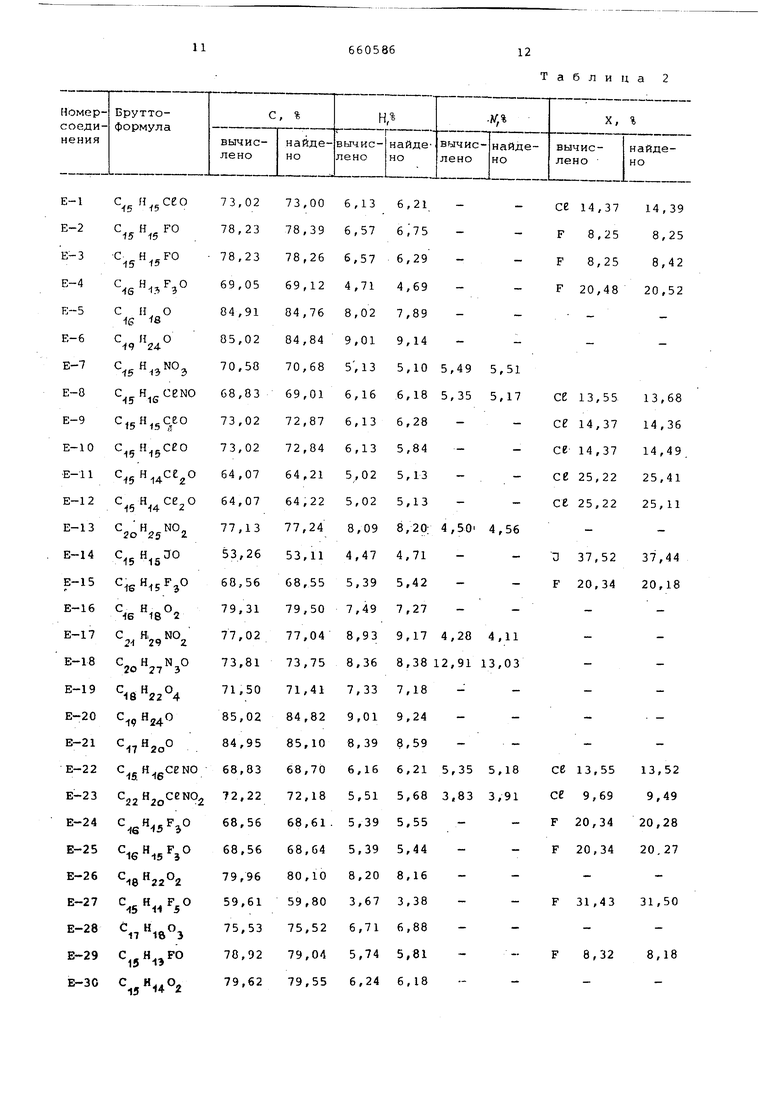
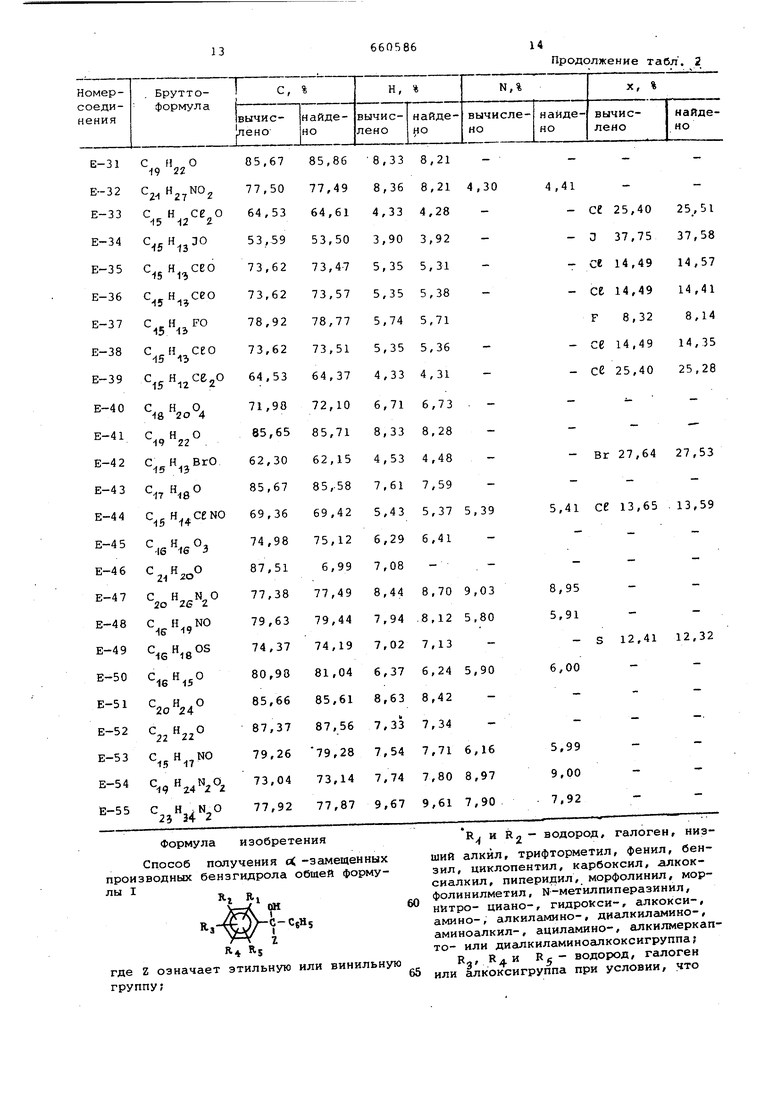
Результаты анализа полученных соединений даны в табл.2.
Х,-Замещенные производные бензгидрола общей
Таблица 1 формулы I
Таблица Формула изобретения Способ получения с -замещенных производных бензгидрола общей формулы I I к., он где Z означает этильную или винильну группу ший алкйл, трифторметил, фенил, бензил, циклопентил, карбоксил, алкоксиалкил, пиперидил, морфолинил, морфолинилметил, N-метилпиперазинил, нйтро- циано-, гидрокси-, алкокси-, амино-, алкиламино-, диалкиламино-, аминоалкил-, ациламино-, алкилмеркапто- или диалкиламиноалкоксигруппа; ИЛП хлпи Rg, 5 водород, галоген о „ р - волооод, галоген или алкоксигруппа при условии, что
15
осли Z - этил, то . не могут все одновременно означать водород, есЛй R, R и s водород, то R и R не могут означать аминогруппу в ,2или 4-положении, диметиламиногруппу в 2- или 4-положении, бром, метил или. метоксигруппу в 4-положении, не могут одновременно означать метоксигруппу в 2- и 4- или 3- и 4-положениях, RJ, Н-и Rg не могут означать Три метокоигруппы в положениях 2,4,5нли Г,4,б-, 4-мётокси-З,5-диметил и 2-аМино-З,5-дибром, если Z - винильная группа, то R.-R не могут все одновременно означать водород, если RJ-R. водород, то R не может означать 4-матил, или их кислотно-адди ивных или четвертичных аммониевых солей, отличающийся тем, что бензофеноны обшей формулы II
б f, О 5 86
ач Us
в которой имеют вьпиеприведенные значения,
подвергают взаимодействию с этилили винилмагнийгалогенидом при температуре от -10 до в среде органического растворителя, с последующим выделением соединений формулы I в свободном виде или в виде их кислотноаддитивных или четвертичных аммониевых солей.
Источники информации, принятые во внимание при экспертизе
1. Препаративная органическая химия. Издание второе. М-Л., Химия , 1964, с. 662.




| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных -этилбензгидрола или их солей | 1976 |
|
SU596159A3 |
| Способ получения -замещенных производных бензгидрола или их солей | 1976 |
|
SU649306A3 |
| Способ получения замещенных производных 3-нитробензофенона | 1974 |
|
SU673175A3 |
| Способ получения диаминобензофенонов | 1974 |
|
SU506290A3 |
| Способ получения -этинилбензгирола | 1974 |
|
SU689613A3 |
| Способ получения производных 3-хлорпрегнана | 1982 |
|
SU1181551A3 |
| Способ получения производных 3-амино-17а-аза- -гомо-5 - андростана или их солей, или их четвертичных солей | 1978 |
|
SU722487A3 |
| Способ получения 2,6-бис-(хлорметилоксикарбонилоксиметил)-пиридина | 1987 |
|
SU1510717A3 |
| Способ получения производных бензодиазепина | 1975 |
|
SU1080744A3 |
| Способ получения рацемического или оптически активного 4-замещенного 1,3,4,5-тетрагидро-2н-1,4-бензодиазепин-2-она | 1975 |
|
SU942594A3 |


Авторы
Даты
1979-04-30—Публикация
1974-08-14—Подача