Изобретение относится к высокомолекулярным соединениям, а именно к синтезу огне- терме- и теплостойких полимеров, которые могут быть использованы в различных областях техники. Известен способ получения политриазолохиназолинов, основанный на реакции взаимодействия ароматически диаминов, содержащих в о-положениях к аминогруппам триазольные циклы, с галоидамгидридами ароматических карбоновых кислот в условиях,цизкотемпературной поликонденсации в ,сре де амидных растворителей .с последую щей твердофазной полициклодегидрата цией образовавшихся полимерных продуктов при 350-370° С 1. Недостатком данного способа явля ется то, что используемые в качестве мономеров ароматические диамин обладают низкой нуклеофильной реакционной способностью вследствие наличия триазольных о-заместителей У аминогрупп, что ограничивает возможность получения политриазолохиназолинов с высоким молекулярным ве;сом, кроме того, осуществление проijecca твердофазной полициклодег55Д ратации щ омежуточных полимерных продуктов при очень высоких температурах () вызывает протекание побочных процессов - сшивки, деструкции и т.д., что приводит к образованию политриазолохиназолинов, раствори11« 1Х только в сильных кислотных растворителях. Известен также способ получения политриазолохиназолкнов, основанный на высокотемпературной поликонденсацни бисамидразонов дикарбоновых кислот с бисбензоксазинонами в счреде амидных растворителей с последующим выделением и термической .полициклодегидратацией образующихся на йервой стадаи процесса промежуточных полимерных продуктов при 2. Недостатком известного метода синтеза политриазолохиназолинов являются: низкая электрофильная реакционная способность используеглых в качестве мономеров бисбензоксазинонов, затрудняющая получение полимеров с высоким молекулярным весом; необходимость проведения процесса полициклоконденсации при , что не только затрудняет технологическое
оформление процесса, но и приводит к образованию значительного количества гель-фракции в целевых политриазолохиназолинах, что предопределяет их растворимость только в сильйых кислотных растворителях.
Цель изобретения - придание поли- мерам раствори1уюсти, а также повы(иение их молекулярного веса.
Поставленная цель достигается тем, что политриазолохиназолины получают
СО Hat
N К-МНг Haf ОС 1 IIЧ- п
, -2лННа1
С-К-С-ННг0
NК
И II
н R-C С
н
-4nHjO
А
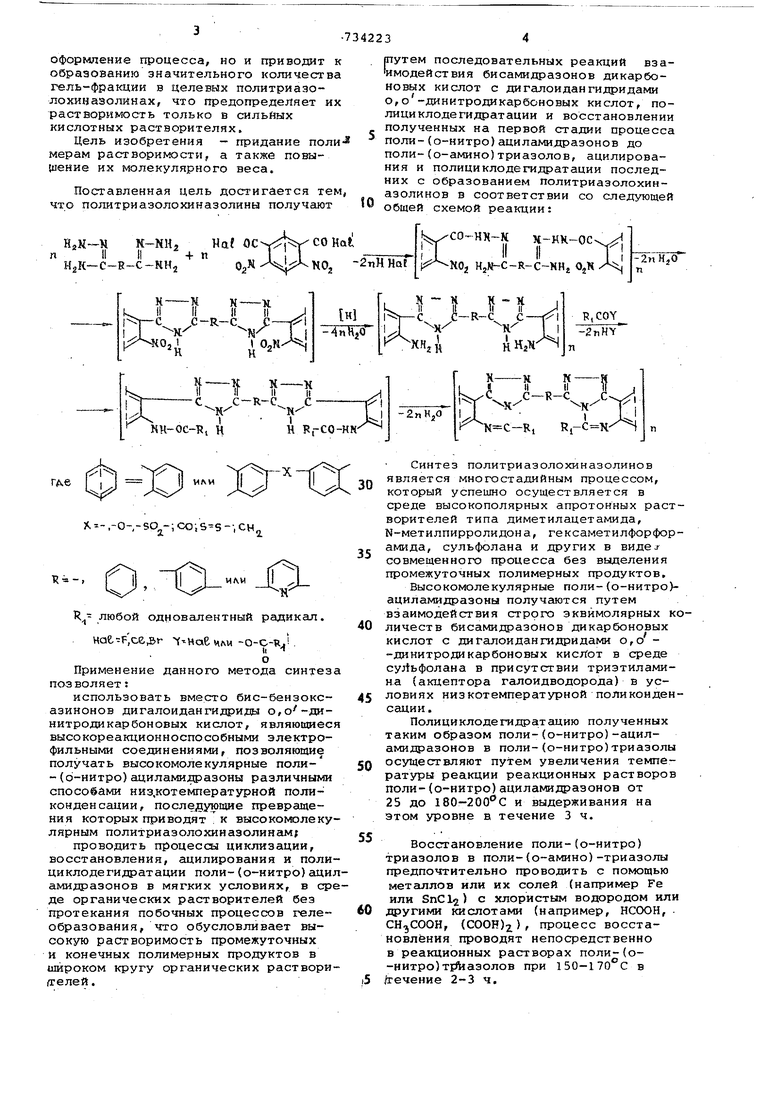
рутем последовательных реакций взаимодействия бисамидразонов дикарбоновых кислот с дигалоидан гидридами о,о -динитродикарбоновь1Х кислот, полициклодегидратации и восстановлении полученных на первой стадии процесса поли-(о-нитро)ациламидраэонов до поли-(о-амино)триазолов, ацилирования и полициклодегидратации последних с образованием политриазолохиназолинов в соответствии со следующей общей схемой реакции:
Ц/со---нх к к-нк-ос
HjN-C-R-C-NHj OjN
-2nHjO n




| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения полихиназолинхиназолонов | 1978 |
|
SU749857A1 |
| Способ получения полибензимидазолимидов | 1978 |
|
SU749859A1 |
| Способ получения поли-(-2-замещенных) хиназолонов | 1977 |
|
SU702036A1 |
| Способ получения полибензоксазолов | 1979 |
|
SU1002310A1 |
| Способ получения полибензимидазолохиназолинов | 1977 |
|
SU734224A1 |
| Способ получения полиамидобензимидазолов | 1978 |
|
SU717090A1 |
| Способ получения растворимых полибензоксазолов | 1972 |
|
SU448205A1 |
| Способ получения полибензимидазолов | 1976 |
|
SU619493A1 |
| Способ получения сополибензимидазолобензоксазолов | 1978 |
|
SU749858A1 |
| Способ получения поли-(1,2-дизамещенных)-бензимидазолов | 1976 |
|
SU652193A1 |

X. --- ,-0--SOj -; COiS-9 --, СН,., любой одновалентный радикал. Нае,-Р, Иае viftM-о-о-я, . Применение данного метода синтез позволяет: использовать вместо бис-бензоксазинонов дигалоидангидриды о,о -динитродикарбоновых кислот, являющиес высокореакционноспособными электрофильными соединениями, позволяющие получать высокомолекулярные поли-(о-нитро)ациламидразоны раэличнылш способами низ.котемпературной поликонденсации, пocлejgyющиe превращения которых приводят к высокомолеку лярным полиггриазолохиназолинам; проводить процессы циклизации, восстановления, ацилирования и поли циклодегидратации поли-(о-иитро)аци амидразонов в мягких условиях, в ср де органических растворителей без протекания побочных процессов гелеобразования, что обусловливает высокую растворимость промежуточных и конечных полимерных продуктов в ижроком кругу органических раствори д-елей. Синтез политриазолохиназолинов является многостадийным процессом, который успешно осуществляется в среде высокополярных апротонных растворителей типа диметилацетамида, N-метилпирролидона, гексаметилфорфорамида, сульфолана и других в видeJ совмещенного процесса без выделения промежуточных полимерных продуктов. Высокомолекулярные поли-(о-нитроЬ ациламидразоны получаются путем взаимодействия строго эквймолярных количеств бисамидразонов дикарбоновых кислот с дигалоидан гидридами о,о -динитродикарбоновых кисЛот в среде суЛьфолана в присутствии триэтиламина (акцептора галоидводорода) в условиях низкотемпературной поликонденсации . Полициклодегидратацию полученных таким образом поли-(о-нитро)-ациламидразонов в поли-(о-нитро)триазолы осуществляют путем увеличения температуры реакции реакционных растворов поли-(о-нитро)ациламидразонов от 25 до 180-200 С и выдерживания на этом уровне в течение 3 ч. Восстановление поли-(о-нитро) триазолов в поли-(о-амино)-триазолы предпочтительно проводить с полющью металлов или их солей (например Ре или SnCl2) с хлористым водородом или другими кислотами (например, НСООН, , (СООН)), процесс восстановления проводят непосредственно в реакционных растворах поли-(о-нитро)т1Л1азолов при ISO-ITO C в |гечение 2-3 ч. Превращение полученных таким образом поли-(о-амино)-триаэолов в поли-(о амидо)триазолы осуществляют путем обработки реакционных растворов поли-(о-амино)триазолов ангидридами или талонд-ангидгоидами монокарбоновых кислот при 25 С в присутствии триэтиламина; при этом образуются поли-(о-амино)триазолы, полициклодегидратацию которых в ко нечные политриазолохиназолины осуществляют путем увеличения темпера туры реакции реакционных растворов поли-(о-амидо)триазолов в присутствии хлористого водорода-катализа тора образования триазолохиназолин Bolo цикла от 25 до 180°С и выдерживания на этом уровне в течение 5ч. Полученные таким образом политриазолохиназолины полностью раств римы- в диметилформамиде, диметилащетамиде, диметипсульфоксиде, гексаметилфосфорамиде, N-метилпирролидоне, сульфолане, смеси тетрахлорэтана с фенолом (3:1), хлориро ванных фенолах, а также в муравьин трифторуксусной монохлоруксусной и серной кислотах с образованием выс коконцентрированных растворов (до 35% по весу полимера). Приведенная вязкость 0,5%-ных растворов политриазолохиназолинов в органических растворителях равна по меньшей мер 0,65 ял/г. На основе политриазолохиназолинов получаются серые, прозрачные и эластичные пленки, обладающие прочностью на разрыв 800 кг/см при 25°С. Синтезированные промежуточные полимерные продукты и политриазолохиназолины характеризуются по приведенной вязкости их растворов, УФ- и ИК-спектрам, данным элементного анализа, результатам динамического и изотермического анализов а также свойствами полученных на и основе пленок. Пример. В трехгорлую колбу емкостью 200 мл, снабженную мешалкой и вводом для инертного газа, загружают 1,932 г (0,01 моль) бисамидразона пиридин-2,6-дикарбоновой кислоты, 40 мл сульфолана и 2,8 мл (0,02 мольтриэтиламина. При перемешивани в токе инертного газа при к реакционному раствору в течение 30 прибавляют 2,930 г (0,01 моль) дихлорангидрида 4,б-динитроизофталев кислоты, а затем снимают охлаждение и температура реакции самопроизвольно поднимается до 25°С. Реакционный раствор перемешивают при 25°С в течение 1 ч, получая светло-желтый однородный раствор поли-(о-нитро)-ациламидразона. Небольшую часть полимера выливают в дистиллированную воду, получая светло-желтые волокна поли-(о-нитро)ациламидразона. Приведенная вязкость 0,5%-ного раствора полученного поли-(о-нитро)ациламидразона в при 25°С 0.45 дл/г. Оставшийся I реакционный раствор нагревают постепенно (в течение одного часа) в токе инертного газа и при перемешивании от 25 до 2О О С и выдерживают на этом уровне 3 ч; при этом раствор постепенно окрашивается в оранжевый цвет. Через три часа реакционный раствор охлаждают -до ,50 С и небольшую часть полимера выливают в дистиллированную воду, получая оранжевые волокна поли-(о-нитро) триазола. Приведенная вязкость 0.5%iro раствора полученного поли-(о-нитро)триазола в HgSO при 25°С Of 12 дл/г. В оставшийся реакционный раствор помещают 5,0 г восстановленного железа и начинают пропускать газообразный нее при . За счет теплоты экзотермической реакцьи, а затем за счет внешнего обогрева температуру смеси поднимают до и выдерживают на этом уровне до полного израсходования железа (3-4 ч); при этом реакционный раствор постепенно окрашивается в бежевый цвет. Через 3-4 ч реакционный раствор охлаждают до и небольшую часть полимера выливают в дистиллированную воду, получая бежевые волокн-а при поли-(о-амино)триазола. Приведенная вязкость 0,5%-ного раствора полученного поли-Со-амино)триазола в диметилацетамиде 0,56 дл/г. В оставшийся реакционный раствор вводят 2,8 мл (0,01 моль) триэтиламина и 2,3 мл (0,02 моль)хлористого бензоила при и интенсивном перемешивании. Процесс бензоилирования продолжают 2 ч. Через два часа небольшую часть полимера выливают в дистиллированную воду, получая бежевые волокна поли-(о-бензаь1идо)триазола. Приведенная вязкость 0,5%-ного раствора полученного поли-(о-бензамидо)триазола в диметилацетамиде при 25°С 0,64 дл/г. В оставшийся реакционный раствор пропускают газообразный НСЕ в течерие 15 мин с постепенным-увеличением температуры реакции до 180°С и выдерживают на этом уровне 5 ч. Через три часа реакционный раствор охлс1ждагот до , пропускают через стеклянный фильтр и выливают в воду, получая серые волокна политриазолохиназолина. Полимер отфильтровывают, щx)ивaют холодной, а затем горячей ВОДОЙ до нейтральной реакции и экстрагируют этанолом, после чего .сушат а вакууме при до посто ного веса. Аналогичным образом выделяют и сушат все вышеописанные промежуточные полимерные продукты. Выход политриазолохиназолина количественный. Приведенная вязкость 0,5%-ного раствора полимера в диметилацетамиде при 1,22 дл/г. Из 20,%-го раствора полученного таким образом политриазолохиназолин в диметилацетамиде получают прозрачные, серые и эластичные пленки, обладающие разрывной прочностью при 25°С 1000 кг/см Пример 2, Синтез полимера осуществляют в соответствии с методикой, приведен ной в примере 1, с той разницей, что вместо 0,01 моль дихлорангидрИ 4,б-динитроизофталевой кислоты используют 0,01 моль дихлорангидрида бис-{З-нитро-4-карбоксифенил)оксид Выход политриазолохиназолина количественный. Приведенная вязкость 0,95 дл/г, прочность, пленки на его основе при 25°С 880 кг/см. Пример 3. Синтез полимера осуществляют в соответствии с методикой примера 1, но вместо 0,01 моль дихлорангидрида 4,б-динитроизофталевой кислоты используют 0,01 моль дихлорангидрида бис-(З-нитро-4-карбоксифенил)метана Выход полимера количественный. Приведенная вязкость 0,90 дл/г. Пример 4. Синтез полимера осуществляют и соответствии с методикой примера 1 с той разницей, что вместо 0,01 мо дихлорангидрида 4,6-динитроизофтал вой кислоты используют 0,01 моль дихлорангидрида бис-(3-нитро-4-кар оксифенила), Выход политриазолохин азолина 96%. Приведенная вязкость 0,84 дл/г. Синтез полимера осуществляют в соответствии с методикой примера 1, с той разницей, что вместо 0,01 моль дихлорангидрида 4,6-динитроизофталевой кислоты используют 0,01 моль дихлорангидрида бис-(З-нитро-4-карбоксифенил)кетона. Выход коли.чественный. Приведенная вязкость 0,78 дл/г. Пример 6. Синтез полимера осуществляют в соответствии с методикой примера 1, но вместо 0,01 моль дихлорангидрида 4, б-динитроизофталевой кислоты ICпользуют 0,01 моль дихлорангидрида бис-(З-нитро-4-карбоксиJ сульфона. Выход 92%. Приведенная вязкость 0,65 дл/г. Пример 7. f--1fjfl С Синтез полимера осуществляют в соответствии с методикой, приведенной в примере 1, с той разницей, что вместо 0,01 моль дихлорангидрида 4,6-динитроизофталевой кислоты используют 0,01 моль дихлорангидрида бис-(З-нитро-4-карбоксифенил)дисульфида. Выход полимера 94%. Приведенная вязкость 0,68 дл/г. Пример 8. Синтез полимера Ъсушествляют в соответствии с методикой приведенной в примере 1, но вместо 0,01 моль бисамидразона пиридин-2,б-дикарбонобой кислоты используют 0,01 моль оксалилбисамидразона. Выход полимера koличecтвенный. Приреденная вязкость дп/г.
Синтез политриазолохиназолина осуществляют в ееответствии с методикой, приведенной в примере 1,с той разницей, что вместо 0,01 моль бисамидразЬна пиридин-2,6-дикарбоновой кислоты используют 0,01 моль бисамидразона терефталевой кислоты Выход полимера количественный. Приведенная вязкость дл/г.
10Пример-II,
Синтез политриазолохнназолича осуществляют в соответствии с методикой примера 1, но что вместо сульфолана в качестве растворит-аля исполь.- зуют N-метилпирролидон. Выход полимера количественный; приведенная вязкость 0,85 дл/г.
Свойства полученных полимеров и их 20 растворимость представлены в/ таблице.
1,22А/Н,Б/Н,Г,Д/Н,Е
0,95А,Б,В/Н,Г,Д,Е
0,90А./Н,Б/Н,Г,Д,Е
0,84Б/Н,Г/Д/Н,Е
0,76А/Н,Б/Н,Г,Д/Н,Е
0,65А,Б,В/Н,Г,Д,Е
0,68А,Б,В,Г,Д,Е
0,72А/Н,Б/Н,Г,Д,Е
0,98А/Н,Б,Г,Д,Е
0,66Г,Д/Н,Е
и м ё ч а н и eT j - растворим в амндных раствори- ;
телях (да1мет лформагжде, диметилaцвтa шдe и N -метилпирролндоне);
Б - растворим в д|-5метилсульфоксидег
В - растворим в сульфолане;
Г - растворим в тетрахлорэтана с ф(нолом (3:1) г
Д -- растворим в м крезоле,
Е - растворим в концентрированных H-SO, НСООН CF jCOOH
А/Н, Б/Н,В/К,Г/НрД/Н,Е/Н - растворим нагреванием до в соответствуюйдах растворителях.
8-10
3-5
2-3
2-3
1-2
1-2
1-2
3-5 tttrt f # 11 ., f/ 5ft f J f Формула изобретения Способ получения политриазолозшназолннов поликонденсацией бисамилразонов дикарбоновых кислот и азотсхэдержащего соединения с последующим превращением образующихся промежуточных полимерных продуктов, отли чающий ся тем, что, с целью придания полимерам растворилюсти, а также повышения их молекулярного веса, в качестве азотсодержащего соединения используют дигалоидангидрид О}о-динитродикарбоновой кислоты формулы 3 На& F, се, Вг со , S0, полученные поли(о-нитро)ациламидразоны подвергают терьгообработке, восстанавливают до поли(о-амино)триазолов, затем ацилируют и подвергают полициклодегидратации. Источники информации, принятые во внимание при экспертизе 1, Авторское свидетельство СССР 413847, кл. С 08 g 33/04, 1972.
HatOC,,x|VCOHae
D,M Т NO,

Авторы
Даты
1980-05-15—Публикация
1977-12-21—Подача