(54) СПОСбБ ПОЛУЧЕНИЯ ПОЛИХИНАЗОЛИНХИНАЗОЛОНОВ



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения политриазолохиназолинов | 1977 |
|
SU734223A1 |
| Способ получения поли-(-2-замещенных) хиназолонов | 1977 |
|
SU702036A1 |
| Способ получения полибензимидазолохиназолинов | 1977 |
|
SU734224A1 |
| Способ получения полибензоксазолов | 1979 |
|
SU1002310A1 |
| Способ получения полибензимидазолимидов | 1978 |
|
SU749859A1 |
| Способ получения полиамидобензимидазолов | 1978 |
|
SU717090A1 |
| Способ получения растворимых полибензоксазолов | 1972 |
|
SU448205A1 |
| Способ получения поли-(1,2-дизамещенных)-бензимидазолов | 1976 |
|
SU652193A1 |
| Способ получения сополибензимидазолобензоксазолов | 1978 |
|
SU749858A1 |
| Способ получения полибензимидазолов | 1976 |
|
SU619493A1 |

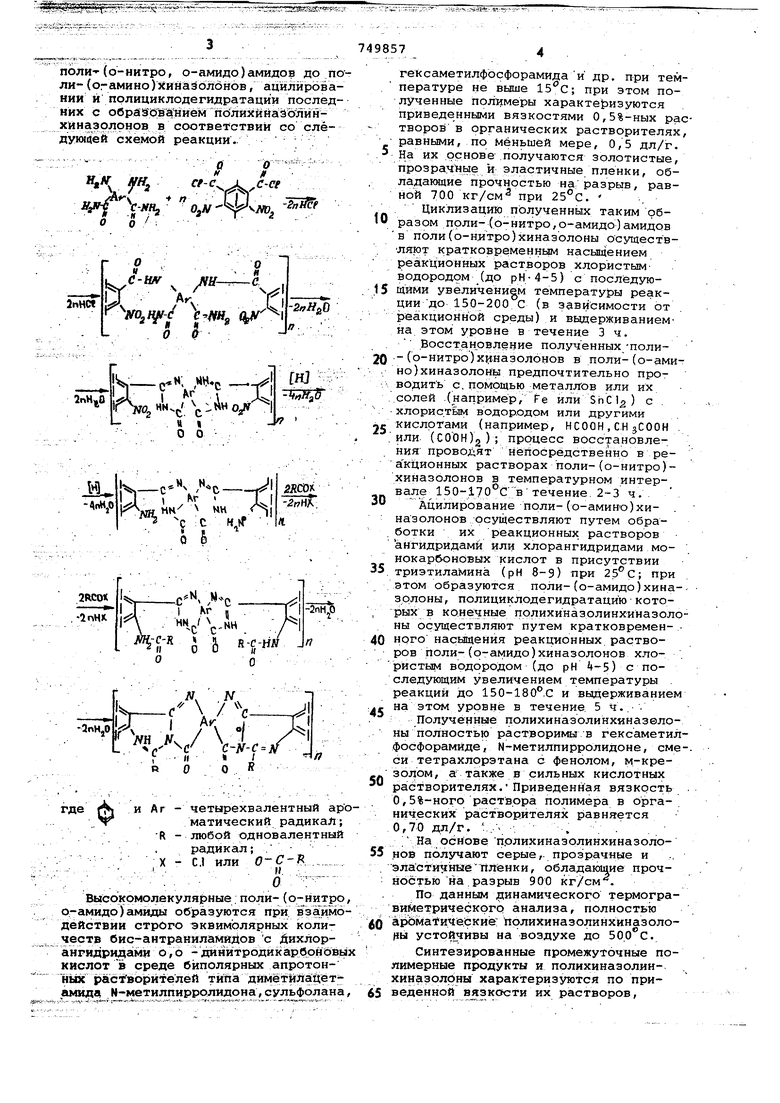
Изобретение относится к высокомолекулярным соединениям, а именно к синтезу огне-, термо- и теплостойких полимеров, которые могут быть исполь зованы в различных областях техники. Известен способ получения полихиназолинхиназолонов, основанный на реакции взаимодействия бис-бензоксазинонов с бис-антраниламидами в условиях высокотемпературной поликонденсации в среде органических растворителей или полифосфорной кислоты в температурном интервале 200-250°С с пос.г:едующей твердофазной полициклодегидратацией полученных промежуточных полимерных продуктов при и выше Щ . Недостатками известного способа являются образование низкомолекулярных порошкообразных полихинозолинхиназолонов (приведенная вязкость в HnSO равняется 0,3 дл/г) вследствие использования в качестве мономеров бис-бензоксазинонов, обладающих низкой электрофильной реакционной способностью, а также нерастворимость полимеров в органических растворите.лях В результате проведен1 я процесса полициклодегидратации в жестких условиях при 350 С и выше, предопределяющих протекание побочных процессов гелеобразования в полимерах; при этом полученные полихиназолинхиназолоны растворяются только в концентрированной серной кислоте. Цель изобретения - получение пленкообразующих полимеров линейного строений, обладающих растворимостью в органических растворителях. Предлагаемый способ получения полихиназолинхиназолонов заключается в последовательных реакциях взаимодействия бис-антраниламидов с дихлорангидридами о,о-динитродикарбоновых кислот формулы О О , // C( Х --сн -.-о циклизации и восстановлении полученных на первой стадии процесса
ПОЛИ(о-нитро, о-амидо)амидов до поли- (о.-амино)хинаЭЬлбнов, ацилйровании и прлициклодегидратации последних с обрё ЗёШиёнпдлкШйА : уМ хйназрлрнов в соответствии со слёдукиаей схемой реакции.
.,
п
. ,,Г , I
, i
я о
jW. JV
c AK
AA-t
nHjO
/
k
fi
0
0
и Ar - четырехвалентный apoгде .ЛИ матический радикал; R - любой одновалентный
радикал; . X - C.I или O-C-R
.-.--. , . - Q ..,.-,,.----Высокомолекуля| ные поли- (о-йитро, о-амидо)амвды образуются при вза;им6действии строго эквимолярных количеств бис-антраниламиДов с Дихлорангидридами о/о - дййитроди к ар бой бвых кислот S среде биполярных апротонных растворйтелей типа диметйлайётамида М-метилпирррлидона,сульфолана,
гексаметилфосфорамида и др. при температуре не выше при этом полученные полимеры характе иэуются приведенными вязкостями 0,5%-ных растворов в органических растворителях, равными, по меньшей мере, 0,5 дл/г. На их основе получаются золотистые, прозрачные,и эластичные пленки, обладающие прочностью на; разрыв, равной 700 кг/см при 25°С. ,
Циклизацию полученных таким образом поли-(о-нитро,о-амидо)амидов в поли(о-нитро)хиназолоны осуществяют кратковременньлм насыщением реакционных растворов хлористым водородом (до рН-4-5) с последующими увеличением температуры реакции до 150-200 С (в зависимости от . реакционной среды) и вьщерживаниемна этом уровне в течение 3ч. Восстановление полученных -поли- (о-нитро)х 1назол6нов в поли-(о-амино)хиназолоны предпочтительно проводить с,помощью металлов или их солей .(например, Fe или ShCl) с . хлористым водородом или другими кислотами (например, НСООН , С:Н jCOOH . или (СООнУд ) ; процесс восстановления проводят непосредственно в реакционных растворах поли- (о-нитро)хиназолонов в температурном интервале 150-170 Св течение. 2-3 ч.
Ацилирование поли-(о-амино)хи- . назолонов осуществляют путем обработки их реакционных растворов ангидридами или хлорангидридами монокарбоновых кислот в присутствии триэтилаМина (рН 8-9) при 25С; при этом образуются поли-(о-амидо)хина-зрлоны, полициклодегидратацию которых в ко.нечные прлихиназолинхиназолоны осуществляют путем кратковремен- ного насьпцения реакционных растворов поли-(о-амидо)хиназолонов хло- . рйстым водородом (до рН А-5) с последующим увеличением температуры . реакций до 150-180 .С и вьщерживанием на этом уровне в течение. 5 Ч..-Полученные полихиназолинхиназелоНы полностью растворимы В гексаметилосфорамиде, N-метилпирролидоне, сме-. си тетрахлорэтана с фенолом, м-крезолом, а также в сильных кислотных растворителях.Приведенная вязкость . 0,5%-ного раств.ора полимера в орга-. нических растворителях равняется 0,70 дл/г. . . . . .
На основе полихиназолинхиназоло.нов п6л5чают серые,- прозрачные и .. эластйчйыёплёнки, обладающие прочностью на.разрыв 900 кг/см.
По данным динамического термогравиметрического анализа, полностью ароматиЧеские полихиназолинхиназоло(ibj устрй чивы на воздухе до 500 С.
Синтезированные промежуточные полимерные продукты и прлихиназрлинхиназолрны характеризуются по приведенной вязкостк кх растворов. ИК-спектрам, данным элементного ана лиза, результатам динамического и изотермического анализов, а также свойствам полученных на их осн.ове пленок. . Пример.в трехгорлую колбу емкостью 200 мл, снабженную мешалкой и вводом для инертного газа, загружают 2,8433 г (0,01 моль) бис-(3-амидо-4-аминофенил)метана и 30 мл N-метил-2-пирролидона. При перемешивании в токе инертного газа при -20 С к реакционному раствору в течение 30 мин прибавляют 2,930 г (0,01 моль) дихлорангидрида 4,б-динитроизофталевой кислоты, а затем снимают охлаждение, и температура реакции самопроизвольно поднимается до 25°С. Реакционный раствор перемешивают при в течение 1 ч, получая светло-желтый однородный раствор поли-(о-нитро, о-амидо)амида. Необхо димую часть полимера выливают в дистиллированную воду, получая светло-желтые волокна полимера. П.риве- . денная вязкость 0,5%-ного раствора полученного поли-(о-нитро, о-амидо)амида в диметилсульфоксиде равняет-. -ся.0,52 дл/г при 25°С. .Оставшийся реакционный раствор насыщают кратковременно хлористым водородом (рН4-5), постепенно нагревают (в- течение 1 ч) в токе инерт ного газа при перемешивании,от 25 до 170°С и выдерживают на этом уровне в течение 3 ч; при этом раствор постепенно окрашивается -в оранжевый цвет. Через 3 ч реакционный раствор охлаждают до и небольшую часть полимера выливают в дистиллированную воду, получая оранжевые волокна поли -(о-нитро)хиназолона. Приведенная ; вязкость 0,5%-ного раствора полученного полимера в при 25С ... 0,70 дл/г. В оставшийся.реакционный раствор помещают 5,0 г восстановленного железа и н.ачинают пропускать газообразный НС1 при 80°С. За счет теплоты экзотермической реакций, а, затем за счёт внешнего обогрева температуру смеси поднимают, до 160°С и выдерживают на этом до полного израсходования жёлеза (3-4); этом реакционный раствор постепенно окрашивается в бежевый цвет. Через 3-4 ч реакционный раствор охлаждают до 50° С и небольшую часть полимера .выливают в дистиллированную воду получая бежевые волокна поли-(о-амино)хиназолона. Приведенная вязкость 0,5%-ного раствора полученного поли-(о-амино)хиназолона в диметил- сульфоксиде 0,б8дл/г. В оставшийся реакционный раствор вводят 2,8 мл (0,02 моль) триэтиламина и 2,3 мл (0,.02 мо.ль) хлористого бензоила при и интенсивном перемешивании. Процесс бензоилирования продолжают в течение 2 ч, после чего небольшую часть полимера выливают в дистиллированную воду, получая светло-бежевые волокна поли-(о-бензамида)хиназолона. Приведенная вязкость 0,5%ного раствора полученного .полимера в диметилсульфоксиде при 0,6.0 дл/г. В оставшийся реакционный раствор пропускают.газообразный НС1 в течение 15 мин с постепенным увеличением температуры реакции до 180 С и выдерживают на этом уровне в .течение 5 ч, затем реакционный раствор охлаждают до , пропускают через стеклянный . фильтр и выливают в воду, получая серые волокна полихиназолинхиназолона. Полимер отфильтровывают, промывают холодной, а затем горячей водой до. нейтральной реакции и экстрагируют этанолом, после чего сушат в вакууме при lOOc. до постоянного весаГ Аналогичным образом выделяют и сушат, все вышеописанные промежуточные полимерные продукты. . Выход полихиназолинхиназолона количественный; приведенная вязкость 0,5%-ного раствора полимера в смеси тетрахлорэтана с фенолам при 25°С 1,30 дл/г. . Из 10%-ного раствора полученного таким образом полихиназолинхиназоло- на в. смеси тетрахлорэтана с фенолом (3:1) получают прозрачные серые иэластичные пленки, обладающие разрывной прочностью равной 950 кг/.см и удлинением 6-8% при 25С. .. П р и м е р 2. Синтез полимера осуществляют в соответствии с методикой, приведенной в примере 1,- с той разницей, .что вместо 0,01 моль дихлорангидрида 4,6-динитроизофталевой кислоты используют 0,01 моль дихлорангидрида бис-(З-нитро-4-карбоксифенил)оксида. Выход полихиназолинхиназолона количественный; приведенная вязкость 1,25 дл/г, прочность пленки на его основе 900 кг/см и удлинение 8-10% при . Примерз. Синтез полимера осуществляют в соответствия с методикой п)иведенной в примере 1, с той разницей, чтовместо 0,01 моль дихлорангидрида 4,6-динитроизофталевой кислоты используют 0,01 моль дихлорангидрида бис-{3-нитро-4-карбоксифенил)метана. .. . Выход полимера количественный. Приведенная вязкость 1,08 дл/г, прочность .пленки на его основе 850 кг/см и удлийение 5-6% при . Пример4. Синтез.полимера осуществляют в соответствии с методикой, приведенной в примере 1, с той разницей, что вместо 0,01 моль дихлорангидрида 4,6-динитроизофталевой кислоты используют 0,01 моль ди. S.- wir:-:,-:--:.-:- r:
хлорангидрида бис-(З-нитро-4-карбоксифенила).
Выход полихиназолинхиназолона 96%. Приведенная вязкость 0,96 дл/г, прочность пленки на его основе 800 кг/см и удлинение 2-3% при .
П р и м е р 5. Синтез полимера ,осуществляют в соответствии с методикой, приведенной в примере 1, с той разницей, что вместо 0,01 моль дйхлорангидрида 4,б-динитроизофталевой Примечание: АБ В Г д Е А/Нрас в c рас . хло Применение предлагаемого способа получёния полихиназолйнхиназолондв обеспечивает образование пленкообразующих полиХиназолинхиназолонов вследствие использования высокореакционноспособных дихлорангидридов о,о-динитродикарбоновых кислот, а также высокую растворимость синтезированных полимеров в органйческйх растворителях в результат проведения процесса поликонденсации и последующих превращений образующихся промежуточных продуктов в мягких условиях (в среде органических растворителей не выше 180°С) без протекания процессов гелеобразования. Формула изобретения Способ получения полихиназолинхинаэолонов поликонденсацией бис-ант749857
8
кислоты используют 0,01 моль дихлорангидрида бис-(3-нитро-4-карбоксифенил)оксида.
Выход полимера количественный. Приведенная вязкость 1,25 дл/г, прочность пленки 950 кг/см и удлинение 3-4% при .
Для наглядности основные свойства пленок на основе синтезированных полихиназолинхиназолонов и их растворимость приведены в таблице. растворим в амидных растворителях (диметилформамиде, диметилацетамиде и N-метилпирролидоне); растворим в диметилсульфоксирастворим в сульфолане; растворим в смеси тетрахлорэтана . с фенолом (3:1); растворим в м-крезоле; растворим в концентрированных HiSOj,, НС ООН и СРзСООН; Б/П В/Н, Г/Н,Д/Н/ Е/Н--„ ворим нагреванием до 100 С oтвeтcтвs oIциx растворителях. риведенная вязкость 0,5%-ного вора полимера в смеси тетраэтана с фенолом (3:1) при 25 С. раниламидов и электрофильного соединения с последующим превращением промежуточного продукта, отличающийся тем, что, с целью придания полимерам растворимости и пленкообразующих свойств, в качестве электрофильных соединений используют дихлорангидрид о,о-динитродикарб:оновой кислоты формулы X - отсутствует, -о-.; 9 причем образующиеся промежуточные продукты циклизуют, восстанавливают, ацилйруют и подвергают попициклодегидратации. 74985710 принятые во внимание при экспертизе 1. Патент Японии 12746, Источники информации, кл. 26 (0) 5, 1975 (прототип).
Авторы
Даты
1980-07-23—Публикация
1978-06-30—Подача