В результате реакции металлического олова, галоидводорода и олефина, активированного одной или более карбонильной группой, достигается очень высокий выход продукта реакций в расчете на олово даже при нормальных температурных условиях и давлении без использования катализатора. В качесте галоидводорода предпочтительно использовать относительно недорогой хлористый водород. Реакцию можно проводить в среде растворителя, такого как простые эфи ры, спирты, хлорированные или нехлорированные углеводороды. Растворителем может также служить избыток олефина. Металлическое олово может быть использовано в любом виде. Предпочтительно использовать поро11 кообразное олово, поскольку в результате большой доступной площади поверхнос ти олова скорости его реакций велик Однако может быть непосредственно использовано выпускаемое промышленностью гранулированное олово. В этом случае для повышения скорости реакции желательно несколько повысить температуру реакции. Способ обычно сопровождается обр зованием функционально замещенных оловоорганических двугалоидных соединений общей формулы (R 2SnX2, где R обозначает указанный радика RI «3 сн- с сг 2 4 X - хлор или бром. Эти новые соединения являются ис ходными продуктаК1И для получения вы кокачественных новых оловоорганичес стабилизаторов для поливинилхлорида и других полимеров при помощи известных методов, в которых атом галогена замещается обычными органиче кими остат1 ами, таким как кислотная тиоэфирная или тиоалкильная группа. Из представленных далее примеров ясно, что количество тригалогенида в оловоорганическом галоидном соеди нении может меняться в широких пред лах, например от О до 95 вес.%. Такую смесь обычно используют в количестве 5-60 вес.%. Для одновременного образования в продуктах реакций произвольного к личёства тригалогенида важно, чтобы конкурирующие реакции между оловом и галоидоводородом, с одной стороны и между.этими соединениями и активированным олефином, с другой сторо ны, направлялись в сторону протекания первой из них. Образование указанных продуктов может быть промотировано, особенно за счет изменения соотношения реактантов, порядка и/или скорости введения реактантов, доступной площади поверхности олова и (в меньшей степени) путем изменения температуры. Таким образом, использование, например, избытка олефина, медленное введение галоидводорода и снижение доступной площади поверхности олова приведут исключительно к образованию двугалогенида (R)2SnHaГ. Изменяя условия реакции в обратном направлении, повышают выход тригалогенида RSnHa. Далее описаны способы получения оловоорганических дзугалоидных соединений, сопровождающиеся или нет одновременным образованием тригалоидных соединений. Пример 1. Трехгорлую колбу на 500 мл, помещенную в охлаждающую баню и снабжённую мешалкой, термометром, холодильником и выводами для газа, загружают 60 г порошкообразного олова, 87,4 г метилакрилата и в качестве растворителя l40 мл диэтилового эфира. В течение 3 ч при 20с в смесь при перемешивании продувают 87 г сухого хлористого водорода. После этого эфир выпаривают, а остаток экстрагируют 300 мл горячего хлороформа. Из хлороформенного экстракта при и давлении 4 мм рт.ст. удаляют хлороформ, после чего остается 177,2 г белого кристаллического вещества,гВ результате анализа (ядерный спиновый резонанс) этого вещества найдено, что оно представляет собой смесь оловоорганических дву- и тригалоидных соединений, а именно (CH2CH2COOCH3)2H С1 SnCH CHjCOCCH, (27 вес.%). Выход в расчете на прореагировавшее олово количественный. После промывки смеси диэтиловым эфиром, в котором хорошо растворяется трихлорид, остается белое кристаллическое вещество, которое после повторного анализа (ик-скопия, ядерной спиновый резонанс, элементарный анализ) идентифицировано как чистый CE2Sn{CH2CH2COOMe)2 С т.пл. 132°С. Пример 2. Аналогично примеру 1 в реакционную колбу загружают 60 г порошкообразного олова, 95,7 г метилакрилата и 110 мл диэтилового эфира. В смесь в течение примерно 14 ч при пропускают 42 кг сухого хлористого водорода. Как и в примере 1, растворитель удаляют, а остаток экстрагируют, после чего остается 3,7 г непрореагировавшего олова, и из экстракта извлекают 167,2 г белого кристаллического вещества. Это вещество представляет .собой смесь С125п(СН2СН2СООСН5}2И ,. CijSnCHjCHiCOOCHa (З.з вес.%). Выход,
рассчитанный на количество использованного олова, 98%.
Пример 3, Аналогично примеру 1 в реакционную колбу загружают 60 г порошкообразного олова, 37,1 г метилакрилата и 140 мл гексана и в течение 12,5 ч через смесь продувают 46 г сухого хлористого водорода. Реакционную смесь отфильтровывают, промывают 100 мл гексана и экстрагируют горячим хлороформом, после чего остается 1,5 г непрореагировавшего олова, а из экстракта выделяют 173 г кристаллического вещества.
В результате анализа этого соединения установлено, что оно представляет собой смесь (CHgCHgCOOCHg) ;и cejSnCHjCOGCHj (15,9 вес.%). Выход, рассчитанный на вес использованного олова, 99%.
Пример 4.В такую же реакционную колбу, как в примере 1, помещают 60 г порошкообразного олова и 95,7 г метилакрилата. Б течение 45 мин при перемешивании в смесь вводят 115 г соляной кислоты (35,4%), после чего перемешивание продолжают еще в течение 4 ч, Затем реакционную смесь отфильтровывают, промывают водой и экстрагируют хлороформом. Остается 14,9 г непрореагировавшего олова, а из экстракта получают 103,5 г твердого вещества, которое в результате анализа идентифицируют как чистый СEjSn(СН2СН2СООСН)2 , а остаток в виде хлористого олова содержится в промывочных водах.
Пример 5. Как и в примере 1 в реакционную колбу загружают 60 г порошкообразного олова и 174,2 г метилакрилата (также являющегося и растворителем). Затем в течение 15 ч в смесь вводят 40 г сухого хлористого водорода. Реакционную смесь отфильтровывают и промывают 20 г метилакрилата .
После экстракции хлороформом остается 5,0 г непрореагировавшего олова, а из экстракта извлекают 141,2 г кристаллического продукта, который оказывается чистым СEgSn(СН2СН2СООСНз)) что составляет 84,6% выхода в расчете на прореагировавшее олово. В фильтрате содержится 17,3 г указанного продукта, а общий выход составляет 95%.
Пример 6. При помощи метода, использованного в примере 1, в реакционную колбу загружают бОг порошкообразного олова, 95,7 г метилакрилата и 140 мл диэтилового эфира, затем в течение 10,5 ч в смес вводят 110 г сухого бромистсуго водорода.
После удаления растворителя остаток экстрагируют 300 мл горячего хлороформа, в результате чего остается 9,5 г непрореагиров&вшего олова.
После выпаривания экстракта получают 196,0 г твердого вещества,которое после анализа идентифицируют как смесь Br«Sn(CHc,CH7COOCH3J2(.137C) и Bri SnCHzCHjtCOOCHs (19,7 ), Выход в расчете на превращенное олово количественный.
Пример 7. В реакционную колбу, такую же, как в примере 1, загружают 60 г порошкообразного олова,
99,2 г окиси мезитила и 140 мл диэтилового эфира. Затем в смесь в течение 10,5 ч вводят 70 г сухого хлористого водорода.
После фильтрования и промывания
150 МЛ охлажденного в ледяной бане эфира полученный остаток экстрагируют 300 мл хлороформа. Из экстракта выделяют 84,6 г светло-коричневого кристаллического вещества СК25п(СМе2СН2СОСНз)2 С т.пл. 158 С.
Выход, рассчитанный на прореагировавшее олово, составляет 43%. После выпаривания эфирного фильтрата получают еще 89,5 г темно-коричневого продукта, который, как оказалось,
содержит 40 Бес.%
CE2Sn C(CH)2 СН2СОСН312 40 вес . % CEjSnC (СН ;2CHgCOCHg. Конечный общий выход оловоорганических соединений примерно 80%.
Пример 8.В реакционную колбу, такую же, как в примере 1, загружают 60 г порошкообразного олова, 78,0 г метилвинилкетона и 40 мл диэтилового эфира. Затем в течение
14 ч в смесь вводят 54 г сухого хлористого водорода. Реакционную смесь отфильтровывают для удаления следов непрореагировавшего олова (примерно 0,1 г), а затем выпаривают при
температуре 100°С и давлении 4 мм рт.ст., в результате чего получают 162,4 г темно-коричневого твердого вещества. В результате анализа было найдено, что это вещество содержит
примерно 40 вес.% С CjSn (CHj CHj СОСНэ)
и 40 вес.% CE SnCHjСН СОСНз.
Общий выход оловоорганических соединений примерно 80% в расчете на прореагировавшее олово.
Пример 9.В реакционную колбу, такую же, как в примере 1, загружают 60 г порошкообразного олова, 91,5 г хлористого акрилоила и 140 мл диэтилового эфира, В течение
19,5 ч в смесь вводят 60 г сухого .
хлористого водорода. После фильтрования реакционной смеси из нее удаляют 24 г непрореагировавшего олова, а затем смесь выпаривают. Остаток экстрагируют 300 мл горячего хлороформа, после чего экстракт упаривг ют и получают 103 г твердого коричневого вещества. В результате анализа установлено, что это вещество содержит в основном СtgSnCHjСН СОСJ
к некоторое количество
CEgSnCCHjCHjCOCE) . Точное определение выхода оказалось невозможно провести вследствие наличия органиче.ского материала.
Пример 10. В реакционную колбу, такую же как в примере 1, загружают 60 г порошкообразного олова, 129,6 г н-бу гилакрилата и 140 г диэтилового эфира. В течение 20 ч в колбу вводят 54 г сухого хлористого водорода. После фильтрован-ия реакционной смеси отделяют 0,2 г непрореагировавшего олова, после чего фильтрат упаривают и получают 224 г чистой бесцветной жидкости, которая, как установлено в результате анализа, состоит в основном иэ СtgS(CHgСНзСООСдН а и небольшого количества
СЕ2,-5пСН2 СН2СООС4Н9 . Общий выход составляет примерно 97% в расчете на прореагировавшее олово.
Пример 11. В реакционную .колбу, такую же как в примере 1, загружают 60 г порошкообразного олова 101,2 г метилметакрилата и 140 мл диэтилового эфира. Затем в течение 22 ч вводят 44 г сухого хлористого водорода. Реакционную смесь выпаривают и остаток экстрагируют 300 мл горячего хлороформа, В результате этого отделяют 33,3 г непрореагировавшего олова, а из экстракта выделяют 67,3 г кристаллического вещества, которое состоит из СГ25п(СНлСНСНэСООСНз)2 С т.пл. и Cf-jSnCHCHgCOOCHg (57,5 вес.%). Общий выход в расчете на прореагировавшее олово 84%.
Приме.р 12. В реакционную колбу, такую как в примере 1, снабженную рубашкой для обогрева, загружают 60 г гранулированного олова и 129,6 г н-бутилакрилата. Затем содержимое колбы нагревают до 129с, после чего в течение 12 ч пропускают 78 г сухого хлористого водорода. Реакционную смесь отфильтровывают для отделения непрореагировавшего олова (9,8 г), а фильтрат выпаривают для удаления оставшихся в качестве побочных продуктов бутилакрилата и хлористоводородного акрилата. После этогоостается 179,8 г чистой, практически бесцветной жидкости, которая, как установлено в результате анализа, содержит в основном
CEjSn (СН2 CHCOOC4H-f )2 Г Выход в расчете на прореагировавшее олово 95%. Конечный продукт слегка загрязнен полибутил акрилатом .
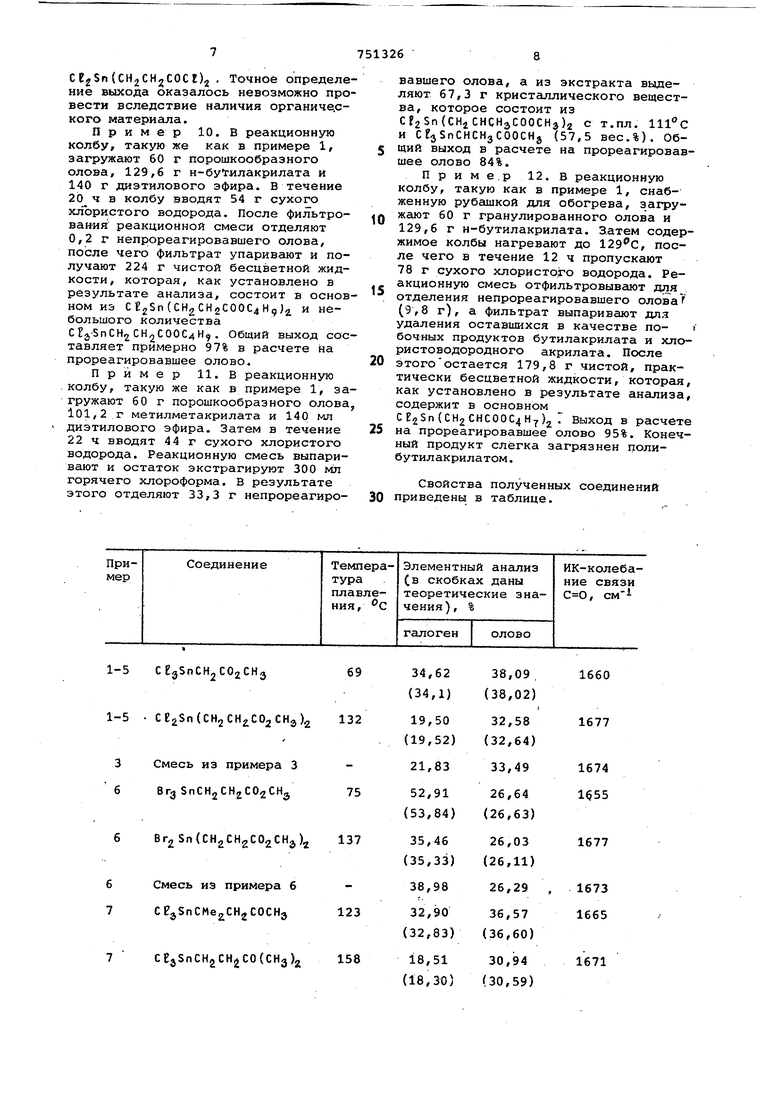
Свойства полученных соединений 30 приведены в таблице.



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения 2-хлорциклобутанонов или 2-хлорциклобутен2-онов | 1975 |
|
SU608468A3 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 3-АМИНОИЗОХИНОЛИНА | 1987 |
|
SU1540231A1 |
| Способ получения галоидводородных солей адриамицина | 1986 |
|
SU1428207A3 |
| Способ получения производных оксимов | 1980 |
|
SU1005656A3 |
| Способ получения октагидро- @ -пирроло- @ 2,3- @ -изохинолинов или их солей,рацематов или цис-,или транс-изомеров | 1981 |
|
SU1048985A3 |
| 4-МЕТИЛ-4-(1,1-ДИХЛОРО-2-ЦИКЛОПРОПИЛМЕТОКСИЭТИЛ)-1,3-ДИОКСАН, ОБЛАДАЮЩИЙ ГЕРБИЦИДНОЙ АКТИВНОСТЬЮ | 1993 |
|
RU2086547C1 |
| СПОСОБ ПОЛУЧЕНИЯ АЛКИЛОВЫХ ЭФИРОВ | 1971 |
|
SU297183A1 |
| Способ получения производных 3-азабицикло (3,1,0)-гексана или их солей, рацематов или оптически-активных антиподов | 1977 |
|
SU786891A3 |
| Способ получения производных гексагидроазепина или пиперидина, или пирролидина (его варианты) | 1978 |
|
SU1301311A3 |
| Способ получения производных пиридина или их солей | 1974 |
|
SU633475A3 |

1-5CEgSnCHjCOjCHg 1-5 СЕ2$п(СН2СН2;С02СНэ)2 132 3 Смесь из примера 3 6Вгз 5пСН2СН2С02СНд Вг25п(СН2СН2С02СН5)2 137 Смесь из примера 6 CEgSnCMe CHgCOCHg СЕз5пСН2СН,СО(СНз)2158 38,09 . 34,62 (38,02) (34,1) 19,50 32,58 (32,64) 19,52) 21,83 33,49 38,98 26,29 32,90 36,57 (36,60) 32,83) 18,51 30,94 18,30) (30,59) соединений общей формулы (R)2SnX2 и/или RSnXj R - радикал структуры сн-с - X - хлор или бром, отличающийся тем, что пр водят взаимодействие металлического ,олова/ галоидводорода и. олефина общей формулы
Продолжение таблицы. где R. R2 R3 И- CHjj Кд -СОСНэ, -СООСНд, -СОС или СООС4Н9, при температуре 20-100 С. Источники информации, принятые во внимание при экспертизе 1.Кочетков К.А. и др. Методы элементоорганической химии. М, наука , 1968, с. 181. 2.Патент Нидерландов № 144283, кл. С 07 F 7/33, опублик. 1971.
Авторы
Даты
1980-07-23—Публикация
1976-03-17—Подача