Изобретение относится к способу получения новых, не описанных в литературе 4-дифенилметилен-1-оксибен зилпиперидинов общей формулы где R. - Кд - независимо друг от дру га один водород или галоген, один галоидмётил или алкил или алкоксил с 1-4 атомами углерода, или их соле которые обладают фармакологическими свойствами. в частности оказывают благоприятное воздействие на мозговое, периферическое и коронарное кровообращение, а также противоспаз матическое действие на центральную нервную систему. В патентной и технической литера туре щирово описано алкилирование пиперидина галоидалкилами 1. Целью изобретения является разра ботка способа получения новых произ водных пиперидина или их солей, обладающих ценными свойствами. Поставленная цель достигается предлагаемым способом, который основан на известной вышеизложенной реакции . Согласно изобретению описывается способ получения 4-дифенилметилен-1-оксибёнзилпиперидинов общей формулы I или их солей, заключающийся в том, что 4-дифенилметиленпиперидин общей формулы KI R4 имеют указанные значения. с производным подвергают конденсации бензила общей формулы X- Йнг где X - галоген, Rg.- защитная для оксигруппы группа, такая как бензоил, в присутствии акцептора кислоты в инертном растворителе с последующим щелочным гидролизом полученного при этом соединения и выделением целевого продукта в свободном виде или в виде соли.
Предпочтительно в качестве инертного растворителя используют ксилол, в качестве акцептора кислоты - неорганическое основание, например карбонат натрия.
Для выделения целевого продукта в виде соли используют фармацевтически приемлемые кислоты, например соляную.
Пример. 1, 4-(4-трет-Бутилдифенилметилен) -1- (4-оксибензил)-пиперидин.
а В течение 4 ч при 120с нагревают смесь 18,.4 г 4-(4-трет-бутилдифенилметилен)-пиперидина, 20 г бромида 4-бензоилоксибензила и 9,5 г безводного карбоната натрия в 50 мл ксилола. Реакционную среду фильтруют после охлаждения для отделения образовавшегося бромида натрия а фильтрат экстрагируют с разбавленной соляной кислотой (15 мл концентрированной соляной кислоты, разведенные в 40 мл воды). 1-(4-Бензоилоксибензил) -4-.С4-трет-бутилдифенилметилен)-пиперидин осаждают в виде его хлоргидрата, который является Малорастворимым и который отделяют фильтрованием. Его рекристаллизуют в изопропаноле. Выход 85%, т.пл.. 259261°С (изопропанол).
б) Нагревают с обратным потоком смесь 10 г ранее полученного соединения и 10 г гидроокиси калия в 200 мл этанола. Продолжают отгонять спирт и постепенно заменяют его водой. После отгонки спирта медленно добавляют разбавленную соляную кислоту (20 мл концентрированной соляной кислоты, разбавленные в 25 мл воды). Мало-, растворимый хлоргидрат осаждается и отделяется при декантации реакционной среды. Затем осадок дважды промывают теплой водой и подвергают его рекристаллизации.в изопропаноле для получения хлоргидрата 4-(4-трет-бутилфенилметилен)-1-(4-оксибензил)-пиперидина, т.пл. 202-204С (изопропанол). Выход 72%.
Следующие промежуточные {стадия а) и целевые (стадия б) соединения были получены аналогичным образом.
Представленные точки плавления, если только нет других указаний, являются точками плавления хлоргидратов. В действительности точки плавления зачастую не очень четкие (пределы отклонения 1-5°С), это объясняется тем, что полученные соединения часто содержат малые количества растворителя.
2) 4-(4-трет-Бутилдифенилметилен-1-(2-оксибензил)-пиперидин
а)С.збН,,-,102НС, т.пл, 205-207°С (изопропанол)
б)C qH g NO-HC, т.пл. 150-152С (ацетонитрил)
3) 4-Дифенилметилен-1-(4-оксибензил)-пиперидин
а)Ц2 29 02-нее, т.пл. 246-248с (изопропанол)
б),. НС, т.пл. 244-24бс (изопропанол), 189-190 С (свободное
основание)
4) 4-Дифенилметилен-1-(3-оксибензил)-пиперидин
а)СззН Од. НС1, т.пл. 249-251 с
б)С дНгбО.НС, т.пл. 148-150 С (ацетонитрил)
5 4-Дифенилметилен-1-(2-оксибензил )-пиперидин
а)C32H2pN02.-HCl, т.пл. 214-21б С
б)Cgs Нд5.ЫОH.CF, т.пл. 156-158С (ацетонитрил) (размягчается уже при
132С), 148-149 С (свободное основание)
6) 4-(2-Хлордифенилметилен)-1-(4-оксибензил)-пиперидин а) CsgHggCINOg-HCl, т.пл. 26426бС (изопропанол)
6)C25-tt24CNO-НС1 , т.пл. 248250 С {изопропанол), 193-194С (свободное основание),-т.пл. фумарата 130-140°С, т.пл. малеата 110-112с.
7)4-(2-Хлордифенилметилен)-1-(3-оксибензил)-пиперидин
а) C, т.пл. 254256 0 (изопропанол)
) С, H.CING-HCI , т.пл. 242244 0
8)4-(2-Хлордифенилметилен)-1-(2-оксибензил)-пиперидин
а)С,„Н-,,С1МО„- НС) , т.пл. 200202°С 26
б)C25-H24CINOнС , т.пл.
9)4-(3-Хлордифенилметилен)-1-(4-оксибензил)-пиперидин
а)C aHggClNO - НС1, т.пл. 242244°С (изопропанол)
б)С25 H 24CINOHC1 , т.пл. 23423б°С изопропанол
10)4-(3-Хлордифенилметилен)-1-(3-оксибензил)-пиперидин
а) С,,,Н5йС1НО„ НС1 , т.пл. 221223°С
б) C25H24C1NO.НС1, т.пл. 156157 с изопропанол
.11) 4-(4-ХлорДифенилметилен)-1-(4-оксибензил)-пиперидин а) С„„Н«дС1НО-. НС1, т.пл. 244246 0
б) Cgj H Cl-NO-HCl , т.пл. 232-233 С (изопропанол)
12) 4-(4-Хлордифенилметилен)-1-(3-оксибензил)-пиперидин
а) С.„Н„дС) НС1, т.пл. 1921940с
.6) С,,H54C1NOHC1, т.пл. 1431450с (бензол)
13) 4-(4-Хлорлифенилметилен)-1-(2-оксибензил)-пиперидин
а) 1 NOg НС1 (на одну молекулу ацетона кристаллизации), т.пл. 112-114°С (ацетон) б) С 5 24С 0-МС т.пл. 240-241с 14)4-(4-Фтордифенилметилен)-1-(4-окси6ензил)-пиперидин а)Сj2H2efNOg- НС1, т.пл. 233234С (изопропанол) б) НС1 , т.пл. 230-232 (бензол) 15)4-(4-Фтордифенилметилен)-1-(3-оксибензил)-пиперидин а)Сз2НоеРМО„-НС, т.пл. 227,228°С (бензол) б)Ci H FNOHCl , т.пл. 125-126 (бензол) 16)4-(4-Фтордифенилметилен)-1-(2-оксибензйл)-пиперидин а)С.Э2Н28 ОйИС1., т.пл. 100102С (бензол) б)С2зН24 0 С1, т.пл. 211-213 17)4-(3-Фтордифенилметилен)-1-(4-оксибензил)-пиперидин а)CaoHoaFfJOo НС1 , т.пл. 254256 С (бензол) б)Сг Н РМОHCI, т.пл. 242-. 24б°С (изопропанол) 18)4-(3-Фтордифенилметилен)-1-(3-оксибензил)-пиперидин а)Сз2HsfiFNOg-НС1, т.пл. 241243°С (ксилол) б)C H24FNO-HC1 , т.пл. 145147°С (ацетонитрил) 19)4-(2-Фтордифенилметилен)-1-(4-оксибензил)-пиперидин а)С52Н2в ОйНС1 ,. т.пл. 267269°С (изопропанол) б)C25Ha4NO НС1 , т.пл. 245-247 20)1-(4-Оксибензил)-4-(4-трифторметилдифенилметилен)-пипериди а; Cjj ,.,- НС1 , т.пл. 242 ri Ч V. б) C2 H24F3NO-HC1 , т.пл. 228229°C (этилацетат) 21)1-(3-Оксибензил)-4-(4-триф метилдифенилметилен)-пиперидин а)Сз,,Н2е FjNOjjНС1 , т.пл. 201203 0 (эгилацетат) б)C-ft H xF NO-HCl , т.пл. 129131 С22)1-(4-Оксибензил)-4-(3-триф метилдифенилметилен)-пиперидин а) NO,-HC1 , т.пл. 229231 С (метанол) б)CjjHa FjjNO-HCl, т.пл. 229230С (этилацетат) 23)1- (3-Оксибензил)-4-(3-триф метилдифенилметилен)-пиперидин а)е H,,oFaNO, НС1 , т.пл. 215217 Сб)C26H24F NO-HC1, Т.ПЛ. 148-1 24)1-(2-Оксибензил)-4-(3-триф метилдифенилметилен)-пиперидин а)Производное бензоилокси был подвергнуто гидролизу без изолиро ния б)C26H.24FxNO- НС1 , Т.пл. 158-15 ((изопропанол) 25)1-(4-Оксибензил)-4-(2-триф метилдифенилметилен)-пиперидин а)C HjgFjNOj. НС1 , т.пл. 242244 0б).F,N0-НС 1 , т.пл. 2502S2C (метанол) 26) 1- (2-Оксибе.чзил )-4- (2-трифторетилдифенилметилен)-пиперидин а)C,, 0 . НС1 , т.пл. 12527 СS С- Н F-N0 .НС , т.пл. 13234°С21) 1-.(4-Оксибензил )-4- (4-метокси-, ифенилметилен)-пиперидин ) . ,,., NO.J- НС1 , т.пл. 243б)С2.6Н27 NOj. НС1 , т.пл. 222-223 0, 28)1-(2-Оксибензил)-4-(4-метокидифенилметилен)-пиперидин а) №г-НС1 , т.пл. 115-120°С этилацетат) (мало четкости) б) HsvNO-j.-НС) , т.пл. 2 3-224°С 29)1-(4-Оксибензил)-4-(2-метокидифенилметилен)-пиперидин а) NO,-HC1 , т.пл. 242-243°С изопропанол) б)C26H27N02.-НС1 , Т.ПЛ. 251-252°С 30)1-(3-Оксибензил)-4-(2-метокидифенилметилен)-пиперидин а)Ci-iH-i, НС1 , т.лл. 210-212С (бёнзолУ б)C.2J, , т.пл. 220-222°С (изопропанол) 31)1-(2-Оксибензил)-4-(2-метоксиифенилметилен)-пиперидин а)С j Н,,1 N0,,- НС1 , т.пл. 181-182с б)Со Н тМО-г.. НС , т .пл. 128-130с (бензол) 32)4-(3,4-Диметилдифенилметилен)1-(4-оксибензил)-пиперидин а),-НС , т.пл. 2б7-2б8°С метанол б)C27H2 NO.HCI, т.пл. 248-250°С 33)4-(3,4-Диметилдифенилметилен)1-(3-оксибеИзил)-пиперидин а)Cj Hj NO --НС1 , т.пл. 235-23бс (изопропанол) б)Cj-jH O-HC , т.пл. 147-149 0 (бензол) 34) 4-(3,4-Диметилдифенилметилен) 1- (2-оксибензил)-пиперидин а)C H NOj-HC, т.пл. 162-164 с б)C,H.j,NO-HC , т.пл. 203-205С (этилацетат) 35) 4-(4-Хлор-4-фтордифенилметиен)-1-(4-оксибензил)-пиперидин а)Сз2Н,С НС , Т.пл. 221-. (бензол) б)(jHjjCl FNO-НС , (на 1 молекулу ензола кристаллизации), т.пл. 1343бс36 ) 4- (4-Хлор-4 фтордифенилмети- , ен)-1-(3-оксибензил)-пиперидин . а)CjjH C FNO НС , Т.пл. 236238 С (избпропанол) б)L2st 2; }f Q-(i , т.пл. 229-230 0 37)4-(4-Фтор-4-трифторметилдифеилметилен)-1-(4-оксибензил)-пипериина) т.пл.228-229 С (изопропанол) б)С2,Н2/ N0НС1 , т.пл. 223-225 с (бензол) 38)4-(4-Фтор-4-трифторметилдифенилметилен)(3-оксибензил)-пипериин
а)Производное бензоилокси было подвергнуто гидролизу без изолирования
б)C2(,.HCl , т.пл. 134-135°С (ацетонитрйл)
39)4-(4-Фтор-З-трифторметилдифенилметилен)-1-(4-оксибензил)-пиперидин
а)CgaHjyF НС1 , т.пл. 21б-218с (бензЬл;
б) N0-НС1 , т.пл. 234-235С
40)4-(4-Фтор-З-трифторметилдифенилметилен)(3-оксибензил)-пиперидин
а) С,Н2/ N0,2 НС1 , т.пл. 174-17б с (этилацетат)
б) N0 НС1, т.пл. 133-135°С . 41) 4-(4-Фтop-4-мeтoкcидифeнилмeтилeн )-1-(4-оксибеизил)-пиперидин
а)С Н , т.пл. 223-225С
оЗ р
(этилацетат)
т.пл. 219-220°С
б)C2j,H2/N02 -НС (.изопропанол .
42)4-(4-Фтор-4-метоксидифенилметилен)-1-(3-оксибензил)-пиперидин
т.пл. 195-197С
а) (этилацетат) 140-141С
б) НС1 , т.пл. (изопропанол)
43)1-(4-Оксибензил)-4-(4-пропоксидифенилметилен)-пиперидин
а) C jHgjNO, НС , т.пл, 204-20б°С (ацетонитрйл)
НС1 , т.пл. 225-227°С
6) (ацетонитрйл 7
44)1-(4-Оксибензил)-4-(4-изопропилдифенилметилен)-пиперидин CoJk NO НС1, т.пл. 253-254°С (эт1.2.0
нол)
45)4-(4-Хлор-З-метилдифенилметилен)-1-(4-оксибензил)-пиперидин
. С„,Н-,СемО-НС , т.пл. 221-223°С
,Jjdo i:c7.
(этилацетат)
46)4-(4,4-Дихлордифенилметилен)-1-(4-оксибензил)-пиперидин
т.пл. 166-168 С
Cj H cejNo-Hci
(изопропанол).
Формула изобретения
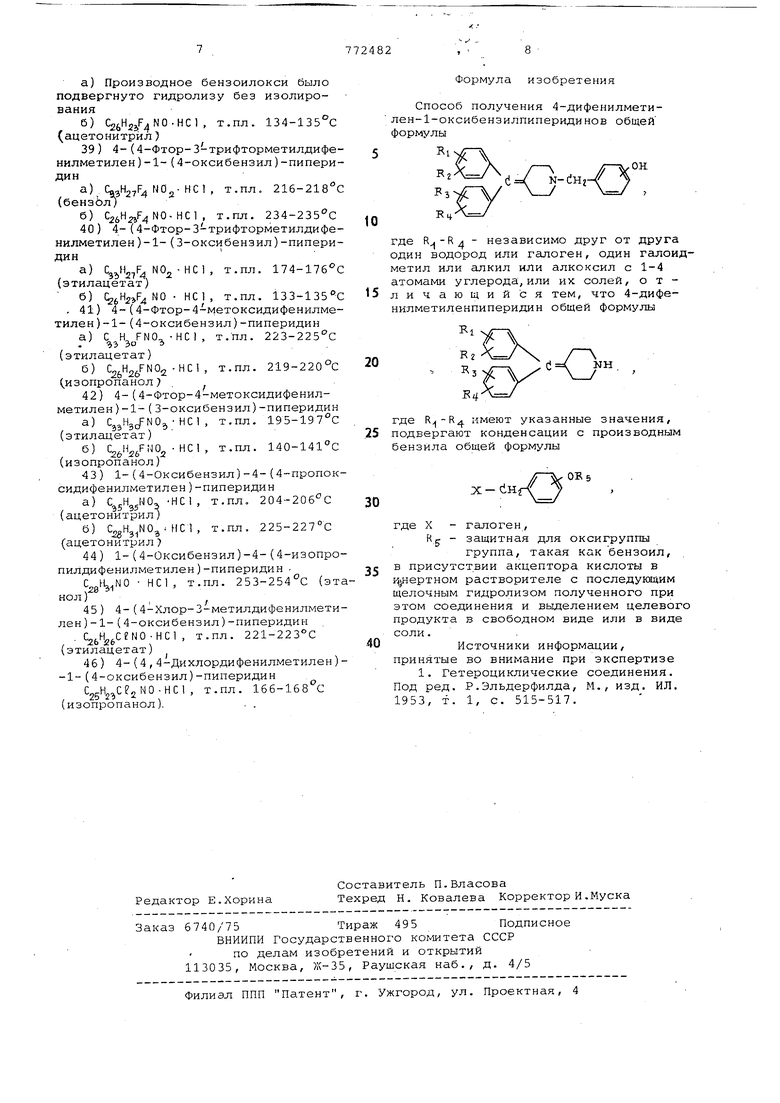
Способ получения 4-дифенилметилен-1-оксибензилпиперидинов общей формулы
где независимо друг от друга один водород или галоген, один галоидметил или алкил или алкоксил с 1-4 атомами углерода,или их солей, отличающийся тем, что 4-дифенилметиленпиперидин общей формулы
где имеют указанные значения, .25 подвергают конденсации с производным бензила общей формулы
где X
галоген,
5 защитная для оксигруппы группа, такая как бензоил, в присутствии акцептора кислоты в ty-iepTHOM растворителе с последующим щелочным гидролизом полученного при этом соединения и вьщелением целевог продукта в свободном виде или в виде соли.
Источники информации, принятые во внимание при экспертизе 1. Гетероциклические соединения. Под ред. Р.Эльдерфилда, М., изд. ИЛ. 1953, т. 1, с. 515-517.




Авторы
Даты
1980-10-15—Публикация
1978-01-10—Подача