Гидрохлориды формулы I получают конденсацией 4-дифенилметиленпиперидина формулы где А и А имеют приведенные значения, с бензилом формулы OAj . (ю) где X - атом галогена или реакцион способнгш эквивалентная группа; А - защитная группа гидроксиль ной группы, легко удаляема путем гидролиза, например бензоильвая группа, в присутствии акцептора кислоты в растворе инертного растворителя, например в ксилоле, и подвергают гидролизу полученный таким образом 1-бензил-4-дифенилметиленпипериди О-™ - А имеют приведенные знагде А, чения. Исходные 4-дифенилметиленпириди ны и 4-дифенил ютиленпиперидины об .щей фирмуjoj II имеют следуюгкие сво ства: 4- С2 Е РИфторметиддифенилметиле -пиперидин, т. кип. 128-130 С/О,0 рт. ст.); 4-(З-Фтордифенилметилен)-пипери дин, т. кип. 142-144 С/О,001 мм рт.ст.,т, пл. 45-4бс, 4-(4-фтор-4 -трвфторметилдифеии метилен)-пиперидин, т. кип. 130134 С/0,001 мм рт.ст. Пример 1. 4-Дифенита1етилен-1 дроксибенэилпиперидин. 4-(2-Хлордифенилмвхилен)-1-(4роксиОенэил)-пиперидин. В течение 4 ч при нагрев смесь 20 г (0,07 моль) 4-(2-хлордифенилметилеи)-пиперидина, 24 г бромистого 4-бе11зоилоксибензила и 12 г безводного углекислого нат рия в 45 мл ксилола. Реакционную смесь отфильтровывают после охлаж |деиия с целью отделения образовав шегося бромистого натрия. Фильтра экстрагируют разбавленной соляной ., кислотой (15 мл соляной кислоты разбавляют 80 мл воды). Осажденный в виде его хлоргидрата малорастворимый 1-(4-бензоилоксибензил)-4-(2-хлордифенилметилен)-пиперидин отделяют фильтрованием и перекристаллизовывают из изопропилового спирта. Выход составляет 81,6% (30,3 г). Т. пл. 275-277 С (изопропиловый спирт). Элементный анализ. Рассчитано %: хлор общий 13,36, CI® 6,68;N 2,64. .eCINO - НС I Найдено, %: хлор общий 13,25 CI® 6,75, N 2,63. Кипятят смесь 30 г полученного соединения и 11 г перекиси калия в 450 мл этанола. Спирт отгоняют и последовательно замещают его водой. Затем медленно добавляют избыточное количество хлористоводородной кислоты, разбавленной до 50%. Осажденный малорастворимый хлоргидрат отделяют фильтрованием. Осадок промывают два раза теплой водой и производят перекристаллизацию из ацетонитрила. Получают 20 г (выход 67%) хлоргидрата 4-(2-хлордифенилметилен)-1 -(4-гидроксибензил)-пиперидина. Т. пл. 249-251с (ацетонитрил). Т. пл. основания 193-194 С, т. пл. фумарата 130-140с, т,.пл. малеата 110-И2С. Элементный анализ. Рассчитано, %: хлор общий 16,63; С1 8,31; N 3,28. ,CINO HCI Найдено, %: хлор общий 16,30; С1 8,36; N3,34. Аналогичным образом получают и последуницие соединения. Указанные температуры плавления относятся к хлоргидратам. Температуры плавления иногда недостаточно четко вырешены (расхождение на 1- С). Это объясН}1 ется тем, что приготовленные сое- динения часто удерживают незначительное количество использованного растворителя. Через а) указан промежуточный 1-бензоилоксибенэил-4-дифенилметиленпиперидин общей формулы IV, через б) - /1онечный 4-дифенилметилён-1-гидроксибензилпипёридинобщей формулы I. П р и м е р 2. 4-Дифенилметилен-1-(4-гидроксибензил)-пиперидин. Рассчитано, %: ,14; N 2,80. а)C,-Il2.QNOi HCI Найдено, %: CI® 7,08; N 2,78. Т. пл. 246-248с (изопропиловый спирт). Рассчитано, %: CI® 9,04; N 3,57. б)C eHzsNO- HCI Найдено, %: CI® 9,20; N 3,56. Т. пл. 244-246 С (иэопропиловый спирт), т. пл, основания 189-190 С (этанол). Пример 3. 4-(3-Хлордифенилметилен)-1 -(4-гидроксибензил)-пиперидин. Рассчитано, %: хлор общий 13,36, CI® 6,68-, N 2,64. а)CjaH-j.gCIN02- HCI Найдено, %: общий хлор 12,92, CI® 6,й5; N 2,70. Т. пл. 242-244 С (изопропиловый спирт). Рассчитано, %: хлор общий 16,63; CI 8,31; N 3,28. б)Ci5Ha.4CINO-I CI Найдено, %: хлор общий 16,75, С1 8,30, N 3,36. Т. пл. 234-236 С (изопропиловый спирт)... Пример 4. 4-(4-Хл9РДИфенилметилен)-1 -(4-гидроксибеизил)-пиперидин. Рассчитано, %: хлор общий 13,36 С1 6,68, N 2,64. а)Cj HieCINQi-HCI Найдено, %: хлор общий 13,10; CI® 6,95; N 2,73. Т. пл. 244-246 С. Рассчитано, %: хлор общий 16,63 С1 8,31; N 3,28. б)Cj5 H-i CINO-HCI На1йдено, %: хлор общий 16,40; |С1 8,35; N 3,33. Т. пл. 232-233 0 (изопропиловый спирт). Пример 5. 4-(4-Фтордифенилметилен-1-(4-гидроксибензил)-пиперидин. Рассчитано, %: С1 6,90; N 2,72. а)CjjHa P Or HCI Найдено, %: С1 7,00, N 2,72. Т. пл. 233-234С (изопропиловый спирт) ., Рассчитано, %: С1 8,65; N 3,41. б)C:a.sHi4FNO- HCI Найдено, %: CI 8,72; N 3,42. Т. пл. 230-232 С (бензол). Пример 6. 4- 4-Фтордифенилметилен)(2-гидроксибензил)пиперидин. Рассчитано, %: С1 6,90; N 2,72. а)CjiH eFNOa HCI Найдено, %: CI 6,85, N 2,50. Т. пл. 100-102 С (бензол). Рассчитано, %: CI® 8,65/ N 3,41. б) ltd Найдено, %: CI 9,00; N 3,30. Т. пл. 211-213 с. Пример 7, 4-(3-Фторди фенилметилен)-1-(4-гидроксибензил)-пиперидин. Рассчитано, %: С1® 6,90; N 2,72. а) C5iH2.jFK(- HCI Найдено, %: CI® 6,95; N 2,74. Т. пл. 254-256 0 (бензол). сп бе ме t5 бе ле 20 зи 25, сп бе ме 30 35. -тр -ги 40 спи 45 50 ращ ни ан ве ус ми (А по щим мо ных фор 65;воо Рассчитано, %; CI® 8,65-; N 3,41. б) Ci5-H24.FNO- HCI Найдено, %: Си® 8,84, N 3,52. Т. пл. 242-24бС (изопропиловый ирт). Пример 8. 1-(4-Гидроксинзил)-4-(4-трифторметилдифенилтилен) -пиперидин. Рассчитано, %: С1 6,28; N 2,48. а)CjjHjgFjNOiHCI Найдено, %: ,53; N 2,56. Т. пл. 242-244 С. Рассчитано, %t CI 7,70; N 3,06. б)CU. Hi4F5NO-HCT Найдено, %: ,75; N 3,08. т. пл. 228-229 С (этилацетат). Пример 9. 1-(2-Гидроксинзил) -4- .(З-трифторметиЗтдифенилметин)-пиперидин. Бензоилоксипроизводное гидролировалось без выделения. Рассчитано, %: С1 7г70, N 3,06i б) C26H2 4l NO-HCI Найдено, %: С1®7,40, N 2,92. Т. пл. 158-160С (изопропиловый рт) . Пример 10. 1-(4-Гидроксизил)-4-(2-трифторметилдифенилилрн) -пиперидин . Рассчитано, %: ,28, N 2,48. а) (, Найдено, %: СГ 6,18; N 2,49. Т. пл. 242-244°С. Рассчитано, %: С1®7,70; N 3,06. б) Ci6H.z.4F,,NO-HCI Найдено, %: CI® 7,95, N 3,14. Т. пл. 250-252С( метанол). Пример 11. 4-(4-Фтор-4ифторметилдифенилметилан)-1-(4дроксибензил)-пиперидин. Рассчитано, %: С1®6,49; N 2,40. а),,llijf4 0 J CI Найдено, %: ,50; N 2,39. Т. пл. 228-22 С (изопропиловый рт). Рассчитано, %: С1 7,4i; N 2,93. б)СгбЯ зРд О-НС Найдено, %: Clf 7,35; N 2,98. Т. пл. 223-225 С {бензол). Фармакологические свойства. Активное воздействие на кровообение. Гемодинамический эффект соединеобщей формулы I наблюдают на стезированной собаке при искусстном дыхании в экспери14ентальных овиях. Измерения проводят зондапомещенными вокруг бедеренных , сонных (В) , j opOHapHoA (С) и воночной (D) артерий, определяюи мысоечно-кожный, сердечный и говой дебиты. Из полученных данследует, что соединения общей мулы Т значительно улучшают кробращение. При этих экспериментёос максимёОхьную оценку (2) давали тому соединению, под влиянием которого кровообращение повыиайпось за 20 мин, не менее чем на 20%. Максимгшьная оценка опыта, проводившегося на двух собаках, равняется,следовательно , 4. Возможны промежуточные оценки: от О до 4. Для сравнения приведены оценки для двух известных соединений - папаверина (х) и теофиллина {у) . Полученные результаты представлены в табл. 1. Как видно из табл. 1, сумма оценок дебитометрии для каждого испытанного соедданения свидетельствует о наличии явной сосудорасширяющей способности. Вместе с тем, обнаруживается известная специфичность действия в тех случаях, когда йсполь зованные для сравнения соединения оказг лись малодейственными. Указанные соединения представляют интерес для лечения заболеваний, вызванных недостаточным центральным или периферическим кровообращением. Токсичность. Токсичность предлагаемых.:, соединений относительно незначительна. В табл. 2 указана токсичность этих соединений, определенная на мышах, путем введения в брюшину, Токсичная доза - доза, убивгиощая одно животное из трех. Предлагаемые соединения могут вводиться орально внутрь, ректально парентерально. Разовый прием 10-50 мг, в зависимости от метода введения. Применяется с жидкими или твердыми наполнителями, Указанные гидрохлориды общей Формулы 1 улучшают кровообращение, обладают сосудорасширяющим действием. Т а б л и ц а 1
10 Продолжение табл.2



Формула изобретения
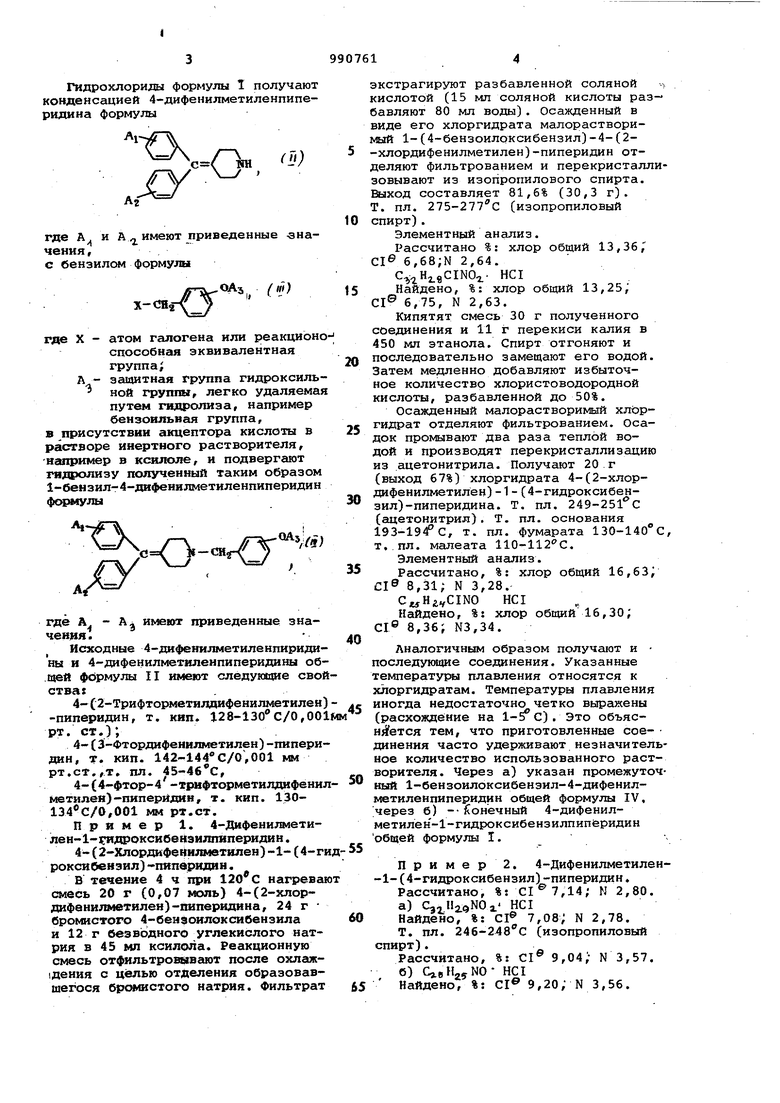
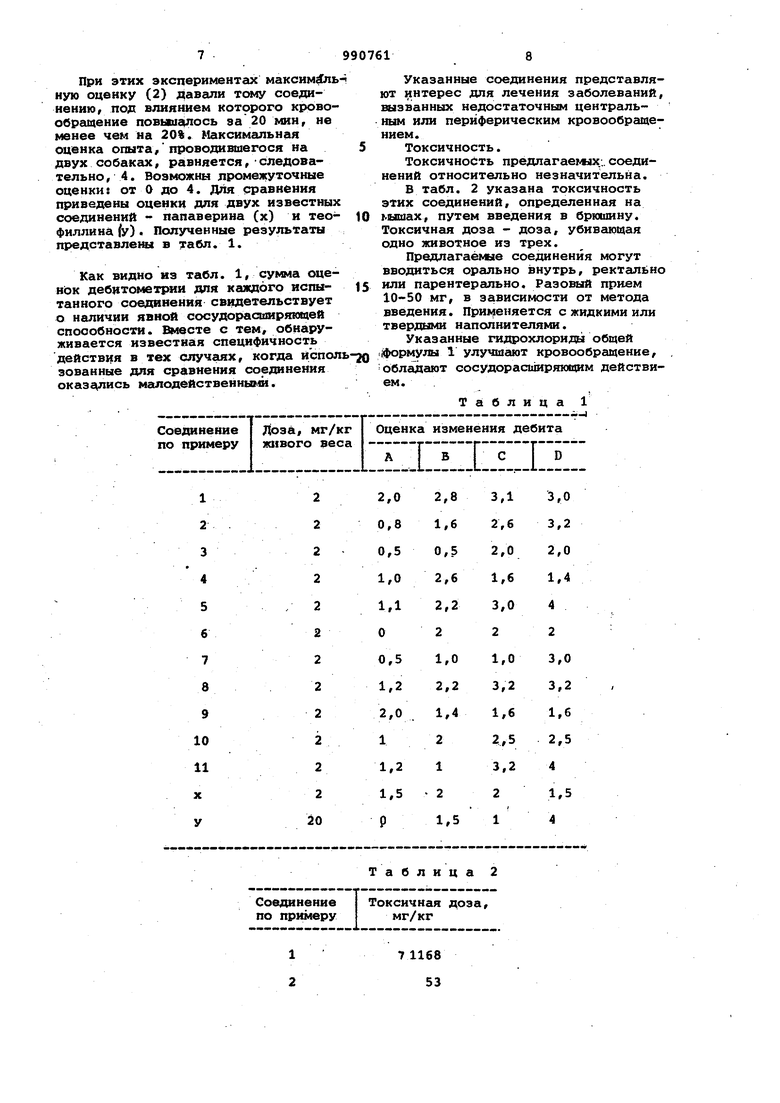
Гидрохлориды производных 4-дифенилметилен-1-гидроксибензилпиперидина общей формулы
Огде, если ОН-группа находится в-положении 4 бензольного кольца, то А обозначает атом водорода или атом хлора, находящийся в положении 2, 3 или 4 бензольного кольца, или атс фтора, находящийся в положении
3 или 4,- или трифторметил, находящийся в положении 2 или 4 бензольного кольца, а А - атом водорода, или Л - атом фтора в положении 4,
0 а АЗ - трифторметил в положении 4 бензольного кольца, если ОН-группа находится в положении 2, то А атом фтора в положении 4 или трифторметил в положении 3 бензольного
5 кольца, а А - атом водорода,
обладающие свойством улучшать кровообращение.
Источники информации, принятые во внимание при экспертизе
0

Авторы
Даты
1983-01-23—Публикация
1978-07-17—Подача