Выход ,37%; т. лл. 180° С.
Найдено, %: С 53,41; Н 5,31; N 4,75.
CuHisClNOs.
Вычислено, %: С 53,59; Н 5, N 4,46.
б)Гидратированный дихлоргидрат 5-ацетам,идо-4,7-диметоксин6-(4-метилстиперазиноэтокси)-бензофурана.
В течение 8 ч нагревают с обратным холодильником раствор L5,5 г (0,06 моль) 5-ацетамидо-6-(2-хлорэтокси)-4,7-диметоксибензофурана, приготовленного в .предыдущем примере, и 15 г (0,15 моль) N-мет.илпипераэина в 100 мл толуола. Фильтруют, упаривают в вакууме, вновь помещают остаток в спирт и добавляют хлористоводородный спирт. Фильтруют и кристаллизуют в абсолютном спирте.
Выход 55%; т. лл. 160° С.
Найдено, %: С 46,76; Н 6,73; N 8,34;
C.gHsgClaNsOs + 9/4 Н,О.
Вычислено, %: С 46,48; Н 6,88; N 8,56.
в)5-Ами.ноЧ,7-д.името1Кси-6-1 2- (iN-метилП|ИперазИнил)-этОКси -ббнзофура1н.
Нагревают с обратным холодильником 4 ч раствор 16,9 г гидратированного дихлоргидрата 5-ацетам1идо,7-диметокси-б-(4-метилпиперазиноэтокои)-бензофурана в 60 мм 2 Н. соляной кислоты. Подщелачивают концентрированной щелочью натрия, экстрагируют хлороформом и упаривают растворитель. Получают 9 г .кристалл и зов аи но го яродукта:
Выход 100%, т. пл. 62° С, мол. в.337, 394.
Найдено, %: С 60,i56; Н 7,62; N 12,67; Вычислено, %: iC 60,87; Н 7,51; N 12,53.
г)4,7-Диметокси-5-амИНО-М-метилкарба.моил-6- 2-(Ы - метилпиперазиинл) - этокаи бензофуран.
Нагревают до 70° С в течение 4 ч смесь 9 г 5-ами НО-4,7-диметойои-6-: 2-(:М-метилпипера3|инил)-этокои -бензофурана и 1,7 г метйлизоцианата в 100 мл толуола. Затем jnaривают растворитель, остаток вводят в изопропило1вый эфир, фильтруют, кристаллизуют в смеси 40-60% бензола и гептана.
.Получают 8 г целевого продукта. Выход 80%; т. пл. 1:18° С; мол. в. 410,46. Найдено, %: С 55,48; Н 7,08; N 13,93;
C,9«2 N40s-f« 0.
Вычислено, %: С 55,59; Н 7,37; N 13,65.
Пример 2. 4,7-Диметоксн-5- (N-метилкарбамиламино) -б- (пинеридинозтоксн) -бензофуран.
а)Хлоргидрат 5-ацетамидо-4,7-диметоксн-6- (пипериди)ноэтокси) -бензофураиа.
В течение 2 ч нагревают с обратным холодильником смесь 25,1 г (0,1 моль) 5-ацетамидо-4,7-димето:Ксин6-этоксибензофурана, 22,2 г (0,16 моль) 2-1пипер1Иди«охлорэтана и
41,.6 г (0,3 моль) карбоната калия в 250 мл ацетона. Затем фильтруют, упаривают растворитель, вновь помещают полученный остаток в ацетон и добавляют 20 мл хлористоводородного этанола 7N. Фильтруют
и кристаллизуют в 400 мл пропанола.
Выход 33%, т. пл. 260°С;
Найдено, %: С 57,35; Н 7,03; N 7,08;
C,9H27CIN205.
Вычислено, %: С 67,21; Н 6,82; N 7,02.
б)Дихлоргидрат б-амино-4,7-диметО(КСИ6-(2-пиперид.иноэтокси)-беизофурана.
В течение 10 ч нагревают с обрат1ным холодильником раствор 25,1 г (0,4 моль) 5-ацетамидо-4,7-диметокси-6- (2-.пиперидиноэтокои) -бензофура1на, .приготовленного на предыдущем этапе, в 200 мл соляной кислоты 2N. Затем нейтрализуют концентрированной содой, извлекают этилацетатом.
Упаривают растворитель, вновь помещают остаток в ацетон и добавляют 30 мл хлористоводородного этанола 7iN. Фильтруют и кристаллизуют в эташоле.
Выход 43%, т. пл., 203° С.
Найдено, %: С 51,72; Н 6,63; N 6,81;
Cl7H26Cl2N O4.
|Вычислено, %: С 51,48; Н i6,74; N 6,91. в) 4,7 - Диметокси-5-1М-метилкарбамидамнно-6-(2-п.и.перидиноэтокси)-бензофуран.
В течение 3 ч выдерживают при 80- 90° С в автоклаве смесь Ii6 г (0,05 моль)
5-ами1Но-4,7-диметокси-6- (2-и И1перидиноэтокси)-бензофурана, приуготовленного на иредыдущем этапе, и 3,2 мл (0,055 моль) изоцианата метила в 530 мл толуола. Затем испа)ряют растворитель, кристаллизуют полученное масло в петролей1ном эфире и рекристаллизуют в 1изоп1ропиловом эфире, т. пл. 120° С.
Выход 37%. Найдено, %: С 60,42; Н 7,29; N 11,30;
CigH27 N3O5.
Вычислено, %: С 60,46; Н 7,21; N 11,13.
ОСНз/
NH-CO-NC
O-CH-lCH lmI
OCHjR4:
Таблица

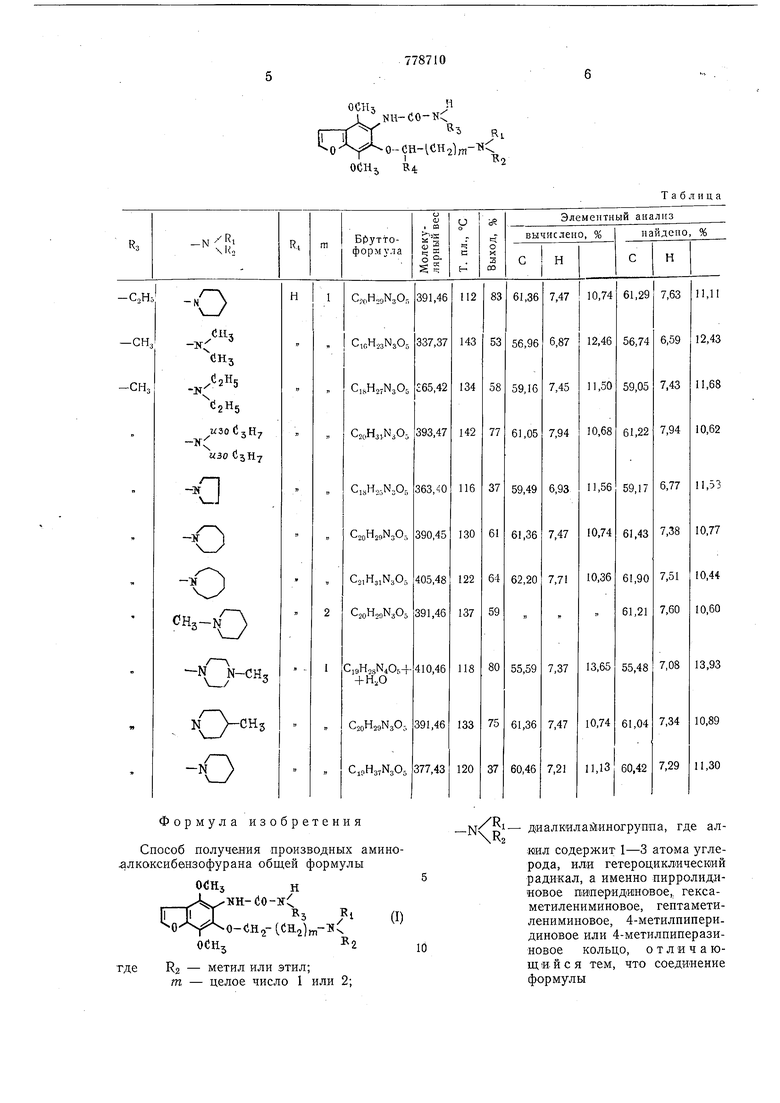


odH,
0- о-сн2-(н,) (
X
оси.
где m и имеют вышеуказанные
Ко
значения, подвергают взаимодействию с язоцианатом формулы
RgNCO(III)
где R2 - имеет вышеуказанные значения, в среде толуола при температуре 70-90° С.
Источник информации, принятый во внимание при экспертизе:
Приоритеты ло признакам:
12:07.76 при группа -N о -диалкил г 2
аминогруппа, где алиил содержит 1-3 атома углерода, или гетероциклический радикал, а именно пиррол.иди1новое, пииеридииОВое или 4-мепилли:перазиновое кольцо, т-целое число, равное 1 или 2, и Ra - метил или этил;
циклический радикал, а именно гексаметилениминовое, гептаметилениминовое или 4-метилниперидиновое кольцо, т - целое число, равное 1 или 2, и R2 - метил или этил.
Авторы
Даты
1980-11-07—Публикация
1978-12-25—Подача