Изобретение относится к области микробиологии, к получению антибиотиков. Предложенный антибиотик новый и способ его получения в патентной и научно-технической литературе не описан. Целью изобретения является полу чение нового антибиотика К. 582 М. Эта цель достигается тем; что штамм Hetarhizium anisopliae (Metsch) Sorok.Var,anisopliae 582 выращивают в аэробных условиях в жидкой питательной среде при 20-37 .и рН 3,0-8,0 с последующим выделением целевого продукта. Штамм Metarhizium anisopliae (Metsch) Sorok.Var .gni sopl iae 582 продуцирующий антибиотик, депониро ван в коллекции (банк вирусов) ведомства Японии (Kogyog I inВ i se i bu tsn-Kogyo - lejutsuiKen Kyujo и зарегистрирован под номером PER М-Р 4217 и под номером ЛТСС 20500. Культурально-морфологические пр знаки. Колонии на солодовом агаре достигают диаметра Ж,5-5,0 см за д недели при 25°с, имеют форму пучка или снопа. Колонии плоские или в некоторых случаях радиально вдавленные,, цвет колонии от темно-сероватозеленого до желтовато-зеленого и белого по краям. Обратная сторона колонии от желтого до кремового цвета. Мицелий бесцветный, имеет перегородки и ответвления-, конидиофоры короткие, бесцветные и имеют перегородки, мицелий мелкоразветвленной формы, затем образует массу тесно скомпонованных гирлянд. Гирлянда имеет цилиндрическую форму, бесцветная, концы тонкие с длинными цепями конидий. Конидий представляют собой одноклеточные плоские героспоры бледного желтовато-зеленого цвета, которые имеют цилиндрическую или удлиненную эллипсоидную форму и черыте закругленных угла. Длина и ширина конидии составляет 4,0-8,0 и 2,0-2,5 мкм соответственно. Агар Чапека: рост хороший, форма подушки, край-ресничный, образует споры от желтовато-зеленого до темно-зеленого цвета, пигмен г продуцирует . Агар Докса-Чапека: рост хороший, форма пуговицы, споры от желтоватозеленого до темно-зеленого цвета, пигмент продуцирует. Лгар Сабуро: рост хороший, форма подушки, образу эт споры от Желтовато-зеленого до темно-зеленого цвета. Пигмент отсутствует.
Лгар на отваре из кукурузной муки: рост плохой, край в Лорме зубцов в нерегулярном наборе, образует споры темно-зеленого цвета. Пигмент отсутствует.
Солодовый агар: рост довольйо плохой. Мицелий представляет собой тонкую плоскую структуру, край волнообразный, опоры от серовато-зеленого до темно-зеленого цвета. Пигмент продуцирует. Картофельный агар с декстрозой: рост довольно плохой, мицелий тонкий и плоский, край ресничный. Образует . темно-зеленого цвета. Пигмент продуцирует.
Желатиновый агар: рост довольно плохой, мицелий тонкий и плоский, край волнообразный, споры темно-зеленого цвета. Пигмента нет.
Обычный агар: рост плохой. Г .ицелий имеет Лорму тяжелых снежных хлопьев, край волнообразный. Спор нет, пигмента не образует.
В качестве среды для культивирования используют различные питательные вещества.
В качестве источников углерода используют различные сахара, такие как декстроза, сахароза, левулеза (Лруктоза), манноза, глицерин, различные сорта крахмала, мальтозу, ксилозу, лактозу, мелассу, маннан.
В качестве источников азота используют различные неорганические соли, такие как нитрат натрия, нитрат аммония, хлористый аммоний,а также органические азотистые вещества, такие как питательный бульон, пептон, жидкий кукурузный экстракт, дрожжевой экстракт, осевая мука, мука земляного (арахиса.) , аминокислоты. При необходимости -используют подходящие неорганические соли и вспомогательные вещества.
Культивирование предпочтительно осу1цествлять в жидкой среде.
Культивирование проводят в аэробHbjx условиях при 20-37, предпочтительно 28-30 С при рН 3,0-8,0, предпочтительно рН 5,4-5,6.
При необходимости в среду добавляют пеногаситель.
После завершения ферментации выделяют продукт Ферментации путем осаждения гидрофильным органическим растворителем, таким как этанол, ацетон, органической кислотой, например пикриновой, флавиановой, фосФовольфрг мовой кислотой, пентахлорфенолятом натрия, бензальдегидом, экстракцией метанолом или активными адсорбентами различного типа. А также используют способ очистки, основанный на применении ионообменных носителей, хроматогра 1ии на молекулярных ситах, способа плотности ориейтации, метода противоточного распределения, способа Фракционирования солями, растворителями или ионами металлов, метода электрофореза в различных его вариантах, способа выделения путем образования комплексного вещества.
Целевой продукт может быть выделен из культуральной среды с помощью осаждения с очисткой ионообменными смолами. Способ включает стадии фильтрования культуральной среды с применением фильтрующих средств,
5 обработки фильтрата катионообменной смолой в кислой среде или основным ионообменником и последующего элюирования целевого продукта кислотой или щелочью.
Полученный таким образом концен0трат дополнительно концентрируют ионообменной смолой, после чего к нему прибавляют соответствующие количества этанола и ацетона.
В результате получают сырую по5рошкообразную смесь К 582 М-А и К 582 М-В.
Полученный сырой порошок обрабатывают затем метанолом, окисью алюминия, активированным углем и прово0дят хроматографирование с помощью молекулярных сит, в результате чего получают очищенный продукт.
Полученный очищенный продукт может быть в дальнейшем подвергнут обработке различными хроматографическими методами с использованием таких сорбентов и носителей, как полиакриламидный гель, карбоксиметил (СМ)-сефадекс, с целью выделения индивидуальных продуктов К 582 М-Л
0 и К 582 М-В.
В табл.1 приведены физико-химические свойства полученных продуктов К 582 М-А и К 582. М-В.
Т аблица 1
5
50
55
«О
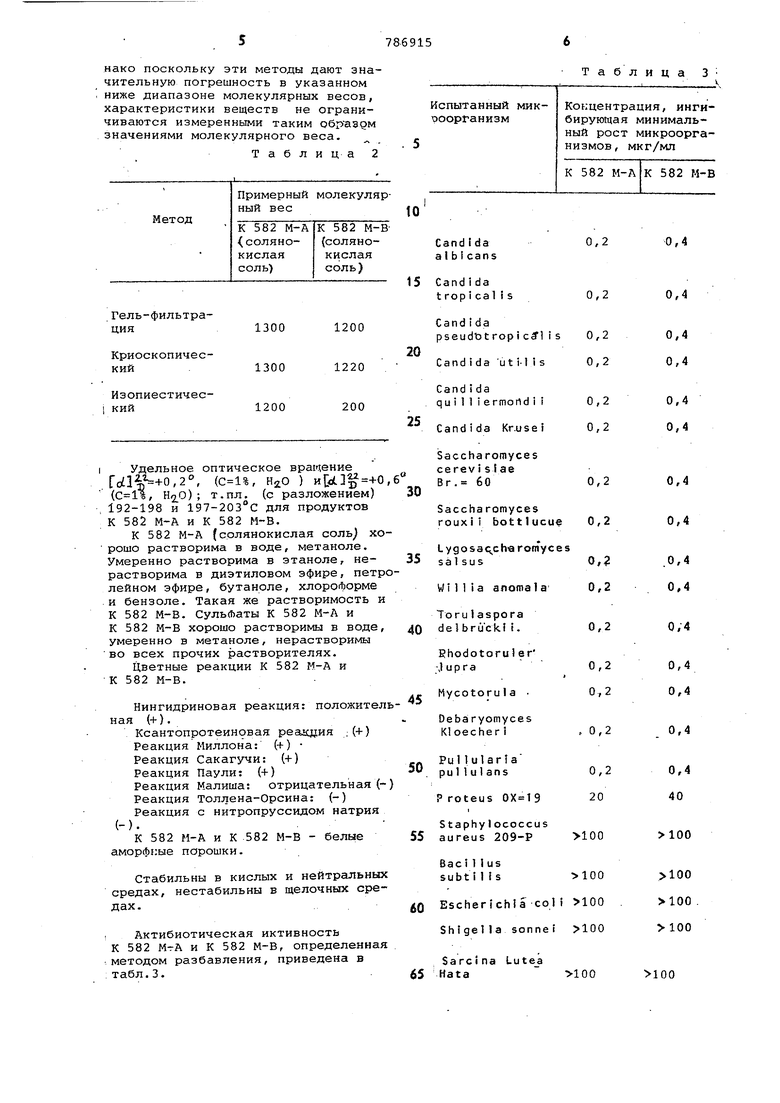
В табл.2 приведен молекулярный вес указанных продуктов, измеренный
65 тремя овисанньлми ниже методами ; однако поскольку эти методы дают значительную погрешность в указанном ниже диапазоне молекулярных весов, характеристики веществ не ограничиваются измеренными таким образдм значениями молекулярного веса.
Таблица 2
Таблица 3





| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения антибиотика @ -19393 @ и/или @ -19393 @ | 1980 |
|
SU1075984A3 |
| Способ получения баумицина а и в | 1977 |
|
SU867318A3 |
| Способ получения антибиотического комплекса | 1978 |
|
SU1039446A3 |
| Способ получения антибиотической смеси | 1979 |
|
SU1071226A3 |
| Способ получения антибиотика | 1972 |
|
SU470964A3 |
| Способ получения антибиотика казугамицина | 1964 |
|
SU454749A3 |
| Способ получения антибиотиков | 1975 |
|
SU528038A3 |
| Способ получения антибиотика 2188 и штамм плесневого гриба РеNIсILLIUм RUGULоSUм FERM ВР-142,используемый для получения антибиотика 2188 | 1983 |
|
SU1419521A3 |
| Способ получения веществ, обладающих антипаразитарной активностью | 1977 |
|
SU716524A3 |
| Способ получения антибиотиков А51568-фактора А и А51568-фактора В | 1983 |
|
SU1194285A3 |

1200 1300
1220
1300
1200
200 I Удельное оптическое вращение rotl% +0,2°, (, НгО ) иСс13 +0, (, ) ; т.пл, (с разложением) 192-198 и 197-203°С для продуктов К 582 М-А и К 582 М-В. К 582 М-А (солянокислая соль) хо рошо растворима в воде, метаноле. Умеренно растворима в этаноле, нерастворима в диэтиловом эфире, петро лейном эфире, бутаноле, хлороформе и бензоле. Такая же растворимость и К 582 М-В. Сульфаты К 582 М-А и К 582 М-В хорошо растворимы в воде, умеренно в метаноле, нерастворимы во всех прочих растворителях. Цветные реакции К 582 М-А и К 582 М-В. Нингидриновая реакция: положитель ная (+). Ксантопротеиновая реаэдия .(+) Реакция Миллона: (+) Реакция Сакагучи: (+) Реакция Паули: (+) Реакция Малиша: отрицательная (Реакция Толлена-Орсина: (-) Реакция с нитропруссидом натрия К 582 М-А и К 582 М-В - белые аморфные порошки. Стабильны в кислых и нейтральных средах, нестабильны в щелочных средах. Актибиотическая иктивность К 582 М-А и К 582 М-В, определенная методом разбавления, приведена в табл.3.
Продолжение табл. 3
Как видно из данных, приведенных в табл.3, К 582М-А и К 582 М-В проявляют высокую антибиотическую активность против микроорганизмов рода Candida и других дроЛжей.
Данные, характеризующие острую токсичность продуктов К 582 М-А и К 582 М-В, приведены в табл.4.
(Т а б л ц а 4
Активность к 582 М-А и К 582 М-В в ингибировании роста раковых опухолей. Противоопухолевое действие указанных веществ испытывалось на крысах, являющихся носителями раковых клеток.
Нескольким группам крыс, каждая из которых состояла из десяти крыс линии Донриу (самки весом 150- 200 г трансплантировали по Ю асцитных клеток рака печени АН 44 и АН 66, соответственно, причем пересадку клеток производили в хвостовую вену животных. По прошествии 72 ч подопытны крысам вводили перорально препараты К 582 М-А или К 582 М-В в дозе 30 мг/кг непрерывно в течение 10 дней, после чего крысы находились под наблюдением в течение 60 дней. Затем определяли процент выживаемости крыс, участвовавших в эксперименте. Как видно из данных, приведен-, ных в табл.5, при использовании указанных препаратов в каждой группе крыс, которым предварительно пересаживали раковые клетки, отчетливо проявлялся эффект ингибирования {подавления) опухолевых клеток, особенно наглядный при сравнении с выживаемостью в контроле, где крысы после пересадки опухоли получали только кормовую диетУ.
Таблица 5
в результате различных экспериментов обнаружено,что продукты К и К 582 способны оказывать влияние на иммунитет живых организмов (как гуморальный, так и клеточный) . Вещества обладают как ускоряющим, так и тормозящим (ингибирующим) действием на иммунную систему, что было показано гемолизиновым титровальньом методом при введении 30 эритроцитов овцы.
Нескольким группам мышей, каждая из которых состояла.из 5-10 самок линии ddli вводили внутрибрюшинно препарат К 582 МгВ в дозе 25 мг/кг и в озе 2,5 мг/кг в течение 4 дней, затем в хвостовые вены трансплантировали каждой 4-10 эритроцитов овцы и введение К 582 М-В проолжали еще в течение 4 дней. После завершения, этой процедуры производили измерение уровня антител в крови. Группа мышей, которым вводили по 25 мг/кг препарата К 582 М-В, показала содержание антител в крови на уровне 77% в расчете на аналогичную величину у контрольной группы, тогда как группа мышей, которым вводили 2,5 Мг/кг, показала средний уровень антител в крови порядка 234%, считая на содержание антител в крови животных контрольной группы. Группы мышей, которые получали более высокие концентрации при введении указанного препарата, продемонстрировали тенденцию к ингибированию иммунитета, тогда как группы, получавшие более низкие концентрации препарата К 582 М-В, продемонстрировали тенденцию к акселерации иммунитета.
- :Было обнаружено,что при введении препаратов К 582 М-А и К 582 М-В в живой организм наблюдается повышение уровня индуцирования интерферона в крови.
Пример, а) 200мл культура -льной среды (рН около 6), имеющей состав, %: 3,0 глюкозы,1,0 полипептона, 0,2 нитрата, натрия,0,1 дигидрофосфат калия, 0,05 хлористого калия, 0,05 сульфата магния, 0,01 сульфата двухвалентного железа, инокулируют куль.турой Metarhizlum anisopliae (Metsch Sorok .Var .anisopliае 582 M (штамм BIkoken FERM-P 4217, ATCC № 20500) И проводят культивацию в условиях встряхивания при температуре 30®С в течение 14-20 дней.
.б) Процедуру примера 1а) повторяют, но вместо 1,0% полипептона в культуральную. среду добавляют 0,1% смеси аминокислот (глицина, аспарагина, аргинина, гистидина, аланина и некоторых других, которые добавляют отдельно} ..
Пример 2.5л (5)ильтрата культурального бульйона,полученного в примере 1, фильтруют с добавлением гифло-суперцеля (средства, представляющего собой очищенную диатомитовую землю).
После доведения величины рН -до 6,0-7,0 полученный фильтрат пропускают через колонку, имеющую внутренний диаметр 20 и высоту 500 мм. и заполненную ионообменной смолой JPC-50 в смешанной водородно-натровой форме (Н Na) с целью поглощения; целевых веществ из культурального бу.льона. Колонку промывают водой и затем пропускают через нее 500 мл 1,0 н. раствора соляной кислоты со скоростью 10 мл/мин для элюирования целевых веществ. Величину рН элюата доводят до 6,0 и нейтрализованный таким образом элюат концентрируют в вакууме. Полученный концентрат оставляют на-ночь при температуре 35 С с добавлением пентахлорфенолята натрия с тем, чтобы вызвать осаждение
пентахлорфенолята смеси К 582 М-А и К 582 М-В. Полученный осадок пентахлорфенолята смеси К 582 М-А и К 582 М-В промывают ведой, затем растворяют в бутилацетате и полученный раствор дважды экстрагируют в делительной воронке разбавленным раствором соляной кислоты, имеющим рН 2,0-3,0 с целью получения водного раствора смеси солянокислых солей С гидрохлоридов) К 582 М-А и К 582 М.-В.
o Этот водный раствор промывают несколько раз бутилацетатом, водный слой доводят до рН 4,0 и затем концентрируют при пониженном давлении. К остатку прибавляют количество
5 этанола, достаточное для осаждения смеси солянокислых солей К 582 М-А и К 582 М-В. Таким образом получают 5,0 г сырого порошка, представляющего .собой смесь солянокислых
0 солей К 582 М-А и К 582 М-В.
Полученной порошок снова растворяют в метаноле и, прибавляя к метанольному раствору достаточное ;количество ацетона и этанола, производят осаждение смеси солянокислых
5 солей К 582 М-А и К 582 М-В, которую отделяют фильтрованием. Полученную таким образом смесь К 582 М-А и К 582 М-В (в виде солянокислых солей) растворяют в метаноле и очища0ют пропусканием через колонку с :сеЛадексом LH-20, в результате чего получают 4,0 г смеси К 582 М-А и ;К 582 М-В (в виде солянокислых солей), представляющей собой белое
5 порошкоЪбразное вещество.
Пример 3. 1г смеси солянокислых солей К 582 М-А и К 582 М-В, полученной в соответствии с процедурой , описанной в примере 2, раство0ряют в 5 мл воды и водный раствор обрабатывают хроматографически, используя колонку (внутренний диаметр 26, высота 1200 мм) с биогелем Р-2, имеющим размер частиц 100-200 меш. Используя в качестве элюата 0,1 М
i водный раствор хлористого натрия и проводя элюацию со скоростью.30 мл/ч, получают на выходе из колонки сначала фракцию К 582 М-В (тоже g виде солянокислой соли). Полученные таким
O образом элюаты А и В снова хроматографируют и после повторного выхода из колонки концентрируют при пониженном давлении. К полученным в остатке веществам прибавляют для осаждения
5 смесь ацетона и этанола (4:1) и после высушивания полученные осадки повторно экстрагируют метанолом.Метанольный раствор концентрируют в вакууме и остаток дифундируют доQбавлением смеси ацетона и этанола . (4;1). После высушивания полученных осадков получают в виде порошкообразных продуктов К 582 М-А (солянокислую соль) или К 582 М-В (солянокислую соль). Затем каждый из полу5
ченных порошков А и В растворяют в небольшом количестве 801-ного метанола и полученные метанольные раствйры очищают хроматографически с использованием колонки (внутренний диаметр 26, высота 1200 мм), заполненной сефадексом LH-20, Полученные элюаты концентрируют при пониженном давлении и вещества, содержащиеся в остатках после упаривания, осаждают смесью ацетона и этанола (4:1). После высушивания полученных осадков до постоянного веса получают 0,41 г К 582 М-А в виде солянокисло соли (выход 41,0%) и 0,35 г К 582 М тоже в виде солянокислой соли (выход 35,0%) .
Пример 4. 1г смеси солянокислых солей К 582 М-А и К 582 М-В, полученной в соответствии с примером 2,растворяют в-5 мл воды и этот водный раствор хроматографируют, ис.пользуяколонку (внутренний диаметр 20, высота 500 мм) с карбоксиметилсефадексом С-25 (100-200 меш). Хроматографию проводят при использовании в качестве элюатов сначала 0,1 М буферного раствора фосфорной кислоты (рН 6), затем 0,4 М раствора хлористого натрия и в заключение 0,9 М раствора хлористого натрия. После изменения элюата на 0,9 М раствор NaCl сначала из колонки элюируется К 582 М-А (в виде соля .нокислой соли),а затем К 582 М-В
(тоже в виде соляной соли). Элюаты к 582 М-А (солянокислая соль) и К 582 М-В (солянокислая соль)концентрируют, высушивают,повторно экстрагируют метанолом и полученные метанольные растворы сначала концентрируют в вакууме до образования небольшого по объему остатка, а затем этот остаток обрабатывают смесью ацетона и этанола (4:1) с целью,получения соответственно К 582 М-А (солянокислой соли) и К 582 М-В (тоже солянокислой соли). Каждый из полученных таким образом порошков растворяют в небольшом количестве 80%-ного метанола и этот метанольный раствор очищают обессоливанием с помощью хроматографии на колонке с сефадексом LH-20, После концентрирования соответствующих элюатов при .пониженном давлении нещества, содержащиеся .в остатках, осаждсЦОГ прибавлением смеси ацето-. на и этанола (4:1). После высушивания осадков получают соответственно 0,40 г очищенного К 582 М-А (солянокислой соли) (выход 40,0%) и 0,43 г очищенного К 582 М-В (солянокислой соли) (выход 43,0%).
Пример .5.5л культурально среды, полученной в соответствий с примером 1, фильтруют с добавлением 10 г гифло-суперцеля. Полученный фильтрат доводят до рИ 5,0-6,0, концентрируют до объема, составляющего 1/10 - 1/20 от первоначального объема, удаляют содержащиеся в концентрате неорганические соли, снова упаривают (на этот раз досуха) и полученный остаток экстрагируют несколькими порциями метанола общим объемом 200 мл.Объединенный экстрак концентрируют в вакууме и остаток повторно экстрагируют метанолом, используя для этой цели последовательно уменьшающиеся количества метанола. Полученные экстракты полностью растворяют в воде и этот водный раствор хроматографируют на колонке (внутренний диаметр 50, высота 1000 мм) с биогелем Р-2 (IOO-2OO меш При использовании в качестве элюента 0,1 М раствора хлористого натрия пропускаемого через упомянутую колонку со скоростью 30 мл/ч, сначала получают (Ьракцию К 582 М-А (солянокислую соль), а затем Фракцию К 582 М-В {солянокислую соль). Элюаты, соответствующие этим Фракциям, очищают каждый путем обессоливания в соответствии с процедурой, описанной в примере 3 (экстракция метанолом, прибавление смеси ацетона и этанола, хрбматография на колонке с сефадексом LH-20) , в результате чего получают 1, 4 г высушенного К582 М-А солянокислую соль) и 1,2 г высушенного К 582 М-В (солянокислую соль) , соо.тветственнЬ.
П р и М е р . 6. 5л культуральной среды, полученной в соответствии с .примером 1, фильтруют с добавлением фильтрующего средства гиЛло-суперцель. После концентрирования в вакууме фильтрат отделяют от выделившихся твёрдых веществ фильтрованием, доводят его рН до величины порядка 5,0-7,0 и затем пропускают через колонку (внутренний диаметр 20 , высота 1000 мм) с СМ-сефадексом С-25 (100-200 меш.) с целью поглощения целевых веществ. Затем адсорбированные вещества элюируют с колонки 0,1 М буферным раствором фосЛор ной кислоты/ имеющим рН 6,0, затем 0,4 М раствором хлористого натрия и в дальнейшем 0,9 М раствором NaCl После замены элюирующего раствора на 0,9. М раствор хлористого натрия из колонки выходит сначала фракция К 582 М-А (солянокислая соль),а затем фракция К 582 М-В в виде солянокислой соли).Эти разделенные на фракции элюаты,один из которых содержит солянокислую соль К 582 Ма другой солянокислую соль К 582 Мконцентрируют. в вакууме , обессоливаю с помощью метода,описанного в примере 4 (метанольная экстракция, добавление смеси ацетона и этанола, хроматография на колонке с сефадексом LH-20), высушивают и получают в итоге 1,2 г, высушенного К 582 М-А
(его солянокислой соли) и 1,3 г высушенного К 582 М-В (солянокислой соли) соответственно.
Пример 7. 2г гидрохлорида К 582 М-А, полученного по методу, описанному в примере 3 или М, растворяют в -5 мл дистиллированной воды и-раствор наносят на колонку со слоббкислотным катионитом.Амберлит IRC-50 (4-25 см). После промывки колонки 400 мл дистиллированной воды К 582 М-А (сульфат) элюируют 1н.раствором серной кислоты. Элгоат, содержащий К 582 Н-А в виде сульфата, обрабатывают ионитом IPA-400. После доведения рН смеси до 6,0 смолу отфильтровывают и фильтрат концентрируют в вакууме. К этому концентрату прибавляют смесь ацетона и этанола (4:1) и выпавший осадок отделяют
фильтрованием. Полученный К 5а2 М-А (сульфат) хроматографируют с целью Ьбесооливания и очистки на колонке с сеФадексом LH-20 (колонка 2,2 У 80 см)« Для элюирования вещества из колонки используют дистиллированную воду.
Предложенный способ позволяет получить новый антибиотик К 582 М.
.Формула изобретения
Способ получения антибиотика К 582 М, отличающийся тем, что штамм Metarhizlum anisopliae (Metsch) Sorok. Var. anisopliae 582 M
5 выращивают в аэробных условиях в жидкой питательной среде при 20-37 0 и рН 3,0-8,0 с последующим вьщелением целевого продукта.
Авторы
Даты
1980-12-07—Публикация
1978-12-28—Подача