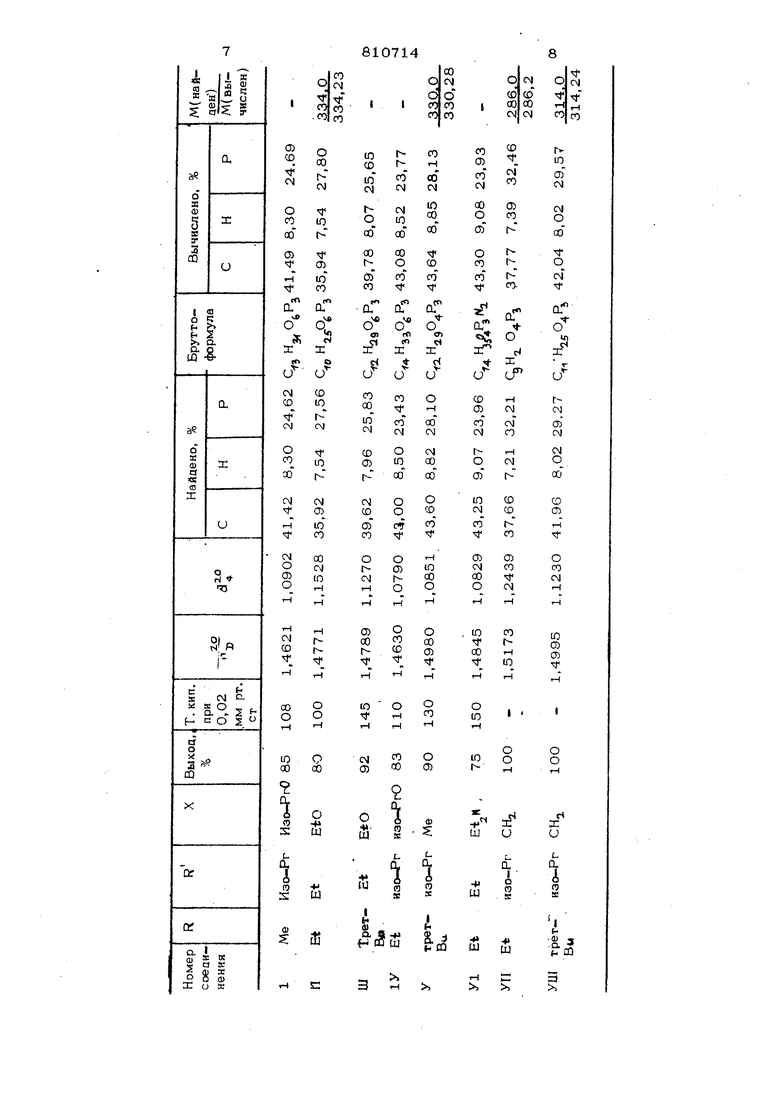
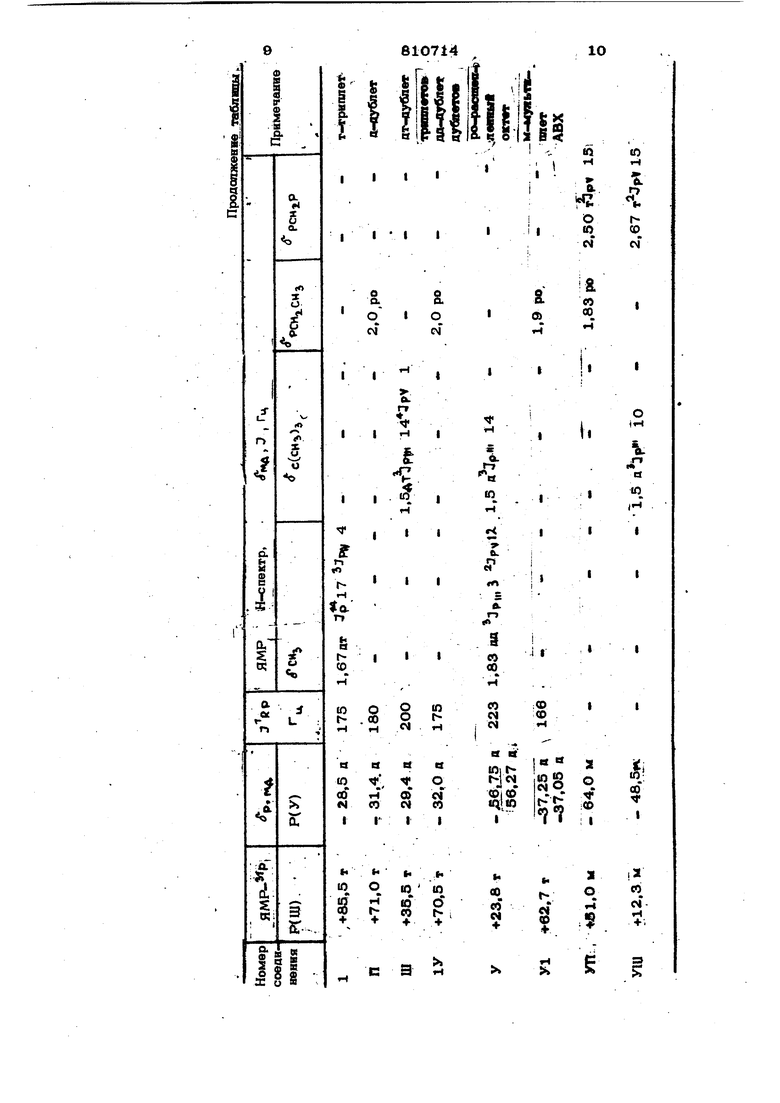
фор (У) замещенные фосфины, содержащие два асимметрических атома фосфора или обладающие циклической структурой,не были получены. -Целью изобретения является повыше- ние выхода целевых продуктов, упрощение процесса и расширение области его применения. . Предлагается способ получения дифосфор (У) замещенных фосфинов формулы 1, который заключается в том, что алкилдийодфосфин подвергают взаимодействию с эфиром, кислоты трехкбординационн го фосфора общей формулы ( X - представляет собой R, (Rb), РСН,; R и R - алкил, в среде органического.растворителя в ат мосфеое инертного газа при охлаждении до температуры от -40 до - 7О С. В реакцию желательно вводить 10- 2О%-ный избыток эфира кислоты трехкоординационного фосфора. Отличительными признаками, способа являются использование в качестве алкил дигалоидфосфина алкилцииоцфосфина, в ка честве эфира кислоты трехкоординационно .го фосфора соединения формулы (RO).,PX, где X, .R Р имеют указанные выше зна чения, и проведение процесса при охлаждении до температуры от - 40 до - ТСТС в вышеописанных условиях. Предлагаемый способ получения дифос фор (У) замещенных фосфинов исключает большое Количество примесей, характеризуется легкостью выделения целевых про дуктов и позволяет повысить выход целевых продуктов до 75-1 ОО%. Кроме того, такой способ дает возможность- получать целевых продукты самого разнообразного строения - как простейшие, так и содержащие два асимметрических атома фосфора или обладающие циклической структурой, и является новым методом образования фрагмента Р-Р-Р в молекулах. Полученные соединения - устойчивые бесцветные жидкости, перегоняющиеся при пониженном давлении, или масла, которые могут храниться в течение длител кого времени, без изменения, Состав и строение полученных соединений подтверж дены данными элементного анализа. ЯМР Н и р спектроскопии и массспектрометрии, которые приведены в таблице. Все реакции проводят в атмосфере инертного газа (сухого аргона) и в абсолютных растворителях. Пример 1. Метилбис (диизо- пропоксифосфиноксидо)фосфин (1). . К раствору 5О г (0,24 моль, 2О%ный избыток) триизопропилфосфита в 100 мл. хлористого метилена, охлажден- ,ному до - 7О С, добавляют раствор ;ЗО г (ОД моль) метилдийодфосфина в 1ОО мл хлористого метилена. Затем температуру смеси быстро доводят до комнатной температуры, растворитель и йодистый изопропил отгоняют в вакууме, создаваемом с помощью водоструйного насоса, остаток перегоняют. Получаюг 31,9 г соединения (1). Аналогично получают этилбис(диэтоксифосфиноксидоУфосфин (П). Пример 2. Трет-бутилбис1(диэтоксифосфиноксидо)фосфин (Ш). К раствору 14,3 г (0,086 моль, избыток) триэтилфосфита в 60 мл дихлорэтана, охлажденному до , добавляют раствор 13,3 г (0,О39 моль) трет-бутилдийодфосфина в 40 мл дихлорэтана. Затем смесь быстро размораживают, растворитель и йодистый этил отгоняют в вакууме, создаваемом с помощью водоструйного насоса, остаток перегоняют.. Получают 13 г со динения (Ш). Аналогично получают этилбис(диизопропоксифосфиноксидо)фосфин (1 у). Пример 3. Третт утилбис(метил изопропоксифосфиноксидо) фосфин (У). К раствору 20,8 г (0,127 моль, 15%-«ый избыток) диизопропоксиметилфосфонита в 100 мл хлороформа, охлажденному до , добавляют раствор 19 г (0,055 моль) трет- утилдийодфосфина в 5О МП хлороформа. Затем смесь быстро размораживают, растворитель и й.одистый изопропил отгоняют в вакууме, создаваемом с помощью водоструйного насоса, остаток перегоняют. Получают 16,4 г соединения (У). Аналогично получают этилбис(диэткламидоэтоксифосфиноксицо) фосфин (У1). Пример 4. 2-Этил-1,3-диизопропокси-1,3-аноксо-1,2,3-трифосфациклобутан (УП). К раствору 15,6 г (0,05 моль) тетраизопропнлметилендифосфонита в 400 мл хлористого метилена, охлажденному до -7О С, медленно добавляют раствор 15,7 г (О,О5 моль) этилоийоцфосфина в 10О мл хлористого метилена. Затем рмесь бьютро размораживают, раствора- гель и йодистый изопропил отгоняют в закууме, созааваемом с помощью воао- струйного насоса, остаток выдерживают |i вакууме 0,5 мм рт. ст. в течение i3 ч. Получают 14,3 г соединення (УП. в107 5 46 Аналогнчно получают 2-трет- утил-1,3-днизопропокси-1,3-аи оксо- 1,2,3- -трифосфациклобутан (УШ). Физвко-химические констани, данные алеменгносо анализа, ;ЯМР Н, Р спектроскопии и масс спектрометрии полученных соединений 1 приведены в табпвце.
Гю
О)
см
см
о
со
t о
CNj
of о
0
О) см
см
о
оо



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения дифосфор (у) замещенных фосфинов или их бис-аналогов | 1980 |
|
SU910645A1 |
| Способ получения замещенных алкоксикарбонилфосфинов | 1985 |
|
SU1294811A1 |
| Способ получения фосфорзамещенных метилфосфинатов | 1976 |
|
SU653261A1 |
| Способ получения N, N-тетразамещенных 0-триметилсилилбис-(аминометил)фосфинатов | 1989 |
|
SU1659416A1 |
| Способ получения N-дизамещенных О,О-бис-(триметилсилил)аминометилфосфонитов | 1989 |
|
SU1659420A1 |
| Способ получения фосфорилированных полуацеталей полуаминалей кетена | 1989 |
|
SU1682358A1 |
| Способ получения -фосфор /ш/ замещенных кетонов | 1977 |
|
SU697520A1 |
| Способ получения третичных метилфосфиноксидов | 1975 |
|
SU589925A3 |
| Способ получения дигалоидангидридов @ -триметилсилил /гермил/- @ -галоид- @ -алкоксивинилфосфонистых кислот | 1980 |
|
SU899569A1 |
| Способ получения производных пиразола | 1972 |
|
SU519132A3 |

to
CD О)
т
X
и
L
0.
I.
Ф .
е-с ш
S.
Ш ш
и со
-(
, ,
11
Формулаиаобретени
rqe R и R - алкил,
X -представляют I, QI, или 2Х образуют СН -группу, взаимодействием алкЕпднгалоидфосфвна с эфиром кислоты трехкоордииационыого-фосфора в среде органического растворителя в атмосфере инертного газа о т ли чающийс я тем, что, с целью повышения выхода целевых продуктов, упрощения процесса и расширения области его применения, в качестве алкилдигалоидфосфана используют алкнлдийодфосфин, а. в качестве эфи81О714
12
ра кислоты трехкоординационного фосфорй соединение общей формулу
(Ro)fX,
где X - представляет собой R, OR, R ц
Щп (Roji PCHj; R и R - алкил,
и процесс ведут при охлаждении до температуры от - 40 до - 70®С.
принятые во внимание при экспертизе
превращения, Изв. АН СССР, сер, хим. 1957, с. 179-186 (прототип).
Авторы
Даты
1981-03-07—Публикация
1979-05-28—Подача