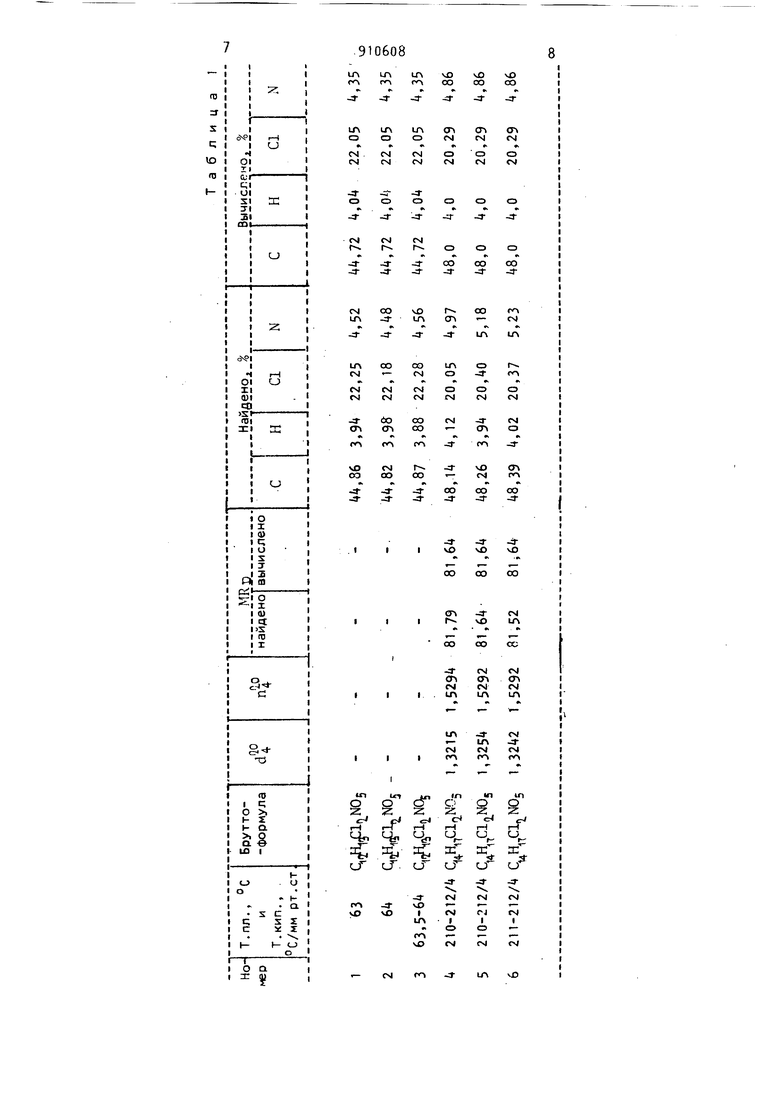
39 ко ограничено, а в южных районах страны запрещено. Известен N-метилкарбамат 2,Ц-f хлорфеноксиэтанолаCl- OCHgCH OCONHCHj С1 содержащий в своем составе фенильны радикал с двумя заместителями - С1 в положениях 2,,этокси- и метилкарбаминовую группы. Соединение обладает гербицидными свойствами 2 Это соединение проявляет гербицидные свойства на широколисных рас тениях, в частности на пятностой фасоли, индийской горчице, амаранте щавеле; вызывая полное угнетение и гибель их в дозах 10 кг/га при довсходовой обработке и 5 кг/га при послевсходовой обработке. На лисохвост действует слабо, т.е. проявля ет избирательность действия. Недостатком этого соединения является его невысокая гербицидность, что ведет к большим нормам расхода препарата при применении. Целью изобретения являёстя расширение арсенала средств воздействи на живой организм. Предлагаются N-метилкарбаматы (Ь-оксиэтилового эфира 2,4-дихлорарилоксиалканкарбоновой кислоты общей формулы , НО НИ о Н Н - //VV ч 1 II 1 I /-0- -с--0-C-C-0-C-N-C-H (L е ДАНи где R-H, CfiHj. Новые соединения формулы 1 получают взаимодействием (i-оксиэтилового эфира арилоксиалканкарбоновой ки слоты, например 2,4-дихлорфеноксиуксусной или 2,4-дихлорфеноксимасля ной кислот, взятых в количестве 0,25-0,5 моль, в присутствии 2 мл катализатора - триэтиламина и метилизоцианата, взятого в количестве 0,25-0,6 моль, при перемешивании при ЗОС в течение 5 ч, а затем при 5-50°С в течение 15 ч, после чего смесь охлаждают, промывают, сушат и выделяют. Выход 56-88 от теории. N-Метилкарбамат (Ь-оксиэтилового эфи ра 2,4-дихлорфеноксиуксусной кислот представляет собой белое кристаллич ское вещество, т.пл.63-6 С. Молекулярная масса 321,8-322,0. 4 N-Метилкарбамат fb-оксиэтилового эфира 2,4-дихлорфеноксимасляной кислоты представляет собой маслянистую жидкость, т.пл. 210-212°C/i мм рт.ст. . Физико-химические свойства соединений формулы 1 представлены в табл.1. Структура соединений подтверждена ЯМР- и ИК-спектрами. Полученные соединения обладают гербицидными свойствами. Результаты изучения их гербицир-ной активности представлены в табл.2. Пример 1. В реакционную колбу помещают 66,2 г (0,25 моль} (i-оксиэтилового эфира 2,4-дихлорфеноксиуксусной кислоты, 2 мл триэтиламина, 200 мл бензола, при перемешивании прибавляют It,2 г (0,25 моль) метилизоцианата. Соотношение реагирующих компонентов 1:1. Перемешивание при 45-50°С продолжают 20 ч. После охлаждения и промывки выделяют 52,3 г (65 от теории) белых игольчатых кристаллов N-метилкарбамата |Ь -оксиэтилового эфира 2,-дихлорфеноксиуксусной кислоты. Пример 2. В реакционную колбу помещают 66,2 г (0,25 моль) |i-оксиэтилового эфира 2, -дихлорфеноксиуксусной кислоты, 200 мл бензола, 2 мл триэтиламина. Затем прибавляют при перемешивании 15,7 г (0,275 моль) метилизоцианата, что определяет соотношение 3 : 1 , 1 . Перемешивание при 5-50°С продолжают 20 ч. После обработки выделяют 5б,3 г (70 от теории) белых игольчатых кристаллов N-метилкарбамата (i-оксиэтилового эфира 2,-дихлорфеноксиуксусной кислоты. Пример З-В реакционную колбу помещают 132,5 г (0,5 моль) (Ь-оксиэтилового эфира 2, -дихлорфеноксиуксусной кислоты, 200 мл бензола, мл триэтиламина, прибавляют при перемешивании 3,2 г (0,6 моль) метилизоцианата, что обусловливает соотношение 1:1,2, Перемешивание при 30°С продолжают 5 ч. Затем температуру повышают до 5-50°С и перемешивают при данной температуре 15 ч. В результате реакции выделяют 1t1,68r (88 от теории) белых игольчатых кристаллов N -метилкарбамата (Ь-оксиэтилового эфира 2,-дихлорфеноксиуксусной кислоты.
Пример . В реакционную колбу помещают 87,9 г (0,3 моль) Ь-оксиэтилового эфира fll-(2,-/ ихлорфенокси)-масляной кислоты, 3 мл триэтиламина, 150 мл бензола, при перемешивании прибавляют 17,1 г (0,3 моль) -метилизоцианата. Соотношение реагирующих компонентов 1:1, Перемешивание при 45-50°С продолжают 18 ч. После охлаждения перегонкой выделяют 58,8 г (5б% от теории) прозрачной маслянистой жидкости, представляющей собой N-метилкарбамат (i-оксиэтилового эфира cL-(2, -дихлорфенокси)-масляной кислоты,
Пример 5. В реакционную колбу помещают 87,9 г (0,3 моль) |Ь-оксиэтилового эфира с1-(2,-дихлорфенокси)-масляной кислоты, 3 мл триэтиламина, 150 мл бензола, при перемешивании прибавляют 19,95 г (0, моль) метилизоцианата. Соотношение реагирующих компонентов 1:1,15. Перемешивание при 0-50°С продолжают 18 ч. После охлаждения и перегонки выделяют 71, г (68% от теории) прозрачной маслянистой жидкости, представляющей собой N-метилкарбамат | -оксиэтилового эфира о1-(2-дихлорфенокси)-масляной кислоты.
Пример 6, В реакционную колбу помещают 117,2 г (0,k моль Р)-ЭКСИЭТИЛОВОГО эфира (А.-(2, -дихлорфенокси)-масляной кислоты, 3 мл триэтиламина, 150 мл бензола, при перемешивании прибавляют 27, г (0, моль) метилизоцианата. Соотношение реагирующих компонентов 1:1,2. Перемешивание при продолжают 5 ч. Затем температуру повышают до 5-50°С и перемешивают при этой температуре 13 ч. После охлаждения и перегонки выделяют 116,3 г (83 от теории) прозрачной маслянистой жидкости - N-метилкарбамата f -оксиэтилового эфира cL- (2, -дихлорфенокси) масляной кислоты,.
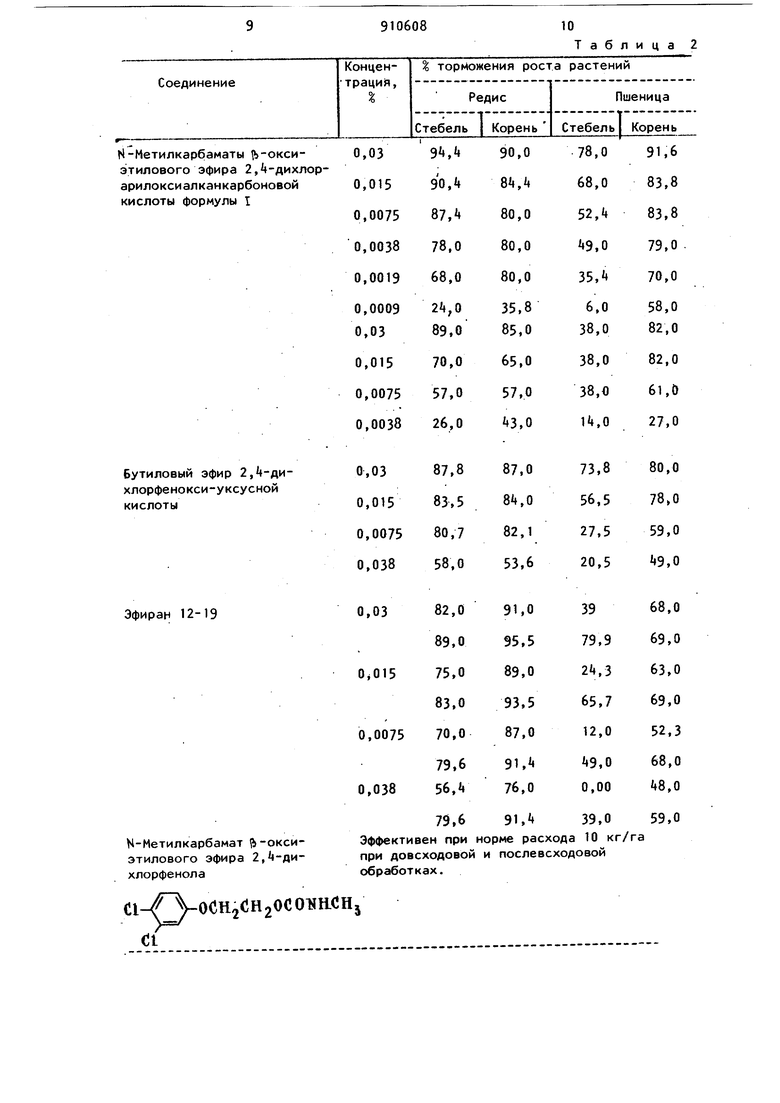
Новые соединения испытывались в лабораторных условиях в виде ацетонового раствора различных концентраций: 0,03; 0,015; 0,0075; 0,0038; 0,d019.
В качестве эталона применяли гербицид эфирен 12-19 и бутиловый эфир 2, кислоты 3 .
По данным табл.2 новые соединения -N-метилкарбаматы Г ;-оксиэтилового эфира 2, 4-дихлорарилоксиалканкарбоновой кислоты по гербицидной активности и избирательности действия превосходят N-метилкарбамат 2, -дихлорфеноксиэтанол и не уступают эталонам - эфирану 12-19 и бутиловому эфиру 2, Д-кислоты. Нормы расхода последних 300-450 г/га (по 2, кислоте) ,
Таблица 2 11910 Формула изобретения N-Метилкарбаматы |Ь-оксиэтилового эфира 2,-дихлорарилоксиалканкарбоновой кислоты общей формулы odHdoocii,dH20dONHCH3 8 где R - Н, , проявляющие гербицидные свойства. Источники информации, принятые во внимание при экспертизе 1.Краткий справочник по ядохимикатам. М., 1973, c.nt-US. 2.Патент США № 3 39021, кл.260-482, опублик. 1969. 3.Мельников Н.Н. Химия пестицидов. М., 1968, с.168.



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения 2,4-дихлорфеноксиуксусного эфира 2-оксиэтиловых эфиров синтетических жирных кислот фракции с @ -с @ | 1978 |
|
SU889657A1 |
| СПОСОБ ПОЛУЧЕНИЯ ИЗОЦИАНАТОВ | 1969 |
|
SU239945A1 |
| Ацилоксиэтиловые эфиры /2,4-дихлорфенокси/-масляной кислоты | 1974 |
|
SU504756A1 |
| Способ получения карбамоилфторида | 1976 |
|
SU886737A3 |
| СПОСОБ ПОЛУЧЕНИЯ СЛОЖНЫХ ЭФИРОВ ЭТИЛЕНГЛИКОЛЯ и 2,4-ДИХЛОРФЕНОКСИУКСУСНОЙ КИСЛОТЫ И ЖИРНЫХкислот С5~Сб | 1973 |
|
SU389078A1 |
| ПРОИЗВОДНЫЕ ПИРИМИДИНА, СПОСОБ БОРЬБЫ С СОРНЯКАМИ И ГЕРБИЦИДНЫЙ СОСТАВ | 1990 |
|
RU2041214C1 |
| СПОСОБ ПОЛУЧЕНИЯ N-ЗАМЕЩЕННЫХ 5-АМИНО-1,3,4--ТИАДИЛЗОЛА | 1970 |
|
SU266655A1 |
| Простые эфиры алифатического ряда в качестве регулятора роста пшеницы | 1978 |
|
SU739054A1 |
| Способ получения замещенных алкоксикарбонилдитиокарбаматов | 1983 |
|
SU1318155A3 |
| 6-АМИНОБЕНЗОДИОКСАН-1,4(2,4-ДИХЛОРФЕНОКСИ)-АЦЕТАТ, ОБЛАДАЮЩИЙ ГЕРБИЦИДНОЙ И РОСТСТИМУЛИРУЮЩЕЙ АКТИВНОСТЬЮ | 1992 |
|
RU2041222C1 |


Авторы
Даты
1982-03-07—Публикация
1980-07-01—Подача