формулы (I) или их солей или оптичес ких изомеров на основе 14-оксо-гомоэбурнана, отличительной особенностью которого является то, .что производные 15-Ькси-Е-гомоэбурнана общей фор мулы Ш) Н к где R и X имеют указанные значения, в виде рацемической смеси или их оптических изомеров, обрабатывают хлор окисью фосфора в среде хлорбензола (желательно при кипении) и полученны соединения формулы в виде.рацемической смеси или их опг тических изомеров где R и X имеют указанные значения, подвергают взаимодействию с нитритом щелочного металла в присутствии кислоты, после чего целевые продукты выделяютв сво бодном Й11де, в виде солей и/или разделяют на оптические изомеры. Преимуществом способа является исключение адсорбирующих воду и токсичных реагентов, что упрощает процесс. Изобретение относится также к способу получения производных нового промежуточного 15-хлор-Е-гомоэбурна.на общей формулы (III) , где R - этил х - атом водорода или брома или их солей или оптических изомеров, ос нованному на известной реакции замещения гидроксила на хлор 2, заключающемуся в том, что производные 15-окси-Е-гомоэбурнана общей формулы (II) где R и Х имеют указанные значения, в виде рацемической смеси или оптических изомеров, обрабатывают хлорокисью фосфора в средехлорбен зола и полученные соединения формулы (III) выделяют в свободном виде, в виде ролей или разделяют 15-эпиме ры и/или разделяют рацематы на оптические изомеры. Пример. 15-эпимеры(+)-3(S) 17 (S) -оксо-15- хлор-Е-го1 юэбурнана 4,2 .г (13 моль) ( + )-3(3) 17(S)-14-OKсо-15-окси-Е-гомоэбурнана(смесь 15-эпимеров) кипятят 3 ч с обратным холодильником в 100 мл хлорбензола в присутствии 4,2 г хлорокиси фосфора. Смесь заТэм охлаждают, разбавляют при перемешивании 100 г ледяной воды устанавливают ее рй с помощью 5%-го . водного раствора карбоната натрия равным 8,5 и встряхивают в делительной воронке. Нижнюю фазу сливают, а верхнюю, водную фазу дважды подвергают экстракции дихлорметаном, порциями по 50 мл. Органические фазы объ- единяют, высушивают безводным сульфатом магния, фильтруют и выпаривают фильтрат в вакууме досуха. Остаток после упаривания, представляющий собой смесь эпимеров, можно без очистки использовать в качестве исходного продукта на последующей стадии. Выход 3,50 г (81% теоретического выхода); т.пл. 140-152с. Полученньлй описанным способом сырой продукт можно разделить с помощью препаративной тонкослойной хроматографии на два стереомерных хлорированных производных. Разделение осуществляют на силикагеле марки KG-PF264fЭ5ь используя в качестве подвижной фазы смесь бензола и метанола, взятых в соотношении 14:3. Элюирование проводят с помощью ацетона. Изомер с большим значением Н плавится при 155°С (после перекристаллизации из метанола). ИК(в КВг): :1700 см (лактам - СО); масс-спектроскопия м/е,%: 342 (M-t-, 100) , 279(26), 252(37) , 251(21) ; 250(17), 249(48), 237(13) , 223(13) 194(16), 180(27) 169(27). j Изомер с меньшим значением Rf плавится при 142С (после перекристаллизации из метанола). ИК(в КВг): 1720 СМ (лактам-СО) ; масс-спектроскопия м/е,%: 342(М ,71) , 307(63), 308(100), 280(22), 252(45), 249(34), 223(18), 169(20). (с1),3 (,01, в хлороформе). При м е р 2. (+)-3(S), 17(S)-14-оксо-15-оксиимино-Е-гомоэбурнан0,20 г (0,058 ммоль) -смеси эпимеров (+)-3(5), 17(S)-14-ОКСО-15-хлор-Е- -гомоэбурнана (полученного по примеру 1) растворяют в 4 мл уксусной кислоты, раствор разбавляют 1 мл воды и добавляют к нему при постоянном перемешивании при комнатной температуре по каплям раствор 1,2 г нитрита натрия и 4 мл воды. Смесь оставляют стоять при комнатной температуре в течение 24 ч, подщелачивают ее, до- . бавляя концентрированный водный раствор гидрата окиси аммония до рН: равного 9 и трижды проводят из нее экстракцию дихлорметаном, порциями по 5 мл. объединенные дихлорметановые вытяжки высушивают безводным сульфатом магния, который затем отфильтровывают, а фильтрат упаривают В вакууме досуха. Получаемую в результате упаривания маслянистую жидкость (0,19 г) очищают с помощью препаративной тонкослойной хроматографии (KG-PF2.56+366 подвижная фаза бензол-метанол в соотношении 14:3, элюент смесь дихлорметана и метанола в соотношении 20:5); величина R непрореагировавшего исходного соединения выше, чем у целевого продукта. После удаления из элюата растворителя получают 0,13 г(+)-3(5)-14-оксо-15-оксиимино-Е-гомоэбурнана (68% от теоретического выхода); т.ил. i90°C (после перекристаллизации из эфира); (c)+6l (, в дихлорметане) . ИК(в КВг):3200 (ОН), 1705 CNf (лактам-СО) / 1642 см- ()., результаты .анализа (из расчета на C pH-y- jOj мол.в. 337,4) : Рассчита но, %: С 71,19, Н 6, 12,45; Найдено, %: С 71,30, Н 6,60, N 12,65 Для получения хлористоводородной соли 0,13 г полученного продукта растворяют в 1 мл метанола, подкисляют раствор с помощью метанольного раствора соляной кислоты до рН 5, выпада ющий в осадок гидрохлорид отфильтровывают и высушивают. Полученная хлористоводородная соль плавится при 256-257с после перекристаллизации из метанола). Приме p3.( + )-3(S), 17(S)-11-бром-14-оксо-15-хлор-Е-гомоэбурнан(смесь 15-эпимеров). 1,00 г(2,48 ммоль) смеси 15-эпимеров (+)-3(S), 17(S)-ll-бpoм-l4-oкco- 15-окси-Е-гомоэбурнана растворяют в А9 мл хлорбензола, полученный раст вор смешивают при постоянном перемешивании с раствором 0,85 г хлорокиси фосфора в 1 мл хлорбензола и кипятят С ч с обратным холодильником. После охлаждения реакционную смесь встряхивают в делительной воронке при охлаждении льдом с 15 мл 15%-го водного раствора карбоната натрия и отделяют нижннж), органическую фазу. Из водной щелоч1 ой фазы трижды проводят экстракцию дихлорметаном, содержащим 1% метанола (порциями по 10 мл). Оргйнические вытяжки объединяют, высушивают безводным сульфатом магния, который затем отфильтровывают, а фил трат упаривают в вакууме досуха; Получаемая в результате маслянистая жидкость (1,00 г) представляет собой смесь 15-эпимеров целевого продукта, которая без дополнительной очистки может использоваться в качестве исходного продукта на последующей стадии . При желании 15-эпимеры могут быть разделены с помсяцью препаративной , тонкослойной хроматографии (KG подвижная фаза бензол/метанол в соотношении 14:3; элюент ацетон(дихлор метан в соотношении .2:1) . В результате разделения получают 0,32 г (30,5% от теоретического вы-, хода) изомера (а) с более низким зна чением R т.пл. 215-216С (после перекристаллизации из ацетона) ; (о) +55,6 (с 1,024, в CHCl). ИК(в КВг) 1705 см (лактам-СО) . Результаты анализа (из расчета С,. H. ВгС1;1АП,В 421,77) . г Рассчитано, %: С 56,95, Н 5,25, N 6,64; Найдено, %. С 56,70, Н 5,35,N 6,45. Изомер (в) с более высоким значением R{ получается в результате разделения в виде маслянистой жидкости в количестве О,45 г (43% от теоретического выхода) путем взаимодействия с метанольным раствором соляной кислоты его переводят в хлористоводородную соль; т.пл. 269С (с разложением, после перекристаллизации из ацетона)} (Л)(с-1,05, в дихлорметане). Ик(в КВг): 1705 см- (лактам-СО) . Результаты анализа (из расчета на C oH jjNOBrCl-i; мол.вес 458,23). Рассчитано. %: С 52,41, Н 5,05, N 6,11; Найдено, %:С 52,34,Н 5,27,N6,20. Пример 4. (1)-3(S) ,17(S)-1,1-бром-14-оксо-15-ОКСИИМИНО-Е-ГОМО-:збурнан. 0,50 г(1,18 ммоль)(+)-3(8), 17(3)-11-бром-14-оксо-15-хлор-Е-гомоэбурнана (смеси 15-зпимеров) полученной по способу в соответствии с примером 3 растворяют в 11 мл ледяной уксусной кислоты, к полученному раствору при постоянном перемешивании, при комнатной температуре добавляют по каплям раствор 2,70 г нитрита натрия в 9 МП воды и оставляют его стоять в течение 30 ч. Реакционную смесь выливают затем в 20 г ледяной йоды, подщелачивают ее путем добавления концентрированного раствора гидрата окиси аммония до рН 9 и трижды проводят из нее экстракцию дихлорметаном, порциями по 10 мл. Объединенные органические вытяжки высушивают безводным сульфатом магйия, который затем отфильтровывают, а фильтрат упаривают досуха. Получающуюся в результате маслянистую жидкость (0,50 г) очищают с помощью препаративной тонкослойной хроматографии (KG-RF2. подвижная фаза: смесь бензола и метанола в соотношении 14:3; элюент: дихлорметана). Величина R непрореагированаего исходного соединения выше, чемКг целевого прог дукта. В результате получают 0,32 г маслянистого целевого продукта (60,5% от теоретического выхода). Полученный описанным способом в виде маслянистой жидкости (+)-3(S), 17(3)-11-бром-14-оксо-15-оксиимино-Е-гомоэбурнан переводят обычным способом путем взаимодействия с метанольным раствором соляной кислоты, в кристаллическую хлористоводородную соль.
Кристаллизующийся из метанола гидрохлорид плавится при 235-236С, (о) +44,9(,10 в диметилформамиде). ИК{в КВг):3460 см-Мон), 1710 см- (лактам-СО) , 1622 CM(). Массспектроскопия М/е,%: 415 (М , 62).
Формула изобретения
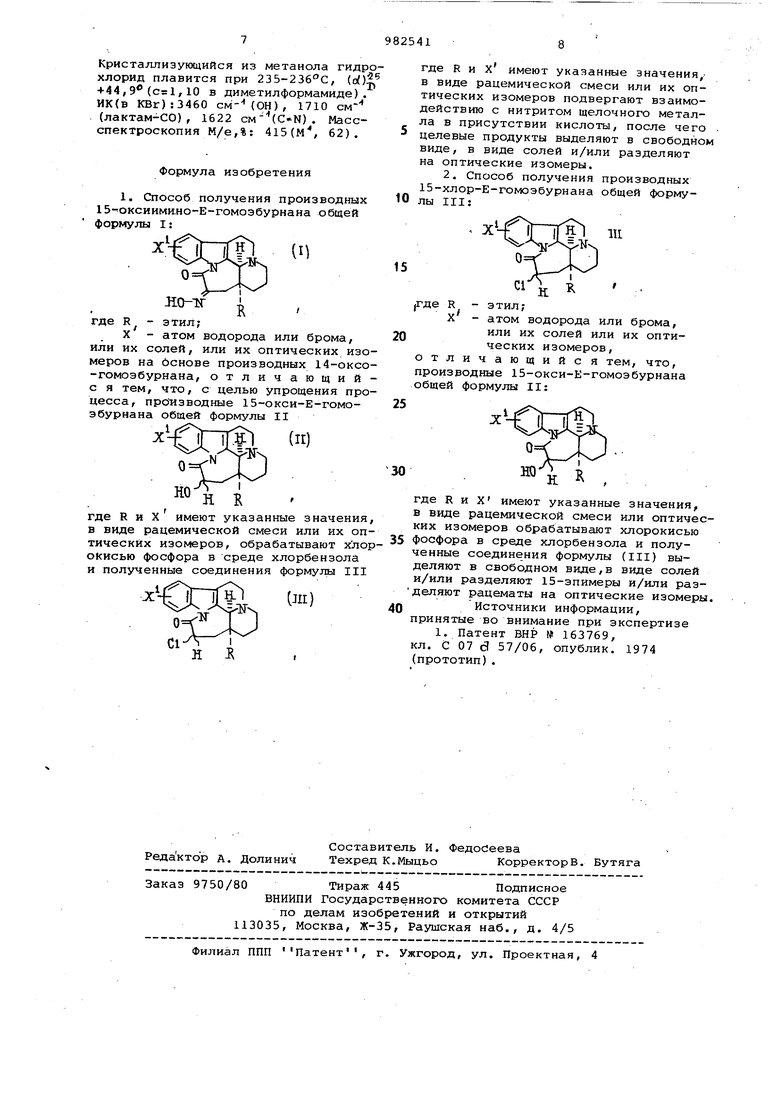
1. Способ получения производных 15- оксиими,но-Е-гомоэбурнана общей формулы I:
,-1 Г rt-r 1Г л/ ,
ЯО-1Г
/
где R - этил;
X - атом водорода или брома, или их солей, или их оптических изомеров на йснове производных 14-оксо-гомоэбурнана, отличающийс я тем, что, с целью упрощения процесса, производные 15-окси-Е-гомоэбурнана общей формулы II
(И)
н
где R и X имеют указанные значения, в виде рацемической смеси или их оптических изомеров, обрабатывают хлорокисью фосфора в среде хлорбензола и полученные соединения формулы III
JII)
где R и X имеют указанные значения,в виде рацемической смеси или их оптических изомеров подвергают взаимодействию с нитритом щелочного металла в присутствии кислоты, после чего . целевые продукты выделяют в свободном виде, в виде солей и/или разделяют на оптические изомеры.
2. Способ получения производных 15-хлор-Е-гомоэбурнана общей формулы III:
(Где К - этил;
X - атом водорода или брома, или их солей или их опти20ческих изомеров,
отличающийся тем, что,
производные 15-окси-Е-гомоэбурнана
общей формулы II:
25
30
где Них имеют указанные значения, в виде рацемической смеси или оптических изомеров обрабатывают хлорокисью
35 фосфора в среде хлорбензола и полученные соединения формулы (III) выделяют в свободном виде,в виде солей и/или разделяют 15-эпимеры и/или разделяют рацематы на оптические изомеры
40 Источники информации,
принятые во внимание при экспертизе
1. Патент ВНР № 163769, кл. С 07 d 57/06, опублик. 1974 (прототип).




Авторы
Даты
1982-12-15—Публикация
1980-07-11—Подача