Предлагаемое изобретение относится к медицине, а именно к гастроэнтерологии, и может быть использовано в хирургии в послеоперационном периоде после панкреатодуоденальной резекции (ПДР).
За прошедший 60-летний период своего развития ПДР из операции, сопровождающейся тяжелыми ранними и поздними послеоперационными осложнениями, высокой послеоперационной летальностью и низкой 5-летней выживаемостью, стала операцией, широко применяемой в различных хирургических клиниках без развития фатальных осложнений и с 5-летней выживаемостью, достигающей 30% (Carey L.C. , 1992). В связи с этим интерес к процессам, протекающим как в ранний послеоперационный период, так и в отдаленные послеоперационные сроки, не ослабевает в течение достаточно долгого времени. Представляется актуальным исследование, направленное на изучение адаптации пищеварительно-транспортного конвейера в раннем и отдаленных послеоперационных периодах, достижения улучшения качества жизни пациентов.
Эвакуация содержимого желудка является одним из выражений функциональной активности этого органа и его участия в процессе пищеварения. Порционность выхода пищевого содержимого из желудка в кишечник чрезвычайно важна для достижения эффективного гидролиза и всасывания питательных веществ в кишечнике.
В качестве аналогов оценки адаптационно-компенсаторных показателей гастропанкреатоэнтерального комплекса после ПДР можно представить следующие классические методы.
Исследование желудочной секреции соляной кислоты и пепсиногена. Проводят путем определения концентрации и дебита HCl и активности пепсина с расчетом его часового дебита в содержимом желудка, полученном с помощью зондирования, натощак и после стимуляции секреции желудка пентагастрином (6 мкг на 1 кг массы тела обследуемого). Базальную секрецию кислоты (БСК) и максимальную секрецию кислоты (МСК) вычисляют по номограмме В.В. Калиниченко (норма БСК - 1,5-5,5 МЭК/час, норма МСК - 18-26 МЭЮ/час). Базальную и максимальную секрецию пепсина (БСП и МСП) вычисляют по времени створаживания молока в растворе, состоящем из: 45,0 NaOH + 92 мл ледяной уксусной кислоты + дистиллированная вода до 1 л = 1 л молока (pH = 5). В 20 мл раствора добавляют каплю желудочного содержимого и определяют время створаживания молока в секундах (норма БСП - 46-63 мг/час, норма МСП - 100-150 мг/час) (Фишзон-Рысс Ю. И. Современные методы исследования желудочной секреции. М.: Медицина, 1972). Метод определения кислоты и пепсиногена в полученном с помощью зондирования тонким зондом желудочным содержимом широко применяется в клинике и отвечает основным требованиям к методам зондовой оценки секреторной деятельности желудка (Пятницкий Н.П. Простой способ определения пепсина в желудочном соке. Клиническая медицина, 1955, N 4, стр. 74-76).
После ПДР ни один из показателей, вне зависимости от срока, прошедшего после операции, не приближается к нижней границе нормы, указанной выше. Гипотрофические трансформации секреторного аппарата желудка в разной мере и в разной временной динамике касаются главных и оксинтных клеток - главные клетки оказались более резистентными, чем оксинтные. Это имеет при ПДР адаптационное значение, т.к. HCl утрачивает свою регуляторную роль для гастропанкреатоэнтерального комплекса. В этих условиях роль секреции пепсиногена сохранена.
Недостатками этого способа являются следующие: во-первых, этот способ является косвенным в определении адаптации гастропанкреатоэнтерального комплекса после ПДР, а во-вторых, с помощью только этого метода нельзя дать достоверную оценку компенсаторно-адаптационных показателей гастропанкреатоэнтерального комплекса после ПДР, он может быть использован в комплексе с другими клиническими и инструментальными способами.
Следующим аналогом определения адаптационно-компенсаторных возможностей гастропанкреатоэнтерального комплекса можно представить ультразвуковое исследование (УЗИ) поджелудочной железы (ПЖ).
УЗИ поджелудочной железы заключается в обследовании зоны проекции всей железы, определении контуров и размеров ее, плотности ткани. Неизмененная ПЖ имеет на ультразвуковом срезе форму "запятой" или "гантели". Ткань железы на эхограмме однородна, контуры ровные, по плотности она мало отличается от окружающих тканей. Характерным является пульсация всей железы или участка ткани над проходящими за ней крупными сосудами. При хроническом панкреатите выявляется неровность контуров железы, размеры ее нормальны или уменьшены. Характерно увеличение плотности ткани ПЖ, которая более отчетливо дифференцируется от окружающих тканей. (М.В. Данилов и соавт. Хронический панкреатит. М.: Медицина, 1985). После операций на поджелудочной железе, в частности ПДР, ультразвуковым методом можно установить наличие или отсутствие сонографических признаков панкреатита. Развитие хронических воспалительных изменений ПЖ в ответ на операционную травму и предшествующий обтурационный панкреатит является одной из причин внешнесекреторной недостаточности ПЖ (Федишин П.С., Шалимов С.А. Изменение функционального состояния системы пищеварения после частичного и полного удаления поджелудочной железы. Врачебное дело, 1981, N 4, стр. 41-45).
Недостатками этого способа являются: во-первых, то, что УЗИ поджелудочной железы дает представление о морфологической структуре культи, о ее анатомо-топографических особенностях, что является косвенной оценкой адаптации и компенсации ПЖ после ПДР, и, во-вторых, анализ ультразвуковых эхограмм только в совокупности с клиническими данными позволяет дать оценку состояния панкреатоэнтерального комплекса, т. е. самостоятельно УЗИ не может оценить его адаптационно-компенсаторное состояние.
Прототипом способа, предлагаемого в данном изобретении, является комплекс клинических и лабораторных показателей, оцениваемых у пациентов, перенесших ПДР (Шелагуров А.А. Болезни поджелудочной железы. М.: Медицина, 1980, 360 с).
1. Жалобы. По предъявляемым жалобам можно определить клинический статус больного (боли в эпигастрии, их характер, время появления, чем купируются; наличие аппетита или его отсутствие; имеют ли место диспепсические расстройства; характер стула, его количество и частота; принимает ли препараты заместительной терапии (пищеварительные ферменты, желудочный сок).
2. Росто-весовой показатель используют для определения общей характеристики состояния пищеварения и степени компенсации больными интраоперационной потери массы тела. Показатель рассчитывают по формуле: B/P - 100, где В - вес в килограммах, P - рост в сантиметрах. В норме он равен 1. У больных с росто-весовым показателем меньше 1 в раннем послеоперационном периоде после ПДР, как правило, выявляют различные осложнения: сахарный диабет, пептическая язва гастро-энтеро анастомоза и др.
3. Биохимические показатели сыворотки крови: общий белок и белковые фракции (определяемые по методу Уодля), выявляющие нарушение белкового обмена. Снижение этих показателей указывает на нарушение белково-синтетической функции печени.
Недостатком приведенного выше прототипа является то, что для оценки уровня компенсации и адаптации гастропанкреатоэнтерального комплекса после ПДР нужно использовать весь комплекс клинических, инструментальных и лабораторных методов исследования, который занимает много времени; требует госпитализации больного на время обследования и является относительно дорогостоящим.
Цель: упрощение способа оценки адаптационно - компенсаторных показателей гастропанкреатоэнтерального комплекса, снижение себестоимости исследования и времени обследования больного после панкреатодуоденальной резекции.
Задачи:
1. Исследовать адаптационно-компенсаторные механизмы гастропанкреатоэнтерального комплекса у больных после ПДР, используя традиционные методы (клинический осмотр, лабораторные данные, росто-весовой показатель, УЗИ поджелудочной железы, исследование секреторной функции желудка).
2. Исследовать особенности адаптационно-компенсаторного состояния гастропанкреатоэнтерального комплекса у больных в различные сроки после ПДР.
3. Провести сравнительный анализ исследования уровня адаптационно-компенсаторного состояния гастропанкреатоэнтерального комплекса после ПДР традиционными методами и методом дифференцированной эвакуации желудочного содержимого.
4. На основании полученных данных оценить уровень адаптационно-компенсаторного состояния гастропанкреатоэнтерального комплекса.
Сущность изобретения состоит в определении скорости эвакуации желудочного содержимого при последовательном неоднократном введении больному "углеводного", "белкового" и "жирового" завтраков с радиоактивной меткой. При условии скорости эвакуации тестовых завтраков в последовательности "белковый", "углеводный", "жировой" определяют нормальный уровень адаптационно-компенсаторного состояния, а при других нарушениях дифференцировки эвакуации тестовых завтраков определяют декомпенсацию гастропанкреатоэнтерального комплекса. Оценку последовательной эвакуации тестовых завтраков осуществляют по истечении 6-ти месяцев после ПДР.
Пищеварение является сложным физиологическим и биохимическим процессом, в ходе которого пища подвергается физическим и химическим изменениям в пищеварительном тракте. Указанные процессы протекают в определенной последовательности, "наслаиваясь" по отделам ЖКТ, имея для различных видов пищи существенные особенности. Моторный аппарат ЖКТ распределяет пищеварение во времени и пространстве. Три сопряженных процесса - полостного пищеварения, пристеночного пищеварения и всасывания составляют сущность пищеварительно-транспортного конвейера (Уголев А.М., 1963). Выделяют ряд конкретных выражений последовательности пищеварения: преемственность биотехнологических процессов, органная преемственность, преемственность полостного и пристеночного пищеварения, преемственность ферментной деполимеризации питательных веществ (Коротько Г.Ф., 1987).
Состояние гастропанкреатоэнтерального комплекса после ПДР рассматривалось нами с точки зрения конвейерности устройства пищеварительной системы. Для освещения статуса экзосекреторного аппарата в нашем изобретении мы показали процесс дифференцированной эвакуации нутриентов.
Способ осуществляют следующим образом: Пациент принимает пищевые пробные завтраки разного состава. Состав завтраков был определен эмпирическим путем. 1. "Углеводный" завтрак (У): 200 г 10% манной каши, 200 мл сладкого чая. 2. "Белковый" (Б): 140 г 10% манной каши, 60 г сырого яичного белка, 200 мл сладкого чая. 3. "Жировой" (Ж): 160 г 10% манной каши, 40 г сливочного масла, 200 мл сладкого чая. Общий объем каждого из завтраков составляет 400 мл, все три разновидности тестовой пищи одинаковы по вязкости и pH, близком к нейтральному (Коротько Г. Ф., Аблязов А.А. Способ диагностики нарушений эвакуаторной функции желудка. 1991). В каждый из завтраков вводят радиоактивную метку - 99 m Тс. Регистрацию информации проводят радиометром с использованием двух коллиматоров, устанавливаемых - один над телом желудка, второй - в проекции отводящей петли тонкой кишки. Определение местоположения коллиматоров осуществляют двумя способами: рентгенологическим и с помощью звуковой индикации активности над исследуемым органом. При вычислении начальную максимальную импульсацию над уровнем желудка принимают за 100%, а затем импульсацию сравнивают с начальной до уровня, составляющего 50% от исходного, что составляет время полувыведения желудочного содержимого. Гастрограммы, полученные при исследовании эвакуаторной деятельности гастроэнтерального комплекса методом радиоизотопной гастрографии, приведены в приложении. Кривая справа (см. приложения) отражает эвакуацию желудочного содержимого (регистрация активности получена с коллиматора, установленного над телом желудка). Кривая слева (см. приложения) показывает изменение активности в проекции отводящей кишки. Сложность реконструкции отводящей кишки, наличия межкишечных анастомозов, спаечный процесс с образованием конгломерата петель, делают невозможным детальное исследование пассажа пищи из отводящей кишки данным методом. Характер кривой слева крайне вариабелен. Анализ данной кривой показывает наличие равномерных волн различной амплитуды. При анализе кривой справа видна порционность эвакуации с периодическим возвратом содержимого из антрального отдела в тело желудка, что соответствует нормальному явлению перемешивания пищи в желудке. Время эвакуации рассчитано по кривой справа и результаты приведены в таблице.
В норме быстрее всего эвакуируется из желудка углеводная пища, медленнее белковая и наиболее медленно жиры, что описывается соотношением: У =>Б =>Ж. (У: 29,5 + 1,4 мин Б: 37,8 + 1,7 мин Ж: 48,1 + 1,2 мин) (Коротько Г.Ф., Аблязов А. А., 1991). В группе больных, обследованных до 6 месяцев послеоперационного периода, соотношение приобретает вид - Ж => У => Б, причем достоверна только разница в эвакуации белков и жиров (p < 0,01). В группе больных, обследованных до 12 месяцев, соотношение эвакуируемых завтраков - Б => Ж => У, но достоверной является только разница в эвакуации углеводов и белков (p < 0,05). В группе больных, обследованных в отдаленный послеоперационный период, происходит достоверное удлинение времени эвакуации жирной пищи по сравнению с белковой (p < 0,05) и соотношение приобретает вид - Б => У => Ж.
В целом можно отметить, что в динамике имеет место замедление времени эвакуации жирной пищи, и достоверное ускорение времени эвакуации белковой пищи во II группе больных. Таким образом в каждой из обследованных групп произошла сложная трансформация дифференцированности эвакуации - изменение соотношения скорости эвакуируемых продуктов и отсутствие достоверной разницы во времени эвакуации различных тестовых завтраков.
Проведено сравнение полученных данных с нормальными показателями эвакуации: "углеводный" завтрак - 29,5 + 1,4; "белковый" - 37,8 + 1,7; "жировой" - 48,1 + 1,2 мин (Аблязов А.А., 1992 г). В I группе больных отмечено достоверное ускорение времени эвакуации жирной пищи (p < 0,001). Во II группе - достоверное ускорение времени эвакуации белковой (p < 0,001) и жировой пищи (p < 0,01). В III группе только белковый завтрак эвакуировался достоверно быстрее, чем в группе здоровых лиц (p < 0,01).
При сравнении с нормальными показателями в ранние сроки послеоперационного периода происходит ускорение эвакуации жирной пищи, нормализующееся в поздние сроки и резко замедлено эвакуируется белковая пища. Через год после операции происходит ускорение эвакуации белковой пищи, сохраняющееся в отдаленном послеоперационном периоде.
На основании полученных данных можно сделать вывод об адаптации и компенсации гастропанкреатоэнтерального комплекса в различные сроки после ПДР.
Таким образом, адаптационно-компенсаторные перестройки в органах гастропанкреатоэнтеральной зоны после ПДР развиваются в течение первых 6 месяцев послеоперационного периода.
Примеры.
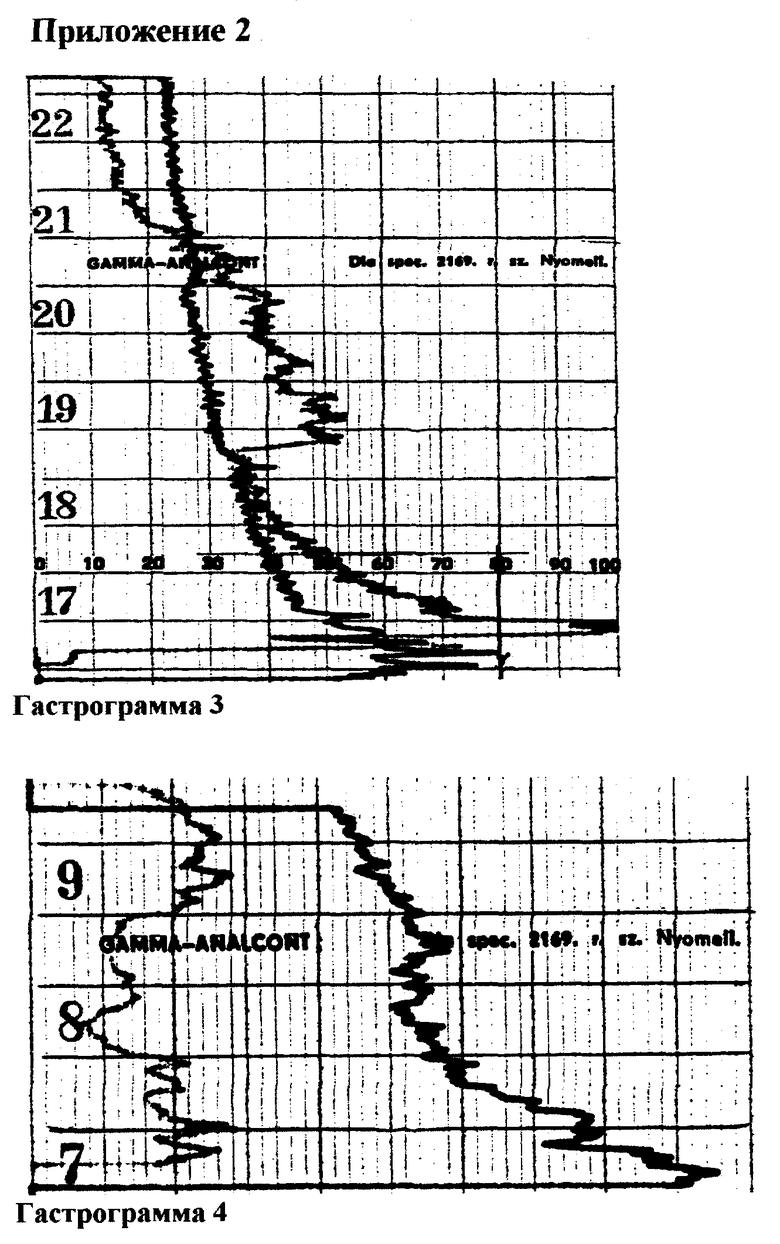
1. Больной А. , 32 г, история болезни N 7375 (1992 г). Диагноз: высоко дифференцированная аденокарцинома поджелудочной железы (ПГИ N 7617-7823). ПДР от 10.04.92 г. С 12.08.92 г по 15.08.92 г был обследован радионуклидным способом определения дифференцированной эвакуации тестовых завтраков, меченных 99 m Тс (первые 6 месяцев после ПДР). На гастрограмме 1 (см. приложение 1) мы видим, что период полувыведения "углеводного" завтрака составил 25 мин (кривая справа) (скорость движения ленты 1 см/ 5 мин, отсчет времени начинается с цифры 30 по горизонтальной оси), на гастрограмме 2 показан период полувыведения "белкового" завтрака, который составил 20 мин (кривая справа) (отсчет времени начинается с цифры 23 по горизонтальной оси). Кривая справа на гастрограмме 3 (см. приложение 2) (отсчет начинается с цифры 27 по горизонтальной оси) выражает период полувыведения "жирового" завтрака: 18 мин.
Состояние больного на момент осмотра удовлетворительное, жалоб не предъявляет, сонографических признаков хронического панкреатита нет, пептических язв гастроэнтеро анастомоза гастроскопически не выявлено. Эти показатели указывают на компенсацию ГПЭК в этот срок после ПДР.
2. Больная К. , 52 г., история болезни N 143 (1994 г). Диагноз: Аденокарцинома большого дуоденального соска (БДС). ПГИ N 1911- 9847. Произведена ПДР 02.02.94 г. С 11.05.94 г по 14.05.94 г произведено радионуклидное исследование дифференцированной эвакуации тестовых завтраков, меченных 99 m Тс (3 месяца после операции).
На гастрограмме 4 (приложение 2) мы видим, что период полувыведения "углеводного" завтрака составил 23 мин. Период полувыведения "белкового" завтрака (гастрограмма 5, приложение 3, отсчет времени ведется от цифры 27 по горизонтальной оси) составил 27,5 мин. Соответственно "жирового" (гастрограмма 6) - 19 мин. На момент осмотра больная в удовлетворительном состоянии, жалоб не предъявляет, УЗ-признаков хронического панкреатита культи поджелудочной железы не выявлено, пептических язв гастроэнтероанастомоза не обнаружено. Эти показатели, как и в первом примере, указывают на компенсацию ГПЭК после ПДР.
Медико-социальная эффективность.
Этот метод прост, доступен, занимает мало времени и заменяет целый комплекс клинических, инструментальных и лабораторных исследований, дает полную оценку адаптационно-компенсаторного состояния гастропанкреатоэнтерального комплекса после панкреатодуоденальной резекции. При условии удовлетворительного уровня адаптации и компенсации следует ставить вопрос о восстановлении трудоспособности через 12 месяцев после операции, что имеет несомненный экономический эффект.



Способ может быть использован в медицине, а именно в гастроэнтерологии. Определяют скорость эвакуации желудочного содержимого при последовательном введении больному углеводного, белкового, жирового завтраков с радиоактивной меткой. При условии изменения скорости эвакуации тестовых завтраков в последовательности белковый, углеводный, жировой определяют нормальный уровень адаптационно-компенсаторного состояния. При нарушениях дифференцировки эвакуации тестовых завтраков определяют декомпенсацию гастропанкреатоэнтерального комплекса. Способ обеспечивает упрощение опенки и сокращение времени ее проведения. 1 табл., 6 ил.
Способ оценки адаптационно-компенсаторных показателей гастропанкреатоэнтерального комплекса после панкреатодуоденальной резекции, включающий выявление клинических данных, отличающийся тем, что больному вводят последовательно углеводный, белковый, жировой завтраки с радиоактивной меткой и при условии эвакуации желудочного содержимого в последовательности преимущественно белковые, углеводные, жировые компоненты, определяют нормальный уровень адаптационно-компенсаторного состояния, а при условии нарушения данной последовательности определяют нарушение компенсаторных показателей.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Шелагуров А.А | |||
| Болезни поджелудочной железы | |||
| - М.: Медицина, 1980, с.360 | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Способ исследования органов пищеварительной системы | 1980 |
|
SU942711A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Способ диагностики синдрома нарушенного кишечного всасывания | 1980 |
|
SU957866A1 |
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| 1979 |
|
SU826244A1 | |
Авторы
Даты
1999-12-27—Публикация
1998-11-30—Подача