Изобретение относится к новым пирролиденметильным производным, к использованию известных и новых пирролиденметильных производных в качестве терапевтических средств, в частности, в качестве иммунологических средств, к способу их получения, а также к фармацевтическим композициям, содержащим их.
В литературе имеются сообщения о нескольких производных пирролиденметила, например, в приведенных ниже работах /J. Antibiotics 24, 636 (1971); Mar. Biol. 34, 223 (1976); Can. J. Microbiol. 22, 658 (1976); Can. J. Chem. 56, 1155 (1978); Tetrahedro Letters 24, 2797 (1983) J. Antibiotics 38, 128 (1985); Gen. Microbiol 132, 1899 (1986); J. Antibiotics 28, 194 (1975); Nature 213, 903 (1967); Tetrahedron Letters 24, 2701 (1983); J. Antibiotics 39, 1155 (1986); J. 6 1280 429-A и J 0 2250 828-A).
Большая часть из приведенных выше ссылок относится к пирролиденметильным производным, обладающим антибактериальной, антибиотической, антимикробной и/или цитотоксической активностью. И только лишь некоторые из них относятся к производным продигнозина, проявляющим иммуносупрессивное действие.
Объектом настоящего изобретения являются новые производные 5-[(2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррола, которые имеют следующую формулу /I/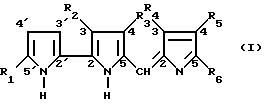
в которой R1 обозначает водород, галогеновую, фенильную, C1-C20 алкильную или C2-C20 алкенильную группу, при этом алкильная или алкенильная группы могут быть не замещены или замещены в количестве от 1 до 3 заместителями, отобранными независимо друг от друга из галогена, C1-C6 алкокси, гидрокси, арильной и арилоксигрупп;
R2 обозначает водород, C1-C6 алкильную, циано, карбокси или (C1-C6 алкокси)карбонильную группы;
R3 обозначает галогеновую, гидрокси или C1-C11 алкоксигруппы, незамещенные или замещенные фенилом;
R4 обозначает водород, C1-C6 алкил или фенил;
каждый из R5 и R6 обозначают независимо друг от друга водород, C2-C20 алканоильную, C3-C20 алкеноильную, фенильную, C1-C20 алкильную или C2-C20 алкенильную группы, при этом алканоильная, алкеноильная, алкильная и алкенильная группы могут быть не замещены или замещены в количестве от 1 до 3 заместителями, отобранными независимо друг от друга из галогена, C1-C6 алкокси, гидрокси, арила, арилокси, циано, карбокси, (C1-C6 алкокси)карбонила, (C3-C4 алкенил)карбамоила, аралкилкарбамоила, арилкарбамоила и CONRcRd, в которых каждый из Rc и Rd представляют независимо друг от друга водород или C1-C6 алкил или Rc и Rd, взятые вместе с атомом азота, с которым они связаны, образуют морфолиновое или пиперидиновое кольцо; или два заместителя из R4, R5 и R6, взятые вместе, образуют C4-C12 полиметиленовую цепь, которая может быть не замещена или замещена C1-C12 алкильной, C2-C12 алкенильной или C1-C12 алкилиденовой группами, при этом алкильная, алкенильная и алкилиденовая группы могут быть, в свою очередь, не замещены или замещены заместителем, выбранным из галогена, C1-C6 алкокси, гидрокси, циано, карбокси, (C1-C6 алкокси)карбонила, арилокси и арила; остающиеся группы представлены водородом или C1-C12 алкилом;
а также их фармацевтически приемлемые соли; и в которой
в случае, если R3 представляет собой метокси, а R1, R2, R4 и R5 являются водородами, то R6 отличается от водорода, н-нонила или н-ундецила; и в которой
в том случае, если R3 представляет собой метоксигруппу, а R1, R2, R4 и R6 являются водородами, то R5 отличается от н-ундецила; и в которой
в том случае, если R3 представляет собой метоксигруппу, а R1 и R2 являются водородами, тогда как R4 и R6 обозначают метилы, то R5 не должен быть водородом или этилом; и в которой
в том случае, если R3 представляет собой метоксигруппу, а R1, R2 и R5 являются водородами, то R4 и R6, взятые вместе, отличаются от α-этил-нонаметиленовой или α-бутил-гептаметиленовой цепи; и в которой
в том случае, когда R3 представляет собой метоксигруппу, R6 представляет собой метил, а R1, R2 и R4 являются водородами, то R5 отличается от н-пентила, н-гексила, н-гептила или н-ундецила; и в которой
в том случае, если R3 представляет собой метоксигруппу, а R1, R2 и R4 являются водородами, то R5 и R6, взятые вместе, отличаются от α-бутил-гептаметиленовой цепи; или если R5 обозначает метил, то R6 отличается от н-пентила; или если R5 обозначает этил, то R6 отличается от н-бутила; и в которой
если R3 представляет собой гидроксигруппу, а R1, R2 и R4 обозначают водород, а R6 обозначает метил, то R5 отличается от н-пентила; и в которой
если R3 представляет собой метоксигруппу, а R1 и R2 обозначают водород, тогда как R6 обозначает метил, то R4 и R5, взятые вместе, отличаются от α-метил-тетраметиленовой или β- метил-тетраметиленовой цепи; или если R4 обозначает н-пропил, то R5 отличается от н-гептила.
Настоящее изобретение включает в свой объем все возможные изомеры - стереоизомеры и оптические изомеры, а также их смеси, метаболиты и метаболические предшественники, или биопредшественники соединений формулы /I/.
Соединения настоящего изобретения могут быть представлены следующей таутомерной формулой /Ia/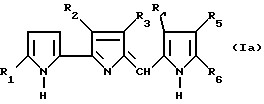
в которой R1, R2, R3, R4, R5 и R6 соответствуют определениям, данным выше. Химические соединения настоящего изобретения на протяжении всего описания изобретения именуются в соответствии с химической номенклатурой, относящейся к соединениям либо формулы /I/, либо формулы /Ia/, которые на основе структурных особенностей того или иного соединения может идентифицировать любой специалист в данной области.
Атом галогена является в предпочтительном варианте хлором или фтором. Алкильная, алкокси, алкенильная, алканоильная, алкеноильная, алкадиеноильная и алкилиденовая группы могут иметь разветвленную или линейную цепочку.
Арильная группа, выполняющая как роль заместителя, как и составляющей арилокси, аралкильной или арилкарбамоильной группы, т. е. ароматической C6-C20 моно- или поли-ядерной структуры, в типичном случае представляет фенил, который может быть не замещен или замещен в количестве от одного до двух заместителей, отобранных из галогена, гидрокси, C1-C6 алкила и C1-C6 алкокси.
Соответственно, если аралкильная группа представлена бензилом или фенэтилом, то фенильное кольцо может быть необязательно замещено в количестве от одного до двух заместителями, отобранными независимо друг от друга из галогена, гидрокси, C1-C6 алкила и C1-C6 алкокси.
C4-C12 полиметиленовая цепь представлена предпочтительно C4-C9 полиметиленовой цепью.
C3-C4 или C3-C6 алкенильная группа представлена предпочтительно аллильной группой.
C1-C6 алкильная группа представлена предпочтительно C1-C4 алкильной группой, в частности, метильной или этильной группами.
C1-C12 алкильная группа представлена предпочтительно C1-C6 алкильной группой.
Незамещенная C1-C11 алкоксигруппа представлена предпочтительно C1-C4 алкокси или C8-C11 алкоксигруппой, в типичном случае - метокси, этокси, пропокси, бутокси или ундецилоксигруппами.
C1-C6 алкоксигруппа, замещенная фенилом, представлена предпочтительно фенил-C1-C4 алкоксигруппой, в типичном случае - бензилокси или фенилэтоксигруппой.
C1-C20 алкильная группа представлена предпочтительно C5-C14 алкильной группой, в частности ундецильной группой.
C2-C20 алкенильная группа представлена предпочтительно C5-C14 алкенильной группой, в частности, ундеценильной группой.
C2-C20 алканоильная группа представлена предпочтительно C5-C14 алканоильной группой, в частности, ундеканоильной группой.
C3-C20 алкеноильная группа представлена предпочтительно C5-C14 алкеноильной группой, в частности, ундеценоильной группой.
C1-C12 алкилиденовая группа представлена предпочтительно C1-C8 алкилиденовой группой, в частности, C4-C6 алкилиденовой группой.
C2-C12 алкенильная группа представлена предпочтительно C3-C6 алкенильной группой.
(C1-C6 алкокси) карбонильная группа представлена предпочтительно (C1-C4 алкокси)карбонильной группой.
Примеры фармацевтически приемлемых солей включают либо соли, полученные на основе неорганических оснований, таких как гидроксиды натрия, калия, кальция и алюминия, либо на основе органических оснований, таких как лизин, аргинин, N-метил-глюкамин, триэтиламин, триэтаноламин, дибензиламин, метилбензиламин, ди-(2-этил-гексил)-амин, пиперидин, N-этилпиперидин, N,N-диэтиламиноэтиламин, N-этилморфолин, β- фенэтиламин, N-бензил- β- фенэтиламин, N-бензил-N,N-диметиламин и другие приемлемые органические амины, а также соли, полученные либо на основе неорганических кислот, таких как соляная, бромистоводородная и серная кислоты, либо на основе органических кислот, таких как лимонная, винная, малеиновая, яблочная, фумаровая, метансульфоновая и этансульфоновая кислоты.
Как было упомянуто выше, настоящее изобретение включает также в свой объем фармацевтически приемлемые биопредшественники /известные также как пролекарства/ соединений формулы /I/, т.е. соединения, которые имеют формулу, отличную от приведенной выше формулы /I/, однако которые при введении в организм человека превращаются in vivo прямо или непрямо в соединения формулы /I/.
Предпочтительными соединениями настоящего изобретения являются соединения формулы /I/, в которых при соблюдении указанных выше условий
R1 обозначает водород, C1-C12 алкил или C2-C12 алкенил, при этом упомянутые алкильная и алкенильная группы могут быть не замещены или замещены арилом или арилокси;
R2 обозначает водород, циано, карбокси или /C1-C4 алкокси/ карбонил;
R3 обозначает гидрокси или C1-C11 алкоксигруппы, не замещенные или замещенные фенилом;
R4 обозначает водород или C1-C4 алкил;
каждый из R5 и R6 обозначают независимо друг от друга водород, C3-C14 алкил или C3-C14 алкенил, при этом алкильная и алкенильная группы могут быть не замещены или замещены заместителем, отобранным из галогена, C1-C4 алкокси, гидрокси, арила, арилокси, циано, карбокси, /C1-C4 алкокси/карбонила, аралкилкарбамоила, арилкарбамоила и -CONRcRd, в которых каждый из Rc и Rd представляют собой независимо друг от друга водород или C1-C4 алкил или Rc и Rd, взятые вместе с атомом азота, с которым они соединены, образуют морфолиновое или пиперидиновое кольцо; или две группировки из R4, R5 и R6, взятые вместе, образуют C4-C9 полиметиленовую цепь, которая может быть не замещена или замещена C1-C6 алкильной, C3-C6 алкенильной или C1-C8 алкилиденовой группами, при этом алкильная, алкенильная и алкилиденовая группы могут быть, в свою очередь, не замещены или замещены заместителем, отобранным из галогена, C1-C4 алкокси, гидрокси, циано, карбокси, (C1-C4 алкокси)карбонила, арилокси и арила; тогда как остающиеся положения заняты водородом или C1-C6 алкилом; и их фармацевтически приемлемые соли.
Примеры наиболее предпочтительных соединений настоящего изобретения включают:
4-метокси-5-{ [5-(ундец-10-ен-1-ил)- 2H-пиррол-2-илиден]метил}-2,2'-би-1H-пиррол;
4-этокси-5-[(5-децил- 2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол;
4-этокси-5-[5-додецил- 2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол;
4-этокси-5-[(3,5-нонаметилен- 2H-пиррол-2-илиден)метил] -2,2'-би-1H-пиррол;
4-этокси-5-[(5-ундецил- 2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол;
4-пропокси-5-[(5-ундецил- 2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол;
4-этокси-5-{ [5-(ундец-10-ен-1-ил)- 2H-пиррол-2-илиден]метил}-2,2'-би-1H-пиррол;
4-изопропокси-5-[(5-ундецил- 2H-пиррол-2-илиден)метил] -2,2'-би-1H-пиррол;
4-амилокси-5-[(5-ундецил- 2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол;
4-ундецилокси- 5-[(5-ундецил-2H-пиррол-2-илиден)метил] -2,2'-би-1H-пиррол;
4-бензилокси- 5-[(5-ундецил-2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол;
4-бензилокси- 5-[(2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол;
4-ундецилокси- 5-[(2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол;
4-метокси- 5-[(5-тридецил-2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол;
4-этокси- 5-[(5-тридецил-2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол;
4-бутокси- 5-[(5-тридецил-2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол;
4-бензилокси- 5-[(5-тридецил-2H-пиррол-2-илиден)метил] -2,2'-би-1H-пиррол;
4-метокси- 5-[[(5-фенокси-пент-1-ил)-2H-пиррол-2-илиден] метил] -2,2'-би-1H-пиррол;
4-этокси- 5-[[(5-фенокси-пент-1-ил)-2H-пиррол-2-илиден]метил]-2,2'-би-1H-пиррол;
4-бутокси- 5-[[5-(5-фенокси-пент-1-ил)-2H-пиррол-2-илиден]метил]-2,2'-би-1H-пиррол;
4-бензилокси- 5-[[5-(5-фенокси-пент-1-ил)-2H-пиррол-2-илиден] метил] -2,2'-би-1H-пиррол;
4-метокси-5-[[5-(6-фтор-гекс-1-ил)- 2H-пиррол-2-илиден]метил]-2,2'-би-1H-пиррол;
4-метокси-5-[[5-(6-гидрокси-гекс-1-ил)- 2H-пиррол-2-илиден] метил] -2,2'-би-1H-пиррол;
4-метокси-5-[[5-(5-морфолинокарбоксамидо-пент-1-ил)- 2H-пиррол-2-илиден] метил]-2,2'-би-1H-пиррол; и
4-метокси-5-[[5-(7-циано-гепт-1-ил)- 2H-пиррол-2-илиден] метил] -2,2'-би-1H-пиррол;
и их фармацевтически приемлемые соли, в частности гидрохлориды, гидробромиды и метансульфонаты.
Кроме того, настоящее изобретение относится к соединению формулы /IB/
в которой R'1 обозначает водород, фенильную, C1-C20 алкильную или C2-C20 алкенильную группы, при этом алкильная и алкенильная группы могут быть или не замещены, или замещены в количестве от 1 до 3 заместителями, отобранными из галогена, C1-C6-алкокси, гидрокси, арила и арилокси;
R'2 обозначает водород, C1-C6 алкил, циано, карбокси или (C1-C6 алкокси)карбонил;
R'3 обозначает галоген, гидрокси или C1-C11 алкоксигруппы, незамещенные или замещенные фенилом;
R'4 обозначает водород, C1-C6 алкил или фенил;
каждый из R'5 и R'6 представляют собой независимо друг от друга водород, C2-C20 алканоил, C3-C20 алкеноил, фенил, C1-C20 алкил или C2-C20 алкенил, при этом алканоильная, алкеноильная, алкильная и алкенильная группы могут быть не замещены или замещены в количестве от 1 до 3 заместителями, отобранными независимо друг от друга из галогена, C1-C6 алкокси, гидрокси, арила, арилокси, циано, карбокси, (C1-C6 алкокси)карбонила, (C3-C4 алкенил)карбамоила, аралкилкарбамоила, арилкарбамоил и -CONRcRd, в которых каждый из Rc и Rd представляют собой независимо друг от друга водород или C1-C6 алкил, или Rc и Rd, взятые вместе с атомом азота, с которым они соединены, образуют морфолиновое или пиперидиновое кольцо; или две группировки из R'4, R'5 и R'6, взятые вместе, образуют C4-C12 полиметиленовую цепь, которая может быть незамещенной или может быть замещена C1-C12 алкильной, C2-C12 алкенильной или C1-C12 алкилиденовой группой, при этом алкильная, алкенильная и алкилиденовая группы могут быть, в свою очередь, не замещены или замещены заместителем, отобранным из галогена, C1-C6 алкокси, гидрокси, циано, карбокси, (C1-C6 алкокси)карбонила, арилокси и арила; тогда как остающиеся положения заняты водородом или C1-C12 алкилом; или их фармацевтически приемлемые соли;
и в которой
в том случае, если R'3 представляет собой метоксигруппу, а R'1, R'2, R'4 и R'5 являются водородами, то R'6 отличен от н-нонила или н-ундецила; и в которой
в том случае, если R'3 представляет собой метокси, а R'1, R'2 и R'5 являются водородами, то R'4 и R'6, взятые вместе, не должны представлять собой α-этил-нонаметиленовую цепь; и
в которой
в том случае, если R'3 представляет собой метоксигруппу, R'6 обозначает метил, а R'1, R'2 и R'4 являются водородами, то R'5 отличен от н-пентила: и в которой
в том случае, если R'3 представляет собой метоксигруппу, а R'1, R'2 и R'4 являются водородами, то R'5 и R'6, взятые вместе, отличаются от α-бутил-гептаметиленовой цепи; и в которой
в том случае, если R'3 представляет собой гидроксигруппу, а R'1, R'2 и R'4 обозначают водород, тогда как R'6 обозначает метил, то R'5 отличен от н-пентила; и в которой
в том случае, если R'3 представляет собой метоксигруппу, а R'1 и R'2 являются водородами, тогда как R'6 является метилом, то R'4 и R'5, взятые вместе, отличаются от α-метил-тетраметиленовой цепи;
которое используется в качестве лекарственного препарата, в частности в качестве иммуномодулирующего средства, в особенности в качестве иммуносупрессивного средства.
Аналогично соединениям формулы /I/, соединения формулы /IB/ также могут быть представлены в виде соответствующей таутомерной формулы, как это очевидно для специалистов в данной области.
Предпочтительными значениями заместителей R'1, R'2 R'3, R'4, R'5 и R'6, встречающихся в формуле /IB/, являются те значения, которые приведены для соответствующих заместителей в описании, относящемся к формуле /I/.
Примерами фармацевтически приемлемых солей соединения формулы /IB/ являются те же соединения, которые указаны выше применительно к соединениям формулы /I/.
Предпочтительными соединениями настоящего изобретения, как указано выше, являются те соединения, в которых при соблюдении указанных выше условий
R'1 обозначает водород C1-C12 алкил или C2-C12 алкенил, при этом упомянутые алкильная и алкенильная группы могут быть не замещены или замещены арилом или арилокси;
R'2 обозначает водород, циано, карбокси или (C1-C4 алкокси) карбонил;
R'3 обозначает водород или C1-C11 алкоксигруппу, не замещенную или замещенную фенилом;
R'4 обозначает водород или C1-C4 алкил;
каждый из R'5 и R'6 обозначают независимо друг от друга водород, C3-C14 алкил или C3-C14 алкенил, при этом алкильная и алкенильная группы могут быть не замещены или замещены заместителем, отобранным из галогена, C1-C4 алкокси, гидрокси, арила, арилокси, циано, карбокси, (C1-C4 алкокси) карбонила, аралкилкарбамоила, арилкарбамоила и -CONRcRd, в которых каждый из Rc и Rd представляют собой независимо друг от друга водород или C1-C4 алкил или Rc и Rd, взятые вместе с атомом азота, с которым они соединены, образуют морфолиновое или пиперидиновое кольцо; или две группировки из R'4, R'5 и R'6, взятые вместе, образуют C4-C9 полиметиленовую цепь, которая может быть не замещена или замещена C1-C6 алкильной, C3-C6 алкенильной или C1-C8 алкилиденовой группами, при этом алкильная, алкенильная и алкилиденовая группы могут быть, в свою очередь, не замещены или замещены заместителем, отобранным из галогена, C1-C4 алкокси, гидрокси, циано, карбокси, (C1-C4 алкокси)карбонила, арилокси и арила; тогда как остающиеся положения заняты водородом или C1-C6 алкилом;
и их фармацевтически приемлемые соли,
Примерами отдельных соединений формулы /IB/ являются следующие соединения:
4-метокси-5-{ [5-(ундец-10-ен-1-ил)-2H-пиррол-2-илиден] метил] -2,2'-би- 1H-пиррол;
4-этокси-5-[(5-децил-2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол;
4-этокси-5-[(5-додецил-2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол;
4-этокси-5-[(3,5-нонаметилен-2H-пиррол-2-илиден)метил] -2,2'-би-1H- пиррол;
4-этокси-5-[(5-ундецил-2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол;
4-пропокси-5-[(5-ундецил-2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол;
4-этокси-5-{ [5-(ундец-10-ен-1-ил)-2H-пиррол-2-илиден]метил}-2,2'-би-1H- пиррол;
4-метокси-5-[(4-этил-3,5-диметил-2H-пиррол-2-илиден)метил] -2,2'-би-1H- пиррол;
4-метокси-5-[(4-гексил-5-метил-2H-пиррол-2-илиден)метил] -2,2'-би-1H- пиррол;
4-метокси-5-[(5-метил-4-ундецил-2H-пиррол-2-илиден]-2,2'-би-1H-пиррол;
4-изопропокси-5-[(5-ундецил-2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол;
4-амилокси-5-[(5-ундецил-2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол;
4-ундецилокси-5-[(5-ундецил-2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол;
4-бензилокси-5-[(5-ундецил-2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол;
4-бензилокси-5-[(2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол;
4-ундецилокси-5-[(2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол;
4-метокси-5-[(5-тридецил-2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол;
4-этокси-5-[(5-тридецил-2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол;
4-бутокси-5-[(5-тридецил-2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол;
4-бензилокси-5-[(5-тридецил-2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол;
4-метокси-5-[[5-(5-фенокси-пент-1-ил)-2H-пиррол-2-илиден] метил]-2,2' -би-1H-пиррол;
4-этокси-5-[[5-(5-фенокси-пент-1-ил)-2H-пиррол-2-илиден)метил] -2,2' -би-1H-пиррол;
4-бутокси-5-[[5-(5-фенокси-пент-1-ил)-2H-пиррол-2-илиден)метил] -2,2' -би-1H-пиррол;
4-бензилокси-5-[[5-(5-фенокси-пент-1-ил)-2H-пиррол-2-илиден)метил] -2,2' -би-1H-пиррол;
4-метокси-5-[[5-(6-фтор-гекс-1-ил)-2H-пиррол-2-илиден)метил] -2,2'-би- 1H-пиррол;
4-метокси-5-[[5-(6-гидрокси-гекс-1-ил)-2H-пиррол-2-илиден)метил] -2,2' -би-1H-пиррол;
4-метокси-5-[[5-(5-морфолинокарбоксамидо-пент-1-ил)-2H-пиррол-2-илиден) метил]-2,2'-би-1H-пиррол; и
4-метокси-5-[[5-(7-циано-гепт-1-ил)-2H- пиррол-2-илиден] метил] -2,2'-би-1H-пиррол;
и их фармацевтически приемлемые соли, в частности гидрохлориды, гидробромиды и метансульфонаты.
Настоящее изобретение относится также к фармацевтической композиции, включающей в качестве активного ингредиента эффективное количество соединений формулы /I/ или формулы /IB/, представленных в настоящем описании, или их фармацевтически приемлемые соли, а также фармацевтически приемлемый носитель и/или разбавитель.
Настоящее изобретение относится также к использованию соединений формулы /IC/
в которой R''1 обозначает водород, фенильную, C1-C20 алкильную или C2-C20 алкенильную группы, при этом алкильная и алкенильная группы могут быть или не замещены, или замещены в количестве от 1 до 3 заместителями, отобранными из галогена, C1-C6 алкокси, гидрокси, арила и арилокси;
R''2 обозначает водород, C1-C6 алкил, циано, карбокси или (C1-C6 алкокси)карбонил;
R''3 обозначает галоген, гидрокси или C1-C11 алкоксигруппы, незамещенные или замещенные фенилом;
R''4 обозначает водород, C1-C6 алкил или фенил;
каждый из R''5 и R''6 представляют собой независимо друг от друга водород, C2-C20 алканоил, C3-C20 алкеноил, фенил, C1-C20 алкил или C2-C20 алкенил, при этом алканоильная, алкеноильная, алкильная и алкенильная группы могут быть не замещены или замещены в количестве от 1 до 3 заместителями, отобранными независимо друг от друга из галогена, C1-C6 алкокси, гидрокси, арила, арилокси, циано, карбокси, (C1-C6 алкокси)карбонила, (C3-C4 алкенил)карбамоила, аралкилкарбамоила, арилкарбамоила и -CONRcRd, в которых каждый из RcRd. представляют собой независимо друг от друга водород или C1-C6 алкил, или Rc и Rd, взятые вместе в атомом азота, с которым они соединены, образуют морфолиновое или пиперидиновое кольца; или две группировки из R''4, R''5 и R''6, взятые вместе, образуют C4-C12 полиметиленовую цепь, которая может быть незамещенной или может быть замещена C1-C12 алкильной, C2-C12 алкенильной или C1-C12 алкилиденовой группой, при этом алкильная, алкенильная и алкилиденовая группы могут быть, в свою очередь, не замещены или замещены заместителем, отобранным из галогена, C1-C6 алкокси, гидрокси, циано, карбокси, (C1-C6 алкокси)карбонила, арилокси и арила; тогда как остающиеся положения заняты водородом или C1-C12 алкилом; или их фармацевтически приемлемые соли;
и в которой
в том случае, если R''3 представляет собой метоксигруппу, а R''1, R''2, R''4 и R''5 являются водородами, то R''6 отличен от н-ундецила; и в которой
в том случае, если R''3 представляет собой метоксигруппу, а R''1, R''2 и R''5 являются водородами, то R''4 и R''6 взятые вместе, не должны представлять собой α-этил-нонаметиленовую цепь; и в которой
в том случае, если R''3 представляет собой метоксигруппу, а R''1, R''2 и R''4 являются водородами, то R''5 и R''6, взятые вместе, отличаются от α-бутил-гептаметиленовой цепи;
для приготовления лекарственного препарата, обладающего иммуномодулирующей, в особенности иммуносупрессивной активностью.
Настоящее изобретение относится также, аналогично приведенному выше, к фармацевтической композиции, которая включает в качестве активного ингредиента эффективное количество соединения формулы /IC/, определенного выше, или его фармацевтически приемлемую соль, обладающих иммуномодулирующей, в особенности иммуносупрессивной активностью, а также фармацевтически приемлемый носитель и/или разбавитель.
Аналогично соединениям формулы /I/ и формулы /IB/, соединения формулы /IC/, как это очевидно специалисту данной области, также могут быть представлены в виде соответствующей таутомерной формулы.
Предпочтительными значениями заместителей R''1, R''2, R''3, R''4, R''5 и R''6, встречающихся в формуле /IC/, являются те значения, которые приведены для соответствующих заместителей от R1 до R6 в описании, относящемся к формуле /I/.
Примерами фармацевтически приемлемых солей соединения формулы /IC/ являются те же соединения, которые указаны выше применительно к соединениям формулы /I/.
Предпочтительными соединениями формулы /IC/, как указано выше, являются те соединения, в которых при соблюдении указанных выше условий
R''1 обозначает водород, C1-C12 алкил или C2-C12 алкенил, при этом упомянутые алкильная и алкенильная группы могут быть не замещены или замещены арилом или арилокси;
R''2 обозначает водород, циано, карбокси или (C1-C4 алкокси) карбонил;
R''3 обозначает галоген, гидрокси или C1-C11 алкоксигруппы, не замещенные или замещенные фенилом;
R''4 обозначает водород или C1-C4 алкил;
каждый из R''5 и R''6 обозначают независимо друг от друга водород, C3-C14 алкил или C3-C14 алкенил, при этом алкильная и алкенильная группы могут быть не замещены или замещены заместителем, отобранным из галогена, C1-C4 алкокси, гидрокси, арила, арилокси, циано, карбокси, (C1-C4 алкокси)карбонила, аралкилкарбамоила, арилкарбамоила и -CONRcRd, в которых каждый из Rc и Rd представляют собой независимо друг от друга водород или C1-C4 алкил или Rc и Rd, взятые вместе, образуют морфолиновое или пиперидиновое кольцо; или две группировки из R''4, R''5 и R''6, взятые вместе, образуют C4-C9 полиметиленовую цепь, которая может быть не замещена или замещена C1-C6 алкильной, C3-C6 алкенильной или C1-C8 алкилиденовой группами, при этом алкильная, алкенильная и алкилиденовая группы могут быть, в свою очередь, не замещены или замещены заместителем, отобранным из галогена, C1-C4 алкокси, гидрокси, циано, карбокси, (C1-C4 алкокси)карбонила, арилокси и арила; тогда как остающиеся положения заняты водородом или C1-C6 алкилом;
и их фармацевтически приемлемые соли.
Примерами специфичных соединений формулы /IC/ являются следующие соединения:
4-метокси-5-{ [5-(ундец-10-ен-1-ил)-2H-пиррол-2-илиден]метил}- 2,2'-би-1H-пиррол;
4-этокси-5-[(5-децил-2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол;
4-этокси-5-[(5-додецил-2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол;
4-этокси-5-[(3,5-нонаметилен-2H-пиррол-2-илиден)метил] -2,2'- би-1H-пиррол;
4-этокси-5-[(5-ундецил-2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол;
4-пропокси-5-[(5-ундецил-2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол;
4-этокси-5-{ (5-ундец-10-ен-1-ил)-2H-пиррол-2-илиден] метил} -2,2'- би-1H-пиррол;
4-метокси-5-[(4-этил-3,5-диметил-2H-пиррол-2-илиден)метил] -2,2'- би-1H-пиррол;
4-метокси-5-[(4-гексил-5-метил-2H-пиррол-2-илиден)метил] -2,2'- би-1H-пиррол;
4-метокси-5-[(5-метил-4-ундецил-2H-пиррол-2-илиден)метил] -2,2'- би-1H-пиррол;
4-метокси-5-[(5-нонил-2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол;
4-метокси-5-[(5-метил-4-пентил-2H-пиррол-2-илиден)метил] -2,2'- би-1H-пиррол;
4-изопропокси-5-[(5-ундецил-2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол;
4-амилокси-5-[(5-ундецил-2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол;
4-ундецилокси-5-[(5-ундецил-2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол;
4-бензилокси-5-[(5-ундецил-2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол;
4-бензилокси-5-[(2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол;
4-ундецилокси-5-[(2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол;
4-метокси-5-[(5-тридецил-2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол;
4-этокси-5-[(5-тридецил-2H-пиррол-2-илиден]-2,2'-би-1H-пиррол;
4-бутокси-5-[(5-тридецил-2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол;
4-бензилокси-5-[(5-тридецил-2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол;
4-метокси-5-[[5-(5-фенокси-пент-1-ил)-2H-пиррол-2-илиден] метил]- 2,2'-би-1H-пиррол;
4-этокси-5-[[5-(5-фенокси-пент-1-ил)-2H-пиррол-2-илиден]метил]- 2,2'-би-1H-пиррол;
4-бутокси-5-[[5-(5-фенокси-пент-1-ил)-2H-пиррол-2-илиден] метил]- 2,2'-би-1H-пиррол;
4-бензилокси-5-[[5-(5-фенокси-пент-1-ил)-2H-пиррол-2-илиден] метил] - 2,2'-би-1H-пиррол;
4-метокси-5-[[5-(6-фтор-гекс-1-ил)-2H-пиррол-2-илиден] метил]- 2,2'-би-1H-пиррол;
4-метокси-5-[[5-(6-гидрокси-гекс-1-ил)-2H-пиррол-2-илиден] метил] - 2,2'-би-1H-пиррол;
4-метокси-5-[[5-(5-морфолинокарбоксамидо-пент-1-ил)-2H-пиррол-2- илиден] метил]-2,2'-би-1H-пиррол; и
4-метокси-5-[[5-(7-циано-гепт-1-ил)-2H-пиррол-2-илиден] метил] - 2,2'-би-1H-пиррол;
и их фармацевтически приемлемые соли, в частности гидрохлориды, гидробромиды и метансульфонаты.
Новые соединения формулы /I/, а также уже известные соединения, описываемые формулами /IB/ и /IC/, и их фармацевтически приемлемые соли могут быть получены с помощью одних и тех же способов.
В соответствии с предпочтительным вариантом настоящего изобретения, соединение формулы /I/ и его соли могут быть получены с применением метода, включающего:
А) реакцию соединения формулы /II/
в которой R1, R2 и R3 соответствуют данным выше определениям, с соединением формулы /III/
в которой R4, R5 и R6 соответствуют данным выше определениям; или
Б) реакцию соединения формулы /IV/
в которой Ra соответствует R1, за исключением водорода, а R2 и R3 соответствуют данным выше определениям, с соединением формулы /V/
в которой R4, R5 и R6 соответствуют данным выше определениям, с целью получения соединения формулы /I/, определенного выше, в котором R1 отличен от водорода; и, если нужно, превращения соединения формулы /I/ в другое соединение формулы /I/ и/или, при необходимости, превращения соединения формулы /I/ в его фармацевтически приемлемую соль и/или, при необходимости, превращения соли в свободное соединение и/или, при необходимости, разделения смеси изомеров соединения формулы /I/ и получения единичного изомера.
Реакция между соединением формулы /II/ и соединением формулы /III/, так же, как и реакция между соединением формулы /IV/ и соединением формулы /V/, может быть проведена, например, в органическом растворителе, таком как низший алканол, т.е. метанол или этанол; тетрагидрофуран, этилацетат, дихлорметан или их смеси, при температуре, варьирующей от 0oC до температуры кипения с обратным холодильником, в присутствии неорганической кислоты, такой, как соляная, бромистоводородная, метансульфоновая кислота или BF3-этерат, предпочтительно в безводных условиях.
Соединение формулы /I/ может быть превращено, как указывалось выше, в другое соединение формулы /I/ с помощью известных методов; например, в соединениях формулы /I/ карбоксигруппа может быть превращена в соответствующую (C1-C6 алкил)- или арилкарбамоильную группы посредством реакции, соответственно, с подходящим C1-C6 алкиламином или ариламином, в присутствии подходящего карбодиимида, такого, в частности, как дициклогексилкарбодиимид или 1-(3-диметиламино-пропил)-3-этил-карбодиимид, в инертном растворителе, таком, как дихлорметан или тетрагидрофуран, при температуре, меняющейся от примерно 0 до примерно 30oC.
Необязательный процесс превращения соединения формулы /I/ в соль, так же, как и превращение соли в свободное соединение, и разделение смеси изомеров с выделением единичного изомера также могут быть проведены с применением традиционных методик. Так, например, при разделении оптических изомеров может быть проведено превращение соединения в соль с помощью оптически активных основания или кислоты с проведением последующей фракционной кристаллизации диастереоизомеров солей и затем восстановлением оптически изомерной кислой или основной форм соответственно.
Соединение формулы /II/ могут быть получены, исходя из соединения формулы /VI/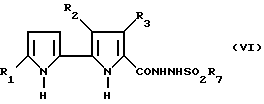
в которой R1, R2 и R3 соответствуют данным выше определениям, а R7 представляет собой арил, в частности, 4-метилфенил или 2,4,6-триизопропилфенил, с применением хорошо известного способа синтеза альдегидов по Макфадайену-Стивенсу (McFadyen-Stevens) из ацил-сульфонил-гидразидов, в соответствии, например, с обычной методикой (J. Org, Chem. 53, 1405 (1988)) или в соответствии с усовершенствованной методикой, описанной в J. Amer. Chem. Soc. 80, 862 (1958) и Tetrahedron Letters 21, 4645 (1980).
Альтернативно, соединения формулы /II/, в которых R1 отличен от водорода, могут быть получены, например, реакцией подходящего соединения формулы /IV/ с реагентом Вилсмейера, в соответствии с хорошо известной методикой /в частности, приведенной в J.Heter. Chem., 13, 497 (1976).
Соединения формулы /III/ либо представляют собой известные соединения, либо могут быть приготовлены с использованием несложных изменений методик, опубликованных в литературе, в частности, которые описаны в приведенных ниже работах
Tetrahedron, - 32, 1851 (1976);
Tetrahedron, - 32, 1967 (1976);
Tetrahedron, - 32, 1863 (1976);
Tetrahedron Letters - 25, 1387 (1984);
J. Org. Chem., - 53, 1410 (1988);
J, Org. Chem., - 28, 857 (1963);
J. Am. Chem. Soc. - 84, 4655 (1962);
Ann., - 450, 181 (1926);
Ber., - 99, 1414 (1966)).
Новые соединения формулы /IV/, которые являются предметом настоящего изобретения, могут быть синтезированы, например, посредством гидролиза и декарбоксилирования соединений формулы /VII/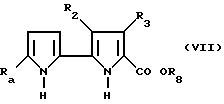
в которой R1, R2 и R3 соответствуют приведенным выше определениям, а R8 представляет собой C1-C6 алкил, полученный, к примеру, по методу, описанному в J. Heter. Chem.,13, 197 (1976).
Альтернативно, соединения настоящего изобретения формулы /IV/ могут быть получены с применением нового метода синтеза, который является еще одним объектом настоящего изобретения и который включает конденсацию соединения формулы /VIII/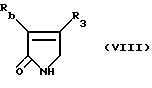
в которой R3 соответствует приведенному выше описанию, а R6 соответствует R2, определенному выше, за тем исключением, что не включает карбоксигруппу,
с соединением формулы /IX/
в которой Ra соответствует приведенному выше определению,
с получением соединения формулы /IV/, соответствующее вышеприведенным определениям, в котором R2 отличен от карбокси.
Реакция конденсации между соединением формулы /VIII/ и соединением формулы /IX/ может быть проведена под воздействием ROCl3 в отсутствие растворителя или же в присутствии инертного растворителя, такого, в частности, как дихлорметан или дихлорэтан, при температуре, меняющейся от примерно 0 до примерно 50oC.
Соединения формулы /V/, в которых R6 отличен от водорода, могут быть получены, в соответствии с хорошо известной химической методикой, при воздействии реагента Вилсмейера на соединения формулы /III/, в которых R6 отличен от водорода.
Соединения формулы /VI/ и /VII/ могут быть получены с использованием вариаций опубликованных в химической литературе методик, в частности в нижеприведенных работах /J. Org. Chem., 53, 1405 (1988); Tetrahedron Letters, 26, 1725 (1989); Tetrahedron Letters, 26, 2259 (1977)).
Когда в соединениях настоящего изобретения и в промежуточных продуктах имеются такие группы, как COOH и/или OH, которые необходимо защищать перед тем, как ввести их в описанные виды реакций, их перед реакцией подвергают защите, а затем, в соответствии с хорошо известными в органической химии методами, удаляют защищающие группы.
Соединения формулы /I, /IB/ и /IC/, а также их фармацевтически приемлемые соли определены в описании как "соединения настоящего изобретения", "соединения изобретения" или "активные ингредиенты фармацевтических композиций изобретения".
Как было показано в нескольких биологических испытаниях, соединения изобретения обладают иммуномодулирующей, в частности, иммуносупрессивной активностью.
Например, была проведена сравнительная оценка соединений настоящего изобретения и стандартного соединения - ундецилпродигиозином /VII/ - с использованием следующих тестов.
1. Пролиферация муриновых спленоцитов, индуцированных митогеном Конкавалином A.
2. Пролиферация муриновых спленоцитов, индуцированных облученными аллогенными муриновыми клетками селезенки /MLR/.
3. Пролиферация линий опухолевых клеток /линии эритролейкоза К562 человека, муриновой меланомы B16/.
Тесты 1 и 2 позволяют исследовать соединения в рамках модели пролиферации, опосредованной T-клеточными ростовыми факторами, /т.е. IL-2/, которые считаются иммунологически специфичными.
Тест 3 дает возможность исследовать ингибирующее действие соединений настоящего изобретения на видоспецифичный способ пролиферации, независимо от действия иммуноспецифичных ростовых факторов.
Указанные тесты были выполнены следующим образом:
Тест1
У мышей C 57 B 1/6 в асептических условиях удаляют селезенку, после чего на основе полной среды готовят суспензию клеток. Жизнеспособность клеток оценивают по методу исключения с помощью трипана синего.
Клетки селезенки /4•105/ культивируют в тройном повторе в объеме 0,15 мл на чашках для микрокультивирования с плоским дном в отсутствие или в присутствии оптимальной концентрации КонА (17 мкг/мл) и различных концентраций исследуемого соединения. Культуры инкубируют в течение 72 часов при 37 oC, в условиях увлажнения и поддержания содержания CO2 на уровне 5%; за 18 часов до окончания культивирования в каждую ячейку вносят 0,2 мкCi [метил-H3] тимидина. Клетки собирают на фильтрах из стекловолокна и с помощью жидкостного сцинтилляционного счетчика подсчитывают поглощение [H3] TдP (CPm).
Тест 2
У мышей C57B1/6 /респондеры/ и у мышей Balb /c /стимуляторы/ в асептических условиях удаляют селезенку и на основе полной среды готовят суспензию клеток. Клетки респондеры /1 • 106/ в тройном повторе культивируют совместно с облученными /1500 R/ клетками стимуляторами /5 • 105/ в объеме 0,15 мл в присутствии или в отсутствии различных концентраций исследуемых соединений на чашках для микрокультивирования с плоским дном. Культуры инкубируют в течение 96 часов при 37oC в условиях увлажнения в инкубаторе с 5% содержанием CO2; последние 18 часов инкубация проводится в присутствии 0,2 мк Ci H3-TдP.
Клетки собирают на стеклянно-волокнистом фильтре, после чего на жидкостно-сцинтилляционном счетчике определяют поглощение H3-TдP (cpm).
Тест 3
Опухолевые клетки собирают в логарифмической фазе роста и высевают с тройным повтором на чашки для микрокультивирования с плоским дном в концентрации 1 • 104 в присутствии или в отсутствие различных концентраций исследуемого соединения. После 48 часов инкубации при 37oC в присутствии 5% CO2 оценивают жизнеспособность клеток по колориметрическому методу на основе 3-(4,5-диметилтиазол-2-ил)-2,5-дифенилтетразолия бромида /метод MTT/ (Ferrari et al., J. Immunol. Methods (1990) 131, 1965-72).
Концентрация, ингибирующая на 50% пролиферацию клеток /ИК50/ в различных вариантах была вычислена как для исследуемых соединений, так и для стандарта VII. Соотношение между средними значениями ИК50 для роста опухолевых клеток /тест 3/ и значениями ИК50 для пролиферации лимфоцитов /определенные с помощью тестов 1 и 2/ характеризует терапевтический индекс /ТИ/ соединений.
В табл. 1 представлены данные, полученные в указанных испытаниях.
В табл. 1 стандартное соединение UP /VII/ представляет собой 4-метокси-5-[(5-ундецил-2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол, гидрохлорид.
FCE 28512 представляет собой 4-этокси-5-[(5-ундецил-2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол, гидрохлорид.
FCE 28526 представляет собой 4-метокси-5-[(5-тридецил-2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол, гидрохлорид.
FCE 28733 представляет собой 4-этокси-5-[(5-тридецил-2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол, гидрохлорид.
FCE 28789 представляет собой 4-бутокси-5-[(5-ундецил-2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол, гидрохлорид.
FCE 29002 представляет собой 4-бензилокси-5-[(5-ундецил-2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол, гидрохлорид.
Эти данные показывают, что представленные соединения настоящего изобретения обеспечивают значительно более высокий уровень ТИ, чем стандартное соединение, демонстрируя, что их иммуносупрессивное действие более специфично относительно активированных лимфоцитов. В соответствии с этим, соединения настоящего изобретения обладают более значимыми иммунофармакологическими свойствами, чем известное соединение - ундецилпродигиозин.
Исходя из этого, соединения настоящего изобретения могут использоваться для млекопитающих, включая человека, в качестве иммуносупрессивных агентов для профилактики и лечения реакции отторжения, связанной с трансплантацией тканей и органов, болезнью "трансплантат против хозяина" и аутоиммунными заболеваниями. Человека или животное подвергают лечению с помощью методов, включающих введение терапевтически эффективного количества соединения изобретения или фармацевтически приемлемой его соли. И таким образом можно достигнуть улучшения состояния пациента - человека или животного.
Предпочтительные случаи состояний, связанных с трансплантацией, которые могут успешно излечиваться с помощью соединений настоящего изобретения, описанных выше, включают, например, случаи трансплантации сердца, почки и костного мозга. Предпочтительные случаи аутоиммунных заболеваний, которые могут быть успешно излечены с помощью соединений настоящего изобретения, включают, например, такие состояния и заболевания, как ревматоидный артрит, системная красная волчанка, юношеский диабет, аутоиммунная гемолитическая анемия, миастения, множественный склероз, псориаз, язвенный колит, идиопатическая геморрагическая пурпура, активный хронический гепатит, гломерулонефрит, идиопатическая лейкоцитопения, первичный билиарный цирроз, тиреоидит, тиреотоксикоз, дерматомиозит, дискоидная красная волчанка, псориазный артрит, реплональный энтерит, нефротический сидром, волчаночный нефрит, волчаночный гепатит, синдром Шегрена, синдром Гудпастура, гранулематоз Вегенера, склеродермия, синдром Сезари, увент и орхит, возникший как осложнение эпидемического паротита. В типичном случае такими заболеваниями являются ревматоидный артрит, системная красная волчанка, юношеский диабет, миастения, множественный склероз и псориаз.
Используемый способ лечения различных клинических синдромов должен быть адаптирован к типу той или иной патологии, при этом, как обычно, должен быть подобран соответствующий способ введения препарата, форма, в которой предпочтительно вводить указанное активное соединение с учетом возраста, веса и состояния пациента.
При этом пероральный способ введения является приемлемым для всех состояний, для лечения которых необходимо введение такого соединения. Для лечения острых состояний предпочтение отдается внутривенной инъекции или инфузии.
Для проведения курсов поддерживающего лечения предпочтительно использование перорального или парентерального, т.е. внутримышечного или подкожного, способов. Для этих целей соединения настоящего изобретения, а именно: FCE 28512 может вводиться перорально в дозах, варьирующих от примерно 1 до примерно 20 мг/кг веса тела взрослого человека в день.
Меняющиеся дозы активных соединений, а именно от примерно 0,25 до примерно 5 мг/кг веса в день, могут применяться для парентерального введения и внутривенных инъекций или инфузий взрослым людям. Конечно, с целью достижения оптимального терапевтического эффекта режим дозирования может быть соответствующим образом изменен.
Состав фармацевтической композиции, содержащей соединения настоящего изобретения в сочетании с фармацевтически приемлемыми носителями или разбавителями будет, конечно, зависеть от выбранного способа введения.
Композиции могут быть получены традиционным способом с применением обычных ингредиентов. Так, соединения настоящего изобретения могут вводиться в виде водных или масляных растворов или суспензий, таблеток, драже, желатиновых капсул, сиропов, капель и суппозиториев.
Так, в случае применения перорального способа фармацевтические композиции, содержащие соединения настоящего изобретения, предпочтительно вводить в виде таблеток, драже или желатиновых капсул, содержащих активное вещество в сочетании с такими разбавителями, как лактоза, декстроза, сахароза, маннит, сорбит, целлюлоза; со смазочными веществами, такими, например, как кремнезем, тальк, стеариновая кислота, стеарат магния или кальция и/или полиэтиленгликоли; кроме того, они могут содержать такие связывающие вещества, как крахмалы, желатин, метилцеллюлоза, карбоксиметилцеллюлоза, аравийскую камедь, трагант, поливинилпирролидон; средства, способствующие разложению, такие как крахмалы, альгиновая кислота, альгинаты, крахмал-натрий-гликолят; шипучие смеси; красители; подсластители; увлажняющие вещества, такие как лецитин, полисорбаты, лаурилсульфаты и, в целом, нетоксичные и фармакологически неактивные вещества, применяемые для приготовления фармацевтических средств.
Указанные фармацевтические препараты могут быть приготовлены с применением известных способов, включающих смешивание, гранулирование, таблетирование, нанесение сахарного или пленочного покрытия.
В качестве жидких дисперсий для перорального введения могут использоваться, в частности, сиропы, эмульсии и суспензии.
Сиропы могут содержать в качестве носителя, например, сахарозу или смесь сахарозы с глицерином и/или маннитом и/или сорбитом.
Суспензии и эмульсии могут содержать в качестве носителя, например, натуральную камедь агар, альгинат натрия, пектин, метилцеллюлозу, карбоксиметилцеллюлозу или поливиниловый спирт.
Суспензии или растворы для внутримышечного введения могут содержать, в дополнение к активному соединению, фармацевтически приемлемый носитель, в частности, стерильную воду, оливковое масло, этилолеат, гликоли, в том числе пропиленгликоль и, при необходимости, подходящее количество гидрохлорида лидокаина.
Растворы для внутривенных инъекций или инфузий могут содержать в качестве носителя, например, стерильную воду или в предпочтительном варианте их готовят на основе стерильных водных изотонических солевых растворов.
Суппозитории могут содержать, в дополнение к активному соединению, фармацевтически приемлемый носитель, такой как масло какао, полиэтиленгликоль, поверхностно-активный эфир жирной кислоты и полиоксиэтиленсорбитана или лецитин.
Настоящее изобретение относится также к продуктам, содержащим соединение формулы /IC/ или его фармацевтически приемлемые соли, и дополнительные лекарственные средства, входящие в комбинированный препарат для одновременного, раздельного или последовательного использования его в ходе иммуносупрессивной терапии млекопитающих. Таким дополнительным лекарственным средством могут быть, например, кортикостероид, иммуносупрессивное или противоопухолевое средство, а также смеси двух или более таких компонентов.
Термин "противоопухолевое средство" в применяемом контексте включает как единичный противоопухолевый лекарственный препарат, так и их "коктейли", т. е. смесь таких лекарств, созданную на основе результатов клинической практики.
Примеры противоопухолевых средств, которые могут быть объединены с соединением формулы /IC/, включают метотрексат, микофеноловую кислоту и циклофосфамид, а также их смеси.
Термин "иммуносупрессивное средство" в применяемом контексте включает как единичный иммуносупрессивный препарат, так и "коктейли", т.е. смеси, созданные на основе результатов клинической практики.
Примеры иммуносупрессивных средств, которые могут быть объединены с соединением формулы /IC/, включают циклоспорин A, F K506, рапамицин и азатиоприн, а также их смеси. Аналогично, предпочтительным примером кортикостероидов является дексаметазон.
Следующие ниже примеры приведены только лишь с целью иллюстрации настоящего изобретения, но не ограничения его.
Пример 1
Этиловый эфир 3-гидрокси-пиррол-2-карбоновой кислоты (2,5 г), приготовленный в соответствии с описанной в литературе методикой /Chem. Pharm. Bull. , 26, 2228 (1978)); в тетрагидрофуране (25 мл) добавляют по каплям при перемешивании при 25oC к суспензии 60% NaH (0,71 г) в тетрагидрофуране /25 мл/. После прекращения шипения /примерно через 30 минут/ добавляют диэтилсульфат /3,16 мл/, и реакционную смесь выдерживают при перемешивании при комнатной температуре в течение 64 часов. Полученный раствор обрабатывают 10% NH4OH в течение 10 минут, затем экстрагируют этилацетатом, промывают солевым раствором и выпаривают досуха в вакууме.
Остаток чистят на флэш-колонке с использованием для элюции смеси толуол/этилацетат /8: 2/, получая при этом 3,35 г этилового эфира 3-этокси-пиррол-2-карбоновой кислот. Tпл 81-83oC, который растворяют в тетрагидрофуране /65 мл/ и затем добавляют по каплям при перемешивании при температуре 25 - 30oC к суспензии 60% NaH (0,73 г); после прекращения через 10 минут шипения полученный раствор добавляют по каплям при перемешивании при температуре 20oC к раствору ангидрида пиррол-1-карбоновой кислоты /4,05 г/ и дициклогексилкарбодиимида /15 г/ в дихлорметане /105 мл/ (в соответствии с J.Org. Chem. 52, 2319 (1987)). Реакционную смесь оставляют для прохождения реакции при комнатной температуре в течение 2,5 часов, а затем фильтруют и выпаривают в вакууме досуха. Остаток чистят на флэш-хроматографии с использованием для элюции смеси толуол/этилацетат (10/1) с получением этилового эфира 3-этокси-1,1'-карбонилдипиррол-2-карбоновой кислоты, Т.пл. 58 - 60oC, (3,15 г), который растворяют в уксусной кислоте /75 мл/ и проводят далее реакцию с ацетатом палладия /II/ (1,3 г) в атмосфере инертного газа при температуре 80oC в течение 7 часов. После охлаждения реакционную смесь фильтруют и выпаривают досуха в вакууме. Остаток чистят на флэш-колонке с использованием для элюции смеси толуол/этилацетат (10:1), получая 0,87 г этилового эфира 4-этокси-1,1'-карбонил-2,2'-бипиррол-5-карбоновой кислоты, Tпл 100 - 103oC, и 1,32 г восстановленного исходного материала.
Полученный бипиррол растворяют в метаноле /63 мл/ и обрабатывают метоксидом лития /3,17 мл 1N раствора в метаноле/ при перемешивании в течение 40 минут при комнатной температуре. Реакционную смесь разбавляют ледяной водой, полученный осадок фильтруют и тщательно промывают водой до нейтральной реакции, при этом получают чистый этиловый эфир 4-этокси-2,2'-бипиррол-2-карбоновой кислоты, Tпл 189 - 191oC, /0,7 г/, который вводят в реакцию с гидратом гидразина /20 мл/ при перемешивании в течение 8 часов при температуре 60oC. После охлаждения реакционную смесь разбавляют ледяной водой, а полученный осадок фильтруют и тщательно промывают водой до нейтральной реакции с получением 4-этокси-2,2'-бипиррол-5-карбогидразина, Tпл 255 - 257oC, /0,63 г/, который далее вводят в реакцию с п-толуолсульфонилхлоридом /0,51 г/ в пиридине /18 мл/ при перемешивании в течение 1 часа при комнатной температуре. Реакционную смесь разбавляют ледяной водой и подкисляют с помощью 37% HCl до pH 4. Осадок фильтруют и промывают водой до нейтральной реакции с получением 4-этокси-2,2'-бипиррол-5-карбоксил-толуолсульфонилгидразида, Tпл 272-275oC, /0,97 г/, который растворяют в этиленгликоле /10 мл/ при температуре 150oC и затем обрабатывают при перемешивании при этой температуре в течение 3 минут безводным карбонатом натрия /0,92 г/. После охлаждения реакционную смесь разбавляют ледяной водой, а осадок экстрагируют этилацетатом, промывают водой до нейтральной реакции и выпаривают в вакууме досуха. Остаток чистят на флэш-колонке с применением для элюции смеси гексан/этилацетат /7: 3/ с получением 0,28 г 4-этокси-2,2'-бипиррол-5-карбоксальдегида. Tпл 218-220oC. Указанный выше альдегид /0,05 г/ вступает в реакцию с 2-ундецил-пирролом /0,065 г/ в метаноле /40 мл/ при перемешивании в присутствии 10 экв. газообразной HCl в эфире при комнатной температуре в течение 18 часов.
Реакционную смесь разбавляют водой /200 мл/ и экстрагируют дихлорметаном. Органический слой взбалтывают с 5% раствором гидроксида аммония, после чего выпаривают досуха. Осадок чистят на короткой колонке с основным AL2O3 с использованием для элюции этилацетат. Собранные фракции взбалтывают с 1N HCl, после чего выпаривают досуха в вакууме с получением осадка, который кристаллизуют при обработке пентаном, получая 0,036 г 4-этокси-5-[(5-ундецил-2H-пиррол-2-илиден)метил] -2,2'-бипиррол, гидрохлорида. Tпл 94 - 96oC. ЯМР (CDCl3) δ ppm : 0,85 (м) (3H, -(CH2)9-CH3), 1,1 - 1,9 (м) (21H, - (CH2)9 ± OCH2CH3), 2,95 (м) (2H, -CH2-(CH2)9-), 4,25 (к., J = 7,0 Гц) 2H, OCH2-CH3), 6,05 (д., J = 1,8 Гц) (1H, C-3 протон бипиррола), 6,21 (дд., J - 1,5 Гц, J = 4,0 Гц) (1H, C-4 протон пиррола), 6,37 (м) (1H, C-4' протон бипиррола), 6,86 (дд. , J = 4,0 Гц, J = 2,4 Гц) (1H, C-3 протон пиррола), 6,94 (м) (1H, C-3' протон бипиррола), 7,03 (с) (1H, -CH=), 7,25 (м) (1H, C-5' протон бипиррола), 12,6 - 13 (два шс.) (3H, - NH-).
При проведении аналогичных реакций могут быть получены следующие соединения:
4-этокси-5-{ [5-(ундец-10-ен-1-ил)-2H-пиррол-2-илиден] метил} -2,2'-би- 1H-пиррол, гидрохлорид. Tпл = 80 - 97oC;
4-этокси-5-[(5-децил-2H-пиррол-2-илиден)метил] -2,2'-би-1H-пиррол, гидрохлорид;
4-этокси-5-[(5-додецил-2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол, гидрохлорид;
4-этокси-5-[(5-фенэтенил-2H-пиррол-2-илиден)метил] -2,2'-би-1H-пиррол, гидрохлорид;
4-этокси-5-{ [5-(5-фенокси-пент-1-ил)-2H-пиррол-2-илиден] -метил} - -2,2'-би-1H-пиррол, гидрохлорид. Tпл 110 - 120oC;
4-этокси-5-[(5-тридецил-2H-пиррол-2-илиден)метил] - -2,2'-би-1H-пиррол, гидрохлорид. Tпл 88 - 93oC; и
4-этокси-5-[(5-метил-2H-пиррол-2-илиден)метил] - -2,2'-би-1H-пиррол, гидрохлорид. Tпл 200oC /разлож./.
Пример 2
При использовании методик примера 1, проводят конденсацию подходящих 4-алкокси-2,2'-би-1H-пиррол-5-карбоксальдегидов с подходящими замещенными пирролами, при этом могут быть получены следующие соединения:
4-амилокси-5-[(5-ундецил-2H-пиррол-2-илиден)метил] - 2,2'-би-1H-пиррол, гидрохлорид;
4-ундецилокси-5-[(5-ундецил-2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол, гидрохлорид;
4-ундецилокси-5-[(2H-пиррол-2-илиден)метил] - 2,2'-би-1H-пиррол, гидрохлорид;
4-бутокси-5-[(тридецил-2H-пиррол-2-илиден)метил] - 2,2'-би-1H-пиррол, гидрохлорид;
4-бензилокси-5-[(5-тридецил-2H-пиррол-2-илиден)метил] - 2,2'-би-1H-пиррол, гидрохлорид;
4-бутокси-5-[5-(5-фенокси-пент-1-ил)-2H-пиррол-2-илиден)метил] - 2,2'-би-1H-пиррол, гидрохлорид;
4-бензилокси-5-[[5-(фенокси-пент-1-ил)-2H-пиррол-2-илиден] метил] - 2,2'-би-1H-пиррол, гидрохлорид;
4-пропокси-5-[(5-ундецил-2H-пиррол-2-илиден)метил] -2,2'-би-1H-пиррол, гидрохлорид. Tпл 73 - 77oC;
4-бутокси-5-[(5-ундецил-2H-пиррол-2-илиден)метил] -2,2'-би-1H-пиррол, гидрохлорид. Tпл 81 - 83oC;
4-изопропокси-5-[(5-ундецил-2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол, гидрохлорид;
4-пропокси-5-[(5-децил-2H-пиррол-2-илиден)метил] -2,2'-би-1H-пиррол, гидрохлорид;
4-пропокси-5-[(5-додецил-2H-пиррол-2-илиден)метил] -2,2'-би-1H-пиррол, гидрохлорид;
4-пропокси-5-{ [5-(ундец-10-ен-1-ил)-2H-пиррол-2-илиден] метил} - 2,2'-би-1H-пиррол, гидрохлорид;
4-пропокси-5-{ [5-(5-фенокси-пент-1-ил)-2H-пиррол-2-илиден] метил} - 2,2'-би-1H-пиррол, гидрохлорид;
4-бензилокси-5-[(5-ундецил-2H-пиррол-2-илиден)метил] -2,2'-би-1H-пиррол, гидрохлорид. Tпл 90 - 93oC; и
4-бензилокси-5-[(2H-пиррол-2-илиден)метил] -2,2'-би-1H-пиррол, гидрохлорид. Tпл 200-202oC.
Пример 3
При использовании методик примера 1 проводят конденсацию 4-метокси-2,2'-би-1H-пиррол-5-карбоксальдегида с подходящими замещенными пирролами, при этом могут быть получены следующие соединения:
4-метокси-5-[[-(7-циано-гепт-1-ил)-2H-пиррол-2-илиден] метил]-2,2'- 1H-пиррол, гидрохлорид;
4-метокси-5-{ (5-ундец-10-ен-1-ил)-2H-пиррол-2-илиден] метил}-2,2'- би-1H-пиррол, гидрохлорид;
4-метокси-5-[(5-децил-2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол, гидрохлорид. Tпл 100 - 116oC;
4-метокси-5-[(5-додецил-2H-пиррол-2-илиден)метил] -2,2'-би-1H-пиррол, гидрохлорид;
4-метокси-5-[(5-тридецил-2H-пиррол-2-илиден)метил] -2,2'-би-1H-пиррол, гидрохлорид. Tпл 80 - 100oC;
4-метокси-5-[(5-пентадецил-2H-пиррол-2-илиден)метил] -2,2'-би-1H-пиррол, гидрохлорид. Tпл 100 - 104oC;
4-метокси-5-[(5-пропил-2H-пиррол-2-илиден)метил] -2,2'-би-1H-пиррол, гидрохлорид;
4-метокси-5-[(5-гептил-2H-пиррол-2-илиден)метил] -2,2'-би-1H-пиррол, гидрохлорид. Tпл 140 - 145oC;
4-метокси-5-[(5-фенэтил-2H-пиррол-2-илиден)метил] -2,2'-би-1H-пиррол, гидрохлорид. Tпл 170oC /разлож./;
4-метокси-5-[(5-метил-4-ундецил-2H-пиррол-2-илиден)метил] -2,2'- би-1H-пиррол, гидрохлорид;
4-метокси-5-[(5-пропил-4-ундецил-2Н-пиррол-2-илиден)-метил] -2,2'-би-1Н-пиррол, гидрохлорид;
4-метокси-5-{ [5-(5-фенокси-пент-1-ил)-2H-пиррол-2-илиден]метил}- 2,2'-би-1H-пиррол, гидрохлорид; Tпл 126 - 129oC;
4-метокси-5-[(4-этил-4,5-диметил-2H-пиррол-2-илиден)метил] -2,2'- би-1H-пиррол, гидрохлорид;
4-метокси-5-[(4-гексил-5-метил-2H-пиррол-2-илиден)метил] -2,2'- би-1H-пиррол, гидрохлорид;
4-метокси-5-[(5-нонил-2H-пиррол-2-илиден)метил] -2,2'-би-1H-пиррол, гидрохлорид;
4-метокси-5-[(5-метил-4-пентил-2H-пиррол-2-илиден)метил] -2,2'- би-1H-пиррол, гидрохлорид;
4-метокси-5-{ [5-(5-карбокси-пент-1-ил)-2H-пиррол-2-илиден] метил}-2,2'- би-1H-пиррол, гидрохлорид. Tпл 157 - 165oC;
Метиловый эфир 4-метокси-5-{[5-(5-карбокси-пент-1-ил)-2H-пиррол- 2-илиден]метил}-2,2'-би-1H-пиррола, гидрохлорид. Tпл 138 - 140oC;
4-метокси-5-{ [5-(6-гидрокси-гекс-1-ил)-2H-пиррол-2-илиден] метил}-2,2'- би-1H-пиррол, гидрохлорид. Tпл 118 - 121oC;
4-метокси-5-{ [5-(6-фтор-гекс-1-ил)-2H-пиррол-2-илиден]метил}-2,2'- би-1H-пиррол, гидрохлорид. Tпл 115 - 124oC; и
4-метокси-5-{[5-(5-морфолинокарбоксамидо-пент-1-ил)-2H-пиррол-2- илиден] метил}-2,2'-би-1H-пиррол, гидрохлорид.
Пример 4
Применяя методики, описанные в примерах 1 и 2, с использованием соответствующих замещенных пирролов, можно получить следующие соединения:
4-этокси-5-[(5-этил-4-пентил-2H-пиррол-2-илиден)метил] -2,2'- би-1H-пиррол, гидрохлорид;
4-этокси-5-[(5-метил-4-пентил-2H-пиррол-2-илиден)метил] -2,2'- би-1H-пиррол, гидрохлорид;
4-этокси-5-[(5-этил-4-ундецил-2H-пиррол-2-илиден)метил] -2,2'- би-1H-пиррол, гидрохлорид;
4-этокси-5-[(5-метил-4-ундецил-2H-пиррол-2-илиден)метил] -2,2'- би-1H-пиррол, гидрохлорид;
4-этокси-5-[(5-гептил-4-ундецил-2H-пиррол-2-илиден)метил] -2,2'- би-1H-пиррол, гидрохлорид;
4-пропокси-5-[(5-этил-4-ундецил-2H-пиррол-2-илиден)метил] -2,2'- би-1H-пиррол, гидрохлорид;
4-этокси-5-[(4-этил-3,5-диметил-2H-пиррол-2-илиден)метил] -2,2'- би-1H-пиррол, гидрохлорид;
4-этокси-{ [5-(5-карбокси-пент-1-ил)-2H-пиррол-2-илиден] метил} -2,2'- би-1H-пиррол;
4-пропокси-5-{ [5-(5-карбокси-пент-1-ил)-2H-пиррол-2-илиден]метил}-2,2'- би-1H-пиррол;
4-этокси-5-{ [5-(6-гидрокси-гекс-1-ил)-2H-пиррол-2-илиден] метил} -2,2'- би-1H-пиррол;
4-пропокси-5-{ [5-(6-гидрокси-гекс-1-ил)-2H-пиррол-2-илиден]метил}-2,2'- би-1H-пиррол;
4-пропокси-5-{ [5-(11-карбокси-ундец-1-ил)-2H-пиррол-2-илиден] метил} - 2,2'-би-1H-пиррол;
4-пропокси-5-{ [5-(12-карбокси-додец-1-ил)-2H-пиррол-2-илиден] метил} - 2,2'-би-1H-пиррол;
4-пропокси-5-{ [5-(12-гидрокси-додец-1-ил)-2H-пиррол-2-илиден] метил} - 2,2'-би-1H-пиррол, гидрохлорид;
4-пропокси-5-{ [5-(13-гидрокси-тридец-1-ил)-2H-пиррол-2-илиден] метил} - 2,2'-би-1H-пиррол, гидрохлорид;
4-пропокси-5-{ [5-(11-циано-ундец-1-ил)-2H-пиррол-2-илиден] метил} - 2,2'-би-1H-пиррол, гидрохлорид;
4-пропокси-5-{ [5-(11-карбамоил-ундец-1-ил)-2H-пиррол-2-илиден] метил} - 2,2'-би-1H-пиррол, гидрохлорид;
4-пропокси-5-{ [5-(11-этоксикарбонил-ундец-1-ил)-2H-пиррол-2- илиден] метил}-2,2'-би-1H-пиррол, гидрохлорид;
4-этокси-5-[(5-ундеканоил-2H-пиррол-2-илиден)метил] -2,2'-би-1H-пиррол, гидрохлорид;
4-этокси-5-{ [5-(11-карбокси-ундец-1-ил)-2H-пиррол-2-илиден] метил} - 2,2'-би-1H-пиррол;
4-этокси-5-{ [5-(12-карбокси-додец-1-ил)-2H-пиррол-2-илиден] метил} - 2,2'-би-1H-пиррол;
4-этокси-5-{ [5-(12-гидрокси-додец-1-ил)-2H-пиррол-2-илиден] метил} - 2,2'-би-1H-пиррол, гидрохлорид;
4-этокси-5-{ [5-(13-гидрокси-тридец-1-ил)-2H-пиррол-2-илиден] метил} - 2,2'-би-1H-пиррол, гидрохлорид;
4-этокси-5-{ [5-(11-циано-ундец-1-ил)-2H-пиррол-2-илиден] метил}- 2,2'-би-1H-пиррол, гидрохлорид;
4-этокси-5-{ [5-(11-карбамоил-ундец-1-ил)-2H-пиррол-2-илиден] метил} - 2,2'-би-1H-пиррол, гидрохлорид; и
4-этокси-5-{[5-(11-этоксикарбонил-ундец-1-ил)-2H-пиррол-2-илиден]метил}- 2,2'-би-1H-пиррол, гидрохлорид.
Пример 5
Применяя методики, описанные в примерах 1 - 3 с использованием для конденсации подходящих 4-алкокси-2,2'-би-1H-пиррол-карбоксальдегида и пирролов, имеющих нужные циклические заместители, можно получить следующие соединения:
4-метокси-5-[(4,5,6,7-тетрагидро-2H-индол-2-илиден)- метил-2,2'-би-1H-пиррол, гидрохлорид. Tпл 212oC /разлож./;
4-метокси-5-[(4-гексил-4,5,6,7-тетрагидро-2H-индол-2-илиден) метил] -2,2'-би-1H-пиррол, гидрохлорид. Tпл 181 - 184oC;
4-этокси-5-[(4-гексил-4,5,6,7-тетрагидро-2H-индол-2-илиден) метил] -2,2'-би-1H-пиррол, гидрохлорид;
4-пропокси-5-[(4-гексил-4,5,6,7-тетрагидро-2H-индол-2-илиден) метил] -2,2'-би-1H-пиррол, гидрохлорид;
4-этокси-5-{ [4-(4-(карбокси-бут-1-ил)-4,5,6,7-тетрагидро-2H-индол- 2-илиден]метил}-2,2'-би-1H-пиррол;
4-этокси-5-[(3,5-нонаметилен-2H-пиррол-2-илиден)метил] -2,2'-би- 1H-пиррол, гидрохлорид;
4-пропокси-5-[(3,5-нонаметилен-2H-пиррол-2-илиден)метил] -2,2'-би- 1H-пиррол, гидрохлорид; и
4-этокси-5-{ [4-(4-этоксикарбонил-бут-1-ил)-4,5,6,7-тетрагидро-2H- индол-2-илиден]метил}-2,2'-би-1H-пиррол, гидрохлорид.
Пример 6
При использовании методик, описанных в примерах 1 - 5, проводя реакцию конденсации подходящего 5'-замещенного-4-алкокси- 2,2'-би-1H-пиррол-карбоксальдегида, полученного на основе соответствующей 5-замещенной пиррол-1-карбоновой кислоты, с подходящими замещенными пирролами, можно получить следующие соединения:
4-этокси-5'-метил-[(5-метил-2H-пиррол-2-илиден)метил] -2,2'-би-1H- пиррол, гидрохлорид. Tпл 180oC /разлож./;
4-пропокси-5'-метил-[(5-ундецил-2H-пиррол-2-илиден)метил] -2,2'-би-1H- пиррол, гидрохлорид;
4-этокси-5'-метил-5-{ [5-ундец-10-ен-1-ил)-2H-пиррол-2-илиден] метил}-2,2'-би-1H-пиррол, гидрохлорид;
4-этокси-5'-метил-5-[(5-децил-2H-пиррол-2-илиден) метил]-2,2'-би-1H-пиррол, гидрохлорид;
4-этокси-5'-метил-5-[(5-додецил-2H-пиррол-2-илиден) метил]-2,2'-би-1H-пиррол, гидрохлорид;
4-этокси-5'-метил-5-[(3,5-нонаметилен-2H-пиррол-2-илиден) метил]-2,2'-би-1H-пиррол, гидрохлорид;
4-этокси-5'-гептил-5-[(5-ундецил-2H-пиррол-2-илиден) метил] -2,2'-би-1H-пиррол, гидрохлорид; и
4-этокси-5'-метил-5-[(5-ундецил-2H-пиррол-2-илиден) метил]-2,2'-би-1H-пиррол, гидрохлорид.
Пример 7
При использовании методик, описанных в примерах 1 - 6, проводя реакцию конденсации подходящего 3-циано-4-алкокси- 2,2'-би-1H-пиррол-карбоксальдегида, полученного на основе соответствующего алкильного эфира 4-циано-3-гидрокси-пиррол-2- карбоновой кислоты, с подходящими замещенными пирролами, можно получить следующие соединения:
3-циано-4-пропокси-5-[(5-ундецил-2H-пиррол-2-илиден)метил] - 2,2'-би-1H-пиррол, гидрохлорид;
3-циано-4-этокси-5-[(5-ундецил-2H-пиррол-2-илиден)метил] - 2,2'-би-1H-пиррол, гидрохлорид;
3-циано-4-этокси-5-{ [5-(ундец-10-ен-1-ил)-2H-пиррол-2-илиден] метил}-2,2'-би-1H-пиррол, гидрохлорид; и
3-циано-4-этокси-5'-метил-5-[(5-(ундецил-2H-пиррол-2-илиден) метил] -2,2'-би-1H-пиррол, гидрохлорид.
Пример 8
В ходе реакции, в соответствии с методикой примера 1, подходящих замещенных 2-формил-пирролов с подходящими 5'-замещенными 3-алкоксикарбонил-4-алкокси-2,2'-би-1H-пирролами, приготовленными посредством конденсации подходящих 3-алкоксикарбонил-4-алкокси-3-пирролин-2-онов формулы /VIII/ с подходящими 2-замещенными пирролами формулы /IX/ можно получить следующие соединения:
3-этоксикарбонил-4-пропокси-5'-метил-5-[(5-(ундецил-2H-пиррол- 2-илиден)метил]-2,2'-би-1H-пиррол, гидрохлорид;
3-этоксикарбонил-4-этокси-5'-метил-5-[(5-(ундецил-2H-пиррол- 2-илиден)метил]-2,2'-би-1H-пиррол, гидрохлорид;
3-этоксикарбонил-4-этокси-5'-метил-5-{ [5-(ундец-10-ен-1-ил)- 2H-пиррол-2-илиден]метил}-2,2'-би-1H-пиррол, гидрохлорид;
3-метоксикарбонил-4-метокси-5'-метил-5-[(5-ундецил- 2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол, гидрохлорид;
3-этоксикарбонил-4-этокси-5'-метил-5-[(3:5-нонаметилен- 2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол, гидрохлорид;
3-этоксикарбонил-4-этокси-5'-пропил-5-[(5-ундецил- 2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол, гидрохлорид; и
3-этоксикарбонил-4-пропокси-5'-метил-5-{ [5-ундец-10-ен-1-ил)- 2H-пиррол-2-илиден)метил]-2,2'-би-1H-пиррол, гидрохлорид.
Пример 9
При использовании методики, описанной в примере 8, проводя реакцию конденсации подходящих замещенных 2-формил-пирролов с подходящими 5'-замещенными 3-карбокси-4-алкокси-2,2'-би-1H-пирролами, можно получить следующие соединения:
3-карбокси-4-пропокси-5'-метил-5-[(5-ундецил-2H-пиррол-2- илиден)метил] -2,2'-би-1H-пиррол;
3-карбокси-4-этокси-5'-метил-5-[(5-ундецил-2H-пиррол-2- илиден)метил]-2,2'-би-1H-пиррол;
3-карбокси-4-этокси-5'-метил-5-{ [5-ундец-10-ен-1-ил)- 2H-пиррол-2-илиден]метил}-2,2'-би-1H-пиррол; и
3-карбокси-4-этокси-5'-пропил-5-[(5-ундецил-2H-пиррол-2- илиден)метил] -2,2'-би-1H-пиррол.
Пример 10
Форма препарата: капсулы /150 мг/.
Капсулы, каждая весом по 400 мг, содержащая по 150 мг активного вещества, приготавливаются следующим образом:
Состав:
4-этокси-5-[(5-ундецил-2H-пиррол-2-илиден)метил] -2,2'-би-1H-пиррол, гидрохлорид - 150 мг
Лактоза - 198 мг
Кукурузный крахмал - 50 мг
Стеарат магния - 2 мг
Итого - 400 мг
Вводят полученную массу в двойные твердые желатиновые капсулы (табл. 2).
Соединение: 4-метокси-5-[[5-(7-циано-гепт-1-ил)-2H-пиррол-2- илиден]метил]-2,2'-би-1H-пиррола гидрохлорид.
ЯМР (CDCl3) δ ч./млн.: 1,3 - 1,8 (м, 10H); 2,3 (м, 2H); 3 (м, 2H); 4,04 (c, 3H); 6,1 (g, 1H); 6,2 (gg, 1H); 6,4 (м, 1H); 6,8 (м, 1H); 6,9 (м, 1H); 7,0 (c, 1H); 7,25 (м, 1H); 12,6 - 12,7 (два шир.c, 2H); 12,9 (шир.c, 1H):
Соединение: 4-метокси-5-{ [5-(5-морфолин-карбоксамидо-пент-1- ил)-2H-пиррол-2-илиден]метил]-2,2'-би-1H-пиррола гидрохлорид
ЯМР (CDCl3) δ ч./млн.: 1,2 - 1,8 (м, 6H); 2,2 (м, 2H); 2,8 (м, 2H); 3,4 - 3,5 (м, 8H); 4 (c, 3H); 6,2 (м, 2H); 6,8 (м, 1H); 7,1 (c, 1H); 7,4 - 7,6 (м, 3H); 12,2 - 12,4 (шир.c, 1H); 12,5 - 12,8 (два шир.c, 2H).
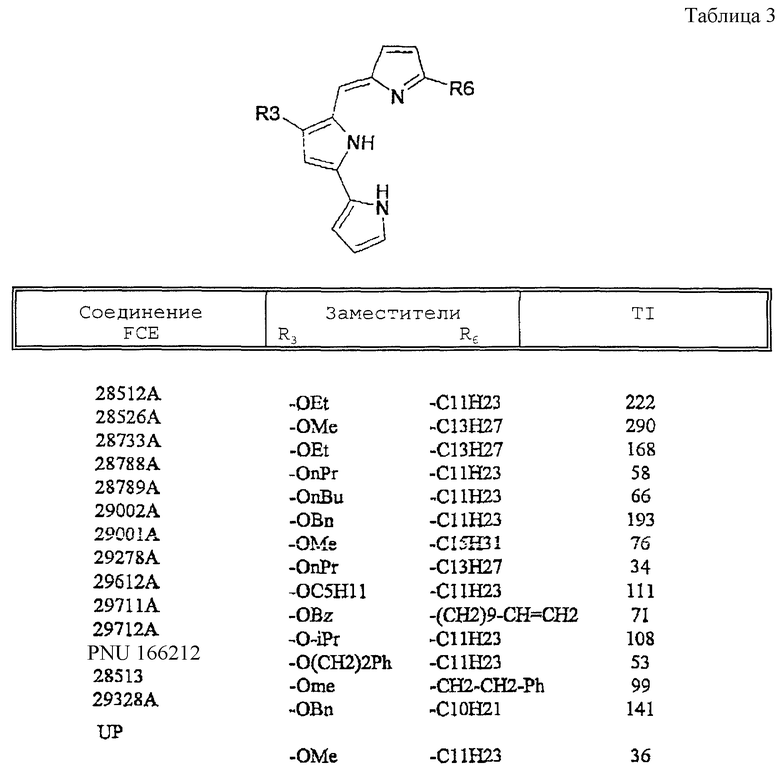
Дополнительные данные по биологической активности соединений (табл. 3)
Химические названия соединений, обозначенных FCE 28512, FCE 28526, FCE 28733, FCE 28788 и FCE 29002, даны выше.
Соединение FCE 28788A: 4-пропокси-5-[(5-ундецил-2H-пиррол- 2-илиден)метил]-2,2'-би-1H-пиррол.
Соединение FCE 29001A: 4-метокси-5-[(5-пентадецил-2H-пиррол- 2-илиден)метил]-2,2'-би-1H-пиррол.
Соединение FCE 29278A: 4-пропокси-5-[(5-тридецил-2H-пиррол- 2-илиден)метил]-2,2'-би-1H-пиррол.
Соединение FCE 29328A: 4-бутокси-5-[(5-децил-2H-пиррол- 2-илиден)метил] -2,2'-би-1H-пиррол.
Соединение FCE 29612A: 4-амилокси-5-[(5-ундецил-2H-пиррол- 2-илиден)метил]-2,2'-би-1H-пиррол.
Соединение FCE 29711A: 4-бутокси-5-[(5-ундец-10-ен-1-ил-2H-пиррол- 2-илиден)метил]-2,2'-би-1H-пиррол.
Соединение FCE 29712A: 4-изопропокси-5-[(5-ундецил-2H-пиррол- 2-илиден)метил]-2,2'-би-1H-пиррол.
Соединение PNU 166212: 4-фенилэтокси-5-[(5-ундецил-2H-пиррол- 2-илиден)метил]-2,2'-би-1H-пиррол.
Соединение FCE 28513A: 4-метокси-5-[(5-фенэтил-2H-пиррол- 2-илиден)метил]-2,2'-би-1H-пиррол.


Предложены производные 5[(2Н-пиррол-2-илиден)метил]-2,2'-би-1Н-пиррола общей формулы I, где R обозначает Н или C1-C6-алкил; R2, R4, R5 обозначают водород; R3 обозначает C1-C6-алкоксигруппу, незамещенную или замещенную фенилом; R6 обозначает водород, C3-C14-алкенил или C1-C20-алкил, незамещенный или замещенный галогеном, гидрокси, фенилом, фенилокси, карбокси, циано или -СО-морфолиногруппой; или R5 и R6 вместе образуют C4-C9 полиметиленовую цепь, которая может быть замещена C1-C6- алкилом, их фармацевтически приемлемые соли, которые обладают иммуномоделирующей активностью. Предложены также способ получения соединения формулы I взаимодействием соединения формулы II с соединением формулы III, фармацевтическая композиция, обладающая иммуномоделирующей активностью. 5 с. и 7 з.п., 3 табл.
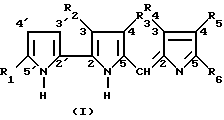


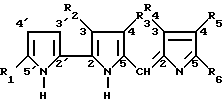
в которой R1 обозначает водород или C1 - C6-алкил;
R2 обозначает водород;
R3 обозначает C1 - C6-алкоксигруппу, незамещенную или замещенную фенилом;
R4 обозначает водород;
R5 обозначает водород;
R6 обозначает водород, C1 - C20 алкил или C3 - C14 алкенил, при этом алкильная группа может быть замещена заместителем, независимо выбранным из галогена, гидрокси, фенила, фенилокси, карбокси, циано и -CO-морфолино;
или R5 и R6 вместе образуют C4 - C9-полиметиленовую цепь, которая может быть не замещена или замещена C1 - C12 алкилом, тогда как оставшиеся группы являются водородом или C1 - C6 алкилом, а также их фармацевтически приемлемые соли,
и в которой в случае, если R3 представляет собой метокси, а R1, R2, R4 и R5 являются водородами, то R6 отличен от водорода, н-нонила или н-ундецила, и если R3 представляет метокси и R1, R2 и R4 представляют водород, то R5 и R6, взятые вместе, отличны от альфа-бутилгептаметиленовой цепи.
4-этокси-5-[(5-ундецил-2Н-пиррол-2-илиден)метил]-2,2'-би-1Н-пиррол;
4-пропокси-5-[(5-ундецил-2Н-пиррол-2-илиден)метил]-2,2'-би-1Н-пиррол;
4-этокси-5-{ [(5-ундец-10-ен-1-ил)-2Н-пиррол-2-илиден] метил} -2,2'-би-1Н-пиррол;
4-амилокси-5-[(5-ундецил-2Н-пиррол-2-илиден)метил]-2,2'-би-1Н-пиррол;
4-ундецилокси-5-[(5-ундецил-2Н-пиррол-2-илиден)метил]-2,2'-би-1Н-пиррол;
4-бензилокси-5-[(5-ундецил-2Н-пиррол-2-илиден)метил]-2,2'-би-1Н-пиррол;
4-бензилокси-5-[(2Н-пиррол-2-илиден)метил]-2,2'-би-1Н-пиррол;
4-ундецилокси-5-[(2Н-пиррол-2-илиден)метил]-2,2'-би-1Н-пиррол;
4-метокси-5-[(5-тридецил-2Н-пиррол-2-илиден)метил]-2,2'-би-1Н-пиррол;
4-этокси-5-[(5-тридецил-2Н-пиррол-2-илиден)метил]-2,2'-би-1Н-пиррол;
4-бутокси-5-[(5-тридецил-2Н-пиррол-2-илиден)метил]-2,2'-би-1Н-пиррол;
4-бензилокси-5-[(5-тридецил-2Н-пиррол-2-илиден)метил]-2,2'-би-1Н-пиррол;
4-метокси-5-[[(5-фенокси-пент-1-ил)-2Н-пиррол-2-илиден] метил]-2,2'-би-1Н-пиррол;
4-этокси-5-[[5-(5-фенокси-пент-1-ил)-2Н-пиррол-2-илиден] метил] -2,2'-би-1Н-пиррол;
4-метокси-5-[[(5-(6-фтор-гекс-1-ил)-2Н-пиррол-2-илиден] метил]-2,2'-би-1Н-пиррол;
4-метокси-5-[[5-(6-гидрокси-гекс-1-ил)-2Н-пиррол-2-илиден] метил]-2,2'-би-1Н-пиррол;
4-метокси-5-[[5-(5-морфолинокарбоксамидо-пент-1-ил)-2Н-пиррол-2-илиден] метил]-2,2'-би-1Н-пиррол, и их фармацевтически приемлемые соли.
в которой R1, R2 и R3 определены в п.1, с соединением формулы III
в которой R4, R5 и R6 определены в п.1,
с получением соединения формулы I, определенного в п.1, в котором R1 отличен от водорода, и, если нужно, превращения соединения формулы I в другое соединение формулы I, и/или, при необходимости, превращения соединения формулы I в его фармацевтически приемлемую соль, и/или, при необходимости, превращения соли в свободное соединение, и/или, при необходимости, разделения смеси изомеров соединения формулы I и получения индивидуального изомера.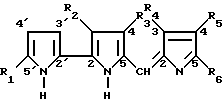
в которой R1 обозначает водород или C1 - C6-алкил;
R2 обозначает водород;
R3 обозначает C1 - C6-алкоксигруппу, незамещенную или замещенную фенилом;
R4 обозначает водород;
R5 обозначает водород;
R6 обозначает водород, C1 - C20 алкил или C3 - C14 алкенил, при этом алкильная группа может быть замещена заместителем, независимо выбранным из галогена, гидрокси, фенила, фенилокси, карбокси, циано и -CO-морфолино;
или R5 и R6 вместе образуют C4 - C9-полиметиленовую цепь, которая может быть не замещена или замещена C1 - C12 алкилом, тогда как оставшиеся группы являются водородом или C1 - C6 алкилом, а также их фармацевтически приемлемые соли,
и в которой в случае, если R3 представляет собой метокси, а R1, R2, R4 и R5 являются водородами, то R6 отличен от водорода, н-нонила или н-ундецила; и если R3 представляет метокси и R1, R2 и R4 представляют водород, то R5 и R6 взятые вместе, отличны от альфа-бутилгептаметиленовой цепи, обладающие иммуномоделирующей активностью.
4-этокси-5-[(5-ундецил-2Н-пиррол-2-илиден)метил]-2,2'-би-1Н-пиррол;
4-пропокси-5-[(5-ундецил-2Н-пиррол-2-илиден)метил]-2,2'-би-1Н-пиррол;
4-этокси-5-{ [(5-ундец-10-ен-1-ил)-2Н-пиррол-2-илиден] метил} -2,2'-би-1Н-пиррол;
4-амилокси-5-[(5-ундецил-2Н-пиррол-2-илиден)метил]-2,2'-би-1Н-пиррол;
4-ундецилокси-5-[(5-ундецил-2Н-пиррол-2-илиден)метил]-2,2'-би-1Н-пиррол;
4-бензилокси-5-[(5-ундецил-2Н-пиррол-2-илиден)метил]-2,2'-би-1Н-пиррол;
4-бензилокси-5-[(2Н-пиррол-2-илиден)метил]-2,2'-би-1Н-пиррол;
4-ундецилокси-5-[(2Н-пиррол-2-илиден)метил]-2,2'-би-1Н-пиррол;
4-метилокси-5-[(5-тридецил-2Н-пиррол-2-илиден)метил]-2,2'-би-1Н-пиррол;
4-этокси-5-[(5-тридецил-2Н-пиррол-2-илиден)метил]-2,2'-би-1Н-пиррол;
4-бутокси-5-[(5-тридецил-2Н-пиррол-2-илиден)метил]-2,2'-би-1Н-пиррол;
4-бензилокси-5-[(5-тридецил-2Н-пиррол-2-илиден)метил]-2,2'-би-1Н-пиррол;
4-метокси-5-[[5-(5-фенокси-пент-1-ил)-2Н-пиррол-2-илиден] -метил]-2,2'-би-1Н-пиррол;
4-этокси-5-[[5-(5-фенокси-пент-1-ил)-2Н-пиррол-2-илиден] метил] -2,2'-би-1Н-пиррол;
4-метокси-5-[[(5-(6-фтор-гекс-1-ил)-2Н-пиррол-2-илиден] метил]-2,2'-би-1Н-пиррол;
4-метокси-5-[[5-(6-гидрокси-гекс-1-ил)-2Н-пиррол-2-илиден] метил]-2,2'-би-1Н-пиррол;
4-метокси-5-[[5-(5-морфолинокарбоксамидо-пент-1-ил)-2Н-пиррол-2-илиден] метил]-2,2'-би-1Н-пиррол и их фармацевтически приемлемые соли.
в которой R1 обозначает водород или C1 - C6-алкил; R2 обозначает водород; R3 обозначает C1 - C6-алкоксигруппу, незамещенную или замещенную фенилом; R4 обозначает водород; R5 обозначает водород; R6 обозначает водород; C1 - C20 алкил или C3 - C14 алкенил, при этом алкильная группа может быть замещена заместителем, независимо выбранным из галогена, гидрокси, фенила, фенилокси, карбокси, циано и -CO-морфолино;
или R5 и R6 вместе образуют C4 - C9-полиметиленовую цепь, которая может быть не замещена или замещена C1 - C12 алкилом, тогда как оставшиеся группы являются водородом или C1 - C6 алкилом, а также их фармацевтически приемлемые соли,
и в которой в случае, если R3 представляет собой метокси, а R1, R2, R4 и R5 являются водородами, то R6 отличен от водорода, н-нонила или н-ундецила, и если R3 представляет метокси и R1, R2 и R4, представляют водород, то R5 и R6, взятые вместе, отличны от альфа-бутилгептаметиленовой цепи, пригодные для приготовления фармацевтической композиции, обладающей иммуномодулирующей активностью.
4-этокси-5-[(5-ундецил-2Н-пиррол-2-илиден)метил]-2,2'-би-1Н-пиррол;
4-пропокси-5-[(5-ундецил-2Н-пиррол-2-илиден)метил]-2,2'-би-1Н-пиррол;
4-этокси-5-[[(5-ундец-10-ен-1-ил)-2Н-пиррол-2-илиден] метил] -2,2'-би-1Н-пиррол;
4-амилокси-5-[(5-ундецил-2Н-пиррол-2-илиден)метил]-2,2'-би-1Н-пиррол;
4-ундецилокси-5-[(5-ундецил-2Н-пиррол-2-илиден)метил]-2,2'-би-1Н-пиррол;
4-бензилокси-5-[(5-ундецил-2Н-пиррол-2-илиден)метил]-2,2'-би-1Н-пиррол;
4-бензилокси-5-[(2Н-пиррол-2-илиден)метил]-2,2'-би-1Н-пиррол;
4-ундецилокси-5-[(2Н-пиррол-2-илиден)метил]-2,2'-би-1Н-пиррол;
4-метокси-5-[(5-тридецил-2Н-пиррол-2-илиден)метил]-2,2'-би-1Н-пиррол;
4-этокси-5-[(5-тридецил-2Н-пиррол-2-илиден)метил]-2,2'-би-1Н-пиррол;
4-бутокси-5-[(5-тридецил-2Н-пиррол-2-илиден)метил]-2,2'-би-1Н-пиррол;
4-бензилокси-5-[(5-тридецил-2Н-пиррол-2-илиден)метил]-2,2'-би-1Н-пиррол;
4-метокси-5-[[5-(5-фенокси-пент-1-ил)-2Н-пиррол-2-илиден] метил] -2,2'-би-1Н-пиррол;
4-этокси-5-[[5-(5-фенокси-пент-1-ил)-2Н-пиррол-2-илиден] метил] -2,2'-би-1Н-пиррол;
4-метокси-5-[[(5-(6-фтор-гекс-1-ил)-2Н-пиррол-2-илиден] метил]-2,2'-би-1Н-пиррол;
4-метокси-5-[[5-(6-гидрокси-гекс-1-ил)-2Н-пиррол-2-илиден] метил]-2,2'-би-1Н-пиррол;
4-метокси-5-[[5-(5-морфолинокарбоксамидо-пент-1-ил)-2Н-пиррол-2-илиден] метил]-2,2'-би-1Н-пиррол;
4-метокси-5-[(5-нонил-2Н-пиррол-2-илиден] метил] -2,2'-би-1Н-пиррол, или их фармацевтически приемлемые соли.
| Patent Abstracts of Japan, v | |||
| Походная разборная печь для варки пищи и печения хлеба | 1920 |
|
SU11A1 |
| Винтовой безударный прибор для разгонки зазоров железнодорожных рельсов | 1925 |
|
SU2586A1 |
| Annalls of the New York Academy of Science, vol | |||
| Катодный усилитель с питанием усилительной лампы переменным током | 1923 |
|
SU685A1 |
| Ручной ткацкий станок | 1922 |
|
SU339A1 |
| Transplantation, A.Makomura et al., "Suppresion of Cytotoxic T-Cell Jnduction invivo by prodigiosin, 25-C1", vol | |||
| Способ очищения сернокислого глинозема от железа | 1920 |
|
SU47A1 |
| МЕТАЛЛИЧЕСКИЙ КАЛОРИФЕР | 1923 |
|
SU1013A1 |
| J | |||
| of the Chemical Sosiety Perkin Transactions, Brown David et al., "Synthesis of N-Substituted prodigiosenes, v | |||
| Походная разборная печь для варки пищи и печения хлеба | 1920 |
|
SU11A1 |
| Снеговая лыжа для самолетов | 1913 |
|
SU455A1 |
| J | |||
| of Org.Chem., Hearn Walter et al., "Prodigiosene [5-(2-pirryl)-2,2'-dipyrrylmethene] and some substituted prodigiosenes", vol | |||
| Скоропечатный станок для печатания со стеклянных пластинок | 1922 |
|
SU35A1 |
| Рогульчатое веретено | 1922 |
|
SU142A1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ИНТЕРФЕРОНИНДУЦИРУЮЩЕЙ И ИММУНОМОДУЛИРУЮЩЕЙ (ИММУНОСТИМУЛИРУЮЩЕЙ) АКТИВНОСТЬЮ | 1987 |
|
RU2033157C1 |
| Машковский М.Д | |||
| Лекарственные средства | |||
| - М.: Медицина, 1985, ч | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Универсальный двойной гаечный ключ | 1920 |
|
SU169A1 |
Авторы
Даты
2000-02-27—Публикация
1994-12-02—Подача