Изобретение относится к содержащим серу производным арила, обладающим антибактериальной и антивирусной активностью, в частности к арилтиосоединениям нижепредставленной формулы (I), их фармацевтически приемлемым солям и сольватам, фармацевтической композиции, обладающей антибактериальной и антивирусной активностью, и способу лечения бактериальных или вирусных инфекций.
Известны содержащие серу производные арила, обладающие биологической активностью в частности антибактериальной и антивирусной активностью (см. заявку W092/06683, C 07 C 317/14, F 61 К 31/10, 30.04.1992 г.).
Задачей изобретения является расширение ассортимента арилтиосоединений, обладающих антибактериальной и антивирусной активностью.
Поставленная задача решается предлагаемыми арилтиосоединениями общей формулы (I)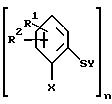
где R1 и R2 независимы друг от друга и означают водород, галоген, алкил с 1-6 атомами углерода, алкокси с 1-6 атомами углерода, циклоалкил с 3-6 атомами углерода, гидроксил, циано, фенил(CR5R6)m, группы Het(CR5R6)m, NR3R4, NR3COR4, CO2R3, CONR3R4, S(O)mR3, S(O)mNR3R4, COR3 или вместе означают оксогруппу или метилендиокси, где R3 и R4 независимы друг от друга и означают водород, алкил с 1-6 атомами углерода, циклоалкил с 3-6 атомами углерода, фенил (CR5R6)m, где R5 и R6 независимы друг от друга и означают водород, алкил с 1-6 атомами углерода, гидроксил, карбоксил, аминогруппу, группу CONH2 или цианогруппу, Het - циклическое или бициклическое кольцо с 4-10 атомами, 1-4 из которых означают кислород, серу или азот, m - 0, 1 или 2; X - группы 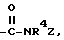
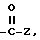
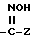 или SO2NR4Z,
или SO2NR4Z,
где Z - галоген, замещенный алкил с 1-6 атомами углерода, группы CO-алкил с 1-6 атомами углерода в алкильной части, циклоалкил-(CR5CR6) с 3-6 атомами углерода в циклоалкильной части, фенил(CR5CR6)m, где R5, R6 и m имеют вышеуказанное значение, a R4 имеет вышеуказанное значение,
Y - водород или группа SZ, если n = 1, или простая связь, если n = 2, причем Z имеет вышеуказанное значение,
n - 1 или 2,
причем указанные остатки алкила, циклоалкила, фенила и Het могут быть замещены 1-3 остатками из группы, включающей галоген, алкил с 1-6 атомами углерода, алкокси с 1-6 атомами углерода, трифторметил, гидроксил, циано, нитро, NR3R4, NR3COR4, CO2R3,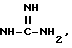 CONR3R4, S(O)mR3, PO4(R3)3, S(O)mNR3R4, COR3, где R3, R4 и m
CONR3R4, S(O)mR3, PO4(R3)3, S(O)mNR3R4, COR3, где R3, R4 и m
имеют вышеуказанное значение,
и их фармацевтически приемлемыми солями и сольватами.
В первую группу предпочтительных арилтиосоединений формулы (I) входят соединения, у которых Х означает группу формулы 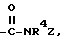 где R4 имеет вышеуказанное значение, Z означает вышеуказанное значение, в частности фенил (CR5R6)m, где m означает 0, Y означает группу - SZ, где Z имеет вышеуказанное значение или связь и означает 1, 2.
где R4 имеет вышеуказанное значение, Z означает вышеуказанное значение, в частности фенил (CR5R6)m, где m означает 0, Y означает группу - SZ, где Z имеет вышеуказанное значение или связь и означает 1, 2.
Представителями первой группы предпочтительных арилтиосоединений формулы (I) являются соединения, выбранные из группы, включающей 2,2'-дитиобис[N-[4-(1,1 - диметилэтил)фенил] бензамид] , 2,2'-дитиобис[N- (3-метилфенил) бензамид] , 2,2'-дитиобис[N- (3-бромфенил)бензамид], 2,2'- дитиобис[N-[3,5 -бис(трифторметил) фенил]-бензамид], 2,2'- дитиобис[N-[4- хлор-3-(трифторметил) фенил] бензамид], 2,2'- дитиобис[N- (3,4-дихлорфенил) бензамид] , 2,2'-дитиобис[N-(2,4- дихлорфенил)бензамид] , 2,2'-дитиобис[N-[3-(трифторметил) фенил] бензамид], 2,2'-дитиобис[N-(2-метоксифенил) бензамид], 2,2'- дитиобис[N-[4-(трифторметил) фенил] бензамид] , 2,2'-дитиобис[N-(4- цианофенил)бензамид] , 2,2'-дитиобис[N-[4- (метилсульфонил)фенил] бензамид], 2,2'-дитиобис[N-(4-йодфенил) бензамид] , 2,2'-дитиобис[N-(2-метилфенил) бензамид] , 2,2'- дитиобис[N-(2-этилфенил) бензамид], 2,2'-дитиобис[N-(2- хлорфенил)бензамид] , 2,2'-дитиобис[N-[2-(1- метилэтил)фенил] бензамид] , 2,2'-дитиобис[N- (3-йодфенил)бензамид] , 4,4'-[дитиобис(2,1-фениленкарбонилимино) бисбензойную кислоту] , 2,2'-дитиобис(2,1-фениленкарбонилимино) бисбензойную кислоту, (4-{2-[2-(4-карбоксиметилфенилкарбамоил)- фенилдисульфанил]-бензоиламино}-фенил)-уксусную кислоту, дигидрохлорид 2,2'-дитиобис[N- (4-аминофенил)бензамида] , 2,2'- дитиобис[N-[4-(аминокарбонил) фенил]бензамид] , 4,4'-дитиобис(2- фениленкарбонилиминометилен) бисбензойную кислоту, [R-(R*,R*)] 2,2'-дитиобис[N-(2-гидрокси -1-фенилэтил)бензамид].
Во вторую группу предпочтительных арилтиосоединений формулы (I) входят соединения, у которых X означает группу 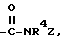 где R4 имеет указанное в п. 1 значение, a Z - группу формулы
где R4 имеет указанное в п. 1 значение, a Z - группу формулы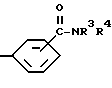
где R3 и R4 имеют указанные в п. 1 значения.
Представителями второй группы предпочтительных соединений формулы (I) являются соединения, представляющие собой сложный бис- 1,1-диметилэтиловый эфир N, N-[дитиобис [2,1-фениленкарбонилимино] - 4,1-фениленкарбонилимино] бис-1-L-аланина, [S-(R*,R*)]-2-[4-(2-{2-[4- (1-карбоксиэтилкарбамоил)- фенилкарбамоил] -фенилдисульфанил} - бензоиламино)-бензоиламино] -пропионовую кислоту.
В третью группу предпочтительных арилтиосоединений формулы (I) входят соединения, у которых X означает группу 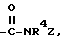 где R4 имеет указанное в п. 1 значение, а Z - фенил(CR5R6)m, где R5 и R6 имеют указанное в п.1 значение или алкил с 1-6 атомами углерода, незамещенный или замещенный гидроксилом или группой NR3R4, где R3 и R4 имеют указанное в п.1 значение.
где R4 имеет указанное в п. 1 значение, а Z - фенил(CR5R6)m, где R5 и R6 имеют указанное в п.1 значение или алкил с 1-6 атомами углерода, незамещенный или замещенный гидроксилом или группой NR3R4, где R3 и R4 имеют указанное в п.1 значение.
В качестве представителя третьей группы предпочтительных арилтиосоединений формулы (I) можно назвать [S-(R*,R*)]-2,2'-дитиобис[N -[1-(гидроксиметил)-3-метилбутил]-бензамид], 2,2'- дитиобис[N -2-(диметиламино)этилбензамид].
В четвертую группу предпочтительных арилтиосоединений формулы (I) входят соединения, у которых Х означает группу 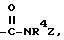 где R4 имеет вышеуказанное значение, a Z - группу формулы
где R4 имеет вышеуказанное значение, a Z - группу формулы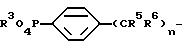
где R3, R5, R6 и n имеют вышеуказанные значения.
В качестве представителя четвертой группы предпочтительных арилтиосоединений формулы (I) можно назвать сложный диэтиловый эфир [4-(2-{2-[4-(диэтоксифосфорилметил)-фенилкарбамоил] - фенилдисульфанил}-бензоиламино) -бензил]-фосфоновой кислоты.
В пятую группу предпочтительных арилтиосоединений формулы (I) входят соединения, у которых X означает группу 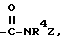 где R4 имеет вышеуказанное значение, а Z - группу СОалкил с 1-6 атомами углерода в алкильной части.
где R4 имеет вышеуказанное значение, а Z - группу СОалкил с 1-6 атомами углерода в алкильной части.
В качестве представителя пятой группы предпочтительных арилтиосоединений формулы (I) можно назвать 2,2'- дитиобис(N-ацетил-N-метил) бензамид.
В шестую группу предпочтительных арилтиосоединений формулы (I) входят соединения, у которых X означает группу SO2NR4Z, где R4 и Z имеют вышеуказанные значения, в частности представляют собой соединения общей формулы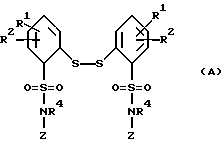
где R1, R2, R4 и Z имеют вышеуказанные значения.
Представителями шестой группы предпочтительных арилтиосоединений формулы (I) являются соединения, представляющие собой 2,2'-дитиобис[N- [4-(аминосульфонил)фенил]]- бензолсульфонамид, 2,2'-дитиобис[N-(4-нитрофенил)]- бензолсульфонамид, 2,2'-дитиобис[N-(4-метоксифенил)] - бензолсульфонамид, 2,2'-дитиобис [5-хлор]-бензолсульфонамид.
В седьмую группу предпочтительных арилтиосоединений формулы (I) входят соединения, у которых X означает группу 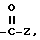 где Z имеет вышеуказанное значение, в частности представляют собой соединения общей формулы Б
где Z имеет вышеуказанное значение, в частности представляют собой соединения общей формулы Б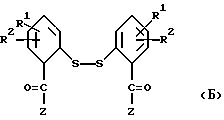
где R1, R2 и Z имеют вышеуказанное значение
В качестве представителя седьмой группы предпочтительных арилтиосоединений формулы (I) можно назвать [2-(2-бензоилфенилдисульфанил) -фенил]-фенилметанон.
В восьмую группу предпочтительных арилтиосоединений формулы (I) входят соединения, у которых X означает группу 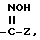 где Z имеет вышеуказанное значение, в частности представляют собой соединения общей формулы B
где Z имеет вышеуказанное значение, в частности представляют собой соединения общей формулы B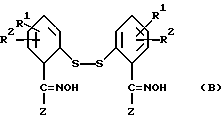
где R1, R2 и Z имеют вышеуказанное значение.
В девятую предпочтительных арилтиосоединений формулы (I) входят соединения, у которых Y - группа - SZ, где Z имеет вышеуказанное значение, в частности представляют собой соединения общей формулы Г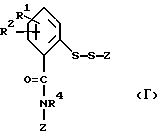
где R1, R2, R4 и Z имеют вышеуказанные значения.
В десятую группу предпочтительных арилтиосоединений формулы (I) входят соединения, у которых X означает группу 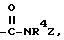 где R4 имеет вышеуказанное значение, а Z - алкил с 1-6 атомами углерода, замещенный остатками
где R4 имеет вышеуказанное значение, а Z - алкил с 1-6 атомами углерода, замещенный остатками 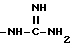 и CO2R3, где R3 имеет указанное в п.1 значение.
и CO2R3, где R3 имеет указанное в п.1 значение.
В качестве представителя десятой группы предпочтительных арилтиосоединений формулы (I) можно назвать сложный бис(1,1- диметилэтиловый) эфир N-N'-[дитиобис(2,1-фениленкарбонил) бис-L-аргинина] и N-N'-[дитиобис(2,1-фениленкарбонил) бис-L-аргинин.
В одиннадцатую группу предпочтительных арилтиосоединений формулы (I) входят соединения, у которых X означает группу 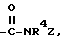 где R4 имеет вышеуказанное значение, а Z - циклоалкил-(CR5R6)m с 3-6 атомами углерода в циклоалкильной части, причем циклоалкил может быть замещен.
где R4 имеет вышеуказанное значение, а Z - циклоалкил-(CR5R6)m с 3-6 атомами углерода в циклоалкильной части, причем циклоалкил может быть замещен.
В качестве представителя одиннадцатой группы предпочтительных арилтиосоединений формулы (I) можно назвать 2,2'-дитиобис(N- циклопропилбензамид) и 4,4'-[дитиобис(2,1- фениленкарбонилиминометилен)] бистрансциклогексанкарбоновую кислоту.
В двенадцатую группу предпочтительных арилтиосоединений формулы (I) входят соединения, представляющие собой соединения общей формулы (Iа)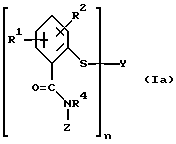
где R1 и R2 независимы друг от друга и означают водород, галоген, алкил с 1-6 атомами углерода, гидроксил, алкокси с 1-6 атомами углерода, карбоксил, алкоксикарбонил с 1-6 атомами углерода в алкоксильной части, группу NR3R4, где R3 и R4 независимы друг от друга и означают водород или алкил с 1-6 атомами углерода,
Y - водород, если n = 1, или простая связь, если n = 2,
Z - алкил с 1-6 атомами углерода, циклоалкил с 3-6 атомами углерода, незамещенные или замещенные 1 или 2 остатками из группы, включающей гидроксил, галоген, нитро, остаток NR3R4 и карбоксил, где R3 и R4 имеют вышеуказанные значения, или остаток формулы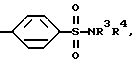
где R3 и R4 имеют вышеуказанные значения
n - 1 или 2,
и фармацевтически приемлемые соли и сольваты.
В качестве представителя двенадцатой группы предпочтительных арилтиосоединений формулы (I) можно назвать 2-[[2-[2-(1-карбокси 2-метилбутилкарбамоил)-фенилдисульфанил] -бензоил] амино] -3- метилпентановую кислоту, сложный трет-бутиловый эфир [S-(R*,R*)]-2-[2-[2-(1-трет- бутоксикарбонил-2-метилбутилкарбамоил)-6-фторфенилдисульфанил] - 3-фторбензоиламино]-3-метилпентановой кислоты, сложный трет-бутиловый эфир [S-(R*,R*)]-2- [2-[2-(1-трет-бутоксикарбонил-3- метилбутилкарбамоил)-5-фторфенилдисульфанил] -4-фторбензоиламино] - 4-метилпентановой кислоты, сложный трет-бутиловый эфир [S- (R*,R*)]-2-[2-[2- (1-трет-бутоксикарбонил-3- метилбутил-карбамоил)- 4-фторфенилдисульфанил] -5-фторбензоиламино] -4-метилпентановой кислоты, сложный трет-бутиловый эфир [S-(R*, R*)] -2-[2-[2-(1- трет-бутоксикарбонил-3- метилбутилкарбамоил)-6-метоксифенилди- сульфанил]-3-метоксибензоиламино] -4-метилпентановой кислоты, сложный трет-бутиловый эфир [S-(R*,R*)]-2- [2-[2-(1-трет- бутоксикарбонил -3-метилбутилкарбамоил)-5-метоксифенилдисульфанил] -4- метоксибензоиламино]-4-метилпентановой кислоты, сложный трет-бутиловый эфир [S-(R*,R*)]-2-[2-[2-(1- трет-бутоксикарбонил-3-метилбутилкарбамоил)-4- метоксифенилдисульфанил]-5-метоксибензоиламино] -4-метилпентановой кислоты, сложный трет-бутиловый эфир [S-(R*,R*)]-2-[2-[2-(1- трет-бутоксикарбонил -3-метилбутилкарбамоил)-6-метилфенилдисульфанил] -3- метилбензоиламино]-4-метилпентановой кислоты, сложный трет-бутиловый эфир [S-(R*, R*)]-2-[2-[2- (1-трет-бутоксикарбонил- 3-метилбутилкарбамоил) -5-метилфенилдисульфанил]-4- метилбензоиламино] -4-метилпентановой кислоты, сложный трет- бутиловый эфир [S-(R*,R*)]-2-[2-[2- (1-трет-бутоксикарбонил-3- метилбутилкарбамоил)-3-метилфенилдисульфанил] -6- метилбензоиламино]-4-метилпентановой кислоты, сложный ди-трет- бутиловый эфир [S-(R*,R*)]-{2-[2-(1,2-бис- трет- бутоксикарбонилэтилкарбамоил) -фенилдисульфанил]-бензоиламино}- янтарной кислоты, сложный ди-трет- бутиловый эфир [S-(R*,R*)]-2-{2-[2- (1,3-бис-трет- бутоксикарбонилпропилкарбамоил) -фенилдисульфанил]-бензоиламино}- глютаровой кислоты, сложный ди-трет-бутиловый эфир [S-(R*, R*)]-2-{2-[2- (1,4-бис-трет-бутоксикарбо- нилбутилкарбамоил) -фенилдисульфанил] -бензоиламино}-адипиновой кислоты, сложный трет-бутиловый эфир [R-(R*,R*)]-(2-{2- [(трет-бутоксикарбонилфенилметил) -карбамоил]-фенилдисульфанил}-бензоиламино) -фенилуксусной кислоты, сложный бис[O-(1,1-диметилэтил)] бис(1,1'- диметилэтиловый)] эфир N, N'-[дитиобис(2,1-фениленкарбонил)] бис- L-серина, сложный трет-бутиловый эфир L, L-2-[(2-{2- [(1-трет- бутоксикарбонил-3-метилбутил) -метилкарбамоил] -фенилдисульфанил}- бензоил)-метиламино] -4-метилпентановой кислоты, сложный бис (1,1- диметилэтиловый) эфир 4,4'-[дитиобис(2,1-фениленкарбонилимино)] - бисбутановой кислоты, сложный трет-бутиловый эфир [S-(R*, R*)] 2-{ 5-ацетиламино -2-[4-ацетиламино-2-(1 -трет -бутоксикарбонил-3- метилбутилкарбамоил) -фенилдисульфанил] бензоиламино} -4- метилпентановой кислоты, сложный трет-бутиловый эфир [S- (R*,R*)]-2-{5- этиламино-2-[4-этиламино-2- (1-трет-бутоксикарбонил-2- метилбутилкарбамоил)-фенилдисульфанил] -бензоиламино}-3- метилпентановой кислоты, L,L-2-{2-[2-(1-карбокси-2,2- диметилпропилкарбамоил)-фенилдисульфанил]-бензоиламино}-3,3- диметилмасляную кислоту, 2-[2-(2-{2-[1 -(1-карбоксиэтилкарбамоил)- 3-метилбутилкарбамоил]-фенилдисульфанил} -бензоиламино)-4- метилпентаноиламино]-пропионовую кислоту, [S-(R*,R*)]-2-{2-[2-(1- карбокси-2-метилбутилкарбамоил) -6-фторфенилдисульфанил] -3-фторбензоиламино}- 3-метилпентановую кислоту, [S-(R*,R*)]2-{2-[2-(1- карбокси-3-метилбутилкарбамоил) -5-фторфенилдисульфанил] -4- фторбензоиламино} -4- метилпентановую кислоту, [S-(R*,R*)]-2-{2-[2-(1 -карбокси-3- метил-бутилкарбамоил)-4-фторфенилдисульфанил] -5- фторбензоиламино}-4-метилпентановую кислоту, [S-(R*, R*)]-{[(2- карбамоил)-6-метоксифенилдисульфанил] -3-метокси-бензоиламино}-4- метилпентановую кислоту, [S-(R*,R*)] 2-{ 2- [2-(1-карбокси-3- метилбутилкарбамоил)-5-метоксифенилдисульфанил]-4- метоксибензоиламино} -4-метилпентановую кислоту, [S-(R*,R*)]-2-{2- [2-(1-карбокси-3-метилбутилкарбамоил) -4-метоксифенилдисульфанил] - 5-метоксибензоиламино} -4-метилпентановую кислоту, [S-(R*,R*)]-2- {2-[2-(1-карбокси-3-метилбутилкарбамоил) -6- метилфенилдисульфанил] -3-метилбензоиламино}-4-метилпентановую кислоту, [S-(R*,R*)]-2-{2-[2- (1-карбокси-3-метилбутилкарбамоил)- 5-метилфенилди-сульфанил] -4-метилбензоиламино}-4-метилпентановую кислоту, L,L-2-{2-[2-(1-карбокси -3-метилбутилкарбамоил)-3- метилфенилдисульфанил] -6-метилбензоиламино} -4-метилпентановую кислоту, L,L-2-[(2-{2-[(1-карбокси -3-метилбутил)- метилкарбамоил]-фенилдисульфанил} -бензоил)-метиламино] -4-метилпентановую кислоту, [S-(R*,R*)]2-{5-ацетиламино-2- [4-ацетиламино- 2-(1-карбокси -3-метилбутилкарбамоил) -фенилдисульфанил]- бензоиламино} -4-метилпентановую кислоту, N,N'-[дитио-бис[[5- (этиламино)-2,1-фенилен] карбонил] ] бис-L-изолейцин, L,L-2-{2-[2- (1,2-дикарбоксиэтилкарбамоил) -фенилдисульфанил] -бензоиламино} - янтаруную кислоту, L,L-2-{2-[2-(1,3-дикарбоксипропилкарбамоил) -фенилдисульфанил]- бензоиламино}-глютаровую кислоту, [S-(R*,R*)]-2- {2-[2-(1,4-дикарбоксибутил-карбамоил) -фенилдисульфанил]- бензоиламино}-адипиновую кислоту, 4,4'-[дитиобис(2,1 - фениленкарбонилимино)] бисбутановую кислоту, [R-(R*,R*)](2-{2-[(карбоксифенилметил) -карбамоил]- фенилдисульфанил}-бензоиламино)- фенилуксусную кислоту, [S-(R*,R*)] -3-трет-бутокси-2-{ 2- [2-(2-трет-бутокси-1-карбоксиэтилкарбамоил)- фенилдисульфанил] -бензоиламино}-пропионовую кислоту, 3,3'- [дитиобис(2,1 -фениленкарбонилимино)] -биспропионовую кислоту, сложный бис(1,1-диметилэтиловый) эфир N,N'-бис [дитиобис (2,1 - фениленкарбонил)бис[6- [[(1,1-диметилэтокси) карбонил]амино]-L- норлейцина]].
Благодаря антибактериальной и антивирусной активности предлагаемые арилтиосоединения формулы (I) или их фармацевтически приемлемые соли или сольваты могут представлять собой активное вещество фармацевтической композиции, которая помимо по меньшей мере одной фармацевтически приемлемой добавки из группы, включающей разбавитель, носитель и наполнитель, содержит эффективное количество активного вещества.
Данная фармацевтическая композиция с антибактериальной и антивирусной активностью является вторым объектом изобретения.
Третьим объектом изобретения является способ лечения бактериальных и вирусных инфекций путем введения пациенту соединения формулы (I) в эффективном количестве.
Введение соединения формулы (I) можно также осуществлять в комбинации по меньшей мере с одним другим антибактериальным и антивирусным средством.
Под понятием "алкил с 1-6 атомами углерода" подразумевается алифатическая группа с прямой или разветвленной цепью, имеющая от 1 до 6 атомов углерода. Примеры включают метил, этил, изобутил, н-пентил и изогексил. Под понятием алкокси с 1-6 атомами углерода подразумеваются указанные выше алкильные группы, связанные через атом кислорода, примерами этих групп являются метоксигруппа, этоксигруппа, изопропоксигруппа, трет-бутоксигруппа и им подобные. Типичные группы, представляющие циклоалкил с 3-6 атомами углерода, включают циклопропил, циклопентил, циклогексил и тому подобные группы.
Типичными группами Het являются остатки формул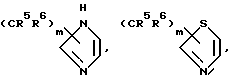
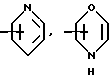
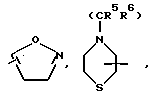
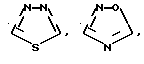
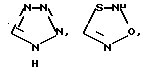
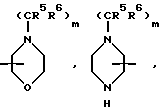
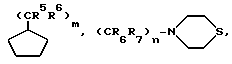
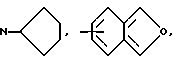
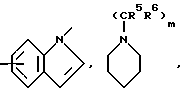
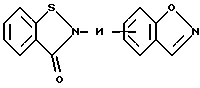
и тому подобные группировки. Другими типичными Het-группами являются пиримидин, пиридазин, пиразин, оксазол, пиразол, тиазол и им подобные.
Типичные замещенные алкильные группы включают, например, хлорметил, 3-бромпропил, трифторметил, 4-гидроксигексил, 1- карбокси-2-метилбутил, 3-метилтиобутил, 4-метилсульфонилбутил, диметиламинометил, 2,3-дибромбутил, 2-амино-3-хлор-4- карбоксибутил, 3-ацетамидопропил, 2-ацетилэтил, 2- метоксикарбонилэтил, 1,1-диацетилпропил и им подобные.
Предпочтительными замещенными алкильными группами являются группы, имеющие один, два или три заместителя, выбранные из таких, как галоген, гидроксигруппа или карбоксильная группа. Такие предпочтительные группы включают 1-бром-2-гидроксипропил, 1,1- диметил-3-гидроксипропил, 1-гидроксиметил-2-фторметил-3- карбоксибутил, 1 -карбокси-2-метилбутил, 1 -карбокси-3-метилбутил, 1,2,3-тригидроксипентил и им подобные.
Типичные замещенные циклоалкильные группы включают 2-фторциклопропил, 2,2-дибромциклопропил, 2-карбоксициклобутил, 2-аминосульфонилциклопентил, 2-амино-3-карбоксициклопентил и 3-изопропилсульфинилциклогексил.
Типичные заместители NR3R4 фенилового остатка в группе фенил-(CR5R6)m включают аминогруппу, метиламиногруппу, диметиламиногруппу, этилизогексиламиногруппу, циклопропиламиногруппу, N-ацетиламиногруппу, N-метил-N- ацетиламиногруппу, бензиламиногруппу и 3-хлорбензиламиногруппу.
Типичные заместители NR3COR4 фенилового остатка в группе фенил-(CR5R6)m включают циклопропилкарбониламиногруппу, N-изобутил- N-циклогексилкарбонил-аминогруппу и им подобные. Типичные группы CO2R3 фенилового остатка в группе фенил-(CR5R6)m включают свободную карбоновую кислоту, когда R3 является водородом, и сложные эфиры, такие как алкильные эфиры (алкил с 1 - 6 атомами углерода), бензиловые эфиры, циклобутиловые эфиры и им подобные. Амидные заместители CONR3R4 фенилового остатка в группе фенил-(CR5R6)m включают карбоксамид, N-метилкарбоксамид и N,N-диэтилкарбоксамид. Типичные замещающие группы S(O)mR3 фенилового остатка в группе фенил-(CR5R6)m включают метилтиогруппу, этилсульфинильную группу, циклопропилсульфонильную группу и им подобные. Сульфонамидные заместители включают N-метилсульфонамид, N,N-диметилсульфонамид и им подобные. Типичные группы фенил-(CR5R6)m, замещенные вышеупомянутыми замещающими группами, таким образом, включают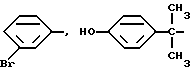
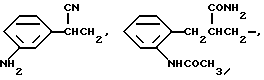
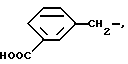
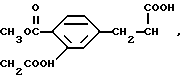
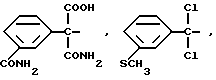
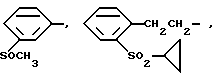
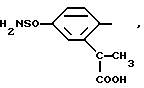
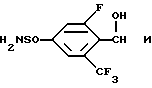
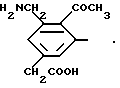
Типичные группы Het-(CR5R6)m включают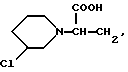
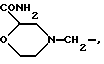
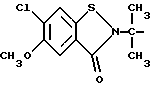
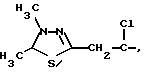
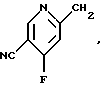
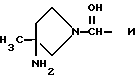
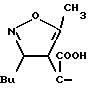
Арилтиосоединения формулы I могут быть получены при использовании любого способа из числа синтетических способов, известных специалистам в области органической химии. Так, замещенная тиольной группой арилкарбоновая кислота или арилсульфокислота может быть превращена в дитиобисарилкарбоновую кислоту или дитиобисарилсульфокислоту при реакции с окислителем, таким как перекись водорода или йод. Дитиобисарилкарбоновые кислоты и дитиобисарилсульфокислоты могут быть непосредственно подвергнуты реакции с амином в присутствии реагента, способствующего сочетанию пептидов, такого как дициклогексилкарбодиимид (ДЦГК) или 2-этокси-1-этоксикарбонил-1,2- дигидрохинолин (ЭЭДХ), обычно в общем инертном растворителе, таком как дихлорметан или хлороформ, чтобы получить дитиобисарилкарбоксамиды и дитиобисарилсульфонамиды по изобретению. Вышеописанные реакции иллюстрируются следующей общей схемой: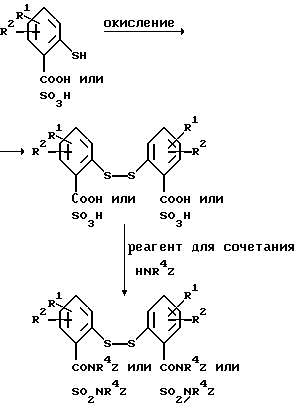
где R1, R2, A, R4 и Z являются такими, как указано выше.
Карбоксамиды и сульфонамиды альтернативно могут быть получены при реакции амина с соответствующим галогенангидридом кислоты. Дитиобисарилкарбоновые кислоты и дитиобисарилсульфокислоты легко превращаются в соответствующие галогенангидриды, например в хлорангидриды при реакции с таким хлорирующим агентом, как тионилхлорид или оксалилхлорид. Хлорангидриды кислот легко подвергаются превращению в дитиобисариламиды в соответствии с изобретением при реакции с амином, например, в соответствии с представленной ниже схемой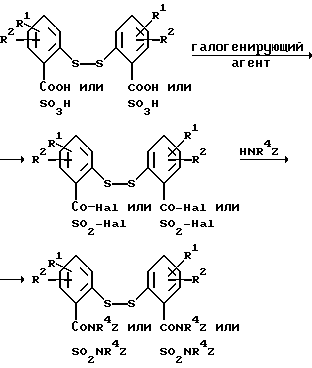
где R1, R2, A, R4 и Z являются такими, как указано выше.
Реакцию образования амида обычно осуществляют при взаимодействии двух молярных эквивалентов амина ZNHR4 с одним молярным эквивалентом дитиобисароилхлорида. Реагенты обычно смешивают в общем растворителе, таком как дихлорметан, ацетон, толуол или им подобные, и реакция обычно в основном заканчивается в пределах от двух до шести часов, когда она проводится при температуре от около 0o до 100oC. Слабое основание, как триэтиламин или пиридин, может быть добавлено по желанию для удаления кислоты. Продукт легко выделяют при удалении растворителя, и обычно продукт может быть при необходимости очищен кристаллизацией или другим похожим способом.
Полученные таким образом дитиобисариламиды легко могут быть подвергнуты превращению в тиоариламиды согласно изобретению при реакции с восстановителем, таким как 1,4-дитиотреитол, согласно следующей схеме: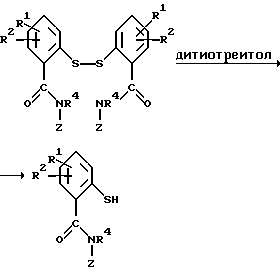
где R1, R2, R4 и Z являются такими, как указано выше. Реакцию гидролиза обычно проводят в одном растворителе, таком как этанол или ацетон, и, как правило, она заканчивается в пределах от 0,5 часа до 2 часов, когда проводится при температуре примерно от 5o до 50oC. Полученный тиол легко выделяют путем удаления растворителя и кристаллизации продукта.
Альтернативный способ получения дитиобисариламидов по изобретению состоит из реакции 2-галогенариламида с элементарной серой или моносульфидом натрия в соответствии со схемой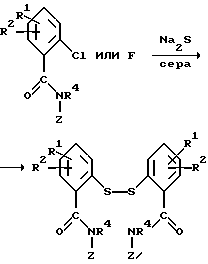
Для реакции характерно проведение ее в одном растворителе, таком как метанол или этанол, и обычно реакция, по существу, заканчивается в пределах от одного до двух часов, когда ее проводят при температуре примерно от 25o до 100oC. Дитиобисариламид легко выделяют при удалении растворителя реакции и кристаллизации продукта из такого растворителя, как изопропиловый спирт или ему подобного.
Дитиобисарилкетоны и дитиобисарилоксимы (то есть формула I, где Х является -C(=O)-Z и -C(=NOH)-Z соответственно) могут быть получены, если сначала арилтиол подвергают реакции с сильным основанием, таким как н-бутиллитий, для получения орто-литиевого производного арилтиола, а затем литиированное промежуточное соединение подвергают реакции с N-алкил-N-алкоксиамидом. Реакция иллюстрируется следующей схемой: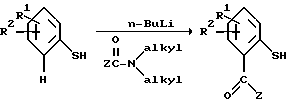
Арилтиол, как правило, подвергается реакции с примерно двумя молярными эквивалентами н-бутиллития обычно при пониженной температуре от около -40o до 0oC в инертном органическом растворителе, таком как серный эфир, тетрагидрофуран или гексан. Литиированный арилтиол подвергают реакции с N-алкил-N-алкоксиамидом (например, N-метил-N-метокси-бензамидом) для получения замещенного тиольной группой арилкетона. Арилкетон может быть подвергнут реакции с гидроксиламином с образованием соответствующего оксима или он может быть подвергнут превращению в соответствующий дитиобисарилкетон при реакции с примерно эквимолярным количеством диэтилового эфира азодикарбоновой кислоты /СН3СН2O-С(= O)-N=N-C(=O)-ОСН2СН3/ обычно в инертном растворителе, таком как дихлорметан. Дитиобисарилкетон, соединения формулы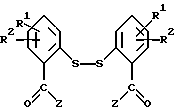
легко превращаются в соответствующие оксимы при реакции с гидроксиламином, обычно в органическом растворителе, таком как этиловый спирт и ему подобные. При желании могут быть использованы такие основания, как пиридин или триэтиламин, в качестве акцепторов кислоты.
Если в вышеописанных реакциях заместители R1 и R2 сами по себе реакционноспособны, например, если R1 является гидроксилом, карбоксилом или аминогруппой, заместители могут сами быть защищены в соответствии с известными в этой области способами для предотвращения нежелательных побочных реакций. Например, реакционноспособные группы могут быть превращены в соответствующие производные, что защитит заместитель от нежелательных побочных реакций, а затем защитная группа может быть удалена, чтобы восстановить первоначальный заместитель. Может быть применено множество известных защитных групп. Например, типичные защитные группы для гидроксила включают защитные группы, которые могут быть присоединены к гидроксигруппе, а затем при необходимости легко удалены. Эти группы охватывают ацильные группы, такие как формил и ацетил, а также бензил, триметилсилил и им подобные. Аминогруппы также могут нуждаться в защите, и типичные защитные группы для аминогруппы включают ацильные группы, такие как ацетил, пивалоил и трет-бутоксикарбонил (БОК), и арилалкильные группы, такие как п-нитробензил и им подобные. Карбоксильные группы, как правило, подвергаются превращению в сложноэфирные, получают трет-бутиловый и 2,2,2-трихлорэтиловый эфиры, все такие защитные группы могут быть при желании легко удалены, например, путем гидролиза в присутствии кислоты, такой как соляная кислота или трифторуксусная кислота. Примеры многих из этих типичных защитных групп можно найти в книге "Защитные группы в органическом синтезе", Т. W. Greene и P. Wuts, John Wiley & Sons, 1991.
Как указано выше, одна из предпочтительных групп соединений включает соединения формулы I, где Х является -C(=O)-NR4Z и Z является алкилом, замещенным, как минимум, одной карбоксильной группой. Особо предпочтительным способом получения таких соединений является реакция дитиобисароилгалогенида с аминокислотой. Типичными аминокислотами, которые могут быть использованы, являются те а-аминокислоты, которые входят обычно в состав белков, например глицин, аланин, валин, лейцин, изолейцин, фенилаланин, серин, треонин, лизин, d-гидроксилизин, аргинин, аспарагиновая кислота, аспарагин, глутаминовая кислота, глутамин и тому подобные. Типичный синтез изображен ниже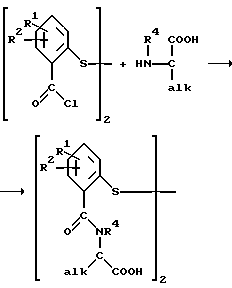
где R1 и R2 являются такими, как указано выше, и alk означает остаток низшего алкила, который может быть замещен такими группами, как карбоксильная группа, гидроксигруппа, аминогруппа, карбоксамид и им подобные. Карбоксильные группы обычно защищают, превращая их в ходе реакции в сложноэфирные, например получают соответствующий трет-бутиловый эфир, бензиловый эфир и им подобные, сложноэфирные группы могут быть легко подвергнуты гидролизу по окончании реакции с образованием свободных кислот.
Несимметричные соединения формулы I, то есть соединения формулы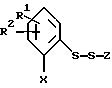
могут быть получены при реакции тиола формулы HS-Z1 с изотиазолоном в соответствии со следующей схемой: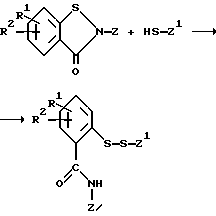
где R1, R2, А и Z являются такими, как указано выше, и Z1 является одной из групп, обозначенных Z, но Z и Z1 в вышеуказанном продукте не должны быть одинаковыми группами.
Реакцию изотиазолона и тиола обычно проводят путем смешивания примерно эквимолярных количеств реагентов в одном растворителе, таком как метанол, толуол, ксилол и им подобные, и нагревания реакционной смеси до примерно 30oC - 100oC в течение 8 - 24 часов. Продукт выделяют, удаляя растворитель, затем продукт может быть очищен путем кристаллизации или хроматографии. Изотиазолоны, используемые в вышеуказанной реакции, легко могут быть получены при простой реакции дитиобисариламида согласно изобретению с окисляющим агентом, таким как хлор или бром, или с галогенкарбонилсульфенилгалогенидом, например, в соответствии со следующей схемой: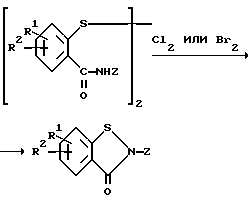
Некоторые из реакций, описанных выше, могут приводить к смеси изомеров. К примеру, некоторые соединения содержат один или более асимметрических атомов углерода и сами по себе могут существовать как стереохимические изомеры. Смеси при желании могут быть разделены с помощью известных для специалистов способов на индивидуальные изомеры, например при фракционной перегонке, кристаллизации и/или хроматографии. Альтернативно, конкретные изомеры могут быть получены при использовании стереоспецифического синтеза, например, применяя оптически активную а-аминокислоту (например, L-лейцин или L-аспарагиновую кислоту) в реакции с дитиобисароилгалогенидом.
Некоторые из соединений этого изобретения могут образовывать соли и сольваты. Например, соединения, в которых R1 или R2 является аминогруппой, могут взаимодействовать с неорганическими и органическими кислотами с образованием солей в результате присоединения кислот. Обычно используемые типичные кислоты включают соляную кислоту, серную кислоту, уксусную кислоту, малоновую кислоту, п-толуолсульфокислоту и им подобные. Соединения с кислотной группой, например, когда Z содержит свободную карбоксильную группу, могут вступать в реакцию с органическими и неорганическими основаниями с образованием солей. Типичные основания включают гидрат окиси натрия, триэтиламин, пиридин, карбонат калия и им подобные.
Сольваты обычно образуются при кристаллизации соединений по изобретению из таких растворителей, как вода, этиловый спирт, изопропиловый спирт и им подобные.
Синтез соединений данного изобретения далее иллюстрируется следующими примерами. Примеры не следует интерпретировать как ограничивающие изобретение в каком-то отношении. Исходные вещества, используемые в примерах, вполне доступны из коммерческих источников или могут быть получены с помощью методик, описанных в научной литературе. Например, Bell P., J. Am. Chem. Soc., 1942: 2905, описывает ряд бензамидов, которые могут быть использованы. Способы, изложенные М. L. Carmellino и др., Eur. J. Med. Chem. 1994; 29: 743-751, обеспечивают получение фторированных тиопроизводных бензойной кислоты, которые могут быть использованы. Способы, описанные О. Francis Bennett и др. , Organic Prep. and Proced. Int., 1974; 6(6): 287-293, дают возможность получить ряд алкокситиопроизводных бензойной кислоты. Способы, описанные Т. Vitali и др., II Farmaco Ed. Sc. 1968; 23:468-476, приводят к алкилтиопроизводным бензойной кислоты, которые затем могут быть использованы.
Примеры А-С иллюстрируют получение промежуточных продуктов, а пример 1 - получение целевых соединений формулы (I).
Пример А
2.2'-Дитиобисбензоилхлорид
Смесь 2,2'-дитиобис(бензойной кислоты) (25 г, 81.6 ммоля) нагревали в 350 мл тионилхлорида при кипении в течение 18 часов. Полученный раствор охлаждали примерно до 30oC и избыток тионилхлорида удаляли в вакууме. Технический твердый продукт суспендировали в гексане и указанное в названии вещество выделяли при фильтрации, выход 21.2 г. Это вещество использовали без дальнейшей очистки, т. пл. 150-151oC.
ЯМР (дейтерохлороформ): d 8.4 (м, 2H), 7.7 (д, 2H), 7.5 (м, 2H), 7.3 - 7.4 (м, 2H).
Пример Б
2.2'-Дитиобис[3-фторбензоилхлорид]
Смесь 2,2'-дитиобис[3-фторбензойной кислоты] (0.4 г, 1.0 ммоль) и хлористого тионила (10 мл) подвергали реакции в соответствии с методикой, описанной в примере А, и получали 0.3 г 2,2'-дитиобис[3- фторбензоилхлорида]. Это соединение использовалось без дальнейшей очистки.
Пример В
2.2'-Дитиобис[4-фторбензоилхлорид]
Смесь 2,2'-дитиобис[4-фторбензойной кислоты] (5.0 г, 14.6 ммоля) и хлористого тионила подвергали реакции в соответствии с методикой, описанной в примере А, и получали 4.1 г 2,2'-дитиобис[4- фторбензоилхлорида]. Это соединение использовали без дальнейшей очистки.
Пример Г
2.2'-Дитиобис[5-фторбензоилхлорид]
Смесь 2,2'-дитиобис[5-фторбензойной кислоты] (5.0 г, 14.6 ммоля) и хлористого тионила (40 мл) подвергали реакции в соответствии с методикой, описанной в примере А, и получали 4.9 г 2,2'-дитиобис[5-фторбензоилхлорида]. Это соединение использовали без дальнейшей очистки.
Пример Д
2.2'-Дитиобис[3-метоксибензоилхлорид]
Смесь 2,2'-дитиобис[3-метоксибензойной кислоты] (2.0 г, 5.0 ммолей) и хлористого тионила (30 мл) подвергали реакции в соответствии с методикой, описанной в примере А, и получали 1.9 г 2,2'-дитиобис[3-метоксибензоилхлорида]. Это соединение использовали без дальнейшей очистки.
Пример Е
2.2'-Дитиобис[4-метоксибензоилхлорид]
Смесь 2,2'-дитиобис[4-метоксибензойной кислоты] (2.2 г, 6.6 ммоля) и хлористого тионила (20 мл) подвергали реакции в соответствии с методикой, описанной в примере А, и получали 2.1 г 2,2'- дитиобис[4-метоксибензоилхлорида]. Это соединение использовали без дальнейшей очистки.
Пример Ж
2.2'-Дитиобис[5-метоксибензоилхлорид]
Смесь 2,2'-дитиобис[5-метоксибензойной кислоты] (0.8 г, 2.0 ммоля) и хлористого тионила (10 мл) подвергали реакции в соответствии с методикой, описанной в примере А, и получали 0.8 г 2,2'- дитиобис[5-метоксибензоилхлорида]. Это соединение использовали без дальнейшей очистки.
Пример З
2.2'-Дитиобис[3-метилбензоилхлорид]
Смесь 2,2'-дитиобис[3-метилбензойной кислоты] (2.9 г, 8.6 ммоля) и хлористого тионила (40 мл) подвергали реакции в соответствии с методикой, описанной в примере А, и получали 2.6 г 2,2'- дитиобис[3-метилбензоилхлорида]. Это соединение использовали без дальнейшей очистки.
Пример И
2.2'-Дитиобис[4-метилбензоилхлорид]
Смесь 2,2'-дитиобис[4-метилбензойной кислоты] (3.8 г, 11.9 ммоля) и хлористого тионила (50 мл) подвергали реакции в соответствии с методикой, описанной в примере А, и получали 3.6 г 2,2'- дитиобис[4-метилбензоилхлорида]. Это соединение использовали без дальнейшей очистки.
Пример К
2.2'-Дитиобис[5-метилбензоилхлорид]
Смесь 2,2'-дитиобис[5-метилбензойной кислоты] (0.6 г, 1.8 ммоля) и хлористого тионила (10 мл) подвергали реакции в соответствии с методикой, описанной в примере А, и получали 0.3 г 2,2'- дитиобис[5-метилбензоилхлорида]. Это соединение использовали без дальнейшей очистки.
Пример Л
2.2'-Дитиобис[6-метилбензоилхлорид]
Смесь 2,2'-дитиобис[6-метилбензойной кислоты] (0.6 г, 1.8 ммоля) и хлористого тионила (10 мл) подвергали реакции в соответствии с методикой, описанной в примере А, и получали 0.3 г 2,2'- дитиобис[6-метилбензоилхлорида]. Это соединение использовали без дальнейшей очистки.
Пример М
2.2'-Дитиобис[3-пиридинкарбонилхлорид]
Смесь 2,2'-дитиобис[3-пиридинкарбоновой кислоты] (1.5 г, 4.8 ммоля) и хлористого тионила (20 мл) подвергали реакции в соответствии с методикой, описанной в примере А, и получали 1.3 г 2,2'- дитиобис[3-пиридинкарбонилхлорида]. Это соединение использовали без дальнейшей очистки.
Пример Н
4-(3-Оксо-3H-бензо[d]изотиазол-2-ил)бензолсульфонамид
Раствор 60 мл метилового спирта и 60 мл тетрагидрофурана охлаждали до 0oC и к нему прибавляли по каплям 3.9 г (30.0 ммолей) хлоркарбонилсульфенилхлорида. Смесь перемешивали при 0oC в течение 20 минут и обрабатывали 9.0 г (29.2 ммоля) 2-тио-N-(4-сульфамоилфенил)бензамида (см. нижепредставленный пример 6). Реакционную смесь перемешивали при 0oC в течение получаса, а затем давали температуре подняться до комнатной температуры в течение 18 часов. Суспензию разбавляли 200 мл эфира, перемешивали в течение часа и твердый остаток отделяли при фильтрации. После промывания эфиром осадок сушили в вакууме и получали 7.8 г указанного в названии соединения. Дополнительно получали 2.2 г при концентрировании маточных растворов и растирании остатка с эфиром. Т.пл. обеих фракций была 283 - 285oC.
Пример О
[S-(R*, R*)] -3-Метил-2-(3-оксо-3Н-бензо[d] изотиазол- 2-ил)валериановая кислота
К перемешиваемой при комнатной температуре суспензии 5.3 г (10.0 ммолей) [S-(R*,R*)]-2-[2-[2-(1-карбокси-2- метилбутилкарбамоил)фенилдисульфанилбензоиламино]-3-метил- валериановой кислоты (приготовленной обычным способом по примеру 5) в 200 мл дихлорметана прибавляли по каплям 2.4 г (15.0 ммолей) жидкого брома. Реакционную смесь перемешивали при комнатной температуре 2 часа, растворитель упаривали в вакууме. Остаток растирали с дихлорметаном, который также упаривали в вакууме для удаления избытка брома. Остаток распределяли между дихлорметаном /5% бикарбонатом натрия (200 мл каждого). Водный слой отделяли, промывали дихлорметаном и подкисляли до pH 1.5 6.0 М соляной кислотой. После экстрагирования дихлорметаном (2 х 75 мл) объединенные органические слои промывали водой, сушили (сернокислым магнием), фильтровали и упаривали в вакууме, получали 4.8 г соединения, указанного в названии, т.пл. 50-52oC.
Пример П
2-Меркаптобензофенон
К раствору N,N,N',N'-тетраметилендиамина (4.4 г, 0.038 моля) и тиофенола (2 г, 0.018 моля) в циклогексане (40 мл) прибавляли по каплям н-бутиллитий (24 мл, 0.038 моля) при комнатной температуре. Суспензию перемешивали в атмосфере азота в течение 16 часов, после чего прибавляли по каплям N-метокси-N-метилбензамид (3.3 г, 0.019 моля). После перемешивания в течение 20 минут реакционную смесь прибавляли к холодной разбавленной водой соляной кислоте (1 н.). Продукт разделяли между этилацетатом и кислотным раствором. Слои разделяли и органический слой промывали соляным раствором, сушили (сернокислым натрием), фильтровали и фильтрат подвергали концентрированию в вакууме. Полученную жидкость подвергали очистке с помощью хроматографии на силикагеле (75% гексан/ 25% этилацетат), получали 2.3 г указанного в названии соединения в виде вязкой желтой жидкости.
ЯМР (дейтерохлороформ): d 7.8-7.2 (м, 9H), 4.2 (с, 1H) м.д.
Пример Р
2-Меркапто-5-хлорбензолсульфонамид
К 34.0 г (0.15 моля) 2,5-дихлорбензолсульфонамида в 200 мл диметилформамида прибавляли 16.0 г (0.28 моля) кислого сернистого натрия. Смесь подвергали кипячению в течение 18 часов, затем охлаждали, концентрировали и твердый остаток отфильтровывали. Отфильтрованный твердый остаток растворяли в горячей воде, доводили pH до 4.0 и осадок отфильтровывали. После высушивания продукта получали 10.1 г указанного в названии вещества, т.пл. 142-144oC.
Пример С
2-Хлор-5-нитробензамид
Смесь 2-хлор-5-нитробензойной кислоты (15.0 г, 74.0 ммоля) в 200 мл дихлорметана подвергали реакции при 24oC с хлорангидридом щавелевой кислоты (16.2 мл, 186.0 ммолей) и каталитическим количеством диметилформамида. Через 3 часа растворитель удаляли в вакууме, а остаток заново растворяли в 200 мл свежего дихлорметана. Раствор охлаждали до 0oC и в раствор барботировали аммиак в течение 5 минут, после чего продукт осаждался из раствора. Продукт отфильтровывали и получали 6.8 г 2-хлор-5-нитробензамида, т. пл. 174-175oC.
ЯМР (дейтерированный диметилсульфоксид): d 8.2 (м, 2H), 8.2 (с, 1H), 7.8 - 7.9 (м, 2H).
Пример 1
2.2'-Дитиобис[4'-сульфамоилбензанилид] (общий метод)
Раствор 2,2'-дитиобисбензоилхлорида (5.0 г, 14.0 ммолей) в 50 мл дихлорметана прибавляли по каплям к раствору 4- (аминосульфонил)-анилина (6.2 г, 36.0 ммолей) в 125 мл пиридина, охлажденного до 0oC. Смесь перемешивали 18 часов при 0oC и образовавшийся твердый осадок удаляли при фильтрации, промывали 1 н. соляной кислотой, водой, сушили в вакууме, получали 7.6 г технического продукта. Этот технический продукт (6.5 г) суспендировали в 50 мл диметилформамида/ 60 мл этилового спирта, фильтровали и осаждали из отфильтрованного раствора при прибавлении 10 мл 4% водного раствора бикарбоната натрия. Продукт отфильтровывали, промывали этиловым спиртом и водой, получали 4.3 г указанного в названии соединения, т. пл. 311-312oC.
ЯМР (дейтерированный диметилсульфоксид): d 10.9 (с, 2H), 7.7-8.0 (м, 12H), 7.5 (м, 2H), 7.4 (м, 2H), 7.3 (с, 4H).
Описываются новые арилтиосоединения общей формулы I, где R1 и R2 независимы друг от друга и означают водород, галоген, алкил с 1-6 атомами углерода, алкокси с 1-6 атомами углерода, циклоалкил с 3-6 атомами углерода, гидроксил, циано, фенил (CR5R6)m, группы Het-(CR5R6)m, NR3R4, NR3COR4,
CO2R3, CONR3R4, S(O)mR3, S(O)mNR3R4, COR3 или вместе означают оксогруппу или метилендиокси, где R3 и R4 независимы друг от друга и означают водород, алкил с 1-6 атомами углерода, циклоалкил с 3-6 атомами углерода, фенил (CR5R6)m, R5 и R6 независимы друг от друга и означают водород, алкил с 1-6 атомами углерода, гидроксил, карбоксил, аминогруппу, группу CONH2 или цианогруппу, Het - циклическое или бициклическое кольцо с 4-10 атомами, 1-4 из которых означают кислород, серу или азот, m - 0, 1 или 2, Х - группы -(О)= С-NR4Z, -(O)=C-Z, -(NOH)=C-Z или SO2NR4Z, где Z - галоген, замещенный алкил с 1-6 атомами углерода, группы СО-алкил с 1-6 атомами углерода в алкильной части, циклоалкил-(CR5CR6) с 3-6 атомами углерода в циклоалкильной части, фенил (CR5CR6)m, где R5, R6 и m имеют вышеуказанное значение, a R4 имеет вышеуказанное значение, Y - водород или группа SZ, если n = 1, или простая связь, если n = 2, причем Z имеет вышеуказанное значение, n = 1 или 2, причем указанные остатки алкила, циклоалкила, фенила и Het могут быть замещены 1-3 остатками из группы, включающей галоген, алкил с 1-6 атомами углерода, алокси с 1-6 атомами углерода, трифторметил, гидроксил, циано, нитро, NR3R4, NR3COR4, СO2R3, -NH(NH)= C-NH2, CONR3R4, S(O)3R3, PO4(R3)3, S(O)mNR3R4, COR3, где R3, R4 и m имеют вышеуказанное значение, и их фармацевтически приемлемые соли и сольваты. Эти соединения проявляют антибактериальную и противовирусную активность и пригодны для лечения бактериальных и вирусных инфекций. Описывается также способ лечения и фармацевтическая композиция на основе соединений формулы I. 3 с. и 44 з.п. ф-лы.
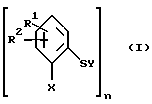
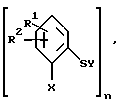
где R1 и R2 независимы друг от друга и означают водород, галоген, алкил с 1 - 6 атомами углерода, алкокси с 1 - 6 атомами углерода, циклоалкил с 3 - 6 атомами углерода, гидроксил, циано, фенил(CR5R6)m, группы Het-(CR5R6)m, NR3R4, NR3COR4, CO2R3, CONR3R4, S(O)mR3, S(O)mNR3R4, COR3 или вместе означают оксогруппу или метилендиокси, где R3 и R4 независимы друг от друга и означают водород, алкил с 1 - 6 атомами углерода, циклоалкил с 3 - 6 атомами углерода, фенил(CR5R6)m, R5 и R6 независимы друг от друга и означают водород, алкил с 1 - 6 атомами углерода, гидроксил, карбоксил, аминогруппу, группу CONH2 или цианогруппу, Het - циклическое или бициклическое кольцо с 4 - 10 атомами, 1 - 4 из которых означают кислород, серу или азот, m - 0,1 или 2;
X - группы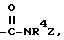
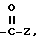
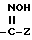
или SO2NR4Z, где Z - галоген, замещенный алкил с 1 - 6 атомами углерода, группы COалкил с 1 - 6 атомами углерода в алкильной части, циклоалкил-(CR5CR6)m с 3 - 6 атомами углерода в циклоалкильной части, фенил (CR5CR6)m, где R5, R6 и m имеют вышеуказанное значение, а R4 имеет вышеуказанное значение,
Y - водород или группа SZ, если n = 1, или простая связь, если n = 2, причем Z имеет вышеуказанное значение,
n - 1 или 2,
причем указанные остатки алкила, циклоалкила, фенила и Het могут быть замещены 1 - 3 остатками из группы, включающей галоген, алкил с 1 - 6 атомами углерода, алкокси с 1 - 6 атомами углерода, трифторметил, гидроксил, циано, нитро, NR3R4, NR3COR4, CO2R3, 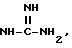 CONR3COR4, S(O)mR3, PO4(R3)3,
CONR3COR4, S(O)mR3, PO4(R3)3,
S(O)mNR3R4, COR3, где R3, R4 и m имеют вышеуказанное значение,
и их фармацевтически приемлемые соли и сольваты.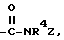
где R4 и Z имеют указанные в п. 1 значения.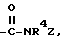 где R4 имеет указанное в п.1 значение, а Z - группу формулы
где R4 имеет указанное в п.1 значение, а Z - группу формулы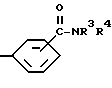
где R3 и R4 имеют указанные в п.1 значения.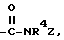 где R4 имеет указанное в п.1 значение, а Z - фенил(CR5R6)m, где R5 и R6 имеют указанное в п.1 значение.
где R4 имеет указанное в п.1 значение, а Z - фенил(CR5R6)m, где R5 и R6 имеют указанное в п.1 значение.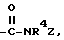 где R4 имеет указанное в п.1 значение, а Z - алкил с 1 - 6 атомами углерода, замещенный гидроксилом или группой NR3R4, где R3 и R4 имеют указанное в п.1 значение.
где R4 имеет указанное в п.1 значение, а Z - алкил с 1 - 6 атомами углерода, замещенный гидроксилом или группой NR3R4, где R3 и R4 имеют указанное в п.1 значение.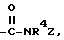 где R4 имеет указанное в п.1 значение, а Z - группу формулы
где R4 имеет указанное в п.1 значение, а Z - группу формулы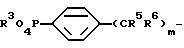
где R3, R5, R6 и m имеют указанные в п.1 значения.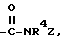 где R4 имеет указанное в п.1 значение, а Z - группу COалкил с 1 - 6 атомами углерода в алкильной части.
где R4 имеет указанное в п.1 значение, а Z - группу COалкил с 1 - 6 атомами углерода в алкильной части.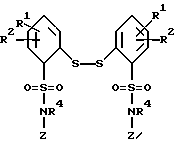
где R1, R2, R4 и Z имеют указанные в п.1 значения.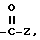 где Z имеет указанное в п.1 значение.
где Z имеет указанное в п.1 значение.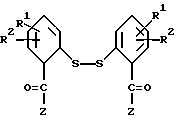
где R1, R2 и Z имеют указанное в п.1 значение.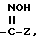 где Z имеет указанное в п.1 значение.
где Z имеет указанное в п.1 значение.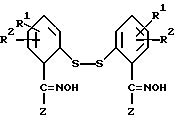
где R1, R2 и Z имеют указанное в п.1 значение.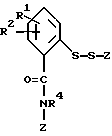
где R1, R2, R4 и Z имеют указанные в п.1 значения.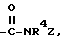 где R4 имеет указанное в п.1 значение, а Z - алкил с 1 - 6 атомами углерода, замещенный остатками
где R4 имеет указанное в п.1 значение, а Z - алкил с 1 - 6 атомами углерода, замещенный остатками 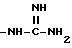 и CO2R3, где R3 имеет указанное в п.1 значение.
и CO2R3, где R3 имеет указанное в п.1 значение.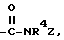 где R4 имеет указанное в п. 1 значение, а Z - циклоалкил(CR5R6)m с 3 - 6 атомами углерода в циклоалкильной части, причем циклоалкил может быть замещен.
где R4 имеет указанное в п. 1 значение, а Z - циклоалкил(CR5R6)m с 3 - 6 атомами углерода в циклоалкильной части, причем циклоалкил может быть замещен.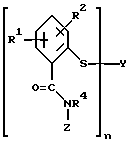
где R1 и R2 независимы друг от друга и означают водород, галоген, алкил с 1 - 6 атомами углерода, гидроксил, алкокси с 1 - 6 атомами углерода, карбоксил, алкоксикарбонил с 1 - 6 атомами углерода в алкоксильной части, группу NR3R4, где R3 и R4 независимы друг от друга и означают водород или алкил с 1 - 6 атомами углерода;
Y - водород, если n = 1, или простая связь, если n = 2;
Z - алкил с 1 - 6 атомами углерода, циклоалкил с 3 - 6 атомами углерода, незамещенные или замещенные 1 или 2 остатками из группы, включающей гидроксил, галоген, нитро, остаток NR3R4 и карбоксил, где R3 и R4 имеют вышеуказанные значения,
n - 1 или 2,
и фармацевтически приемлемые соли и сольваты.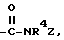 где R4 и Z имеют указанное в п.1 значение.
где R4 и Z имеют указанное в п.1 значение.
Приоритет по признакам:
05.08.1994 - R1, R2 независимы друг от друга и означают водород, галоген, алкил C1-C6, алкоксиC1-C6, гидроксил, карбоксил, группа NR3R4, где R3 означает водород или алкил C1-C6, а R4 - водород или алкил C1-C6; n = 1, 2; Y означает водород, если n равно 1, или простую связь, если n равно 2, X означает C(O)NR4Z, R4 - водород или алкил C1-C6, а Z означает фенил (CR5R6)m, m равно 0, а фенил замещен группой S(O)mNR3R4, где m равно 2, а R3 и R4 имеют вышеуказанные значения, фармацевтически приемлемые соли и сольваты;
01.06.1995 - все остальные значения радикалов R1, R2, X и Y.
Авторы
Даты
2000-09-20—Публикация
1995-07-11—Подача