Область техники, к которой относится изобретение
Изобретение относится к химическим технологиям и может быть использовано в металлургии для получения особо чистых редких тугоплавких металлов и в химической промышленности для получения высокочистых неметаллов указанного ряда.
Уровень техники
К тугоплавким редким металлам относятся переходные элементы IV-VII групп Периодической системы, у которых происходит достройка электронного d-уровня: титан Ti, цирконий Zr, ванадий V, ниобий Nb, тантал Та, молибден Мо, вольфрам W и рений Re. Известны промышленно освоенные способы получения редких тугоплавких металлов, например ниобия или титана, магниетермическим восстановлением из их высших хлоридов NbCl5, TiCl4 (см. А.Н.Зеликман. Металлургия тугоплавких редких металлов. М:
Металлургия, 1986 г., стр.387-403). Способы отличаются невысокой скоростью процесса. сложностью проведения операций и использованием дорогостоящего восстановителя.
Известно получение чистого вольфрама и молибдена из их галогенидов (паров фторидов или хлоридов) электролитическим восстановлением в расплавленных средах (см. А.Н.Зеликман. Металлургия редких металлов. М., Металлургия, 1980 г.). Известен способ электролитического получения титана из тетрахлорида титана (см. авторское свидетельство №1433081, опубл. 23.11.89 г.). Указанные способы также характеризуются низкой производительностью процесса и трудоемкостью его осуществления.
Известно получение мышьяка восстановлением водородом из хлорида AsCl3 (см. Химический энциклопедический словарь. М.: Советская энциклопедия, 1983 г., стр.357).
Известно получение кристаллического бора из его галогенидов BCl3 или BF3 разложением при t=1000-1500°C (см. Химическая энциклопедия, т.1, М., Советская энциклопедия, 1988 г., стр.300), характеризующееся сложностью осуществления высокотемпературных реакций.
Кроме того, чистота простого вещества, получаемого любым из вышеуказанных способов, определяется чистотой исходного соединения, в частности галогенида.
Наиболее производительными являются плазменные методы получения простых веществ, например способ производства кремния, применяемого в солнечных элементах (см. патент №1602391, МПК: С01В 33/02, опубл. 23.10.90 г.), включающий генерирование газовой плазмы при помощи электродов и подачу в плазму двуокиси кремния и твердой восстанавливающей добавки. Однако данным способом невозможно получить особо чистые вещества, т.к. поверхность электродов, находящихся в прямом контакте с химически активной реакционной средой под действием высоких температур и электрического разряда, подвергается эрозии. Микроскопические частицы материала электродов, попадая в плазменную дугу, загрязняют ее.
Уменьшение эрозии электродов за счет создания вокруг них защитной оболочки из аргона, служащего в качестве плазмообразующего газа, а также возможности выведения их из зоны реакции предложено в способе получения молибдена из молибденита (см. Пархоменко В.Д., Сорока. Плазма в химической технологии. Киев: Техника, 1986 г., стр.92-94). Однако и в нем не решена полностью проблема загрязнения готового продукта.
Известно получение бора из газообразного фторида BF3 или хлорида BCl3 в высокотемпературной плазме (см. Пархоменко В.Д., Сорока. Плазма в химической технологии. Киев: Техника, 1986 г., стр.114-118). Однако чистота бора, получаемого таким методом, принципиально ограничена чистотой исходного галида.
Таким образом, и в плазменных способах получения простых веществ чистота конечного продукта определяется чистотой исходных соединений. Однако редкие тугоплавкие металлы, кремний, бор, фосфор, сера, мышьяк распространены в природе в виде минералов, имеющих в основном сложный комплексный состав. Поэтому, как правило, необходимо осуществить целый ряд технологических процессов по обогащению, очистке от примесей и комплексной переработке природного рудного сырья для получения соединений высокой степени чистоты, предназначенных для дальнейшего восстановления из них простых веществ.
Наибольшее распространение в промышленной практике получил хлоридный способ комплексной переработки концентратов, включающий взаимодействие оксидов с элементным хлором и разделение смеси полученных газообразных хлоридов для последующего восстановления из них чистых веществ. В случае переработки сульфидных концентратов хлоридным методом предварительно осуществляют окисление сульфидов кислородом с целью получения оксидов вещества. Однако хлоридным способом невозможно добиться высокой степени очистки получаемых хлоридов от примесей, образующих с хлором летучие соединения, характеризующиеся близкими по значению параметрами, не позволяющими осуществить четкое разделение всех составляющих. Кроме того, способ многостадийный, сложный в аппаратурном оформлении из-за агрессивности хлора и характеризуется большим количеством вредных отходов.
Наиболее близким по наличию существенных признаков и решаемой задаче является способ проведения гомогенных и гетерогенных химических реакций с использованием плазмы, позволяющий получать особо чистые простые вещества (см. патент на изобретение №2200058, B01J 19/08, опубл. 2003.03.10), выбранный за прототип. Известно получение указанным способом поликристаллического кремния высокой степени чистоты, включающее непрерывную подачу реакционного газа, содержащего моносилан SiH4 и гелий, из источника реакционного газа, в котором поддерживается высокое давление, в вакуумную реакционную камеру. Образованный на границе входного в камеру отверстия перепад давления позволяет получить расширение реакционного газа или сверхзвуковой поток, имеющий на входе в своей центральной части зону разрежения. Сверхзвуковой поток активируют воздействием электронного пучка, введенного в упомянутую зону разрежения, с образованием электронно-пучковой плазмы. Выделение чистого кремния происходит на поверхности металлической подложки, помещенной в нагреваемую цилиндрическую кварцевую трубу, ось которой совпадает с осью потока реакционного газа. Отслаивание полученных слоев кремния с подложки осуществляют посредством резкого охлаждения ленты подложки на выходе из реакционной камеры.
Способ характеризуется низкими энергозатратами и при этом имеет высокую производительность, что обусловлено высокими скоростями протекания химических реакций, и тем, что электронно-пучковая активация обеспечивает более высокие, чем в разрядной плазме, скорости диссоциации молекул на радикалы. Кроме того, отсутствие нагреваемых деталей и то, что радикалы образуются внутри газовой струи, препятствующей проникновению молекул фонового газа камеры, обуславливает абсолютную чистоту осуществляемых реакций. Таким образом, чистота получаемого вещества напрямую зависит от чистоты реакционного газа. В качестве реакционного газа в известном способе используют моносилан, являющийся сложным в получении и дорогостоящим (например, см. патент №2050320, МПК: С01В 33/04, опубл. 20.12.1995 г., в котором приведен способ получения моносилана, используемого как сырье для производства поликристаллического кремния высокой чистоты). Данный факт является причиной использования моносилана предпочтительно для получения небольшого количества кремния, например для нанесения тонкопленочных покрытий.
Обобщенный способ получения кремния, объединяющий процессы получения моносилана как исходного соединения и его плазменного восстановления, несмотря на высокую производительность последнего, является достаточно сложным и взрывоопасным, многостадийным и продолжительным и как следствие дорогостоящим.
Раскрытие изобретения
Заявляемым изобретением решается задача упрощения и удешевления производства высокочистых веществ, среди которых бор, фосфор, кремний, мышьяк, сера и редкие тугоплавкие металлы, за счет возможности использования различного исходного сырья, в том числе невысокой степени чистоты, упрощения получения из него высокочистых соединений для последующего восстановления из них простых веществ и создания круговорота используемых химических реагентов.
Поставленная задача решена за счет того, что в способе получения вещества, выбранного из ряда редких тугоплавких металлов или из ряда неметаллов: кремний, бор. фосфор, мышьяк, сера, включающем подачу реакционного газа в виде соединения получаемого вещества из его источника в вакуумную реакционную камеру, формирование в ней сверхзвукового потока подаваемого газа, активирование упомянутого потока воздействием на него электронным пучком с образованием струи электронно-пучковой плазмы, разложение реакционного газа в струе электронно-пучковой плазмы с получением и сбором чистого вещества на возобновляемой подложке, согласно заявляемому изобретению в качестве реакционного газа используют фторид выбранного вещества, выделенный из смеси газов, полученной в результате фторирования соединения выбранного вещества в виде его оксида или сульфида элементным фтором, при разложении упомянутого фторида в струе электронно-пучковой плазмы из объема реакционной камеры удаляют смесь газообразных продуктов разложения фторида, выделяют из них элементный фтор и направляют его на фторирование оксида или сульфида выбранного вещества.
Способ позволяет использовать любое исходное сырье, в том числе дешевое загрязненное примесями, и уже на стадии вскрытия извлекать из него вещества в виде высокочистых фторидов и использовать последние в качестве исходных для дальнейшего получения простых веществ. Высшие фториды характеризуются устойчивостью и хорошо различимыми физическими свойствами (атомной массой, температурой возгонки) от аналогичных характеристик фторидов основных сопутствующих указанным веществам примесей, что позволяет четко выделить фторид выбранного вещества из состава получаемой при фторировании исходного сырья газовой смеси. Указанный результат достигается благодаря использованию в качестве окислителя элементного фтора. Однако фтор имеет очень большую реакционную способность, настолько, что практически не встречается в элементарном состоянии. Элементный фтор можно получить и, сконденсировав жидким азотом, хранить или транспортировать в баллонах, однако это сопряжено с большими трудностями и опасностью.
Из уровня техники известно применение элементного фтора для фторирования оксида циркония (см. А.Н.Зеликман. Металлургия тугоплавких редких металлов. М., Металлургия, 1986 г., стр.414-415). Полученный в результате фторирования тетрафторид циркония восстанавливают кальцием до чистого циркония. Однако при этом фтор остается связанным кальцием в соединении дифторида кальция. Фтор является дорогостоящим окислителем и его получение отдельным производством с доставкой к месту использования, специально для введения в процесс, как указывалось ранее, сопряжено с большими трудностями.
В заявляемом решении, в отличие от указанного способа, осуществляют круговорот элементного фтора, т.е. не только расходуют фтор, но и получают его в процессе производства, причем процесс получения фтора совмещен с процессом получения чистого вещества в струе электронно-пучковой плазмы. Элементный фтор выделяют из предварительно удаленных из реакционной камеры газообразных продуктов разложения фторида и используют его снова для фторирования оксидов (или сульфидов). За счет круговорота окислителя элементного фтора технология становится практически безреагентной, исключается тепловое и химическое загрязнение окружающей среды.
Кроме того, использование в качестве окислителя элементного фтора, а не его соединений, позволило исключить образование дополнительных побочных продуктов реакции фторирования, являющихся отходами производства, что также направлено на упрощение производства.
Заявляемый способ применим ко всем указанным металлам и неметаллам, что обусловлено схожестью (однотипностью) их поведения со фтором. Все перечисленные вещества образуют со фтором летучие фториды, имеющие невысокие температуры плавления.
В конкретном случае реализации способа разделение полученной в результате фторирования оксид- или сульфидсодержащего сырья смеси газов и выделение фторида выбранного вещества можно осуществить методом конденсации, основанном на разности температур кипения (конденсации) фторидов.
Элементный фтор также может быть выделен из смеси газообразных продуктов разложения фторида методом конденсации.
Химическая реакция разложения в струе плазмы протекает с очень большой скоростью, поэтому фторид не успевает полностью разложиться и в смеси газообразных продуктов, удаляемой из вакуумной реакционной камеры, будут содержаться непрореагировавшие фториды вещества. С целью повышения выхода конечного продукта и более полного использования реакционного газа непрореагировавшие фториды выделяют и возвращают в источник реакционного газа.
Сбор чистого вещества на возобновляемой подложке целесообразно осуществлять при температуре 18-150°С. Снижение температуры ниже 18°С ведет к замедлению скорости осаждения чистого вещества, превышение температурой 150°С способствует началу структурных изменений вещества.
Слой выделившегося на подложке чистого вещества периодически удаляют, стряхивая его посредством электрического удара по подложке.
Предпочтительным является использование в качестве исходного оксид- или сульфидсодержащего сырья природных рудных концентратов. Например, рутила, содержащего 97% масс. TiO2, кварцита -97% масс.SiO2, для получения ниобия, тантала и титана - лопарита и т.д. (остальная доля масс. - это примеси в виде оксидов железа, алюминия, магния и проч.) Концентраты являются доступным и дешевым сырьем, а проблема выделения нужного соединения и его очистки от сопутствующих примесей решена заявляемым способом. Зачастую получить нужное чистое соединение проще, выполнив фторирование исходного сырья.
Фторирование твердых соединений кремния, фосфора, мышьяка, серы и редких тугоплавких металлов можно осуществить в пламенных реакторах шахтного типа распылением измельченного в порошок сырья в струе элементного фтора. Реакция взаимодействия происходит при простом смешивании реагентов при комнатной температуре. При этом примеси, образующие с фтором твердые нелетучие фториды, включая кальций, алюминий, железо, удаляются в виде образующегося при сжигании огарка.
Фторирование оксида бора осуществляют барботированием элементного фтора через расплав оксида.
Фторирование газообразных оксидов фосфора и серы осуществляют в газовой горелке, смешивая их с элементным фтором.
Несмотря на высокую реактивность и токсичность, фтор характеризуется низким коррозионным воздействием на аппаратуру и коммуникации, некоторые металлы (например, Al, Cu, Fe), покрываясь пленкой фторида, перестают взаимодействовать со фтором. При правильной организации проведения фторидных технологических процессов можно эксплуатировать оборудование без капитальных ремонтов в течение 10 и более лет.
Осуществление изобретения
Пример 1. Получение высокочистого порошка поликристаллического кремния
Способ был осуществлен в лабораторных условиях с применением струйного источника радикалов (СИР), защищенного патентом №2200058.
На чертеже приведена структурная схема технологического процесса получения кремния.
Осуществляют фторирование кварцевого песка, содержащего 95-97% диоксида кремния, элементным фтором в пламенном реакторе шахтного типа. Для этого в форсунку реактора 1 специальной фтородувкой подают элементный фтор, являющийся самым сильным из простых веществ окислителем, туда же подают предварительно измельченный в порошок кварцевый песок. Реакции взаимодействия с фтором протекают на поверхности соприкосновения твердой и газовой фаз, чем выше удельная поверхность соприкосновения фтора и твердой фазы, тем выше скорость реакции, поэтому осуществляют распыление порошка кварцита в струе фтора. Газовзвесь вспыхивает без какого-либо подогрева и сгорает в факеле. При этом осуществляется реакция:
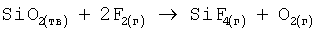
В результате фторирования образуется газовая фаза, содержащая тетрафторид кремния и кислород. Примеси кальция, алюминия, железа и др., на долю которых приходится 3-5% масс. концентрата, образуют при взаимодействии с элементным фтором нелетучие соединения (CaF2, AlF3, FeF3 и др.), которые удаляют в виде твердого огарка из реактора 2 выгрузки огарка, размещенного под реактором 1, и используют, например, в качестве фторидных флюсов в цветной или черной металлургии.
Газовую смесь, содержащую тетрафторид кремния и кислород, охлаждают в охладителе 3, пропускают через фильтр 4 тонкой очистки, позволяющий отделить уносимую газовой фазой пыль, содержащую частицы твердых фторидов и непрореагировавших оксидов. Затем пропускают смесь через установку 5 конденсации, содержащую трубчатый конденсатор, где, охлаждаясь до температуры -86°С, тетрафторид кремния конденсируется и выводится из состава смеси. Установка 5 может включать компрессор, предварительно осуществляющий сжатие газов с целью увеличения температуры конденсации тетрафторида. Газообразный кислород через систему санитарной очистки сбрасывают в атмосферу.
Сжиженный трифторид кремния испаряют в испарителе 6 при комнатной температуре и подают в источник 7 реакционного газа и далее в вакуумную реакционную камеру 8. В камере размещена электронная пушка 9.
На границе входного в камеру 8 отверстия образуется перепад давления, позволяющий получить расширение реакционного газа или сверхзвуковой поток 10, имеющий на входе в своей центральной части зону разряжения. Далее активируют сверхзвуковой поток воздействием электронного пучка 11, введенного в упомянутую зону разрежения с образованием электронно-пучковой плазмы 12. Тетрафторид кремния разлагается в плазме на радикалы, которые постепенно восстанавливаются до чистого кремния и фтора. Чистый кремний выделяется на возобновляемой подложке 13. Чтобы удалить образовавшийся на поверхности подложки слой 14 чистого кремния, на подложку 13 воздействуют электрическим ударом, подложка «вздрагивает» и кремний ссыпается в бункер 15.
Выделившуюся в объем реакционной камеры 8 в результате реакции газовую смесь, включающую элементный фтор и непрореагировавшие фториды, удаляют из объема камеры и осуществляют ее разделение на установке 16 конденсации. Для этого охлаждают газовую смесь до t=-90-110°С, либо сначала компремируют смесь до 25 атм., после чего охлаждают до t=-60°С, при этом непрореагировавшие высшие фториды переходят в жидкое состояние, выводятся и направляются далее в испаритель 6 для повторной подачи на плазменное восстановление. Газообразный элементный фтор направляют в пламенный реактор 1 для фторирования кварцевого песка.
По результатам проведенного исследования полученный чистый поликристаллический кремний характеризуется очень незначительным количеством микропримесей: так наличие примеси по бору составило 10-14 атомов/см3.
Фоточувствительность ФЭП, изготовленных из полученного кремния, составила 1100 единиц (для сравнения фоточувствительность ФЭП, изготовленных из кремния, полученного из моносилана способом-прототипом, составляет 1000 ед.).
Пример.2 Получение высокочистых редких металлов ниобия, тантала и титана из лопаритовых концентратов
Рудный концентрат, поступающий в переработку, содержит 8.5-9% (Nb2O5 и Та2O5), 34-36% TiO2, 6-8% СаО, а также оксиды Al, Fe, Si, В, Се, К и др.
Фторирование оксидов элементным фтором осуществляют в пламенном реакторе шахтного типа аналогично примеру 1. При этом происходят реакции:

В результате фторирования образуется газовая фаза, содержащая TiF4, NbF5, TaF5, кислород и, возможно, другие летучие фториды неуказанных примесей, например кремния, бора и др., и нелетучий остаток примесей, включающий фторидные соединения алюминия, кальция и железа (CaF2, AlF3, FeF3). Твердый огарок примесей удаляют для последующего использования, а газовую смесь охлаждают, пропускают через фильтр тонкой очистки и разделяют на индивидуальные компоненты, используя различия температур кипения составляющих газов на установке конденсации:
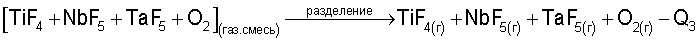
Значительные различия температур кипения (или иначе конденсации) позволяют четко отделить фториды титана, тантала и ниобия от летучих фторидов примесей кремния, бора, фосфора и др. Таким образом, применение элементного фтора позволяет уже на стадии вскрытия концентрата получать фториды в высокочистом виде (более 99,99% масс.) и использовать их в качестве исходных соединений для дальнейшего восстановления из них чистых веществ.
Выделенный очищенный тетрафторид титана испаряют и направляют в источник реакционного газа для плазменного разложения, осуществляемого аналогично примеру 1. В результате получают высокочистый порошок металлического титана с содержанием не менее 99.99% масс. Элементный фтор выделяют и направляют на операцию фторирования исходного сырья. Фториды тантала и ниобия подвергают индивидуальному восстановлению аналогичным образом.
Пример 3. Получение высокочистого порошка бора из ангидрида бора В2O3. Порошок ангидрида бора загружают в герметичный реактор и плавят при t=450-475°C. Под слой расплавленного В2O3 подают через барботер элементный фтор и осуществляют процесс фторирования по реакции:
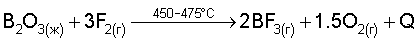
Образовавшуюся газовую смесь подают в трубчатый конденсатор, охлаждаемый жидким азотом, и при t=-93-100°С сжижают трифторид бора, который собирают в охлаждаемый герметичный баллон. Несконденсированный газообразный кислород сбрасывают через аппарат санитарной очистки в атмосферу. Сжиженный трифторид бора испаряют из баллона при комнатной температуре и подают в источник реакционного газа и далее в вакуумную реакционную камеру. Дальнейшее разложение фторида бора в СИР с выделением чистого порошка бора на возобновляемой подложке осуществляется аналогично примеру 1.
Пример 4. Получение высокочистого порошка фосфора
Процесс отличается от вышеприведенного примера получением фторида фосфора. Исходное сырье в виде порошка оксида фосфора Р4O10 плавят при t=24-26°С и испаряют при 175-200°С. Получаемые пары Р4O10 смешивают в горелке с элементным фтором и осуществляют реакцию фторирования:
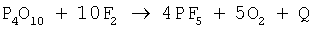
Аналогичным образом может быть осуществлено в газовой горелке фторирование оксида серы согласно реакции: SO2+3F2→SF6+O2↑
Пример 5. Получение молибдена и рения из сульфидов
Предварительно измельченный в порошок рудный концентрат, например молибденит, включающий сульфиды молибдена и рения, фторируют элементным фтором в химическом реакторе факельного типа аналогично процессу, описанному в примерах 1 и 2, при этом происходят реакции окисления:
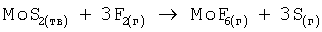
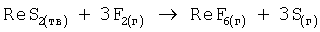
Выделение фторидов из смесей газов и дальнейшее восстановление из них чистых веществ осуществляют аналогично вышеприведенным с получением в конечном итоге высокочистого порошка молибдена и рения.
В результате применения заявляемого способа для получения указанных металлов из их сульфидов одновременно получают еще один товарный продукт - чистую серу.
Получение высокочистого мышьяка осуществляют, проведя фторирование, например, его оксида As2O3 или сульфидсодержащего концентрата - аурипигмента - As2S3 элементным фтором, процессы выделения фторидов и их дальнейшее разложение в струе электронно-пучковой плазмы осуществляют аналогично приведенным примерам.
Технологический процесс с использованием элементного фтора может быть осуществлен на оборудовании предприятий ядерного топливного цикла, где также отработано строгое обеспечение санитарных норм. Использование в качестве основного реагента рециркулирующего элементного фтора приводит к практически полному исключению образования и сброса в окружающую среду технологических отходов. Высокое тепловыделение и скорость фторирования, полное использование фторирующего реагента, отсутствие газообразных и жидких выбросов обуславливают высокую производительность технологических процессов и труда, и как следствие, высокую рентабельность производства.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ВЕЩЕСТВА, ВЫБРАННОГО ИЗ РЯДА: БОР, ФОСФОР, КРЕМНИЙ И РЕДКИЕ ТУГОПЛАВКИЕ МЕТАЛЛЫ (ВАРИАНТЫ) | 2005 |
|
RU2298589C2 |
| СПОСОБ ПРОИЗВОДСТВА ЭНЕРГИИ | 2005 |
|
RU2291349C2 |
| СПОСОБ ПОЛУЧЕНИЯ ВЫСОКОЧИСТОГО ПОРОШКА КРЕМНИЯ ИЗ ТЕТРАФТОРИДА КРЕМНИЯ С ОДНОВРЕМЕННЫМ ПОЛУЧЕНИЕМ ЭЛЕМЕНТНОГО ФТОРА, СПОСОБ ОТДЕЛЕНИЯ КРЕМНИЯ ОТ РАСПЛАВА СОЛЕЙ, ПОЛУЧЕННЫЕ ВЫШЕУКАЗАННЫМ СПОСОБОМ ПОРОШОК КРЕМНИЯ И ЭЛЕМЕНТНЫЙ ФТОР И СПОСОБ ПОЛУЧЕНИЯ ТЕТРАФТОРИДА КРЕМНИЯ | 2004 |
|
RU2272785C1 |
| СПОСОБ ФТОРИРОВАНИЯ ТВЕРДОГО МИНЕРАЛЬНОГО СЫРЬЯ И РЕАКТОР ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2006 |
|
RU2329949C2 |
| СПОСОБ ПОЛУЧЕНИЯ ТЕТРАФТОРИДА КРЕМНИЯ, СПОСОБ ОТДЕЛЕНИЯ ТЕТРАФТОРИДА КРЕМНИЯ ОТ КИСЛОРОДА И ВЫСОКОЛЕТУЧИХ ФТОРИДОВ ПРИМЕСЕЙ, СПОСОБ ПОЛУЧЕНИЯ ПОРОШКА КРЕМНИЯ ИЗ ТЕТРАФТОРИДА КРЕМНИЯ | 2003 |
|
RU2324648C2 |
| СПОСОБ ВЫДЕЛЕНИЯ ТЕТРАФТОРИДА КРЕМНИЯ ИЗ ГАЗОВОЙ СМЕСИ И УСТАНОВКА ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2006 |
|
RU2348581C2 |
| СПОСОБ ПОЛУЧЕНИЯ ТЕТРАФТОРИДА КРЕМНИЯ И УСТРОЙСТВО ДЛЯ ЕГО РЕАЛИЗАЦИИ | 2010 |
|
RU2454366C2 |
| НЕОРГАНИЧЕСКИЙ ПИГМЕНТ НА ОСНОВЕ СУЛЬФИДА МЕТАЛЛА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1997 |
|
RU2108355C1 |
| СПОСОБ ПОЛУЧЕНИЯ ИЗОТРОПНОГО ОПТИЧЕСКИ ПРОЗРАЧНОГО БЕЗГИДРОКСИЛЬНОГО КВАРЦЕВОГО СТЕКЛА | 1993 |
|
RU2080308C1 |
| СПОСОБ ПОЛУЧЕНИЯ ТЕТРАФТОРИДА КРЕМНИЯ | 2001 |
|
RU2182558C1 |
Изобретение предназначено для применения в металлургии и химической промышленности для получения высокочистых редких тугоплавких металлов и неметаллов указанного ряда. Способ включает фторирование оксида или сульфида выбранного вещества элементным фтором, выделение из полученной смеси газов фторида выбранного вещества и дальнейшее разложение полученного высокочистого фторида в струе электронно-пучковой плазмы с выделением чистого вещества на возобновляемой подложке. При этом из объема реакционной камеры удаляют газообразные продукты разложения фторида, выделяют из них элементный фтор и направляют его на операцию фторирования оксидов или сульфидов. Техническим результатом является то, что способ позволяет использовать любое исходное оксид- или сульфидсодержащее сырье, в том числе дешевое загрязненное примесями, например природные рудные концентраты, уже на стадии вскрытия извлекать из него вещества в виде высокочистых фторидов и использовать последние в качестве исходных соединений для дальнейшего получения простых веществ. За счет круговорота окислителя - фтора - технология становится практически безреагентной, исключается тепловое и химическое загрязнение окружающей среды. 9 з.п. ф-лы, 1 ил.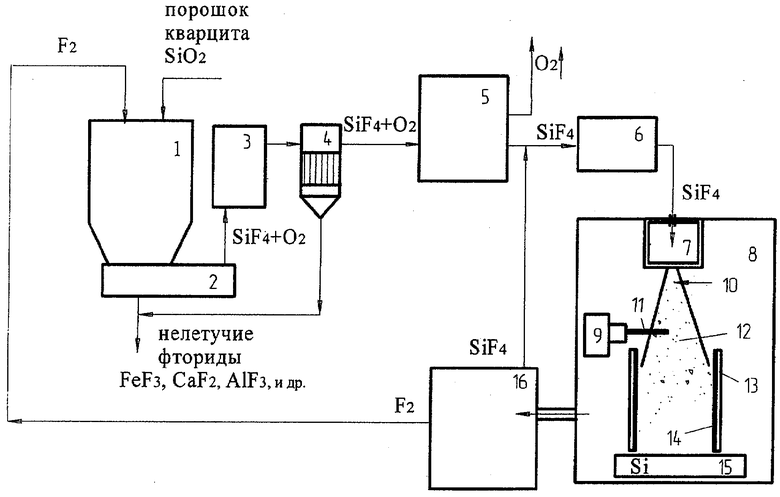
| СПОСОБ ПРОВЕДЕНИЯ ГОМОГЕННЫХ И ГЕТЕРОГЕННЫХ ХИМИЧЕСКИХ РЕАКЦИЙ С ИСПОЛЬЗОВАНИЕМ ПЛАЗМЫ | 2002 |
|
RU2200058C1 |
| СПОСОБ НАНЕСЕНИЯ ПЛЕНОК АМОРФНОГО КРЕМНИЯ И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2000 |
|
RU2188878C2 |
| SU 904223 A1, 20.07.1999 | |||
| Способ правки изразцов или других керамических изделий | 1960 |
|
SU143701A1 |
| Машина для разделения сыпучих материалов и размещения их в приемники | 0 |
|
SU82A1 |
| УСТРОЙСТВО, ВЫПОЛНЕННОЕ С ВОЗМОЖНОСТЬЮ ДЕТЕКТИРОВАНИЯ ФИЗИЧЕСКОЙ ВЕЛИЧИНЫ ДВИЖУЩЕЙСЯ ТЕКУЧЕЙ СРЕДЫ, И СООТВЕТСТВЕННЫЙ СПОСОБ | 2010 |
|
RU2555206C2 |
Авторы
Даты
2007-05-10—Публикация
2005-07-21—Подача