Изобретение относится к медицине и ветеринарии и может быть использовано при дискэлектрофоретическом разделении белка кишечного сока на фракции в полиакриламидном геле.
Электрофорез широко применяют в исследовательской и клинико-лабораторной практике. Посредством его выявляют и выделяют белки, липопротеиды, гликопротеиды, нуклеиновые кислоты. Подавляющее большинство исследований с помощью электрофореза позволяет получить представление о биохимической и физиологической роли тех или иных биологических соединений, или их фракций, установить связи с аномальными явлениями в живом организме.
В медико-биологических исследованиях применяют множество вариантов двух главных модификаций электрофоретического метода электрофореза в свободной жидкости (свободно-проточный электрофорез) и зонального электрофореза (зонный электрофорез, или электрофорез на инертных носителях).
Однако надо отметить, что свободно-проточный электрофорез (по Тизелису) не вошел в повседневную практическую работу клинико-диагностических лабораторий. Основным недостатком электрофореза в свободной жидкости является ее тепловое движение, мешающее четкому разделению фракций и размывающее границы зон (В.М.Холод, 1983).
Для разделения белков плазмы крови широкое распространение получил зонный электрофорез на поддерживающих средах-носителях. Зонный электрофорез можно осуществлять с использованием смоченных буферным раствором (рН-8,6) полосок хроматографической бумаги, ацетататцеллюлозной пленки, агарового геля и других носителей.
В качестве инертных носителей используется фильтровальная бумага; картон из фильтровальной бумаги; асбестовое волокно; пластины; селикогель; стеклянный порошок; целлюлоза; целлюлозные нити; ацетилцеллюлоза; агаровый, агарозный, крахмальный и полиакриламидный гели. Наиболее эффективным методом разделения белков считают метод дискэлектрофореза в полиакриламидном геле, где можно получить большее количество белковых фракций нежели при использовании других перечисленных выше способов. Однако разделить белки кишечного сока собак на фракции на указанных носителях не представляется возможным, так как на бумагу надо наносить 1 мл кишечного сока, что не позволит провести разделение последнего на фракции.
Известен способ разделения на фракции белков коровьего молока. При данном методе молоко обезжиривают, центрифугируют, по каплям вносят 1 мл 10% водного раствора СН3СООН. Казеин, выпавший в осадок, отделяют центрифугированием (10 мин при 3000 об/мин) от сыворотки молока. Сыворотка молока фильтруется через бумажный фильтр и используется для электрофореза.
Для электрофоретического разделения белков сыворотки молока применяют веронал - щелочной буфер рН-8,6; ширина бумажной ленты 3 см; сила тока 0,2 мА на 1 см ширины бумажной ленты, время разгонки - 7 часов. Количество наносимой на одну бумажную ленту сыворотки молока 0,06 мл (П.Ф.Дьяченко, Е.А.Жданова, 1962).
Недостатком данного метода является то, что при данной методике можно провести разделение белков только сыворотки крови и обезжиренного молока.
Разделить же белки кишечного сока на фракции не представляется возможным.
Известен способ электрофоретического разделения на фракции казеина (Дьяченко П.Ф., Жданова Е.А., 1962). Для этого центрифугируют молоко, осаждают казеин. Отделенный от сыворотки казеин трижды промывается дистиллированной водой. К промытому казеину приливается вероналовый буфер до общего объема 10 мл. При помешивании стеклянной палочкой казеин растворяется в буферном растворе. После чего центрифугируется 10 минут при 3000 об/мин. После центрифугирования на поверхности раствора появляется тонкая, белая пленка, состоящая из остатков жира, которую осторожно удаляют с помощью водоструйного насоса.
Основные условия для электрофоретического разделения на фракции казеина: веронал - щелочной буфер рН - 8,6; ширина бумажной ленты - 3 см; напряжение тока 4 V на 1 см длины бумажной ленты; время разгонки 20 часов; количество наносимого на бумажную ленту казеина - 0,02 мл; быстрая хроматографическая фильтровальная бумага. Раствор казеина наносят на бумажные ленты, смоченные буферным раствором и отжатые между листами фильтровальной бумаги.
Высушивание фореграмм проводится в сушильном шкафу при температуре 100-105°С в течение 30 минут, после чего окрашиваются красителем в течении 20 минут.
Не связанная с белком краска удаляется прополаскиванием фореграмм в 1% водном растворе СН3СООН, отмывание бумажных лент продолжается до тех пор, пока фон фореграмм не станет белым, а раствор уксусной кислоты перестанет окрашиваться в желтый цвет.
Элюирование белковых фракций молока и казеина проводят по общепринятым методам.
Недостатком данной методики электрофореза является то, что при данной методике можно разделить на фракции казеин молока, но невозможно провести разделение белков кишечного сока на фракции.
Известен способ электрофоретического разделения белков спермы и секретов половых желез и спермы в агаровом геле (В.А.Яблонский, 1986). Секреты половых желез получают из половых органов свежеубитых животных.
Перед началом разгонки в исследуемом материале определяют содержимое общего белка и доводят до 1,75-2,0%, разбавляя буферным раствором.
Агар-агар, толщиной 4-5 мм, наносят на пластинки из стекла размером 21×16 см, которые перед нанесением агар-агара тщательно моют горячей водой с мылом и обезжиривают спирт эфирной смесью.
В агар-агаре готовят конические желобки, отступая примерно 8 см от одного края стекла. Длина желобка 0,8-1,0 см, ширина сверху 2,5-3,0 мм, расстояние между желобками 0,6-0,8 см.
Для нанесения исследуемого материала на пластинки пользуются эритроцитарными меланжерами, набирая материал до условной метки 0,75-1,0, выдувают материал медленно во избежание разбрызгивания его за пределы желобков.
Стеклянные пластинки кладут в камеру, соединяя бумажными мостиками, которые погружаются в буферные растворы. Напряжение электрического тока на концах пластины в 1 час 50 В, а затем 75 В. Длительность электрофореза 3,5-5,0 часов в зависимости от материала и буфера.
Окраску, фиксирование и элюирование проводят по общепринятой методике.
Недостатком данной методики электрофореза является то, что при данной методике можно разделить на фракции белки спермы, но невозможно провести разделение белков кишечного сока на фракции.
Известен способ разделения белков на фракции, используя электрофорез в полиакриламидном геле (Ю.Я.Гофман, 1965; Э.К.Мухаметжанов, 1967). Этот метод нашел самое широкое применение в биохимических и научных исследованиях. Он используется для изучения белков, липо- и гликопротеинов, пептидов, гормонов, ферментов и нуклеиновых кислот.
Этот метод с успехом используют для анализа чистоты препаратов белков и ферментов, оценки метода экстракции и очистки, определения относительной концентрации белков, обнаружения антигенов, при определении молекулярной массы молекул, в серологических, иммунологических и других исследованиях.
При этом способе колонку небольшого сечения (около 1 см2) заполняют буферным раствором, содержащим растворенный мономер (акриламид), небольшое количество вещества-сшивателя (бис-N-метиленметакриламида) и вещество - инициатор полимеризации. Через некоторое время при комнатной температуре в колонке образуется однородный гель. Если с помощью электрофореза в свободной жидкости по Тизелиусу в сыворотке крови обнаруживают 5 белковых фракций, то при электрофоретическом разделении белков сыворотки крови их насчитывают не менее 25. Разрешающая способность электрофореза в полиакриламидном геле значительно повышается при использовании в качестве носителя системы гелей (обычно двух - «рабочего», мелкопористого и непосредственно над ним «формирующего», крупнопористого). Кроме степени пористости эти гели резко различаются по величине рН и молярности буферных растворов, в которых они полимеризуются. Такой электрофорез называют ступенчатым или дискэлектрофорезом.
Из всех модификаций метода электрофореза наиболее простой считают методику дифференциального электрофореза, где используется двух- и более компонентный разделяющий гель с различной конфигурацией по акриламиду. При использовании геля с двумя и более размерами пор эффект молекулярной ультрафильтрации усиливается.
Методика очень эффективна для разделения на фракции белков сыворотки крови и других биологических жидкостей, количество необходимой сыворотки 0,01-0,015 мл. Однако придерживаясь указанной выше дозы, в точности выдерживая методику подготовки и разделения белков, кишечный сок собак разделить на белковые фракции не удается.
Цель изобретения - разработать способ разделения белков кишечного сока у собак на фракции методом дискэлектрофореза в полиакриламидном геле.
Дли достижения поставленного технического результата предлагается в способе разделения белков на фракции методом дискэлектрофореза в полиакриламидном геле после операции полимеризации крупнозернистого геля и отсасывания воды в него наслаивать 0,9-1,1 мл кишечного сока, разделение кишечного сока проводить при температуре минус 40 - минус 49°С в морозильной камере с регулятором температуры.
Проведенные исследования позволили установить, что температура тающего льда или снега, используемая для охлаждения, неэффективна. Одновременно было установлено, что рекомендуемое для анализа количество 0,01-0,015 мл непригодно для разделения белков кишечного сока. При зарядке такого количества кишечного сока положительный результат не получают.
Для качественного разделения белка кишечного сока наиболее оптимальное количество его 0,9-1,0 мл, так как белков в кишечном соке предельно мало. Разделение проводят при той же силе тока и напряжении. Разделение белков кишечного сока необходимо проводить в морозильной камере холодильника с регулятором охлаждения.
Оптимальная температура для разделения гомогенизированного кишечного сока составляет минус 40-49°С.
Пример выполнения. В опыт ставили собак на шесть часов, в течение которых исследовали уровень секреции кишечного сока в разрезе по часам. В гомогенизированном кишечном соке собак исследовали ферменты: липазу, пептидазу, энтерокиназу, щелочную фосфатазу и проводили разделение белков кишечного сока на фракции методом дискэлектрофореза в полиакриламидном геле.
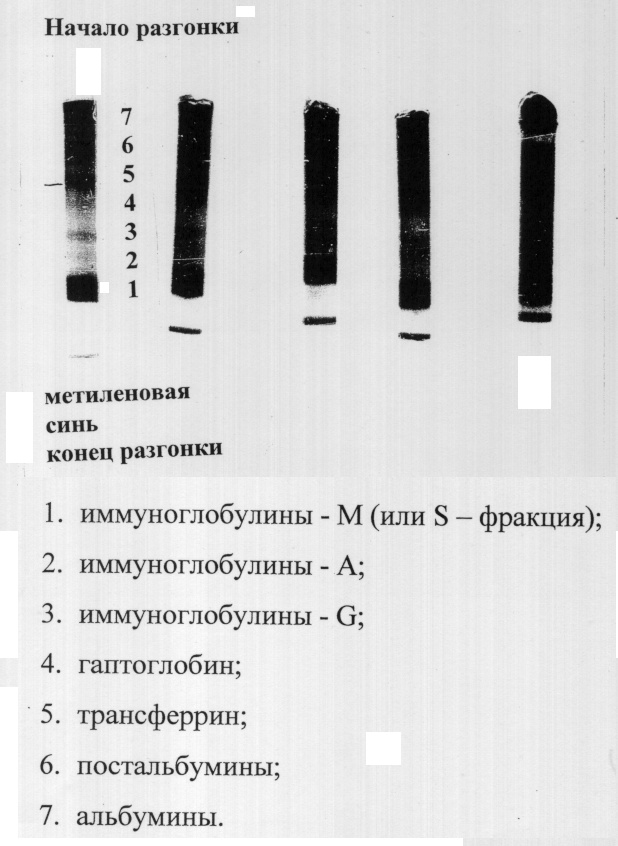
На чертеже приведен пример разгонки методом дискэлектрофореза гомогенизированного кишечного сока собаки, полученным от собаки Пальма с изолированной петлей тонкого кишечного сока по Тири-Велла (1887).
Способ разделения белков кишечного сока на фракции осуществляют следующим образом.
Гель полимеризуется в стеклянных трубках длинной 12 см и внутренним диаметром 6 мм.
Трубки помещают в штативе строго вертикально, нижнюю часть их устраивают в резиновые пробки или прижимают к слою пластилина для обеспечения водонепроницаемости. С помощью шприца на 5-10 мл до деления 1 осторожно наслаивают мелкопористый гель до отметки, аккуратно покрывают слоем воды толщиной 2-3 мм и оставляют на 40-60 минут, в течение которых протекает полимеризация мелкопористых гелей. После чего воду отсасывают, промывают поверхность крупнозернистым гелем и заливают до метки концентрирующий слой (гель-прокладку) крупнопористого геля. Крупнопористый гель покрывают слоем воды, и в течение 20-30 минут происходит полимеризация геля при интенсивном освещении лампами дневного света.
После чего с верхнего слоя шприцом отсасывают воду и до верхнего края трубки заливают пробу гомогенизированного кишечного сока в объеме 0,9-1,1 мл (в известном способе заливается проба сыворотки крови объемом 0,01-0,015 мл, растворенной в мелкопористом геле).
Снова наслаивают воду и гель ставят на полимеризацию в течение 20-30 минут.
Трубки с заполимеризировавшимся гелем вставляют в верхнюю электрозарядную камеру так, чтобы край трубки выступал внутрь камеры на 1,5-2,0 см, после чего заливают в верхнюю и нижнюю кюветы электродный буфер, предварительно охлажденный до 4°С.
Подготовленную камеру подключают к источнику постоянного тока, электрофорез начинают при силе тока 2 мА, на трубку до вхождения белка в разделительный гель, после чего сила тока увеличивается до 4 мА.
Электрофорез проводят до тех пор, пока мителеновая синь не достигнет отметки 1! см. После разгонки трубки вынимают из аппарата и помещают в ледяную воду на 15-20 минут. Гели извлекают из стеклянных трубок, обводя их тонкой металлической иглой по внутренней поверхности трубки.
Полиакриламидные столбики окрашивают раствором 0,5% амидошварца в 7% уксусной кислоте в течение 30 минут при комнатной температуре. Отмывают от избытка краски в растворе 3% уксусной кислоты путем многократной смены раствора до тех пор, пока не перестанет окрашиваться.
Оценку, элюирование электрофореграмм производят по следующей методике. Электрофореграмму разделяют по видимым границам раздела по числу окрашенных пятен (фракции). Каждый отрезок помещают в отдельную пробирку и заливают 0,01 н. раствором едкого натра по 10 мл экстрагирующего раствора. В качестве контрольного участка служит отрезок электрофореграммы, не содержащий белка. После фотометрирования полученных экстрактов в фотоэлектрокалориметре складывают найденные для каждой электрофореграммы величины экстинкции (по указаниям прибора), сумму этих величин принимают за 100 и вычисляют, какой процент по отношению к ней составляет экстинкция пятна из фракций по отношению к электрофореграмме. Существенные отличительные признаки:
1). Пробу гомогенизированного кишечного сока для исследования берут в объеме 0,9-1.1 мл;
2). Разделение белков кишечного сока на фракции проводят при температуре минус 40-49°С.
Указанную температуру - 40-49°С для разгонки белков кишечного сока на фракции поддерживают в холодильной камере с регулятором.
При разделении белков кишечного сока собак на белковые фракции по предлагаемой нами методике на чертеже четко видны фракции белков кишечного сока: альбумины, α-глобулины, трансферрин, гаптоглобин, G-глобулины, А-глобулины, S-фракция.
Источники информации
1. Дьяченко П.Ф., Жданова Е.А. Новое в химии молока и методах их определения. М., 1962. С.123.
2. Яблонский В.А. К методике электрофоретического разделения белков спермы и секретов половых желез в агаровом геле. // Методики исследований по физиологии и биохимии сельскохозяйственных животных. - Киев, 1986. - С.104-108.
3. Холод В.М. Белки сыворотки крови в клинической и экспериментальной ветеринарии. - Минск: Урдажай, 1983. - 78 С.
4. Ларский Э.Г. К методике электрофореза белков сыворотки крови. // Лабораторное дело. - 1968, №9, С.65-66.
5. Красов В.М. Электрофоретические исследования белков крови животных. - Алма-Ата: Наука, 1969. - 234 С.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ электрофоретического разделения белков сыворотки крови и молока в полиакриламидном геле | 2016 |
|
RU2616906C1 |
| Способ исследования апо-В-липопротеинов в сыворотке крови | 1987 |
|
SU1603280A1 |
| Способ определения фракционного состава растворимых белков кожи | 1980 |
|
SU960625A1 |
| О П И С А Н И ИЗОБРЕТЕНИЯ | 1973 |
|
SU405071A1 |
| Способ приготовления носителя для диск-электрофореза гуминовых кислот почв | 1980 |
|
SU918848A1 |
| Способ выделения лактопероксидазы | 1981 |
|
SU1024501A1 |
| СПОСОБ ДИАГНОСТИКИ ТЯЖЕСТИ ЭНДОГЕННОЙ ИНТОКСИКАЦИИ ПРИ ОСТРЫХ ГНОЙНО-СЕПТИЧЕСКИХ ЗАБОЛЕВАНИЯХ У ДЕТЕЙ | 1996 |
|
RU2122739C1 |
| Способ определения гликопротеидов и белков сыворотки крови | 1990 |
|
SU1827635A1 |
| Способ определения качества сычужных сыров и последующей его оценки | 1980 |
|
SU1015878A1 |
| СПОСОБ ЭКСТРАКЦИИ И РАЗДЕЛЕНИЯ САРКОПЛАЗМАТИЧЕСКИХ И МИОФИБРИЛЛЯРНЫХ БЕЛКОВ МЯСА НА ФРАКЦИИ МЕТОДОМ ОДНОМЕРНОГО ЭЛЕКТРОФОРЕЗА В ПОЛИАКРИЛАМИДНОМ ГЕЛЕ | 2013 |
|
RU2524546C1 |
Изобретение относится к ветеринарной медицине. Для разделения белков кишечного сока собак на фракции методом диск электрофореза в полиакриламидном геле после полимеризации крупнопористого геля на него наслаивают 0,9-1,1 мл гомогенизированного кишечного сока, а разделение белков кишечного сока собак проводят при температуре (-40)-(-49°)С, причем разделение белков кишечного сока на фракции проводят в морозильной камере с регулятором температуры. Способ позволяет производить более качественный анализ состояния белковообразовательной функции печени. 1 ил.
Способ разделения белков кишечного сока у собак на фракции в полиакриламидном геле методом дискэлектрофореза, отличающийся тем, что после полимеризации крупнопористого геля на него наслаивают 0,9-1,1 мл гомогенизированного кишечного сока, разделение кишечного сока проводят при температуре минус 40-49°С.
| Способ идентификации ингибиторов L-амилаз | 1981 |
|
SU969720A1 |
| Способ получения щелочной фосфатазы | 1985 |
|
SU1287593A1 |
| LOMSKY R et | |||
| al., Deltins: immunochemical evidence for a novel population of peptides of the D cells of the gastro-entero-pancreatic endocrine system, Endocrinol, 2001 Mar, 168(3), p.391-400. | |||
Авторы
Даты
2008-04-20—Публикация
2006-05-10—Подача