Настоящее изобретение относится к разделу химии, занимающемуся получением водорода, композициям, предназначенным для реализации этой задачи, способам получения таких композиций и аппаратам, предназначенным для генерации водорода, который в дальнейшем может использоваться для питания топливных элементов, обеспечивающих работоспособность различных переносных аппаратов и приборов, например сотовых телефонов, приемной и передающей полевой радиоаппаратуры, ноутбуков и т.п.
Известна композиция для контролируемой и регулируемой генерации водорода, содержащая 5-10 мас.% гомогенизирующей жидкости (минеральное масло, пентан или гексан), диспергирующий агент (типа триглицерида олеиновой кислоты) и 90-95 мас.% бинарного или комплексного гидрида (например, LiH или LiAlH4, NaH или NaBH4 и NaAlH4, MgH2, СаН2). Выделение водорода происходит в процессе контролируемого разложения композиции при контакте с водой (патент Канады 2434650, МПК7 С01В 3/08, B01J 7/00, С01В 6/04, С01В 6/24. Storage, generation, and use of hydrogen/Kondari R.K., Larsen Ch. A., Rolfe J.L., McClaine A.W. // 29.08.2002; Европейский патент 1355849, МПК7 С01В 3/08, B01J 7/00, С01В 6/04, С01В 6/24. Storage, generation, and use of hydrogen/Kondari R.K., Larsen Ch. A., Rolfe J.L., McClaine A.W. // 29.08.2002; Заявка США 2002166286, МПК7 C10J 1/00; B01J 7/00. Storage, generation, and use of hydrogen/Kondari R.K., Larsen Ch. A., Rolfe J.L., McClaine A.W. // 14.11.2002; Международная заявка 02066369, МПК7 С01В 3/08; С01В 6/04, С01В 6/24, B01J 7/00. Storage, generation, and use of hydrogen/Kondari R.K., Larsen Ch. A., Rolfe J.L., McClaine A.W. // 29.08.2002).
Недостатками указанной композиции являются защелачивание раствора и прекращение выделения водорода в случае NaBH4, возможность резкого увеличения скорости гидролиза вплоть до взрыва в случае применения NaH, LiAlH4 и NaAlH4, неконтролируемое взаимодействие и постепенное затухание реакции гидролиза и скорости выделения водорода в случае применения MgH2 и СаН2, вызванное ограниченной растворимостью образующихся гидроксидов в воде (значения произведения растворимости ПР для Mg(OH)2 и Са(ОН)2 равны 6,0×10-10 и 5,5×10-6 соответственно). Поскольку плотности гомогенизирующей жидкости (масло, пентан или гексан) и диспергирующего агента типа триглицерида олеиновой кислоты (0,7-0,9 г/см3) заметно ниже плотности гидрида (≈1,6 г/см3), вполне реальны процессы седиментации и слеживания композиции при хранении. Перемешивание суспензии гидрида в растворе диспергирующего агента требует затрат энергии. Ингредиенты композиции - гомогенизирующая органическая жидкость и диспергирующий агент, препятствующие, согласно техническому решению, быстрой седиментации гидрида металла, способствуют вспениванию композиции при генерации водорода и попаданию несущей органической жидкости в генерируемый водород. Кроме того, при использовании борогидрида натрия образуются высокотоксичные и пожароопасные бороводороды.
Известен метод приготовления композиции для генерации водорода (Патент Канады 2434650, МПК7 С01В 3/08, B01J 7/00, С01В 6/04, С01В 6/24. Storage, generation, and use of hydrogen/Kondari R.K., Larsen Ch. A., Rolfe J.L., McClaine A.W. // 29.08.2002; Европейский патент 1355849, МПК7 С01В 3/08, B01J 7/00, С01В 6/04, С01В 6/24. Storage, generation, and use of hydrogen/Kondari R.K., Larsen Ch. A., Rolfe J.L., McClaine A.W. // 29.08.2002; Заявка США 2002166286, МПК7 C10J 1/00; B01J 7/00. Storage, generation, and use of hydrogen/Kondari R.K., Larsen Ch. A., Rolfe J.L., McClaine A.W. // 14.11.2002; Международная заявка 02066369, МПК7 С01В 3/08, С01В 6/04, С01В 6/24, B01J 7/00. Storage, generation, and use of hydrogen/Kondari R.K., Larsen Ch. A., Rolfe J.L., McClaine A.W. // 29.08.2002), включающий смешение гидрида со смесью гомогенизирующей жидкости и триглицерида, после чего композицию преобразуют в устойчивую взвесь.
Недостатки известного метода приготовления композиции связаны с невозможностью получения устойчивой взвеси из различающихся по плотности составляющих и седиментацией взвеси при хранении.
Известен аппарат для генерации водорода, включающий сосуд для суспензии гидрида металла и механизм подачи реагента (в частности, воды) к различным порциям суспензии, содержащей гидрид металла (Патент Канады 2434650, МПК7 С01В 3/08, B01J 7/00, С01В 6/04, С01В 6/24. Storage, generation, and use of hydrogen/Kondari R.K., Larsen Ch. A., Rolfe J.L., McClaine A.W. // 29.08.2002; Европейский патент 1355849, МПК7 С01В 3/08, B01J 7/00, С01В 6/04, С01В 6/24. Storage, generation, and use of hydrogen/Kondari R.K., Larsen Ch. A., Rolfe J.L., McClaine A.W. // 29.08.2002; Заявка США 2002166286, МПК7 C10J 1/00; B01J 7/00. Storage, generation, and use of hydrogen/Kondari R.K., Larsen Ch. A., Rolfe J.L., McClaine A.W. // 14.11.2002; Международная заявка 02066369, МПК7 С01В 3/08; С01В 6/04, С01В 6/24, B01J 7/00. Storage, generation, and use of hydrogen/Kondari R.K., Larsen Ch. A., Rolfe J.L., McClaine A.W. // 29.08.2002). Механизм подачи реагента может содержать трубопроводы, снабженные системой для дозирования реагента к отдельным порциям суспензии.
Недостатками указанного аппарата являются: невозможность реализации эффективного и контролируемого выделения водорода, вызванная защелачиванием реакционной среды из-за образования гидроксидов щелочных металлов или, в случае гидридов кальция и магния, ограниченной растворимостью образующихся гидроксидов в воде, и сложность конструкции.
Известно также устройство для получения водорода, включающее наполненный водой сосуд и деформируемую емкость, наполненную жидким материалом, способным к реакции с водой, в частности гидридами кальция, лития или магния, смешанными с нефтью или минеральным маслом (Патент Великобритании 1425590, МПК7 B01J 7/02. Gas generating devices / France Armed Forces. // 18.02.1976; Патент Франции 2207885, МПК7 B01J 7/02. Gas generating devices / France Armed Forces. // 18.02.1976; Патент США 3902425, класс 120/531. Gas generator device within an enclosure / B.J.Kurtzemann. // 02.09.1975).
Недостатками указанного технического решения являются медленное неконтролируемое выделение водорода в случае MgH2 и СаН2 из-за ограниченной растворимости образующихся гидроксидов в воде (значения произведения растворимости ПР для Mg(OH)2 и Ca(OH)2 равны 6,0×10-10 и 5,5×10-6 соответственно), вспенивание суспензии при генерировании водорода, попадание нефти или минерального масла в генерируемый водород и седиментация более тяжелого, по сравнению с нефтью или минеральным маслом, гидрида металла при хранении. В рамках данного технического решения невозможно дозированное (по требованию) выделение водорода.
Известно также устройство для генерирования водорода (Патент Великобритании 2290784, МПК7 С01В 3/06, B01J 7/02. Reactor for generating hydrogen from metal hydride and water / Adlhart O.J. // 10.01.1996; Патент США 5514353, МПК7 B01J 007/00. Demand responsive hydrogen generator based on hydride water reaction/Adlhart O.J. // 07.05.1996), в котором подаваемая контролируемо вода попадает в патрон, выполненный в виде волнистого перфорированного листа металла, покрытого пористым материалом (неорганические или органические волокна, пластмассы), в котором диспергирован гидрид металла (СаН2, LiH, LiAlH4, LiBH4). Согласно техническому решению, выделение водорода начинается после попадания воды в капилляры материала и прекращается после прекращения подачи воды.
Недостатками этого технического решения являются невозможность контролируемого выделения водорода из-за диффузионных затруднений, вызванных низкой растворимостью гидроксида кальция, неприменимость указанного технического решения для других гидридов, в частности для гидрида магния, выделение бороводородов при гидролизе LiBH4 и гидрофильность материала, капиллярно поглощающего воду, в связи с чем процесс генерации водорода прекращается только при полном расходовании воды.
Описан способ интенсификации взаимодействия воды (или воды, подкисленной соляной кислотой) с нанокристаллическими гидридами элементов, содержащих, по меньшей мере, один из элементов из группы Mg, Li, Be, Ca, Na, K, Al, Ti, V, Cr, Mn, Co, Ni, Cu, Fe, Zn, B, Zr, Y, Nb, Mo, In, Sn, Si, H, C, O, F, P, S, La, Pd, Pt, Mm and Re, где Mm - мишметалл и Re - редкоземельный металл, полученными механохимической обработкой поликристаллических форм гидридов, реакционным размолом, газофазной конденсацией, лазерной (плазменной) обработкой или при использовании золь-гель технологии (Патент США 6573836, МПК7 С01В 003/02, С01В 003/04; С01В 003/08. Method for producing gaseous hydrogen by chemical reaction of metals or metal hydrides subjected to intense mechanical deformations / Schulz R., Huot J., Liang G., Boily S. // 03.06.2003). Показано, что высокоэнергетическое воздействие, приводящее к получению наноразмерного MgH2 (средний диаметр частиц ˜12 нм, удельная поверхность ˜9,9 м2/г) или его композита с Ca, Li или LiAlH4, улучшает кинетику гидролиза (Huot J., Liang G., Schulz R. Magnesium-based nanocomposites chemical hydrides. // J. Alloys and Compounds. 2003. V.353. P.L12-L15.). Добавление 1%-ной соляной кислоты также благотворно влияет на кинетику выделения водорода, поскольку образующийся при этом хлорид магния хорошо растворим в воде.
Недостатками указанного технического решения являются высокие энергозатраты (до 1,5 кВт/г) для получения нанокомпозита и высокая реакционная способность вещества, находящегося в метастабильном состоянии, не допускающая его длительного хранения до употребления. Кроме того, при использовании разбавленной соляной кислоты неизбежно попадание хлористого водорода в генерируемый водород.
В части композиции для генерации водорода, наиболее близкой по технической сущности и наибольшему числу существенных признаков к заявляемому решению, является композиция, включающая гидриды (борогидриды, алюмогидриды или их смесь) щелочных и щелочно-земельных (Li, Na, K, Rb, Cs, Mg, Be, Ca, Al или их смесь) металлов или их смеси, 0.1÷15 мас.% катализатора (Ru или его соединения, карбиды кобальта, никеля или вольфрама или их смесь или ацетилацетонаты кобальта, никеля, рутения и платины) и ≥0,5 мас.% полимерного агента (целлюлозные или полиэфирные волокна, полиакриламид или их смесь), принятая за прототип (Международная заявка 2005005311 WO, МКИ С01В 3/00. Hydrogen generator / Salinas С., Cisar A., Clarke E., Murphy О.J., Fiebig B. // 20.01.2005).
Недостатками указанного технического решения-прототипа являются:
- необходимость использования большого количества катализатора (до 15%);
- непроизводительное расходование катализатора из-за взаимодействия его с кислотами;
- неприменимость некоторых кислот из-за их летучести или нерастворимости образующихся солей;
- взаимодействие органических и неорганических кислот в случае их смеси;
- невозможность генерации высокочистого водорода при использовании большинства органических и неорганических кислот, органических растворителей и жидкого аммиака из-за их летучести.
Количество катализатора по изобретению достаточно велика, а неизменность самого катализатора после проведения процесса не доказана, т.е. нет оснований именовать его катализатором. Из-за высокого давления паров и возможности попадания в водород вызывает сомнение целесообразность использования в процессе органических растворителей. К тому же не все из указанных минеральных и карбоновых кислот применимы при гидролизе гидридов магния, кальция и бериллия из-за малорастворимости (например, фосфорная кислота) их солей или из-за их летучести (соляная, азотная, уксусная, пропионовая, масляная кислоты).
Наиболее близким по технической сущности к настоящему изобретению в части способа приготовления композиции является способ приготовления композиции для генерации водорода, избранный в качестве прототипа, включающий растворение или суспендирование гидрида и катализатора в не реагирующем с гидридом, например органическом, растворителе (тетрагидрофуран, эфиры этиленгликоля, безводный аммиак, замещенные амины, пиридин или их смесь), испарение растворителя и удаление композиции в твердом виде (Международная заявка 2005005311 WO, МКИ С01В 3/00. Hydrogen generator/Salinas С., Cisar A., Clarke E., Murphy O.J., Fiebig B. // 20.01.2005).
Недостатками указанного способа-прототипа являются нерастворимость большинства указанных гидридов и катализаторов в перечисленных растворителях, взаимодействие гидридов и катализаторов с растворителями в ходе растворения и разложение гидрида в ходе испарения растворителя, что делает указанный способ нереализуемым.
Наиболее близким по технической сущности к настоящему изобретению в части генератора водорода является известный генератор водорода, включающий реакционный сосуд для хранения композиции, сосуд с водным раствором, соединенный с реакционным сосудом, и средства регулирования скорости подачи водного раствора. К композиции, сформированной в виде таблеток или гранул, или к композиции, закрепленной на пористом носителе, подают водный или органический растворитель, содержащий минеральную или органическую кислоту (или их смесь) и антивспениватель (поверхностно-активные вещества различной природы, гликоль, полиол или их смесь). Регулируемое выделение водорода становится возможным в результате использования пассивного (подбор концентрации катализатора в композиции) и активного (дозированная подача растворителя при высокой концентрации катализатора) контроля (Международная заявка 2005005311 WO, МКИ С01В 3/00. Hydrogen generator/Salinas С., Cisar A., Clarke E., Murphy O.J., Fiebig B. // 20.01.2005).
Генератор не является безопасным и удобным в применении, поскольку:
а. содержит твердый (формованная смесь гидрида, катализатора и связующего или пористого носителя) и жидкий (растворитель, антивспениватель, кислота) компоненты в одном устройстве, что не исключает возможности несанкционированного срабатывания;
б. не регулируем, т.к. пассивное (концентрацией катализатора) регулирование возможно только при приготовлении композиции, активное же (дозированием растворителя) возможно только при высокой концентрации катализатора;
в. не универсален, поскольку скорость выделения водорода может быть предусмотрена только при приготовлении композиции, но не в процессе ее эксплуатации.
Задачей настоящего изобретения является разработка удобной при использовании, безопасной в обращении композиции для регулируемой контролируемой автономной и портативной генерации высокочистого водорода, транспортабельной и пригодной для использования в полевых условиях, способ ее приготовления и аппарат для генерации водорода.
В части композиции для генерации водорода поставленная задача решается тем, что указанная композиция включает гидрид магния, связующее, серную кислоту и сорбент серной кислоты, не взаимодействующий с серной кислотой, в качестве сорбента серной кислоты она содержит материал, выбранный из группы, включающей аэрогели диоксида кремния, диоксида титана, оксида цинка, оксида алюминия, а в качестве связующего содержит вещество, выбранное из группы: фторопласт, полиэтилен, полипропилен, при следующем соотношении компонентов, мас.%:
при мольном соотношении гидрида магния к серной кислоте, равном 1.
Гидрид магния может быть получен любым из возможных способов и использован в виде порошка или гранул, таблеток, окатышей, сформованных из смеси гидрида магния и связующего.
В части способа приготовления композиции для генерации водорода поставленная задача решается тем, что способ приготовления композиции для получения водорода включает сорбцию серной кислоты сорбентом и формование гидрида магния со связующим в виде таблеток, окатышей или гранул. В указанном способе в качестве сорбента серной кислоты используют материал, выбранный из группы, включающей аэрогели диоксида кремния, диоксида титана, оксида цинка, оксида алюминия, а в качестве связующего - вещество, выбранное из группы, включающей фторопласт, полиэтилен, полипропилен.
В части аппарата для генерации водорода поставленная задача решается тем, что аппарат для генерации водорода включает реактор, выполненный в виде сообщающихся сосудов и содержащий указанную композицию для получения водорода, и устройство дозирования воды, причем указанный реактор снабжен редуктором с обратной связью для выпуска водорода и выполнен в виде U-образного сосуда, содержащего указанную композицию. Схематически аппарат для генерации водорода изображен на фиг.3. Аппарат представляет собой два (на схеме - левый 1 и правый) сообщающихся сосуда. Сосуд 1 имеет клапан для выпуска водорода с постоянным расходом 2 и подвижную перфорированную емкость 4 для композиции для получения водорода (гранулы гидрида магния со связующим). Правый сосуд снабжен устройством дозированной подачи воды 3. Регулирование выделения водорода осуществляется двумя путями: дозированной подачей воды к указанной композиции через устройство 3 и регулированной подачей гидрида магния в формованном виде путем опускания или поднимания подвижной емкости 4. Снабжение реактора 1 редуктором с обратной связью 2 позволяет достичь задаваемых условий выпуска водорода и при несоблюдении их накапливать давление в реакторе. Образующееся при этом давление водорода в реакторе вызывает в U-образном сосуде передавливание жидкости во второе колено, отсутствие контакта раствора кислоты с находящейся в подвижной перфорированной емкости 4 композиции гидрида магния со связующим и, таким образом, прекращение выделения водорода.
Настоящее изобретение иллюстрируется чертежами:
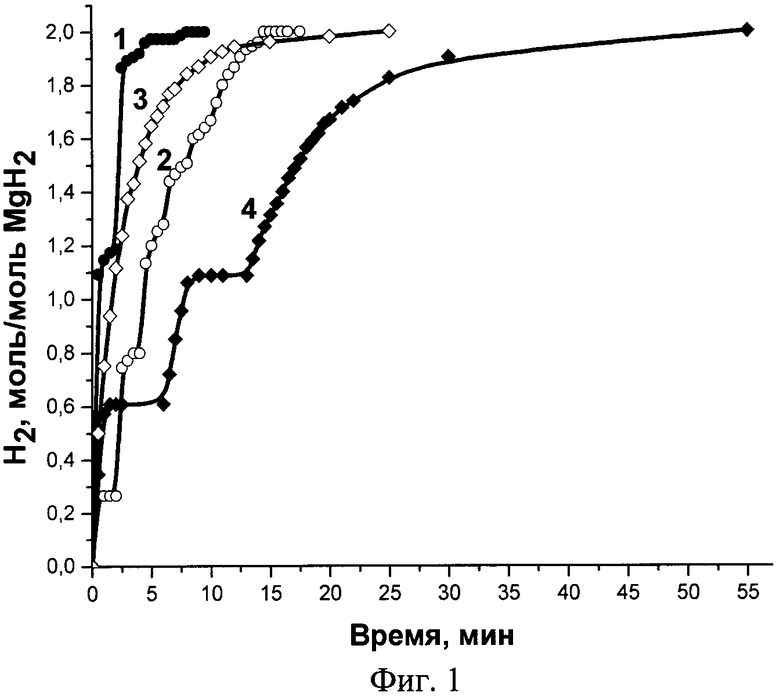
фиг.1, на которой приведены кривые выделения водорода при дозированной подаче воды, когда необходимое количество воды введено одноразово (кривая 1), со скоростью 1 мл/мин (кривая 2) и 0,2 мл/мин, (кривая 3) при соотношении гидрида магния к серной кислоте, равном 1:1 мол. и 1:0,5 мол. (кривая 4);
фиг.2, где приведена зависимость скорости выделения водорода от массы гидрида магния в виде гранул, сформованных из смеси гидрида магния с 10 мас.% аэрогеля диоксида кремния;
фиг.3, где схематически изображен аппарат для генерации водорода, включающий реактор 1, выполненный в виде сообщающихся сосудов и снабженный клапаном для выпуска водорода с постоянным расходом 2, устройством дозирования воды 3 и подвижной перфорированной емкостью для гранул гидрида магния со связующим 4.
Регулирование выделения водорода осуществляется двумя путями: дозированной подачей воды к указанной композиции и регулированной подачей гидрида магния в формованном виде.
При дозированной подаче воды регулированное выделение водорода достигается из-за ограниченной растворимости образующегося сульфата магния (44,5 г на 100 г воды при 20°С). Регулирование генерации водорода путем подачи гидрида магния, формованного со связующим, связано с прямо пропорциональной зависимостью скорости выделения водорода от количества гидрида магния, контактирующего с раствором кислоты (фиг.2), и гидрофобностью связующего, в результате чего водный раствор кислоты не задерживается на гранулах, содержащих гидрид магния, после прекращения контакта гранул с водным раствором кислоты. Скорость выделения водорода при использовании указанной композиции и указанного аппарата для генерации водорода достигается также применением в аппарате реактора, выполненного в виде U-образного сосуда и снабженного редуктором с обратной связью для выпуска водорода. Снабжение реактора 1 редуктором с обратной связью 2 позволяет достичь задаваемых условий выпуска водорода и при несоблюдении их накапливать давление в реакторе. Давление водорода, полученного в результате введения воды или раствора кислоты, в реакторе вызывает в U-образном сосуде передавливание жидкости во второе колено, отсутствие контакта раствора кислоты с находящимися в подвижной перфорированной емкости 4 таблетками, окатышами или гранулами, сформованными из гидрида магния со связующим, и, таким образом, прекращение выделения водорода.
Заявленное техническое решение иллюстрируется следующими примерами конкретного использования.
Опыт 1. В реакционный сосуд, снабженный двумя кранами, вводят 0,207 мл концентрированной серной кислоты плотностью 1,84 г/см3 (96 мас.%, масса 0,366 г, 3,731 ммоль), добавляют 0,100 г аэросила, тщательно перемешивают и прибавляют 0,132 г гидрида магния чистотой 74,3 мас.% (3,731 ммоль) с 0,03 г связующего (полиэтилен). Сосуд закрывают резиновой прокалываемой пробкой и подсоединяют через кран к бюретке объемом 250 см3, продувают водородом, после чего прокалывают пробку шприцом, заполненным 5 мл дистиллированной воды, вводят 0,5 мл воды и регистрируют объем выделяющегося водорода через каждые 0,5 мин, добавляя через каждые 2 мин 0,5 мл воды. За 8 мин при температуре 21°С выделилось 180 см3 (7,462 ммоль) водорода или 2 моль Н2/моль MgH2 (фиг.1, кривая 1).
Опыт 2. В условиях опыта 1 вводят 0,25 мл воды и регистрируют объем выделяющегося водорода через каждые 0,5 мин, добавляя через каждые 2 мин 0,25 мл воды. За 14,5 мин при температуре 21°С выделилось 180 см3 (7,462 ммоль) водорода или 2 моль Н2/моль MgH2 (фиг.1, кривая 2).
Опыт 3. В реакционный сосуд, снабженный двумя кранами, вводят 1 г композиции, включающей 0,83 г серной кислоты с концентрацией 45,4 мас.% (3,845 ммоль), добавляют 0,05 г аэрогеля диоксида кремния, тщательно перемешивают и вводят таблетку, сформованную из 0,100 г гидрида магния (3,845 ммоль) и 0,020 г фторопласта. Соотношение компонентов композиции - 10 мас.% MgH2, 2 мас.% связующего (фторопласт), 83 мас.% серной кислоты и 5 мас.% сорбента (диоксид кремния). Сосуд закрывают резиновой прокалываемой пробкой и подсоединяют через кран к бюретке объемом 500 см3, продувают водородом, после чего прокалывают пробку шприцом, заполненным 5 мл дистиллированной воды, вводят воду и регистрируют объем выделяющегося водорода через каждые 0,5 мин. За 5 мин при температуре 22°С выделилось 186,2 см3 водорода или 7,69 ммоль.
Опыт 4. В реакционный сосуд, снабженный двумя кранами, вводят 1 г композиции, включающей 0,600 г серной кислоты плотностью 1,84 г/см3 (96 мас.%, 5,88 ммоль), добавляют 0,100 г аэрогеля диоксида титана, тщательно перемешивают и вводят таблетку, сформованную из 0,228 г гидрида магния чистотой 67 мас.% (5,88 ммоль) и 0,072 г полиэтилена. Сосуд закрывают резиновой прокалываемой пробкой и подсоединяют через кран к бюретке объемом 500 см3, продувают водородом, после чего прокалывают пробку шприцом, заполненным 5 мл дистиллированной воды, вводят воду и регистрируют объем выделяющегося водорода через каждые 0,5 мин. За 7 мин при температуре 22°С выделилось 284,5 см3 водорода или 11,75 ммоль.
Опыт 5. В реакционный сосуд, снабженный двумя кранами, вводят 1 г композиции, включающей 0,700 г серной кислоты (100 мас.%, 7,143 ммоль), добавляют 0,050 г аэрогеля оксида цинка, тщательно перемешивают и вводят таблетку, сформованную из 0,186 г гидрида магния чистотой 99,5 мас.% (7,143 ммоль) и 0,064 г полипропилена. Сосуд закрывают резиновой прокалываемой пробкой и подсоединяют через кран к бюретке объемом 500 см3, продувают водородом, после чего прокалывают пробку шприцом, заполненным 5 мл дистиллированной воды, вводят воду и регистрируют объем выделяющегося водорода через каждые 0,5 мин. За 7 мин при температуре 22°С выделилось 345,8 см3 водорода или 14,27 ммоль.
Опыт 6. В реакционный сосуд (фиг.3) вводят 0,700 г серной кислоты (7,143 ммоль), добавляют 0,070 г аэрогеля оксида алюминия и тщательно перемешивают. В подвижную перфорированную емкость 4 вносят таблетку, сформованную из 0,186 г гидрида магния (7,143 ммоль) и 0,044 г фторопласта. Сосуд закрывают резиновой прокалываемой пробкой и подсоединяют через кран к бюретке объемом 500 см3, продувают водородом, после чего прокалывают пробку шприцом, заполненным 5 мл дистиллированной воды, вводят 1 мл воды и регистрируют объем выделяющегося водорода через каждые 0,5 мин. Через 2 мин прекращают отбор водорода (перекрывают клапан 2). Жидкость передавливается во второе колено и удаляется от перфорированной емкости 4. Через 3 мин открывают клапан 2, жидкость смачивает таблетку, но водород практически не выделяется. Вводят еще 0,25 мл воды, регистрируют объем выделяющегося водорода, добавляя воду порциями по 0,25 мл через каждые 2 мин. За 30 мин при температуре 22°С выделилось 345,8 см3 водорода или 14,27 ммоль.
Опыт 7. В реакционный сосуд (фиг.3) вводят 0,700 г серной кислоты (7,143 ммоль), добавляют 0,070 г аэрогеля оксида алюминия и тщательно перемешивают. В подвижную перфорированную емкость 4 вносят таблетку, сформованную из 0,186 г гидрида магния (7,143 ммоль) и 0,044 полипропилена. Сосуд продувают водородом, после чего вводят 1 мл воды и регистрируют объем выделяющегося водорода через каждые 0,5 мин. Через 2 мин прекращают отбор водорода (перекрывают клапан 2). Жидкость передавливается во второе колено и удаляется от перфорированной емкости 4. Через 3 мин открывают клапан 2, жидкость смачивает таблетку, но водород практически не выделяется. Вводят еще 0,25 мл воды, регистрируют объем выделяющегося водорода, добавляя воду порциями по 0,25 мл через каждые 2 мин. За 30 мин при температуре 22°С выделилось 345,8 см3 водорода или 14,27 ммоль.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПОЗИЦИЯ ДЛЯ ПОЛУЧЕНИЯ ВОДОРОДА, СПОСОБ ЕЕ ПРИГОТОВЛЕНИЯ И ПРОЦЕСС ПОЛУЧЕНИЯ ВОДОРОДА | 2018 |
|
RU2689587C1 |
| Композитный каталитический материал для получения чистого водорода для водородо-воздушных топливных элементов и способ его изготовления | 2022 |
|
RU2794902C1 |
| Композиция для насыщения продуктов водородом | 2021 |
|
RU2784467C1 |
| СПОСОБ ГЕНЕРАЦИИ ВОДОРОДА И КОНСТРУКЦИЯ ХИМИЧЕСКОГО ИСТОЧНИКА ВОДОРОДА | 2018 |
|
RU2708001C1 |
| Способ улучшения водородсорбционных характеристик порошковой засыпки металлогидридного аккумулятора водорода | 2020 |
|
RU2748480C1 |
| СПОСОБ ГИДРИРОВАНИЯ МАТЕРИАЛА НАКОПИТЕЛЯ ВОДОРОДА - МАГНИЯ | 2007 |
|
RU2359901C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ГИДРИДА МАГНИЯ ДЛЯ ХИМИЧЕСКОГО ГЕНЕРАТОРА ВОДОРОДА | 2018 |
|
RU2686898C1 |
| ВОДОРОДОГЕНЕРИРУЮЩАЯ КОМПОЗИЦИЯ И СПОСОБ ПОЛУЧЕНИЯ ИЗ НЕЕ ВОДОРОДА | 2019 |
|
RU2721697C1 |
| ШИХТА ДЛЯ ПОЛУЧЕНИЯ КОМПОЗИТА НА ОСНОВЕ АЛЮМИНИЯ ДЛЯ ПОЛУЧЕНИЯ ВОДОРОДА | 2011 |
|
RU2478726C1 |
| Способ повышения эффективности металлогидридных теплообменников | 2019 |
|
RU2729567C1 |

Изобретения относится к получению водорода, к композициям, предназначенным для использования в портативных автономных генераторах водорода. Композиция включает гидрид магния, связующее, серную кислоту и сорбент серной кислоты. В качестве сорбента серной кислоты она содержит материал, выбранный из группы, включающей аэрогели диоксида кремния, диоксида титана, оксида цинка, оксида алюминия, а в качестве связующего содержит вещество, выбранное из группы: фторопласт, полиэтилен, полипропилен. Композицию для получения водорода готовят путем сорбции серной кислоты сорбентом, формования гидрида магния со связующим в виде таблеток, окатышей или гранул. В качестве сорбента серной кислоты используют материал, выбранный из группы, включающей аэрогели диоксида кремния, диоксида титана, оксида цинка, оксида алюминия, а в качестве связующего - вещество, выбранное из группы, включающей фторопласт, полиэтилен, полипропилен. Аппарат для генерации водорода включает реактор, выполненный в виде сообщающихся сосудов, содержащий композицию для получения водорода, устройство дозирования воды. Указанный реактор снабжен редуктором с обратной связью для выпуска водорода. Аппарат выполнен в виде U-образного сосуда, содержащего вышеуказанную композицию. Изобретения позволяют генерировать высокочистый водород. 3 н.п. ф-лы, 3 ил.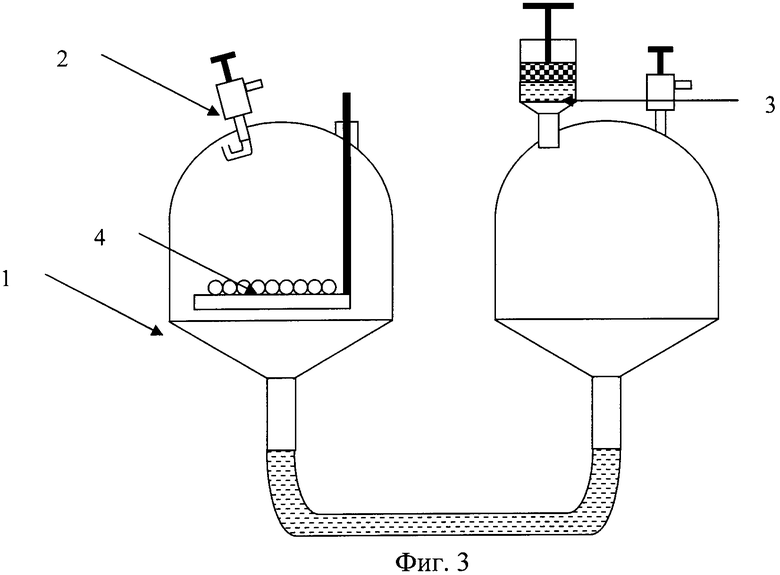
при мольном соотношении гидрида магния к серной кислоте, равном 1.
| WO 2005005311 А2, 20.01.2005 | |||
| Состав для аккумулирования водорода | 1983 |
|
SU1134538A1 |
| СМЕСЬ ГИДРОРЕАГИРУЮЩАЯ | 1997 |
|
RU2131841C1 |
| US 4749558 A, 07.06.1988 | |||
| ОПОРА КОРПУСА ТУРБОМАШИНЫ | 1999 |
|
RU2165532C1 |
| Устройство для получения металлических порошков | 1987 |
|
SU1509184A1 |
Авторы
Даты
2009-02-10—Публикация
2006-11-01—Подача