Предлагаемое изобретение относится к медицине, а именно к фармацевтической химии и фармакологии, и может быть использовано для создания новых иммунотропных и антиагрегационных средств.
Прототипом и препаратом сравнения иммунотропной активности является левамизол (гидрохлорид 6-фенил-2,3,5,6-тетрагидроимидазо[1,2-b]тиазола, декарис, Гедеон Рихтер А.О., Венгрия), который длительное время используется в клинике как иммуномодулирующее средство, стимулирующее клеточные факторы иммунитета (Renoux G. // Drugs. The general immunopharmacology of levamizole. Drugs. 1980. V.20 - P.89-99). Препаратом сравнения антиагрегационной активности является пентоксифиллин (3,7-дигидро-3,7-диметил-1-(5-оксогексил)-1H-пурин-2,6-дион, Aventis, Германия), используемый в клинике как корректор реологических нарушений (Hikiami Н., Goto Н., Sekiya N. [et al.] // Phytomedicine. - 2003. - Vol.10, №6-7. - P.459-466.).
Задача изобретения - расширение арсенала биологически активных веществ, обладающих иммунотропными и антиагрегационными свойствами.
Технический результат - получение вещества, обладающего иммунотропной и антиагрегационной активностью.
Сущность изобретения: дигидрохлорид 3-циклогексиламинометилтиазоло[3,2-a]бензимидазола формулы:
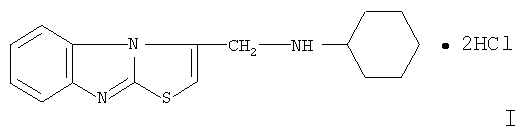 ,
,
проявляющий иммунотропные и антиагрегационные свойства.
Заявляемое соединение - дигидрохлорид 3-циклогексиламинометилтиазоло[3,2-а]бензимидазола (I), получено следующим образцом.
Реакцией 3-хлорметилтиазоло[3,2-а]бензимидазола (Дианов В.М., Сибиряк С.А., Садыков Р.Ф. и др. // Хим.-фарм. журн., - 1991. - №1. - С.40-42.) с циклогексиламином в кипящем этаноле в течение 2 часов образуется 3-циклогексиламинометилтиазоло[3,2-а]бензимидазол. Хлористоводородную соль получают обработкой основания хлористым водородом в этилацетате до pH раствора 1-2.
Пример 1. Синтез дигидрохлорида 3-циклогексиламинометилтиазоло[3,2-а]бензимидазола(I).
Раствор 4,4 г (20 ммоль) 3-хлорметилтиазоло[3,2-а]бензимидазола и 8,0 г (80 ммоль) циклогексиламина в 60 мл этилового спирта нагревают на водяной бане 2 часа. Часть растворителя удаляют под вакуумом. Охлаждают. Выпавший осадок отфильтровывают, промывают водой, сушат. Получают 5,0 г (87,7%) 3-циклогексиламинометилтиазоло[3,2-а]бензимидазола. Хлористоводородную соль 3-циклогексиламинометилтиазоло[3,2-а]бензимидазола получают растворением основания I в этилацетате и пропусканием через раствор газообразного хлористого водорода до pH раствора 1-2. Перекристаллизовывают из этанола. Т. пл. 247-250°C.
Найдено, %: C 53,8; H 6,0; N 11,8; S 9,9; Cl 19,8. C16H19N3S·2РCl. Вычислено: C 53,6; H 5,9; N 11,7; S 8,9; Cl 19,7.
Спектр-ЯМР 1Н (ТФУК, ГМДС), δ, м.д.: 1,17 (сл. м, 10H, CH2-циклогекс), 3,47-3,02 (м, 1Н, N-CH), 4,95-4,50 (д, 2H, CH2-NH), 7,55 сл. м. (5Н, аром.).
ИК спектр: 1480, 1540, 1604, 2950 см-1 (C=C, C=N, CH).
Пример 2. Острая токсичность заявляемого соединения.
Острая токсичность соединения I изучена на белых мышах массой 14-16 г по методу Литчфилда и Уилкоксона (Беленький М.Л. Элементы количественной оценки фармакологического эффекта. - 2-е изд. - Рига, 1963) и на крысах массой 140-160 г по методу Ван дер Вердена (Van der Waerden В.L. // Arch. exp. Path. Pharmacol. - 1990. - Bd.195. - S.389). Результаты испытаний приведены в таблице 1.
Таким образом, заявляемое соединение в зависимости от пути введения в 2-4 раза ниже токсичности левамизола.
Пример 3. Изучение имунотропной активности дигидрохлорида 3-циклогексиламинометилтиазоло[3,2-а]бензимидазола (соединение I).
В качестве модели аутоиммунного процесса использованы адьювантный артрит и экспериментальный аллергический энцефаломиелит у крыс. Адьювантный артрит воспроизводили путем внутрикожной инъекции полного адьюванта Фрейнда (ПАФ) в основание хвоста в объеме 0,1 мл при дозе микробактерий 5 мг в 1 мл. Отек конечностей измеряли на электронно-механическом онкометре. Оценку тяжести артрита проводили в период манифестации (+14 день после индукции) внутрибрюшинно 1 раз в три дня в дозе 20 ЛД50 с +1 по +14 день (всего 5 введений). Левамизол вводили по аналогичной схеме в эквивалентной дозе (табл.2).
При использовании соединения I и левамизола в дозе 1/9 ЛД50 ежедневно внутрибрюшинно с +14 по +22 день эффекта не наблюдалось. Описанный характер действия характерен для иммунотропных препаратов и исключает подавление артрита за счет прямого антифлогистического эффекта.
Экспериментальный аллергический энцефаломиелит воспроизводили путем подкожного введения крысам 0,1 мл энцефалитогенной эмульсии, содержащей 200 мг изологичного спинного мозга и 2 мг в 1 мл БЦЖ в неполном адьюванте Фрейнда. Оценку тяжести неврологических симптомов проводили на +14 день. Соединение I и левамизол вводили внутрибрюшинно в дозе 1/20 ЛД50 1 раз в три дня с +1 по +14 день (табл.4).
Таким образом, в проведенных экспериментах левамизол, при введении в дозе 2,5 мг/кг (1/20 ЛД50) 1 раз в три дня, вызывал лишь тенденцию к снижению тяжести артрита, в то время как соединение I при использовании по аналогичной схеме в эквивалентной дозе вызывало существенное подавление заболевания, превосходя левамизол по активности в 1,6-1,8 раз. Соединение I в условиях использованной модели не обладало антифлогистической активностью, так как при введении соединения с +14 по +22 день болезни эффекта не наблюдалось.
На модели экспериментального аллергического энцефалита у крыс соединение I при внутрибрюшном введении в дозе 1/20 ЛД50 1 раз в 3 дня с +1 по +14 день полностью подавляло развитие болезни, в то время как левамизол эффекта не оказывал.
Для оценки влияния соединения I и левамизола на неспецифическую иммунологическую реактивность был использован интегральный тест-модель летальной инфекции, вызванной введением микробного агента. Инфекцию вызывали внутрибрюшинным введением 1,25 ЛД50 суточной культуры синегнойной палочки, что составило 60-70 млн микробных тел на одно животное.
Соединение I и левамизол вводили в эквивалентных дозах (1/20 ЛД50), используя профилактический режим введения - во всех случаях последнее введение проводилось за сутки (-1 день) до инокуляции возбудителя (0-день). Результаты испытаний приведены в табл.5.
Таким образом, как соединение I, так и эталонный препарат левамизол независимо от пути введения при использовании в дозах, равных 1/20 ЛД50, для соответствующего пути введения вызывали стимуляцию неспецифической резистентности животных, наиболее отчетливый эффект наблюдался при введении в мышцу и в вену. Существенных преимуществ соединения I в сравнении с левамизолом выявлено не было.
Для оценки влияния соединения I и левамизола на опухолевый процесс были использованы перевиваемые штаммы солидных опухолей - карциносаркома Уокера (W-256), саркома Крокера (S-180) и асцитная опухоль Эрлиха (АОЭ-дипл.), полученные из ОНЦ АМН СССР. Методические аспекты эксперимента разработаны, а оценка эффекта проводилась согласно общепринятым требованиям к оценке противоопухолевых препаратов.
Соединение I и левамизол вводили с +1 дня и после имплантации опухолевого материала по +7 день, внутрибрюшинно или в вену, 1 раз в три дня в дозе 1/20 ЛД50 для соответствующего пути введения. Результаты испытаний приведены в табл.6 и 7.
По факту, соединение I угнетает развитие солидных опухолей при введении с 0 дня имплантации опухолевого материала, трехкратно, внутрибрюшинно и внутривенно в дозе 1/20 ЛД50.
Таким образом, как соединение I, так и левамизол угнетают развитие солидных опухолей при введении с 0 дня имплантации опухолевого материала, трехкратно, внутрибрюшинно и внутривенно в дозе 1/20 ЛД50, причем на модели саркомы-180 соединение I существенно угнетало рост опухоли, в то время как левамизол вызывал лишь тенденцию к уменьшению роста. На модели карциносаркомы-256 как соединение I, так и левамизол существенно угнетали рост опухоли, однако эффект соединения I был более выражен. Как соединение I, так и левамизол вызывали тенденцию к уменьшению роста асцитной опухоли.
Антиагрегационная активность соединения I изучена на модели необратимой агрегации тромбоцитов, вызванной (конечная концентрация 2·10-4 М) на плазме здоровых доноров по методу В.А.Люсова с незначительной модификацией (Люсов В.А., Белоусов Ю.Б., Савенков М.П. Метод определения агрегации тромбоцитов и эритроцитов // Лаб. дело. - 1976. - №8. с.463-468). В качестве эталонного антиагреганта использован пентоксифиллин (3,7-дигидро-3,7-диметил-1-(5-оксогексил)-1Н-пурин-2,6-дион, Aventis, Германия), который длительное время используется в клинике как корректор реологических нарушений. Результаты испытаний приведены в таблице 8.
Таким образом, по антиагрегационной активности соединение 1 превосходит пентоксифиллин в 7,9 раз.
Таким образом, новое соединение обладает выраженной иммунотропной активностью, в ряде случаев (аутоиммунитет и опухолевый процесс) превосходящей активность эталонного иммуномодулятора левамизола, выраженной антиагрегационной активностью, также превосходящей активность эталонного дезагреганта пентоксифиллина, и может найти применение в практической медицине.
0, +3, +6,
0, +3, +6
0, +3, +6,
0, +3, +6
0, +3, +6,
0, +3, +6,
0, +3, +6
| название | год | авторы | номер документа |
|---|---|---|---|
| КАЛИЕВАЯ СОЛЬ 2-[1-(1,1ДИОКСОТИЕТАНИЛ-3) БЕНЗИМИДАЗОЛИЛ-2-ТИО]-УКСУСНОЙ КИСЛОТЫ, ПРОЯВЛЯЮЩАЯ ИММУНОТРОПНУЮ АКТИВНОСТЬ | 1996 |
|
RU2115652C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНТИАГРЕГАЦИОННОЙ АКТИВНОСТЬЮ | 1991 |
|
RU2061481C1 |
| ДИГИДРОХЛОРИД 1-(3-НИТРО-4-МЕТОКСИБЕНЗИЛ)-2-[БИС-(2-ХЛОРЭТИЛ)АМИНОМЕТИЛ]ИМИДАЗОЛА, ПРОЯВЛЯЮЩИЙ ПРОТИВООПУХОЛЕВУЮ АКТИВНОСТЬ | 1981 |
|
SU976654A1 |
| СРЕДСТВО ГЕМОРЕОЛОГИЧЕСКОЕ, СНИЖАЮЩЕЕ ИНСУЛИНОРЕЗИСТЕНТНОСТЬ И ВОССТАНАВЛИВАЮЩЕЕ ТОЛЕРАНТНОСТЬ ОРГАНИЗМА К ГЛЮКОЗЕ, И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ЕГО ОСНОВЕ | 2007 |
|
RU2386634C2 |
| КОРРЕКТОР ГЕМОРЕОЛОГИЧЕСКИХ НАРУШЕНИЙ ПРИ ЗАБОЛЕВАНИЯХ, ОСЛОЖНЕННЫХ СИНДРОМОМ ПОВЫШЕННОЙ ВЯЗКОСТИ КРОВИ | 2009 |
|
RU2406500C1 |
| АНТИАРИТМИЧЕСКОЕ СРЕДСТВО | 1983 |
|
RU2068261C1 |
| 1,4-ДИГЛИЦИДИЛ-3-ЭТИЛ-1,2,4-ТРИАЗОЛ-5-ОН, ПРОЯВЛЯЮЩИЙ ПРОТИВООПУХОЛЕВУЮ АКТИВНОСТЬ | 1989 |
|
SU1651525A1 |
| СРЕДСТВО, ПРОЯВЛЯЮЩЕЕ АНТИАГРЕГАНТНУЮ И АНТИТРОМБОГЕННУЮ АКТИВНОСТИ | 2010 |
|
RU2453312C1 |
| ДИГИДРОХЛОРИД 1-(3-МОРФОЛИНОПРОПИЛ)-2-ФЕНИЛИМИДАЗО[1,2-a]-БЕНЗИМИДАЗОЛА, ПРОЯВЛЯЮЩИЙ СВОЙСТВА АНТАГОНИСТА ПУРИНОВЫХ P2Y-РЕЦЕПТОРОВ, АНТИАГРЕГАНТНУЮ И АНТИТРОМБОТИЧЕСКУЮ АКТИВНОСТЬ | 2008 |
|
RU2391345C2 |
| АНТИГЕЛЬМИНТНОЕ СРЕДСТВО | 2001 |
|
RU2219913C2 |
Настоящее изобретение относится к дигидрохлориду 3-циклогексиламинометилтиазоло[3,2-а]бензимидазола формулы I:
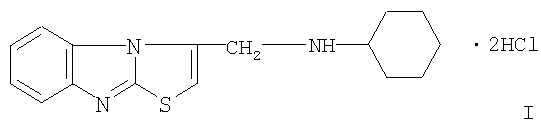
проявляющему иммунотропную и антиагрегационную активность. 1 з.п. ф-лы, 8 табл.
1. Дигидрохлорид 3-циклогексиламинометилтиазоло[3,2-а]бензимидазола формулы
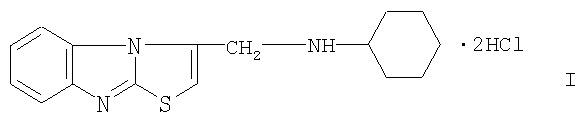
2. Соединение по п.1, обладающее иммунотропными и антиагрегационными свойствами.
| ДИАНОВ В.М | |||
| и др | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Химико-фармацевтический журнал, 1991, том 25, №1, стр.40-42 | |||
| Гидрохлориды 3-(3-хлор-4-алкоксифенил)-5,6-дигидроимидазо/2,1- @ /тиазолов,обладающие мутагенной активностью | 1980 |
|
SU910637A1 |
| Способ получения прозводных имидазо (2,1-в)тиазола или их солей в виде смеси изомеров или отдельных изомеров | 1978 |
|
SU873886A3 |
| 5Н-5-Оксоимидазо(2,1-в)-1,3-бензотиазины и способ их получения | 1987 |
|
SU1414849A1 |
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
Авторы
Даты
2010-12-10—Публикация
2009-07-14—Подача