Изобретение относится к области медицины, в том числе к диагностике онкогематологических заболеваний и предназначено для использования при проведении молекулярно-генетических исследований в клинико-диагностических лабораториях с целью диагностики хронических Ph-негативных миелопролиферативных новообразований.
В соответствии с клиническими рекомендациями [Barbui Т., Thiele J., Gisslinger Н., Finazzi G., Vannucchi A.M, Tefferi A. The 2016 revision of WHO classification of myeloproliferative neoplasms: Clinical and molecular advances. Blood Reviews, 2016. 30: 453-459] основным диагностическим критерием для постановки диагноза Ph-негативных миелопролиферативных новообразований, а именно истинной полицитемии (ИП), эссенциальной тромбоцитемии (ЭТ) и первичного миелофиброза (ПМФ) является выявление одной из пяти наиболее частых патогенетических соматических мутаций в генах янускиназы-2 (V617F JAK2), кальретикулина (CALR 1 типа - с. 1092_1143del и 2 типа - с. 1154_1155insTTGTC) и рецептора тромбопоэтина (MPL W515L и W515К).
Известен алгоритм лабораторной диагностики хронических миелопролиферативных новообразований [Ольховский И.А., Горбенко А.С., Субботина Т.Н., Столяр М.А. Современные возможности молекулярно-генетического анализа в диагностике хронических миелоидных опухолей. Медицинский алфавит, 2015. Т.4 (18): 44-46], который включает последовательное выполнение молекулярно-генетических тестов выявления отдельных мутаций. В лабораторной практике используется алгоритм, учитывающий частоту выявляемых мутаций: вначале выполняется тест на наличие мутации V617F JAK2, при его отрицательном результате - выполняют тест на мутации в гене кальретикулина (CALR 1 и 2 типов), а при их отрицательном значении - определяют мутации гена рецептора тромбопоэтина (MPL W515L и W515K). Выявление хотя бы одной из мутаций считается достаточным основанием для подтверждения диагноза и последующего молекулярно-генетического исследования других более редких патогенетических мутаций как правило не проводится.
Вместе с тем, имеются данные о достаточно частом одновременном сочетании разных патогенетически важных соматических мутаций у одного пациента и предлагается выделять их в отдельную клиническую группу, отличающуюся прогнозом развития заболевания и ответом на терапию [Ahmed RZ, Rashid М, Ahmed N, Nadeem M, Shamsi TS. Coexisting JAK2V617F and CALR Exon 9 Mutations in Myeloproliferative Neoplasms - Do They Designate a New Subtype? Asian Рас J Cancer Prev. 2016; 17(3):923-6].
Поскольку существующие наборы реагентов для выполнения наиболее распространенных в практике клинико-диагностических лабораторий методов детекции мутаций на основе реакции полимеразной цепной реакции (ПЦР) в реальном времени предусматривают возможность проведения исследования только мутаций в отдельных генах, выполнение полного лабораторного тестирования занимает достаточно большой промежуток времени. При этом продолжительность (время проведения) стандартной для медицинских лабораторий ПЦР превышает 3 часа.
Известно одновременное исследование всех возможных мутаций в ДНК с использованием методов секвенирования ДНК [Langabeer SE, Andrikovics Н, Asp J, et al. Molecular diagnostics of myeloproliferative neoplasms. Eur J Haematol. 2015, 95:270-279] и микрочипов
(https://tools.mermofisher.com/content/sfs/brochures/genomewide_snp6_datasheet.pdf).
Однако, требования к оборудованию и квалификации персонала, а также высокая трудоемкость выполнения и стоимость тестирования осложняет широкое использование данных методов в реальной практике клинико-диагностических лабораторий.
Известен способ, который заключается в использовании аллель-специфичных праймеров с регистрацией результатов ПЦР в режиме реального времени с использованием флуоресцентно-меченных проб. Реакционная смесь включает праймеры, отличающиеся для каждого аллеля, и общие для двух аллелей праймер и пробу, а также общий флуоресцентный зонд [RU, п. 2445373, МПК C12Q1/68, опубл. 20.03.2012 г., бюл. №8].
Недостатки способа заключаются в невозможности проведения мультиплексной реакции в виду использования одного флуоресцентного зонда общего для двух анализируемых аллелей.
Наиболее близким набором реактивов для выявления Ph-негативных миелопролиферативных новообразований, к заявляемому набору в группе изобретений, являются наборы реактивов, предлагаемые фирмой ООО «Генотехнология» для выявления мутации V617F в гене JAK2, мутаций 1 и 2 типа в гене CALR и мутаций W515L и W515K в гене MPL (http://www.genetechnology.ru/?q=node/98). (прототип).
Однако данные наборы позволяют выявлять эти мутации только в отдельных генах и в разных постановках ПЦР с помощью разных наборов, что существенно увеличивает время проведения анализа и затраты на его выполнение.
Наиболее близким способом к заявляемому способу в группе изобретений по совокупности признаков является способ диагностики вирусного иммунодефицита крупного рогатого скота методом полимеразной цепной реакции в режиме реального времени с использованием набора для выявления ДНК провируса иммунодефицита крупного рогатого скота содержащего пару специфичных праймеров и ДНК-зонд, следующего состава (5'-3'-): pf-TAGGGTAGTGGGATCTCAGAAATC, pr-ACATCCGTAACATCTCCTACCATC, z-GAGGATGGTAGGAGATGTTACGGAT, при этом реакционную смесь готовят путем смешения буфера 10-кратного для ПЦР - 2,5 мкл, дНТФ (25 мМ) - 0,2 мкл, праймеров pf и рr (10 пмоль/мкл) по 1 мкл, зонда z (10 пмоль/мкл) - 0,5 мкл, Taq полимеразы (5 ед./мкл) - 0,2 мкл, MgCl2 (50 мМ) - 2 мкл, бидистиллированной воды - 7.6 мкл, а амплификацию проводят в следующем режиме: денатурация-95°С-5 мин, циклирование: денатурация (95°С - 20 с) - отжиг (55°С - 20 с) - элонгация (72°С - 20 с), причем цикл денатурация - отжиг - элонгация повторяется 10 раз, циклирование 2 с детекцией: денатурация (95°С - 20 с) - отжиг (55°С - 20 с) - элонгация (72°С - 20 с), причем цикл денатурация - отжиг - элонгация повторяется 25 или 30 раз, при этом флуоресценцию измеряют по каналу Orange при температуре 55°С, и пересечение кривой флуоресценции линии threshold, установленной на уровне 30% от максимального уровня флуоресценции в последнем цикле амплификации, свидетельствует о наличии в образце провируса BIV, причем, чем меньше значение показателя «Ct», тем выше количество провируса BIV в исследуемом образце, в то время как отсутствие пересечения кривой флуоресценции линии threshold свидетельствует об отсутствии провируса BIV в образце [RU, 2595373, МПК C12N 15/49, C12Q 1/68, опубл. 27.08.2016 г., бюл. №24 (прототип)].
Недостаток этого способа заключается в том, что он предусматривает возможность выявления только одной искомой последовательности ДНК.
Задача изобретения - разработка набора реактивов для мультиплексного ПЦР анализа, а также ускоренного и экономичного способа диагностики Ph-негативных миелопролиферативных новообразований на его основе.
Техническим результатом достигаемым заявляемой группой изобретений является изготовление набора реактивов для мультиплексного ПЦР анализа, сокращение рабочего времени на выполнение лабораторных тестов и экономии расходных материалов.
Указанный единый технический результат при осуществлении группы изобретений по объекту набор реактивов достигается тем, что в наборе реактивов для выявления Ph-негативных миелопролиферативных новообразований, содержащем специфичные праймеры и флуоресцентно-меченые ДНК-зонды, новым является то, что он имеет следующий нуклеотидный состав (5-3'-):

в качестве источника флуоресценции в TaqMan зондах на 5' конце применяют красители: флуоресцеин (FAM) и хлорированный флуоресцеин (HEX), а для тушения флуоресценции используют Black Hole Quencher-1 (BHQ1) на 3' конце.
Указанный единый технический результат при осуществлении группы изобретений по объекту способу достигается тем, что в способе диагностики Ph-негативных миелопролиферативных новообразований, включающем проведение полимеразной цепной реакции в режиме реального времени путем смешивания буфера, дНТФ, специфичных праймеров, TaqMan зондов, Taq-полимеразы, MgCI2 и воды в оптимальных объемах и последующую амплификацию, новым является то, что используют мультиплексный вариант полимеразной цепной реакции, с участием специфичных праймеров и зондов имеющих следующий нуклеотидный состав (5'-3'-):
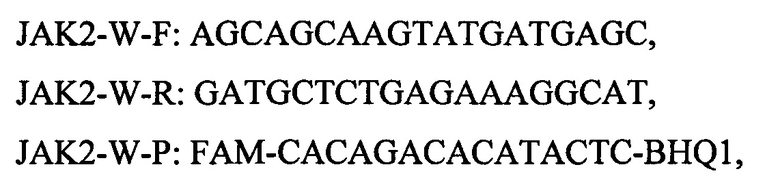

а амплификацию проводят в следующем режиме: предварительная активация при 95°С - 5 минут и последующие циклы включающие денатурацию при 95°С - 15 секунд, отжиг и элонгацию при 60°С - 60 секунд, цикл повторяют 50 раз, результат признают положительным, если значение порогового цикла (Ct) для образца не больше 32.
Заявляемая группа изобретений соответствует требованию единства изобретения, поскольку группа разнообъектных изобретений образует единый изобретательский замысел, причем один из заявляемых объектов - набор реактивов для выявления Ph-негативных миелопролиферативных новообразований, предназначен для использования в другом - способе диагностики Ph-негативных миелопролиферативных новообразований, при этом оба объекта группы изобретений направлены на решение одной и той же задачи с получением единого технического результата.
Сопоставительный анализ с прототипом позволил выявить совокупность существенных по отношению к техническому результату отличительных признаков для каждого из заявляемых объектов группы, изложенных в формулах. Следовательно, каждый из объектов группы изобретений соответствует критерию «новизна».
Из литературы и практики ПЦР-исследований неизвестно о способе мультиплексного ПЦР-анализа и (или) наборе реактивов для одновременного выявления отдельных патогенетических соматических мутаций V617F, с. 1092_1143del, c. 1154_1155insTTGTC, W515L, W515K в генах JAK2, CALR и MPL соответственно, которые были бы идентичны заявляемым, что позволяет сделать вывод о соответствии заявляемого решения критерию «изобретательский уровень».
Сущность изобретения поясняется с помощью графических материалов:
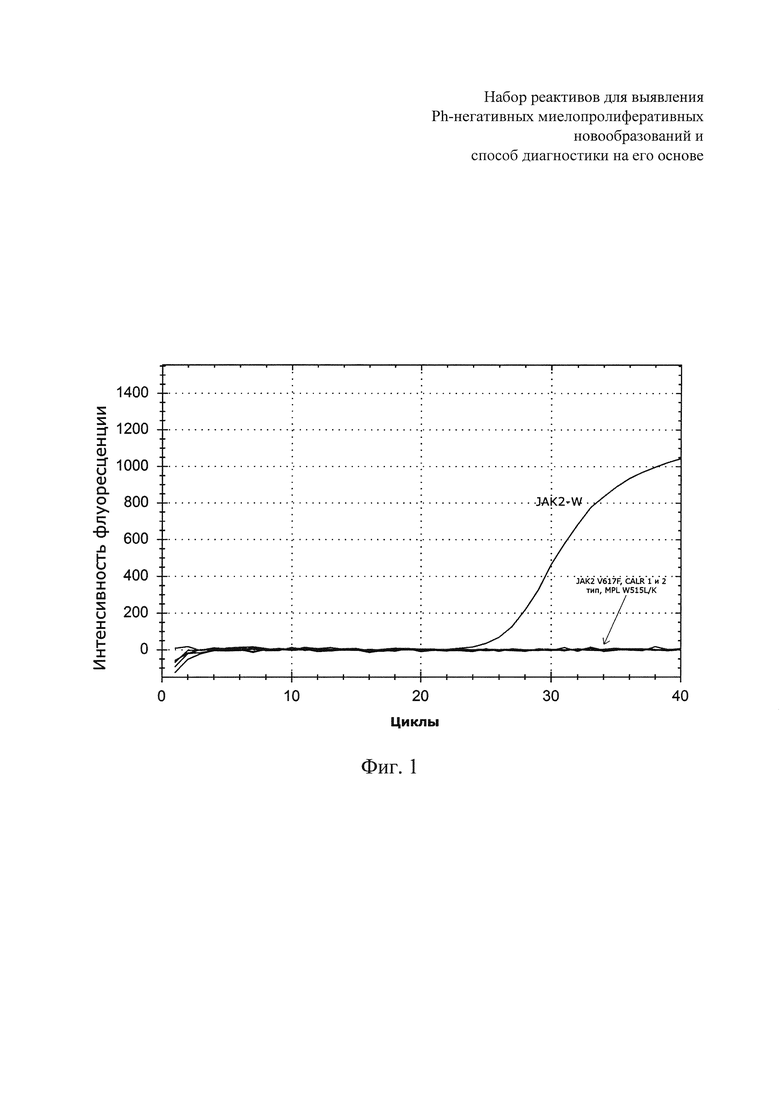
На фиг. 1 представлены кривые накопления флуоресцентного сигнала после проведения ПЦР-РВ для пробы без соматических мутаций.
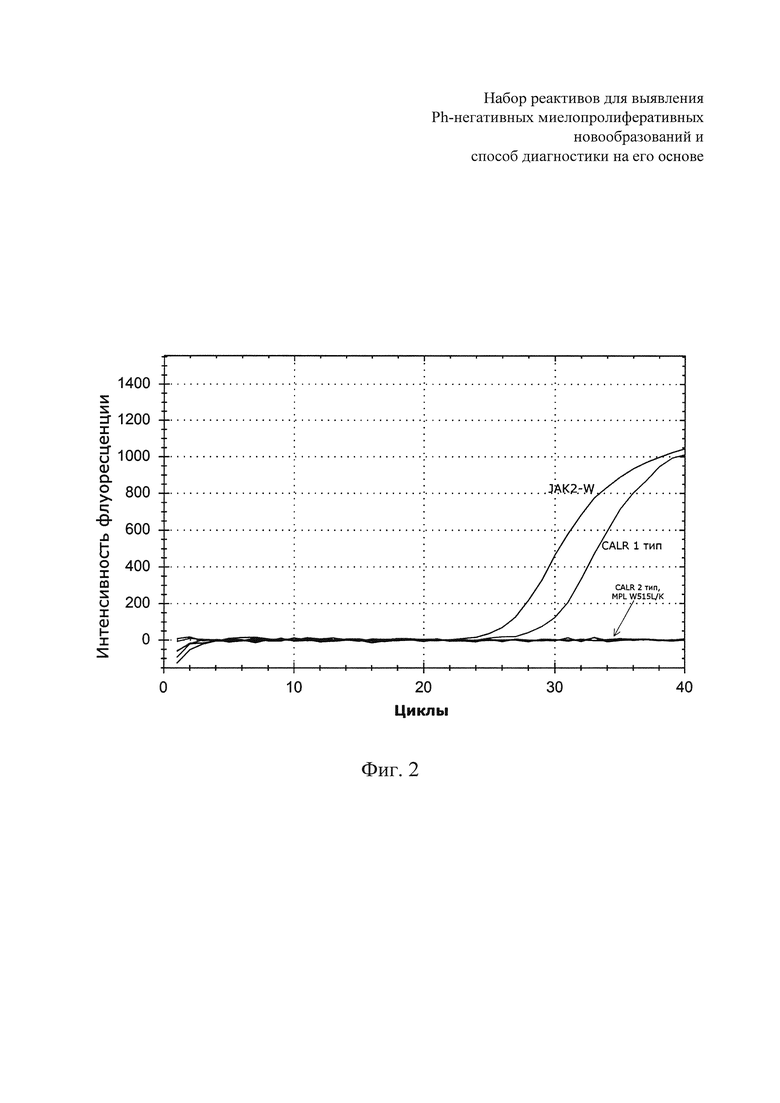
На фиг. 2 представлены кривые накопления флуоресцентного сигнала после проведения ПЦР-РВ для пробы с одной из пяти соматических мутаций.
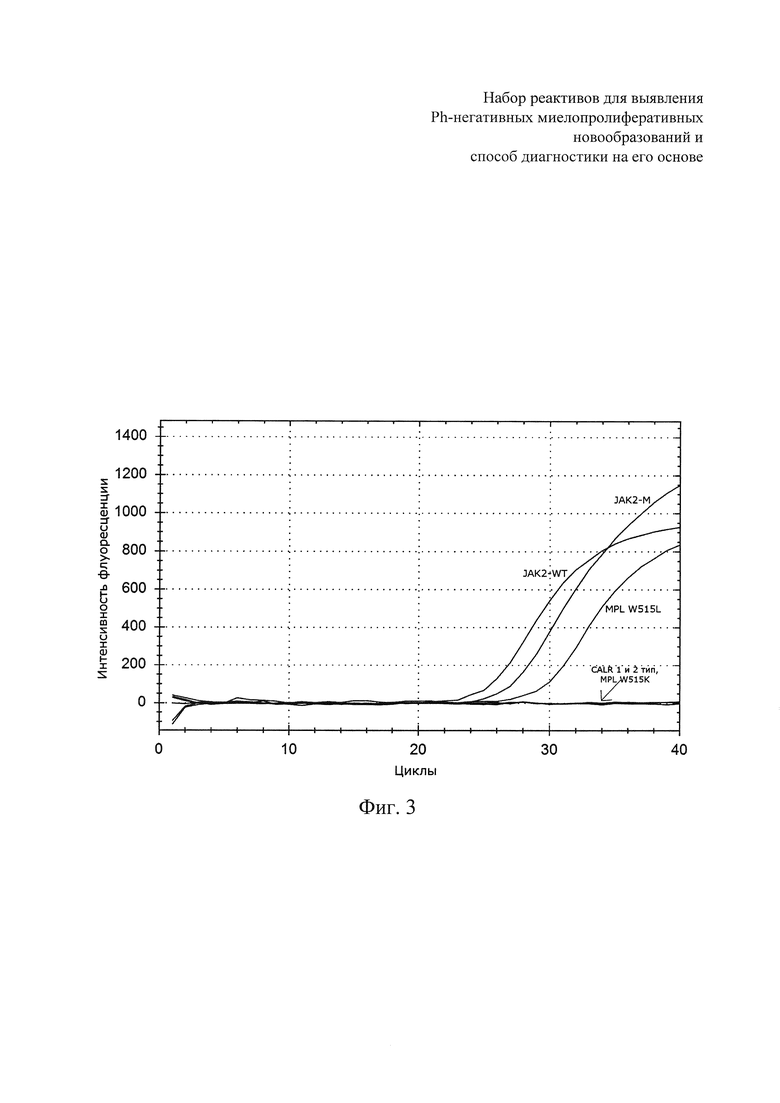
На фиг. 3 представлены кривые накопления флуоресцентного сигнала после проведения ПЦР-РВ для пробы одновременно с двумя соматическим мутациями.
Способ осуществляется следующим образом.
Образцы крови получают из локтевой вены и стабилизируются раствором ЭДТА К2 или 3,8% раствором цитрата натрия в объемном отношении 9:1. В процессе исследования кровь сохраняют в закрытых пластиковых пробирках при комнатной температуре, с соблюдением общепринятых мер предосторожности при работе с клетками крови. В качестве материала для исследования также возможно использование образцов крови в виде сухих капель на целлюлозном носителе, например, на бумаге типа ватман. В этом случае, для выделения ДНК использовали вырезанные фрагменты, пропитанные кровью, на пощади от 0,2 см2. Выделение ДНК из лейкоцитов цельной крови человека и из сухих пятен крови проводится стандартными методами, обеспечивающими выделение ДНК в количестве не менее 40 нг на один образец.
Далее с полученными образцами ДНК проводят мультиплексную ПЦР в режиме реального времени с использованием разработанного набора, содержащего четыре реакционных смеси: №1 (JAK2-W), №2 (JAK2-M), №3 (С ALR1+MPL-K), №4 (CALR2+MPL-L), Taq-полимеразу, положительный контрольный образец (ПКО) и отрицательный контрольный образец (ОКО). ПКО представляет собой человеческую геномную ДНК с наличием мутантных аллелей всех исследуемых генов. ОКО представляет собой человеческую геномную ДНК здорового донора, не имеющего мутаций в исследуемых генах.
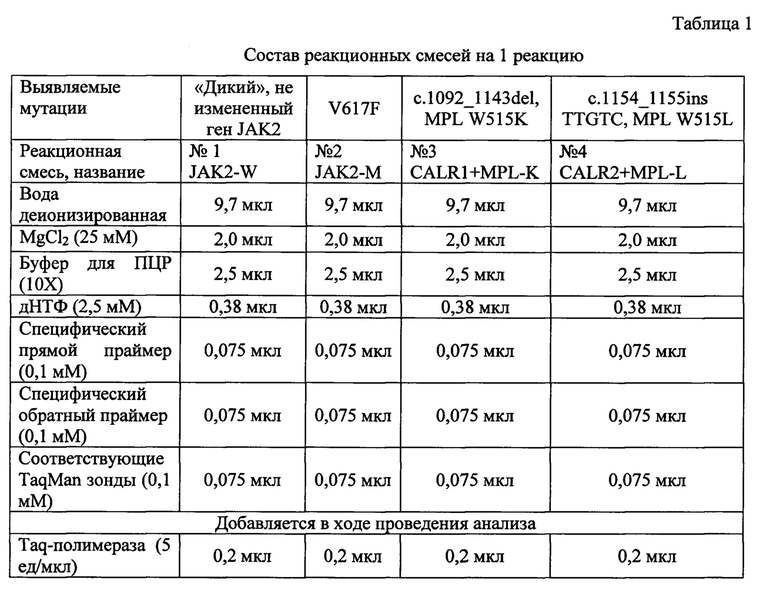
Указанные в таблице 1 реакционные смеси входящие в состав набора включают специфичные праймеры и зонды:
Реакционная смесь №1 используется для контроля прохождения реакции и качества выделенной ДНК, содержит праймеры JAK2-W-F, JAK2-W-R и зонд JAK2-W-P;
Реакционная смесь №2 содержит праймеры JAK2-M-F, JAK2-M-R и зонд JAK2-M-P
Реакционная смесь №3 содержит праймеры CALR-l-F, CALR-l-R, MPL-K-F, MPL-K-R и зонды CALR-1-P, MPL-K-P;
Реакционная смесь №4 содержит праймеры CALR-2-F, CALR-2-R, MPL-L-F, MPL-L-R и зонды CALR-2-P, MPL-L-P.
Праймеры и зонды подбирали с использованием программы «Primer 3». Подобранные последовательности были проанализированы в GenBank с помощью программы BLAST (таблица 2). По итогам анализа не было обнаружено последовательностей в геноме человека, гомологичных подобранным праймерам и зондам.
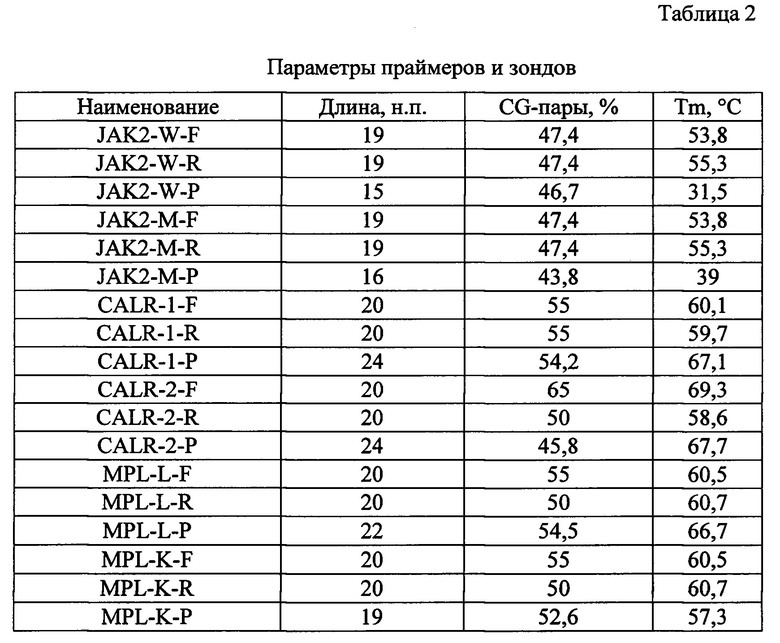
Примечание: Tm - температура плавления
Пример:
Мультиплексную полимеразную цепную реакцию проводят в смеси объемом 25 мкл на 1 пробу ДНК. Для каждого анализируемого образца ДНК пациента готовят 4 пробирки, в которые вносят реакционные смеси соответствующие номеру пробирки (таблица 1). В каждую пробирку добавляют Taq-полимеразу (5 ед/мкл) в объеме 0.2 мкл, а затем ДНК исследуемого образца с концентрацией не менее 40 нг в объеме 10 мкл. При каждом исследовании необходимо использовать две дополнительные пробирки в которые вместо ДНК вносят контрольные образцы ОКО и ПКО.
Температурно-временной режим проведения реакции для амплификатора «CFX96» («Bio-Rad», США) следующий: предварительная активация при 95°С - 5 минут и последующие циклы включающие денатурацию при 95°С - 15 секунд и отжиг и элонгацию при 60°С - 60 секунд, цикл повторяют 50 раз.
Полученные данные - кривые накопления флуоресцентного сигнала анализируют с помощью программного обеспечения используемого прибора для проведения ПЦР в режиме «реального времени» в соответствии с инструкцией к прибору (фиг. 1-3). Необходимо определять пороговый цикл (Ct) для каждой пробирки. Результат признают положительным в случае, если значение Ct для данного образца было не больше 32. Расчет количества мутантного аллеля осуществляют по формуле:
1. для мутации V617F в гене JАК2:
аллельная нагрузка = 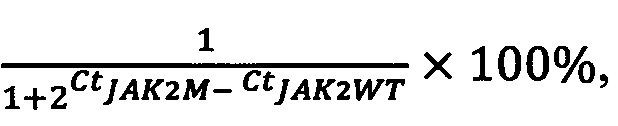
2. для мутаций 1 и 2 типа в гене CALR и мутаций W515L, W515К в гене MPL:
аллельная нагрузка = 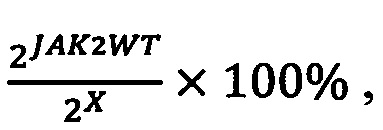 где
где
CtJAK2M - пороговый цикл мутантного аллеля JAK2;
CtJAK2WT - пороговый цикл аллеля дикого типа JAK2;
X - пороговый цикл одного из мутантных аллелей - CALR 1 типа, CALR 2 типа, MPL W515L, MPL W515K.
Кривые накопления флуоресцентного сигнала для образца, не содержащего ни одной из анализируемых мутаций, имеют вид, представленный на фиг. 1. На фиг. 2 представлены кривые для образца с одной соматической мутацией, в данном случае с мутацией CALR 1 типа. На фиг. 3 представлены кривые интенсивности флуоресценции для образца с двумя одновременно выявленными соматическими мутациями - JAK2 V617F и MPL W515L. Во всех примерах - по оси Х - указаны циклы амплификации, по оси У - уровень флюоресценции освобождающегося в реакции продукта амплификации
Проведенные нами исследования позволили разработать два сочетания четырех праймеров и двух TaqMan-зондов для выявления: мутаций CALR 1 тип + MPL W515K и CALR 2 тип + MPL W515L. При этом для идентификации мутантного гена (CALR или MPL) можно использовать TaqMan-зонды с разными флуоресцентными метками. Для выявления дикого (JAK2-W) и мутантного аллеля (JAK2-M) JAK2 были разработаны две соответствующие реакционные смеси, содержащие по два праймера и по одному TaqMan-зонду.
Была проведена сравнительная оценка результатов, полученных с помощью заявляемого способа с использованием заявляемого набора, с результатами, полученными с использованием праймеров, зондов и условий проведения ПЦР-РВ, описанных в следующих статьях:
1. Коммерческий набор фирмы НПО «Генотехнология»
2. Pancrazzi A, Guglielmelli Р, Ponziani V, et al. A Sensitive Detection Method for MPLW515L or MPLW515K Mutation in Chronic Myeloproliferative Disorders with Locked Nucleic Acid-Modified Probes and Real-Time Polymerase Chain Reaction. The Journal of Molecular Diagnostics. 2008; 10(5):435-441.
3. Chi J, Nicolaou KA, Nicolaidou V, et al. Calreticulin gene exon 9 frameshift mutations in patients with thrombocytosis. Leukemia. 2014; 28(5):1152-1154.
Параллельный анализ 20 образцов клинического материала от человека, установил, что во всех образцах совпали положительные результаты ПЦР (таблица 3).
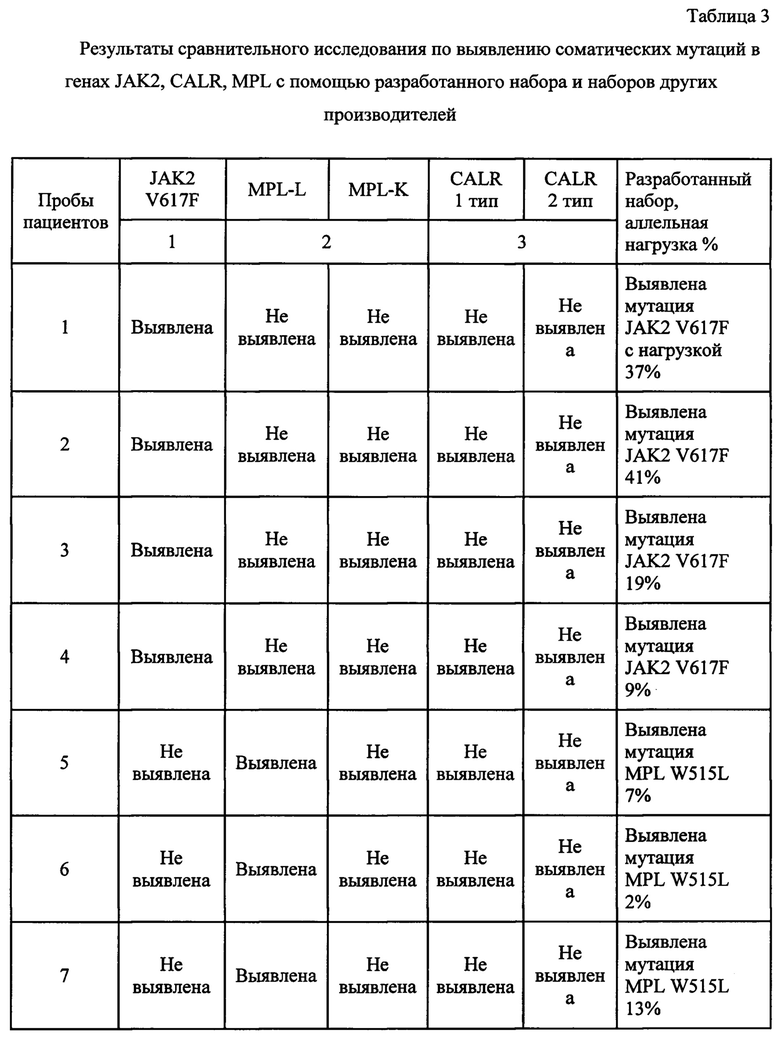
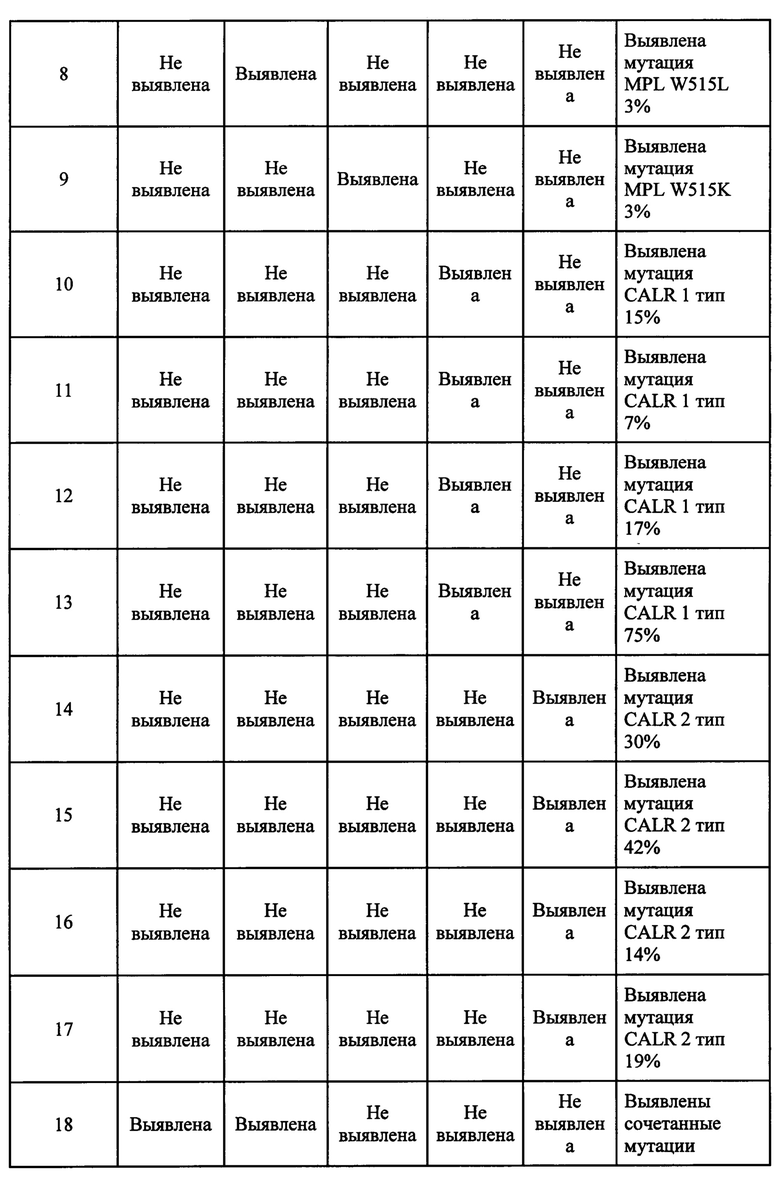
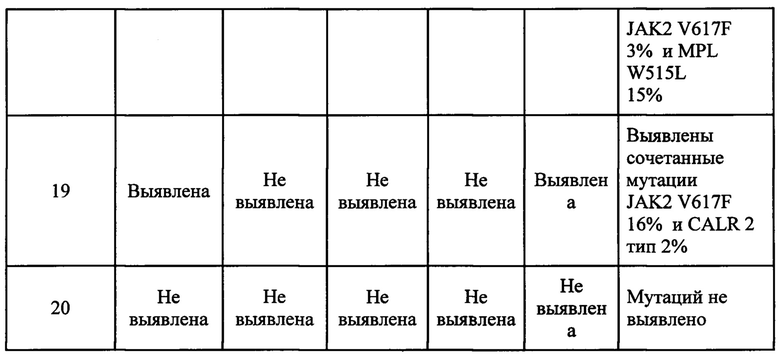
Преимуществом заявляемого изобретения является то, что разработанный набор реактивов и использование мультиплексной ПЦР позволяют проводить одновременное исследование нескольких мутаций в одной аналитической серии, с использованием стандартного оборудования клинико-диагностических лабораторий и имеющегося уровня квалификации персонала. А одновременное выполнение тестирования нескольких мутаций методом мультиплексной ПЦР в реальном времени позволяет получить результат в более короткие сроки, а также способствует более точной диагностике хронических Ph-негативных миелопролиферативных опухолей позволяя выявлять группу пациентов с наличием сочетанных патогенетических мутаций.
Группа изобретений относится к медицине, а именно к онкологии, и может быть использована для диагностики выявления Ph-негативных миелопролиферативных новообразований. Предложен набор, содержащий специфичные праймеры и флуоресцентно-меченые ДНК-зонды. Праймеры имеют следующий нуклеотидный состав (5'-3'-): JAK2-W-F, JAK2-W-R, JAK2-W-P, JAK2-M-F, JAK2-M-R, JAK2-M-P, CALR-l-F, CALR-l-R, MPL-K-F, MPL-K-R, CALR-1-P, MPL-K-P, CALR-2-F, CALR-2-R, MPL-L-F, MPL-L-R, CALR-2-P, MPL-L-P. В TaqMan зондах на 5' конце применяют красители: флуоресцеин (FAM) и хлорированный флуоресцеин (HEX). Для тушения флуоресценции используют Black Hole Quencher-1 (BHQ1) на 3' конце. Также предложен способ диагностики Ph-негативных миелопролиферативных новообразований, включающий проведение полимеразной цепной реакции в режиме реального времени. Группа изобретений позволяет проводить одновременное исследование нескольких мутаций в одной аналитической серии, что приводит к результату в более короткие сроки. А также обеспечивает точную диагностику хронических Ph-негативных миелопролиферативных опухолей, позволяет выявлять группу пациентов с наличием сочетанных патогенетических мутаций. 2 н.п. ф-лы, 3 ил., 3 табл., 1 пр.
1. Набор реактивов для выявления Ph-негативных миелопролиферативных новообразований, содержащий специфичные праймеры и флуоресцентно-меченые ДНК-зонды, ОТЛИЧАЮЩИЙСЯ тем, что имеет следующий нуклеотидный состав (5'-3'-):

в качестве источника флуоресценции в TaqMan зондах на 5' конце применяют красители: флуоресцеин (FAM) и хлорированный флуоресцеин (HEX), а для тушения флуоресценции используют Black Hole Quencher-1 (BHQ1) на 3' конце.
2.Способ диагностики Ph-негативных миелопролиферативных новообразований, включающий проведение полимеразной цепной реакции в режиме реального времени путем смешивания буфера, дНТФ, специфичных праймеров, TaqMan зондов, Taq-полимеразы, MgCI2 и воды в оптимальных объемах и последующую амплификацию, ОТЛИЧАЮЩИЙСЯ тем, что используют мультиплексный вариант полимеразной цепной реакции с участием специфичных праймеров и зондов, имеющих следующий нуклеотидный состав (5'-3'-): 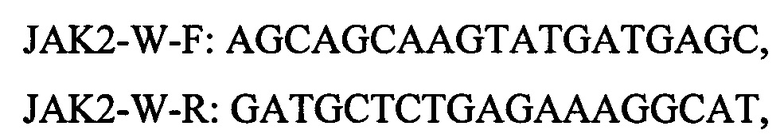

а амплификацию проводят в следующем режиме: предварительная активация при 95°С - 5 минут и последующие циклы, включающие денатурацию при 95°С - 15 секунд, отжиг и элонгацию при 60°С - 60 секунд, цикл повторяют 50 раз, результат признают положительным, если значение порогового цикла (Ct) для образца не больше 32.
| ДУНАЕВА Е | |||
| А | |||
| и др | |||
| КОМПЛЕКС МЕТОДИК, ОСНОВАННЫХ НА ТЕХНОЛОГИИ ПИРОСЕКВЕНИРОВАНИЯ, ДЛЯ ДИАГНОСТИКИ Ph-НЕГАТИВНЫХ ХРОНИЧЕСКИХ МИЕЛОПРОЛИФЕРАТИВНЫХ НЕОПЛАЗИЙ //МОЛЕКУЛЯРНАЯ ДИАГНОСТИКА 2017 | |||
| Автомобиль-сани, движущиеся на полозьях посредством устанавливающихся по высоте колес с шинами | 1924 |
|
SU2017A1 |
| - С | |||
| Канатное устройство для подъема и перемещения сыпучих и раздробленных тел | 1923 |
|
SU155A1 |
| СПОСОБ РАННЕЙ ГЕНЕТИЧЕСКОЙ ДИАГНОСТИКИ РИСКА РАЗВИТИЯ САХАРНОГО ДИАБЕТА 2 ТИПА | 2017 |
|
RU2655635C1 |
| US 20150079091 A1, 19.03.2015 | |||
| МЕЛИКЯН А | |||
| Л | |||
| и др | |||
| Клинические рекомендации по диагностике и терапии Ph-негативных миелопролиферативных заболеваний (истинная полицитемия, эссенциальная тромбоцитемия, первичный миелофиброз) //Гематология и трансфузиология | |||
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| - Т | |||
| Устройство для охлаждения водою паров жидкостей, кипящих выше воды, в применении к разделению смесей жидкостей при перегонке с дефлегматором | 1915 |
|
SU59A1 |
| - N | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| VAN ETTEN R | |||
| A | |||
| et al | |||
| The Ph-positive and Ph-negative myeloproliferative neoplasms: some topical pre-clinical and clinical issues //Haematologica | |||
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| - Т | |||
| Приспособление в пере для письма с целью увеличения на нем запаса чернил и уменьшения скорости их высыхания | 1917 |
|
SU96A1 |
| - | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| - С | |||
| Промывально-чесальная машина для выделения волокон из хвои | 1920 |
|
SU590A1 |
Авторы
Даты
2019-02-12—Публикация
2018-08-01—Подача