Родственная заявка
[01] По настоящей заявке испрашивается приоритет в соответствии с предварительной заявкой на патент США № 62/429782, поданной 3 декабря 2016 г., которая полностью включена в настоящий документ посредством ссылки для всех целей.
Государственные лицензионные права
[02] Настоящее изобретение выполнялось при государственной поддержке в рамках грантов № R01AI118805 и № 2R56AI021548, присужденных NIH/NIAID. Правительство имеет определенные права на изобретение.
Перечень последовательностей
[03] Настоящая заявка содержит перечень последовательностей, который был представлен одновременно в формате ASCII и полностью включен как часть настоящего описания.
Область техники, к которой относится настоящее изобретение
[04] Настоящие варианты осуществления относятся к рекомбинантным пневмококковым белкам, к экспрессирующим их рекомбинантным генетическим конструкциям и к содержащим эти белки антигенам, иммуногенам и вакцинам.
Предшествующий уровень техники настоящего изобретения
[05] Streptococcus pneumoniae, также известный как пневмококк, является основной причиной смерти от бактериальной пневмонии во всем мире. Он также является основной причиной менингита и бактериальной инфекции крови (сепсис), состояний, которые классифицируются как инвазивное пневмококковое заболевание (IPD). Его жертвами являются в основном маленькие дети и пожилые люди. Даже сегодня при широком распространении вакцин в Соединенных Штатах ежегодно происходит приблизительно 50000 случаев пневмококковой бактериемии и 5000 случаев менингита. Более 25% этих пациентов умирают, а у выживших от менингита, как правило, имеются необратимые нарушения; и более 120000 американцев ежегодно подвергаются госпитализации в связи с пневмококковой пневмонией, при которой сепсис не подтвержден. Кроме того, пневмококк представляет собой основную причину развития воспаления среднего уха у детей.
[06] В настоящее время одобренные вакцины содержат несколько пневмококковых поверхностных полисахаридов (также известных как капсульные антигены), либо конъюгированных с белком-носителем (пневмококковые конъюгатные вакцины: PCV), либо неконъюгированных (пневмококковые полисахаридные вакцины: PPSV). Существует более восьмидесяти пневмококковых серотипов, каждый из которых характеризуется капсульным антигеном, поэтому, несмотря на то, что существующие PCV эффективны против нескольких серотипов, они, как правило, не обеспечивают широкой защиты от заболевания, поскольку подавляющее большинство капсульных антигенов просто не включены в вакцины. Данные из нескольких стран указывают на то, что после введения PCV уровень заболеваемостью IPD резко снизился до уровня менее чем 10% от уровня, предшествующего периоду введению PCV; но показатели IPD недавно превысили половину уровня до периода введения PCV у младенцев и превысили уровня до периода введения PCV у пожилых людей. Это увеличение обусловлено почти исключительно серотипами пневмококка, которые не покрывают PCV. Таким образом, существует большая и растущая потребность в вакцине, которая характеризуется более широким охватом против пневмококковой инфекции, чем те, которые предлагаются в настоящее время. Наконец, в отношении PPSV эти вакцины не вызывают защитных иммунных реакций у детей и вызывают только слабые или умеренные реакции у пожилых людей против 23 капсульных антигенов, включенных в эту вакцину.
Сущность изобретения
[07] Согласно настоящим вариантам осуществления предусмотрен новый белок- иммуноген, который максимизирует перекрестную реактивность и обеспечивает защиту от широкого спектра пневмококковых серотипов. Более конкретно, описанные в настоящем документе рекомбинантные конструкции обеспечивают отобранные связанные части поверхностного белка пневмококка A (PspA), которые могут обеспечить широкий иммунитет против пневмококковой инфекции, включая в себя пневмонию, менингит и сепсис, вызванные S. pneumoniae. В частности, эти варианты осуществления обеспечивают новые рекомбинантные антигенные и иммуногенные белки, содержащие альфа-спиральный домен (aHD) или его часть и богатый пролином домен (PRD) или его часть, причем каждый домен происходит из белка PspA другого штамма пневмококка; рекомбинантный белок, упоминаемый в настоящем документе как конструкция aHD-PRD. Настоящие варианты осуществления также предусматривают вакцины, содержащие по меньшей мере одну конструкцию aHD-PRD, такую как одна, две, три или четыре конструкции aHD-PRD. Вакцина может дополнительно содержать рекомбинантный белок aHD, который не связан с полипептидом PRD. В вакцине, содержащей более одной конструкции aHD-PRD, соответствующие части PRD каждой конструкции могут быть выбраны из одной, двух или трех разных групп PRD, которые не были охарактеризованы ранее. Кроме того, согласно настоящим вариантам осуществления предусмотрены молекулы нуклеиновой кислоты (например, ДНК), которые кодируют аминокислоты, составляющие конструкции aHD-PRD; векторы, содержащие такие молекулы нуклеиновой кислоты; рекомбинантные клетки-хозяева, содержащие такие молекулы нуклеиновой кислоты или векторы; продукты экспрессии таких молекул нуклеиновых кислот; применение таких молекул нуклеиновой кислоты для экспрессии конструкций aHD-PRD рекомбинантными способами и применение продуктов экспрессии для вызывания иммунного или защитного ответа против пневмококкового заболевания у подходящего хозяина.
[08] Согласно одному аспекту настоящих вариантов осуществления предусмотрен искусственный химерный белок, состоящий из комбинации антигенного белка aHD и антигенного полипептида PRD: конструкция aHD-PRD. Другими словами, конкретные варианты осуществления предусматривают альфа-спиральные домены PspA или их части (aHD), связанные с богатыми пролином доменами PspA или их частями (PRD) (т.е. слитыми или химерными белками), способными индуцировать иммунный ответ против пневмококкового заболевания (далее по тексту, конструкции aHD-PRD). Согласно некоторым вариантам осуществления aHD связан с PRD прямой пептидной связью конец- в-конец; т.е. C-конец aHD связан пептидной связью непосредственно с N-концом PRD. Согласно некоторым вариантам осуществления aHD и PRD связаны через пептидный «линкер». Согласно другим вариантам осуществления aHD и PRD связаны или конъюгированы через химический фрагмент. Согласно некоторым вариантам осуществления иммуногенная конструкция aHD-PRD или комбинация конструкций aHD- PRD при использовании в качестве компонента вакцины обеспечивает защитный иммунитет против пневмококкового заболевания. Согласно другим вариантам осуществления комбинация конструкций aHD-PRD и несвязанных aHD, когда они используются в качестве компонентов вакцины, обеспечивают защитный иммунитет против пневмококкового заболевания.
[09] Согласно другому аспекту предусмотрен процесс выбора aHD и PRD для включения во множество конструкций aHD-PRD, причем этот процесс выбора максимизирует вероятность защитной перекрестной реактивности против патогенных пневмококков. В частности, конструкции aHD-PRD, содержащие одну из трех различных групп PRD, могут быть выбраны на основе паттерна аминокислотных последовательностей, которые характеризуют эти PRD в группы. Согласно одному варианту осуществления способ предусматривает (а) отбор первого аHD из первой клады в первом семействе пневмококковых серотипов для включения в первую конструкцию aHD-PRD и выбор первого PRD из первой группы серотипов PRD для включения в первую конструкцию aHD-PRD; и (b) выбор второго aHD из второй клады в первом или втором семействе пневмококковых серотипов для включения во вторую конструкцию aHD-PRD и выбор второго PRD из второй группы серотипов PRD для включения во вторую конструкцию aHD-PRD. Этот процесс может быть повторен, чтобы выбрать дополнительные, различные пары aHD и PRD для разработки множества конструкций aHD-PRD.
[010] Согласно дополнительному варианту осуществления предусмотрен способ выбора по меньшей мере одного дополнительного aHD для дополнения композиции, содержащей по меньшей мере одну конструкцию aHD-PRD, причем aHD не связан с PRD и причем несвязанный aHD выбирают таким образом, чтобы увеличить иммуногенную перекрестную реактивность для расширенного охвата пневмококковыми штаммами. Например, дополнительный aHD может быть выбран из клады или семейства, не представленных в конструкции aHD-PRD.
[011] Согласно конкретному варианту осуществления предусмотрена антигенная композиция, иммуногенная композиция или вакцина, содержащая множество конструкций aHD-PRD, причем aHD и PRD выбирают в соответствии с описанным в настоящем документе способом. Согласно дополнительному конкретному варианту осуществления предусмотрена иммуногенная композиция или вакцина, содержащая три конструкции aHD-PRD, причем aHD и PRD выбирают в соответствии с описанным в настоящем документе способом.
[012] По меньшей мере согласно одному варианту осуществления предусмотрена иммуногенная композиция или вакцина, содержащая по меньшей мере один из описанных в настоящем документе белков или конструкций, например, по меньшей мере одну конструкцию aHD-PRD и по меньшей мере один адъювант. Вакцина может дополнительно содержать по меньшей мере один дополнительный несвязанный aHD.
[013] Согласно другому аспекту настоящих вариантов осуществления предусмотрены составы и способы доставки вакцины, как описано в настоящем документе, например, подходящие для введения составы и способы введения таких составов вакцин. Согласно одному варианту осуществления предусмотрена описанная в настоящем документе вакцина, т.е. содержащая по меньшей мере одну конструкцию aHD- PRD, составленную для внутримышечной (IM) инъекции. Согласно другому варианту осуществления предусмотрена описанная в настоящем документе вакцина, составленная для введения через слизистую оболочку; и согласно конкретному варианту осуществления предусмотрены составы, которые можно вводить интраназально (IN), перорально (например, сублингвально [SL]) или путем распыления в бронхи легких. Согласно конкретному варианту осуществления предусмотрена вакцина, содержащая по меньшей мере одну конструкцию aHD-PRD, заключенную в наногель для введения через слизистую поверхность. Например, наногель может содержать несущий катионную холестериновую группу пуллулан (cCHP).
[014] Дополнительный аспект настоящего варианта осуществления относится к антигенным или иммуногенным комбинациям, содержащим другие антигены. По меньшей мере согласно одному варианту осуществления предусмотрены вакцины или иммуногенные композиции, содержащие по меньшей мере одну конструкцию aHD-PRD и по меньшей мере один другой антиген, причем другой антиген усиливает иммунный ответ против S. pneumonia. Согласно конкретному варианту осуществления предусмотрена вакцина против S. pneumonia, содержащая по меньшей мере одну конструкцию aHD-PRD и по меньшей мере один другой антиген S. pneumoniae, такой как пневмолизин или нейраминидаза.
[015] Согласно другому аспекту настоящих вариантов осуществления предусмотрен процесс экспрессии конструкций aHD-PRD с использованием генетически модифицированных клеток, включая в себя генетически модифицированные микроорганизмы. Соответственно, согласно варианту осуществления предусмотрены рекомбинантные нуклеиновые кислоты (полинуклеотиды) (такие как молекулы ДНК), которые кодируют антигенные или иммуногенные конструкции aHD-PRD. Согласно варианту осуществления предусмотрены выделенные молекулы синтетической ДНК или молекулы рекомбинантной ДНК (включая в себя кДНК и полусинтетическую кДНК), которые кодируют описанные в настоящем документе конструкции aHD-PRD.
[016] Описанные в настоящем документе рекомбинантные конструкции aHD-PRD предусматривают выбранные части PspA, которые могут обеспечивать широкий иммунитет против пневмококкового заболевания, включая в себя пневмонию, менингит и сепсис, вызванные S. pneumoniae. В частности, согласно этим вариантам осуществления предусмотрены антигены и иммуногены, содержащие альфа-спиральные домены (aHD) и богатые пролином домены (PRD) PspA; гены или части генов, кодирующие аминокислотные последовательности, которые составляют конструкции aHD-PRD, их применение для экспрессии конструкций aHD-PRD рекомбинантными способами и их применение в вакцинах. Настоящие варианты осуществления также относятся к вакцинам, содержащим одну или несколько из этих иммуногенных конструкций aHD-PRD.
Краткое описание графических материалов
[017] На фиг. 1 показана структура доменов PspA и схематическое отношение PspA к поверхности пневмококковой бактерии; показаны положения и относительные размеры aHD, PRD и холин-связывающих областей, а также связь PspA с поверхностной структурой S. pneumoniae.
[018] Фиг. 2А представляет собой вариант осуществления диаграммы древовидной структуры, в которой сопоставлено 136 штаммов пневмококка, проанализированных и сгруппированных в соответствии с гомологией аминокислот определяющих кладу (CDR) областей в aHD их белков PspA. Группы семейств также указаны. Древовидная диаграмма была построена таким образом, чтобы сумма длин вертикальных линий, соединяющих любые два штамма (или среднее значение любых двух клад), была пропорциональна вероятности аминокислотной замены в любом положении вдоль последовательности CDR, т.е. пропорциональна степени различия в гомологии CDR. Длина ключевой полосы соответствует в среднем 0,2 однопарным аминокислотным заменам на сайт для одинаковой длины вертикального разделения между любым из 136 проанализированных видов. Смотрите пример 2. Стрелками указаны штаммы, из которых были получены пептиды aHD/CDR, используемые в четырех иллюстративных вариантов осуществления конструкций aHD-PRD. Фиг. 2B представляет собой покомпонентное изображение фиг. 2А, на которой показаны штаммы, содержащие PRD группы 1 (светло-серый шрифт) в своих белках PspA (смотрите фиг. 3A-фиг. 3D); на фиг. 2C показаны штаммы, содержащие PRD группы 2 (черный шрифт) и на фиг. 2D показаны штаммы, содержащие PRD группы 3 (серый шрифт).
[019] Фиг. 3 представляет собой вариант новой древовидной диаграммы 136 штаммов пневмококка (тех же штаммов, что и на фиг. 2А), сгруппированных по гомологии аминокислот среди PRD их белков PspA. Насколько известно авторам настоящего изобретения, PRD впервые были охарактеризованы таким образом: выявлены три группы PRD. Группа 1: шрифт полужирный курсив; группа 2: жирный шрифт; группа 3: обычный шрифт; стрелки указывают на штаммы, которые обеспечивали компоненты PRD четырех вариантов осуществления конструкций aHD-PRD, как указано. Фиг. 3B представляет собой покомпонентное изображение фиг. 3А, показывающее представителей группы 1 PRD; на фиг. 3C показаны представители группы 2 PRD; на фиг. 3D показаны представители группы 3 PRD. Шрифт на фиг. 3А показывает, как можно сгруппировать разнообразие среди PRD; и эта информация может использоваться для разработки компонентов вакцины, которые охватывают каждую группу и обеспечивают перекрестную реактивность по меньшей мере в этой группе. Из-за большого количества повторяющихся мотивов в каждой из групп PRD, а также различий в длинах PRD, суммарная длина вертикальных линий, соединяющих штаммы/группы, не позволяет надежно оценить вероятность сайт-специфических замен одной пары аминокислот между видами/группами, как это было возможно для CDR на фиг. 2.
[020] На фиг. 4 показан анализ высокой чистоты ((LDS-PAGE) трех продуктов экспрессии из бактерий-хозяев, генетически сконструированных для получения иллюстративных вариантов осуществления рекомбинантных слитых белков aHD-PRD. Дорожка М: стандарт белка; дорожка 1: 1 мкг/дорожка; дорожка 2: 5 мкг/дорожка, дорожка 3: 10 мкг/дорожка.
[021] На фиг. 5 показана перекрестная реактивность, характеризуемая концентрацией антигенспецифической сыворотки на конструкцию. Титры ИФА сывороточного антигенспецифического IgG (реципрокный log2) определяли в отношении каждой из трех конструкций aHD-PRD (PspA 01.1, PspA 02 или pspA 03) путем иммунизации кроликов IM единственными конструкциями aHD-PRD (два кролика на конструкцию, каждый из которых обозначен конструкцией и суффиксом «R1» или «R2»). Титры, производимые против неиммунизирующих конструкций, указывают на степень перекрестной реактивности против разнородных антигенов PspA. Смотрите пример 4.
[022] На фиг. 6А и фиг. 6B показаны антигенспецифические ответы сывороточных IgG у мышей (n=5 на группу) после первичной (белый) и повторной (черный) IM- иммунизации отдельными иллюстративными конструкциями aHD-PRD (n=5 на группу, столбцы показывают стандартные отклонения, два уровня дозы [фиг. 6А: 3 мкг/доза; фиг. 6В: 10 мкг/доза] для каждой из трех конструкций). Ось y: обратный log2 титр ИФА; столбцы показывают стандартные отклонения. Эти данные иллюстрируют способность IM-иммунизации вызывать сильный антигенспецифический системный IgG-ответ.
[023] На фиг. 7А и фиг. 7B показаны антигенспецифические сывороточные IgG- ответы у мышей (n=5 на группу) после первичной (белый) и вторичной (черный) IN- иммунизации (назально вводимый состав наногеля) индивидуальными иллюстративными конструкциями cCHP-aHD-PRD. Комплексы наногеля (т.е. cCHP-aHD-PRD) получали путем термообработки при двух разных температурах (фиг. 7A: 40°C; фиг.7B: 50°C). Ось у: обратный log2 титр ИФА; столбцы показывают стандартные отклонения; в соответствии с иммунизирующим антигеном. Эти данные иллюстрируют способность каждого из назально вводимых антигенов, составленных в виде наногелей, вызывать сильный системный антигенспецифический IgG-ответ.
[024] На фиг. 8А и фиг. 8B показаны антигенспецифические сывороточные IgG- ответы у мышей после IM (фиг. 8A) или IN (фиг. 8B) иммунизации (включая в себя вторичные) тремя иллюстративными конструкциями aHD-PRD, вводимыми вместе (n=60 на группу, дозы IM, составленные с квасцами, дозы IN, составленные с наногелем). Ось y: обратный log2 титр ИФА; столбцы показывают стандартные отклонения; в соответствии с иммунизирующим антигеном в группе IM или IN. Эти данные показывают, что комбинированное введение антигенов aHD-PRD вызывает сильные системные антигенспецифические IgG-ответы и что ответы, вызванные введением IN-наногеля, эквивалентны ответам, полученным при введении IM.
[025] На фиг. 9 показаны кривые выживаемости после интраназального заражения пятью пневмококковыми штаммами у контрольных мышей (не иммунизированных) и мышей, иммунизированных смесью трех иллюстративных конструкций aHD-PRD (IM или IN; n=10 на группу). Ось у: процент выживания; ось x: дни после интраназального заражения колониеобразующими единицами (КОЕ) на мышь из следующих штаммов: штамм BG8838: 1×108 КОЕ; A66.1: 1×105 КОЕ; BG12730: 1×108 КОЕ; 3JYP2670: 1×106 КОЕ; ATCC6303: 1×107 КОЕ. ○ контроль; ▲ IN; ■ IM; *плохо охвачены PCV13 и PPSV23; **не распространяется на PPSV23. Эти данные свидетельствуют о том, что иммунизация наногелем IM или IN с тремя конструкциями aHD-PRD защищает от пневмококкового заболевания. Защита распространяется даже против штаммов с кладами PspA aHD, не представленных в вакцинных антигенах, и против капсульных типов, не охватываемых современными вакцинами.
Подробное описание изобретения
[026] Следует понимать, что настоящее изобретение не ограничено конкретными описанными в настоящем документе методологиями, протоколами, реагентами и т.д. и, как таковые, они могут варьировать. Используемая в настоящем документе терминология предназначена только для описания конкретных вариантов осуществления и не предназначена для ограничения объема настоящего изобретения, который определяется исключительно формулой изобретения.
[027] Все идентифицированные патенты и другие публикации включены в настоящий документ посредством ссылки с целью описания и раскрытия, например, описанных в таких публикациях методологий, которые могут использоваться в связи с настоящим изобретением, но не предназначены для предоставления определений терминов, несовместимых с представленными в настоящем документе. Эти публикации предоставлены исключительно для их раскрытия до даты подачи настоящей заявки. Ничто в этом отношении не должно быть истолковано как признание того, что авторы настоящего изобретения не имеют права предшествовать такому раскрытию в силу предшествующего изобретения или по любой другой причине. Все заявления относительно даты или представления относительно содержания этих документов основаны на информации, доступной заявителям, и не представляют собой какого-либо признания в отношении правильности дат или содержания этих документов.
[028] Используемые в настоящем документе и в формуле изобретения формы единственного числа включают в себя ссылку на множественное число, если контекст явно не указывает на иное. Во всем настоящем описании, если не указано иное, «содержат», «содержит» и «содержащий» используются включительно, а не исключительно, так что указанное целое число или группа целых чисел могут включать в себя одно или несколько других неуказанных целых чисел или группы целых чисел. Термин «или» является включающим, если не изменен, например, «либо». Таким образом, если контекст не указывает иное, слово «или» означает любого одного представителя конкретного перечня, а также включает в себя любую комбинацию представителей этого перечня.
[029] Все значения являются приблизительными, так как существует некоторое колебание в соотношении молекул-носителей (например, наногеля) или адъюванта (например, квасцов) к антигену, точных композиций этих молекул-носителей, адъювантов и антигенов и в процессах составления. Соответственно, кроме как в рабочих примерах или там, где указано иное, все числа, выражающие количества или условия реакции, используемые в настоящем документе, следует понимать как измененные во всех случаях термином «приблизительно», если не указано иное; «приблизительно» относится, как правило, к ±1% от обозначенного значения, но может допускать ±5% или ±10% от обозначенного значения, как принято в соответствующем контексте специалистом в настоящей области техники.
[030] Способы рекомбинантной ДНК могут быть выполнены в соответствии со стандартными протоколами, известными в настоящей области техники. Смотрите, например, Sambrook et al., Molecular Cloning: Lab. Manual (2nd Ed., Cold Spring Harbor Lab. Press, NY, 1989); Ausubel et al., Current Protocols Molec. Biol. (1994 и дополнения); DNA Cloning: Practical Approach, Vols. 1-4 (Glover & Hames, Eds., IRL Press 1995, 1996), Croy, Plant Molec. Biol. Labfax (BIOS Sci. Pub. Ltd. & Blackwell Sci. Pub., UK, 1993); WO 2015089587.
[031] Заголовки даны только для удобства и не должны рассматриваться как ограничивающие каким-либо образом настоящее изобретение. Если не указано иное, все технические и научные термины, используемые в настоящем документе, имеют то же значение, что и общепринятые для специалиста в настоящей области техники. Используемая в настоящем документе терминология предназначена только для описания конкретных вариантов осуществления и не предназначена для ограничения объема настоящего изобретения, который определяется исключительно формулой изобретения. Для того чтобы настоящее раскрытие могло быть более легко понято, некоторые термины определены; дополнительные определения изложены в подробном описании.
[032] Антиген представляет собой вещество, которое распознается продуктом иммунного ответа. При соответствующих условиях антиген способен действовать как иммуноген: вызывая специфический иммунный ответ в организме; и, соответственно, антиген способен реагировать с продуктом(ами) этого ответа. Вообще говоря, специфическими продуктами иммунного ответа могут быть антитела, которые специфически связываются с антигеном, или Т-лимфоциты, которые сенсибилизированы для реакции с антигеном. Антигены включают в себя чужеродные вещества, такие как белки или их части (полипептиды или пептиды), нуклеиновые кислоты или полисахариды бактерии, вируса, гриба или другого микроба.
[033] Под перекрестной реактивностью, как правило, понимают степень, в которой иммунный ответ на определенный антиген также охватывает другие антигены. Антигены или патогены, которые вызывают наиболее защитные реакции, часто имеют переменную структуру. В случае вакцины, предназначенной для создания защитного ответа против инфекционного микроорганизма, перекрестная реактивность, как правило, относится к степени, в которой иммунный ответ на конкретные антигены в вакцине производит антитела, которые реагируют не только с иммунизирующими антигенами, но также с более широким набором вариантов одного и того же антигена у разных штаммов патогенного организма. Поскольку коммерческое производство вакцины, содержащей все варианты такого антигена, зачастую нецелесообразно, тщательный отбор ряда вариантов антигенов, обладающих высокой перекрестной реактивностью, из ограниченного числа штаммов может вызывать появление антител, которые реагируют на штаммы с множеством разных вариантов антигенов. В случае пневмококка капсульные полисахаридные антигены (т.е. антигены в современных вакцинах) характеризуются низкой перекрестной реактивностью. Некоторые белковые антигены, в частности PspA, обладают высокой перекрестной реактивностью.
[034] Иммунный ответ (иммуногенный ответ) представляет собой ответ хозяина на антиген, на который влияют элементы иммунной системы. Элементы иммунной системы, наиболее часто участвующие в иммунных реакциях, представляют собой лейкоциты (белые клетки), состоящие из нейтрофилов, базофилов, эозинофилов, моноцитов и их потомства, а также лимфоцитов. Лимфоциты, в свою очередь, могут быть классифицированы на естественные клетки-киллеры; В-клетки, которые производят антитела; и Т-клетки, которые представлены различными типами, которые регулируют или усиливают различные аспекты иммунного ответа. Большинство вакцин предназначено для вызывания адаптивного иммунного ответа, который предусматривает идентификацию вакцинного антигена как «чужеродного» с последующим образованием молекул антител или Т-клеток, которые реагируют с этими антигенами. Эффективные реакции антител и Т-клеток могут привести к разрушению патогенов, проявляющих такие антигены. Эффективные ответы антител также могут мешать функционированию молекул вирулентности, которые находятся на поверхности патогена или высвобождаются патогеном.
[035] Иммуноген представляет собой вещество, способное производить иммунный ответ, как правило, антиген. Более конкретно, иммуноген относится к молекуле, которая способна вызывать иммунный ответ иммунной системы организма, тогда как антиген относится к молекуле (гаптену), которая способна связываться с продуктом этого иммунного ответа. Следовательно, иммуноген, как правило, представляет собой антиген, но антиген не обязательно может быть иммуногеном. Соответственно, иммуногенность это способность вызывать гуморальные или клеточно-опосредованные иммунные ответы. Например, когда B-клетка активируется иммуногеном, она дифференцируется в плазматическую B-клетку, которая производит антитела, которые связываются с антигеном. В контексте пневмококковых вакцин капсульные полисахариды представляют собой антигены, но не действуют как иммуногены у детей, если они не конъюгированы с белком-носителем.
[036] Вакцина представляет собой композицию, используемую для индукции иммунного ответа, как правило, для обеспечения специфического и защитного иммунитета против конкретного заболевания, не вызывая тяжелой формы этого заболевания. В случае вакцин против инфекционных заболеваний, вакцина, как правило, содержит средство, которое напоминает антиген(ы) болезнетворного патогена. Часто это средство представляет собой ослабленную (аттенуированную) или убитую форму патогена, его токсоиды (нетоксичные версии токсинов) или один из его поверхностных белков или поверхностных полисахаридов. Средство имитирует патогенный иммуноген и стимулирует иммунную систему организма распознавать патоген как чужеродный (т.е. антиген) и уничтожать его или уничтожать клетки, содержащие патоген. В идеале вакцина также заставляет иммунную систему «запоминать» иммуноген и патоген, из которого он был получен, так что иммунной системе будет легче распознавать и нейтрализовать антигены патогена в будущем. Вакцинные композиции могут быть составлены в любой подходящей форме и могут включать в себя фармацевтически приемлемые вспомогательные вещества, такие как разбавители или носители, или дополнительные ингредиенты. Вспомогательные вещества, как правило, не способствуют эффектам, вызываемым иммуногенами по настоящему изобретению при введении; но предусмотрены ингредиенты или соединения, которые способствуют или модулируют действие настоящих иммуногенных конструкций: в частности, адъюванты. Специалист в настоящей области техники может определить такие подходящие вспомогательные вещества, которые хорошо известны и, в случае вакцин для человека и животных, одобрены FDA. Вакцины можно вводить в соответствующей лекарственной форме путем инъекции, проглатывания, нанесения на кожу или нанесения на поверхности слизистых оболочек.
[037] Как отмечено выше, согласно настоящим вариантам осуществления предусмотрены новые антигены, иммуногены и вакцины против S. pneumoniae, основной причины смерти от бактериальной пневмонии во всем мире, основной причины IPD и основной причины развития воспаления среднего уха у детей.
[038] На основе антигенных капсульных полисахаридов, покрывающих клеточную стенку бактерии, было идентифицировано почти 100 серотипов пневмококка. Современные пневмококковые вакцины содержат смесь нескольких капсульных полисахаридов. Самая ранняя одобренная пневмококковая полисахаридная вакцина (известная как вакцина PPSV14 или Pneumovax®, одобренная FDA в 1977 году) содержала капсульные полисахариды из четырнадцати обычно встречающихся пневмококковых серотипов. Эти антигены были неконъюгированными, т.е. полисахариды не были присоединены (конъюгированы) к белкам, которые служат костимуляторами иммунной системы. Позже была введена вакцина PPSV23 (вакцина Pneumovax®23, одобренная FDA в 1983 году), содержащая дополнительно девять неконъюгированных полисахаридных капсульных антигенов. Однако дети в возрасте до 2 лет, как правило, не реагируют на неконъюгированные капсульные антигены в этих вакцинах. Wald, 40 Clin. Pediatr. 601 (2001). Кроме того, защита у детей старшего возраста является низкой в существующих медицинских условиях. У взрослых в возрасте старше 65 лет PPSV23 снижает риск развития пневмонии, связанной с сепсисом, приблизительно на 45%; но не снижает общий риск развития пневмонии и, вероятно, не снижает общий риск смерти в течение трех лет после вакцинации. Jackson et al., 348 N. Engl. J. Med. (2003); Ladhani et al., 58 Clin. Infect. Dis. 517 (2014).
[039] Более поздние вакцины содержат капсульные полисахариды, конъюгированные с молекулой белка, которая стимулирует иммунную систему. Эти пневмококковые конъюгатные вакцины (PCV) активируют как Т-клеточный иммунный ответ, так и антителообразующий В-клеточный (гуморальный) ответ. Было показано, что PCV снижают риск IPD благодаря охваченным серотипам более чем на 95% у младенцев. Большое исследование среди взрослых в возрасте старше 66 лет показало, что иммунизация PCV на 75% снижает риск развития связанной с сепсисом пневмонии, вызванной охваченными вакциной серотипами, в то же время снижая риск пневмонии без сепсиса благодаря охваченным серотипам приблизительно на 45%. Bonten et al., 372 N. Engl. J. Med. 1114 (2015).
[040] Хотя семь серотипов в первой вакцине PCV (вакцина PCV7 или Prevnar®, одобренная FDA в 2000 г.) выбирали для охвата наиболее распространенных и вирулентных серотипов, частота заболеваемости из-за неохваченных серотипов вскоре начала увеличиваться в популяционном иммунитете, повышенном вакцинами, это явление называется заменой серотипа. В ответ было добавлено еще шесть серотипов для создания PCV13 (вакцина Prevnar13®, одобренная FDA в 2010 году), которая заменила PCV7 в качестве стандарта медицинской помощи в большинстве развитых стран. Несмотря на снижение заболеваемости из-за недавно охваченных шести серотипов, замена серотипов не ослабевает, и показатели заболеваемости могут возрасти из-за серотипов, отличных от тринадцати, охватываемых PCV13. Более конкретно, данные из нескольких стран показывают, что, хотя показатели заболеваемости IPD резко снизились после введения PCV7 - до менее чем 10% от показателей заболеваемости в период до PCV - эти показатели в последнее время превысили половину уровня до вакцины PCV у младенцев и превысили уровни до PCV у пожилых людей. Это увеличение почти полностью обусловлено серотипами, не охваченными PCV-13. CDC, Pink Book 13th Ed. (2015); Leputre et al., 33 Vaccine 359 (2015); Public Health England (Mar. 4, 2016).
[041] Таким образом, существует огромная и возрастающая потребность в пневмококковой вакцине, которая характеризуется более широким охватом, чем PCV13. Простое добавление многих дополнительных капсульных полисахаридных антигенов к PCV13 может в конечном итоге потерпеть неудачу, потому что: (1) процесс конъюгирования полисахаридных антигенов технически сложен и (2) вероятно, что по мере добавления большего количества антигенов иммунные ответы против каждого из существующих тринадцати капсульных антигенов будут уменьшаться, явление, известное как антигенная конкуренция. Paton & Bosiego, Protein Vaccines 421 (Siber, ed., ASM Press, 2008); Andrews et al., 14 Lancet Infect. Dis. 839 (2014).
[042] Пневмококковые белки могут обеспечивать иммуногенную альтернативу обычным вакцинам PPSV и PCV. Было обнаружено несколько антигенных белков вблизи поверхности пневмококков (смотрите фиг. 1). Пневмококковый поверхностный белок A (PspA) является одним из наиболее многообещающих из них с точки зрения антигенности, представленности на поверхности, иммуногенности, перекрестной реактивности среди его различных штаммов и степени, в которой уже произошло некоторое развитие в качестве вакцины. Смотрите патенты США № 6592876 (Briles et al., 2003) и № 5997882 (Briles et al., 1999); Ginsberg et al., 11 Expert Rev. Vaccines 279 (2012); Moreno et al., 17 Clin. Vaccine Immunol. 439 (2010); Daniels et al., 40 Microbial Path. 228 (2006). В своем нативном состоянии PspA функционирует для уменьшения индуцированной пневмококками активации комплемента и, таким образом, является основным фактором выживания и вирулентности пневмококка у инфицированного хозяина. Наиболее дистальное удлинение PspA от поверхности пневмококка (т.е. N-концевой участок PspA) состоит из 280-380 аминокислот, известных как альфа-спиральный домен (aHD) (смотрите фиг. 1). Из всех областей PspA aHD наиболее изучен с точки зрения безопасности и эффективности в качестве вакцинного антигена. Патенты США № 6592876, № 6638516 (Briles et al., 2003); Briles et al., 18 Vaccine 1707 (2000a); Hollingshead et al., 68 Infect. Immun. 5889 (2000); Nabors et al., 18 Vaccine 1743 (2000).
[043] Совсем недавно было показано, что богатый пролином домен (PRD) PspA, который простирается от проксимального С-конца aHD до бактериальной мембраны, также является иммуногенным. Патент США № 8808704 (Hollingshead & Briles, 2014); Daniels et al., 78 Infect. Immun. 2163 (2010). Предыдущие исследования, однако, не полностью распознавали или характеризовали разнообразие PRD, не исследовали перекрестную реактивность PRD и не пытались включить PRD в иммуногенные вакцины на основе описанной в настоящем документе конструкции aHD-PRD.
[044] Проблема, связанная с разработкой эффективных вакцин PspA, заключается в том, чтобы индуцировать сильную перекрестную реактивность против большинства форм PspA, обнаруженных в патогенных пневмококках, при использовании антигенных областей относительно небольшого числа различных белков PspA, чтобы избежать антигенной конкуренции и обеспечить простую в изготовлении вакцину. Эти проблемы разработки не являются уникальными для вакцин на основе PspA, но остаются сложными для разработки и производства большинства вакцин.
[045] Сообщалось, что 30% проксимального конца (С-конца) aHD является его наиболее иммуногенной областью. Hollingshead et al., 2000. Эта часть aHD известна как определяющая кладу область (CDR) PspA. На основе аминокислотных последовательностей их определяющих кладу областей (CDR), aHD могут быть сгруппированы в два основных семейства, которые вместе составляют приблизительно 98% известных патогенных подтипов. Эти семейства, в свою очередь, могут быть сгруппированы в пять клад (клада 1 и клада 2 составляют семейство 1; клады 3, 4 и 5 составляют семейство 2), в зависимости от их аминокислотных последовательностей. Третье семейство состоит только из клады 6 и составляет только приблизительно 2,2% S. pneumoniae, выделенного от пациентов (Hollingshead et al., 2000; Vela Coral et al., 7 Emerging Infect. Dis. 823 (2001); Hotomi et al., PloS one 8:e58124 (2013) и только 3 из 136 уникальных штаммов S. pneumoniae, чьи последовательности генов PspA охарактеризованы в настоящем документе (смотрите пример 2). аHD из одной и той же клады характеризуются сходными аминокислотными последовательностями, в то время как aHD из клад разных семейств характеризуются наименьшей гомологией. Hollingshead & Briles, 2000. Фиг. 2 представляет собой древовидную диаграмму 136 пневмококковых штаммов, чьи последовательности генов PspA проанализировали авторы настоящего изобретения. На ней показаны эти штаммы, картированные в соответствии с гомологией среди аминокислот, которые составляют их CDR. Это подтверждает более ранние исследования кластеризации CDR на три семейства (два из которых являются клинически значимыми) и шесть клад (пять из которых являются клинически значимыми).
[046] Неожиданно исследование также показало, что CDR многих штаммов в одной и той же кладе идентичны, а еще большее число сходно. Это говорит о том, что aHD, содержащие CDR, которые являются общими для ряда клинически важных штаммов, вероятно, являются главными кандидатами на вакцинные антигены. Кроме того, фиг. 2 позволяет приблизительное количественное определение степени гомологии между CDR любого пневмококкового семейства, клады или характеризуемого штамма (смотрите пример 2). Таким образом, древовидная диаграмма на фиг. 2A-фиг. 2D и подробные виды на ней обеспечивают новое и полезное руководство для стратегического выбора ограниченного числа aHD (и их высоко антигенных CDR) для включения в качестве вакцинных антигенов, чтобы максимизировать перекрестную реактивность между выбранными aHD и aHD штаммов пневмококка, не включенных в вакцину.
[047] В отличие от полисахаридных капсульных антигенов, которые характеризуются низкой иммунной перекрестной реактивностью, антитела, вызванные воздействием определенного aHD, как правило, проявляют перекрестную реактивность; не только против пневмококков из одной и той же клады PspA, но также против пневмококков из разных клад в одном и том же семействе (патент США № 6638516; McDaniel et al., 59 Infect. Immun. 222 (1991); Nabors et al., 2000; Vela Coral et al., 2001, Darrieux et al., 75 Infect. Immun. 5930 (2007) и даже, в случае некоторых иммунизирующих aHD, против пневмококков из другого семейства PspA (Roche et al., 71 Infect. Immun. 1033 (2003), Darrieux et al., 57 J. Med. Micro. 273 (2008), Moreno et al., 2010, Fukuyama et al., 2015). Эта перекрестная реактивность в отношении пневмококков с различными aHD поддерживает настоящую стратегию выбора, с новыми указаниями на фиг. 2, относительно небольшого числа aHD в качестве компонентов вакцины, которая может защищать от широкого спектра патогенных пневмококков.
[048] Важно и совершенно неожиданно, что анализ аминокислотных последовательностей PRD во многих штаммах пневмококка показал, что PRD можно определить в одну из трех отдельных групп на основе последовательностей аминокислот, характеризующих PRD (фиг. 3A-фиг. 3D). Внутри каждой из этих групп не только высоки гомологии последовательностей, но часто появляются характерные мотивы повторяющихся аминокислотных последовательностей (таблица 1-таблица 4). Неожиданно оказалось, что многие PRD из разных пневмококковых штаммов в каждой группе идентичны, что помогает сузить диапазон возможных антигенов PRD для включения в вакцину. По меньшей мере некоторые из этих PRD (или их частей) являются антигенными (примеры 4, 6, ниже) (смотрите также патент США № 8808704; Daniels et al., 2010). Из-за высокого сходства повторяющихся мотивов в группах PRD, перекрестная реактивность в группах PRD, вероятно, может оказаться высокой. Таким образом, вакцина, которая содержит по меньшей мере один PRD из каждой из трех групп, характеризуется более высокой вероятностью индукции иммунного ответа, который охватывает многие штаммы патогенных пневмококков. На фиг. 3А-фиг. 3D представлена новая древовидная диаграмма и ее детали для 136 штаммов пневмококка, PRD которых проанализировали авторы настоящего изобретения. Таким образом, древовидная диаграмма на фиг. 3А-фиг. 3D предусматривает новое и полезное руководство для стратегического выбора ограниченного числа PRD для включения в качестве вакцинных антигенов, что максимизирует перекрестную реактивность между выбранными PRD и PRD штаммов пневмококка, не включенных в вакцину.
[049] Настоящие варианты осуществления также обеспечивают подтверждение того, усиливают ли или уменьшают ли определенные признаки PRD иммуногенность. Например, длинные повторы PKPAPA (SEQ ID NO: 7), характерные для полипептидов PRD группы 2, могут быть менее иммуногенными, чем более разнообразные мотивы, обнаруженные в группах 1 и 3, особенно непролиновые блоки (NPB), которые характеризуют группу 3. Daniels, 2010. Как отмечено, выбор PRD также может руководствоваться фиг. 3, на которой представлен новый подход, который предлагает, как в конкретной группе PRD выбрать в качестве кандидата на вакцину конкретный PRD, который относительно близок по гомологии к другим PRD в той же группе. При прочих равных условиях (таких как длина) это может максимизировать вероятность обширной перекрестной реактивности по меньшей мере с другими PRD той же группы.
[050] Комбинируя отбор PRD (или частей PRD) из каждой из трех групп PRD с отбором высокоиммуногенных и перекрестно-реактивных aHD (или их частей) из каждого из семейств aHD для обеспечения одной вакцины, авторы настоящего изобретения могут производить сильный, избыточный, перекрестно-реактивный иммунитет, который защищает почти от всех патогенных штаммов пневмококка.
[051] После этого рассуждения, по меньшей мере согласно одному варианту осуществления предусмотрены рекомбинантные белковые конструкции, которые объединяют один aHD и один PRD (или их части), которые отдельно являются высокоиммуногенными и перекрестно-реактивными (примеры 4 и 5, фиг. 6-фиг. 7). Кроме того, по меньшей мере согласно одному варианту осуществления предусмотрена комбинация множества конструкций aHD-PRD в одной процедуре вакцинации: у лабораторных животных относительно небольшое количество конструкций aHD-PRD, например, трех конструкций aHD-PRD, защищало испытуемых от широкого спектра заражения штаммами, независимо от того, вводятся ли они системно (например, IM) или интраназально (IN) с использованием описанной в настоящем документе композиции наногеля. Штаммы, используемые в защитном заражении, представляют собой не только разные клады PspA и группы PRD, но также представляют собой разные капсульные полисахаридные штаммы. В частности, например, согласно настоящим вариантам осуществления предусмотрена вакцина, которая защищает от штаммов, которые недостаточно хорошо охватываются PCV13 или PPCV23 (пример 6). Таким образом, иммунизация смесью приблизительно трех различных конструкций aHD-PRD может защитить от большинства патогенных пневмококков.
[052] Кроме того, подсегменты aHD и PRD в каждой вакцинной конструкции не обязательно должны быть из одного и того же штамма пневмококка, но могут быть выбраны более широко для оптимальной перекрестной защиты. Например, некоторые из наиболее антигенных конструкций aHD-PRD объединяют с aHD и PRD из штаммов различных клад PspA или иногда из разных семейств PspA.
[053] Хотя было высказано предположение, что пневмококковая вакцина может включать в себя aHD вместе с его встречающимся в природе PRD, как в белке PspA (публикация патента US20150320851; Piao et al., 32 Vaccine 5607 (2014); Darrieux et al., 2007), эти публикации не ссылаются на концепцию характеристики отдельных групп PRD или целесообразного выбора PRD из максимально возможного числа из трех различных групп PRD. Фактически, насколько известно авторам настоящего изобретения, гомологии PDR ранее не были охарактеризованы или отображены, как показано на фиг. 3A. Эти публикации также не описывают и не предлагают химерные слитые белки настоящих конструкций aHD-PRD. Эти публикации также не относятся к вакцине, которая является относительно простой и легкой в изготовлении: композиция, содержащая относительно небольшое количество химерных антигенных белков, которая также сводит к минимуму риск конкуренции антигенов. Вкратце, в этих публикациях не описано и не предлагается создание эффективной (и универсальной) пневмококковой вакцины из трех простых в изготовлении рекомбинантных конструкций aHD-PRD, каждая из которых характеризуется размером не более чем 60 килодальтон (кДа).
[054] Описанные в настоящем документе варианты осуществления вакцин обеспечивают защиту не только при системном введении (т.е. внутримышечно (IM), как в случае большинства вакцин), но также при применении на поверхностях слизистой оболочки носа и полости рта. Предыдущие исследования показали, что люди, которым вводили IM aHD, производили антитела, которые защищали мышей от иного фатального пневмококкового заражения. Briles et al., 182 J. Infect. Dis. 1694 (2000b). Также показано, что составы IM антигенов aHD с использованием Al(OH)3 в качестве адъюванта безопасны для человека. Briles et al., 2000a; Nabors et al., 2000.
[055] Что касается иммунизации IN, состав IN для слизистой оболочки согласно настоящим вариантам осуществления включает в себя в качестве молекулы для доставки гидрофильный полисахарид, к которому были добавлены гидрофобные боковые цепи холестерина. Вариант осуществления такой молекулы доставки также включает в себя положительно заряженные функциональные группы, такие как катионные аминогруппы, на своей поверхности или возле нее. Это позволяет комплексу антиген-молекула доставки дольше удерживаться на отрицательно заряженной поверхности слизистой оболочки носа. Еще один вариант осуществления этой молекулы доставки включает в себя гидрофильный полисахарид пуллулан, полимер мальтотриозных звеньев. Пуллулан применяют в качестве антиоксиданта в косметических и фармацевтических покрытиях, в качестве пищевой добавки и консерванта, а также для полоскания рта, например, средство для полоскания рта LISTERINE® или пластинки для свежести дыхания LISTERINE POCKETPAKS®. Таким образом, конкретный вариант осуществления молекулы для назальной доставки представляет собой несущий катионную холестериновую группу пуллулан (cCHP или наногель). Смотрите патент США № 8961983 (Akiyoshi et al., 2015); WO 2015/122518 (Kiyono et al., 2015). Изготовление варианта осуществления cCHP описано в примере 5.
[056] Предыдущие сообщения указывают на то, что назальные составы, содержащие один антиген aHD, захваченный молекулой cCHP, вызывали сильные защитные иммунные ответы у мышей и нечеловекообразных приматов. Kong et al., 81 Infect. Immun. 1625 (2013); Fukuyama et al., 8 Mucosal Immun. 1144 (2015). В дополнение к защите от летального заражения, иммунизация IN вызывала Т-клеточные иммунные ответы, которые способствовали общему долгосрочному иммунитету, а также предотвращали бактериальную колонизацию в носовых ходах мышей. Успех иммунизации на основе cCHP может быть обусловлен тем, что наногель, по-видимому, защищает белок-иммуноген и продлевает его присутствие на поверхности слизистой оболочки носа, обеспечивая его постепенное всасывание в слизистую оболочку и поглощение ее дендритными клетками на базальной мембране слизистой оболочки. Nochi et al., 9 Nat. Mats. 572 (2010); Kong et al., 2013; Fukuyama et al., 2015. Эта особенность применяется независимо от того, является ли антиген, секвестрируемый в cCHP, конструкцией aHD-PRD или несвязанным aHD. Введение этого IN состава нечеловекообразным приматам не было связано с какими-либо побочными эффектами. В частности, не наблюдалось проникновения наногеля или антигена в обонятельную луковицу или другие части центральной нервной системы. Fukuyama et al, 2015.
[057] Описанные в настоящем документе конструкции aHD-PRD являются стабильными при производстве в рекомбинантных клетках-хозяевах. Конструкции aHD- PRD могут быть экспрессированы в бесклеточной системе экспрессии или в рекомбинантных клетках-хозяевах, таких как бактерии (например, штамм Escherichia coli B, штамм E. coli K12, Corynebacterium ammoniagenes, C. glutamicum, Serratia liquefaciens, Streptomyces lividans и Pseudomonas putida); Baculovirus; грибы, такие как Penicillium camembertii, Acremonium chrysogenum, или дрожжи (например, Saccharomyces cerevisiae и Pichia pastoris); клетки яичника китайского хомяка (СНО) или другие системы экспрессии млекопитающих, системы экспрессии растений и другие рекомбинантные системы экспрессии, известные в настоящей области техники. Процесс генной инженерии, необходимый для такой экспрессии, известен специалистам в настоящей области техники. В случае бактериальных систем экспрессии бактерии генетически сконструированы так, чтобы они содержали векторы (плазмиды), кодирующие желательные конструкции aHD- PRD (смотрите пример 3). В настоящем документе раскрыты четыре варианта осуществления конкретных конструкций aHD-PRD, экспрессированных в рекомбинантных бактериях, полученных с высокой чистотой и выходами (смотрите, например, фиг.4). В дополнение к производству в рекомбинантных системах экспрессии иммуногены согласно настоящим вариантам осуществления могут быть получены полностью синтетическими способами или комбинацией способов рекомбинантного и химического синтеза.
[058] Для получения конструкции посредством экспрессии в рекомбинантных хозяевах на основании ссылки на фиг. 2А-фиг. 3Е, представленных в настоящем документе аминокислотных последовательностей, и знаниях генетического кода специалист в настоящей области техники может сконструировать молекулу нуклеиновой кислоты (например, ДНК), которая кодирует такие слитые белки; необязательно, оптимизированные для экспрессии в желаемой системе клеток-хозяев. Например, ген, кодирующий PspA01.1, может быть получен синтезом de novo: ссылаясь на аминокислотную последовательность SEQ ID NO.1, специалист может выполнить обратную трансляцию выбранной последовательности в последовательность нуклеиновой кислоты и получить синтезированную соответственно молекулу. Специалист в настоящей области техники может также ввести одну или несколько мутаций, включая в себя вставки, замены и делеции, в выбранную аминокислотную последовательность или соответствующую последовательность нуклеиновой кислоты. Для обратной трансляции специалист в настоящей области техники может, как правило, использовать кодоны нуклеиновых кислот, которые отражают частоту кодонов системы-хозяина, предназначенной для экспрессии. Термин «кодон-оптимизированный» хорошо известен в настоящей области техники: кодон-оптимизированная нуклеиновая кислота (полинуклеотид) модифицируется по сравнению с последовательностью нуклеиновой кислоты в организме, из которой происходит эта последовательность, в том смысле, что ее адаптируют к использованию кодона в одном или больше видов хозяев. Как правило, полинуклеотид, в частности кодирующая область, адаптирован для экспрессии в данном организме (таком как бактериальный штамм) путем замены по меньшей мере одного кодона по меньшей мере одним кодоном, который чаще используется в генах планируемого организма-хозяина.
[059] Ссылка на молекулы нуклеиновой кислоты или полинуклеотиды также охватывает варианты или производные конкретных полинуклеотидов, обсуждаемых в настоящем документе, включая в себя ортологи, паралоги или другие гомологи полинуклеотидов или их варианты или производные. Варианты или производные нуклеиновой кислоты отличаются от данного эталонного полинуклеотида по меньшей мере одной нуклеотидной заменой, добавлением или делецией. Такие варианты можно получить, например, с помощью способов на основе ПЦР, таких как амплификация ДНК на основе смешанных олигонуклеотидных праймеров, т.е. с использованием вырожденных праймеров против консервативных доменов белков aHD или полипептидов PRD. Когда эталонный полинуклеотид кодирует антигенный или иммуногенный белок, в частности, химерную конструкцию aHD-PRD или ее часть, антигенная природа кодируемого полипептида должна быть сохранена в вариантном или производном полинуклеотиде, так что вариантная нуклеиновая кислота кодирует полипептид, имеющий антигенные или иммуногенные характеристики, как обсуждается в настоящем документе. Консервативные домены полипептидов по настоящему варианту осуществления подробно обсуждаются в настоящем документе и могут быть идентифицированы путем сравнения их последовательностей нуклеиновых кислот или аминокислот, особенно с использованием фиг. 2 и фиг. 3 в качестве ссылок для выбора перекрестно-реактивных иммуногенных доменов.
[060] Варианты или производные также охватывают комплементы и другие полинуклеотиды, которые включают в себя молекулы нуклеиновой кислоты, способные гибридизоваться с конкретными молекулами нуклеиновой кислоты, описанными в настоящем документе, как правило, в строгих условиях гибридизации. Строгие условия хорошо известны, и квалифицированный специалист знает, как определить условия гибридизации, ссылаясь на стандартные тексты, такие как указанные выше.
[061] Кроме того, варианты включают в себя полинуклеотиды, содержащие последовательности, которые по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85 %, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98%, по меньшей мере на 99% или любой другой процент между ними идентичны нуклеиновым кислотам, показанным в перечнях последовательностей, или могут быть получены из аминокислотных последовательностей, представленных в перечне последовательностей; с оговоркой, что приемлемая антигенность или иммуногенность сохраняется. Подобным образом, функциональный гомолог полипептида или белка, как описано в настоящем документе, может быть по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98%, по меньшей мере на 99% или любой другой процент между ними идентичен описанным в настоящем документе пептидам, полипептидам или белкам. Эти процентные значения идентичности, как правило, рассчитывают по всей молекуле белка или нуклеиновой кислоты. Многие компьютерные программы, использующие различные алгоритмы, доступны специалисту в настоящей области техники для сравнения последовательностей различных нуклеиновых кислот или полипептидов.
[062] Кроме того, при замене аминокислот белка, например, аминокислот, выбранных из SEQ ID NO: 1 - SEQ ID NO: 4, без учета наличия аминокислот в последовательностях других полипептидов, применимо следующее, причем буквы обозначают L-аминокислоты с использованием их обычных сокращений (замены перечислены, как правило, в порядке предпочтения): A можно заменить на S или C, G, T или V; C можно заменить на A; D можно заменить на E или N, Q или S; E можно заменить на D или Q или на K, H, N, R или S; F можно заменить на Y или на W, I, L или M; G можно заменить на A, N или S; H можно заменить на Y или на N, E, Q или R; I можно заменить на V или L или на M или F; K можно заменить на R или на E, Q, N или S; L можно заменить на I или M или на V или F; M можно заменить на L или на I, V, F или Q; N можно заменить на D, H, S, E, G, K, Q, R или T; Q можно заменить на E или на K, R, D, H, M, N или S; R можно заменить на K или на Q, E, H или N; S можно заменить на A, N, T, D, E, G, K или Q; T можно заменить на S, A, N или V; V можно заменить на I или на L, M, A или T; W можно заменить на Y или F и Y можно заменить на F, H или W. Однако следует понимать, что антигенные или иммуногенные свойства описанных в настоящем документе белковых конструкций остаются решающими для любого полипептида или белка, в который вводятся такие замены. Действительно, такие стратегии замены, вероятно, выиграют от ссылки на общие мотивы или шаблоны, представленные в настоящем документе, такие как показанные на фиг. 2A-фиг. 3D. Соответственно, белки согласно настоящим вариантам осуществления могут включать в себя аминокислотные замены, делеции или добавления, которые усиливают иммуногенность.
[063] Для экспрессии в рекомбинантном хозяине экспрессионная кассета, содержащая молекулу нуклеиновой кислоты, кодирующую конкретный представляющий интерес белок, например, конструкцию aHD-PRD, и соответствующие регуляторные контрольные области (например, промоторы, терминаторы), включены в вектор, который может представлять собой фаг, плазмиду или вирусный вектор или искусственную хромосому, такую как бактериальная или дрожжевая искусственная хромосома. Другими словами, вектор согласно настоящим вариантам осуществления может представлять собой вектор экспрессии, который содержит представляющий интерес полинуклеотид, функционально связанный с последовательностями контроля экспрессии (экспрессионной кассетой), который обеспечивает экспрессию в клетках-хозяевах или их выделенных фракциях. Вектор также, как правило, подходит в качестве клонирующего вектора, т.е. реплицируемого в микробных системах; даже если клонирующий вектор предназначен для репликации в одном хозяине, тогда как экспрессионная кассета предназначена для экспрессии в другом хозяине. Вектор, содержащий полипептиды и белки по настоящему изобретению, может дополнительно содержать селектируемый маркер для размножения или селекции в клетке-хозяине. Векторы могут быть введены в прокариотические или эукариотические клетки с помощью традиционных способов трансформации или трансфекции.
[064] Несколько вариантов осуществления конструкций aHD-PDR были испытаны на животных (фиг. 6-10) и являются иммуногенными кандидатами для включения в вакцины для человека. В последующем обсуждении конкретных конструкций их обозначения, происхождение клады aHD и группы PRD и аминокислотные последовательности представляют собой следующие (группы PRD выделены жирным шрифтом. Для каждой конструкции последовательность aHD останавливается там, где начинается PRD):
PspA01.1 (aHD из клады 2 [семейство 1], PRD из группы 2), длина: 384 аминокислоты, масса: 41 кДа: EESPVASQSKAEKDYDAAKKDAKNAKKAVEDAQKALDDAKAAQKKYDEDQKKTEEKAALEKAAS EEMDKAVAAVQQAYLAYQQATDKAAKDAADKMIDEAKKREEEAKTKFNTVRAMVVPEPEQLAET KKKSEEAKQKAPELTKKLEEAKAKLEEAEKKATEAKQKVDAEEVAPQAKIAELENQVHRLEQEL KEIDESESEDYAKEGFRAPLQSKLDAKKAKLSKLEELSDKIDELDAEIAKLEDQLKAAEENNNV EDYFKEGLEKTIAAKKAELEKTEADLKKAVNEPETPAPAPAPAPAPAPAPAPKPAPAPKPAPAP KPAPAPKPAPAPKPAPAPAPAPAPKPAPAPKPAPAPAPAPAPAPKPEKPAEKPAPAPKPETPKT (SEQ ID NO: 1)
PspA01.2 (aHD из клады 2 (семейство 1), PRD из группы 2), длина: 356 аминокислот, масса: 39 кДа: EESPVASQSKAEKDYDAAKKDAKNAKKAVEDAQKALDDAKAAQKKYDEDQKKTEEKAALEKAAS EEMDKAVAAVQQAYLAYQQATDKAAKDAADKMIDEAKKREEEAKTKFNTVRAMVVPEPEQLAET KKKSEEAKQKAPELTKKLEEAKAKLEEAEKKATEAKQKVDAEEVAPQAKIAELENQVHRLEQEL KEIDESESEDYAKEGFRAPLQSKLDAKKAKLSKLEELSDKIDELDAEIAKLEDQLKAAEENNNV EDYFKEGLEKTIAAKKAELEKTEADLKKAVNEPETPAPAPAPAPAPAPAPAPAPAPKPAPAPKP APAPKPAPAPAPAPAPKPEKPAEKPAPAPKPETPKT (SEQ ID NO: 2)
PspA01.3 (aHD из клады 2 (семейство 1), PRD из группы 3 (частично)), длина: 302 аминокислоты, масса: 33 кДа: EESPVASQSKAEKDYDAAKKDAKNAKKAVEDAQKALDDAKAAQKKYDEDQKKTEEKAALEKAAS EEMDKAVAAVQQAYLAYQQATDKAAKDAADKMIDEAKKREEEAKTKFNTVRAMVVPEPEQLAET KKKSEEAKQKAPELTKKLEEAKAKLEEAEKKATEAKQKVDAEEVAPQAKIAELENQVHRLEQEL KEIDESESEDYAKEGFRAPLQSKLDAKKAKLSKLEELSDKIDELDAEIAKLEDQLKAAEENNNV EDYFKEGLEKTIAAKKAELEKTEADLKKAVNEPEKPAPAPETPAPE (SEQ ID NO: 158)
PspA02 (aHD из клады 3 (семейство 2), PRD из группы 1) длина: 495 аминокислот, масса: 55 кДа: EESPQVVEKSSLEKKYEEAKAKADTAKKDYETAKKKAEDAQKKYEDDQKRTEEKARKEAEASQKLNDVAL VVQNAYKEYREVQNQRSKYKSDAEYQKKLTEVDSKIEKARKEQQDLQNKFNEVRAVVVPEPNALAETKKK AEEAKAEEKVAKRKYDYATLKVALAKKEVEAKELEIEKLQYEISTLEQEVATAQHQVDNLKKLLAGADPD DGTEVIEAKLKKGEAELNAKQAELAKKQTELEKLLDSLDPEGKTQDELDKEAEEAELDKKADELQNKVAD LEKEISNLEILLGGADPEDDTAALQNKLAAKKAELAKKQTELEKLLDSLDPEGKTQDELDKEAEEAELDK KADELQNKVADLEKEISNLEILLGGADSEDDTAALQNKLATKKAELEKTQKELDAALNELGPDGDEEETP APAPQPEQPAPAPKPEQPAPAPKPEQPAPAPKPEQPAPAPKPEQPAPAPKPEQPAKPEKPAEEPTQPEKP ATPKT (SEQ ID NO: 3)
PspA03 (aHD из клады 4 (семейство 2), PRD из группы 3) длина: 430 аминокислот, масса: 48 кДа: EEAPVANQSKAEKDYDAAVKKSEAAKKDYETAKKKAEDAQKKYDEDQKKTEAKAEKERKASEKIAEATKE VQQAYLAYLQASNESQRKEADKKIKEATQRKDEAEAAFATIRTTIVVPEPSELAETKKKAEEATKEAEVA KKKSEEAAKEVEVEKNKILEQDAENEKKIDVLQNKVADLEKGIAPYQNEVAELNKEIARLQSDLKDAEEN NVEDYIKEGLEQAITNKKAELATTQQNIDKTQKDLEDAELELEKVLATLDPEGKTQDELDKEAAEAELNE KVEALQNQVAELEEELSKLEDNLKDAETNNVEDYIKEGLEEAIATKKAELEKTQKELDAALNELGPEKPA EETPAPAPKPEQPAEQPKPAPAPQPAPAPKPEKTDDQQAEEDYARRSEEEYNRLPQQQPPKAEKPAPAPK PEQPVPAPKT (SEQ ID NO: 4)
[065] Подробности, касающиеся процедуры экспрессии и выхода антигена, обсуждаются в примере 3. Дополнительные конструкции aHD-PRD, содержащие другие aHD (включая в себя aHD из клады 1 (семейство 1) и 5 (семейство 2)) и другие PRD, пригодны для включения в конструкции aHD-PDR.
[066] Иммунизация кроликов тремя отдельными вариантами осуществлений конструкций aHD-PRD индуцировала сильную иммуногенность, как показано антигенспецифическими ответами сывороточного IgG. Кроме того, две конструкции с aHD семейства 2 вызывали антитела, которые хорошо перекрестно реагировали друг с другом, даже несмотря на то, что конструкции были из разных клад aHD (фиг. 5).
[067] Используя процедуры, известные специалистам в настоящей области техники, авторы настоящего изобретения приготовили составы для внутримышечного введения, используя соединения алюминия в качестве адъювантов. Более конкретно, такие препараты, как правило, предусматривают абсорбцию конструкций aHD-PRD на алюминиевом геле, таком как гидроксид алюминия (Al(OH)3) или фосфат алюминия (AlPO4), или осаждение конструкций aHD-PRD на сульфате алюминия-калия (AlK(SO4)2). Смотрите, например, Lindblad, 2004. Отдельные конструкции aHD-PRD, описанные в настоящем документе и приготовленные с использованием (AlK(SO4)2) или Al(OH)3, вызывали сильные антигенспецифические сывороточные IgG-ответы у мышей, включая в себя устойчивые сильные вторичные иммунные ответы после введения бустерной дозы (фиг.6; пример 4; пример 6).
[068] Примеры конструкций aHD-PRD, описанные в настоящем документе, дополнительно составляли для интраназальной доставки с использованием процедур, описанных ниже (Nochi et al., 2010; Kong et al., 2013; Fukuyama et al., 2015), и они описаны в примере 5. Каждый состав включает в себя вариант осуществления конструкции aHD- PRD, заключенной в сшитую структуру молекулы пуллулана, несущей катионную холестериновую группу (cCHP или наногель). Составы использовали в качестве вакцин, вводимых закапыванием состава в нос мыши или другого лабораторного животного. Этот состав для доставки IN вызывал сильные антигенспецифические сывороточные IgG- ответы у мышей, включая в себя устойчивые вторичные иммунные ответы после вакцинации бустерной дозой (фиг. 7; примеры 5 и 6).
[069] На сегодняшний день ни одно из исследований с лабораторными животными не выявило значительных побочных реакций на составы наногелей cCHP. В частности, исследования PET радиоактивно меченных cCHP-aHD, введенных IN нечеловекообразным приматам, не показало поглощения в обонятельной луковице или других структурах ЦНС. Fukuyama et al., 2015. Это дает уверенность в том, что введение IN не подвергает риску те виды воспаления ЦНС, которые отмечались в прошлом: когда вакцины, содержащие адъюванты, например, термолабильный энтеротоксин, вводили IN людям (Mutsch et al., 350 N. Engl. J. Med. 896 (2004)), или антигены с адъювантом для холерного токсина вводили IN мышам (van Ginkel et al., 165 J. Immunol. 4778 (2000)).
[070] Иммунные ответы, индуцированные описанными в настоящем документе конструкциями aHD-PRD, являются защитными как в составах IM, так и IN, не только против штаммов S. pneumoniae, которые содержат aHD или PRD, которые идентичны таковым конструкций иммунизирующих aHD-PRD, но также против штаммов для проверочного заражения, которые содержат разные aHD или PRD. Другими словами, авторы настоящего изобретения показали, что конструкции aHD-PRD производят перекрестно-реактивный защитный иммунитет (пример 6). Кроме того, этот иммунитет распространяется на пневмококковые штаммы, которые не охватываются современными вакцинами.
ПРИМЕРЫ
[071] Следующие ингредиенты, составы, процессы и процедуры для осуществления раскрытых в настоящем документе способов соответствуют описанным выше. Другие варианты осуществления и применения будут очевидны специалисту в настоящей области техники в свете настоящего раскрытия. Следующие примеры приведены только в качестве иллюстрации различных вариантов осуществления и не должны рассматриваться как каким-либо образом ограничивающие настоящее изобретение.
ПРИМЕР 1: Характеристика трех групп PRD и отбор антигена PRD
[072] PRD представляет собой относительно короткий полипептид, как правило, длиной от 60 до 100 аминокислот. Считается, что PRD начинается в конце aHD, у первого пролина последовательности пролинов, перемежающихся с другими аминокислотами, которые образуют несколько мотивов, которые повторяются внутри и среди PRD, и PRD, как правило, (но не исключительно) заканчивается аминокислотными остатками PKT. Смотрите фиг. 1. Авторы настоящего изобретения идентифицировали и проанализировали 124 уникальных последовательности PspA из 208 полных последовательностей PspA, размещенных на сервере BLAST, предоставленных онлайн Национальной медицинской библиотекой США. Эти последовательности PspA составляют большинство уникальных последовательностей генома PspA, доступных в открытых базах данных. К этим 124 полипептидным последовательностям авторы настоящего изобретения добавили двенадцать полипептидных последовательностей PspA, которые были проанализированы ранее (Hollingshead et al., 2000), но не были включены в те, которые были получены с онлайн-сервера BLAST Национальной библиотеки медицины. Авторы настоящего изобретения извлекли последовательности PRD из этих 136 суммарных аминокислотных последовательностей PspA и выровняли их в Geneious v7.1.7 с использованием аминокислотной матрицы Blosum30. После этого авторы настоящего изобретения построили дендрограммы, используя способ Neighbor Joining (NJ).
[073] Неожиданно этот способ идентифицировал три различные «группы» PRD, как показано на фиг. 3А-фиг. 3D и в таблице 1-таблице 3. Авторы настоящего изобретения также идентифицировали короткие повторяющиеся мотивы, каждый длиной приблизительно 6-8 аминокислот, которые наряду с непролиновым блоком из 22 аминокислот характеризуют большую часть каждого полипептида PRD. Пять коротких повторяющихся мотивов представляют собой: PKPEQP (SEQ ID NO: 5), QPAPAP (SEQ ID NO: 6), PKPAPA (SEQ ID NO: 7), EKPAPAP (SEQ ID NO: 8) и PEKPAE (SEQ ID NO: 9), и эти мотивы указаны в таблице 1-таблице 4. NPB, как правило, представляют собой QQAEEDYARRSEEEYNRLPQQQ (SEQ ID NO: 10) или QQAEEDYARRSEEEYNRLTQQQ (SEQ ID NO: 11). NPB также содержат высоко консервативные фланкирующие области, как правило, состоящие из четырех аминокислот с обеих сторон в PRD.
[074] Каждая из трех групп PRD характеризуется различными паттернами этих мотивов. Это можно увидеть из таблицы 1, таблицы 2 и таблицы 3, которые предоставляют аминокислотную последовательность и мотивы для PRD группы 1, группы
2 и группы 3, соответственно. Подавляющее большинство этих последовательностей не было идентифицировано ранее; известные аминокислотные последовательности охватываются в настоящем документе вариантами осуществления только в той степени, в которой они включены в новые рекомбинантные конструкции aHD-PRD или обеспечивают новые иммуногенные пептиды. В таблице 1 представлены аминокислотные последовательности многих полипептидов PRD группы 1, в которых разные повторяющиеся мотивы указаны разным шрифтом:
[075] Как видно из таблицы 1, каждая из пятидесяти последовательностей в группе 1 демонстрирует характерные повторы двух мотивов: PKPEQP (SEQ ID NO: 5) и QPAPAP (SEQ ID NO: 6), которые примыкают друг к другу и, как правило, перекрываются. Смотрите также таблицу 4.
[076] Двадцать одна аминокислотная последовательность в полипептидах PRD группы 2 (таблица 2) демонстрирует характерные множественные повторы PKPAPA (SEQ ID NO: 7), за исключением двух последовательностей, характеризуемых вместо множественных повторов EKPAPAP (SEQ ID NO: 8). В аминокислотных последовательностях других девятнадцати полипептидов группы 2 PKPAPA (SEQ ID NO: 7), как правило, экспрессировался в виде линейного тандемного повтора, тем самым также повторяя мотив KPAPAP (остатки 2-7 в SEQ ID NO: 8) -тандем повторяет характеристику других последовательностей группы 2. Это объясняет, как можно легко рассматривать, что последовательности, характеризуемые повторами EKPAPAP (SEQ ID NO: 8) или PKPAPA (SEQ ID NO: 7), принадлежат к одной группе. Смотрите также таблицу 4. Полипептиды PRD группы 2 и указанные мотивы показаны в таблице 2.
[077] Шестьдесят пять последовательностей в группе 3 PRD (таблица 3) характеризуются наибольшим разнообразием мотивов; ни один из которых не повторяется в тандеме. Кроме того, каждая из последовательностей группы 3 содержит один NPB, и NPB обнаружены только в полипептидах группы 3:
[078] В таблице 4 суммированы общие мотивы и частота их присутствия (по меньшей мере, один раз) в каждом PRD в каждой из трех групп PRD; таким образом, в таблице 4 показана вероятность того, что каждый мотив появляется по меньшей мере один раз в каждом из полипептидов в каждой группе PRD:
[079] Ранее сообщалось, что полипептиды NPB имеют тенденцию быть высокоиммуногенными, смотрите патент США № 8808704. Также сообщалось, что моноклональное антитело к мотиву PKPEQP (SEQ ID NO: 5), часто встречающемуся в PRD группы 1, защищало мышей от пневмококкового заражения. Daniels et al., 2010. Представленная в настоящем документе информация, в частности примеры 4-6, свидетельствует об иммуногенности других частей неполных и полных полипептидов PRD. Настоящие варианты осуществления поддерживают дополнительные и продолжающиеся исследования для характеристики иммуногенности различных мотивов, комбинаций мотивов и полных полипептидов.
[080] Четкое разделение PRD на три группы и частота общих мотивов в каждой группе позволяют предположить, что вакцина, которая включает в себя один PRD из каждой группы, должна быть способна производить перекрестный защитный иммунитет против большинства штаммов пневмококка. Это связано с тем, что PRD из конкретной группы должен иметь возможность производить перекрестный защитный иммунитет против пневмококков с другими PRD из той же группы - другими словами, с PRD, которые содержат много тех же мотивов, что и PRD вакцины. Поэтому вакцина, содержащая PRD из каждой группы, как определено в настоящем документе, должна вызывать перекрестно-реактивный иммунитет против почти всех PRD. Это лежит в основе настоящей стратегии создания вакцины, которая объединяет по меньшей мере один антиген PRD из каждой из групп PRD, в частности стратегии разработки вакцины, содержащей три конструкции aHD-PRD, в которой PRD включают в себя одну, выбранную из каждой из групп PRD.
[081] Другая стратегия отбора антигенов PRD предлагается по полной или почти идентичной гомологии некоторых PRD, как показано в таблицах 1-3, и обозначена горизонтальными линиями, соединяющими некоторые штаммы на фиг. 3. Следовательно, выбор в качестве вакцинного антигена PRD, который распределяется между несколькими клинически значимыми штаммами, увеличивает вероятность защитного иммунного ответа против всех этих штаммов. Например, DBL1 представляет собой вариант осуществления антигена PRD группы 3 (включенного в PspA03). Этот PRD идентичен таковому для шести других проанализированных штаммов.
[082] Например, вариант осуществления конструкции aHD-PRD, PspA01.1 (смотрите SEQ ID NO: 1), который включает в себя PRD группы 2 из штамма GA47439, стимулировал защитный иммуногенный ответ на моделях животных; и PRD расширили перекрестную реактивность этого ответа (примеры 4-6). Аминокислотная последовательность этого PRD представляет собой:
PETPAPAPAPAPAPAPAPAPKPAPAPKPAPAPKPAPAPKPAPAPKPAPAPAPAPAPKPAPAPKPAPAPAPAPAPAPKPEKPAEKPAPAPKPETPKT (SEQ ID NO: 12).
[083] Другой вариант осуществления конструкции aHD-PRD, PspA01.2 (смотрите SEQ ID NO: 2), который включает в себя PRD группы 2 из штамма ND6012, стимулировал защитный иммуногенный ответ, и этот PRD расширил его ответ. Аминокислотная последовательность этого PRD представляет собой:
PETPAPAPAPAPAPAPAPAPAPAPKPAPAPKPAPAPKPAPAPAPAPAPKPEKPAEKPAPAPKPETPKT (SEQ ID NO: 13).
[084] Аналогично, другой вариант осуществления конструкции aHD-PRD, PspA01.3 (смотрите SEQ ID NO: 158), который включает в себя фрагмент PRD, общий для следующих штаммов PRD группы 3: GA47597, SPN072838, GA19101, 70585, R6, RX1/D39, GA16242, GA17545, NP112, GA13856, 2071247, GA17971, SP18-BS74, GA13224 и GA60132, стимулировал защитный иммуногенный ответ. Аминокислотная последовательность этого PRD представляет собой: PEKPAPAPETPAPE (SEQ ID NO: 157).
[085] Другой вариант осуществления конструкции aHD-PRD, PspA02 (смотрите SEQ ID NO: 3), который включает в себя PRD из штамма группы 1, EF3296, стимулировал защитный иммуногенный ответ на моделях на животных (примеры 4-6). PRD расширил перекрестную реактивность этого ответа. Аминокислотная последовательность этого PDR представляет собой:
PDGDEEETPAPAPQPEQPAPAPKPEQPAPAPKPEQPAPAPKPEQPAPAPKPEQPAPAPKPEQPAKPEKPAEEPTQPEKPATPKT (SEQ ID NO: 14).
[086] PRD шести других штаммов, GA19923, SPN034183, GA47628, GA18523, GA16833 и GA18068, идентичны друг другу и характеризуются высокой гомологией с PRD EF3296 (не содержащим только APAPKPEQ) (например, остатки 19-26 из SEQ ID NO: 14). Таким образом, PRD от всех семи из этих штаммов группы 1, вероятно, являются антигенными и сильными кандидатами для включения в пневмококковую вакцину на основе PspA. Аминокислотная последовательность PRD этих шести штаммов представляет собой:
PDGDEEETPAPAPQPEQPAPAPKPEQPAPAPKPEQPAPAPKPEQPAPAPKPEQPAKPEKPAEEPTQPEKPATPKT (SEQ ID NO: 15).
[087] Другой вариант осуществления конструкции aHD-PRD, PspA03 (смотрите SEQ ID NO: 4), содержащей PRD группы 3 из штамма DBL1, стимулировал защитный иммуногенный ответ в моделях на животных. Этот PRD также расширил перекрестную реактивность иммунного ответа на PspA03. Шесть пневмококковых штаммов содержат точно такой же PRD, что и DBL1: EU-NP04, gamPNI0373, P1031, PNI0153, GA11304 и PCS70012 (смотрите также таблицу 3). Аминокислотная последовательность этого PRD представляет собой:
PEKPAEETPAPAPKPEQPAEQPKPAPAPQPAPAPKPEKTDDQQAEEDYARRSEEEYNRLPQQPPKAEKPAPAPKPEQPVPAPKT (SEQ ID NO: 16)
[088] Представленные в настоящем документе данные позволяют предположить, что иммуногенность этой последовательности может быть частично обусловлена непролиновым блоком (NPB) в этой последовательности:
QQAEEDYARRSEEEYNRLPQQQ (SEQ ID NO: 10).
[089] Четырнадцать других пневмококковых штаммов с анализируемыми PspA, как показано в таблице 3, также содержат этот NPB (SEQ ID NO: 10). Эти штаммы представляют собой: 670-6B, GA47373, Hungary19A-6, GA47210, GA05245, GA41301, SPAR95, GA49138, ATCC6303, SP14-BS69, G54, GA17484, CCRI_1974 и GA41538. PRD этих штаммов являются сильными кандидатами для включения в вакцину на основе PspA, содержащую по меньшей мере одну конструкцию aHD-PRD. Последовательности аминокислот PRD для каждого из этих четырнадцати штаммов показаны в SEQ ID NO: 17 - SEQ ID NO: 24.
[090] Другой вариант осуществления конструкции aHD-PRD, PspA01.3 (смотрите SEQ ID NO: 158), содержащий фрагмент, общий для пятнадцати PRD группы 3, также стимулировал защитный иммуногенный ответ на животных моделях. Fukuyama et al., 2015. Аминокислотная последовательность этого фрагмента PRD представляет собой: PEKPAPAPETPAPE (SEQ ID NO: 157). Пятнадцать штаммов пневмококка с проанализированными PspA, которые содержат этот PRD-фрагмент, представляют собой: GA47597, SPN072838, GA19101, 70585, R6, RX1/D39, GA16242, GA17545, NP112, GA13856, 2071247, GA17971, SP18-BS74, GA13224 и GA63224 и GA632 в таблице 3. Таким образом, включение этого фрагмента также может усиливать перекрестную реактивность в отношении штаммов с идентичными или сходными аминокислотными последовательностями в их PRD.
[091] Хотя не было четкой связи между конкретными группами PRD и конкретными кладами aHD PspA, в ассоциациях была высокая степень неслучайности (фиг. 2), что является значимым моментом (смотрите пример 2).
ПРИМЕР 2: Пять основных групп определяющих клады aHD областей и выбор антигена aHD
[092] Считалось, что определяющая кладу область (CDR), которая, как правило, состоит по итогу из приблизительно 100 аминокислот в aHD, считается наиболее антигенным доменом в пределах aHD. McDaniel et al., 17 Microb. Pathog. 323 (1994); Roche et al., 2003; Vadesilho et al., 21 Clin. Vaccine Immunol. 940 (2014). Используя 124 уникальные последовательности генома PspA, идентифицированные как описано в примере 1, авторы настоящего изобретения извлекли aHD из каждой последовательности. К этой информации авторы настоящего изобретения добавили таковую из последовательностей 12 aHD, проанализированных ранее (смотрите Hollingshead et al., 2000). Авторы настоящего изобретения выровняли CDR всех 136 уникальных аHD на платформе программного обеспечения Geneious (v7.1.7, Biomatters Ltd., Новая Зеландия), используя, в частности, выравнивание Geneious (глобальное выравнивание с матрицей Blosum62); затем авторы настоящего изобретения создали дендрограммы, используя плагин Geneious Tree builder (древовидные структуры, как на фиг. 2). Дендрограммы были выполнены с использованием способа Neighbor Joining (NJ) с моделью генетического расстояния Джукса-Кантора.
[093] Это не был автоматизированный или простой процесс. Хотя характерные аминокислотные последовательности часто отмечают начало CDR (например, приблизительно 70 процентов CDR клады 1 и 2 начинаются с LKEID (например, остатки 1-5 SEQ ID NO: 25) и LKEIG (SEQ ID NO: 86), большинство CDR клады 3 начинаются с LAKKQ (например, остатки 1-5 SEQ ID NO: 32), и большинство CDR клады 4 начинаются с LEK, многие CDR не начинаются с характерных последовательностей. Вместо этого начало CDR отмечается началом паттерна гомологии аминокислот, который характерен для каждой клады. Гомологии часто появляются между однокладовыми штаммами до CDR. В таких случаях, однако, паттерны гомологии между деформациями, как правило, переключаются в начале CDR. Таким образом, переход от областей пре-CDR к пост-CDR aHD часто отмечен переходом в паттернах гомологии. Для определения начала каждого CDR требовались большие навыки и умение правильно разобраться. Основным критерием было выбрать начало области, которая показала высокую гомологию с аналогично расположенными областями от других штаммов, и сделать это так, чтобы это было наименее произвольным для наибольшего процента PspA.
[094] Полученная в результате новая древовидная диаграмма (фиг. 2) позволяет оценивать относительную гомологию последовательности CDR между отдельными пневмококковыми штаммами, кладами и семействами. Диаграмма построена таким образом, что сумма длин вертикальных линий, соединяющих любые два штамма (или среднее значение любых двух клад), пропорциональна вероятности аминокислотной замены в любом положении вдоль последовательности CDR, т.е. пропорциональна степени разницы гомологии CDR. Кроме того, эта вероятность может быть аппроксимирована путем сравнения этой длины с длиной вертикального ключевого столбца, показанной на фиг. 2, что соответствует в среднем 0,2 однопарным аминокислотным заменам на сайт для этой длины вертикального разделения.
[095] Таким образом, например, сравнение длины этого ключевого столбца с суммарной длиной вертикальных линий, соединяющих средний штамм клады 4 и средний штамм клады 5, показывает, что вероятность того, что любая аминокислота в CDR штамма клады 4 отличается на одну конкретную аминокислотную замену от аналогично расположенной аминокислоты в штамме клады 5 составляет приблизительно 0,35. Допустимы значения более 1,0, поскольку вероятности относятся к заменам одной пары. Если, например, в одном и том же положении CDR некоторые штаммы в одной и той же кладе содержат лейцин (L), некоторые штаммы содержат глицин (G), а другие тирозин (Y), считается, что этот сайт содержит две замены одной пары при сравнении между средними штаммами в одной и той же кладе. Вероятность множественных однопарных замен на сайт увеличивается при сравнении штаммов в разных кладах и даже больше при сравнении штаммов в разных семействах.
[096] На фиг. 2 показано четкое разделение CDR (и, следовательно, антигенного сходства общих aHD) на три семейства. Два основных семейства, 1 и 2, состоят из двух и трех клад, соответственно. В семействе 1 клады 1 и 2 характеризуются несколько большей гомологией, чем клады 3, 4 и 5 в семействе 2. В семействе 3 содержится только одна клада, клада 6, которая содержит только три из 136 проанализированных последовательностей штаммов. На сегодняшний день исследования во всем мире указывают на то, что заболевание, вызванное пневмококками с PspA семейства 3 встречается редко. Hollingshead et al., 2000; Vela Coral et al., 2001; Hotomi et al., 2013. Неожиданным результатом этого анализа является высокая степень гомологии CDR между многими штаммами, отнесенными к каждой кладе. На фиг. 2А прямая горизонтальная линия, соединяющая отдельные штаммы, означает полную гомологию между их CDR.
[097] Таким образом, древовидная диаграмма CDR на фиг. 2А-фиг. 2D предполагает стратегии выбора aHD для включения в антигенные конструкции вакцины aHD-PRD. Например, древовидная диаграмма предполагает, что выбор aHD из клады 1 или 2 может вызвать перекрестную реактивность против большинства подтипов пневмококка семейства 1 PspA. Кроме того, несколько большее разнообразие в семействе 2 предполагает, что по меньшей мере два антигена aHD могут быть выбраны из разных клад семейства 2, таких как один из большой клады 3 и один из клад 4 или 5. Эти стратегии определяли выбор aHD, к которым авторы настоящего изобретения присоединили рекомбинантно к PRD для обеспечения трех иллюстративных вариантов осуществления иммуногенных конструкций aHD-PRD: aHD из каждой из клад 2, 3 и 4 (смотрите пример 3).
[098] Данные на животных указывают на то, что aHD в PspA01.1, PspA01.2, PspA02 и PspA03 являются иммуногенными (смотрите примеры 4-6). Существуют дополнительные доказательства того, что перекрестная реактивность некоторых антигенов aHD высока. Nabors et al., 2000; Darrieux et al., 2007 & 2008; Moreno et al., 2010, Fukuyama et al., 2015.
[099] В случае PspA01.1 (SEQ ID NO: 1), PspA01.2 (SEQ ID NO: 2) и PspA01.3 (SEQ ID NO: 158) это означает, что последовательность CDR клады 2, происходящая из штамма D39, является иммуногенной. Вариант этого штамма, Rx1, лишен полисахаридной капсулы, но содержит тот же PspA. Аминокислотная последовательность этого CDR представляет собой:
LKEIDESESEDYAKEGFRAPLQSKLDARKAKLSKLEELSDKIDELDAEIAKLEDQLKAAEENNNVEDYFKEGLEKTIAAKKAELEKTEADLKKAVNE (SEQ ID NO: 25).
[0100] Полная аминокислотная последовательность aHD D39/Rx1 представлена в SEQ ID NO: 159.
[0101] Однако в качестве альтернативных антигенов клады 2 можно выбрать aHD из одного из следующих штаммов: DBL5, CGSP14, GA47439, которые характеризуются следующей последовательностью CDR:
LKDINESDSEDYVKEGLRAPLQSELDTKKAKLLKLEELSGKIEELDAEIAELEVQLKDA EGNNNVEAYFKEGLEKTTAEKKAELEKAEADLKKAVDE (SEQ ID NO: 26);
или из штамма ND6012, который характеризуется следующей, почти гомологичной, последовательностью CDR:
LKEIDESDSEDYIKEGFRAPLQSELDTKKAKLLKLEELSGKIEELDAEIAELEVQLKDA EGNNNVEAYFKEGLEKTTAEKKAELEKAEADLKKAVDE (SEQ ID NO: 27)
[0102] CDR этих четырех штаммов характеризуются близкой гомологией с другими проанализированными последовательностями CDR клады 2 (смотрите фиг. 2). Кроме того, все они содержат PRD группы 2. Выявление иммунитета против этого CDR обеспечивает дополнительный охват против штаммов, которые могут быть недостаточно охвачены иммунизацией антигенами PRD группы 2. Полные аминокислотные последовательности aHD в DBL5, CGSP14, GA47439 и ND6012 представлены в SEQ ID NO: 28 - SEQ ID NO: 31.
[0103] Данные авторов настоящего изобретения на животных показывают, что CDR aHD в PspA02 (смотрите SEQ ID NO: 3), полученной из штамма клады 3, EF3296, также является иммуногенной; аминокислотная последовательность этой CDR представляет собой:
LAKKQTELEKLLDSLDPEGKTQDELDKEAEEAELDKKADELQNKVADLEKEISNLEILLGGADSEDDTAALQNKLATKKAELEKTQKELDAALNELG (SEQ ID NO: 32)
[0104] Двадцать шесть пневмококковых штаммов клады 3, GA47628, GA17301, GA54644, 2070531, CDC1873-00, GA02270, GA02714, 2070109, GA47283, EF3296, GA18068, GA19923, 3063-00, 7533-05, GA16833, SP9-BS GA08780, GA17570, SPAR55, GA47751, CDC1087-00, NP141, GA16531, GA13637, GA49447 и GA40028 (более половины из проанализированных в настоящем документе сорока шести штаммов клады 3) характеризуются существенной идентичностью с этой CDR. Таким образом, aHD, содержащие эту CDR, должны обеспечивать прямой иммунитет против многих штаммов пневмококка. Полные аминокислотные последовательности aHD этих двадцати шести штаммов представлены в SEQ ID NO: 33 - SEQ ID NO: 58.
[0105] Данные на животной модели также указывают на иммуногенность CDR в aHD в конструкции PspA03 (смотрите SEQ ID NO: 4), полученной из штамма EF5668 клады 4. Аминокислотная последовательность этой CDR:
LEKVLATLDPEGKTQDELDKEAAEAELNEKVEALQNQVAELEEELSKLEDNLKDAETNNVEDYIKEGLEEAIATKKAELEKTQKELDAALNELG (SEQ ID NO: 59);
и аминокислотная последовательность ее полного aHD EH5668 показана как SEQ ID NO: 60.
[0106] В качестве альтернативного антигена aHD клады 4 могут быть выбраны aHD с CDR, которые характеризуются еще большей гомологией друг с другом, чтобы увеличить вероятность сильной перекрестной реактивности как можно с большим количеством клинически важных штаммов, насколько это возможно. Три примера представляют собой штаммы CDC0288 04, Netherlands15B-37 и GA47522, которые все содержат CDR со следующей аминокислотной последовательностью:
LEKAEAELENLLSTLDPEGKTQDELDKEAAEAELNKKVEALQNQVAELEEELSKLEDNL KDAETNNVEDYIKEGLEEAIATKQAELEKTQKELDAALNELG (SEQ ID NO: 61).
Таким образом, альтернативным штаммом для белков aHD может быть CDC0288-04, который содержит полную аминокислотную последовательность aHD, показанную в SEQ ID NO: 62.
[0107] Штаммы клады 4 G54, GA17484, CCRI_1974, SP14-BS69, SP19-BS75 и GA41538 также содержат CDR с одинаковой аминокислотной последовательностью:
LEKAEAELENLLSTLDPEGKTQDELDKEAAEAELNKKVEALQNQVAELEEELSKLEDNL KDAETNNVEDYIKEGLEEAIATKKAELEKTQKELDAALNELG (SEQ ID NO: 63).
Следовательно, aHD G54, характеризующийся полной аминокислотной последовательностью, показанной в SEQ ID NO: 64, обеспечивает другой альтернативный источник для антигенов аHD клады 4.
[0108] На фиг. 2 представлены другие рекомендации по выбору дополнительных антигенов aHD, которые могут не быть конъюгированы с PRD. По меньшей мере согласно одному варианту осуществления, например, вакцинная композиция содержит в дополнение к трем конструкциям aHD-PRD по меньшей мере одну, такую как один или два неконъюгированных aHD. Принимая во внимание aHD, в частности конструкции aHD-PRD с гомологическими различиями, показанными на фиг. 2, и в свете особой клинической важности неконъюгированные aHD могут быть выбраны из клады 1 и клады 5, такие как один неконъюгированный aHD из клады 1 и один неконъюгированный aHD из клады 5.
[0109] Что касается штамма клады 1 согласно другому варианту осуществления предусмотрена иммуногенная композиция, содержащая по меньшей мере один неконъюгированный aHD клады 1, выбранный из следующих пневмококковых штаммов: BG8743, NP070, 2061376, SP23-BS72, 2080913, GA58981, GA56348, GA14688, GA44128 или 2071004. Все эти штаммы характеризуются одинаковой последовательностью CDR:
LKEIDESDSEDYIKEGLRAPLQSKLDAKKAKLSKLEELSDKIDELDAEIAKLEKDVEDFKNSDGEQAEQYLVAAKKDLDAKKAELENTEADLKKAVDE (SEQ ID NO: 65).
[0110] Эта область (SEQ ID NO: 65) характеризуется близкой гомологией с CDR других анализируемых областей клады 1 и, таким образом, может вызывать сильную перекрестную реактивность по отношению к другим PspA клады 1.
[0111] Кроме того, все предшествующие штаммы клады 1 содержат PRD группы 2. Вместе они составляют почти половину всех проанализированных штаммов с PRD группы 2, распределенными по всем кладам. В случае, когда антигены PRD группы 2 в PspA01.1 и PspA01.2 обеспечивают недостаточную перекрестную реактивность против пневмококковых штаммов, содержащих PRD группы 2, дополнительный aHD с вышеуказанной CDR (SEQ ID NO: 65) может обеспечивать защиту от таких штаммов. Полные аминокислотные последовательности aHD штаммов BG8743, NP070, 2061376, SP23-BS72, 2080913, GA58981, GA56348, GA14688, GA44128 и 2071004 показаны в SEQ ID NO: 66 - SEQ ID NO: 75, соответственно.
[0112] Альтернативные антигены aHD клады 1, содержащие CDR с близкой гомологией к другим CDR клады 1, включают в себя штаммы SP18-BS74, GA47597, SPN072838, GA19101, GA13224, GA16242, GA17545, NP112, GA13856, GA17971 или 2071247; которые обладают значительной идентичностью в CDR, характеризующейся следующей аминокислотной последовательностью:
LKEIDESDSEDYVKEGLRAPLQSELDAKQAKLSKLEELSDKIDELDAEIAKLEKNVEDFKNSNGEQAEQYRAAAEEDLAAKQAELEKTEADLKKAVNE (SEQ ID NO: 76).
[0113] Другие альтернативные антигены aHD клады 1 включают в себя антигены, полученные из штаммов 670-6B, EU NP04, gamPNI0373, P1031, PNI0153, GA11304 или PCS70012, которые также содержат общую CDR, характеризующуюся аминокислотной последовательностью:
LKGIDESDSEDYVKEGLRAPLQSELDAKRTKLSTLEELSDKIDELDAEIAKLEKNVEYFKKTDAEQTEQYLAAAEKDLADKKAELEKTEADLKKAVNE (SEQ ID NO: 77).
[0114] Таким образом, aHD штаммов NP112 и 670-6B обеспечивают два конкретных альтернативных варианта осуществления антигенов aHD клады 1: по одному из каждой из вышеуказанных групп CDR. Их полные аминокислотные последовательности показаны как SEQ ID NO: 78 и SEQ ID NO: 79, соответственно.
[0115] Что касается возможных неконъюгированных (несвязанных) aHD клады 5, которые могут быть включены в композицию, содержащую по меньшей мере одну конструкцию aHD-PRD, то по меньшей мере согласно одному варианту осуществления они могут быть выбраны из пневмококковых штаммов GA47373, GA05245, GA41301, GA47210 или Hungary19A-6. Эти штаммы составляют большинство проанализированных штаммов клады 5, и их CDR практически полностью гомологичны. Например, ниже приводится CDR GA47373 (полная аминокислотная последовательность aHD GA47373 показана в SEQ ID NO: 81):
LEDAELELEKVLATLDPEGKTQDELDKEAAEDANIEALQNKVADLENKVAELDKEVTRLQSDLKDAEENNVEDYVKEGLDKALTDKKVELNNTQKALDTAQKALDTALNELG (SEQ ID NO: 80).
ПРИМЕР 3: Получение чистых стабильных конструкций aHD-PRD с использованием системы экспрессии E. coli.
[0116] Аминокислотные последовательности рекомбинантных конструкций aHD- PRD разрабатывали в соответствии с вариантом осуществления, описанным в примерах 1 и 2. Для экспрессии выбирали три конкретные конструкции aHD-PRD: одну конструкцию, содержащую aHD семейства 1 из клады 1 или 2; две конструкции, содержащие аHD из семейства 2, одна из которых относится к кладе 3, а остальные aHD могут принадлежать либо кладе 4, либо 5.
[0117] Один вариант осуществления включал в себя aHD клады 2 (из штамма D39), который, как сообщалось, был высокоиммуногенным. Fukuyama et al., 2015. Другой вариант осуществления включал в себя аHD клады 3 (из штамма EF3296), который, как сообщалось, реагирует с человеческими антителами к PspA. Nabors et al., 2000; Roche et al., 2003. Дополнительный вариант осуществления включал в себя aHD клады 4 из штамма EF5668, который в предыдущих исследованиях указывался как высокоиммуногенный для мышей.
[0118] Для завершения конструкций aHD-PRD добавляли последовательности трех различных полных PRD или их фрагментов, по одному на каждый из C-концов каждого из трех изначально выбранных aHD. Добавленный PRD (или его фрагмент) может быть таким же, как обнаруженный у встречающегося в природе пневмококкового штамма, из которого был получен aHD, или он может быть из другого штамма пневмококка, и в этом случае конструкция aHD-PRD будет представлять собой искусственный слитый белок. Согласно одному варианту осуществления каждый из PRD (или их фрагментов) был из другой группы PRD (по одному из каждой из трех групп PRD). Согласно другому варианту осуществления два или даже три из PRD (или их фрагменты) были из одной и той же группы PRD (смотрите пример 7).
[0119] Дополнительные конструкции антигенов вакцины aHD-PRD могут включать в себя PRD, выбранные из групп, которые показывают высокую иммуногенность и перекрестную реактивность или содержат конкретные мотивы (или их комбинации), которые показывают высокую иммуногенность и перекрестную реактивность.
[0120] Как указано в примере 2, вариант осуществления вакцины может включать в себя только три конструкции aHD-PRD и дополнительно включать в себя по меньшей мере один aHD, не связанный с любым PRD. Эти aHD могут быть выбраны из числа клад, не представленных в трех основных конструкциях aHD-PRD. Кроме того, другой вариант осуществления вакцины содержит только две конструкции aHD-PRD и по меньшей мере один aHD, не связанный с каким-либо PRD, поскольку они сами по себе могут обеспечивать достаточную перекрестную реактивность для защиты от большинства патогенных пневмококковых штаммов (смотрите пример 7). Действительно, другой вариант осуществления вакцины может содержать только одну конструкцию aHD-PRD и два или более aHD, не связанных с каким-либо PRD.
[0121] Аминокислотные последовательности исходных конструкций aHD-PRD показаны в настоящем документе. Они могут экспрессироваться в системе бактериальной экспрессии с использованием стандартных способов генной инженерии, известных специалистам в настоящей области техники. Например, молекулы ДНК, кодирующие PspA01.1, PspA01.2, PspA01.3, PspA02 и PspA03, могут отдельно синтезироваться в виде молекул вирусной плазмидной ДНК с использованием трансляционных кодонов, оптимизированных для системы экспрессии E. coli.
[0122] Пример молекулы нуклеиновой кислоты (в частности, ДНК), способной кодировать PspA01.1 (SEQ ID NO: 1), показан в SEQ ID NO: 82. Пример молекулы ДНК, кодирующей PspA01.2 (SEQ ID NO: 2), показан в SEQ ID NO: 83. Пример молекулы ДНК, кодирующей PspA01.03 (SEQ ID NO: 158), показан в SEQ ID NO: 160. Пример молекулы ДНК, кодирующей PspA02 (SEQ ID NO: 3), показан в SEQ ID NO: 84. Наконец, пример молекулы ДНК, кодирующей PspA03 (SEQ ID NO: 4), показан в SEQ ID NO: 85.
[0123] Эти плазмидные ДНК клонировали отдельно в pET17b между сайтами HindIII и EcoRI. Затем плазмиды отдельно трансфицировали в клетки BL21 (DE3) Е. coli. После культивирования трансфицированных E. coli супернатант обработанных ультразвуком клеток загружали в колонки для ионообменной хроматографии на DEAE- и SP-сефарозе. За этим следовали гель-фильтрация на колонке с сефакрилом S-200 и, наконец, объединение активных фракций отдельно для каждого из экспрессированных белков. На фиг. 5 показана чистота продуктов экспрессии с использованием электрофореза в полиакриламидном геле с додецилсульфатом лития. Анализ Вестерн-блоттинг с использованием поликлональных антител к отдельным конструкциям aHD-PRD подтвердил их идентичность, также как и моноклональные антитела, которые связывались с уникальными эпитопами на каждой из конструкций.
ПРИМЕР 4: Исследования иммуногенности с отдельными конструкциями в составе IM
[0124] Составы для внутримышечного (IM) введения, содержащие индивидуальные конструкции aHD-PRD, готовили с использованием квасцового адъюванта. Этот состав с квасцами получали путем абсорбции отдельных описанных в примере 3 конструкций aHD-PRD на геле из гидроксида алюминия (Al(OH)3), как описано. Lindblad, 82 Immuno. Cell Biol. 497 (2004).
[0125] Каждую из трех конструкций aHD-PRD (PspA01.1, PspA02 и PPspA03) исследовали индивидуально, каждую конструкцию на двух кроликах, для оценки прямого и перекрестно-реактивного иммунитета. Каждый кролик обозначен как PspA_R1 или PspA_R2 в соответствии с полученным антигеном. Например, PspA01.1_R1 и PspA01.1_R2 представляли собой два кролика, иммунизированные PspA01.1 (фиг. 5). В день 0 каждого кролика иммунизировали внутримышечно 100 мкг указанного антигена с полным адъювантом Фрейнда. Через две недели каждому кролику вводили внутримышечно 100 мкг указанного антигена с неполным адъювантом Фрейнда. Еще через две недели сыворотки от отдельных кроликов исследовали с помощью непрямого ИФА в лунках, покрытых отдельными конструкциями aHD-PRD (отдельные лунки для каждой конструкции). На фиг. 5 показаны титры сывороточного IgG (реципрокные log2 ИФА-титры), специфически связывающиеся с каждой из трех антигенных конструкций. Титры конечной точки выражали в виде обратного log2 последнего разведения, что давало OD450 на 0,1 больше, чем отрицательный контроль. Ожидались высокие титры антител каждого кролика, произведенные против иммунизирующей конструкции. Примечательно, однако, что титры, которые кролики производили против каждой из двух неиммунизирующих конструкций, показали степень перекрестной реактивности против разнородных антигенов. Как отмечалось ранее, PspA01.1 включает в себя aHD семейства 1, клады 2; в то время как PspA02 и PspA03 включают в себя aHD семейства 2, клады 3 и 4, соответственно. Таким образом, неудивительно, что перекрестная реактивность внутри семейства, но и между кладами выше, чем перекрестная реактивность между семействами.
[0126] Следующие исследования с большим количеством мышей подтвердили иммуногенность и поддержали провокационные исследования.
[0127] Используя следующую процедуру, авторы настоящего изобретения показали, что состав IM вызывает сильный PspA-специфический сывороточный IgG-ответ у мышей после одной первичной IM-иммунизации и одной бустерной инъекции через 7,5 недель: тридцать самок мышей BALB/c в возрасте 7 недель делили на три группы по десять мышей и иммунизировали в каждой группе одной конструкцией aHD-PRD, в состав которой входили адъюванты - одна из каждой из следующих трех конструкций, PspA01.1, PspA02 или PspA03, для каждой из трех групп мышей. Пять мышей в каждой группе получали дозу 3 мкг, а пять получали дозу 10 мкг. Мышам обеих групп вводили 0,02 мл в мышцу верхней части задней ноги. Через 7,5 недель всем мышам вводили одну инъекцию одного и того же антигена в одной и той же дозе и объеме в одну и ту же мышцу, но эта бустерная доза не была приготовлена с квасцами или любым другим адъювантом.
[0128] Анализы ИФА использовали для измерения индивидуальных сывороточных титров антител IgG, связывающихся со специфической конструкцией, которой была иммунизирована каждая мышь. Планшеты (96-луночные) покрывали 1 мкг/мл конструкции в физиологического растворе с фосфатным буфером (PBS) в течение ночи при температуре 4°C. После блокирования 1% BSA в PBS-Tween добавляли двукратные серийные разведения образцов и инкубировали в течение 2 часов при комнатной температуре (RT). После промывания образцов авторы настоящего изобретения добавляли козий конъюгированный с пероксидазой хрена (HRP) антимышиный IgG, разведенный 1:1000, и инкубировали образцы в течение 2 часов при комнатной температуре. После инкубации окраску проявляли с использованием 3,3',5,5'-тетраметилбензидина (TMB) Microwell Peroxidase Substrate System (XPL). Конечные точки титрования выражали как обратный титр log2 последнего разведения, который давал OD450 по меньшей мере на 0,1 больше, чем отрицательный контроль. Повышенные уровни IgG в сыворотке сохранялись более восьми недель после бустерной инъекции, что указывает на устойчивый вторичный иммунный ответ (фиг. 6).
ПРИМЕР 5: Исследования иммуногенности с отдельными конструкциями в составе IN
[0129] Средство доставки для состава IN включало в себя содержащий катионную холестериновую группу пуллулан (cCHP или наногель). Пуллулан представляет собой полимер мальтотриозы. Производство сCHP известно и представлено в другом месте. Смотрите, например, Ayame et al., 19 Bioconj. Chem. 882 (2008); Nochi et al., 2010. Стадии предусматривают использование дрожжевой системы экспрессии для производства пуллулана, укорочение необработанной молекулы до массы от 50 кДа до 100 кДа, ковалентное присоединение холестериновых групп (~ 1,1-1,6 на 100 единиц глюкозы) и ковалентное добавление катионных аминогрупп (~ 20 на 100 единиц глюкозы).
[0130] Один способ изготовления описан следующим образом: содержащий гидроксильную группу углеводород или стерол, содержащий от 12 до 50 атомов углерода, сначала подвергали взаимодействию с диизоцианатным соединением, представленным NCO OCN-R1 (где R1 представляет собой углеводородную группу, содержащую от 1 до 50 атомов углерода) для получения гидрофобного содержащего изоцианатную группу соединения, содержащего одну молекулу содержащего гидроксильную группу углеводорода (или стерола). Полученному содержащему изоцианатную группу гидрофобному соединению давали возможность реагировать с полисахаридом с образованием содержащего гидрофобную группу полисахарида, который содержит углеводородную или стерильную группу с 12-50 атомами углерода. Затем продукт очищали растворителем на основе кетона с получением полисахарида, содержащего гидрофобную группу высокой чистоты.
[0131] Подходящим полисахаридом может быть, например, пуллулан, амилопектин, амилоза, декстран, гидроксиэтилдекстран, маннан, леван, инулин, хитин, хитозан, ксилоглюкан или водорастворимая целлюлоза. По меньшей мере согласно одному варианту осуществления полисахарид представляет собой испуллулан.
[0132] Примеры наногелей, пригодных для вакцины IN, включают в себя содержащий гидрофобную группу холестерина (CHP) полисахарид и производное катионного CHP (cCHP). CHP характеризуется структурой, в которой от 1 до 10, например, от 1 до 2, молекул холестерина добавляются путем замещения на 100 единиц глюкозы пуллулана, имеющих молекулярную массу от 30000 до 200000 кДа. Иллюстративный диапазон молекулярной массы пуллулана составляет от 70000 до 100000 кДа.
[0133] Степень замещения холестерина на 100 единиц глюкозы может быть выбрана исходя из размера и степени гидрофобности антигена. Чтобы дополнительно изменить степень гидрофобности CHP, можно добавить одну или несколько алкильных групп, имеющих от 10 до 30 (например, от приблизительно 12 до 20) атомов углерода. По меньшей мере согласно одному варианту осуществления предусмотрен наногель, характеризующийся размером частиц от 10 до 40 нм, например, от 20 до 30 нм. Такой наногель CHP использовали в клинических испытаниях противораковой вакцины на людях, где наногель CHP служит средством доставки раковых антигенов.
[0134] Согласно другому варианту осуществления предусмотрен наногель cCHP, который включает в себя положительно заряженную функциональную группу, например, катионную аминогруппу. Это позволяет комплексу наногель-антиген дольше удерживаться на отрицательно заряженной поверхности слизистой оболочки носа. Оптимальное соотношение включения катионной аминогруппы зависит от антигена. Оптимальный диапазон для большинства антигенов, включая в себя PspA, составляет от 18 до 22 (например, 20) на 100 единиц глюкозы для cCHP.
[0135] Далее описывается иллюстративный способ объединения аминогрупп с наногелем CHP: лиофилизированный CHP (приблизительно 0,15 г) растворяли в 15 мл диметилсульфоксида (ДМСО) и к нему добавляли 1-1'-карбонилдиимидазол (приблизительно 75 мг) под потоком азота. Реакции позволяли протекать при комнатной температуре в течение нескольких часов (например, приблизительно 1 час). К реакционному раствору постепенно добавляли катионный амин, например, этилендиамин (например, приблизительно 300 мг), и смесь перемешивали в течение нескольких часов в течение дня (например, приблизительно 24 часа). Полученный реакционный раствор подвергали диализу против дистиллированной воды в течение нескольких дней. После диализа реакционный раствор лиофилизировали с получением опалесцирующего твердого вещества. Степень замещения этилендиамина может быть оценена с помощью элементного анализа с использованием, например, H-ЯМР.
[0136] После изготовления наногеля, составы наногеля каждой из трех конструкций aHD-PRD, PspA01.1, PspA02 и PspA03, создавали с использованием описанных процедур. Смотрите, патент № 8961983; Nochi et al., 2010; Kong et al., 2013; Fukuyama et al., 2015. Эти процедуры включали в себя смешивание 2% раствора cCHP с раствором, содержащим конструкцию aHD-PRD, с приблизительным молекулярным соотношением 1:1 при температуре 40°C или 50°C в течение 1 часа, а затем смешивание с забуференным фосфатом солевым раствором (PBS), затем пропускали через мембранный фильтр 0,22 мкм.
[0137] Поскольку cCHP легче растворяется в мочевине, чем в PBS, и (в отличие от растворения в PBS) не требует ультразвукового оборудования, также использовали альтернативную процедуру, более подходящую для более крупносерийного состава. Это включало в себя смешивание с 6 М раствором мочевины (а не с PBS) при температуре приблизительно 4-8°C, с последующим диализом против PBS и затем прохождением через мембранный фильтр 0,22 мкм. Полученные составы составляли из единой конструкции aHD-PRD, заключенной в поперечно-сшитую структуру молекулы cCHP (наногель). Это подтверждали способом резонансного переноса энергии флуоресценции (FRET) с использованием FITC-конъюгированного aHD-PRD и TRITC-конъюгированного наногеля cCHP. Кроме того, динамическое рассеяние света (DLS) подтверждало однородный размер частиц приблизительно 40 нм в диаметре.
[0138] Тридцать самок мышей BALB/c в возрасте 7 недель разделили на три группы по десять, и каждую группу иммунизировали 10 мкг комплекса cCHP-aHD-PRD: одним из каждого из трех комплексов - cCHP-PspA01.1, cCHP-PspA02 или cCHP-PspA03 - для каждой из трех групп мышей. Пять мышей в каждой группе получали комплекс, составленный при температуре 40°C с PBS, в то время как пять мышей в каждой группе получали комплекс, приготовленный при температуре 50°C с PBS. В каждом случае антигенные комплексы содержались в 0,006 мл (6 мкл) раствора, который капали в одну ноздрю.
[0139] Тот же способ капельного введения можно использовать для более крупных животных, таких как кролики или собаки. В случае людей, раствор, содержащий соответствующее количество комплекса cCHP-aHD-PRD (или смеси комплексов), может быть доставлен любым подходящим способом, таким как капание или распыление в каждую ноздрю в разделенных дозах с использованием шприцевого устройства для распыления, такого как AccuSpray® от Becton Dickinson's. Это устройство использовали для эффективной доставки вакцины против гриппа FluMist® в носовые ходы приматов.
[0140] Начальная (первичная) серия иммунизации состояла из трех доз, каждая с интервалом в одну неделю. Последующие эксперименты показали, что две дозы, вводимые с интервалом в неделю, или даже одна доза, также вызывали сильный антигенспецифический IgG-ответ. Всем мышам вводили однократную назальную дозу (один и тот же комплекс антигенов, доза, объем и температура состава) через 7,5 недель.
[0141] Те же анализы ИФА, которые описаны в примере 4, использовали для измерения титров иммунизирующих антигенспецифических IgG-антител в сыворотках отдельных мышей. Эти анализы ИФА также показали устойчивые, сильные вторичные иммунные ответы, сохраняющиеся в течение более 8 недель после бустерной дозы (фиг.7).
ПРИМЕР 6: Исследования иммуногенности и заражения множественными конструкциями.
[0142] Иммунизация мышей тремя конструкциями aHD-PRD вызывала сильные сывороточные IgG-ответы против каждой из отдельных компонентных конструкций, а также выявляла защитный перекрестно-реактивный иммунитет против штаммов S. pneumoniae, имеющих aHD, отличные от таковых иммунизирующих конструкций. Это было достигнуто после введения IM и IN (наногеля).
[0143] Процедуры IM-иммунизации были следующими: смесь, содержащую 10 мкг каждой из трех конструкций aHD-PRD (PspA01.1, PspA02 и PspA03), готовили с квасцами, Al(OH)3). Шестьдесят самок мышей BALB/c в возрасте 7 недель иммунизировали этим составом путем последовательных инъекций в альтернативные мышцы верхней части задней ноги в день 0. Через 7 недель мышам повторно вводили ту же смесь (т.е. 10 мкг каждой из трех конструкций aHD-PRD), но без квасцов, путем последовательных инъекций в альтернативные мышцы верхней части задней лапы.
[0144] Процедуры иммунизации IN были следующими: индивидуальные комплексы cCHP-aHD-PRD изготавливали для каждого из трех образцов конструкций aHD-PRD, PspA01.1, PspA02 и PspA03. Способы составления индивидуальных комплексов описаны в начале примера 5. Все комплексы готовили при температуре 40°С. В день 0 шестьдесят 7- недельных самок мышей BALB/c иммунизировали 10 мкг комплекса cCHP-PspA01.1. Это выполняли путем капельного введения 0,006 мл (6 мкл) раствора, содержащего комплекс cCHP-PspA01.1 (содержащего 10 мкг PspA01.1), в одну ноздрю каждой мыши. В первый день то же самое делали с 6 мкл раствора, содержащего комплекс cCHP-PspA02 (содержащий 10 мкг PspA02). На второй день то же самое выполняли с комплексом cCHP- PspA03 (содержащим 10 мкг PsPA03). Этот процесс повторяли пять дней спустя (одна неделя после дня 0) и снова через две недели после дня 0. Таким образом, к 16 дню все шестьдесят мышей были три раза назально иммунизированы по 10 мкг каждой из трех иллюстративных конструкций aHD-PRD, PspA01.1, PspA02 и PspA03. Через 7 недель мышам вводили 10 мкг каждой из конструкций aHD-PRD, капая 6 мкл раствора, содержащего cCHP-PspA01.1 (10 мкг соответствующей конструкции aHD-PRD), в одну ноздрю каждой мыши. Этот процесс повторяли на следующий день для cCHP-PspA02 и на следующий день для cCHP-PspA03. Другими словами, каждая мышь получала назальную бустерную дозу каждого из трех антигенов, составленных в виде наногелей, в течение трех дней.
[0145] Последующие эксперименты показали, что для начальной дозы достаточно двух или даже только одного назального введения. Кроме того, вместо иммунизации мышей в последовательные дни различными антигенами можно составить смесь всех трех конструкций cCHP-aHD-PRD. Если требуется многократное введение в течение нескольких дней, вводят смесь всех трех антигенных комплексов. Когда вакцину вводят людям, ее также можно вводить в виде смеси отдельных антигенов в комплексе с cCHP, хотя ее можно вводить с помощью спрея, а не жидких капель. Процедуры в кратком описании фиг. 8 описывают этот способ введения смеси комплексов cCHP-PspA.
[0146] Через две недели после бустерной дозы с помощью ИФА определяли титры сывороточного IgG против каждого из трех антигенов. Титры сывороточного антигенспецифического IgG были сходными для иммунизированных IM и IN мышей. Сравните фиг. 6 и фиг. 7; смотрите также фиг. 8. Также титры против каждого отдельного антигена были одинаковыми независимо от того, были ли мыши иммунизированы только этим антигеном (фиг. 6 и фиг. 7 (бустерная доза)) или тремя антигенами вместе (фиг. 8). Полученные результаты свидетельствуют о том, что: (а) конкуренция антигенов была незначительной или отсутствовала, что уменьшало иммунный ответ на каждый антиген, или (b) любая конкуренция антигенов имела место в противовес перекрестной реактивности, например, антитела, полученные против одной конструкции aHD-PRD, также связаны с другими конструкциями.
[0147] Пять штаммов S. pneumoniae отбирали в качестве штаммов заражения: BG8838, A66.1, BG12730, 3JYP2670 и ATCC 6303, которые представляют собой множество различных кладов aHD с 1 по 5, соответственно; а также полисахаридные капсульные серотипы, охваченные хорошо и охваченные слабо PPSV23 и PCV13. Например, A66.1, 3JYP2670 и ATCC6303 демонстрируют полисахаридный капсульный антиген 3, который, хотя он включен в PPSV23 и PCV13, не охватывается хорошо ни одной вакциной. Andrews et al., 2014. BG12730 отображает капсульный серотип 6А, который не охватывается PPCV23. Таким образом, эти штаммы позволили авторам настоящего изобретения оценить способность трех вариантов осуществления вакцинных конструкций aHD-PRD защищать от пневмококковых штаммов, которые актуальны для общественного здравоохранения сегодня.
[0148] Чтобы определить подходящие дозы заражения для каждого из этих штаммов, неиммунизированных мышей заражали в исследовании с повышением дозы, чтобы идентифицировать количество колониеобразующих единиц (КОЕ, т.е. количество жизнеспособных бактерий S. pneumoniae), что приводит к 80% смертности в течение пяти дней. Это было сделано путем введения по каплям 0,05 мл раствора, содержащего 105, 106, 107 или 108 КОЕ, в одну ноздрю каждой мыши. Для каждого штамма и каждого уровня КОЕ интраназально заражали пять мышей. На основании этого исследования первоначально определяли следующие 80% летальные дозы для следующих пяти контрольных штаммов: BG8838: 1×108 КОЕ; A66.1: 1×105 КОЕ; BG12730: 1×108; 3JYP2670: 1×106 и ATCC 6303: 1×107 КОЕ.
[0149] Исследования заражения проводили следующим образом: через пять недель после первой бустерной дозы и через двенадцать недель после первой иммунизации пятьдесят IM-иммунизированных мышей, пятьдесят IN-иммунизированных мышей и пятьдесят наивных контролей интраназально заражали пятью штаммами с содержанием КОЕ, указанным выше. В случае каждого штамма 0,05 мл раствора, содержащего соответствующее количество КОЕ, капали в одну ноздрю десяти IM-иммунизированным мышам, десяти IN-иммунизированным мышам и десяти неиммунизированным контрольным мышам. Исходный протокол требовал, чтобы за мышами следили в течение семи дней, и эту процедуру выполняли для мышей, зараженных A66.1 и 3JYP2670. Исследования для определения подходящих сублетальных доз (исследования с диапазоном доз) повторно проводили для трех других штаммов, поскольку для всех групп исходные показатели выживаемости были либо очень высокими, либо очень низкими. После новых исследований в диапазоне доз, протокол изменили, чтобы следить за мышами в течение десяти дней. Таким образом, данные выживания для BG8838, BG12730 и ATCC6303 представлены для мышей с наблюдением в течение десяти дней после заражения.
[0150] Данные по выживанию на фиг. 9 показывают, что составы IM и наногель-IN защищали мышей от летальных заражений. Штаммы A66.1, 3JYP2670 и ATCC6303 характеризуются серотипом 3 капсульного полисахарида, который плохо охвачен вакцинами PPSV23 и PCV13. Кривые выживания против заражения A66.1, 3JYP2670 и ATCC6303 показывают, что иллюстративная вакцинная композиция имеет преимущество в защите от штаммов, в противном случае плохо охваченных вакцинами PPSV23 и PCV13. Результаты для контрольных штаммов BG8838 (который имеет PspA клады 1) и ATCC6303 (который имеет PspA клады 5) показывают, что вакцинная композиция вызывала перекрестную реактивность против обеих клад. Оба штамма содержат PRD группы 3, поэтому перекрестная защита может была обеспечена иммунитетом против группы 3 PRD, включенной в конструкцию PspA03. Пневмококковый штамм BG12730 имеет капсульный полисахарид серотипа 6А, который охвачен вакциной PCV13, но не вакциной PPSV23. Кривые выживания против заражения штаммом BG12730 показывают, что конструкция aHD-PDR защищала от штамма, не охваченного PPSV23 (смотрите фиг. 9).
ПРИМЕР 7: Иммуногенность конструкции aHD-PRD с коротким PRD.
[0151] Дополнительные эксперименты показали, что замена последовательности PRD группы 2 короткой последовательностью PRD из групп 1 или 3 или даже отсутствием последовательности PRD может привести к еще лучшему иммунологическому ответу. Ввиду гомологии между первыми 14 аминокислотными остатками - PEKPAPAPETPAPE (SEQ ID NO: 157) - пятнадцати PRD группы 3 (смотрите обсуждение в примере 1 и таблице 3), конструкцию aHD-PRD, состоящую из aHD штамма D39 пневмококка, сконструировали с этим фрагментом PRD. Эту конструкцию обозначили PspA01.3 (смотрите SEQ ID NO: 158). Она включает в себя фрагмент белка PspA в природном штамме D39 пневмококка, который может вызывать защитный иммунитет на моделях животных. Смотрите Fukuyama et al., 2015.
[0152] Анализ перекрестной реактивности, сравнивающий антигенспецифический сывороточный IgG, производимый PspA01.1, PspA01.2 и PspA01.3, показал, что PspA01.3, вероятно, является более антигенным, чем любой из двух других антигенов. Когда иммунизировали пятнадцать мышей, пять с PspA01.1, пять с PspA01.2 и пять с PspA01.3, и анализировали титры их антигенспецифических сывороточных антител IgG, каждая группа реагировала лучше всего против PspA01.3, даже мыши, иммунизированные PspA01.1 и PspA01.2. Например, среди сывороток мышей, иммунизированных PspA01.1, средний реципрокный титр log2 против PspA01.3 составлял 15,6, тогда как против PspA01.1 и PspA01.2 он составлял только 15,0. Среди сывороток мышей, иммунизированных PspA01.2, средний реципрокный титр log2 против PspA01.3 составлял 15,8, но он был только 14,4 и 14,8 против PspA01.1 и PspA01.2, соответственно.
[0153] Кроме того, сыворотка мышей, иммунизированных PspA01.3, реагировала лучше против PspA01.1 и PspA01.2, чем сыворотка мышей, иммунизированных специфически против этих антигенов. Например, средний реципрокный log2 титра IgG против PspA01.1 составлял 16,6 в сыворотках мышей, иммунизированных PspA01.3, тогда как в сыворотках мышей, иммунизированных PspA01.1 и PspA01.2, он составлял только 15,0 и 14,4, соответственно. Средний реципрокный log2 титра против PspA01.2 составлял 17,4 в сыворотках мышей, иммунизированных PspA01.3, но только 15,0 и 14,8 в сыворотках мышей, иммунизированных PspA01.1 и PspA01.2, соответственно.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> Токийский университет
Исследовательский фонд UAB
<120> ПНЕВМОКОККОВАЯ ВАКЦИНА, СОЧЕТАЮЩАЯ ВЫБРАННЫЕ АЛЬФА-СПИРАЛЬНЫЕ
ДОМЕНЫ И БОГАТЫЕ ПРОЛИНОМ ДОМЕНЫ ПНЕВМОКОККОВОГО ПОВЕРХНОСТНОГО БЕЛКА
А
<130> 87571.0001\PCT
<140> 62/429,782
<141> 2016-12-03
<160> 160
<170> PatentIn версия 3.5
<210> 1
<211> 384
<212> PRT
<213> Искусственная последовательность
<220>
<223> конструкция aHD-PRD, рекомбинантный белок слияния, обозначенный
PspA01.1
<400> 1
Glu Glu Ser Pro Val Ala Ser Gln Ser Lys Ala Glu Lys Asp Tyr Asp
1 5 10 15
Ala Ala Lys Lys Asp Ala Lys Asn Ala Lys Lys Ala Val Glu Asp Ala
20 25 30
Gln Lys Ala Leu Asp Asp Ala Lys Ala Ala Gln Lys Lys Tyr Asp Glu
35 40 45
Asp Gln Lys Lys Thr Glu Glu Lys Ala Ala Leu Glu Lys Ala Ala Ser
50 55 60
Glu Glu Met Asp Lys Ala Val Ala Ala Val Gln Gln Ala Tyr Leu Ala
65 70 75 80
Tyr Gln Gln Ala Thr Asp Lys Ala Ala Lys Asp Ala Ala Asp Lys Met
85 90 95
Ile Asp Glu Ala Lys Lys Arg Glu Glu Glu Ala Lys Thr Lys Phe Asn
100 105 110
Thr Val Arg Ala Met Val Val Pro Glu Pro Glu Gln Leu Ala Glu Thr
115 120 125
Lys Lys Lys Ser Glu Glu Ala Lys Gln Lys Ala Pro Glu Leu Thr Lys
130 135 140
Lys Leu Glu Glu Ala Lys Ala Lys Leu Glu Glu Ala Glu Lys Lys Ala
145 150 155 160
Thr Glu Ala Lys Gln Lys Val Asp Ala Glu Glu Val Ala Pro Gln Ala
165 170 175
Lys Ile Ala Glu Leu Glu Asn Gln Val His Arg Leu Glu Gln Glu Leu
180 185 190
Lys Glu Ile Asp Glu Ser Glu Ser Glu Asp Tyr Ala Lys Glu Gly Phe
195 200 205
Arg Ala Pro Leu Gln Ser Lys Leu Asp Ala Lys Lys Ala Lys Leu Ser
210 215 220
Lys Leu Glu Glu Leu Ser Asp Lys Ile Asp Glu Leu Asp Ala Glu Ile
225 230 235 240
Ala Lys Leu Glu Asp Gln Leu Lys Ala Ala Glu Glu Asn Asn Asn Val
245 250 255
Glu Asp Tyr Phe Lys Glu Gly Leu Glu Lys Thr Ile Ala Ala Lys Lys
260 265 270
Ala Glu Leu Glu Lys Thr Glu Ala Asp Leu Lys Lys Ala Val Asn Glu
275 280 285
Pro Glu Thr Pro Ala Pro Ala Pro Ala Pro Ala Pro Ala Pro Ala Pro
290 295 300
Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro
305 310 315 320
Lys Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro Lys Pro Ala Pro
325 330 335
Ala Pro Ala Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro Lys Pro
340 345 350
Ala Pro Ala Pro Ala Pro Ala Pro Ala Pro Ala Pro Lys Pro Glu Lys
355 360 365
Pro Ala Glu Lys Pro Ala Pro Ala Pro Lys Pro Glu Thr Pro Lys Thr
370 375 380
<210> 2
<211> 356
<212> PRT
<213> Искусственная последовательность
<220>
<223> конструкция aHD-PRD, рекомбинантный белок слияния, обозначенный
PspA01.2
<400> 2
Glu Glu Ser Pro Val Ala Ser Gln Ser Lys Ala Glu Lys Asp Tyr Asp
1 5 10 15
Ala Ala Lys Lys Asp Ala Lys Asn Ala Lys Lys Ala Val Glu Asp Ala
20 25 30
Gln Lys Ala Leu Asp Asp Ala Lys Ala Ala Gln Lys Lys Tyr Asp Glu
35 40 45
Asp Gln Lys Lys Thr Glu Glu Lys Ala Ala Leu Glu Lys Ala Ala Ser
50 55 60
Glu Glu Met Asp Lys Ala Val Ala Ala Val Gln Gln Ala Tyr Leu Ala
65 70 75 80
Tyr Gln Gln Ala Thr Asp Lys Ala Ala Lys Asp Ala Ala Asp Lys Met
85 90 95
Ile Asp Glu Ala Lys Lys Arg Glu Glu Glu Ala Lys Thr Lys Phe Asn
100 105 110
Thr Val Arg Ala Met Val Val Pro Glu Pro Glu Gln Leu Ala Glu Thr
115 120 125
Lys Lys Lys Ser Glu Glu Ala Lys Gln Lys Ala Pro Glu Leu Thr Lys
130 135 140
Lys Leu Glu Glu Ala Lys Ala Lys Leu Glu Glu Ala Glu Lys Lys Ala
145 150 155 160
Thr Glu Ala Lys Gln Lys Val Asp Ala Glu Glu Val Ala Pro Gln Ala
165 170 175
Lys Ile Ala Glu Leu Glu Asn Gln Val His Arg Leu Glu Gln Glu Leu
180 185 190
Lys Glu Ile Asp Glu Ser Glu Ser Glu Asp Tyr Ala Lys Glu Gly Phe
195 200 205
Arg Ala Pro Leu Gln Ser Lys Leu Asp Ala Lys Lys Ala Lys Leu Ser
210 215 220
Lys Leu Glu Glu Leu Ser Asp Lys Ile Asp Glu Leu Asp Ala Glu Ile
225 230 235 240
Ala Lys Leu Glu Asp Gln Leu Lys Ala Ala Glu Glu Asn Asn Asn Val
245 250 255
Glu Asp Tyr Phe Lys Glu Gly Leu Glu Lys Thr Ile Ala Ala Lys Lys
260 265 270
Ala Glu Leu Glu Lys Thr Glu Ala Asp Leu Lys Lys Ala Val Asn Glu
275 280 285
Pro Glu Thr Pro Ala Pro Ala Pro Ala Pro Ala Pro Ala Pro Ala Pro
290 295 300
Ala Pro Ala Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro Lys Pro
305 310 315 320
Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro Ala Pro Ala Pro Ala Pro
325 330 335
Lys Pro Glu Lys Pro Ala Glu Lys Pro Ala Pro Ala Pro Lys Pro Glu
340 345 350
Thr Pro Lys Thr
355
<210> 3
<211> 495
<212> PRT
<213> Искусственная последовательность
<220>
<223> конструкция aHD-PRD, рекомбинантный белок слияния, обозначенный
PspA02
<400> 3
Glu Glu Ser Pro Gln Val Val Glu Lys Ser Ser Leu Glu Lys Lys Tyr
1 5 10 15
Glu Glu Ala Lys Ala Lys Ala Asp Thr Ala Lys Lys Asp Tyr Glu Thr
20 25 30
Ala Lys Lys Lys Ala Glu Asp Ala Gln Lys Lys Tyr Glu Asp Asp Gln
35 40 45
Lys Arg Thr Glu Glu Lys Ala Arg Lys Glu Ala Glu Ala Ser Gln Lys
50 55 60
Leu Asn Asp Val Ala Leu Val Val Gln Asn Ala Tyr Lys Glu Tyr Arg
65 70 75 80
Glu Val Gln Asn Gln Arg Ser Lys Tyr Lys Ser Asp Ala Glu Tyr Gln
85 90 95
Lys Lys Leu Thr Glu Val Asp Ser Lys Ile Glu Lys Ala Arg Lys Glu
100 105 110
Gln Gln Asp Leu Gln Asn Lys Phe Asn Glu Val Arg Ala Val Val Val
115 120 125
Pro Glu Pro Asn Ala Leu Ala Glu Thr Lys Lys Lys Ala Glu Glu Ala
130 135 140
Lys Ala Glu Glu Lys Val Ala Lys Arg Lys Tyr Asp Tyr Ala Thr Leu
145 150 155 160
Lys Val Ala Leu Ala Lys Lys Glu Val Glu Ala Lys Glu Leu Glu Ile
165 170 175
Glu Lys Leu Gln Tyr Glu Ile Ser Thr Leu Glu Gln Glu Val Ala Thr
180 185 190
Ala Gln His Gln Val Asp Asn Leu Lys Lys Leu Leu Ala Gly Ala Asp
195 200 205
Pro Asp Asp Gly Thr Glu Val Ile Glu Ala Lys Leu Lys Lys Gly Glu
210 215 220
Ala Glu Leu Asn Ala Lys Gln Ala Glu Leu Ala Lys Lys Gln Thr Glu
225 230 235 240
Leu Glu Lys Leu Leu Asp Ser Leu Asp Pro Glu Gly Lys Thr Gln Asp
245 250 255
Glu Leu Asp Lys Glu Ala Glu Glu Ala Glu Leu Asp Lys Lys Ala Asp
260 265 270
Glu Leu Gln Asn Lys Val Ala Asp Leu Glu Lys Glu Ile Ser Asn Leu
275 280 285
Glu Ile Leu Leu Gly Gly Ala Asp Pro Glu Asp Asp Thr Ala Ala Leu
290 295 300
Gln Asn Lys Leu Ala Ala Lys Lys Ala Glu Leu Ala Lys Lys Gln Thr
305 310 315 320
Glu Leu Glu Lys Leu Leu Asp Ser Leu Asp Pro Glu Gly Lys Thr Gln
325 330 335
Asp Glu Leu Asp Lys Glu Ala Glu Glu Ala Glu Leu Asp Lys Lys Ala
340 345 350
Asp Glu Leu Gln Asn Lys Val Ala Asp Leu Glu Lys Glu Ile Ser Asn
355 360 365
Leu Glu Ile Leu Leu Gly Gly Ala Asp Ser Glu Asp Asp Thr Ala Ala
370 375 380
Leu Gln Asn Lys Leu Ala Thr Lys Lys Ala Glu Leu Glu Lys Thr Gln
385 390 395 400
Lys Glu Leu Asp Ala Ala Leu Asn Glu Leu Gly Pro Asp Gly Asp Glu
405 410 415
Glu Glu Thr Pro Ala Pro Ala Pro Gln Pro Glu Gln Pro Ala Pro Ala
420 425 430
Pro Lys Pro Glu Gln Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Ala
435 440 445
Pro Ala Pro Lys Pro Glu Gln Pro Ala Pro Ala Pro Lys Pro Glu Gln
450 455 460
Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Ala Lys Pro Glu Lys Pro
465 470 475 480
Ala Glu Glu Pro Thr Gln Pro Glu Lys Pro Ala Thr Pro Lys Thr
485 490 495
<210> 4
<211> 430
<212> PRT
<213> Искусственная последовательность
<220>
<223> конструкция aHD-PRD, рекомбинантный белок слияния, обозначенный
PspA03
<400> 4
Glu Glu Ala Pro Val Ala Asn Gln Ser Lys Ala Glu Lys Asp Tyr Asp
1 5 10 15
Ala Ala Val Lys Lys Ser Glu Ala Ala Lys Lys Asp Tyr Glu Thr Ala
20 25 30
Lys Lys Lys Ala Glu Asp Ala Gln Lys Lys Tyr Asp Glu Asp Gln Lys
35 40 45
Lys Thr Glu Ala Lys Ala Glu Lys Glu Arg Lys Ala Ser Glu Lys Ile
50 55 60
Ala Glu Ala Thr Lys Glu Val Gln Gln Ala Tyr Leu Ala Tyr Leu Gln
65 70 75 80
Ala Ser Asn Glu Ser Gln Arg Lys Glu Ala Asp Lys Lys Ile Lys Glu
85 90 95
Ala Thr Gln Arg Lys Asp Glu Ala Glu Ala Ala Phe Ala Thr Ile Arg
100 105 110
Thr Thr Ile Val Val Pro Glu Pro Ser Glu Leu Ala Glu Thr Lys Lys
115 120 125
Lys Ala Glu Glu Ala Thr Lys Glu Ala Glu Val Ala Lys Lys Lys Ser
130 135 140
Glu Glu Ala Ala Lys Glu Val Glu Val Glu Lys Asn Lys Ile Leu Glu
145 150 155 160
Gln Asp Ala Glu Asn Glu Lys Lys Ile Asp Val Leu Gln Asn Lys Val
165 170 175
Ala Asp Leu Glu Lys Gly Ile Ala Pro Tyr Gln Asn Glu Val Ala Glu
180 185 190
Leu Asn Lys Glu Ile Ala Arg Leu Gln Ser Asp Leu Lys Asp Ala Glu
195 200 205
Glu Asn Asn Val Glu Asp Tyr Ile Lys Glu Gly Leu Glu Gln Ala Ile
210 215 220
Thr Asn Lys Lys Ala Glu Leu Ala Thr Thr Gln Gln Asn Ile Asp Lys
225 230 235 240
Thr Gln Lys Asp Leu Glu Asp Ala Glu Leu Glu Leu Glu Lys Val Leu
245 250 255
Ala Thr Leu Asp Pro Glu Gly Lys Thr Gln Asp Glu Leu Asp Lys Glu
260 265 270
Ala Ala Glu Ala Glu Leu Asn Glu Lys Val Glu Ala Leu Gln Asn Gln
275 280 285
Val Ala Glu Leu Glu Glu Glu Leu Ser Lys Leu Glu Asp Asn Leu Lys
290 295 300
Asp Ala Glu Thr Asn Asn Val Glu Asp Tyr Ile Lys Glu Gly Leu Glu
305 310 315 320
Glu Ala Ile Ala Thr Lys Lys Ala Glu Leu Glu Lys Thr Gln Lys Glu
325 330 335
Leu Asp Ala Ala Leu Asn Glu Leu Gly Pro Glu Lys Pro Ala Glu Glu
340 345 350
Thr Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Ala Glu Gln Pro Lys
355 360 365
Pro Ala Pro Ala Pro Gln Pro Ala Pro Ala Pro Lys Pro Glu Lys Thr
370 375 380
Asp Asp Gln Gln Ala Glu Glu Asp Tyr Ala Arg Arg Ser Glu Glu Glu
385 390 395 400
Tyr Asn Arg Leu Pro Gln Gln Gln Pro Pro Lys Ala Glu Lys Pro Ala
405 410 415
Pro Ala Pro Lys Pro Glu Gln Pro Val Pro Ala Pro Lys Thr
420 425 430
<210> 5
<212> PRT
<213> Streptococcus pneumoniae
<400> 5
Pro Lys Pro Glu Gln Pro
1 5
<210> 6
<211> 6
<212> PRT
<213> Streptococcus pneumoniae
<400> 6
Gln Pro Ala Pro Ala Pro
1 5
<210> 7
<211> 6
<212> PRT
<213> Streptococcus pneumoniae
<400> 7
Pro Lys Pro Ala Pro Ala
1 5
<210> 8
<211> 7
<212> PRT
<213> Streptococcus pneumoniae
<400> 8
Glu Lys Pro Ala Pro Ala Pro
1 5
<210> 9
<211> 6
<212> PRT
<213> Streptococcus pneumoniae
<400> 9
Pro Glu Lys Pro Ala Glu
1 5
<210> 10
<211> 22
<212> PRT
<213> Streptococcus pneumoniae
<400> 10
Gln Gln Ala Glu Glu Asp Tyr Ala Arg Arg Ser Glu Glu Glu Tyr Asn
1 5 10 15
Arg Leu Pro Gln Gln Gln
20
<211> 22
<212> PRT
<213> Streptococcus pneumoniae
<400> 11
Gln Gln Ala Glu Glu Asp Tyr Ala Arg Arg Ser Glu Glu Glu Tyr Asn
1 5 10 15
Arg Leu Thr Gln Gln Gln
20
<210> 12
<211> 96
<212> PRT
<213> Streptococcus pneumoniae
<400> 12
Pro Glu Thr Pro Ala Pro Ala Pro Ala Pro Ala Pro Ala Pro Ala Pro
1 5 10 15
Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro
20 25 30
Lys Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro Lys Pro Ala Pro
35 40 45
Ala Pro Ala Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro Lys Pro
50 55 60
Ala Pro Ala Pro Ala Pro Ala Pro Ala Pro Ala Pro Lys Pro Glu Lys
65 70 75 80
Pro Ala Glu Lys Pro Ala Pro Ala Pro Lys Pro Glu Thr Pro Lys Thr
85 90 95
<210> 13
<211> 68
<212> PRT
<213> Streptococcus pneumoniae
<400> 13
Pro Glu Thr Pro Ala Pro Ala Pro Ala Pro Ala Pro Ala Pro Ala Pro
1 5 10 15
Ala Pro Ala Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro Lys Pro
20 25 30
Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro Ala Pro Ala Pro Ala Pro
35 40 45
Lys Pro Glu Lys Pro Ala Glu Lys Pro Ala Pro Ala Pro Lys Pro Glu
50 55 60
Thr Pro Lys Thr
65
<210> 14
<211> 84
<212> PRT
<213> Искусственная последовательность
<220>
<223> модифицированный PRD PspA штамма EF3296
<400> 14
Pro Asp Gly Asp Glu Glu Glu Thr Pro Ala Pro Ala Pro Gln Pro Glu
1 5 10 15
Gln Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Ala Pro Ala Pro Lys
20 25 30
Pro Glu Gln Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Ala Pro Ala
35 40 45
Pro Lys Pro Glu Gln Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Ala
50 55 60
Lys Pro Glu Lys Pro Ala Glu Glu Pro Thr Gln Pro Glu Lys Pro Ala
65 70 75 80
Thr Pro Lys Thr
<210> 15
<211> 75
<212> PRT
<213> Streptococcus pneumoniae
<400> 15
Pro Asp Gly Asp Glu Glu Glu Thr Pro Ala Pro Ala Pro Gln Pro Glu
1 5 10 15
Gln Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Ala Pro Ala Pro Lys
20 25 30
Pro Glu Gln Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Ala Pro Ala
35 40 45
Pro Lys Pro Glu Gln Pro Ala Lys Pro Glu Lys Pro Ala Glu Glu Pro
50 55 60
Thr Gln Pro Glu Lys Pro Ala Thr Pro Lys Thr
65 70 75
<210> 16
<211> 85
<212> PRT
<213> Streptococcus pneumoniae
<400> 16
Pro Glu Lys Pro Ala Glu Glu Thr Pro Ala Pro Ala Pro Lys Pro Glu
1 5 10 15
Gln Pro Ala Glu Gln Pro Lys Pro Ala Pro Ala Pro Gln Pro Ala Pro
20 25 30
Ala Pro Lys Pro Glu Lys Thr Asp Asp Gln Gln Ala Glu Glu Asp Tyr
35 40 45
Ala Arg Arg Ser Glu Glu Glu Tyr Asn Arg Leu Pro Gln Gln Gln Pro
50 55 60
Pro Lys Ala Glu Lys Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Val
65 70 75 80
Pro Ala Pro Lys Thr
85
<210> 17
<211> 94
<212> PRT
<213> Streptococcus pneumoniae
<400> 17
Pro Glu Lys Pro Ala Glu Glu Thr Pro Ala Pro Ala Pro Lys Pro Glu
1 5 10 15
Gln Pro Ala Glu Gln Pro Lys Pro Ala Pro Ala Pro Gln Pro Ala Pro
20 25 30
Ala Pro Lys Pro Glu Lys Thr Asp Asp Gln Gln Ala Glu Glu Asp Tyr
35 40 45
Ala Arg Arg Ser Glu Glu Glu Tyr Asn Arg Leu Pro Gln Gln Gln Pro
50 55 60
Pro Lys Ala Glu Lys Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Val
65 70 75 80
Pro Ala Pro Lys Pro Glu Gln Pro Val Pro Ala Pro Lys Thr
85 90
<210> 18
<211> 85
<212> PRT
<213> Streptococcus pneumoniae
<400> 18
Pro Asp Gly Asp Glu Glu Glu Thr Pro Ala Pro Ala Pro Lys Pro Glu
1 5 10 15
Gln Pro Ala Glu Gln Pro Lys Pro Ala Pro Ala Pro Gln Pro Ala Pro
20 25 30
Ala Pro Lys Pro Glu Lys Thr Asp Asp Gln Gln Ala Glu Glu Asp Tyr
35 40 45
Ala Arg Arg Ser Glu Glu Glu Tyr Asn Arg Leu Pro Gln Gln Gln Pro
50 55 60
Pro Lys Ala Glu Lys Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Val
65 70 75 80
Pro Ala Pro Lys Thr
85
<210> 19
<211> 85
<212> PRT
<213> Streptococcus pneumoniae
<400> 19
Pro Asp Gly Asp Glu Glu Glu Thr Pro Ala Pro Ala Pro Lys Pro Glu
1 5 10 15
Gln Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro Gln Pro Ala Pro
20 25 30
Ala Pro Lys Pro Glu Lys Thr Asp Asp Gln Gln Ala Glu Glu Asp Tyr
35 40 45
Ala Arg Arg Ser Glu Glu Glu Tyr Asn Arg Leu Pro Gln Gln Gln Pro
50 55 60
Pro Lys Ala Glu Lys Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Val
65 70 75 80
Pro Ala Pro Lys Thr
85
<210> 20
<211> 87
<212> PRT
<213> Streptococcus pneumoniae
<400> 20
Pro Asp Gly Asp Glu Glu Glu Thr Pro Ala Pro Ala Pro Lys Pro Glu
1 5 10 15
Gln Pro Ala Glu Gln Pro Lys Pro Ala Pro Ala Pro Gln Pro Ala Pro
20 25 30
Ala Pro Lys Pro Glu Lys Thr Asp Asp Gln Gln Ala Glu Glu Asp Tyr
35 40 45
Ala Arg Arg Ser Glu Glu Glu Tyr Asn Arg Leu Pro Gln Gln Gln Pro
50 55 60
Pro Lys Ala Glu Lys Pro Ala Pro Ala Pro Ala Pro Lys Pro Glu Gln
65 70 75 80
Pro Ala Pro Ala Pro Lys Thr
85
<210> 21
<211> 77
<212> PRT
<213> Streptococcus pneumoniae
<400> 21
Pro Asp Gly Asp Glu Glu Glu Thr Pro Ala Pro Ala Pro Lys Pro Glu
1 5 10 15
Gln Pro Ala Glu Gln Pro Lys Pro Ala Pro Ala Pro Lys Pro Glu Lys
20 25 30
Thr Asp Asp Gln Gln Ala Glu Glu Asp Tyr Ala Arg Arg Ser Glu Glu
35 40 45
Glu Tyr Asn Arg Leu Pro Gln Gln Gln Pro Pro Lys Ala Glu Lys Pro
50 55 60
Ala Pro Ala Pro Lys Pro Glu Gln Pro Val Pro Ala Pro
65 70 75
<210> 22
<211> 97
<212> PRT
<213> Streptococcus pneumoniae
<400> 22
Pro Asp Gly Asp Glu Glu Glu Thr Pro Ala Pro Ala Pro Gln Pro Glu
1 5 10 15
Lys Pro Ala Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Ala Pro Ala
20 25 30
Pro Ala Pro Lys Pro Glu Gln Pro Ala Pro Ala Pro Ala Pro Lys Pro
35 40 45
Glu Lys Thr Asp Asp Gln Gln Ala Glu Glu Asp Tyr Ala Arg Arg Ser
50 55 60
Glu Glu Glu Tyr Asn Arg Leu Pro Gln Gln Gln Pro Pro Lys Ala Glu
65 70 75 80
Lys Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Val Pro Ala Pro Lys
85 90 95
Thr
<210> 23
<211> 84
<212> PRT
<213> Streptococcus pneumoniae
<400> 23
Pro Asp Gly Asp Glu Glu Glu Thr Pro Ala Pro Ala Pro Gln Pro Glu
1 5 10 15
Lys Pro Ala Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Ala Pro Ala
20 25 30
Pro Lys Pro Glu Lys Thr Asp Asp Gln Gln Ala Glu Glu Asp Tyr Ala
35 40 45
Arg Arg Ser Glu Glu Glu Tyr Asn Arg Leu Pro Gln Gln Gln Pro Pro
50 55 60
Lys Ala Glu Lys Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Val Pro
65 70 75 80
Ala Pro Lys Thr
<210> 24
<211> 86
<212> PRT
<213> Streptococcus pneumoniae
<400> 24
Pro Asp Gly Asp Glu Glu Glu Thr Pro Ala Pro Ala Pro Gln Pro Glu
1 5 10 15
Lys Pro Ala Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Ala Pro Ala
20 25 30
Pro Ala Pro Lys Pro Glu Lys Thr Asp Asp Gln Gln Ala Glu Glu Asp
35 40 45
Tyr Ala Arg Arg Ser Glu Glu Glu Tyr Asn Arg Leu Pro Gln Gln Gln
50 55 60
Pro Pro Lys Ala Glu Lys Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro
65 70 75 80
Val Pro Ala Pro Lys Thr
85
<210> 25
<211> 97
<212> PRT
<213> Streptococcus pneumoniae
<400> 25
Leu Lys Glu Ile Asp Glu Ser Glu Ser Glu Asp Tyr Ala Lys Glu Gly
1 5 10 15
Phe Arg Ala Pro Leu Gln Ser Lys Leu Asp Ala Arg Lys Ala Lys Leu
20 25 30
Ser Lys Leu Glu Glu Leu Ser Asp Lys Ile Asp Glu Leu Asp Ala Glu
35 40 45
Ile Ala Lys Leu Glu Asp Gln Leu Lys Ala Ala Glu Glu Asn Asn Asn
50 55 60
Val Glu Asp Tyr Phe Lys Glu Gly Leu Glu Lys Thr Ile Ala Ala Lys
65 70 75 80
Lys Ala Glu Leu Glu Lys Thr Glu Ala Asp Leu Lys Lys Ala Val Asn
85 90 95
Glu
<210> 26
<211> 97
<212> PRT
<213> Streptococcus pneumoniae
<400> 26
Leu Lys Asp Ile Asn Glu Ser Asp Ser Glu Asp Tyr Val Lys Glu Gly
1 5 10 15
Leu Arg Ala Pro Leu Gln Ser Glu Leu Asp Thr Lys Lys Ala Lys Leu
20 25 30
Leu Lys Leu Glu Glu Leu Ser Gly Lys Ile Glu Glu Leu Asp Ala Glu
35 40 45
Ile Ala Glu Leu Glu Val Gln Leu Lys Asp Ala Glu Gly Asn Asn Asn
50 55 60
Val Glu Ala Tyr Phe Lys Glu Gly Leu Glu Lys Thr Thr Ala Glu Lys
65 70 75 80
Lys Ala Glu Leu Glu Lys Ala Glu Ala Asp Leu Lys Lys Ala Val Asp
85 90 95
Glu
<210> 27
<211> 97
<212> PRT
<213> Streptococcus pneumoniae
<400> 27
Leu Lys Glu Ile Asp Glu Ser Asp Ser Glu Asp Tyr Ile Lys Glu Gly
1 5 10 15
Phe Arg Ala Pro Leu Gln Ser Glu Leu Asp Thr Lys Lys Ala Lys Leu
20 25 30
Leu Lys Leu Glu Glu Leu Ser Gly Lys Ile Glu Glu Leu Asp Ala Glu
35 40 45
Ile Ala Glu Leu Glu Val Gln Leu Lys Asp Ala Glu Gly Asn Asn Asn
50 55 60
Val Glu Ala Tyr Phe Lys Glu Gly Leu Glu Lys Thr Thr Ala Glu Lys
65 70 75 80
Lys Ala Glu Leu Glu Lys Ala Glu Ala Asp Leu Lys Lys Ala Val Asp
85 90 95
Glu
<210> 28
<211> 280
<212> PRT
<213> Streptococcus pneumoniae
<400> 28
Glu Glu Ala Pro Val Ala Ser Gln Ser Lys Ala Glu Lys Asp Tyr Asp
1 5 10 15
Ala Ala Met Glu Lys Tyr Lys Ala Ala Glu Glu Asp Leu Glu Lys Ala
20 25 30
Glu Ala Ala Gln Arg Lys Tyr Asp Glu Asp Gln Lys Lys Ser Glu Glu
35 40 45
Asn Glu Lys Glu Thr Glu Glu Ala Ser Glu Arg Gln Gln Ala Ala Thr
50 55 60
Leu Lys Tyr Gln Leu Lys Leu Arg Glu Tyr Leu Lys Tyr Ile Gln Glu
65 70 75 80
Lys Asn Lys Glu Lys Ile Ala Lys Ala Glu Lys Glu Met Asn Glu Ala
85 90 95
Lys Gln Glu Glu Asp Lys Glu Lys Ala Asn Leu Asn Lys Val Leu Ala
100 105 110
Lys Val Ile Pro Ser Asp Arg Glu Leu Glu Lys Thr Arg Gln Glu Ala
115 120 125
Glu Lys Ala Lys Lys Asn Ile Pro Glu Leu Lys Lys Lys Val Glu Glu
130 135 140
Ala Lys Gln Lys Val Asp Ala Ala Lys Gln Lys Val Asp Ala Glu His
145 150 155 160
Ala Lys Glu Val Ala Pro Gln Ala Lys Ile Ala Glu Leu Glu Asn Gln
165 170 175
Val His Arg Leu Glu Gln Asp Leu Lys Asp Ile Asn Glu Ser Asp Ser
180 185 190
Glu Asp Tyr Val Lys Glu Gly Leu Arg Ala Pro Leu Gln Ser Glu Leu
195 200 205
Asp Thr Lys Lys Ala Lys Leu Leu Lys Leu Glu Glu Leu Ser Gly Lys
210 215 220
Ile Glu Glu Leu Asp Ala Glu Ile Ala Glu Leu Glu Val Gln Leu Lys
225 230 235 240
Asp Ala Glu Gly Asn Asn Asn Val Glu Ala Tyr Phe Lys Glu Gly Leu
245 250 255
Glu Lys Thr Thr Ala Glu Lys Lys Ala Glu Leu Glu Lys Ala Glu Ala
260 265 270
Asp Leu Lys Lys Ala Val Asp Glu
275 280
<210> 29
<211> 280
<212> PRT
<213> Streptococcus pneumoniae
<400> 29
Glu Glu Ala Pro Val Ala Ser Gln Ser Lys Ala Glu Lys Asp Tyr Asp
1 5 10 15
Ala Ala Met Glu Lys Tyr Lys Ala Ala Glu Glu Asp Leu Lys Lys Ala
20 25 30
Glu Ala Ala Gln Arg Lys Tyr Asp Glu Asp Gln Lys Lys Thr Glu Glu
35 40 45
Lys Ala Lys Glu Thr Glu Glu Ala Ser Lys Arg Gln Gln Ala Ala Asn
50 55 60
Leu Lys Tyr Gln Leu Lys Leu Arg Glu Tyr Leu Lys Tyr Ile Gln Glu
65 70 75 80
Lys Asn Lys Glu Lys Ile Ala Lys Ala Glu Lys Glu Met Asn Glu Ala
85 90 95
Lys Gln Glu Glu Asp Lys Glu Lys Ala Asn Leu Asn Lys Val Leu Ala
100 105 110
Lys Val Ile Pro Ser Asp Arg Glu Leu Glu Lys Thr Arg Gln Glu Ala
115 120 125
Glu Lys Ala Lys Lys Asn Ile Pro Glu Leu Lys Lys Lys Val Glu Glu
130 135 140
Ala Lys Gln Lys Val Asp Ala Ala Lys Gln Lys Val Asp Ala Glu His
145 150 155 160
Ala Lys Glu Val Ala Pro Gln Ala Lys Ile Ala Glu Leu Glu Asn Gln
165 170 175
Val His Arg Leu Glu Gln Asp Leu Lys Asp Ile Asn Glu Ser Asp Ser
180 185 190
Glu Asp Tyr Val Lys Glu Gly Leu Arg Ala Pro Leu Gln Ser Glu Leu
195 200 205
Asp Thr Lys Lys Ala Lys Leu Leu Lys Leu Glu Glu Leu Ser Gly Lys
210 215 220
Ile Glu Glu Leu Asp Ala Glu Ile Ala Glu Leu Glu Val Gln Leu Lys
225 230 235 240
Asp Ala Glu Gly Asn Asn Asn Val Glu Ala Tyr Phe Lys Glu Gly Leu
245 250 255
Glu Lys Thr Thr Ala Glu Lys Lys Ala Glu Leu Glu Lys Ala Glu Ala
260 265 270
Asp Leu Lys Lys Ala Val Asp Glu
275 280
<210> 30
<211> 280
<212> PRT
<213> Streptococcus pneumoniae
<400> 30
Glu Glu Ala Pro Val Ala Ser Gln Ser Lys Ala Glu Lys Asp Tyr Asp
1 5 10 15
Ala Ala Met Glu Lys Tyr Lys Ala Ala Glu Glu Asp Leu Lys Lys Ala
20 25 30
Glu Ala Ala Gln Arg Lys Tyr Asp Glu Asp Gln Lys Lys Thr Glu Glu
35 40 45
Lys Ala Lys Glu Thr Glu Glu Ala Ser Lys Arg Gln Gln Ala Ala Asn
50 55 60
Leu Lys Tyr Gln Leu Lys Leu Arg Glu Tyr Leu Lys Tyr Ile Gln Glu
65 70 75 80
Lys Asn Lys Glu Lys Ile Ala Lys Ala Glu Lys Glu Met Asn Glu Ala
85 90 95
Lys Gln Glu Glu Asp Lys Glu Lys Ala Asn Leu Asn Lys Val Leu Ala
100 105 110
Lys Val Ile Pro Ser Asp Arg Glu Leu Glu Lys Thr Arg Gln Glu Ala
115 120 125
Glu Lys Ala Lys Lys Asn Ile Pro Glu Leu Lys Lys Lys Val Glu Glu
130 135 140
Ala Lys Gln Lys Val Asp Ala Ala Lys Gln Lys Val Asp Ala Glu His
145 150 155 160
Ala Lys Glu Val Ala Pro Gln Ala Lys Ile Ala Glu Leu Glu Asn Gln
165 170 175
Val His Arg Leu Glu Gln Asp Leu Lys Asp Ile Asn Glu Ser Asp Ser
180 185 190
Glu Asp Tyr Val Lys Glu Gly Leu Arg Ala Pro Leu Gln Ser Glu Leu
195 200 205
Asp Thr Lys Lys Ala Lys Leu Leu Lys Leu Glu Glu Leu Ser Gly Lys
210 215 220
Ile Glu Glu Leu Asp Ala Glu Ile Ala Glu Leu Glu Val Gln Leu Lys
225 230 235 240
Asp Ala Glu Gly Asn Asn Asn Val Glu Ala Tyr Phe Lys Glu Gly Leu
245 250 255
Glu Lys Thr Thr Ala Glu Lys Lys Ala Glu Leu Glu Lys Ala Glu Ala
260 265 270
Asp Leu Lys Lys Ala Val Asp Glu
275 280
<210> 31
<211> 302
<212> PRT
<213> Streptococcus pneumoniae
<400> 31
Glu Glu Ala Pro Val Ala Ser Gln Ser Lys Ala Glu Lys Asp Tyr Asp
1 5 10 15
Ala Ala Val Lys Lys Ser Glu Ala Ala Lys Lys His Tyr Glu Glu Val
20 25 30
Lys Ala Lys Phe Glu Ala Ala Lys Lys Glu Tyr Glu Asp Gly Lys Ala
35 40 45
Ala Gln Lys Lys Tyr Glu Asp Asp Gln Lys Lys Thr Glu Glu Lys Ala
50 55 60
Glu Glu Glu Arg Lys Ala Ser Glu Glu Glu Gln Ala Ala Asn Leu Lys
65 70 75 80
Tyr Gln Gln Ala Val Leu Lys Tyr Ile Lys Glu Thr Asp Pro Gln Lys
85 90 95
Arg Val Glu Ala Gln Lys Val Met Asp Glu Ala Gln Lys Glu His Thr
100 105 110
Arg Thr Lys Glu Lys Phe Asp Glu Val Arg Ala Lys Val Ile Pro Ser
115 120 125
Glu Glu Glu Leu Lys Lys Thr Arg Gln Lys Ala Glu Glu Ala Lys Leu
130 135 140
Lys Glu Ala Glu Val Ala Lys Lys Val Glu Glu Thr Lys Lys Gln Glu
145 150 155 160
Glu Glu Ala Lys Ala Lys Leu Glu Glu Ala Glu Lys Lys Ala Thr Glu
165 170 175
Ala Lys Gln Lys Val Asp Ala Glu Glu Val Ala Pro Gln Ala Lys Ile
180 185 190
Ala Glu Leu Glu Asn Gln Val His Arg Leu Glu Gln Glu Leu Lys Glu
195 200 205
Ile Asp Glu Ser Asp Ser Glu Asp Tyr Ile Lys Glu Gly Phe Arg Ala
210 215 220
Pro Leu Gln Ser Glu Leu Asp Thr Lys Lys Ala Lys Leu Leu Lys Leu
225 230 235 240
Glu Glu Leu Ser Gly Lys Ile Glu Glu Leu Asp Ala Glu Ile Ala Glu
245 250 255
Leu Glu Val Gln Leu Lys Asp Ala Glu Gly Asn Asn Asn Val Glu Ala
260 265 270
Tyr Phe Lys Glu Gly Leu Glu Lys Thr Thr Ala Glu Lys Lys Ala Glu
275 280 285
Leu Glu Lys Ala Glu Ala Asp Leu Lys Lys Ala Val Asp Glu
290 295 300
<210> 32
<211> 97
<212> PRT
<213> Streptococcus pneumoniae
<400> 32
Leu Ala Lys Lys Gln Thr Glu Leu Glu Lys Leu Leu Asp Ser Leu Asp
1 5 10 15
Pro Glu Gly Lys Thr Gln Asp Glu Leu Asp Lys Glu Ala Glu Glu Ala
20 25 30
Glu Leu Asp Lys Lys Ala Asp Glu Leu Gln Asn Lys Val Ala Asp Leu
35 40 45
Glu Lys Glu Ile Ser Asn Leu Glu Ile Leu Leu Gly Gly Ala Asp Ser
50 55 60
Glu Asp Asp Thr Ala Ala Leu Gln Asn Lys Leu Ala Thr Lys Lys Ala
65 70 75 80
Glu Leu Glu Lys Thr Gln Lys Glu Leu Asp Ala Ala Leu Asn Glu Leu
85 90 95
Gly
<210> 33
<211> 319
<212> PRT
<213> Streptococcus pneumoniae
<400> 33
Glu Glu Ser Pro Val Ala Ser Gln Ser Lys Ala Glu Lys Asp Tyr Asp
1 5 10 15
Ala Ala Val Lys Lys Ser Glu Ala Ala Lys Lys His Tyr Glu Glu Ala
20 25 30
Lys Lys Lys Ala Glu Asp Ala Gln Lys Lys Tyr Asp Glu Asp Gln Lys
35 40 45
Lys Thr Glu Ala Lys Ala Glu Lys Glu Arg Lys Ala Ser Glu Lys Ile
50 55 60
Ala Glu Ala Thr Lys Glu Val Gln Gln Ala Tyr Leu Ala Tyr Leu Gln
65 70 75 80
Ala Ser Asn Glu Ser Gln Arg Lys Glu Ala Asp Lys Lys Ile Lys Glu
85 90 95
Ala Thr Gln Arg Lys Asp Glu Ala Glu Ala Ala Phe Ala Thr Ile Arg
100 105 110
Thr Thr Ile Val Val Pro Glu Pro Ser Glu Leu Ala Glu Thr Lys Lys
115 120 125
Lys Ala Glu Glu Ala Lys Ala Glu Glu Lys Val Ala Lys Arg Lys Tyr
130 135 140
Asp Tyr Ala Thr Leu Lys Leu Ala Leu Ala Lys Lys Glu Val Glu Ala
145 150 155 160
Lys Glu Leu Glu Ile Glu Lys Leu Gln Tyr Glu Ile Ser Thr Leu Glu
165 170 175
Gln Glu Val Ala Thr Ala Gln His Gln Val Asp Asn Leu Lys Lys Leu
180 185 190
Leu Ala Gly Ala Asp Pro Asp Asp Gly Thr Glu Val Ile Glu Ala Lys
195 200 205
Leu Lys Lys Gly Glu Ala Glu Leu Asn Ala Lys Gln Ala Glu Leu Ala
210 215 220
Lys Lys Gln Thr Glu Leu Glu Lys Leu Leu Asp Ser Leu Asp Pro Glu
225 230 235 240
Gly Lys Thr Gln Asp Glu Leu Asp Lys Glu Ala Glu Glu Ala Glu Leu
245 250 255
Asp Lys Lys Ala Asp Glu Leu Gln Asn Lys Val Ala Asp Leu Glu Lys
260 265 270
Glu Ile Ser Asn Leu Glu Ile Leu Leu Gly Gly Ala Asp Ser Glu Asp
275 280 285
Asp Thr Ala Ala Leu Gln Asn Lys Leu Ala Thr Lys Lys Ala Glu Leu
290 295 300
Glu Lys Thr Gln Lys Glu Leu Asp Ala Ala Leu Asn Glu Leu Gly
305 310 315
<210> 34
<211> 319
<212> PRT
<213> Streptococcus pneumoniae
<400> 34
Glu Glu Ala Pro Val Ala Ser Gln Ser Lys Ala Glu Lys Asp Tyr Asp
1 5 10 15
Ala Ala Val Lys Lys Ser Glu Ala Ala Lys Lys His Tyr Glu Glu Val
20 25 30
Lys Lys Lys Ala Glu Asp Ala Gln Lys Lys Tyr Asp Glu Gly Gln Lys
35 40 45
Lys Thr Val Glu Lys Ala Lys Arg Glu Lys Glu Ala Ser Glu Lys Ile
50 55 60
Ala Glu Ala Thr Lys Glu Val Gln Gln Ala Tyr Leu Ala Tyr Gln Gln
65 70 75 80
Ala Ser Asn Glu Ser Gln Arg Lys Glu Ala Asp Lys Lys Ile Lys Glu
85 90 95
Ala Thr Gln Arg Lys Asp Glu Ala Glu Ala Ala Phe Ala Thr Ile Arg
100 105 110
Thr Thr Ile Val Val Pro Glu Pro Ser Glu Leu Ala Glu Thr Lys Lys
115 120 125
Lys Ala Glu Glu Ala Lys Ala Glu Glu Lys Val Ala Lys Arg Lys Tyr
130 135 140
Asp Tyr Ala Thr Leu Lys Val Ala Leu Ala Lys Lys Glu Val Glu Ala
145 150 155 160
Lys Glu Leu Glu Ile Glu Lys Leu Gln Tyr Glu Ile Ser Thr Leu Glu
165 170 175
Gln Glu Val Ala Thr Ala Gln His Gln Val Asp Asn Leu Lys Lys Leu
180 185 190
Leu Ala Gly Ala Asp Pro Asp Asp Gly Thr Glu Val Ile Glu Ala Lys
195 200 205
Leu Asn Lys Gly Glu Ala Glu Leu Asn Ala Lys Gln Ala Glu Leu Ala
210 215 220
Lys Lys Gln Thr Glu Leu Glu Lys Leu Leu Asp Ser Leu Asp Pro Glu
225 230 235 240
Gly Lys Thr Gln Asp Glu Leu Asp Lys Glu Ala Glu Glu Ala Glu Leu
245 250 255
Asp Lys Lys Ala Asp Glu Leu Gln Asn Lys Val Ala Asp Leu Glu Lys
260 265 270
Glu Ile Ser Asn Leu Glu Ile Leu Leu Gly Gly Ala Asp Ser Glu Asp
275 280 285
Asp Thr Ala Ala Leu Gln Asn Lys Leu Ala Thr Lys Lys Ala Glu Leu
290 295 300
Glu Lys Thr Gln Lys Glu Leu Asp Ala Ala Leu Asn Glu Leu Gly
305 310 315
<210> 35
<211> 319
<212> PRT
<213> Streptococcus pneumoniae
<400> 35
Glu Glu Ala Pro Val Ala Ser Gln Ser Lys Ala Glu Lys Asp Tyr Asp
1 5 10 15
Ala Ala Val Lys Lys Ser Glu Ala Ala Lys Lys His Tyr Glu Glu Val
20 25 30
Lys Lys Lys Ala Glu Asp Ala Gln Lys Lys Tyr Asp Glu Gly Gln Lys
35 40 45
Lys Thr Val Glu Lys Ala Lys Arg Glu Lys Glu Ala Ser Glu Lys Ile
50 55 60
Ala Glu Ala Thr Lys Glu Val Gln Gln Ala Tyr Leu Ala Tyr Gln Gln
65 70 75 80
Ala Ser Asn Glu Ser Gln Arg Lys Glu Ala Asp Lys Lys Ile Lys Glu
85 90 95
Ala Thr Gln Arg Lys Asp Glu Ala Glu Ala Ala Phe Ala Thr Ile Arg
100 105 110
Thr Thr Ile Val Val Pro Glu Pro Ser Glu Leu Ala Glu Thr Lys Lys
115 120 125
Lys Ala Glu Glu Ala Lys Ala Glu Glu Lys Val Ala Lys Arg Lys Tyr
130 135 140
Asp Tyr Ala Thr Leu Lys Val Ala Leu Ala Lys Lys Glu Val Glu Ala
145 150 155 160
Lys Glu Leu Glu Ile Glu Lys Leu Gln Tyr Glu Ile Ser Thr Leu Glu
165 170 175
Gln Glu Val Ala Thr Ala Gln His Gln Val Asp Asn Leu Lys Lys Leu
180 185 190
Leu Ala Gly Ala Asp Pro Asp Asp Gly Thr Glu Val Ile Glu Ala Lys
195 200 205
Leu Asn Lys Gly Glu Ala Glu Leu Asn Ala Lys Gln Ala Glu Leu Ala
210 215 220
Lys Lys Gln Thr Glu Leu Glu Lys Leu Leu Asp Ser Leu Asp Pro Glu
225 230 235 240
Gly Lys Thr Gln Asp Glu Leu Asp Lys Glu Ala Glu Glu Ala Glu Leu
245 250 255
Asp Lys Lys Ala Asp Glu Leu Gln Asn Lys Val Ala Asp Leu Glu Lys
260 265 270
Glu Ile Ser Asn Leu Glu Ile Leu Leu Gly Gly Ala Asp Ser Glu Asp
275 280 285
Asp Thr Ala Ala Leu Gln Asn Lys Leu Ala Thr Lys Lys Ala Glu Leu
290 295 300
Glu Lys Thr Gln Lys Glu Leu Asp Ala Ala Leu Asn Glu Leu Gly
305 310 315
<210> 36
<211> 319
<212> PRT
<213> Streptococcus pneumoniae
<400> 36
Glu Glu Ala Pro Val Ala Ser Gln Ser Lys Ala Glu Lys Asp Tyr Asp
1 5 10 15
Ala Ala Val Lys Lys Ser Glu Ala Ala Lys Lys His Tyr Glu Glu Val
20 25 30
Lys Lys Lys Ala Glu Asp Ala Gln Lys Lys Tyr Asp Glu Gly Gln Lys
35 40 45
Lys Thr Val Glu Lys Ala Lys Arg Glu Lys Glu Ala Ser Glu Lys Ile
50 55 60
Ala Glu Ala Thr Lys Glu Val Gln Gln Ala Tyr Leu Ala Tyr Gln Gln
65 70 75 80
Ala Ser Asn Glu Ser Gln Arg Lys Glu Ala Asp Lys Lys Ile Lys Glu
85 90 95
Ala Thr Gln Arg Lys Asp Glu Ala Glu Ala Ala Phe Ala Thr Ile Arg
100 105 110
Thr Thr Ile Val Val Pro Glu Pro Ser Glu Leu Ala Glu Thr Lys Lys
115 120 125
Lys Ala Glu Glu Ala Lys Ala Glu Glu Lys Val Ala Lys Arg Lys Tyr
130 135 140
Asp Tyr Ala Thr Leu Lys Val Ala Leu Ala Lys Lys Glu Val Glu Ala
145 150 155 160
Lys Glu Leu Glu Ile Glu Lys Leu Gln Tyr Glu Ile Ser Thr Leu Glu
165 170 175
Gln Glu Val Ala Thr Ala Gln His Gln Val Asp Asn Leu Lys Lys Leu
180 185 190
Leu Ala Gly Ala Asp Pro Asp Asp Gly Thr Glu Val Ile Glu Ala Lys
195 200 205
Leu Asn Lys Gly Glu Ala Glu Leu Asn Ala Lys Gln Ala Glu Leu Ala
210 215 220
Lys Lys Gln Thr Glu Leu Glu Lys Leu Leu Asp Ser Leu Asp Pro Glu
225 230 235 240
Gly Lys Thr Gln Asp Glu Leu Asp Lys Glu Ala Glu Glu Ala Glu Leu
245 250 255
Asp Lys Lys Ala Asp Glu Leu Gln Asn Lys Val Ala Asp Leu Glu Lys
260 265 270
Glu Ile Ser Asn Leu Glu Ile Leu Leu Gly Gly Ala Asp Ser Glu Asp
275 280 285
Asp Thr Ala Ala Leu Gln Asn Lys Leu Ala Thr Lys Lys Ala Glu Leu
290 295 300
Glu Lys Thr Gln Lys Glu Leu Asp Ala Ala Leu Asn Glu Leu Gly
305 310 315
<210> 37
<211> 218
<212> PRT
<213> Streptococcus pneumoniae
<400> 37
Glu Glu Ala Pro Val Ala Ser Gln Ser Lys Ala Glu Lys Asp Tyr Asp
1 5 10 15
Ala Ala Val Lys Lys Ser Glu Ala Ala Lys Lys Asp Tyr Glu Glu Ala
20 25 30
Lys Lys Lys Ala Lys Glu Ala Gln Lys Lys Tyr Asp Glu Ala Ala Gln
35 40 45
Glu Val Glu Val Ala Lys Lys Glu Val Glu Ala Lys Glu Leu Glu Ile
50 55 60
Glu Lys Leu Gln Asp Glu Ile Ser Thr Leu Glu Gln Glu Val Ala Thr
65 70 75 80
Ala Gln His Gln Val Asp Asn Leu Lys Lys Leu Leu Ala Gly Ala Asp
85 90 95
Pro Asp Asp Gly Thr Glu Val Ile Glu Ala Lys Leu Lys Lys Gly Glu
100 105 110
Ala Glu Leu Asn Ala Lys Gln Ala Glu Leu Ala Lys Lys Gln Thr Glu
115 120 125
Leu Glu Lys Leu Leu Asp Ser Leu Asp Pro Glu Gly Lys Thr Gln Asp
130 135 140
Glu Leu Asp Lys Glu Ala Glu Glu Ala Glu Leu Asp Lys Lys Ala Asp
145 150 155 160
Glu Leu Gln Asn Lys Val Ala Asp Leu Glu Lys Glu Ile Ser Asn Leu
165 170 175
Glu Ile Leu Leu Gly Gly Ala Asp Ser Glu Asp Asp Thr Ala Ala Leu
180 185 190
Gln Asn Lys Leu Ala Thr Lys Lys Ala Glu Leu Glu Lys Thr Gln Lys
195 200 205
Glu Leu Asp Ala Ala Leu Asn Glu Leu Gly
210 215
<210> 38
<211> 329
<212> PRT
<213> Streptococcus pneumoniae
<400> 38
Glu Glu Ala Pro Val Ala Ser Gln Ser Lys Ala Glu Lys Asp Tyr Asp
1 5 10 15
Ala Ala Val Lys Lys Ser Glu Ala Ala Lys Lys Asp Tyr Glu Glu Ala
20 25 30
Lys Lys Lys Ala Lys Glu Ala Gln Lys Lys Tyr Asp Glu Glu Gln Lys
35 40 45
Lys Thr Glu Glu Lys Ala Lys Lys Glu Lys Glu Ala Ala Lys Lys Val
50 55 60
Asp Asp Ala Ser Leu Ala Val Gln Lys Ala His Val Glu Tyr Arg Lys
65 70 75 80
Val Leu Phe Ser Arg Asn Ser Tyr Lys Tyr Lys Ser Asp Tyr Asp Lys
85 90 95
Lys Leu Ala Glu Ala Gln Ala Lys Ile Asp Glu Ala Asn Lys Lys Leu
100 105 110
Thr Ala Ala Asn Asn Glu Phe Gln Thr Val Arg Ala Val Val Val Pro
115 120 125
Glu Pro Asn Ala Leu Ala Glu Thr Lys Lys Lys Ala Glu Glu Ala Lys
130 135 140
Ala Glu Glu Val Val Ala Lys Lys Lys Tyr Asp Glu Ala Ala Gln Glu
145 150 155 160
Val Glu Val Ala Lys Lys Glu Val Glu Ala Lys Glu Leu Glu Ile Glu
165 170 175
Lys Leu Gln Asp Glu Ile Ser Thr Leu Glu Gln Glu Val Ala Thr Ala
180 185 190
Gln His Gln Val Asp Asn Leu Lys Lys Leu Leu Ala Gly Ala Asp Pro
195 200 205
Asp Asp Gly Thr Glu Val Ile Glu Ala Lys Leu Lys Lys Gly Glu Ala
210 215 220
Glu Leu Asn Ala Lys Gln Ala Glu Leu Ala Lys Lys Gln Thr Glu Leu
225 230 235 240
Glu Lys Leu Leu Asp Ser Leu Asp Pro Glu Gly Lys Thr Gln Asp Glu
245 250 255
Leu Asp Lys Glu Ala Glu Glu Ala Glu Leu Asp Lys Lys Ala Asp Glu
260 265 270
Leu Gln Asn Lys Val Ala Asp Leu Glu Lys Glu Ile Ser Asn Leu Glu
275 280 285
Ile Leu Leu Gly Gly Ala Asp Ser Glu Asp Asp Thr Ala Ala Leu Gln
290 295 300
Asn Lys Leu Ala Thr Lys Lys Ala Glu Leu Glu Lys Thr Gln Lys Glu
305 310 315 320
Leu Asp Ala Ala Leu Asn Glu Leu Gly
325
<210> 39
<211> 329
<212> PRT
<213> Streptococcus pneumoniae
<400> 39
Glu Glu Ala Pro Val Ala Ser Gln Ser Lys Ala Glu Lys Asp Tyr Asp
1 5 10 15
Ala Ala Val Lys Lys Ser Glu Ala Ala Lys Lys Asp Tyr Glu Glu Ala
20 25 30
Lys Lys Lys Ala Lys Glu Ala Gln Lys Lys Tyr Asp Glu Glu Gln Lys
35 40 45
Lys Thr Glu Glu Lys Ala Lys Lys Glu Lys Glu Ala Ala Lys Lys Val
50 55 60
Asp Asp Ala Ser Leu Ala Val Gln Lys Ala His Val Glu Tyr Arg Lys
65 70 75 80
Val Leu Phe Ser Arg Asn Ser Tyr Lys Tyr Lys Ser Asp Tyr Asp Lys
85 90 95
Lys Leu Ala Glu Ala Gln Ala Lys Ile Asp Glu Ala Asn Lys Lys Leu
100 105 110
Thr Ala Ala Asn Asn Glu Phe Gln Thr Val Arg Ala Val Val Val Pro
115 120 125
Glu Pro Asn Ala Leu Ala Glu Thr Lys Lys Lys Ala Glu Glu Ala Lys
130 135 140
Ala Glu Glu Val Val Ala Lys Lys Lys Tyr Asp Glu Ala Ala Gln Glu
145 150 155 160
Val Glu Val Ala Lys Lys Glu Val Glu Ala Lys Glu Leu Glu Ile Glu
165 170 175
Lys Leu Gln Asp Glu Ile Ser Thr Leu Glu Gln Glu Val Ala Thr Ala
180 185 190
Gln His Gln Val Asp Asn Leu Lys Lys Leu Leu Ala Gly Ala Asp Pro
195 200 205
Asp Asp Gly Thr Glu Val Ile Glu Ala Lys Leu Lys Lys Gly Glu Ala
210 215 220
Glu Leu Asn Ala Lys Gln Ala Glu Leu Ala Lys Lys Gln Thr Glu Leu
225 230 235 240
Glu Lys Leu Leu Asp Ser Leu Asp Pro Glu Gly Lys Thr Gln Asp Glu
245 250 255
Leu Asp Lys Glu Ala Glu Glu Ala Glu Leu Asp Lys Lys Ala Asp Glu
260 265 270
Leu Gln Asn Lys Val Ala Asp Leu Glu Lys Glu Ile Ser Asn Leu Glu
275 280 285
Ile Leu Leu Gly Gly Ala Asp Ser Glu Asp Asp Thr Ala Ala Leu Gln
290 295 300
Asn Lys Leu Ala Thr Lys Lys Ala Glu Leu Glu Lys Thr Gln Lys Glu
305 310 315 320
Leu Asp Ala Ala Leu Asn Glu Leu Gly
325
<210> 40
<211> 329
<212> PRT
<213> Streptococcus pneumoniae
<400> 40
Glu Glu Ala Pro Val Ala Ser Gln Ser Lys Ala Glu Lys Asp Tyr Asp
1 5 10 15
Ala Ala Val Lys Lys Ser Glu Ala Ala Lys Lys Asp Tyr Glu Glu Ala
20 25 30
Lys Lys Lys Ala Lys Glu Ala Gln Lys Lys Tyr Asp Glu Glu Gln Lys
35 40 45
Lys Thr Glu Glu Lys Ala Lys Lys Glu Lys Glu Ala Ala Lys Lys Val
50 55 60
Asp Asp Ala Ser Leu Ala Val Gln Lys Ala His Val Glu Tyr Arg Lys
65 70 75 80
Val Leu Phe Ser Arg Asn Ser Tyr Lys Tyr Lys Ser Asp Tyr Asp Lys
85 90 95
Lys Leu Ala Glu Ala Gln Ala Lys Ile Asp Glu Ala Asn Lys Lys Leu
100 105 110
Thr Ala Ala Asn Asn Glu Phe Gln Thr Val Arg Ala Val Val Val Pro
115 120 125
Glu Pro Asn Ala Leu Ala Glu Thr Lys Lys Lys Ala Glu Glu Ala Lys
130 135 140
Ala Glu Glu Val Val Ala Lys Lys Lys Ser Asp Glu Ala Ala Gln Glu
145 150 155 160
Val Glu Val Ala Lys Lys Glu Val Glu Ala Lys Glu Leu Glu Ile Glu
165 170 175
Lys Leu Gln Asp Glu Ile Ser Thr Leu Glu Gln Glu Val Ala Thr Ala
180 185 190
Gln His Gln Val Asp Asn Leu Lys Lys Leu Leu Ala Gly Ala Asp Pro
195 200 205
Asp Asp Gly Thr Glu Val Ile Glu Ala Lys Leu Lys Lys Gly Glu Ala
210 215 220
Glu Leu Asn Ala Lys Gln Ala Glu Leu Ala Lys Lys Gln Thr Glu Leu
225 230 235 240
Glu Lys Leu Leu Asp Ser Leu Asp Pro Glu Gly Lys Thr Gln Asp Glu
245 250 255
Leu Asp Lys Glu Ala Glu Glu Ala Glu Leu Asp Lys Lys Ala Asp Glu
260 265 270
Leu Gln Asn Lys Val Ala Asp Leu Glu Lys Glu Ile Ser Asn Leu Glu
275 280 285
Ile Leu Leu Gly Gly Ala Asp Ser Glu Asp Asp Thr Ala Ala Leu Gln
290 295 300
Asn Lys Leu Ala Thr Lys Lys Ala Glu Leu Glu Lys Thr Gln Lys Glu
305 310 315 320
Leu Asp Ala Ala Leu Asn Glu Leu Gly
325
<210> 41
<211> 329
<212> PRT
<213> Streptococcus pneumoniae
<400> 41
Glu Glu Ala Pro Val Ala Ser Gln Ser Lys Ala Glu Lys Asp Tyr Asp
1 5 10 15
Ala Ala Val Lys Lys Ser Glu Ala Ala Lys Lys Asp Tyr Glu Glu Ala
20 25 30
Lys Lys Lys Ala Lys Glu Ala Gln Lys Lys Tyr Asp Glu Glu Gln Lys
35 40 45
Lys Thr Glu Glu Lys Ala Lys Lys Glu Lys Glu Ala Ala Lys Lys Val
50 55 60
Asp Asp Ala Ser Leu Ala Val Gln Lys Ala His Val Glu Tyr Arg Lys
65 70 75 80
Val Leu Phe Ser Arg Asn Ser Tyr Lys Tyr Lys Ser Asp Tyr Asp Lys
85 90 95
Lys Leu Ala Glu Ala Gln Ala Lys Ile Asp Glu Ala Asn Lys Lys Leu
100 105 110
Thr Ala Ala Asn Asn Glu Phe Gln Thr Val Arg Ala Val Val Val Pro
115 120 125
Glu Pro Asn Ala Leu Ala Glu Thr Lys Lys Lys Ala Glu Glu Ala Lys
130 135 140
Ala Glu Glu Val Val Ala Lys Lys Lys Ser Asp Glu Ala Ala Gln Glu
145 150 155 160
Val Glu Val Ala Lys Lys Glu Val Glu Ala Lys Glu Leu Glu Ile Glu
165 170 175
Lys Leu Gln Asp Glu Ile Ser Thr Leu Glu Gln Glu Val Ala Thr Ala
180 185 190
Gln His Gln Val Asp Asn Leu Lys Lys Leu Leu Ala Gly Ala Asp Pro
195 200 205
Asp Asp Gly Thr Glu Val Ile Glu Ala Lys Leu Lys Lys Gly Glu Ala
210 215 220
Glu Leu Asn Ala Lys Gln Ala Glu Leu Ala Lys Lys Gln Thr Glu Leu
225 230 235 240
Glu Lys Leu Leu Asp Ser Leu Asp Pro Glu Gly Lys Thr Gln Asp Glu
245 250 255
Leu Asp Lys Glu Ala Glu Glu Ala Glu Leu Asp Lys Lys Ala Asp Glu
260 265 270
Leu Gln Asn Lys Val Ala Asp Leu Glu Lys Glu Ile Ser Asn Leu Glu
275 280 285
Ile Leu Leu Gly Gly Ala Asp Ser Glu Asp Asp Thr Ala Ala Leu Gln
290 295 300
Asn Lys Leu Ala Thr Lys Lys Ala Glu Leu Glu Lys Thr Gln Lys Glu
305 310 315 320
Leu Asp Ala Ala Leu Asn Glu Leu Gly
325
<210> 42
<211> 411
<212> PRT
<213> Streptococcus pneumoniae
<400> 42
Glu Glu Ser Pro Gln Val Val Glu Lys Ser Ser Leu Glu Lys Lys Tyr
1 5 10 15
Glu Glu Ala Lys Ala Lys Ala Asp Thr Ala Lys Lys Asp Tyr Glu Thr
20 25 30
Ala Lys Lys Lys Ala Glu Asp Ala Gln Lys Lys Tyr Glu Asp Asp Gln
35 40 45
Lys Arg Thr Glu Glu Lys Ala Arg Lys Glu Ala Glu Ala Ser Gln Lys
50 55 60
Leu Asn Asp Val Ala Leu Val Val Gln Asn Ala Tyr Lys Glu Tyr Arg
65 70 75 80
Glu Val Gln Asn Gln Arg Ser Lys Tyr Lys Ser Asp Ala Glu Tyr Gln
85 90 95
Lys Lys Leu Thr Glu Val Asp Ser Lys Ile Glu Lys Ala Arg Lys Glu
100 105 110
Gln Gln Asp Leu Gln Asn Lys Phe Asn Glu Val Arg Ala Val Val Val
115 120 125
Pro Glu Pro Asn Ala Leu Ala Glu Thr Lys Lys Lys Ala Glu Glu Ala
130 135 140
Lys Ala Glu Glu Lys Val Ala Lys Arg Lys Tyr Asp Tyr Ala Thr Leu
145 150 155 160
Lys Val Ala Leu Ala Lys Lys Glu Val Glu Ala Lys Glu Leu Glu Ile
165 170 175
Glu Lys Leu Gln Tyr Glu Ile Ser Thr Leu Glu Gln Glu Val Ala Thr
180 185 190
Ala Gln His Gln Val Asp Asn Leu Lys Lys Leu Leu Ala Gly Ala Asp
195 200 205
Pro Asp Asp Gly Thr Glu Val Ile Glu Ala Lys Leu Lys Lys Gly Glu
210 215 220
Ala Glu Leu Asn Ala Lys Gln Ala Glu Leu Ala Lys Lys Gln Thr Glu
225 230 235 240
Leu Glu Lys Leu Leu Asp Ser Leu Asp Pro Glu Gly Lys Thr Gln Asp
245 250 255
Glu Leu Asp Lys Glu Ala Glu Glu Ala Glu Leu Asp Lys Lys Ala Asp
260 265 270
Glu Leu Gln Asn Lys Val Ala Asp Leu Glu Lys Glu Ile Ser Asn Leu
275 280 285
Glu Ile Leu Leu Gly Gly Ala Asp Pro Glu Asp Asp Thr Ala Ala Leu
290 295 300
Gln Asn Lys Leu Ala Ala Lys Lys Ala Glu Leu Ala Lys Lys Gln Thr
305 310 315 320
Glu Leu Glu Lys Leu Leu Asp Ser Leu Asp Pro Glu Gly Lys Thr Gln
325 330 335
Asp Glu Leu Asp Lys Glu Ala Glu Glu Ala Glu Leu Asp Lys Lys Ala
340 345 350
Asp Glu Leu Gln Asn Lys Val Ala Asp Leu Glu Lys Glu Ile Ser Asn
355 360 365
Leu Glu Ile Leu Leu Gly Gly Ala Asp Ser Glu Asp Asp Thr Ala Ala
370 375 380
Leu Gln Asn Lys Leu Ala Thr Lys Lys Ala Glu Leu Glu Lys Thr Gln
385 390 395 400
Lys Glu Leu Asp Ala Ala Leu Asn Glu Leu Gly
405 410
<210> 43
<211> 411
<212> PRT
<213> Streptococcus pneumoniae
<400> 43
Glu Glu Ser Pro Gln Val Val Glu Lys Ser Ser Leu Glu Lys Lys Tyr
1 5 10 15
Glu Glu Ala Lys Ala Lys Ala Asp Thr Ala Lys Lys Asp Tyr Glu Thr
20 25 30
Ala Lys Lys Lys Ala Glu Asp Ala Gln Lys Lys Tyr Glu Asp Asp Gln
35 40 45
Lys Arg Thr Glu Glu Lys Ala Arg Lys Glu Ala Glu Ala Ser Gln Lys
50 55 60
Leu Asn Asp Val Ala Leu Val Val Gln Asn Ala Tyr Lys Glu Tyr Arg
65 70 75 80
Glu Val Gln Asn Gln Arg Ser Lys Tyr Lys Ser Asp Ala Glu Tyr Gln
85 90 95
Lys Lys Leu Thr Glu Val Asp Ser Lys Ile Glu Lys Ala Arg Lys Glu
100 105 110
Gln Gln Asp Leu Gln Asn Lys Phe Asn Glu Val Arg Ala Val Val Val
115 120 125
Pro Glu Pro Asn Ala Leu Ala Glu Thr Lys Lys Lys Ala Glu Glu Ala
130 135 140
Lys Ala Glu Glu Lys Val Ala Lys Arg Lys Tyr Asp Tyr Ala Thr Leu
145 150 155 160
Lys Val Ala Leu Ala Lys Lys Glu Val Glu Ala Lys Glu Leu Glu Ile
165 170 175
Glu Lys Leu Gln Tyr Glu Ile Ser Thr Leu Glu Gln Glu Val Ala Thr
180 185 190
Ala Gln His Gln Val Asp Asn Leu Lys Lys Leu Leu Ala Gly Ala Asp
195 200 205
Pro Asp Asp Gly Thr Glu Val Ile Glu Ala Lys Leu Lys Lys Gly Glu
210 215 220
Ala Glu Leu Asn Ala Lys Gln Ala Glu Leu Ala Lys Lys Gln Thr Glu
225 230 235 240
Leu Glu Lys Leu Leu Asp Ser Leu Asp Pro Glu Gly Lys Thr Gln Asp
245 250 255
Glu Leu Asp Lys Glu Ala Glu Glu Ala Glu Leu Asp Lys Lys Ala Asp
260 265 270
Glu Leu Gln Asn Lys Val Ala Asp Leu Glu Lys Glu Ile Ser Asn Leu
275 280 285
Glu Ile Leu Leu Gly Gly Ala Asp Pro Glu Asp Asp Thr Ala Ala Leu
290 295 300
Gln Asn Lys Leu Ala Ala Lys Lys Ala Glu Leu Ala Lys Lys Gln Thr
305 310 315 320
Glu Leu Glu Lys Leu Leu Asp Ser Leu Asp Pro Glu Gly Lys Thr Gln
325 330 335
Asp Glu Leu Asp Lys Glu Ala Glu Glu Ala Glu Leu Asp Lys Lys Ala
340 345 350
Asp Glu Leu Gln Asn Lys Val Ala Asp Leu Glu Lys Glu Ile Ser Asn
355 360 365
Leu Glu Ile Leu Leu Gly Gly Ala Asp Ser Glu Asp Asp Thr Ala Ala
370 375 380
Leu Gln Asn Lys Leu Ala Thr Lys Lys Ala Glu Leu Glu Lys Thr Gln
385 390 395 400
Lys Glu Leu Asp Ala Ala Leu Asn Glu Leu Gly
405 410
<210> 44
<211> 400
<212> PRT
<213> Streptococcus pneumoniae
<400> 44
Glu Glu Ser Pro Val Ala Ser Gln Ser Lys Ala Glu Lys Asp Tyr Asp
1 5 10 15
Ala Ala Val Lys Lys Ser Glu Ala Ala Lys Lys His Tyr Glu Glu Ala
20 25 30
Lys Lys Lys Ala Glu Asp Ala Gln Lys Lys Tyr Asp Glu Asp Gln Lys
35 40 45
Lys Thr Glu Ala Lys Ala Glu Lys Glu Arg Lys Ala Ser Glu Lys Ile
50 55 60
Ala Glu Ala Thr Lys Glu Val Gln Gln Ala Tyr Leu Ala Tyr Leu Gln
65 70 75 80
Ala Ser Asn Glu Ser Gln Arg Lys Glu Ala Asp Lys Lys Ile Lys Glu
85 90 95
Ala Thr Gln Arg Lys Asp Glu Ala Glu Ala Ala Phe Ala Thr Ile Arg
100 105 110
Thr Thr Ile Val Val Pro Glu Pro Ser Glu Leu Ala Glu Thr Lys Lys
115 120 125
Lys Ala Glu Glu Ala Lys Ala Glu Glu Lys Val Ala Lys Arg Lys Tyr
130 135 140
Asp Tyr Ala Thr Leu Lys Leu Ala Leu Ala Lys Lys Glu Val Glu Ala
145 150 155 160
Lys Glu Leu Glu Ile Glu Lys Leu Gln Tyr Glu Ile Ser Thr Leu Glu
165 170 175
Gln Glu Val Ala Thr Ala Gln His Gln Val Asp Asn Leu Lys Lys Leu
180 185 190
Leu Ala Gly Ala Asp Pro Asp Asp Gly Thr Glu Val Ile Glu Ala Lys
195 200 205
Leu Lys Lys Gly Glu Ala Glu Leu Asn Ala Lys Gln Ala Glu Leu Ala
210 215 220
Lys Lys Gln Thr Glu Leu Glu Lys Leu Leu Asp Ser Leu Asp Pro Glu
225 230 235 240
Gly Lys Thr Gln Asp Glu Leu Asp Lys Glu Ala Glu Glu Ala Glu Leu
245 250 255
Asp Lys Lys Ala Asp Glu Leu Gln Asn Lys Val Ala Asp Leu Glu Lys
260 265 270
Glu Ile Ser Asn Leu Glu Ile Leu Leu Gly Gly Ala Asp Pro Glu Asp
275 280 285
Asp Thr Ala Ala Leu Gln Asn Lys Leu Ala Ala Lys Lys Ala Glu Leu
290 295 300
Ala Lys Lys Gln Thr Glu Leu Glu Lys Leu Leu Asp Ser Leu Asp Pro
305 310 315 320
Glu Gly Lys Thr Gln Asp Glu Leu Asp Lys Glu Ala Glu Glu Ala Glu
325 330 335
Leu Asp Lys Lys Ala Asp Glu Leu Gln Asn Lys Val Ala Asp Leu Glu
340 345 350
Lys Glu Ile Ser Asn Leu Glu Ile Leu Leu Gly Gly Ala Asp Ser Glu
355 360 365
Asp Asp Thr Ala Ala Leu Gln Asn Lys Leu Ala Thr Lys Lys Ala Glu
370 375 380
Leu Glu Lys Thr Gln Lys Glu Leu Asp Ala Ala Leu Asn Glu Leu Gly
385 390 395 400
<210> 45
<211> 400
<212> PRT
<213> Streptococcus pneumoniae
<400> 45
Glu Glu Ser Pro Val Ala Ser Gln Ser Lys Ala Glu Lys Asp Tyr Asp
1 5 10 15
Ala Ala Val Lys Lys Ser Glu Ala Ala Lys Lys His Tyr Glu Glu Ala
20 25 30
Lys Lys Lys Ala Glu Asp Ala Gln Lys Lys Tyr Asp Glu Asp Gln Lys
35 40 45
Lys Thr Glu Ala Lys Ala Glu Lys Glu Arg Lys Ala Ser Glu Lys Ile
50 55 60
Ala Glu Ala Thr Lys Glu Val Gln Gln Ala Tyr Leu Ala Tyr Leu Gln
65 70 75 80
Ala Ser Asn Glu Ser Gln Arg Lys Glu Ala Asp Lys Lys Ile Lys Glu
85 90 95
Ala Thr Gln Arg Lys Asp Glu Ala Glu Ala Ala Phe Ala Thr Ile Arg
100 105 110
Thr Thr Ile Val Val Pro Glu Pro Ser Glu Leu Ala Glu Thr Lys Lys
115 120 125
Lys Ala Glu Glu Ala Lys Ala Glu Glu Lys Val Ala Lys Arg Lys Tyr
130 135 140
Asp Tyr Ala Thr Leu Lys Leu Ala Leu Ala Lys Lys Glu Val Glu Ala
145 150 155 160
Lys Glu Leu Glu Ile Glu Lys Leu Gln Tyr Glu Ile Ser Thr Leu Glu
165 170 175
Gln Glu Val Ala Thr Ala Gln His Gln Val Asp Asn Leu Lys Lys Leu
180 185 190
Leu Ala Gly Ala Asp Pro Asp Asp Gly Thr Glu Val Ile Glu Ala Lys
195 200 205
Leu Lys Lys Gly Glu Ala Glu Leu Asn Ala Lys Gln Ala Glu Leu Ala
210 215 220
Lys Lys Gln Thr Glu Leu Glu Lys Leu Leu Asp Ser Leu Asp Pro Glu
225 230 235 240
Gly Lys Thr Gln Asp Glu Leu Asp Lys Glu Ala Glu Glu Ala Glu Leu
245 250 255
Asp Lys Lys Ala Asp Glu Leu Gln Asn Lys Val Ala Asp Leu Glu Lys
260 265 270
Glu Ile Ser Asn Leu Glu Ile Leu Leu Gly Gly Ala Asp Pro Glu Asp
275 280 285
Asp Thr Ala Ala Leu Gln Asn Lys Leu Ala Ala Lys Lys Ala Glu Leu
290 295 300
Ala Lys Lys Gln Thr Glu Leu Glu Lys Leu Leu Asp Ser Leu Asp Pro
305 310 315 320
Glu Gly Lys Thr Gln Asp Glu Leu Asp Lys Glu Ala Glu Glu Ala Glu
325 330 335
Leu Asp Lys Lys Ala Asp Glu Leu Gln Asn Lys Val Ala Asp Leu Glu
340 345 350
Lys Glu Ile Ser Asn Leu Glu Ile Leu Leu Gly Gly Ala Asp Ser Glu
355 360 365
Asp Asp Thr Ala Ala Leu Gln Asn Lys Leu Ala Thr Lys Lys Ala Glu
370 375 380
Leu Glu Lys Thr Gln Lys Glu Leu Asp Ala Ala Leu Asn Glu Leu Gly
385 390 395 400
<210> 46
<211> 400
<212> PRT
<213> Streptococcus pneumoniae
<400> 46
Glu Glu Ser Pro Val Ala Ser Gln Ser Lys Ala Glu Lys Asp Tyr Asp
1 5 10 15
Ala Ala Val Lys Lys Ser Glu Ala Ala Lys Lys His Tyr Glu Glu Ala
20 25 30
Lys Lys Lys Ala Glu Asp Ala Gln Lys Lys Tyr Asp Glu Asp Gln Lys
35 40 45
Lys Thr Glu Ala Lys Ala Glu Lys Glu Arg Lys Ala Ser Glu Lys Ile
50 55 60
Ala Glu Ala Thr Lys Glu Val Gln Gln Ala Tyr Leu Ala Tyr Leu Gln
65 70 75 80
Ala Ser Asn Glu Ser Gln Arg Lys Glu Ala Asp Lys Lys Ile Lys Glu
85 90 95
Ala Thr Gln Arg Lys Asp Glu Ala Glu Ala Ala Phe Ala Thr Ile Arg
100 105 110
Thr Thr Ile Val Val Pro Glu Pro Ser Glu Leu Ala Glu Thr Lys Lys
115 120 125
Lys Ala Glu Glu Ala Lys Ala Glu Glu Lys Val Ala Lys Arg Lys Tyr
130 135 140
Asp Tyr Ala Thr Leu Lys Leu Ala Leu Ala Lys Lys Glu Val Glu Ala
145 150 155 160
Lys Glu Leu Glu Ile Glu Lys Leu Gln Tyr Glu Ile Ser Thr Leu Glu
165 170 175
Gln Glu Val Ala Thr Ala Gln His Gln Val Asp Asn Leu Lys Lys Leu
180 185 190
Leu Ala Gly Ala Asp Pro Asp Asp Gly Thr Glu Val Ile Glu Ala Lys
195 200 205
Leu Lys Lys Gly Glu Ala Glu Leu Asn Ala Lys Gln Ala Glu Leu Ala
210 215 220
Lys Lys Gln Thr Glu Leu Glu Lys Leu Leu Asp Ser Leu Asp Pro Glu
225 230 235 240
Gly Lys Thr Gln Asp Glu Leu Asp Lys Glu Ala Glu Glu Ala Glu Leu
245 250 255
Asp Lys Lys Ala Asp Glu Leu Gln Asn Lys Val Ala Asp Leu Glu Lys
260 265 270
Glu Ile Ser Asn Leu Glu Ile Leu Leu Gly Gly Ala Asp Pro Glu Asp
275 280 285
Asp Thr Ala Ala Leu Gln Asn Lys Leu Ala Ala Lys Lys Ala Glu Leu
290 295 300
Ala Lys Lys Gln Thr Glu Leu Glu Lys Leu Leu Asp Ser Leu Asp Pro
305 310 315 320
Glu Gly Lys Thr Gln Asp Glu Leu Asp Lys Glu Ala Glu Glu Ala Glu
325 330 335
Leu Asp Lys Lys Ala Asp Glu Leu Gln Asn Lys Val Ala Asp Leu Glu
340 345 350
Lys Glu Ile Ser Asn Leu Glu Ile Leu Leu Gly Gly Ala Asp Ser Glu
355 360 365
Asp Asp Thr Ala Ala Leu Gln Asn Lys Leu Ala Thr Lys Lys Ala Glu
370 375 380
Leu Glu Lys Thr Gln Lys Glu Leu Asp Ala Ala Leu Asn Glu Leu Gly
385 390 395 400
<210> 47
<211> 400
<212> PRT
<213> Streptococcus pneumoniae
<400> 47
Glu Glu Ser Pro Val Ala Ser Gln Ser Lys Ala Glu Lys Asp Tyr Asp
1 5 10 15
Ala Ala Val Lys Lys Ser Glu Ala Ala Lys Lys His Tyr Glu Glu Ala
20 25 30
Lys Lys Lys Ala Glu Asp Ala Gln Lys Lys Tyr Asp Glu Asp Gln Lys
35 40 45
Lys Thr Glu Ala Lys Ala Glu Lys Glu Arg Lys Ala Ser Glu Lys Ile
50 55 60
Ala Glu Ala Thr Lys Glu Val Gln Gln Ala Tyr Leu Ala Tyr Leu Gln
65 70 75 80
Ala Ser Asn Glu Ser Gln Arg Lys Glu Ala Asp Lys Lys Ile Lys Glu
85 90 95
Ala Thr Gln Arg Lys Asp Glu Ala Glu Ala Ala Phe Ala Thr Ile Arg
100 105 110
Thr Thr Ile Val Val Pro Glu Pro Ser Glu Leu Ala Glu Thr Lys Lys
115 120 125
Lys Ala Glu Glu Ala Lys Ala Glu Glu Lys Val Ala Lys Arg Lys Tyr
130 135 140
Asp Tyr Ala Thr Leu Lys Leu Ala Leu Ala Lys Lys Glu Val Glu Ala
145 150 155 160
Lys Glu Leu Glu Ile Glu Lys Leu Gln Tyr Glu Ile Ser Thr Leu Glu
165 170 175
Gln Glu Val Ala Thr Ala Gln His Gln Val Asp Asn Leu Lys Lys Leu
180 185 190
Leu Ala Gly Ala Asp Pro Asp Asp Gly Thr Glu Val Ile Glu Ala Lys
195 200 205
Leu Lys Lys Gly Glu Ala Glu Leu Asn Ala Lys Gln Ala Glu Leu Ala
210 215 220
Lys Lys Gln Thr Glu Leu Glu Lys Leu Leu Asp Ser Leu Asp Pro Glu
225 230 235 240
Gly Lys Thr Gln Asp Glu Leu Asp Lys Glu Ala Glu Glu Ala Glu Leu
245 250 255
Asp Lys Lys Ala Asp Glu Leu Gln Asn Lys Val Ala Asp Leu Glu Lys
260 265 270
Glu Ile Ser Asn Leu Glu Ile Leu Leu Gly Gly Ala Asp Pro Glu Asp
275 280 285
Asp Thr Ala Ala Leu Gln Asn Lys Leu Ala Ala Lys Lys Ala Glu Leu
290 295 300
Ala Lys Lys Gln Thr Glu Leu Glu Lys Leu Leu Asp Ser Leu Asp Pro
305 310 315 320
Glu Gly Lys Thr Gln Asp Glu Leu Asp Lys Glu Ala Glu Glu Ala Glu
325 330 335
Leu Asp Lys Lys Ala Asp Glu Leu Gln Asn Lys Val Ala Asp Leu Glu
340 345 350
Lys Glu Ile Ser Asn Leu Glu Ile Leu Leu Gly Gly Ala Asp Ser Glu
355 360 365
Asp Asp Thr Ala Ala Leu Gln Asn Lys Leu Ala Thr Lys Lys Ala Glu
370 375 380
Leu Glu Lys Thr Gln Lys Glu Leu Asp Ala Ala Leu Asn Glu Leu Gly
385 390 395 400
<210> 48
<211> 400
<212> PRT
<213> Streptococcus pneumoniae
<400> 48
Glu Glu Ala Pro Val Ala Ser Gln Ser Lys Ala Glu Lys Asp Tyr Asp
1 5 10 15
Ala Ala Val Lys Lys Ser Glu Ala Ala Lys Lys His Tyr Glu Glu Val
20 25 30
Lys Lys Lys Ala Glu Asp Ala Gln Lys Lys Tyr Asp Glu Gly Gln Lys
35 40 45
Lys Thr Val Glu Lys Ala Lys Arg Glu Lys Glu Ala Ser Glu Lys Ile
50 55 60
Ala Glu Ala Thr Lys Glu Val Gln Gln Ala Tyr Leu Ala Tyr Gln Gln
65 70 75 80
Ala Ser Asn Glu Ser Gln Arg Lys Glu Ala Asp Lys Lys Ile Lys Glu
85 90 95
Ala Thr Gln Arg Lys Asp Glu Ala Glu Ala Ala Phe Ala Thr Ile Arg
100 105 110
Thr Thr Ile Val Val Pro Glu Pro Ser Glu Leu Ala Glu Thr Lys Lys
115 120 125
Lys Ala Glu Glu Ala Lys Ala Glu Glu Lys Val Ala Lys Arg Lys Tyr
130 135 140
Asp Tyr Ala Thr Leu Lys Val Ala Leu Ala Lys Lys Glu Val Glu Ala
145 150 155 160
Lys Glu Leu Glu Ile Glu Lys Leu Gln Tyr Glu Ile Ser Thr Leu Glu
165 170 175
Gln Glu Val Ala Thr Ala Gln His Gln Val Asp Asn Leu Lys Lys Leu
180 185 190
Leu Ala Gly Ala Asp Pro Asp Asp Gly Thr Glu Val Ile Glu Ala Lys
195 200 205
Leu Asn Lys Gly Glu Ala Glu Leu Asn Ala Lys Gln Ala Glu Leu Ala
210 215 220
Lys Lys Gln Thr Glu Leu Glu Lys Leu Leu Asp Ser Leu Asp Pro Glu
225 230 235 240
Gly Lys Thr Gln Asp Glu Leu Asp Lys Glu Ala Glu Glu Ala Glu Leu
245 250 255
Asp Lys Lys Ala Asp Glu Leu Gln Asn Lys Val Ala Asp Leu Glu Lys
260 265 270
Glu Ile Ser Asn Leu Glu Ile Leu Leu Gly Gly Ala Asp Pro Glu Asp
275 280 285
Asp Thr Ala Ala Leu Gln Asn Lys Leu Ala Ala Lys Gln Ala Glu Leu
290 295 300
Ala Lys Lys Gln Thr Glu Leu Glu Lys Leu Leu Asp Ser Leu Asp Pro
305 310 315 320
Glu Gly Lys Thr Gln Asp Glu Leu Asp Lys Glu Ala Glu Glu Ala Glu
325 330 335
Leu Asp Lys Lys Ala Asp Glu Leu Gln Asn Lys Val Ala Asp Leu Glu
340 345 350
Lys Glu Ile Ser Asn Leu Glu Ile Leu Leu Gly Gly Ala Asp Ser Glu
355 360 365
Asp Asp Thr Ala Ala Leu Gln Asn Lys Leu Ala Thr Lys Lys Ala Glu
370 375 380
Leu Glu Lys Thr Gln Lys Glu Leu Asp Ala Ala Leu Asn Glu Leu Gly
385 390 395 400
<210> 49
<211> 400
<212> PRT
<213> Streptococcus pneumoniae
<400> 49
Glu Glu Ala Pro Val Ala Ser Gln Ser Lys Ala Glu Lys Asp Tyr Asp
1 5 10 15
Ala Ala Val Lys Lys Ser Glu Ala Ala Lys Lys His Tyr Glu Glu Val
20 25 30
Lys Lys Lys Ala Glu Asp Ala Gln Lys Lys Tyr Asp Glu Gly Gln Lys
35 40 45
Lys Thr Val Glu Lys Ala Lys Arg Glu Lys Glu Ala Ser Glu Lys Ile
50 55 60
Ala Glu Ala Thr Lys Glu Val Gln Gln Ala Tyr Leu Ala Tyr Gln Gln
65 70 75 80
Ala Ser Asn Glu Ser Gln Arg Lys Glu Ala Asp Lys Lys Ile Lys Glu
85 90 95
Ala Thr Gln Arg Lys Asp Glu Ala Glu Ala Ala Phe Ala Thr Ile Arg
100 105 110
Thr Thr Ile Val Val Pro Glu Pro Ser Glu Leu Ala Glu Thr Lys Lys
115 120 125
Lys Ala Glu Glu Ala Lys Ala Glu Glu Lys Val Ala Lys Arg Lys Tyr
130 135 140
Asp Tyr Ala Thr Leu Lys Val Ala Leu Ala Lys Lys Glu Val Glu Ala
145 150 155 160
Lys Glu Leu Glu Ile Glu Lys Leu Gln Tyr Glu Ile Ser Thr Leu Glu
165 170 175
Gln Glu Val Ala Thr Ala Gln His Gln Val Asp Asn Leu Lys Lys Leu
180 185 190
Leu Ala Gly Ala Asp Pro Asp Asp Gly Thr Glu Val Ile Glu Ala Lys
195 200 205
Leu Asn Lys Gly Glu Ala Glu Leu Asn Ala Lys Gln Ala Glu Leu Ala
210 215 220
Lys Lys Gln Thr Glu Leu Glu Lys Leu Leu Asp Ser Leu Asp Pro Glu
225 230 235 240
Gly Lys Thr Gln Asp Glu Leu Asp Lys Glu Ala Glu Glu Ala Glu Leu
245 250 255
Asp Lys Lys Ala Asp Glu Leu Gln Asn Lys Val Ala Asp Leu Glu Lys
260 265 270
Glu Ile Ser Asn Leu Glu Ile Leu Leu Gly Gly Ala Asp Pro Glu Asp
275 280 285
Asp Thr Ala Ala Leu Gln Asn Lys Leu Ala Ala Lys Gln Ala Glu Leu
290 295 300
Ala Lys Lys Gln Thr Glu Leu Glu Lys Leu Leu Asp Ser Leu Asp Pro
305 310 315 320
Glu Gly Lys Thr Gln Asp Glu Leu Asp Lys Glu Ala Glu Glu Ala Glu
325 330 335
Leu Asp Lys Lys Ala Asp Glu Leu Gln Asn Lys Val Ala Asp Leu Glu
340 345 350
Lys Glu Ile Ser Asn Leu Glu Ile Leu Leu Gly Gly Ala Asp Ser Glu
355 360 365
Asp Asp Thr Ala Ala Leu Gln Asn Lys Leu Ala Thr Lys Lys Ala Glu
370 375 380
Leu Glu Lys Thr Gln Lys Glu Leu Asp Ala Ala Leu Asn Glu Leu Gly
385 390 395 400
<210> 50
<211> 400
<212> PRT
<213> Streptococcus pneumoniae
<400> 50
Glu Glu Ala Pro Val Ala Ser Gln Ser Lys Ala Glu Lys Asp Tyr Asp
1 5 10 15
Ala Ala Val Lys Lys Ser Glu Ala Ala Lys Lys His Tyr Glu Glu Val
20 25 30
Lys Lys Lys Ala Glu Asp Ala Gln Lys Lys Tyr Asp Glu Gly Gln Lys
35 40 45
Lys Thr Val Glu Lys Ala Lys Arg Glu Lys Glu Ala Ser Glu Lys Ile
50 55 60
Ala Glu Ala Thr Lys Glu Val Gln Gln Ala Tyr Leu Ala Tyr Gln Gln
65 70 75 80
Ala Ser Asn Glu Ser Gln Arg Lys Glu Ala Asp Lys Lys Ile Lys Glu
85 90 95
Ala Thr Gln Arg Lys Asp Glu Ala Glu Ala Ala Phe Ala Thr Ile Arg
100 105 110
Thr Thr Ile Val Val Pro Glu Pro Ser Glu Leu Ala Glu Thr Lys Lys
115 120 125
Lys Ala Glu Glu Ala Lys Ala Glu Glu Lys Val Ala Lys Arg Lys Tyr
130 135 140
Asp Tyr Ala Thr Leu Lys Val Ala Leu Ala Lys Lys Glu Val Glu Ala
145 150 155 160
Lys Glu Leu Glu Ile Glu Lys Leu Gln Tyr Glu Ile Ser Thr Leu Glu
165 170 175
Gln Glu Val Ala Thr Ala Gln His Gln Val Asp Asn Leu Lys Lys Leu
180 185 190
Leu Ala Gly Ala Asp Pro Asp Asp Gly Thr Glu Val Ile Glu Ala Lys
195 200 205
Leu Asn Lys Gly Glu Ala Glu Leu Asn Ala Lys Gln Ala Glu Leu Ala
210 215 220
Lys Lys Gln Thr Glu Leu Glu Lys Leu Leu Asp Ser Leu Asp Pro Glu
225 230 235 240
Gly Lys Thr Gln Asp Glu Leu Asp Lys Glu Ala Glu Glu Ala Glu Leu
245 250 255
Asp Lys Lys Ala Asp Glu Leu Gln Asn Lys Val Ala Asp Leu Glu Lys
260 265 270
Glu Ile Ser Asn Leu Glu Ile Leu Leu Gly Gly Ala Asp Pro Glu Asp
275 280 285
Asp Thr Ala Ala Leu Gln Asn Lys Leu Ala Ala Lys Gln Ala Glu Leu
290 295 300
Ala Lys Lys Gln Thr Glu Leu Glu Lys Leu Leu Asp Ser Leu Asp Pro
305 310 315 320
Glu Gly Lys Thr Gln Asp Glu Leu Asp Lys Glu Ala Glu Glu Ala Glu
325 330 335
Leu Asp Lys Lys Ala Asp Glu Leu Gln Asn Lys Val Ala Asp Leu Glu
340 345 350
Lys Glu Ile Ser Asn Leu Glu Ile Leu Leu Gly Gly Ala Asp Ser Glu
355 360 365
Asp Asp Thr Ala Ala Leu Gln Asn Lys Leu Ala Thr Lys Lys Ala Glu
370 375 380
Leu Glu Lys Thr Gln Lys Glu Leu Asp Ala Ala Leu Asn Glu Leu Gly
385 390 395 400
<210> 51
<211> 410
<212> PRT
<213> Streptococcus pneumoniae
<400> 51
Glu Glu Ala Pro Val Ala Ser Gln Ser Lys Ala Glu Lys Asp Tyr Asp
1 5 10 15
Ala Ala Val Lys Lys Ser Glu Ala Ala Lys Lys Asp Tyr Glu Glu Ala
20 25 30
Lys Lys Lys Ala Lys Glu Ala Gln Lys Lys Tyr Asp Glu Glu Gln Lys
35 40 45
Lys Thr Glu Glu Lys Ala Lys Lys Glu Lys Glu Ala Ala Lys Lys Val
50 55 60
Asp Asp Ala Ser Leu Ala Val Gln Lys Ala His Val Glu Tyr Arg Lys
65 70 75 80
Val Leu Phe Ser Arg Asn Ser Tyr Lys Tyr Lys Ser Asp Tyr Asp Lys
85 90 95
Lys Leu Ala Glu Ala Gln Ala Lys Ile Asp Glu Ala Asn Lys Lys Leu
100 105 110
Thr Ala Ala Asn Asn Glu Phe Gln Thr Val Arg Ala Val Val Val Pro
115 120 125
Glu Pro Asn Ala Leu Ala Glu Thr Lys Lys Lys Ala Glu Glu Ala Lys
130 135 140
Ala Glu Glu Val Val Ala Lys Lys Lys Tyr Asp Glu Ala Ala Gln Glu
145 150 155 160
Val Glu Val Ala Lys Lys Glu Val Glu Ala Lys Glu Leu Glu Ile Glu
165 170 175
Lys Leu Gln Asp Glu Ile Ser Thr Leu Glu Gln Glu Val Ala Thr Ala
180 185 190
Gln His Gln Val Asp Asn Leu Lys Lys Leu Leu Ala Gly Ala Asp Pro
195 200 205
Asp Asp Gly Thr Glu Val Ile Glu Ala Lys Leu Lys Lys Gly Glu Ala
210 215 220
Glu Leu Asn Ala Lys Gln Ala Glu Leu Ala Lys Lys Gln Thr Glu Leu
225 230 235 240
Glu Lys Leu Leu Asp Ser Leu Asp Pro Glu Gly Lys Thr Gln Asp Glu
245 250 255
Leu Asp Lys Glu Ala Glu Glu Ala Glu Leu Asp Lys Lys Ala Asp Glu
260 265 270
Leu Gln Asn Lys Val Ala Asp Leu Glu Lys Glu Ile Ser Asn Leu Glu
275 280 285
Ile Leu Leu Gly Gly Ala Asp Pro Glu Asp Asp Thr Ala Ala Leu Gln
290 295 300
Asn Lys Leu Ala Ala Lys Gln Ala Glu Leu Ala Lys Lys Gln Thr Glu
305 310 315 320
Leu Glu Lys Leu Leu Asp Ser Leu Asp Pro Glu Gly Lys Thr Gln Asp
325 330 335
Glu Leu Asp Lys Glu Ala Glu Glu Ala Glu Leu Asp Lys Lys Ala Asp
340 345 350
Glu Leu Gln Asn Lys Val Ala Asp Leu Glu Lys Glu Ile Ser Asn Leu
355 360 365
Glu Ile Leu Leu Gly Gly Ala Asp Ser Glu Asp Asp Thr Ala Ala Leu
370 375 380
Gln Asn Lys Leu Ala Thr Lys Lys Ala Glu Leu Glu Lys Thr Gln Lys
385 390 395 400
Glu Leu Asp Ala Ala Leu Asn Glu Leu Gly
405 410
<210> 52
<211> 410
<212> PRT
<213> Streptococcus pneumoniae
<400> 52
Glu Glu Ala Pro Val Ala Ser Gln Ser Lys Ala Glu Lys Asp Tyr Asp
1 5 10 15
Ala Ala Val Lys Lys Ser Glu Ala Ala Lys Lys Asp Tyr Glu Glu Ala
20 25 30
Lys Lys Lys Ala Lys Glu Ala Gln Lys Lys Tyr Asp Glu Glu Gln Lys
35 40 45
Lys Thr Glu Glu Lys Ala Lys Lys Glu Lys Glu Ala Ala Lys Lys Val
50 55 60
Asp Asp Ala Ser Leu Ala Val Gln Lys Ala His Val Glu Tyr Arg Lys
65 70 75 80
Val Leu Phe Ser Arg Asn Ser Tyr Lys Tyr Lys Ser Asp Tyr Asp Lys
85 90 95
Lys Leu Ala Glu Ala Gln Ala Lys Ile Asp Glu Ala Asn Lys Lys Leu
100 105 110
Thr Ala Ala Asn Asn Glu Phe Gln Thr Val Arg Ala Val Val Val Pro
115 120 125
Glu Pro Asn Ala Leu Ala Glu Thr Lys Lys Lys Ala Glu Glu Ala Lys
130 135 140
Ala Glu Glu Val Val Ala Lys Lys Lys Tyr Asp Glu Ala Ala Gln Glu
145 150 155 160
Val Glu Val Ala Lys Lys Glu Val Glu Ala Lys Glu Leu Glu Ile Glu
165 170 175
Lys Leu Gln Asp Glu Ile Ser Thr Leu Glu Gln Glu Val Ala Thr Ala
180 185 190
Gln His Gln Val Asp Asn Leu Lys Lys Leu Leu Ala Gly Ala Asp Pro
195 200 205
Asp Asp Gly Thr Glu Val Ile Glu Ala Lys Leu Lys Lys Gly Glu Ala
210 215 220
Glu Leu Asn Ala Lys Gln Ala Glu Leu Ala Lys Lys Gln Thr Glu Leu
225 230 235 240
Glu Lys Leu Leu Asp Ser Leu Asp Pro Glu Gly Lys Thr Gln Asp Glu
245 250 255
Leu Asp Lys Glu Ala Glu Glu Ala Glu Leu Asp Lys Lys Ala Asp Glu
260 265 270
Leu Gln Asn Lys Val Ala Asp Leu Glu Lys Glu Ile Ser Asn Leu Glu
275 280 285
Ile Leu Leu Gly Gly Ala Asp Pro Glu Asp Asp Thr Ala Ala Leu Gln
290 295 300
Asn Lys Leu Ala Ala Lys Gln Ala Glu Leu Ala Lys Lys Gln Thr Glu
305 310 315 320
Leu Glu Lys Leu Leu Asp Ser Leu Asp Pro Glu Gly Lys Thr Gln Asp
325 330 335
Glu Leu Asp Lys Glu Ala Glu Glu Ala Glu Leu Asp Lys Lys Ala Asp
340 345 350
Glu Leu Gln Asn Lys Val Ala Asp Leu Glu Lys Glu Ile Ser Asn Leu
355 360 365
Glu Ile Leu Leu Gly Gly Ala Asp Ser Glu Asp Asp Thr Ala Ala Leu
370 375 380
Gln Asn Lys Leu Ala Thr Lys Lys Ala Glu Leu Glu Lys Thr Gln Lys
385 390 395 400
Glu Leu Asp Ala Ala Leu Asn Glu Leu Gly
405 410
<210> 53
<211> 410
<212> PRT
<213> Streptococcus pneumoniae
<400> 53
Glu Glu Ala Pro Val Ala Ser Gln Ser Lys Ala Glu Lys Asp Tyr Asp
1 5 10 15
Ala Ala Val Lys Lys Ser Glu Ala Ala Lys Lys Asp Tyr Glu Glu Ala
20 25 30
Lys Lys Lys Ala Lys Glu Ala Gln Lys Lys Tyr Asp Glu Glu Gln Lys
35 40 45
Lys Thr Glu Glu Lys Ala Lys Lys Glu Lys Glu Ala Ala Lys Lys Val
50 55 60
Asp Asp Ala Ser Leu Ala Val Gln Lys Ala His Val Glu Tyr Arg Lys
65 70 75 80
Val Leu Phe Ser Arg Asn Ser Tyr Lys Tyr Lys Ser Asp Tyr Asp Lys
85 90 95
Lys Leu Ala Glu Ala Gln Ala Lys Ile Asp Glu Ala Asn Lys Lys Leu
100 105 110
Thr Ala Ala Asn Asn Glu Phe Gln Thr Val Arg Ala Val Val Val Pro
115 120 125
Glu Pro Asn Ala Leu Ala Glu Thr Lys Lys Lys Ala Glu Glu Ala Lys
130 135 140
Ala Glu Glu Val Val Ala Lys Lys Lys Ser Asp Glu Ala Ala Gln Glu
145 150 155 160
Val Glu Val Ala Lys Lys Glu Val Glu Ala Lys Glu Leu Glu Ile Glu
165 170 175
Lys Leu Gln Asp Glu Ile Ser Thr Leu Glu Gln Glu Val Ala Thr Ala
180 185 190
Gln His Gln Val Asp Asn Leu Lys Lys Leu Leu Ala Gly Ala Asp Pro
195 200 205
Asp Asp Gly Thr Glu Val Ile Glu Ala Lys Leu Lys Lys Gly Glu Ala
210 215 220
Glu Leu Asn Ala Lys Gln Ala Glu Leu Ala Lys Lys Gln Thr Glu Leu
225 230 235 240
Glu Lys Leu Leu Asp Ser Leu Asp Pro Glu Gly Lys Thr Gln Asp Glu
245 250 255
Leu Asp Lys Glu Ala Glu Glu Ala Glu Leu Asp Lys Lys Ala Asp Glu
260 265 270
Leu Gln Asn Lys Val Ala Asp Leu Glu Lys Glu Ile Ser Asn Leu Glu
275 280 285
Ile Leu Leu Gly Gly Ala Asp Pro Glu Asp Asp Thr Ala Ala Leu Gln
290 295 300
Asn Lys Leu Ala Ala Lys Gln Ala Glu Leu Ala Lys Lys Gln Thr Glu
305 310 315 320
Leu Glu Lys Leu Leu Asp Ser Leu Asp Pro Glu Gly Lys Thr Gln Asp
325 330 335
Glu Leu Asp Lys Glu Ala Glu Glu Ala Glu Leu Asp Lys Lys Ala Asp
340 345 350
Glu Leu Gln Asn Lys Val Ala Asp Leu Glu Lys Glu Ile Ser Asn Leu
355 360 365
Glu Ile Leu Leu Gly Gly Ala Asp Ser Glu Asp Asp Thr Ala Ala Leu
370 375 380
Gln Asn Lys Leu Ala Thr Lys Lys Ala Glu Leu Glu Lys Thr Gln Lys
385 390 395 400
Glu Leu Asp Ala Ala Leu Asn Glu Leu Gly
405 410
<210> 54
<211> 410
<212> PRT
<213> Streptococcus pneumoniae
<400> 54
Glu Glu Ala Pro Val Ala Ser Gln Ser Lys Ala Glu Lys Asp Tyr Asp
1 5 10 15
Ala Ala Val Lys Lys Ser Glu Ala Ala Lys Lys Asp Tyr Glu Glu Ala
20 25 30
Lys Lys Lys Ala Lys Glu Ala Gln Lys Lys Tyr Asp Glu Glu Gln Lys
35 40 45
Lys Thr Glu Glu Lys Ala Lys Lys Glu Lys Glu Val Ala Lys Lys Val
50 55 60
Asp Asp Ala Ser Leu Ala Val Gln Lys Ala His Val Glu Tyr Arg Lys
65 70 75 80
Val Leu Phe Ser Arg Asn Ser Tyr Lys Tyr Lys Ser Asp Tyr Asp Lys
85 90 95
Lys Leu Ala Glu Ala Gln Ala Lys Ile Asp Glu Ala Asn Lys Lys Leu
100 105 110
Thr Ala Ala Asn Asn Glu Phe Gln Thr Val Arg Ala Val Val Val Pro
115 120 125
Glu Pro Asn Ala Leu Ala Glu Thr Lys Lys Lys Ala Glu Glu Ala Lys
130 135 140
Ala Glu Glu Val Val Ala Lys Lys Lys Ser Asp Glu Ala Ala Gln Glu
145 150 155 160
Val Glu Val Ala Lys Lys Glu Val Glu Ala Lys Glu Leu Glu Ile Glu
165 170 175
Lys Leu Gln Asp Glu Ile Ser Thr Leu Glu Gln Glu Val Ala Thr Ala
180 185 190
Gln His Gln Val Asp Asn Leu Lys Lys Leu Leu Ala Gly Ala Asp Pro
195 200 205
Asp Asp Gly Thr Glu Val Ile Glu Ala Lys Leu Lys Lys Gly Glu Ala
210 215 220
Glu Leu Asn Ala Lys Gln Ala Glu Leu Ala Lys Lys Gln Thr Glu Leu
225 230 235 240
Glu Lys Leu Leu Asp Ser Leu Asp Pro Glu Gly Lys Thr Gln Asp Glu
245 250 255
Leu Asp Lys Glu Ala Glu Glu Ala Glu Leu Asp Lys Lys Ala Asp Glu
260 265 270
Leu Gln Asn Lys Val Ala Asp Leu Glu Lys Glu Ile Ser Asn Leu Glu
275 280 285
Ile Leu Leu Gly Gly Ala Asp Pro Glu Asp Asp Thr Ala Ala Leu Gln
290 295 300
Asn Lys Leu Ala Ala Lys Gln Ala Glu Leu Ala Lys Lys Gln Thr Glu
305 310 315 320
Leu Glu Lys Leu Leu Asp Ser Leu Asp Pro Glu Gly Lys Thr Gln Asp
325 330 335
Glu Leu Asp Lys Glu Ala Glu Glu Ala Glu Leu Asp Lys Lys Ala Asp
340 345 350
Glu Leu Gln Asn Lys Val Ala Asp Leu Glu Lys Glu Ile Ser Asn Leu
355 360 365
Glu Ile Leu Leu Gly Gly Ala Asp Ser Glu Asp Asp Thr Ala Ala Leu
370 375 380
Gln Asn Lys Leu Ala Thr Lys Lys Ala Glu Leu Glu Lys Thr Gln Lys
385 390 395 400
Glu Leu Asp Ala Ala Leu Asn Glu Leu Gly
405 410
<210> 55
<211> 410
<212> PRT
<213> Streptococcus pneumoniae
<400> 55
Glu Glu Ala Pro Val Ala Ser Gln Ser Lys Ala Glu Lys Asp Tyr Asp
1 5 10 15
Ala Ala Val Lys Lys Ser Glu Ala Ala Lys Lys Asp Tyr Glu Glu Ala
20 25 30
Lys Lys Lys Ala Lys Glu Ala Gln Lys Lys Tyr Asp Glu Glu Gln Lys
35 40 45
Lys Thr Glu Glu Lys Ala Lys Lys Glu Lys Glu Ala Ala Lys Lys Val
50 55 60
Asp Asp Ala Ser Leu Ala Val Gln Lys Ala His Val Glu Tyr Arg Lys
65 70 75 80
Val Leu Phe Ser Arg Asn Ser Tyr Lys Tyr Lys Ser Asp Tyr Asp Lys
85 90 95
Lys Leu Ala Glu Ala Gln Ala Lys Ile Asp Glu Ala Asn Lys Lys Leu
100 105 110
Thr Ala Ala Asn Asn Glu Phe Gln Thr Val Arg Ala Val Val Val Pro
115 120 125
Glu Pro Asn Ala Leu Ala Glu Thr Lys Lys Lys Ala Glu Glu Ala Lys
130 135 140
Ala Glu Glu Val Val Ala Lys Lys Lys Ser Asp Glu Ala Ala Gln Glu
145 150 155 160
Val Glu Val Ala Lys Lys Glu Val Glu Ala Lys Glu Leu Glu Ile Glu
165 170 175
Lys Leu Gln Asp Glu Ile Ser Thr Leu Glu Gln Glu Val Ala Thr Ala
180 185 190
Gln His Gln Val Asp Asn Leu Lys Lys Leu Leu Ala Gly Ala Asp Pro
195 200 205
Asp Asp Gly Thr Glu Val Ile Glu Ala Lys Leu Lys Lys Gly Glu Ala
210 215 220
Glu Leu Asn Ala Lys Gln Ala Glu Leu Ala Lys Lys Gln Thr Glu Leu
225 230 235 240
Glu Lys Leu Leu Asp Ser Leu Asp Pro Glu Gly Lys Thr Gln Asp Glu
245 250 255
Leu Asp Lys Glu Ala Glu Glu Ala Glu Leu Asp Lys Lys Ala Asp Glu
260 265 270
Leu Gln Asn Lys Val Ala Asp Leu Glu Lys Glu Ile Ser Asn Leu Glu
275 280 285
Ile Leu Leu Gly Gly Ala Asp Pro Glu Asp Asp Thr Ala Ala Leu Gln
290 295 300
Asn Lys Leu Ala Ala Lys Gln Ala Glu Leu Ala Lys Lys Gln Thr Glu
305 310 315 320
Leu Glu Lys Leu Leu Asp Ser Leu Asp Pro Glu Gly Lys Thr Gln Asp
325 330 335
Glu Leu Asp Lys Glu Ala Glu Glu Ala Glu Leu Asp Lys Lys Ala Asp
340 345 350
Glu Leu Gln Asn Lys Val Ala Asp Leu Glu Lys Glu Ile Ser Asn Leu
355 360 365
Glu Ile Leu Leu Gly Gly Ala Asp Ser Glu Asp Asp Thr Ala Ala Leu
370 375 380
Gln Asn Lys Leu Ala Thr Lys Lys Ala Glu Leu Glu Lys Thr Gln Lys
385 390 395 400
Glu Leu Asp Ala Ala Leu Asn Glu Leu Gly
405 410
<210> 56
<211> 410
<212> PRT
<213> Streptococcus pneumoniae
<400> 56
Glu Glu Ala Pro Val Ala Ser Gln Ser Lys Ala Glu Lys Asp Tyr Asp
1 5 10 15
Ala Ala Val Lys Lys Ser Glu Ala Ala Lys Lys Asp Tyr Glu Glu Ala
20 25 30
Lys Lys Lys Ala Lys Glu Ala Gln Lys Lys Tyr Asp Glu Glu Gln Lys
35 40 45
Lys Thr Glu Glu Lys Ala Lys Lys Glu Lys Glu Ala Ala Lys Lys Val
50 55 60
Asp Asp Ala Ser Leu Ala Val Gln Lys Ala His Val Glu Tyr Arg Lys
65 70 75 80
Val Leu Phe Ser Arg Asn Ser Tyr Lys Tyr Lys Ser Asp Tyr Asp Lys
85 90 95
Lys Leu Ala Glu Ala Gln Ala Lys Ile Asp Glu Ala Asn Lys Lys Leu
100 105 110
Thr Ala Ala Asn Asn Glu Phe Gln Thr Val Arg Ala Val Val Val Pro
115 120 125
Glu Pro Asn Ala Leu Ala Glu Thr Lys Lys Lys Ala Glu Glu Ala Lys
130 135 140
Ala Glu Glu Val Val Ala Lys Lys Lys Ser Asp Glu Ala Ala Gln Glu
145 150 155 160
Val Glu Val Ala Lys Lys Glu Val Glu Ala Lys Glu Leu Glu Ile Glu
165 170 175
Lys Leu Gln Asp Glu Ile Ser Thr Leu Glu Gln Glu Val Ala Thr Ala
180 185 190
Gln His Gln Val Asp Asn Leu Lys Lys Leu Leu Ala Gly Ala Asp Pro
195 200 205
Asp Asp Gly Thr Glu Val Ile Glu Ala Lys Leu Lys Lys Gly Glu Ala
210 215 220
Glu Leu Asn Ala Lys Gln Ala Glu Leu Ala Lys Lys Gln Thr Glu Leu
225 230 235 240
Glu Lys Leu Leu Asp Ser Leu Asp Pro Glu Gly Lys Thr Gln Asp Glu
245 250 255
Leu Asp Lys Glu Ala Glu Glu Ala Glu Leu Asp Lys Lys Ala Asp Glu
260 265 270
Leu Gln Asn Lys Val Ala Asp Leu Glu Lys Glu Ile Ser Asn Leu Glu
275 280 285
Ile Leu Leu Gly Gly Ala Asp Pro Glu Asp Asp Thr Ala Ala Leu Gln
290 295 300
Asn Lys Leu Ala Ala Lys Gln Ala Glu Leu Ala Lys Lys Gln Thr Glu
305 310 315 320
Leu Glu Lys Leu Leu Asp Ser Leu Asp Pro Glu Gly Lys Thr Gln Asp
325 330 335
Glu Leu Asp Lys Glu Ala Glu Glu Ala Glu Leu Asp Lys Lys Ala Asp
340 345 350
Glu Leu Gln Asn Lys Val Ala Asp Leu Glu Lys Glu Ile Ser Asn Leu
355 360 365
Glu Ile Leu Leu Gly Gly Ala Asp Ser Glu Asp Asp Thr Ala Ala Leu
370 375 380
Gln Asn Lys Leu Ala Thr Lys Lys Ala Glu Leu Glu Lys Thr Gln Lys
385 390 395 400
Glu Leu Asp Ala Ala Leu Asn Glu Leu Gly
405 410
<210> 57
<211> 410
<212> PRT
<213> Streptococcus pneumoniae
<400> 57
Glu Glu Ala Pro Val Ala Ser Gln Ser Lys Ala Glu Lys Asp Tyr Asp
1 5 10 15
Ala Ala Val Lys Lys Ser Glu Ala Ala Lys Lys Asp Tyr Glu Glu Ala
20 25 30
Lys Lys Lys Ala Lys Glu Ala Gln Lys Lys Tyr Asp Glu Glu Gln Lys
35 40 45
Lys Thr Glu Glu Lys Ala Lys Lys Glu Lys Glu Ala Ala Lys Lys Val
50 55 60
Asp Asp Ala Ser Leu Ala Val Gln Lys Ala His Val Glu Tyr Arg Lys
65 70 75 80
Val Leu Phe Ser Arg Asn Ser Tyr Lys Tyr Lys Ser Asp Tyr Asp Lys
85 90 95
Lys Leu Ala Glu Ala Gln Ala Lys Ile Asp Glu Ala Asn Lys Lys Leu
100 105 110
Thr Ala Ala Asn Asn Glu Phe Gln Thr Val Arg Ala Val Val Val Pro
115 120 125
Glu Pro Asn Ala Leu Ala Glu Thr Lys Lys Lys Ala Glu Glu Ala Lys
130 135 140
Ala Glu Glu Val Val Ala Lys Lys Lys Tyr Asp Glu Ala Ala Gln Glu
145 150 155 160
Val Glu Val Ala Lys Lys Glu Val Glu Ala Lys Glu Leu Glu Ile Glu
165 170 175
Lys Leu Gln Asp Glu Ile Ser Thr Leu Glu Gln Glu Val Ala Thr Ala
180 185 190
Gln His Gln Val Asp Asn Leu Lys Lys Leu Leu Ala Gly Ala Asp Pro
195 200 205
Asp Asp Gly Thr Glu Val Ile Glu Ala Lys Leu Lys Lys Gly Glu Ala
210 215 220
Glu Leu Asn Ala Lys Gln Ala Glu Leu Ala Lys Lys Gln Thr Glu Leu
225 230 235 240
Glu Lys Leu Leu Asp Ser Leu Asp Pro Glu Gly Lys Thr Gln Asp Glu
245 250 255
Leu Asp Lys Glu Ala Glu Glu Ala Glu Leu Asp Lys Lys Ala Asp Glu
260 265 270
Leu Gln Asn Lys Val Ala Asp Leu Glu Lys Glu Ile Ser Asn Leu Glu
275 280 285
Ile Leu Leu Gly Gly Ala Asp Pro Glu Asp Asp Thr Ala Ala Leu Gln
290 295 300
Asn Lys Leu Ala Ala Lys Gln Ala Glu Leu Ala Lys Lys Gln Thr Glu
305 310 315 320
Leu Glu Lys Leu Leu Asp Ser Leu Asp Pro Glu Gly Lys Thr Gln Asp
325 330 335
Glu Leu Asp Lys Glu Ala Glu Glu Ala Glu Leu Asp Lys Lys Ala Asp
340 345 350
Glu Leu Gln Asn Lys Val Ala Asp Leu Glu Lys Glu Ile Ser Asn Leu
355 360 365
Glu Ile Leu Leu Gly Gly Ala Asp Ser Glu Asp Asp Thr Ala Ala Leu
370 375 380
Gln Asn Lys Leu Ala Thr Lys Lys Ala Glu Leu Glu Lys Thr Gln Lys
385 390 395 400
Glu Leu Asp Ala Ala Leu Asn Glu Leu Gly
405 410
<210> 58
<211> 410
<212> PRT
<213> Streptococcus pneumoniae
<400> 58
Glu Glu Ala Pro Val Ala Ser Gln Ser Lys Ala Glu Lys Asp Tyr Asp
1 5 10 15
Ala Ala Val Lys Lys Ser Glu Ala Ala Lys Lys Asp Tyr Glu Glu Ala
20 25 30
Lys Lys Lys Ala Lys Glu Ala Gln Lys Lys Tyr Asp Glu Glu Gln Lys
35 40 45
Lys Thr Glu Glu Lys Ala Lys Lys Glu Lys Glu Ala Ala Lys Lys Val
50 55 60
Asp Asp Ala Ser Leu Ala Val Gln Lys Ala His Val Glu Tyr Arg Lys
65 70 75 80
Val Leu Phe Ser Arg Asn Ser Tyr Lys Tyr Lys Ser Asp Tyr Asp Lys
85 90 95
Lys Leu Ala Glu Ala Gln Ala Lys Ile Asp Glu Ala Asn Lys Lys Leu
100 105 110
Thr Ala Ala Asn Asn Glu Phe Gln Thr Val Arg Ala Val Val Val Pro
115 120 125
Glu Pro Asn Ala Leu Ala Glu Thr Lys Lys Lys Ala Glu Glu Ala Lys
130 135 140
Ala Glu Glu Val Val Ala Lys Lys Lys Ser Asp Glu Ala Ala Gln Glu
145 150 155 160
Val Glu Val Ala Lys Lys Glu Val Glu Ala Lys Glu Leu Glu Ile Glu
165 170 175
Lys Leu Gln Asp Glu Ile Ser Thr Leu Glu Gln Glu Val Ala Thr Ala
180 185 190
Gln His Gln Val Asp Asn Leu Lys Lys Leu Leu Ala Gly Ala Asp Pro
195 200 205
Asp Asp Gly Thr Glu Val Ile Glu Ala Lys Leu Lys Lys Gly Glu Ala
210 215 220
Glu Leu Asn Ala Lys Gln Ala Glu Leu Ala Lys Lys Gln Thr Glu Leu
225 230 235 240
Glu Lys Leu Leu Asp Ser Leu Asp Pro Glu Gly Lys Thr Gln Asp Glu
245 250 255
Leu Asp Lys Glu Ala Glu Glu Ala Glu Leu Asp Lys Lys Ala Asp Glu
260 265 270
Leu Gln Asn Lys Val Ala Asp Leu Glu Lys Glu Ile Ser Asn Leu Glu
275 280 285
Ile Leu Leu Gly Gly Ala Asp Pro Glu Asp Asp Thr Ala Ala Leu Gln
290 295 300
Asn Lys Leu Ala Ala Lys Gln Ala Glu Leu Ala Lys Lys Gln Thr Glu
305 310 315 320
Leu Glu Lys Leu Leu Asp Ser Leu Asp Pro Glu Gly Lys Thr Gln Asp
325 330 335
Glu Leu Asp Lys Glu Ala Glu Glu Ala Glu Leu Asp Lys Lys Ala Asp
340 345 350
Glu Leu Gln Asn Lys Val Ala Asp Leu Glu Lys Glu Ile Ser Asn Leu
355 360 365
Glu Ile Leu Leu Gly Gly Ala Asp Ser Glu Asp Asp Thr Ala Ala Leu
370 375 380
Gln Asn Lys Leu Ala Thr Lys Lys Ala Glu Leu Glu Lys Thr Gln Lys
385 390 395 400
Glu Leu Asp Ala Ala Leu Asn Glu Leu Gly
405 410
<210> 59
<211> 94
<212> PRT
<213> Streptococcus pneumoniae
<400> 59
Leu Glu Lys Val Leu Ala Thr Leu Asp Pro Glu Gly Lys Thr Gln Asp
1 5 10 15
Glu Leu Asp Lys Glu Ala Ala Glu Ala Glu Leu Asn Glu Lys Val Glu
20 25 30
Ala Leu Gln Asn Gln Val Ala Glu Leu Glu Glu Glu Leu Ser Lys Leu
35 40 45
Glu Asp Asn Leu Lys Asp Ala Glu Thr Asn Asn Val Glu Asp Tyr Ile
50 55 60
Lys Glu Gly Leu Glu Glu Ala Ile Ala Thr Lys Lys Ala Glu Leu Glu
65 70 75 80
Lys Thr Gln Lys Glu Leu Asp Ala Ala Leu Asn Glu Leu Gly
85 90
<210> 60
<211> 345
<212> PRT
<213> Streptococcus pneumoniae
<400> 60
Glu Glu Ala Pro Val Ala Asn Gln Ser Lys Ala Glu Lys Asp Tyr Asp
1 5 10 15
Ala Ala Val Lys Lys Ser Glu Ala Ala Lys Lys Asp Tyr Glu Thr Ala
20 25 30
Lys Lys Lys Ala Glu Asp Ala Gln Lys Lys Tyr Asp Glu Asp Gln Lys
35 40 45
Lys Thr Glu Ala Lys Ala Glu Lys Glu Arg Lys Ala Ser Glu Lys Ile
50 55 60
Ala Glu Ala Thr Lys Glu Val Gln Gln Ala Tyr Leu Ala Tyr Leu Gln
65 70 75 80
Ala Ser Asn Glu Ser Gln Arg Lys Glu Ala Asp Lys Lys Ile Lys Glu
85 90 95
Ala Thr Gln Arg Lys Asp Glu Ala Glu Ala Ala Phe Ala Thr Ile Arg
100 105 110
Thr Thr Ile Val Val Pro Glu Pro Ser Glu Leu Ala Glu Thr Lys Lys
115 120 125
Lys Ala Glu Glu Ala Thr Lys Glu Ala Glu Val Ala Lys Lys Lys Ser
130 135 140
Glu Glu Ala Ala Lys Glu Val Glu Val Glu Lys Asn Lys Ile Leu Glu
145 150 155 160
Gln Asp Ala Glu Asn Glu Lys Lys Ile Asp Val Leu Gln Asn Lys Val
165 170 175
Ala Asp Leu Glu Lys Gly Ile Ala Pro Tyr Gln Asn Glu Val Ala Glu
180 185 190
Leu Asn Lys Glu Ile Ala Arg Leu Gln Ser Asp Leu Lys Asp Ala Glu
195 200 205
Glu Asn Asn Val Glu Asp Tyr Ile Lys Glu Gly Leu Glu Gln Ala Ile
210 215 220
Thr Asn Lys Lys Ala Glu Leu Ala Thr Thr Gln Gln Asn Ile Asp Lys
225 230 235 240
Thr Gln Lys Asp Leu Glu Asp Ala Glu Leu Glu Leu Glu Lys Val Leu
245 250 255
Ala Thr Leu Asp Pro Glu Gly Lys Thr Gln Asp Glu Leu Asp Lys Glu
260 265 270
Ala Ala Glu Ala Glu Leu Asn Glu Lys Val Glu Ala Leu Gln Asn Gln
275 280 285
Val Ala Glu Leu Glu Glu Glu Leu Ser Lys Leu Glu Asp Asn Leu Lys
290 295 300
Asp Ala Glu Thr Asn Asn Val Glu Asp Tyr Ile Lys Glu Gly Leu Glu
305 310 315 320
Glu Ala Ile Ala Thr Lys Lys Ala Glu Leu Glu Lys Thr Gln Lys Glu
325 330 335
Leu Asp Ala Ala Leu Asn Glu Leu Gly
340 345
<210> 61
<211> 101
<212> PRT
<213> Streptococcus pneumoniae
<400> 61
Leu Glu Lys Ala Glu Ala Glu Leu Glu Asn Leu Leu Ser Thr Leu Asp
1 5 10 15
Pro Glu Gly Lys Thr Gln Asp Glu Leu Asp Lys Glu Ala Ala Glu Ala
20 25 30
Glu Leu Asn Lys Lys Val Glu Ala Leu Gln Asn Gln Val Ala Glu Leu
35 40 45
Glu Glu Glu Leu Ser Lys Leu Glu Asp Asn Leu Lys Asp Ala Glu Thr
50 55 60
Asn Asn Val Glu Asp Tyr Ile Lys Glu Gly Leu Glu Glu Ala Ile Ala
65 70 75 80
Thr Lys Gln Ala Glu Leu Glu Lys Thr Gln Lys Glu Leu Asp Ala Ala
85 90 95
Leu Asn Glu Leu Gly
100
<210> 62
<211> 364
<212> PRT
<213> Streptococcus pneumoniae
<400> 62
Glu Glu Ala Pro Val Ala Ser Gln Ser Lys Ala Glu Lys Asp Tyr Asp
1 5 10 15
Ala Ala Val Lys Lys Ser Glu Ala Ala Lys Lys Ala Tyr Glu Glu Ala
20 25 30
Lys Lys Lys Ala Glu Asp Ala Gln Lys Lys Tyr Asp Glu Asp Gln Lys
35 40 45
Lys Thr Glu Glu Lys Ala Glu Asn Glu Lys Lys Ala Ala Ala Asp Leu
50 55 60
Asn Glu Ala Thr Glu Val His Gln Lys Ala Tyr Val Arg Tyr Phe Glu
65 70 75 80
Ile Gln Arg Ala Lys Asp Ser Lys Lys Tyr Lys Asn Asn Arg Asp Lys
85 90 95
Tyr Asn Lys Asp Leu Ala Glu Ala Asp Gln Lys Ile Lys Asp Thr Lys
100 105 110
Thr Val Leu Asp Glu Lys Gln Ser Lys Phe Tyr Ala Val Arg Ala Val
115 120 125
Val Val Pro Glu Ala Lys Glu Leu Ala Val Thr Lys Gln Lys Ala Glu
130 135 140
Glu Thr Lys Lys Gly Ala Glu Val Ala Lys Glu Lys Tyr Asp Lys Ala
145 150 155 160
Ala Gln Glu Val Glu Val Ala Lys Lys Glu Val Glu Ala Glu Glu Ala
165 170 175
Glu Leu Asp Lys Lys Val Ala Glu Leu Gln Asn Lys Val Ala Asp Leu
180 185 190
Glu Lys Glu Ile Ala Asp Ala Glu Lys Thr Val Ala Asp Leu Glu Lys
195 200 205
Glu Val Ala Lys Leu Glu Lys Asp Val Glu Gly Phe Lys Glu Ser Asp
210 215 220
Gly Glu Tyr Ala Lys Phe Tyr Leu Glu Ala Ala Glu Lys Asp Leu Ala
225 230 235 240
Thr Lys Lys Ala Lys Leu Ala Glu Ala Lys Ile Lys Ala Ala Thr Lys
245 250 255
Lys Ala Glu Leu Glu Pro Glu Leu Glu Lys Ala Glu Ala Glu Leu Glu
260 265 270
Asn Leu Leu Ser Thr Leu Asp Pro Glu Gly Lys Thr Gln Asp Glu Leu
275 280 285
Asp Lys Glu Ala Ala Glu Ala Glu Leu Asn Lys Lys Val Glu Ala Leu
290 295 300
Gln Asn Gln Val Ala Glu Leu Glu Glu Glu Leu Ser Lys Leu Glu Asp
305 310 315 320
Asn Leu Lys Asp Ala Glu Thr Asn Asn Val Glu Asp Tyr Ile Lys Glu
325 330 335
Gly Leu Glu Glu Ala Ile Ala Thr Lys Gln Ala Glu Leu Glu Lys Thr
340 345 350
Gln Lys Glu Leu Asp Ala Ala Leu Asn Glu Leu Gly
355 360
<210> 63
<211> 101
<212> PRT
<213> Streptococcus pneumoniae
<400> 63
Leu Glu Lys Ala Glu Ala Glu Leu Glu Asn Leu Leu Ser Thr Leu Asp
1 5 10 15
Pro Glu Gly Lys Thr Gln Asp Glu Leu Asp Lys Glu Ala Ala Glu Ala
20 25 30
Glu Leu Asn Lys Lys Val Glu Ala Leu Gln Asn Gln Val Ala Glu Leu
35 40 45
Glu Glu Glu Leu Ser Lys Leu Glu Asp Asn Leu Lys Asp Ala Glu Thr
50 55 60
Asn Asn Val Glu Asp Tyr Ile Lys Glu Gly Leu Glu Glu Ala Ile Ala
65 70 75 80
Thr Lys Lys Ala Glu Leu Glu Lys Thr Gln Lys Glu Leu Asp Ala Ala
85 90 95
Leu Asn Glu Leu Gly
100
<210> 64
<211> 357
<212> PRT
<213> Streptococcus pneumoniae
<400> 64
Glu Ala Ala Pro Gln Val Val Glu Lys Ser Ser Leu Glu Lys Lys Tyr
1 5 10 15
Glu Glu Ala Lys Ala Lys Ala Asp Thr Ala Lys Lys Asp Tyr Glu Thr
20 25 30
Ala Lys Lys Lys Ala Ala Glu Ala Gln Lys Lys Tyr Glu Asp Asp Gln
35 40 45
Lys Arg Thr Glu Glu Lys Gly Ala Leu Glu Glu Glu Thr Ser Arg Lys
50 55 60
Val Asn Asp Ala Thr Leu Glu Val Gln Asn Ala Tyr Val Glu Tyr Gly
65 70 75 80
Glu Ala Asn Lys Lys Lys Gly Lys Asp Arg Glu Lys Lys Leu Ala Asp
85 90 95
Ala Gln Lys Lys Ile Asp Glu Ala Gln Glu Lys Leu Thr Lys Ala Lys
100 105 110
Asn Glu Phe Gln Ser Val Arg Ala Met Val Val Pro Glu Pro Glu Gln
115 120 125
Leu Ala Glu Thr Lys Lys Lys Ala Glu Glu Ala Lys Ala Glu Glu Ala
130 135 140
Val Ala Lys Glu Lys Ser Asp Lys Ala Ala Lys Glu Val Glu Val Ala
145 150 155 160
Lys Lys Arg Val Glu Ala Glu Glu Ala Glu Leu Asp Lys Lys Val Ala
165 170 175
Glu Leu Gln Asn Lys Val Ala Asp Leu Glu Lys Glu Ile Ala Asp Ala
180 185 190
Glu Lys Thr Val Ala Asp Leu Glu Lys Glu Val Ala Lys Leu Glu Lys
195 200 205
Asp Val Glu Asp Phe Lys Asn Ser Asn Gly Glu Gln Ala Glu Gln Tyr
210 215 220
Leu Ala Ala Ala Glu Lys Asp Leu Val Ala Lys Lys Ala Glu Leu Ala
225 230 235 240
Glu Ala Lys Ile Lys Ala Ala Thr Lys Lys Ala Glu Leu Glu Pro Glu
245 250 255
Leu Glu Lys Ala Glu Ala Glu Leu Glu Asn Leu Leu Ser Thr Leu Asp
260 265 270
Pro Glu Gly Lys Thr Gln Asp Glu Leu Asp Lys Glu Ala Ala Glu Ala
275 280 285
Glu Leu Asn Lys Lys Val Glu Ala Leu Gln Asn Gln Val Ala Glu Leu
290 295 300
Glu Glu Glu Leu Ser Lys Leu Glu Asp Asn Leu Lys Asp Ala Glu Thr
305 310 315 320
Asn Asn Val Glu Asp Tyr Ile Lys Glu Gly Leu Glu Glu Ala Ile Ala
325 330 335
Thr Lys Lys Ala Glu Leu Glu Lys Thr Gln Lys Glu Leu Asp Ala Ala
340 345 350
Leu Asn Glu Leu Gly
355
<210> 65
<211> 98
<212> PRT
<213> Streptococcus pneumoniae
<400> 65
Leu Lys Glu Ile Asp Glu Ser Asp Ser Glu Asp Tyr Ile Lys Glu Gly
1 5 10 15
Leu Arg Ala Pro Leu Gln Ser Lys Leu Asp Ala Lys Lys Ala Lys Leu
20 25 30
Ser Lys Leu Glu Glu Leu Ser Asp Lys Ile Asp Glu Leu Asp Ala Glu
35 40 45
Ile Ala Lys Leu Glu Lys Asp Val Glu Asp Phe Lys Asn Ser Asp Gly
50 55 60
Glu Gln Ala Glu Gln Tyr Leu Val Ala Ala Lys Lys Asp Leu Asp Ala
65 70 75 80
Lys Lys Ala Glu Leu Glu Asn Thr Glu Ala Asp Leu Lys Lys Ala Val
85 90 95
Asp Glu
<210> 66
<211> 302
<212> PRT
<213> Streptococcus pneumoniae
<400> 66
Glu Glu Ala Pro Val Ala Lys Gln Ser Gln Ala Glu Arg Asp Tyr Asp
1 5 10 15
Ala Ala Met Lys Lys Ser Glu Ala Ala Lys Lys Glu Tyr Glu Glu Ala
20 25 30
Lys Lys Asp Leu Glu Glu Ala Lys Ala Ala Gln Lys Lys Tyr Glu Asp
35 40 45
Asp Gln Lys Lys Thr Glu Glu Lys Ala Lys Leu Val Gln Lys Ala Asp
50 55 60
Glu Glu Arg Gln Lys Ala Asn Val Ala Val Gln Lys Ala Tyr Leu Lys
65 70 75 80
Leu Arg Glu Ala Gln Glu Gln Leu Asn Lys Ser Pro Asn Asn Lys Lys
85 90 95
Asn Ala Ala Gln Gln Lys Leu Lys Asp Ala Leu Ala His Ile Asp Glu
100 105 110
Val Thr Leu Lys Gln Lys Glu Ala Glu Ala Asn Phe Asn Lys Glu Gln
115 120 125
Ala Lys Val Val Pro Glu Ala Asp Lys Leu Ala Glu Thr Lys Lys Lys
130 135 140
Ala Glu Gln Ala Glu Lys Lys Glu Pro Glu Leu Ala Lys Lys Val Ala
145 150 155 160
Glu Ala Lys Ala Lys Ala Glu Glu Ala Glu Lys Lys Ala Val Glu Ala
165 170 175
Lys Gln Lys Val Asp Ala Glu Lys Tyr Ala Leu Glu Ala Lys Ile Ala
180 185 190
Glu Leu Glu Tyr Glu Val Gln Gly Leu Glu Lys Glu Leu Lys Glu Ile
195 200 205
Asp Glu Ser Asp Ser Glu Asp Tyr Ile Lys Glu Gly Leu Arg Ala Pro
210 215 220
Leu Gln Ser Lys Leu Asp Ala Lys Lys Ala Lys Leu Ser Lys Leu Glu
225 230 235 240
Glu Leu Ser Asp Lys Ile Asp Glu Leu Asp Ala Glu Ile Ala Lys Leu
245 250 255
Glu Lys Asp Val Glu Asp Phe Lys Asn Ser Asp Gly Glu Gln Ala Glu
260 265 270
Gln Tyr Leu Val Ala Ala Lys Lys Asp Leu Asp Ala Lys Lys Ala Glu
275 280 285
Leu Glu Asn Thr Glu Ala Asp Leu Lys Lys Ala Val Asp Glu
290 295 300
<210> 67
<211> 302
<212> PRT
<213> Streptococcus pneumoniae
<400> 67
Glu Glu Ala Pro Val Ala Lys Gln Ser Gln Ala Glu Arg Asp Tyr Asp
1 5 10 15
Ala Ala Met Lys Lys Ser Glu Ala Ala Lys Lys Glu Tyr Glu Glu Ala
20 25 30
Lys Lys Asp Leu Glu Glu Ala Lys Ala Ala Gln Lys Lys Tyr Glu Asp
35 40 45
Asp Gln Lys Lys Thr Glu Glu Lys Ala Lys Leu Val Gln Lys Ala Asp
50 55 60
Glu Glu Arg Gln Lys Ala Asn Val Ala Val Gln Lys Ala Tyr Leu Lys
65 70 75 80
Leu Arg Glu Ala Gln Glu Gln Leu Asn Lys Ser Pro Asn Asn Lys Lys
85 90 95
Asn Ala Ala Gln Gln Lys Leu Lys Asp Ala Leu Ala His Ile Asp Glu
100 105 110
Val Thr Leu Lys Gln Lys Glu Ala Glu Ala Asn Phe Asn Lys Glu Gln
115 120 125
Ala Lys Val Val Pro Glu Ala Asp Lys Leu Ala Glu Thr Lys Lys Lys
130 135 140
Ala Glu Gln Ala Glu Lys Lys Glu Pro Glu Leu Ala Lys Lys Val Ala
145 150 155 160
Glu Ala Lys Ala Lys Ala Glu Glu Ala Glu Lys Lys Ala Val Glu Ala
165 170 175
Lys Gln Lys Val Asp Ala Glu Lys Tyr Ala Leu Glu Ala Lys Ile Ala
180 185 190
Glu Leu Glu Tyr Glu Val Gln Gly Leu Glu Lys Glu Leu Lys Glu Ile
195 200 205
Asp Glu Ser Asp Ser Glu Asp Tyr Ile Lys Glu Gly Leu Arg Ala Pro
210 215 220
Leu Gln Ser Lys Leu Asp Ala Lys Lys Ala Lys Leu Ser Lys Leu Glu
225 230 235 240
Glu Leu Ser Asp Lys Ile Asp Glu Leu Asp Ala Glu Ile Ala Lys Leu
245 250 255
Glu Lys Asp Val Glu Asp Phe Lys Asn Ser Asp Gly Glu Gln Ala Glu
260 265 270
Gln Tyr Leu Val Ala Ala Lys Lys Asp Leu Asp Ala Lys Lys Ala Glu
275 280 285
Leu Glu Asn Thr Glu Ala Asp Leu Lys Lys Ala Val Asp Glu
290 295 300
<210> 68
<211> 302
<212> PRT
<213> Streptococcus pneumoniae
<400> 68
Glu Glu Ala Pro Val Ala Lys Gln Ser Gln Ala Glu Arg Asp Tyr Asp
1 5 10 15
Ala Ala Met Lys Lys Ser Glu Ala Ala Lys Lys Glu Tyr Glu Glu Ala
20 25 30
Lys Lys Asp Leu Glu Glu Ala Lys Ala Ala Gln Lys Lys Tyr Glu Asp
35 40 45
Asp Gln Lys Lys Thr Glu Glu Lys Ala Lys Leu Val Gln Lys Ala Asp
50 55 60
Glu Glu Arg Gln Lys Ala Asn Val Ala Val Gln Lys Ala Tyr Leu Lys
65 70 75 80
Leu Arg Glu Ala Gln Glu Gln Leu Asn Lys Ser Pro Asn Asn Lys Lys
85 90 95
Asn Ala Ala Gln Gln Lys Leu Lys Asp Ala Leu Ala His Ile Asp Glu
100 105 110
Val Thr Leu Lys Gln Lys Glu Ala Glu Ala Asn Phe Asn Lys Glu Gln
115 120 125
Ala Lys Val Val Pro Glu Ala Asp Lys Leu Ala Glu Thr Lys Lys Lys
130 135 140
Ala Glu Gln Ala Glu Lys Lys Glu Pro Glu Leu Ala Lys Lys Val Ala
145 150 155 160
Glu Ala Lys Ala Lys Ala Glu Glu Ala Glu Lys Lys Ala Val Glu Ala
165 170 175
Lys Gln Lys Val Asp Ala Glu Lys Tyr Ala Leu Glu Ala Lys Ile Ala
180 185 190
Glu Leu Glu Tyr Glu Val Gln Gly Leu Glu Lys Glu Leu Lys Glu Ile
195 200 205
Asp Glu Ser Asp Ser Glu Asp Tyr Ile Lys Glu Gly Leu Arg Ala Pro
210 215 220
Leu Gln Ser Lys Leu Asp Ala Lys Lys Ala Lys Leu Ser Lys Leu Glu
225 230 235 240
Glu Leu Ser Asp Lys Ile Asp Glu Leu Asp Ala Glu Ile Ala Lys Leu
245 250 255
Glu Lys Asp Val Glu Asp Phe Lys Asn Ser Asp Gly Glu Gln Ala Glu
260 265 270
Gln Tyr Leu Val Ala Ala Lys Lys Asp Leu Asp Ala Lys Lys Ala Glu
275 280 285
Leu Glu Asn Thr Glu Ala Asp Leu Lys Lys Ala Val Asp Glu
290 295 300
<210> 69
<211> 302
<212> PRT
<213> Streptococcus pneumoniae
<400> 69
Glu Glu Ala Pro Val Ala Lys Gln Ser Gln Ala Glu Arg Asp Tyr Asp
1 5 10 15
Ala Ala Met Lys Lys Ser Glu Ala Ala Lys Lys Glu Tyr Glu Glu Ala
20 25 30
Lys Lys Asp Leu Glu Glu Ala Lys Ala Ala Gln Lys Lys Tyr Glu Asp
35 40 45
Asp Gln Lys Lys Thr Glu Glu Lys Ala Lys Leu Val Gln Lys Ala Asp
50 55 60
Glu Glu Arg Gln Lys Ala Asn Val Ala Val Gln Lys Ala Tyr Leu Lys
65 70 75 80
Leu Arg Glu Ala Gln Glu Gln Leu Asn Lys Ser Pro Asn Asn Lys Lys
85 90 95
Asn Ala Ala Gln Gln Lys Leu Lys Asp Ala Leu Ala His Ile Asp Glu
100 105 110
Val Thr Leu Lys Gln Lys Glu Ala Glu Ala Asn Phe Asn Lys Glu Gln
115 120 125
Ala Lys Val Val Pro Glu Ala Asp Lys Leu Ala Glu Thr Lys Lys Lys
130 135 140
Ala Glu Gln Ala Glu Lys Lys Glu Pro Glu Leu Ala Lys Lys Val Ala
145 150 155 160
Glu Ala Lys Ala Lys Ala Glu Glu Ala Glu Lys Lys Ala Val Glu Ala
165 170 175
Lys Gln Lys Val Asp Ala Glu Lys Tyr Ala Leu Glu Ala Lys Ile Ala
180 185 190
Glu Leu Glu Tyr Glu Val Gln Gly Leu Glu Lys Glu Leu Lys Glu Ile
195 200 205
Asp Glu Ser Asp Ser Glu Asp Tyr Ile Lys Glu Gly Leu Arg Ala Pro
210 215 220
Leu Gln Ser Lys Leu Asp Ala Lys Lys Ala Lys Leu Ser Lys Leu Glu
225 230 235 240
Glu Leu Ser Asp Lys Ile Asp Glu Leu Asp Ala Glu Ile Ala Lys Leu
245 250 255
Glu Lys Asp Val Glu Asp Phe Lys Asn Ser Asp Gly Glu Gln Ala Glu
260 265 270
Gln Tyr Leu Val Ala Ala Lys Lys Asp Leu Asp Ala Lys Lys Ala Glu
275 280 285
Leu Glu Asn Thr Glu Ala Asp Leu Lys Lys Ala Val Asp Glu
290 295 300
<210> 70
<211> 302
<212> PRT
<213> Streptococcus pneumoniae
<400> 70
Glu Glu Ala Pro Val Ala Lys Gln Ser Gln Ala Glu Arg Asp Tyr Asp
1 5 10 15
Ala Ala Met Lys Lys Ser Glu Ala Ala Lys Lys Glu Tyr Glu Glu Ala
20 25 30
Lys Lys Asp Leu Glu Glu Ala Lys Ala Ala Gln Lys Lys Tyr Glu Asp
35 40 45
Asp Gln Lys Lys Thr Glu Glu Lys Ala Lys Leu Val Gln Lys Ala Asp
50 55 60
Glu Glu Arg Gln Lys Ala Asn Val Ala Val Gln Lys Ala Tyr Leu Lys
65 70 75 80
Leu Arg Glu Ala Gln Glu Gln Leu Asn Lys Ser Pro Asn Asn Lys Lys
85 90 95
Asn Ala Ala Gln Gln Lys Leu Lys Asp Ala Leu Ala His Ile Asp Glu
100 105 110
Val Thr Leu Lys Gln Lys Glu Ala Glu Ala Asn Phe Asn Lys Glu Gln
115 120 125
Ala Lys Val Val Pro Glu Ala Asp Lys Leu Ala Glu Thr Lys Lys Lys
130 135 140
Ala Glu Gln Ala Glu Lys Lys Glu Pro Glu Leu Ala Lys Lys Val Ala
145 150 155 160
Glu Ala Lys Ala Lys Ala Glu Glu Ala Glu Lys Lys Ala Val Glu Ala
165 170 175
Lys Gln Lys Val Asp Ala Glu Lys Tyr Ala Leu Glu Ala Lys Ile Ala
180 185 190
Glu Leu Glu Tyr Glu Val Gln Gly Leu Glu Lys Glu Leu Lys Glu Ile
195 200 205
Asp Glu Ser Asp Ser Glu Asp Tyr Ile Lys Glu Gly Leu Arg Ala Pro
210 215 220
Leu Gln Ser Lys Leu Asp Ala Lys Lys Ala Lys Leu Ser Lys Leu Glu
225 230 235 240
Glu Leu Ser Asp Lys Ile Asp Glu Leu Asp Ala Glu Ile Ala Lys Leu
245 250 255
Glu Lys Asp Val Glu Asp Phe Lys Asn Ser Asp Gly Glu Gln Ala Glu
260 265 270
Gln Tyr Leu Val Ala Ala Lys Lys Asp Leu Asp Ala Lys Lys Ala Glu
275 280 285
Leu Glu Asn Thr Glu Ala Asp Leu Lys Lys Ala Val Asp Glu
290 295 300
<210> 71
<211> 302
<212> PRT
<213> Streptococcus pneumoniae
<400> 71
Glu Glu Ala Pro Val Ala Lys Gln Ser Gln Ala Glu Arg Asp Tyr Asp
1 5 10 15
Ala Ala Met Lys Lys Ser Glu Ala Ala Lys Lys Glu Tyr Glu Glu Ala
20 25 30
Lys Lys Asp Leu Glu Glu Ala Lys Ala Ala Gln Lys Lys Tyr Glu Asp
35 40 45
Asp Gln Lys Lys Thr Glu Glu Lys Ala Lys Leu Val Gln Lys Ala Asp
50 55 60
Glu Glu Arg Gln Lys Ala Asn Val Ala Val Gln Lys Ala Tyr Leu Lys
65 70 75 80
Leu Arg Glu Ala Gln Glu Gln Leu Asn Lys Ser Pro Asn Asn Lys Lys
85 90 95
Asn Ala Ala Gln Gln Lys Leu Lys Asp Ala Leu Ala His Ile Asp Glu
100 105 110
Val Thr Leu Lys Gln Lys Glu Ala Glu Ala Asn Phe Asn Lys Glu Gln
115 120 125
Ala Lys Val Val Pro Glu Ala Asp Lys Leu Ala Glu Thr Lys Lys Lys
130 135 140
Ala Glu Gln Ala Glu Lys Lys Glu Pro Glu Leu Ala Lys Lys Val Ala
145 150 155 160
Glu Ala Lys Ala Lys Ala Glu Glu Ala Glu Lys Lys Ala Val Glu Ala
165 170 175
Lys Gln Lys Val Asp Ala Glu Lys Tyr Ala Leu Glu Ala Lys Ile Ala
180 185 190
Glu Leu Glu Tyr Glu Val Gln Gly Leu Glu Lys Glu Leu Lys Glu Ile
195 200 205
Asp Glu Ser Asp Ser Glu Asp Tyr Ile Lys Glu Gly Leu Arg Ala Pro
210 215 220
Leu Gln Ser Lys Leu Asp Ala Lys Lys Ala Lys Leu Ser Lys Leu Glu
225 230 235 240
Glu Leu Ser Asp Lys Ile Asp Glu Leu Asp Ala Glu Ile Ala Lys Leu
245 250 255
Glu Lys Asp Val Glu Asp Phe Lys Asn Ser Asp Gly Glu Gln Ala Glu
260 265 270
Gln Tyr Leu Val Ala Ala Lys Lys Asp Leu Asp Ala Lys Lys Ala Glu
275 280 285
Leu Glu Asn Thr Glu Ala Asp Leu Lys Lys Ala Val Asp Glu
290 295 300
<210> 72
<211> 302
<212> PRT
<213> Streptococcus pneumoniae
<400> 72
Glu Glu Ala Pro Val Ala Lys Gln Ser Gln Ala Glu Arg Asp Tyr Asp
1 5 10 15
Ala Ala Met Lys Lys Ser Glu Ala Ala Lys Lys Glu Tyr Glu Glu Ala
20 25 30
Lys Lys Asp Leu Glu Glu Ala Lys Ala Ala Gln Lys Lys Tyr Glu Asp
35 40 45
Asp Gln Lys Lys Thr Glu Glu Lys Ala Lys Leu Val Gln Lys Ala Asp
50 55 60
Glu Glu Arg Gln Lys Ala Asn Val Ala Val Gln Lys Ala Tyr Leu Lys
65 70 75 80
Leu Arg Glu Ala Gln Glu Gln Leu Asn Lys Ser Pro Asn Asn Lys Lys
85 90 95
Asn Ala Ala Gln Gln Lys Leu Lys Asp Ala Leu Ala His Ile Asp Glu
100 105 110
Val Thr Leu Lys Gln Lys Glu Ala Glu Ala Asn Phe Asn Lys Glu Gln
115 120 125
Ala Lys Val Val Pro Glu Ala Asp Lys Leu Ala Glu Thr Lys Lys Lys
130 135 140
Ala Glu Gln Ala Glu Lys Lys Glu Pro Glu Leu Ala Lys Lys Val Ala
145 150 155 160
Glu Ala Lys Ala Lys Ala Glu Glu Ala Glu Lys Lys Ala Val Glu Ala
165 170 175
Lys Gln Lys Val Asp Ala Glu Lys Tyr Ala Leu Glu Ala Lys Ile Ala
180 185 190
Glu Leu Glu Tyr Glu Val Gln Gly Leu Glu Lys Glu Leu Lys Glu Ile
195 200 205
Asp Glu Ser Asp Ser Glu Asp Tyr Ile Lys Glu Gly Leu Arg Ala Pro
210 215 220
Leu Gln Ser Lys Leu Asp Ala Lys Lys Ala Lys Leu Ser Lys Leu Glu
225 230 235 240
Glu Leu Ser Asp Lys Ile Asp Glu Leu Asp Ala Glu Ile Ala Lys Leu
245 250 255
Glu Lys Asp Val Glu Asp Phe Lys Asn Ser Asp Gly Glu Gln Ala Glu
260 265 270
Gln Tyr Leu Val Ala Ala Lys Lys Asp Leu Asp Ala Lys Lys Ala Glu
275 280 285
Leu Glu Asn Thr Glu Ala Asp Leu Lys Lys Ala Val Asp Glu
290 295 300
<210> 73
<211> 302
<212> PRT
<213> Streptococcus pneumoniae
<400> 73
Glu Glu Ala Pro Val Ala Lys Gln Ser Gln Ala Glu Arg Asp Tyr Asp
1 5 10 15
Ala Ala Met Lys Lys Ser Glu Ala Ala Lys Lys Glu Tyr Glu Glu Ala
20 25 30
Lys Lys Asp Leu Glu Glu Ala Lys Ala Ala Gln Lys Lys Tyr Glu Asp
35 40 45
Asp Gln Lys Lys Thr Glu Glu Lys Ala Lys Leu Val Gln Lys Ala Asp
50 55 60
Glu Glu Arg Gln Lys Ala Asn Val Ala Val Gln Lys Ala Tyr Leu Lys
65 70 75 80
Leu Arg Glu Ala Gln Glu Gln Leu Asn Lys Ser Pro Asn Asn Lys Lys
85 90 95
Asn Ala Ala Gln Gln Lys Leu Lys Asp Ala Leu Ala His Ile Asp Glu
100 105 110
Val Thr Leu Lys Gln Lys Glu Ala Glu Ala Asn Phe Asn Lys Glu Gln
115 120 125
Ala Lys Val Val Pro Glu Ala Asp Lys Leu Ala Glu Thr Lys Lys Lys
130 135 140
Ala Glu Gln Ala Glu Lys Lys Glu Pro Glu Leu Ala Lys Lys Val Ala
145 150 155 160
Glu Ala Lys Ala Lys Ala Glu Glu Ala Glu Lys Lys Ala Val Glu Ala
165 170 175
Lys Gln Lys Val Asp Ala Glu Lys Tyr Ala Leu Glu Ala Lys Ile Ala
180 185 190
Glu Leu Glu Tyr Glu Val Gln Gly Leu Glu Lys Glu Leu Lys Glu Ile
195 200 205
Asp Glu Ser Asp Ser Glu Asp Tyr Ile Lys Glu Gly Leu Arg Ala Pro
210 215 220
Leu Gln Ser Lys Leu Asp Ala Lys Lys Ala Lys Leu Ser Lys Leu Glu
225 230 235 240
Glu Leu Ser Asp Lys Ile Asp Glu Leu Asp Ala Glu Ile Ala Lys Leu
245 250 255
Glu Lys Asp Val Glu Asp Phe Lys Asn Ser Asp Gly Glu Gln Ala Glu
260 265 270
Gln Tyr Leu Val Ala Ala Lys Lys Asp Leu Asp Ala Lys Lys Ala Glu
275 280 285
Leu Glu Asn Thr Glu Ala Asp Leu Lys Lys Ala Val Asp Glu
290 295 300
<210> 74
<211> 302
<212> PRT
<213> Streptococcus pneumoniae
<400> 74
Glu Glu Ala Pro Val Ala Lys Gln Ser Gln Ala Glu Arg Asp Tyr Asp
1 5 10 15
Ala Ala Met Lys Lys Ser Glu Ala Ala Lys Lys Glu Tyr Glu Glu Ala
20 25 30
Lys Lys Asp Leu Glu Glu Ala Lys Ala Ala Gln Lys Lys Tyr Glu Asp
35 40 45
Asp Gln Lys Lys Thr Glu Glu Lys Ala Lys Leu Val Gln Lys Ala Asp
50 55 60
Glu Glu Arg Gln Lys Ala Asn Val Ala Val Gln Lys Ala Tyr Leu Lys
65 70 75 80
Leu Arg Glu Ala Gln Glu Gln Leu Asn Lys Ser Pro Asn Asn Lys Lys
85 90 95
Asn Ala Ala Gln Gln Lys Leu Lys Asp Ala Leu Ala His Ile Asp Glu
100 105 110
Val Thr Leu Lys Gln Lys Glu Ala Glu Ala Asn Phe Asn Lys Glu Gln
115 120 125
Ala Lys Val Val Pro Glu Ala Asp Lys Leu Ala Glu Thr Lys Lys Lys
130 135 140
Ala Glu Gln Ala Glu Lys Lys Glu Pro Glu Leu Ala Lys Lys Val Ala
145 150 155 160
Glu Ala Lys Ala Lys Ala Glu Glu Ala Glu Lys Lys Ala Val Glu Ala
165 170 175
Lys Gln Lys Val Asp Ala Glu Lys Tyr Ala Leu Glu Ala Lys Ile Ala
180 185 190
Glu Leu Glu Tyr Glu Val Gln Gly Leu Glu Lys Glu Leu Lys Glu Ile
195 200 205
Asp Glu Ser Asp Ser Glu Asp Tyr Ile Lys Glu Gly Leu Arg Ala Pro
210 215 220
Leu Gln Ser Lys Leu Asp Ala Lys Lys Ala Lys Leu Ser Lys Leu Glu
225 230 235 240
Glu Leu Ser Asp Lys Ile Asp Glu Leu Asp Ala Glu Ile Ala Lys Leu
245 250 255
Glu Lys Asp Val Glu Asp Phe Lys Asn Ser Asp Gly Glu Gln Ala Glu
260 265 270
Gln Tyr Leu Val Ala Ala Lys Lys Asp Leu Asp Ala Lys Lys Ala Glu
275 280 285
Leu Glu Asn Thr Glu Ala Asp Leu Lys Lys Ala Val Asp Glu
290 295 300
<210> 75
<211> 302
<212> PRT
<213> Streptococcus pneumoniae
<400> 75
Glu Ala Ala Pro Val Ala Asn Gln Ser Gln Ala Glu Lys Asn Tyr Asp
1 5 10 15
Val Ala Lys Lys Asp Val Glu Asn Ala Lys Lys Ala Val Glu Asp Ala
20 25 30
Gln Lys Ala Leu Asp Asp Ala Lys Ala Ala Gln Lys Lys Tyr Glu Asp
35 40 45
Asp Gln Lys Lys Thr Glu Glu Lys Ala Lys Leu Val Gln Lys Ala Asp
50 55 60
Glu Glu Arg Gln Lys Ala Asn Val Ala Val Gln Lys Ala Tyr Leu Lys
65 70 75 80
Leu Arg Glu Ala Gln Glu Gln Leu Asn Lys Ser Pro Asn Asn Lys Lys
85 90 95
Asn Ala Ala Gln Gln Lys Leu Lys Asp Ala Leu Ala His Ile Asp Glu
100 105 110
Val Thr Leu Lys Gln Lys Glu Ala Glu Ala Asn Phe Asn Lys Glu Gln
115 120 125
Ala Lys Val Val Pro Glu Ala Asp Lys Leu Ala Glu Thr Lys Lys Lys
130 135 140
Ala Glu Gln Ala Glu Lys Lys Glu Pro Glu Leu Ala Lys Lys Val Ala
145 150 155 160
Glu Ala Lys Ala Lys Ala Glu Glu Ala Glu Lys Lys Ala Val Glu Ala
165 170 175
Lys Gln Lys Val Asp Ala Glu Lys Tyr Ala Leu Glu Ala Lys Ile Ala
180 185 190
Glu Leu Glu Tyr Glu Val Gln Gly Leu Glu Lys Glu Leu Lys Glu Ile
195 200 205
Asp Glu Ser Asp Ser Glu Asp Tyr Ile Lys Glu Gly Leu Arg Ala Pro
210 215 220
Leu Gln Ser Lys Leu Asp Ala Lys Lys Ala Lys Leu Ser Lys Leu Glu
225 230 235 240
Glu Leu Ser Asp Lys Ile Asp Glu Leu Asp Ala Glu Ile Ala Lys Leu
245 250 255
Glu Lys Asp Val Glu Asp Phe Lys Asn Ser Asp Gly Glu Gln Ala Glu
260 265 270
Gln Tyr Leu Val Ala Ala Lys Lys Asp Leu Asp Ala Lys Lys Ala Glu
275 280 285
Leu Glu Asn Thr Glu Ala Asp Leu Lys Lys Ala Val Asp Glu
290 295 300
<210> 76
<211> 98
<212> PRT
<213> Streptococcus pneumoniae
<400> 76
Leu Lys Glu Ile Asp Glu Ser Asp Ser Glu Asp Tyr Val Lys Glu Gly
1 5 10 15
Leu Arg Ala Pro Leu Gln Ser Glu Leu Asp Ala Lys Gln Ala Lys Leu
20 25 30
Ser Lys Leu Glu Glu Leu Ser Asp Lys Ile Asp Glu Leu Asp Ala Glu
35 40 45
Ile Ala Lys Leu Glu Lys Asn Val Glu Asp Phe Lys Asn Ser Asn Gly
50 55 60
Glu Gln Ala Glu Gln Tyr Arg Ala Ala Ala Glu Glu Asp Leu Ala Ala
65 70 75 80
Lys Gln Ala Glu Leu Glu Lys Thr Glu Ala Asp Leu Lys Lys Ala Val
85 90 95
Asn Glu
<210> 77
<211> 98
<212> PRT
<213> Streptococcus pneumoniae
<400> 77
Leu Lys Gly Ile Asp Glu Ser Asp Ser Glu Asp Tyr Val Lys Glu Gly
1 5 10 15
Leu Arg Ala Pro Leu Gln Ser Glu Leu Asp Ala Lys Arg Thr Lys Leu
20 25 30
Ser Thr Leu Glu Glu Leu Ser Asp Lys Ile Asp Glu Leu Asp Ala Glu
35 40 45
Ile Ala Lys Leu Glu Lys Asn Val Glu Tyr Phe Lys Lys Thr Asp Ala
50 55 60
Glu Gln Thr Glu Gln Tyr Leu Ala Ala Ala Glu Lys Asp Leu Ala Asp
65 70 75 80
Lys Lys Ala Glu Leu Glu Lys Thr Glu Ala Asp Leu Lys Lys Ala Val
85 90 95
Asn Glu
<210> 78
<211> 294
<212> PRT
<213> Streptococcus pneumoniae
<400> 78
Glu Glu Ala Pro Val Ala Ser Gln Ser Lys Ala Glu Lys Asp Tyr Asp
1 5 10 15
Ala Ala Met Glu Lys Tyr Lys Ala Ala Lys Lys Glu Tyr Glu Asp Ala
20 25 30
Lys Lys Val Leu Ala Asp Ala Lys Ala Ala Gln Lys Lys Tyr Asp Glu
35 40 45
Asp Gln Lys Lys Thr Glu Lys Lys Ala Ala Ala Val Lys Lys Ile Asp
50 55 60
Glu Glu His Gln Ala Ala Asn Leu Lys Ser Gln Gln Ala Leu Val Glu
65 70 75 80
Phe Leu Ala Ala Gln Arg Glu Gly Asn Pro Lys Lys Lys Lys Ala Ala
85 90 95
Gln Ala Lys Leu Glu Ala Glu Lys Ala Glu Lys Glu Lys Lys Lys Glu
100 105 110
Phe Asp Lys Ala Gln Ala Val Val Val Pro Glu Ala Thr Glu Leu Ala
115 120 125
Glu Thr Lys Lys Lys Ala Asp Glu Ala Lys Val Lys Glu Pro Glu Leu
130 135 140
Thr Lys Lys Leu Glu Glu Ala Lys Ala Lys Ser Glu Glu Ala Glu Lys
145 150 155 160
Lys Ala Thr Glu Ala Lys Gln Lys Val Asp Ala Glu His Ala Lys Glu
165 170 175
Val Val Pro Gln Ala Lys Ile Ala Glu Leu Glu Asn Glu Val Gln Lys
180 185 190
Leu Glu Lys Asp Leu Lys Glu Ile Asp Glu Ser Asp Ser Glu Asp Tyr
195 200 205
Val Lys Glu Gly Leu Arg Ala Pro Leu Gln Ser Glu Leu Asp Ala Lys
210 215 220
Gln Ala Lys Leu Ser Lys Leu Glu Glu Leu Ser Asp Lys Ile Asp Glu
225 230 235 240
Leu Asp Ala Glu Ile Ala Lys Leu Glu Lys Asn Val Glu Asp Phe Lys
245 250 255
Asn Ser Asn Gly Glu Gln Ala Glu Gln Tyr Arg Ala Ala Ala Glu Glu
260 265 270
Asp Leu Ala Ala Lys Gln Ala Glu Leu Glu Lys Thr Glu Ala Asp Leu
275 280 285
Lys Lys Ala Val Asn Glu
290
<210> 79
<211> 310
<212> PRT
<213> Streptococcus pneumoniae
<400> 79
Met Asn Lys Lys Lys Met Ile Leu Thr Ser Leu Ala Ser Val Ala Ile
1 5 10 15
Leu Gly Ala Gly Phe Val Ala Ser Gln Pro Thr Val Val Arg Ala Glu
20 25 30
Glu Ala Pro Val Ala Ser Gln Ser Lys Ala Glu Lys Asp Tyr Asp Ala
35 40 45
Ala Lys Arg Asp Ala Glu Asn Ala Lys Lys Ala Leu Glu Glu Ala Lys
50 55 60
Arg Ala Gln Lys Lys Tyr Glu Asp Asp Gln Lys Lys Thr Glu Glu Lys
65 70 75 80
Ala Lys Glu Glu Lys Gln Ala Ser Glu Ala Glu Gln Lys Ala Asn Leu
85 90 95
Lys Tyr Gln Leu Leu Leu Gln Lys Tyr Val Ser Glu Ser Asp Gly Lys
100 105 110
Lys Lys Lys Glu Ile Glu Lys Gln Ala Asp Ala Ala Lys Lys Glu Asn
115 120 125
Glu Ile Lys Lys Ala Glu Leu Asn Lys Ile Arg Gln Glu Ile Val Val
130 135 140
Pro Ser Ser Gln Gln Leu Glu Val Thr Arg Arg Lys Ala Glu Val Ala
145 150 155 160
Lys Ala Lys Glu Pro Gly Leu Arg Lys Arg Val Glu Glu Ala Glu Lys
165 170 175
Lys Val Thr Glu Ala Lys Gln Lys Leu Asp Ala Glu Arg Ala Lys Glu
180 185 190
Val Ala Leu Gln Ala Lys Ile Ala Glu Leu Glu Asn Glu Val Tyr Arg
195 200 205
Leu Glu Thr Glu Leu Lys Gly Ile Asp Glu Ser Asp Ser Glu Asp Tyr
210 215 220
Val Lys Glu Gly Leu Arg Ala Pro Leu Gln Ser Glu Leu Asp Ala Lys
225 230 235 240
Arg Thr Lys Leu Ser Thr Leu Glu Glu Leu Ser Asp Lys Ile Asp Glu
245 250 255
Leu Asp Ala Glu Ile Ala Lys Leu Glu Lys Asn Val Glu Tyr Phe Lys
260 265 270
Lys Thr Asp Ala Glu Gln Thr Glu Gln Tyr Leu Ala Ala Ala Glu Lys
275 280 285
Asp Leu Ala Asp Lys Lys Ala Glu Leu Glu Lys Thr Glu Ala Asp Leu
290 295 300
Lys Lys Ala Val Asn Glu
305 310
<210> 80
<211> 112
<212> PRT
<213> Streptococcus pneumoniae
<400> 80
Leu Glu Asp Ala Glu Leu Glu Leu Glu Lys Val Leu Ala Thr Leu Asp
1 5 10 15
Pro Glu Gly Lys Thr Gln Asp Glu Leu Asp Lys Glu Ala Ala Glu Asp
20 25 30
Ala Asn Ile Glu Ala Leu Gln Asn Lys Val Ala Asp Leu Glu Asn Lys
35 40 45
Val Ala Glu Leu Asp Lys Glu Val Thr Arg Leu Gln Ser Asp Leu Lys
50 55 60
Asp Ala Glu Glu Asn Asn Val Glu Asp Tyr Val Lys Glu Gly Leu Asp
65 70 75 80
Lys Ala Leu Thr Asp Lys Lys Val Glu Leu Asn Asn Thr Gln Lys Ala
85 90 95
Leu Asp Thr Ala Gln Lys Ala Leu Asp Thr Ala Leu Asn Glu Leu Gly
100 105 110
<210> 81
<211> 368
<212> PRT
<213> Streptococcus pneumoniae
<400> 81
Glu Glu Ala Pro Val Ala Asn Gln Ser Lys Ala Glu Lys Asp Tyr Asp
1 5 10 15
Ala Ala Val Lys Lys Ser Glu Ala Ala Lys Lys Asp Tyr Glu Thr Ala
20 25 30
Lys Lys Lys Ala Glu Asp Ala Gln Lys Lys Tyr Asp Glu Asp Gln Lys
35 40 45
Lys Thr Glu Glu Lys Ala Glu Leu Val Arg Lys Ala Asp Glu Lys Arg
50 55 60
Gln Lys Ala Asn Leu Ala Val Gln Glu Ala Tyr Val Lys Phe Gln Glu
65 70 75 80
Ala Gln Arg Glu Phe Asn Glu Ser Pro Ser Arg Lys Lys Ser Asp Ala
85 90 95
Lys Lys Lys Leu Asp Asp Ala Ser Ala His Ile Glu Glu Val Lys Leu
100 105 110
Lys Gln Lys Glu Ala Asp Ala Asn Phe Asn Lys Glu Gln Ala Lys Val
115 120 125
Ile Pro Glu Ala Ser Asp Leu Ala Val Thr Lys Gln Lys Ala Glu Glu
130 135 140
Ala Lys Lys Glu Ala Glu Val Ala Lys Glu Lys Tyr Asp Lys Ala Val
145 150 155 160
Gln Glu Val Glu Val Glu Lys Asn Lys Ile Leu Glu Gln Asp Ala Glu
165 170 175
Asn Glu Lys Lys Ile Asp Val Leu Gln Asn Lys Val Ala Asp Leu Glu
180 185 190
Lys Gly Ile Ala Pro Tyr Gln Asn Lys Val Ala Glu Leu Asn Lys Glu
195 200 205
Ile Ala Arg Leu Gln Ser Asp Leu Lys Asp Ala Glu Glu Asn Asn Val
210 215 220
Glu Asp Tyr Ile Lys Glu Gly Leu Glu Gln Ala Ile Ala Asp Lys Lys
225 230 235 240
Ala Glu Leu Ala Thr Thr Gln Gln Asn Ile Asp Lys Thr Gln Lys Asp
245 250 255
Leu Glu Asp Ala Glu Leu Glu Leu Glu Lys Val Leu Ala Thr Leu Asp
260 265 270
Pro Glu Gly Lys Thr Gln Asp Glu Leu Asp Lys Glu Ala Ala Glu Asp
275 280 285
Ala Asn Ile Glu Ala Leu Gln Asn Lys Val Ala Asp Leu Glu Asn Lys
290 295 300
Val Ala Glu Leu Asp Lys Glu Val Thr Arg Leu Gln Ser Asp Leu Lys
305 310 315 320
Asp Ala Glu Glu Asn Asn Val Glu Asp Tyr Val Lys Glu Gly Leu Asp
325 330 335
Lys Ala Leu Thr Asp Lys Lys Val Glu Leu Asn Asn Thr Gln Lys Ala
340 345 350
Leu Asp Thr Ala Gln Lys Ala Leu Asp Thr Ala Leu Asn Glu Leu Gly
355 360 365
<210> 82
<211> 1074
<212> ДНК
<213> Искусственная последовательность
<220>
<223> ДНК, кодирующая PspA01.1 [SEQ ID NO:1]. ATG, кодирующий
метионин добавляли в начале в качестве инициатора,а
TGA добавляли в конце в качестве стоп-кодона
<400> 82
atggaagaaa gcccggtggc gagccagagc aaagcggaaa aagattatga tgcggcgaaa
60
aaagatgcga aaaacgcgaa aaaagcggtg gaagatgcgc agaaagcgct ggatgatgcg
120 aaagcggcgc agaaaaaata cgatgaagac cagaaaaaaa ccgaagaaaa agcggcgctg
180 gaaaaagcgg cgagcgaaga aatggataaa gcggtggcgg cggtgcagca
ggcgtatctg 240 gcgtatcagc aggcgaccga taaagcggcg aaagatgcgg
cggataaaat gattgatgaa 300 gcgaaaaaac gcgaagaaga agcgaaaacc
aaatttaaca ccgtgcgcgc gatggtggtt 360 ccggaaccgg aacagctggc
ggaaaccaaa aagaaaagcg aagaagcgaa acagaaagcg 420 ccggaactga
ccaaaaaact ggaagaagcg aaagcgaaac tggaagaagc cgagaaaaaa 480
gcgaccgaag ccaaacaaaa ggttgatgcg gaagaagtgg cgccgcaggc gaaaattgcg
540 gaactggaaa accaggtgca tcgcctggaa caggaactga aagaaattga tgaaagcgaa
600 agcgaagatt atgcgaaaga aggctttcgc gcgccgctgc agagcaaact
ggatgcgaaa 660 aaagccaagc tgagcaaact ggaagaactg agcgataaaa
ttgatgaact ggatgcggaa 720 attgcgaaac tggaagatca gctgaaagcg
gcggaagaaa acaacaacgt ggaagattat 780
tttaaagaag gcctggaaaa aaccattgcg gcgaaaaaag cggaacttga aaaaaccgaa
840 gcggatctga aaaaagcggt taatgaaccg gaaaccccgg caccggcgcc ggcaccggcg
900 ccggccccgg ccccggcccc agcgcccgcg ccggccccga agccagcccc
ggctcccaaa 960 ccggcaccgg ccccgaaacc ggcccctgcg cccgcccccg
cgcccgcgcc gaaaccggaa 1020 aaaccggcag aaaaaccggc tccggcacct
aaaccagaga ccccgaaaac ctga 1074
<210> 83
<211> 1158
<212> ДНК
<213> Искусственная последовательность
<220>
<223> ДНК, кодирующая PspA01.2 [SEQ ID NO:2]. ATG, кодирующий
метионин добавляли в начале в качестве инициатора,а
TGA добавляли в конце в качестве стоп-кодона
<400> 83
atggaagaaa gcccggtggc gagccagagc aaagcggaaa aagattatga tgcggcgaaa 60
aaagatgcga aaaacgcgaa aaaagcggtg gaagatgcgc agaaagcgct ggatgatgcg 120
aaagcggcgc agaaaaaata cgatgaagac cagaaaaaaa ccgaagaaaa agcggcgctg 180
gaaaaagcgg cgagcgaaga aatggataaa gcggtggcgg cggtgcagca ggcgtatctg 240
gcgtatcagc aggcgaccga taaagcggcg aaagatgcgg cggataaaat gattgatgaa 300
gcgaaaaaac gcgaagaaga agcgaaaacc aaatttaaca ccgtgcgcgc gatggtggtt 360
ccggaaccgg aacagctggc ggaaaccaaa aagaaaagcg aagaagcgaa acagaaagcg 420
ccggaactga ccaaaaaact ggaagaagcg aaagcgaaac tggaagaagc cgagaaaaaa 480
gcgaccgaag ccaaacaaaa ggttgatgcg gaagaagtgg cgccgcaggc gaaaattgcg 540
gaactggaaa accaggtgca tcgcctggaa caggaactga aagaaattga tgaaagcgaa 600
agcgaagatt atgcgaaaga aggctttcgc gcgccgctgc agagcaaact ggatgcgaaa 660
aaagccaagc tgagcaaact ggaagaactg agcgataaaa ttgatgaact ggatgcggaa 720
attgcgaaac tggaagatca gctgaaagcg gcggaagaaa acaacaacgt ggaagattat 780
tttaaagaag gcctggaaaa aaccattgcg gcgaaaaaag cggaacttga aaaaaccgaa 840
gcggatctga aaaaagcggt taatgaaccg gaaaccccgg caccggcgcc ggcaccggcg 900
ccggccccgg ccccggcccc agcgcccaaa ccggcaccgg ccccgaaacc ggcccctgca 960
ccaaaaccgg cgccggctcc taaacccgcg ccggccccga agccagcccc ggctcccgcc 1020
cccgcgcccg cgccgaaacc ggcgccggcc cctaagccgg caccggctcc agccccggcg 1080
ccggcccctg cgccgaagcc cgaaaaaccg gcagaaaaac cggctccggc acctaaacca 1140
gagaccccga aaacctga 1158
<210> 84
<211> 1491
<212> ДНК
<213> Искусственная последовательность
<220>
<223> ДНК, кодирующая PspA02 [SEQ ID NO:3]. ATG, кодирующий метионин
добавляли в начале в качестве инициатора,а TGA добавляли в конце в
качестве стоп-кодона
<400> 84
atggaagaaa gcccgcaggt ggtggaaaaa agcagcctgg aaaaaaaata tgaagaagcg 60
aaagcgaaag cggataccgc gaaaaaagat tatgaaaccg cgaaaaagaa agcggaagat 120
gcgcagaaaa aatacgaaga cgatcagaaa cgcaccgaag aaaaagcgcg caaagaagcg 180
gaagcgagcc agaaactgaa cgatgtggcg ctggtggtgc agaacgcgta taaagaatat 240
cgcgaagtgc agaaccagcg cagcaaatat aaaagcgatg cggaatatca gaaaaaactg 300
accgaagtgg atagcaaaat tgaaaaagcg cgtaaggagc agcaggatct gcagaacaaa 360
tttaacgaag tgcgtgcggt ggtggttccg gaaccgaatg cgctggcgga aaccaaaaaa 420
aaagccgaag aggccaaagc agaggaaaaa gtggcgaaac gcaaatatga ttatgcgacc 480
ctgaaagtgg cgctggcgaa aaaagaagtg gaagcgaaag aactggaaat tgaaaaactg 540
cagtatgaaa ttagcaccct ggaacaggaa gtggcgaccg cgcagcatca ggtggataac 600
ctgaaaaaac tgctggcggg cgcggatccg gatgatggca ccgaagtgat tgaagcgaaa 660
ctgaaaaaag gcgaagcgga actgaacgcg aaacaggcgg aactggcgaa aaaacagacc 720
gaactggaaa aactgctgga tagcctggat ccggaaggca aaacccagga tgaactggat 780
aaagaagccg aagaagccga gctggacaaa aaagcagatg aactgcagaa caaagtggcg 840
gatctggaaa aagaaattag caatttggag attctgctgg gcggtgcaga cccggaagac 900
gataccgcag cgctgcaaaa taaactggcc gcgaaaaaag cggaactggc gaaaaaacaa 960
accgaactgg agaagctgct tgattcgctg gatccggagg gtaaaacgca agatgaactg 1020
gataaagaag cggaagaagc ggagctggat aaaaaagcgg acgaactgca gaataaggtg 1080
gccgacctgg agaaagaaat cagcaatctc gagatcctgc tgggtggcgc cgacagcgaa 1140
gatgatacgg ccgcgctgca gaataaactc gccaccaaaa aagccgagct cgagaagacc 1200
cagaaagaac tggatgcggc gctgaacgaa ctgggcccgg atggtgatga agaagaaacc 1260
ccggcaccgg caccgcaacc ggaacaaccg gcgccggccc ccaagccgga acagccggca 1320
ccggccccaa agccggagca gccggccccg gcccccaaac cggaacaacc ggcgcctgca 1380
ccgaagccag aacagccggc gccagcgcct aaaccggaac agccagcgaa accggagaag 1440
ccagcggaag aaccgaccca gccggagaaa ccggcaaccc cgaaaacctg a 1491
<210> 85
<211> 1296
<212> ДНК
<213> Искусственная последовательность
<220>
<223> ДНК, кодирующая PspA03 [SEQ ID NO:4]. ATG, кодирующий
метионин добавляли в начале в качестве инициатора,а
TGA добавляли в конце в качестве стоп-кодона
<400> 85
atggaagaag cgccggtggc gaaccagagc aaagcggaaa aagattatga tgcggcggtg 60
aaaaaaagcg aagcggcgaa aaaagattac gagaccgcga aaaagaaagc ggaagatgcg 120
cagaaaaaat atgatgaaga tcagaaaaaa accgaagcga aagcggaaaa agaacgcaaa 180
gcgagcgaaa aaattgcgga agcgaccaaa gaagtgcagc aggcgtatct ggcgtatctg 240
caggcgagca acgaaagcca gcgcaaagaa gcggataaaa aaattaaaga agcgacccag 300
cgcaaagatg aagcggaagc ggcgtttgcg accattcgca ccaccattgt ggtgccggaa 360
ccgagcgaac tggcggaaac caaaaaaaaa gccgaagaag caacgaaaga ggccgaagtg 420
gcgaaaaaga aaagcgaaga agcggcgaaa gaagtggaag tggaaaaaaa caaaattctg 480
gaacaggatg cggaaaacga aaagaaaatt gatgtgctgc agaacaaagt ggcggatctg 540
gaaaaaggca ttgcgccgta tcagaatgaa gtcgccgagc tcaacaaaga aattgcgcgt 600
ttgcaaagcg atctgaaaga tgcggaagaa aacaacgtgg aagattacat taaagaaggc 660
ctggaacagg cgattaccaa caaaaaagcg gaactggcga ccacccagca gaacattgat 720
aaaacccaga aagatctgga agacgcggag ctggaactgg aaaaagtgct ggcgaccctg 780
gatccggaag gcaaaaccca ggatgaactg gataaagaag cggcggaagc ggaactgaac 840
gaaaaagtgg aagcgctgca gaaccaggtg gcggaactgg aagaagaact gagcaaactg 900
gaagataacc tgaaagacgc cgagaccaac aatgttgaag attacattaa agagggtctg 960
gaggaagcga ttgcgaccaa aaaagccgag ctcgaaaaaa cgcaaaaaga gttagatgcg 1020
gcgctgaacg aactgggccc ggaaaaaccg gcagaagaaa ccccggcacc ggcgccgaaa 1080
ccggaacagc cggccgagca gccgaaaccg gcaccggcac cgcaaccggc cccggcgcca 1140
aagccagaga agaccgatga tcagcaggcg gaagaagatt atgcgcgccg cagcgaagaa 1200
gaatataacc gcctgccgca gcagcagccg ccgaaagcag aaaaaccggc gccggccccg 1260
aaaccagaac aaccagttcc ggcaccgaaa acctga 1296
<210> 86
<211> 5
<212> PRT
<213> Streptococcus pneumoniae
<400> 86
Leu Lys Glu Ile Gly
1 5
<210> 87
<211> 98
<212> PRT
<213> Streptococcus pneumoniae
<400> 87
Pro Glu Thr Pro Ala Pro Ala Pro Lys Pro Ala Pro Thr Pro Glu Ala
1 5 10 15
Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala
20 25 30
Pro Ala Pro Thr Pro Glu Ala Pro Ala Pro Ala Pro Lys Pro Ala Pro
35 40 45
Ala Pro Lys Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro Ala Pro
50 55 60
Thr Pro Glu Ala Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro Lys
65 70 75 80
Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro Lys Pro Glu Thr Pro
85 90 95
Lys Thr
<210> 88
<211> 108
<212> PRT
<213> Streptococcus pneumoniae
<400> 88
Pro Glu Thr Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro Ala Pro
1 5 10 15
Thr Pro Glu Ala Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro Lys
20 25 30
Pro Ala Pro Ala Pro Ala Pro Thr Pro Glu Ala Pro Ala Pro Ala Pro
35 40 45
Lys Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro Lys Pro Ala Pro
50 55 60
Ala Pro Ala Pro Thr Pro Glu Ala Pro Ala Pro Ala Pro Lys Pro Ala
65 70 75 80
Pro Ala Pro Lys Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro Lys
85 90 95
Pro Ala Pro Ala Pro Lys Pro Glu Thr Pro Lys Thr
100 105
<210> 89
<211> 84
<212> PRT
<213> Streptococcus pneumoniae
<400> 89
Pro Glu Thr Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro Ala Pro
1 5 10 15
Thr Pro Glu Ala Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro Lys
20 25 30
Pro Ala Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro Lys Pro Ala
35 40 45
Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala
50 55 60
Pro Lys Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro Lys Pro Glu
65 70 75 80
Thr Pro Lys Thr
<210> 90
<211> 74
<212> PRT
<213> Streptococcus pneumoniae
<400> 90
Pro Glu Thr Pro Ala Pro Ala Pro Ala Pro Ala Pro Ala Pro Ala Pro
1 5 10 15
Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro
20 25 30
Ala Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro Lys Pro Ala Pro
35 40 45
Ala Pro Ala Pro Ala Pro Lys Pro Glu Lys Pro Ala Glu Lys Pro Ala
50 55 60
Pro Ala Pro Lys Pro Glu Thr Pro Lys Thr
65 70
<210> 91
<211> 82
<212> PRT
<213> Streptococcus pneumoniae
<400> 91
Pro Glu Thr Pro Ala Pro Ala Pro Ala Pro Ala Pro Ala Pro Ala Pro
1 5 10 15
Ala Pro Ala Pro Ala Pro Ala Pro Ala Pro Ala Pro Lys Pro Ala Pro
20 25 30
Ala Pro Lys Pro Ala Pro Ala Pro Ala Pro Ala Pro Ala Pro Lys Pro
35 40 45
Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro Ala Pro Ala Pro Lys Pro
50 55 60
Glu Lys Pro Ala Glu Lys Pro Ala Pro Ala Pro Lys Pro Glu Thr Pro
65 70 75 80
Lys Thr
<210> 92
<211> 76
<212> PRT
<213> Streptococcus pneumoniae
<400> 92
Pro Glu Thr Pro Ala Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro
1 5 10 15
Ala Pro Thr Pro Glu Ala Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala
20 25 30
Pro Lys Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro Lys Pro Ala
35 40 45
Pro Ala Pro Lys Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro Lys
50 55 60
Pro Ala Pro Ala Pro Lys Pro Glu Thr Pro Lys Thr
65 70 75
<210> 93
<211> 75
<212> PRT
<213> Streptococcus pneumoniae
<400> 93
Pro Glu Thr Pro Ala Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro
1 5 10 15
Ala Pro Thr Pro Glu Ala Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala
20 25 30
Pro Lys Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro Lys Pro Ala
35 40 45
Pro Ala Pro Lys Pro Ala Pro Lys Pro Glu Lys Pro Ala Glu Lys Pro
50 55 60
Ala Pro Ala Pro Lys Pro Glu Thr Pro Lys Thr
65 70 75
<210> 94
<211> 65
<212> PRT
<213> Streptococcus pneumoniae
<400> 94
Pro Glu Thr Pro Ala Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro
1 5 10 15
Ala Pro Thr Pro Glu Ala Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala
20 25 30
Pro Lys Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro Lys Pro Ala
35 40 45
Pro Ala Pro Lys Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro Lys
50 55 60
Pro
65
<210> 95
<211> 86
<212> PRT
<213> Streptococcus pneumoniae
<400> 95
Pro Asp Gly Asp Glu Glu Glu Thr Pro Ala Pro Ala Pro Gln Pro Glu
1 5 10 15
Lys Pro Ala Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Ala Pro Ala
20 25 30
Pro Lys Pro Glu Lys Ser Ala Asp Gln Gln Ala Glu Glu Asp Tyr Ala
35 40 45
Arg Arg Ser Glu Glu Glu Tyr Asn Arg Leu Thr Gln Gln Gln Pro Pro
50 55 60
Lys Ala Glu Lys Pro Ala Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro
65 70 75 80
Ala Pro Ala Pro Lys Thr
85
<210> 96
<211> 101
<212> PRT
<213> Streptococcus pneumoniae
<400> 96
Pro Glu Thr Pro Ala Pro Ala Pro Ala Pro Ala Pro Ala Pro Ala Pro
1 5 10 15
Thr Pro Glu Ala Pro Ala Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala
20 25 30
Pro Lys Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro Lys Pro Ala
35 40 45
Pro Ala Pro Lys Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro Ala
50 55 60
Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro Ala Pro Ala Pro Ala
65 70 75 80
Pro Lys Pro Glu Lys Pro Ala Glu Lys Pro Ala Pro Ala Pro Lys Pro
85 90 95
Glu Thr Pro Lys Thr
100
<210> 97
<211> 83
<212> PRT
<213> Streptococcus pneumoniae
<400> 97
Pro Glu Thr Pro Ala Pro Ala Pro Ala Pro Ala Pro Ala Pro Glu Ala
1 5 10 15
Pro Ala Pro Ala Pro Ala Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala
20 25 30
Pro Lys Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro Lys Pro Ala
35 40 45
Pro Ala Pro Lys Pro Ala Pro Ala Pro Ala Pro Ala Pro Ala Pro Lys
50 55 60
Pro Glu Lys Pro Ala Glu Lys Pro Ala Pro Ala Pro Lys Pro Glu Thr
65 70 75 80
Pro Lys Thr
<210> 98
<211> 83
<212> PRT
<213> Streptococcus pneumoniae
<400> 98
Pro Glu Thr Pro Ala Pro Ala Pro Ala Pro Ala Pro Ala Pro Ala Pro
1 5 10 15
Thr Pro Glu Ala Pro Ala Pro Ala Pro Ala Pro Ala Pro Lys Pro Ala
20 25 30
Pro Ala Pro Lys Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro Lys
35 40 45
Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro Ala Pro Ala Pro Lys
50 55 60
Pro Glu Lys Pro Ala Glu Lys Pro Ala Pro Ala Pro Lys Pro Glu Thr
65 70 75 80
Pro Lys Thr
<210> 99
<211> 81
<212> PRT
<213> Streptococcus pneumoniae
<400> 99
Pro Glu Thr Pro Ala Pro Ala Pro Ala Pro Ala Pro Ala Pro Thr Pro
1 5 10 15
Glu Ala Pro Ala Pro Ala Pro Ala Pro Ala Pro Ala Pro Lys Pro Ala
20 25 30
Pro Ala Pro Lys Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro Lys
35 40 45
Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro Ala Pro Lys Pro Glu
50 55 60
Lys Pro Ala Glu Lys Pro Ala Pro Ala Pro Lys Pro Glu Thr Pro Lys
65 70 75 80
Thr
<210> 100
<211> 85
<212> PRT
<213> Streptococcus pneumoniae
<400> 100
Pro Glu Thr Pro Ala Pro Ala Pro Ala Pro Ala Pro Ala Pro Ala Pro
1 5 10 15
Thr Pro Glu Ala Pro Ala Pro Ala Pro Ala Pro Ala Pro Lys Pro Ala
20 25 30
Pro Ala Pro Lys Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro Lys
35 40 45
Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala
50 55 60
Pro Ala Pro Ala Pro Lys Pro Glu Lys Pro Ala Glu Lys Pro Ala Pro
65 70 75 80
Ala Pro Lys Pro Glu
85
<210> 101
<211> 56
<212> PRT
<213> Streptococcus pneumoniae
<400> 101
Pro Glu Thr Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro Ala Pro
1 5 10 15
Thr Pro Glu Ala Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro Lys
20 25 30
Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala
35 40 45
Pro Lys Pro Glu Thr Pro Lys Thr
50 55
<210> 102
<211> 64
<212> PRT
<213> Streptococcus pneumoniae
<400> 102
Pro Glu Thr Pro Ala Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro
1 5 10 15
Ala Pro Thr Pro Glu Ala Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala
20 25 30
Pro Lys Pro Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro Lys Pro Ala
35 40 45
Pro Ala Pro Lys Pro Ala Pro Ala Pro Lys Pro Glu Thr Pro Lys Thr
50 55 60
<210> 103
<211> 103
<212> PRT
<213> Streptococcus pneumoniae
<400> 103
Pro Glu Thr Pro Ala Pro Ala Pro Gln Pro Ala Pro Ala Pro Glu Lys
1 5 10 15
Pro Ala Pro Ala Pro Glu Lys Pro Ala Pro Ala Pro Glu Lys Pro Ala
20 25 30
Pro Ala Pro Glu Lys Pro Ala Pro Ala Pro Glu Lys Pro Ala Pro Ala
35 40 45
Pro Glu Lys Pro Ala Pro Ala Pro Glu Lys Pro Ala Pro Ala Pro Glu
50 55 60
Lys Pro Ala Pro Ala Pro Glu Lys Pro Ala Pro Ala Pro Glu Lys Pro
65 70 75 80
Ala Pro Ala Pro Glu Lys Pro Ala Pro Ala Pro Glu Lys Pro Ala Pro
85 90 95
Thr Pro Glu Thr Pro Lys Thr
100
<210> 104
<211> 76
<212> PRT
<213> Streptococcus pneumoniae
<400> 104
Pro Glu Thr Pro Ala Pro Ala Pro Gln Pro Ala Pro Ala Pro Glu Lys
1 5 10 15
Pro Ala Glu Lys Pro Ala Pro Ala Pro Ala Pro Glu Lys Pro Ala Pro
20 25 30
Ala Pro Glu Lys Pro Ala Glu Lys Pro Ala Glu Lys Pro Ala Glu Glu
35 40 45
Pro Ala Glu Lys Pro Ala Pro Ala Pro Glu Lys Pro Ala Pro Thr Pro
50 55 60
Glu Lys Pro Ala Pro Thr Pro Glu Thr Pro Lys Thr
65 70 75
<210> 105
<211> 78
<212> PRT
<213> Streptococcus pneumoniae
<400> 105
Pro Asp Gly Asp Glu Glu Glu Leu Pro Ala Arg Ala Leu Gln Pro Glu
1 5 10 15
Gln Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Thr Pro Ala Pro Lys
20 25 30
Pro Glu Gln Pro Thr Pro Ala Pro Lys Pro Glu Gln Pro Ala Pro Ala
35 40 45
Pro Lys Pro Glu Gln Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Ala
50 55 60
Pro Ala Pro Lys Pro Glu Gln Pro Thr Pro Ala Pro Lys Thr
65 70 75
<210> 106
<211> 78
<212> PRT
<213> Streptococcus pneumoniae
<400> 106
Pro Asp Gly Asp Glu Glu Glu Thr Pro Ala Pro Ala Pro Gln Pro Glu
1 5 10 15
Gln Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Thr Pro Ala Pro Lys
20 25 30
Pro Glu Gln Pro Thr Pro Ala Pro Lys Pro Glu Gln Pro Ala Pro Ala
35 40 45
Pro Lys Pro Glu Gln Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Ala
50 55 60
Pro Ala Pro Lys Pro Glu Gln Pro Thr Pro Ala Pro Lys Thr
65 70 75
<210> 107
<211> 78
<212> PRT
<213> Streptococcus pneumoniae
<400> 107
Pro Asp Gly Asp Glu Glu Glu Thr Pro Ala Pro Ala Pro Gln Pro Glu
1 5 10 15
Gln Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Thr Pro Ala Pro Lys
20 25 30
Pro Glu Gln Pro Thr Pro Ala Pro Lys Pro Glu Gln Pro Ala Pro Ala
35 40 45
Pro Lys Pro Glu Gln Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Ala
50 55 60
Pro Ala Pro Lys Pro Glu Gln Pro Thr Pro Gly Pro Lys Ile
65 70 75
<210> 108
<211> 78
<212> PRT
<213> Streptococcus pneumoniae
<400> 108
Pro Asp Gly Asp Glu Glu Glu Thr Pro Ala Pro Ala Pro Gln Pro Glu
1 5 10 15
Gln Pro Ala Pro Ala Pro Gln Pro Glu Gln Pro Ala Pro Ala Pro Lys
20 25 30
35 40 45
Pro Lys Pro Glu Gln Pro Thr Pro Ala Pro Lys Pro Glu Gln Pro Thr
50 55 60
Pro Ala Pro Lys Pro Glu Gln Pro Thr Pro Ala Pro Lys Thr
65 70 75
<210> 109
<211> 69
<212> PRT
<213> Streptococcus pneumoniae
<400> 109
Pro Asp Gly Asp Glu Glu Glu Thr Pro Ala Pro Ala Pro Gln Pro Glu
1 5 10 15
Gln Pro Ala Pro Ala Pro Gln Pro Glu Gln Pro Ala Pro Ala Pro Lys
20 25 30
Pro Glu Gln Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Thr Pro Ala
35 40 45
Pro Lys Pro Glu Gln Pro Thr Pro Ala Pro Lys Pro Glu Gln Pro Thr
50 55 60
Pro Ala Pro Lys Thr
65
<210> 110
<211> 60
<212> PRT
<213> Streptococcus pneumoniae
<400> 110
Pro Asp Gly Asp Glu Glu Glu Thr Pro Ala Pro Ala Pro Gln Pro Glu
1 5 10 15
Gln Pro Ala Pro Ala Pro Gln Pro Glu Gln Pro Ala Pro Ala Pro Lys
20 25 30
Pro Glu Gln Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Thr Pro Ala
35 40 45
Pro Lys Pro Glu Gln Pro Thr Pro Ala Pro Lys Thr
50 55 60
<210> 111
<211> 60
<212> PRT
<213> Streptococcus pneumoniae
<400> 111
Pro Asp Gly Asp Glu Glu Glu Thr Pro Ala Pro Ala Pro Gln Pro Glu
1 5 10 15
Lys Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Ala Pro Ala Pro Lys
20 25 30
Pro Glu Gln Pro Thr Pro Ala Pro Lys Pro Glu Gln Pro Thr Pro Ala
35 40 45
Pro Lys Pro Glu Gln Pro Thr Pro Ala Pro Lys Pro
50 55 60
<210> 112
<211> 81
<212> PRT
<213> Streptococcus pneumoniae
<400> 112
Pro Asp Gly Asp Glu Glu Glu Thr Pro Ala Pro Ala Pro Ala Pro Lys
1 5 10 15
Pro Glu Gln Pro Ala Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Ala
20 25 30
Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Ala Pro Ala Pro Ala Pro
35 40 45
Lys Pro Glu Gln Pro Ala Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro
50 55 60
Ala Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Thr Pro Ala Pro Lys
65 70 75 80
Thr
<210> 113
<211> 92
<212> PRT
<213> Streptococcus pneumoniae
<400> 113
Pro Asp Gly Asp Glu Glu Glu Thr Pro Ala Pro Ala Pro Ala Pro Lys
1 5 10 15
Pro Glu Gln Pro Ala Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Ala
20 25 30
Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Ala Pro Ala Pro Ala Pro
35 40 45
Lys Pro Glu Gln Pro Ala Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro
50 55 60
Ala Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Ala Pro Ala Pro Ala
65 70 75 80
Pro Lys Pro Glu Gln Pro Thr Pro Ala Pro Lys Thr
85 90
<210> 114
<211> 86
<212> PRT
<213> Streptococcus pneumoniae
<400> 114
Pro Asp Gly Asp Glu Glu Glu Thr Pro Ala Pro Ala Pro Gln Pro Glu
1 5 10 15
Gln Pro Ala Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Ala Pro Ala
20 25 30
Pro Lys Pro Glu Lys Ser Ala Asp Gln Gln Ala Glu Glu Asp Tyr Ala
35 40 45
Arg Arg Ser Glu Glu Glu Tyr Asn Arg Leu Thr Gln Gln Gln Pro Pro
50 55 60
Lys Ala Glu Lys Pro Ala Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro
65 70 75 80
Ala Pro Ala Pro Lys Thr
85
<210> 115
<211> 79
<212> PRT
<213> Streptococcus pneumoniae
<400> 115
Pro Asp Gly Asp Glu Glu Glu Thr Pro Ala Pro Ala Pro Gln Pro Glu
1 5 10 15
Gln Pro Ala Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Ala Pro Ala
20 25 30
Pro Ala Pro Lys Pro Glu Gln Pro Ala Pro Ala Pro Ala Pro Lys Pro
35 40 45
Glu Gln Pro Ala Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Ala Pro
50 55 60
Ala Pro Ala Pro Lys Pro Glu Gln Pro Ala Pro Ala Pro Lys Thr
65 70 75
<210> 116
<211> 51
<212> PRT
<213> Streptococcus pneumoniae
<400> 116
Pro Asp Gly Asp Glu Glu Glu Thr Pro Ala Pro Ala Pro Gln Pro Glu
1 5 10 15
Gln Pro Ala Pro Ala Pro Gln Pro Glu Gln Pro Ala Pro Ala Pro Lys
20 25 30
Pro Glu Gln Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Thr Pro Ala
35 40 45
Pro Lys Thr
50
<210> 117
<211> 57
<212> PRT
<213> Streptococcus pneumoniae
<400> 117
Pro Asp Gly Asp Glu Glu Glu Thr Pro Ala Pro Ala Pro Gln Pro Glu
1 5 10 15
Gln Pro Ala Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Ala Pro Ala
20 25 30
Pro Ala Pro Lys Pro Glu Gln Pro Ala Pro Ala Pro Ala Pro Lys Pro
35 40 45
Glu Gln Pro Ala Pro Ala Pro Lys Thr
50 55
<210> 118
<211> 70
<212> PRT
<213> Streptococcus pneumoniae
<400> 118
Pro Asp Gly Asp Glu Glu Glu Thr Pro Ala Pro Ala Pro Ala Pro Lys
1 5 10 15
Pro Glu Gln Pro Ala Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Ala
20 25 30
Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Ala Pro Ala Pro Ala Pro
35 40 45
Lys Pro Glu Gln Pro Ala Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro
50 55 60
Thr Pro Ala Pro Lys Thr
65 70
<210> 119
<211> 87
<212> PRT
<213> Streptococcus pneumoniae
<400> 119
Pro Glu Lys Pro Ala Glu Glu Pro Glu Asn Pro Ala Pro Ala Pro Lys
1 5 10 15
Pro Ala Pro Ala Pro Gln Pro Glu Gln Pro Ala Pro Ala Pro Ala Pro
20 25 30
Lys Pro Glu Gln Pro Ala Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro
35 40 45
Ala Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Ala Pro Ala Pro Ala
50 55 60
Pro Lys Pro Glu Gln Pro Ala Pro Ala Pro Ala Pro Lys Pro Glu Gln
65 70 75 80
Pro Thr Pro Ala Pro Lys Thr
85
<210> 120
<211> 59
<212> PRT
<213> Streptococcus pneumoniae
<400> 120
Pro Asp Gly Asp Glu Glu Glu Thr Pro Ala Pro Ala Pro Ala Pro Lys
1 5 10 15
Pro Glu Gln Pro Ala Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Ala
20 25 30
Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Ala Pro Ala Pro Ala Pro
35 40 45
Lys Pro Glu Gln Pro Thr Pro Ala Pro Lys Ser
50 55
<210> 121
<211> 59
<212> PRT
<213> Streptococcus pneumoniae
<400> 121
Pro Asp Gly Asp Glu Glu Glu Thr Pro Ala Pro Ala Pro Ala Pro Lys
1 5 10 15
Pro Glu Gln Pro Ala Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Ala
20 25 30
Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Ala Pro Ala Pro Ala Pro
35 40 45
Lys Pro Glu Gln Pro Thr Pro Ala Pro Lys Thr
50 55
<210> 122
<211> 61
<212> PRT
<213> Streptococcus pneumoniae
<400> 122
Pro Ala Pro Ala Pro Gln Pro Glu Gln Pro Ala Pro Ala Pro Gln Pro
1 5 10 15
Glu Gln Pro Ala Pro Ala Pro Gln Pro Glu Gln Pro Ala Pro Ala Pro
20 25 30
Gln Pro Glu Gln Pro Ala Pro Ala Pro Gln Pro Glu Gln Pro Ala Pro
35 40 45
Ala Pro Gln Pro Glu Gln Pro Ala Pro Ala Pro Lys Ile
50 55 60
<210> 123
<211> 133
<212> PRT
<213> Streptococcus pneumoniae
<400> 123
Pro Ala Pro Ala Pro Gln Pro Glu Gln Pro Ala Pro Ala Pro Gln Pro
1 5 10 15
Glu Gln Pro Ala Pro Ala Pro Gln Pro Glu Gln Pro Ala Pro Ala Pro
20 25 30
Gln Pro Glu Gln Pro Ala Pro Ala Pro Gln Pro Glu Gln Pro Ala Pro
35 40 45
Ala Pro Gln Pro Glu Gln Pro Ala Pro Ala Pro Gln Pro Glu Gln Pro
50 55 60
Ala Pro Ala Pro Gln Pro Glu Gln Pro Ala Pro Ala Pro Gln Pro Glu
65 70 75 80
Gln Pro Ala Pro Ala Pro Gln Pro Glu Gln Pro Ala Pro Ala Pro Gln
85 90 95
Pro Glu Gln Pro Ala Pro Ala Pro Gln Pro Glu Gln Pro Ala Pro Ala
100 105 110
Pro Gln Pro Glu Gln Pro Ala Pro Ala Pro Gln Pro Glu Gln Pro Ala
115 120 125
Pro Ala Pro Lys Ile
130
<210> 124
<211> 75
<212> PRT
<213> Streptococcus pneumoniae
<400> 124
Pro Asp Gly Asp Glu Glu Glu Thr Pro Ala Pro Ala Pro Gln Pro Glu
1 5 10 15
Gln Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Ala Pro Ala Pro Lys
20 25 30
Pro Glu Gln Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Ala Pro Ala
35 40 45
Pro Lys Pro Glu Gln Pro Ala Lys Pro Glu Lys Pro Ala Glu Glu Pro
50 55 60
Thr Gln Pro Glu Lys Pro Ala Thr Pro Lys Thr
65 70 75
<210> 125
<211> 85
<212> PRT
<213> Streptococcus pneumoniae
<400> 125
Pro Asp Gly Gly Glu Glu Glu Thr Pro Ala Pro Ala Pro Gln Pro Asp
1 5 10 15
Glu Pro Ala Pro Ala Pro Ala Pro Asn Ala Glu Gln Pro Ala Pro Ala
20 25 30
Pro Lys Pro Glu Lys Ser Ala Asp Gln Gln Ala Glu Glu Asp Tyr Ala
35 40 45
Arg Arg Ser Glu Gly Glu Tyr Asn Arg Leu Thr Gln Gln Gln Pro Pro
50 55 60
Lys Ala Glu Lys Pro Ala Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro
65 70 75 80
Ala Pro Ala Pro Asn
85
<210> 126
<211> 57
<212> PRT
<213> Streptococcus pneumoniae
<400> 126
Pro Asp Gly Asp Glu Glu Glu Thr Pro Ala Pro Ala Pro Gln Pro Glu
1 5 10 15
Gln Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Ala Pro Ala Pro Lys
20 25 30
Pro Glu Gln Pro Ala Lys Pro Glu Lys Pro Ala Glu Glu Pro Thr Gln
35 40 45
Pro Glu Lys Pro Ala Thr Pro Lys Thr
50 55
<210> 127
<211> 66
<212> PRT
<213> Streptococcus pneumoniae
<400> 127
Pro Asp Gly Asp Glu Glu Glu Thr Pro Ala Pro Ala Pro Gln Pro Glu
1 5 10 15
Gln Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Ala Pro Ala Pro Lys
20 25 30
Pro Glu Gln Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Ala Lys Pro
35 40 45
Glu Lys Pro Ala Glu Glu Pro Thr Gln Pro Glu Lys Pro Ala Thr Pro
50 55 60
Lys Thr
65
<210> 128
<211> 69
<212> PRT
<213> Streptococcus pneumoniae
<400> 128
Pro Asp Gly Asp Glu Glu Glu Thr Pro Ala Pro Ala Pro Gln Pro Glu
1 5 10 15
Gln Pro Ala Pro Ala Pro Gln Pro Glu Gln Pro Ala Pro Ala Pro Lys
20 25 30
Pro Glu Gln Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Ala Pro Ala
35 40 45
Pro Lys Pro Glu Gln Pro Thr Pro Ala Pro Lys Pro Glu Gln Pro Thr
50 55 60
Pro Ala Pro Lys Thr
65
<210> 129
<211> 92
<212> PRT
<213> Streptococcus pneumoniae
<400> 129
Pro Glu Lys Pro Ala Pro Ala Pro Glu Thr Pro Ala Pro Glu Ala Pro
1 5 10 15
Ala Glu Gln Pro Lys Pro Ala Pro Ala Pro Gln Pro Ala Pro Ala Pro
20 25 30
Lys Pro Glu Lys Pro Ala Glu Gln Pro Lys Pro Glu Lys Thr Asp Asp
35 40 45
Gln Gln Ala Glu Glu Asp Tyr Ala Arg Arg Ser Glu Glu Glu Tyr Asn
50 55 60
Arg Leu Thr Gln Gln Gln Pro Pro Lys Ala Glu Lys Pro Ala Pro Ala
65 70 75 80
Pro Gln Pro Glu Gln Pro Ala Pro Ala Pro Lys Thr
85 90
<210> 130
<211> 83
<212> PRT
<213> Streptococcus pneumoniae
<400> 130
Pro Glu Lys Pro Ala Pro Ala Pro Glu Thr Pro Ala Pro Glu Ala Pro
1 5 10 15
Ala Glu Gln Pro Lys Pro Ala Pro Ala Pro Gln Pro Ala Pro Ala Pro
20 25 30
Lys Pro Glu Lys Pro Ala Glu Gln Pro Lys Pro Glu Lys Thr Asp Asp
35 40 45
Gln Gln Ala Glu Glu Asp Tyr Ala Arg Arg Ser Glu Glu Glu Tyr Asn
50 55 60
Arg Leu Thr Gln Gln Gln Pro Pro Lys Ala Glu Lys Pro Ala Pro Ala
65 70 75 80
Pro Lys Thr
<210> 131
<211> 92
<212> PRT
<213> Streptococcus pneumoniae
<400> 131
Pro Glu Lys Pro Ala Pro Ala Pro Glu Thr Pro Ala Pro Glu Ala Pro
1 5 10 15
Ala Glu Gln Pro Lys Pro Ala Pro Ala Pro Gln Pro Ala Pro Ala Pro
20 25 30
Lys Pro Glu Lys Pro Ala Glu Gln Pro Lys Ala Glu Lys Thr Asp Asp
35 40 45
Gln Gln Ala Glu Glu Asp Tyr Ala Arg Arg Ser Glu Glu Glu Tyr Asn
50 55 60
Arg Leu Thr Gln Gln Gln Pro Pro Lys Ala Glu Lys Pro Ala Pro Ala
65 70 75 80
Pro Lys Pro Glu Gln Pro Ala Pro Ala Pro Lys Ile
85 90
<210> 132
<211> 92
<212> PRT
<213> Streptococcus pneumoniae
<400> 132
Pro Glu Lys Pro Ala Pro Ala Pro Glu Thr Pro Ala Pro Glu Ala Pro
1 5 10 15
Ala Glu Gln Pro Lys Pro Ala Pro Ala Pro Gln Pro Ala Pro Ala Pro
20 25 30
Lys Pro Glu Lys Pro Ala Glu Gln Pro Lys Ala Glu Lys Thr Asp Asp
35 40 45
Gln Gln Ala Glu Glu Asp Tyr Ala Arg Arg Ser Glu Glu Glu Tyr Asn
50 55 60
Arg Leu Thr Gln Gln Gln Pro Pro Lys Ala Glu Lys Pro Ala Pro Ala
65 70 75 80
Pro Lys Pro Glu Gln Pro Val Pro Ala Pro Lys Thr
85 90
<210> 133
<211> 128
<212> PRT
<213> Streptococcus pneumoniae
<400> 133
Pro Ala Pro Glu Ala Pro Ala Glu Gln Pro Lys Pro Glu Lys Ser Ala
1 5 10 15
Glu Gln Gln Ala Glu Glu Asp Tyr Ala Arg Arg Ser Glu Glu Glu Tyr
20 25 30
Asn Arg Leu Thr Gln Gln Gln Pro Pro Lys Ala Glu Lys Pro Ala Glu
35 40 45
Glu Pro Thr Arg Pro Ala Pro Ala Pro Glu Ala Pro Ala Glu Gln Pro
50 55 60
Lys Pro Glu Lys Ser Ala Glu Gln Gln Ala Glu Glu Asp Tyr Ala Arg
65 70 75 80
Arg Ser Glu Glu Glu Tyr Asn Arg Leu Thr Gln Gln Gln Pro Pro Lys
85 90 95
Ala Glu Lys Pro Ala Glu Glu Pro Thr Gln Pro Ala Pro Ala Pro Glu
100 105 110
Gln Pro Thr Glu Pro Thr Gln Pro Glu Lys Pro Val Ala Pro Lys Thr
115 120 125
<210> 134
<211> 90
<212> PRT
<213> Streptococcus pneumoniae
<400> 134
Pro Glu Lys Pro Ala Pro Ala Pro Glu Thr Pro Ala Pro Glu Ala Pro
1 5 10 15
Ala Glu Gln Pro Lys Pro Ala Pro Ala Pro Gln Pro Ala Pro Ala Pro
20 25 30
Lys Pro Glu Lys Pro Ala Glu Gln Pro Lys Ala Glu Lys Pro Ala Asp
35 40 45
Gln Gln Ala Glu Glu Asp Tyr Asp Arg Arg Ser Glu Glu Glu Tyr Asn
50 55 60
Arg Leu Thr Gln Gln Gln Pro Pro Lys Ala Glu Lys Pro Ala Pro Ala
65 70 75 80
Pro Gln Pro Glu Gln Pro Ala Pro Ala Pro
85 90
<210> 135
<211> 92
<212> PRT
<213> Streptococcus pneumoniae
<400> 135
Pro Glu Lys Pro Ala Pro Ala Pro Glu Thr Pro Ala Pro Glu Ala Pro
1 5 10 15
Ala Glu Gln Pro Lys Pro Ala Pro Ala Pro Gln Pro Ala Pro Ala Pro
20 25 30
Lys Pro Glu Lys Pro Ala Glu Gln Pro Lys Ala Glu Lys Pro Ala Asp
35 40 45
Gln Gln Ala Glu Glu Asp Tyr Asp Arg Arg Ser Glu Glu Glu Tyr Asn
50 55 60
Arg Leu Thr Gln Gln Gln Pro Pro Lys Ala Glu Lys Pro Ala Pro Ala
65 70 75 80
Pro Gln Pro Glu Gln Pro Ala Pro Ala Pro Lys Thr
85 90
<210> 136
<211> 106
<212> PRT
<213> Streptococcus pneumoniae
<400> 136
Pro Glu Lys Pro Ala Glu Glu Pro Ser Gln Pro Glu Lys Pro Ala Glu
1 5 10 15
Glu Ala Pro Ala Pro Glu Gln Pro Thr Glu Pro Thr Gln Pro Glu Lys
20 25 30
Pro Ala Glu Gln Pro Gln Pro Ala Pro Ala Pro Gln Pro Glu Lys Pro
35 40 45
Ala Glu Glu Thr Pro Ala Pro Lys Pro Glu Lys Pro Ala Glu Gln Pro
50 55 60
Lys Ala Glu Lys Pro Ala Asp Gln Gln Ala Glu Glu Asp Tyr Ala Arg
65 70 75 80
Arg Ser Glu Glu Glu Tyr Asn Arg Leu Thr Gln Gln Gln Pro Pro Lys
85 90 95
Ala Glu Lys Pro Ala Pro Ala Pro Lys Thr
100 105
<210> 137
<211> 100
<212> PRT
<213> Streptococcus pneumoniae
<400> 137
Pro Glu Lys Ser Ala Glu Glu Pro Ser Gln Pro Glu Lys Pro Ala Glu
1 5 10 15
Glu Ala Pro Ala Pro Glu Gln Pro Thr Glu Pro Thr Gln Pro Glu Lys
20 25 30
Pro Ala Glu Glu Thr Pro Ala Pro Lys Pro Glu Lys Pro Ala Glu Gln
35 40 45
Pro Lys Ala Glu Lys Thr Asp Asp Gln Gln Ala Glu Glu Asp Tyr Ala
50 55 60
Arg Arg Ser Glu Glu Glu Tyr Asn Arg Leu Thr Gln Gln Gln Pro Pro
65 70 75 80
Lys Ala Glu Lys Pro Ala Pro Ala Pro Gln Pro Glu Gln Pro Ala Pro
85 90 95
Ala Pro Lys Thr
100
<210> 138
<211> 93
<212> PRT
<213> Streptococcus pneumoniae
<400> 138
Pro Glu Lys Ser Ala Glu Glu Pro Ser Gln Pro Glu Lys Pro Ala Glu
1 5 10 15
Glu Ala Pro Ala Pro Glu Gln Pro Thr Glu Pro Thr Gln Pro Glu Lys
20 25 30
Pro Ala Glu Glu Thr Pro Ala Pro Lys Pro Glu Lys Pro Ala Glu Gln
35 40 45
Pro Lys Ala Glu Lys Thr Asp Asp Gln Gln Ala Glu Glu Asp Tyr Ala
50 55 60
Arg Arg Ser Glu Glu Glu Tyr Asn Arg Leu Thr Gln Gln Gln Pro Pro
65 70 75 80
Lys Ala Glu Lys Pro Ala Pro Ala Pro Gln Pro Glu Gln
85 90
<210> 139
<211> 87
<212> PRT
<213> Streptococcus pneumoniae
<400> 139
Pro Glu Lys Pro Ala Glu Glu Ser Glu Asn Pro Ala Pro Ala Pro Lys
1 5 10 15
Pro Ala Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Ala Pro Ala Pro
20 25 30
Ala Pro Lys Pro Glu Lys Ser Ala Asp Gln Gln Ala Glu Glu Asp Tyr
35 40 45
Ala Arg Arg Ser Glu Glu Glu Tyr Asn Arg Leu Thr Gln Gln Gln Pro
50 55 60
Pro Lys Ala Glu Lys Pro Ala Pro Ala Pro Ala Pro Lys Pro Glu Gln
65 70 75 80
Pro Ala Pro Ala Pro Lys Thr
85
<210> 140
<211> 86
<212> PRT
<213> Streptococcus pneumoniae
<400> 140
Pro Glu Lys Pro Ala Glu Glu Pro Glu Asn Pro Ala Pro Ala Pro Lys
1 5 10 15
Pro Ala Pro Ala Pro Gln Pro Glu Lys Pro Glu Lys Pro Ala Glu Gln
20 25 30
Pro Lys Pro Glu Lys Pro Asp Asp Gln Gln Ala Glu Glu Asp Tyr Ala
35 40 45
Arg Arg Ser Glu Glu Glu Tyr Asn Arg Leu Thr Gln Gln Gln Pro Pro
50 55 60
Lys Ala Glu Lys Pro Ala Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro
65 70 75 80
Ala Pro Ala Pro Lys Thr
85
<210> 141
<211> 77
<212> PRT
<213> Streptococcus pneumoniae
<400> 141
Pro Glu Lys Pro Ala Glu Glu Pro Glu Asn Pro Ala Pro Ala Pro Lys
1 5 10 15
Pro Ala Pro Ala Pro Gln Pro Glu Lys Pro Glu Lys Pro Ala Glu Gln
20 25 30
Pro Lys Pro Glu Lys Pro Asp Asp Gln Gln Ala Glu Glu Asp Tyr Ala
35 40 45
Arg Arg Ser Glu Glu Glu Tyr Asn Arg Leu Thr Gln Gln Gln Pro Pro
50 55 60
Lys Ala Glu Lys Pro Ala Pro Ala Pro Ala Pro Lys Thr
65 70 75
<210> 142
<211> 129
<212> PRT
<213> Streptococcus pneumoniae
<400> 142
Pro Glu Lys Pro Ala Glu Glu Pro Glu Asn Pro Ala Pro Ala Pro Lys
1 5 10 15
Pro Ala Pro Ala Pro Gln Pro Glu Lys Pro Ala Pro Ala Pro Ala Pro
20 25 30
Ala Pro Lys Pro Glu Lys Ser Ala Asp Gln Gln Ala Glu Glu Asp Tyr
35 40 45
Ala Arg Arg Ser Glu Glu Glu Tyr Asn Arg Leu Thr Gln Gln Gln Pro
50 55 60
Pro Lys Ala Glu Lys Pro Ala Pro Ala Pro Ala Pro Lys Pro Glu Lys
65 70 75 80
Ser Ala Asp Gln Gln Ala Glu Glu Asp Tyr Ala Arg Arg Ser Glu Glu
85 90 95
Glu Tyr Asn Arg Leu Thr Gln Gln Gln Pro Pro Lys Ala Glu Lys Pro
100 105 110
Ala Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Ala Pro Ala Pro Lys
115 120 125
Thr
<210> 143
<211> 89
<212> PRT
<213> Streptococcus pneumoniae
<400> 143
Pro Glu Lys Pro Ala Pro Ala Pro Glu Thr Pro Ala Pro Glu Ala Pro
1 5 10 15
Ala Pro Ala Pro Lys Pro Ala Pro Ala Pro Gln Pro Glu Lys Pro Ala
20 25 30
Pro Ala Pro Lys Pro Glu Lys Pro Ala Glu Gln Pro Lys Pro Glu Lys
35 40 45
Pro Ala Asp Gln Gln Ala Glu Glu Asp Tyr Ala Arg Arg Ser Glu Glu
50 55 60
Glu Tyr Asn Arg Leu Thr Gln Gln Gln Pro Ala Pro Ala Pro Lys Pro
65 70 75 80
Glu Gln Pro Ala Pro Ala Pro Lys Thr
85
<210> 144
<211> 96
<212> PRT
<213> Streptococcus pneumoniae
<400> 144
Pro Glu Lys Pro Ala Pro Ala Pro Ala Pro Glu Thr Pro Ala Pro Glu
1 5 10 15
Ala Pro Ala Glu Gln Pro Lys Pro Ala Pro Glu Thr Pro Ala Pro Ala
20 25 30
Pro Lys Pro Glu Lys Pro Ala Glu Gln Pro Lys Pro Glu Lys Pro Ala
35 40 45
Asp Gln Gln Ala Glu Glu Asp Tyr Ala Arg Arg Ser Glu Glu Glu Tyr
50 55 60
Asn Arg Leu Thr Gln Gln Gln Pro Ala Pro Ala Pro Lys Pro Glu Gln
65 70 75 80
Pro Ala Lys Pro Glu Lys Pro Ala Glu Glu Pro Thr Gln Pro Glu Lys
85 90 95
<210> 145
<211> 85
<212> PRT
<213> Streptococcus pneumoniae
<400> 145
Pro Glu Lys Pro Ala Glu Glu Pro Glu Asn Pro Ala Pro Ala Pro Lys
1 5 10 15
Pro Ala Pro Ala Pro Gln Pro Glu Lys Pro Ala Pro Ala Pro Ala Pro
20 25 30
Lys Pro Glu Lys Ser Ala Asp Gln Gln Ala Glu Glu Asp Tyr Ala Arg
35 40 45
Arg Ser Glu Glu Glu Tyr Asn Arg Leu Thr Gln Gln Gln Pro Pro Lys
50 55 60
Ala Glu Lys Pro Ala Pro Ala Pro Val Pro Lys Pro Glu Gln Pro Ala
65 70 75 80
Pro Ala Pro Lys Thr
85
<210> 146
<211> 86
<212> PRT
<213> Streptococcus pneumoniae
<400> 146
Pro Glu Lys Pro Ala Glu Glu Thr Pro Ala Pro Ala Pro Lys Pro Glu
1 5 10 15
Gln Pro Ala Glu Gln Pro Lys Pro Ala Pro Ala Pro Gln Pro Glu Lys
20 25 30
Pro Ala Glu Glu Pro Glu Asn Pro Ala Pro Ala Pro Gln Pro Glu Lys
35 40 45
Ser Ala Asp Gln Gln Ala Glu Glu Asp Tyr Ala Arg Arg Ser Glu Glu
50 55 60
Glu Tyr Asn Arg Leu Thr Gln Gln Gln Pro Pro Lys Ala Glu Lys Pro
65 70 75 80
Ala Pro Ala Pro Gln Pro
85
<210> 147
<211> 88
<212> PRT
<213> Streptococcus pneumoniae
<400> 147
Pro Glu Thr Pro Ala Pro Ala Pro Lys Pro Glu Thr Pro Ala Pro Ala
1 5 10 15
Pro Glu Ala Pro Ala Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Ala
20 25 30
Pro Ala Pro Lys Pro Glu Lys Ser Ala Asp Gln Gln Ala Glu Glu Asp
35 40 45
Tyr Ala Arg Arg Ser Glu Glu Glu Tyr Asn Arg Leu Thr Gln Gln Gln
50 55 60
Pro Pro Lys Ala Glu Lys Pro Ala Pro Ala Pro Ala Pro Lys Pro Glu
65 70 75 80
Gln Pro Ala Pro Ala Pro Lys Thr
85
<210> 148
<211> 85
<212> PRT
<213> Streptococcus pneumoniae
<400> 148
Pro Glu Lys Pro Ala Glu Glu Pro Glu Asn Pro Ala Pro Ala Pro Lys
1 5 10 15
Pro Ala Pro Ala Pro Gln Pro Glu Lys Pro Ala Pro Ala Pro Ala Pro
20 25 30
Lys Pro Glu Lys Ser Ala Asp Gln Gln Ala Glu Glu Asp Tyr Ala Arg
35 40 45
Arg Ser Glu Glu Glu Tyr Asn Arg Leu Thr Gln Gln Gln Pro Pro Lys
50 55 60
Ala Glu Lys Pro Ala Pro Ala Pro Val Pro Lys Pro Glu Gln Pro Ala
65 70 75 80
Pro Ala Pro Lys Ser
85
<210> 149
<211> 85
<212> PRT
<213> Streptococcus pneumoniae
<400> 149
Pro Asp Gly Asp Glu Glu Glu Thr Pro Ala Pro Glu Ala Pro Ala Glu
1 5 10 15
Gln Pro Lys Pro Glu Lys Pro Ala Glu Glu Thr Pro Ala Pro Ala Pro
20 25 30
Lys Pro Glu Lys Ser Ala Asp Gln Gln Ala Glu Glu Asp Tyr Ala Arg
35 40 45
Arg Ser Glu Glu Glu Tyr Asn Arg Leu Thr Gln Gln Gln Pro Pro Lys
50 55 60
Ala Glu Lys Pro Ala Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Ala
65 70 75 80
Pro Ala Pro Lys Thr
85
<210> 150
<211> 84
<212> PRT
<213> Streptococcus pneumoniae
<400> 150
Pro Asp Gly Asp Glu Glu Glu Thr Pro Ala Pro Glu Ala Pro Ala Glu
1 5 10 15
Gln Pro Lys Pro Glu Lys Pro Ala Glu Glu Thr Pro Ala Pro Ala Pro
20 25 30
Lys Pro Glu Lys Ser Ala Asp Gln Gln Ala Glu Glu Asp Tyr Ala Arg
35 40 45
Arg Ser Glu Glu Glu Tyr Asn Arg Leu Thr Gln Gln Gln Pro Pro Lys
50 55 60
Ala Glu Lys Pro Ala Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Ala
65 70 75 80
Pro Ala Pro Lys
<210> 151
<211> 85
<212> PRT
<213> Streptococcus pneumoniae
<400> 151
Pro Asp Gly Asp Glu Glu Glu Thr Pro Pro Pro Glu Ala Pro Ala Glu
1 5 10 15
Gln Pro Lys Pro Glu Lys Pro Ala Glu Glu Thr Pro Ala Pro Ala Pro
20 25 30
Lys Pro Glu Lys Ser Ala Asp Gln Gln Ala Glu Glu Asp Tyr Ala Arg
35 40 45
Arg Ser Glu Glu Glu Tyr Asn Arg Leu Thr Gln Gln Gln Pro Pro Lys
50 55 60
Ala Glu Lys Pro Ala Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Ala
65 70 75 80
Pro Ala Pro Lys Ser
85
<210> 152
<211> 118
<212> PRT
<213> Streptococcus pneumoniae
<400> 152
Pro Asp Gly Asp Glu Glu Glu Thr Pro Ala Pro Glu Ala Pro Ala Glu
1 5 10 15
Gln Pro Lys Pro Glu Lys Pro Ala Glu Glu Thr Pro Ala Pro Ala Pro
20 25 30
Lys Pro Glu Lys Ser Ala Asp Gln Gln Ala Glu Glu Asp Tyr Ala Arg
35 40 45
Arg Ser Glu Glu Glu Tyr Asn Arg Leu Thr Gln Gln Gln Pro Pro Lys
50 55 60
Ala Glu Lys Pro Ala Pro Ala Pro Ala Pro Lys Pro Glu Gln Pro Asp
65 70 75 80
Pro Ala Pro Lys Pro Glu Gln Pro Ala Pro Ala Pro Lys Pro Glu Gln
85 90 95
Pro Ala Lys Pro Glu Lys Pro Ala Glu Glu Pro Thr Gln Pro Glu Lys
100 105 110
Pro Ala Thr Pro Lys Thr
115
<210> 153
<211> 80
<212> PRT
<213> Streptococcus pneumoniae
<400> 153
Pro Asp Gly Asp Glu Glu Glu Thr Pro Ala Pro Ala Pro Gln Pro Glu
1 5 10 15
Lys Pro Ala Glu Glu Pro Glu Asn Pro Ala Pro Ala Pro Lys Pro Glu
20 25 30
Lys Ser Ala Asp Gln Gln Ala Glu Glu Asp Tyr Ala Arg Arg Ser Glu
35 40 45
Glu Glu Tyr Asn Arg Leu Thr Gln Gln Gln Pro Pro Lys Ala Glu Lys
50 55 60
Pro Ala Pro Ala Pro Gln Pro Glu Gln Pro Ala Pro Ala Pro Lys Ile
65 70 75 80
<210> 154
<211> 85
<212> PRT
<213> Streptococcus pneumoniae
<400> 154
Pro Asp Gly Asp Glu Glu Glu Thr Pro Ala Pro Ala Pro Gln Pro Ala
1 5 10 15
Pro Ala Pro Lys Pro Ala Pro Ala Pro Gln Pro Glu Lys Pro Ala Glu
20 25 30
Gln Pro Lys Ala Glu Lys Pro Ala Asp Gln Gln Ala Glu Glu Asp Tyr
35 40 45
Ala Arg Arg Ser Glu Glu Glu Tyr Asn Arg Leu Thr Gln Gln Gln Pro
50 55 60
Pro Lys Ala Glu Lys Pro Ala Pro Ala Pro Gln Pro Glu Gln Pro Ala
65 70 75 80
Pro Ala Pro Lys Thr
85
<210> 155
<211> 92
<212> PRT
<213> Streptococcus pneumoniae
<400> 155
Pro Glu Lys Pro Ala Pro Ala Pro Glu Thr Pro Ala Pro Glu Ala Pro
1 5 10 15
Ala Glu Gln Pro Lys Pro Ala Pro Ala Pro Gln Pro Ala Pro Ala Pro
20 25 30
Lys Pro Glu Lys Pro Ala Glu Gln Pro Lys Ala Glu Lys Pro Ala Asp
35 40 45
Gln Gln Ala Glu Glu Asp Tyr Ala Arg Arg Ser Glu Glu Glu Tyr Asn
50 55 60
Arg Leu Thr Gln Gln Gln Pro Pro Lys Ala Glu Lys Pro Ala Pro Ala
65 70 75 80
Pro Gln Pro Glu Gln Pro Ala Pro Ala Pro Lys Thr
85 90
<210> 156
<211> 89
<212> PRT
<213> Streptococcus pneumoniae
<400> 156
Pro Glu Lys Pro Ala Pro Ala Pro Glu Thr Pro Ala Pro Glu Ala Pro
1 5 10 15
Ala Glu Gln Pro Lys Pro Ala Pro Ala Pro Gln Pro Ala Pro Ala Pro
20 25 30
Lys Pro Glu Lys Pro Ala Glu Gln Pro Lys Ala Glu Lys Thr Asp Asp
35 40 45
Gln Gln Ala Glu Glu Asp Tyr Ala Arg Arg Ser Glu Glu Glu Tyr Asn
50 55 60
Arg Leu Thr Gln Gln Gln Pro Pro Lys Ala Glu Lys Pro Ala Pro Ala
65 70 75 80
Pro Lys Pro Glu Gln Pro Ala Pro Ala
85
<210> 157
<211> 14
<212> PRT
<213> Streptococcus pneumoniae
<400> 157
Pro Glu Lys Pro Ala Pro Ala Pro Glu Thr Pro Ala Pro Glu
1 5 10
<210> 158
<211> 302
<212> PRT
<213> Artificial Sequence
<220>
<223> aHD-PRD construct designated PspA01.3
<400> 158
Glu Glu Ser Pro Val Ala Ser Gln Ser Lys Ala Glu Lys Asp Tyr Asp
1 5 10 15
Ala Ala Lys Lys Asp Ala Lys Asn Ala Lys Lys Ala Val Glu Asp Ala
20 25 30
Gln Lys Ala Leu Asp Asp Ala Lys Ala Ala Gln Lys Lys Tyr Asp Glu
35 40 45
Asp Gln Lys Lys Thr Glu Glu Lys Ala Ala Leu Glu Lys Ala Ala Ser
50 55 60
Glu Glu Met Asp Lys Ala Val Ala Ala Val Gln Gln Ala Tyr Leu Ala
65 70 75 80
Tyr Gln Gln Ala Thr Asp Lys Ala Ala Lys Asp Ala Ala Asp Lys Met
85 90 95
Ile Asp Glu Ala Lys Lys Arg Glu Glu Glu Ala Lys Thr Lys Phe Asn
100 105 110
Thr Val Arg Ala Met Val Val Pro Glu Pro Glu Gln Leu Ala Glu Thr
115 120 125
Lys Lys Lys Ser Glu Glu Ala Lys Gln Lys Ala Pro Glu Leu Thr Lys
130 135 140
Lys Leu Glu Glu Ala Lys Ala Lys Leu Glu Glu Ala Glu Lys Lys Ala
145 150 155 160
Thr Glu Ala Lys Gln Lys Val Asp Ala Glu Glu Val Ala Pro Gln Ala
165 170 175
Lys Ile Ala Glu Leu Glu Asn Gln Val His Arg Leu Glu Gln Glu Leu
180 185 190
Lys Glu Ile Asp Glu Ser Glu Ser Glu Asp Tyr Ala Lys Glu Gly Phe
195 200 205
Arg Ala Pro Leu Gln Ser Lys Leu Asp Ala Lys Lys Ala Lys Leu Ser
210 215 220
Lys Leu Glu Glu Leu Ser Asp Lys Ile Asp Glu Leu Asp Ala Glu Ile
225 230 235 240
Ala Lys Leu Glu Asp Gln Leu Lys Ala Ala Glu Glu Asn Asn Asn Val
245 250 255
Glu Asp Tyr Phe Lys Glu Gly Leu Glu Lys Thr Ile Ala Ala Lys Lys
260 265 270
Ala Glu Leu Glu Lys Thr Glu Ala Asp Leu Lys Lys Ala Val Asn Glu
275 280 285
Pro Glu Lys Pro Ala Pro Ala Pro Glu Thr Pro Ala Pro Glu
290 295 300
<210> 159
<211> 288
<212> PRT
<213> Streptococcus pneumoniae
<400> 159
Glu Glu Ser Pro Val Ala Ser Gln Ser Lys Ala Glu Lys Asp Tyr Asp
1 5 10 15
Ala Ala Lys Lys Asp Ala Lys Asn Ala Lys Lys Ala Val Glu Asp Ala
20 25 30
Gln Lys Ala Leu Asp Asp Ala Lys Ala Ala Gln Lys Lys Tyr Asp Glu
35 40 45
Asp Gln Lys Lys Thr Glu Glu Lys Ala Ala Leu Glu Lys Ala Ala Ser
50 55 60
Glu Glu Met Asp Lys Ala Val Ala Ala Val Gln Gln Ala Tyr Leu Ala
65 70 75 80
Tyr Gln Gln Ala Thr Asp Lys Ala Ala Lys Asp Ala Ala Asp Lys Met
85 90 95
Ile Asp Glu Ala Lys Lys Arg Glu Glu Glu Ala Lys Thr Lys Phe Asn
100 105 110
Thr Val Arg Ala Met Val Val Pro Glu Pro Glu Gln Leu Ala Glu Thr
115 120 125
Lys Lys Lys Ser Glu Glu Ala Lys Gln Lys Ala Pro Glu Leu Thr Lys
130 135 140
Lys Leu Glu Glu Ala Lys Ala Lys Leu Glu Glu Ala Glu Lys Lys Ala
145 150 155 160
Thr Glu Ala Lys Gln Lys Val Asp Ala Glu Glu Val Ala Pro Gln Ala
165 170 175
Lys Ile Ala Glu Leu Glu Asn Gln Val His Arg Leu Glu Gln Glu Leu
180 185 190
Lys Glu Ile Asp Glu Ser Glu Ser Glu Asp Tyr Ala Lys Glu Gly Phe
195 200 205
Arg Ala Pro Leu Gln Ser Lys Leu Asp Ala Lys Lys Ala Lys Leu Ser
210 215 220
Lys Leu Glu Glu Leu Ser Asp Lys Ile Asp Glu Leu Asp Ala Glu Ile
225 230 235 240
Ala Lys Leu Glu Asp Gln Leu Lys Ala Ala Glu Glu Asn Asn Asn Val
245 250 255
Glu Asp Tyr Phe Lys Glu Gly Leu Glu Lys Thr Ile Ala Ala Lys Lys
260 265 270
Ala Glu Leu Glu Lys Thr Glu Ala Asp Leu Lys Lys Ala Val Asn Glu
275 280 285
<210> 160
<211> 912
<212> ДНК
<213> Искусственная последовательность
<220>
<223> ДНК, кодирующая PspA01.3 [SEQ ID NO:158]. ATG, кодирующий
метионин добавляли в начале в качестве инициатора,а
TGA добавляли в конце в качестве стоп-кодона
<400> 160
atggaagaaa gcccggtggc gagccagagc aaagcggaaa aagattatga tgcggcgaaa 60
aaagatgcga aaaacgcgaa aaaagcggtg gaagatgcgc agaaagcgct ggatgatgcg 120
aaagcggcgc agaaaaaata tgatgaagat cagaaaaaaa ccgaagaaaa agcggcgctg 180
gaaaaagcgg cgagcgaaga aatggataaa gcggtggcgg cggtgcagca ggcgtatctg 240
gcgtatcagc aggcgaccga taaagcggcg aaagatgcgg cggataaaat gattgatgaa 300
gcgaaaaaac gcgaagaaga agcgaaaacc aaatttaaca ccgtgcgcgc gatggtggtg 360
ccggaaccgg aacagctggc ggaaaccaaa aaaaaaagcg aagaagcgaa acagaaagcg 420
ccggaactga ccaaaaaact ggaagaagcg aaagcgaaac tggaagaagc ggaaaaaaaa 480
gcgaccgaag cgaaacagaa agtggatgcg gaagaagtgg cgccgcaggc gaaaattgcg 540
gaactggaaa accaggtgca tcgcctggaa caggaactga aagaaattga tgaaagcgaa 600
agcgaagatt atgcgaaaga aggctttcgc gcgccgctgc agagcaaact ggatgcgaaa 660
aaagcgaaac tgagcaaact ggaagaactg agcgataaaa ttgatgaact ggatgcggaa 720
attgcgaaac tggaagatca gctgaaagcg gcggaagaaa acaacaacgt ggaagattat 780
tttaaagaag gcctggaaaa aaccattgcg gcgaaaaaag cggaactgga aaaaaccgaa 840
gcggatctga aaaaagcggt gaacgaaccg gaaaaaccgg cgccggcgcc ggaaaccccg 900
gcgccggaat ga 912
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| ПНЕВМОКОККОВЫЕ ПОВЕРХНОСТНЫЕ БЕЛКИ | 2020 |
|
RU2818278C2 |
| УЛУЧШЕННЫЕ ВАРИАБЕЛЬНЫЕ ДОМЕНЫ ИММУНОГЛОБУЛИНА | 2015 |
|
RU2809788C2 |
| УЛУЧШЕННЫЕ ВАРИАБЕЛЬНЫЕ ДОМЕНЫ ИММУНОГЛОБУЛИНА | 2015 |
|
RU2746738C2 |
| ПОЛИПЕПТИД, ВКЛЮЧАЮЩИЙ АНТИГЕНСВЯЗЫВАЮЩИЙ ДОМЕН И ТРАНСПОРТИРУЮЩИЙ СЕГМЕНТ | 2018 |
|
RU2815452C2 |
| СПОСОБ ПОВЫШЕНИЯ ИММУНОГЕННОСТИ БЕЛКОВОГО/ПЕПТИДНОГО АНТИГЕНА | 2021 |
|
RU2830627C1 |
| УЛУЧШЕННЫЕ ОДИНОЧНЫЕ ВАРИАБЕЛЬНЫЕ ДОМЕНЫ ИММУНОГЛОБУЛИНА, СВЯЗЫВАЮЩИЕСЯ С СЫВОРОТОЧНЫМ АЛЬБУМИНОМ | 2017 |
|
RU2765384C2 |
| CD8A-СВЯЗЫВАЮЩИЕ ДОМЕНЫ ТИПА III ФИБРОНЕКТИНА | 2017 |
|
RU2759952C2 |
| ПОЛИПЕПТИД, СОДЕРЖАЩИЙ АНТИГЕНСВЯЗЫВАЮЩИЙ ДОМЕН И ТРАНСПОРТИРУЮЩИЙ СЕГМЕНТ | 2017 |
|
RU2827545C2 |
| НОВЫЕ КОНСТРУКЦИИ ХИМЕРНОГО АНТИГЕННОГО РЕЦЕПТОРА, СОДЕРЖАЩИЕ ДОМЕНЫ TNFR2 | 2019 |
|
RU2808254C2 |
| CD3-СВЯЗЫВАЮЩИЙ ДОМЕН | 2015 |
|
RU2742691C2 |
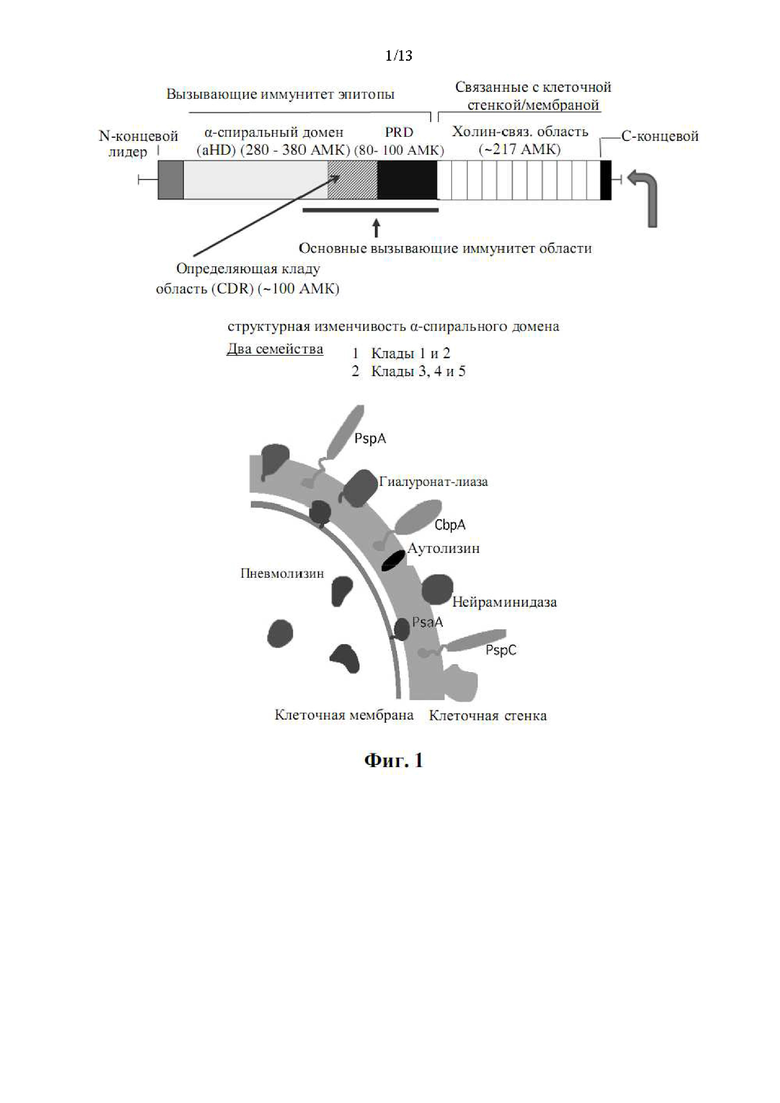
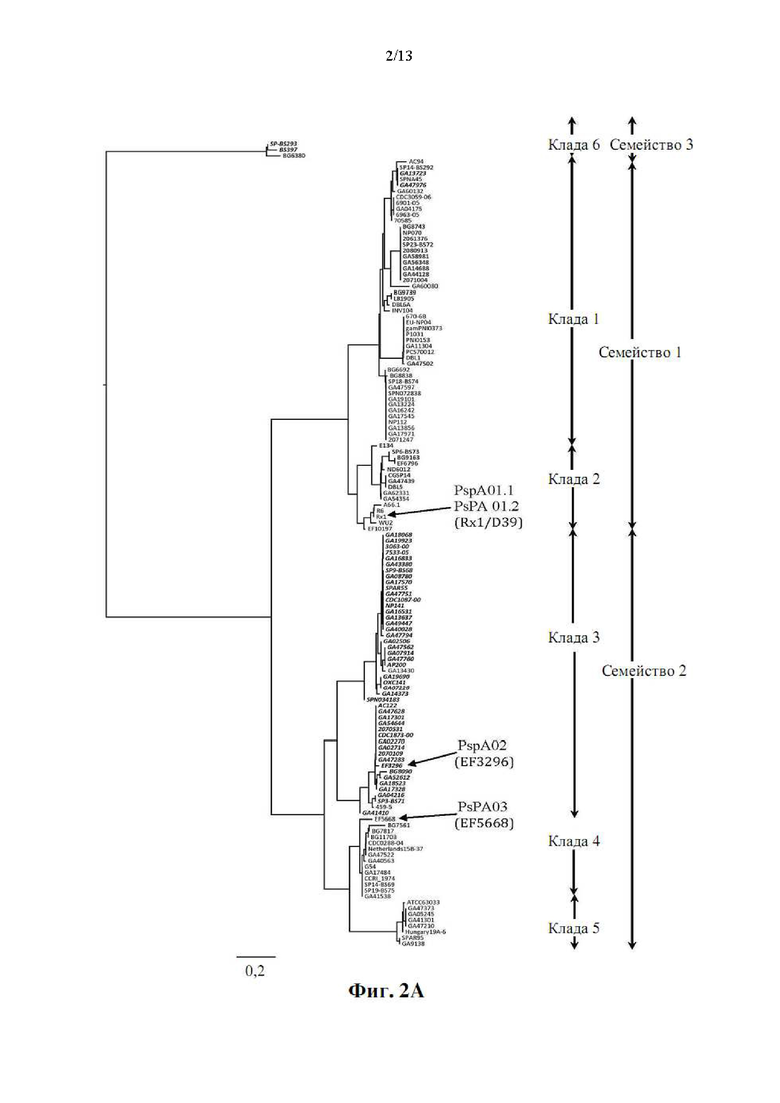
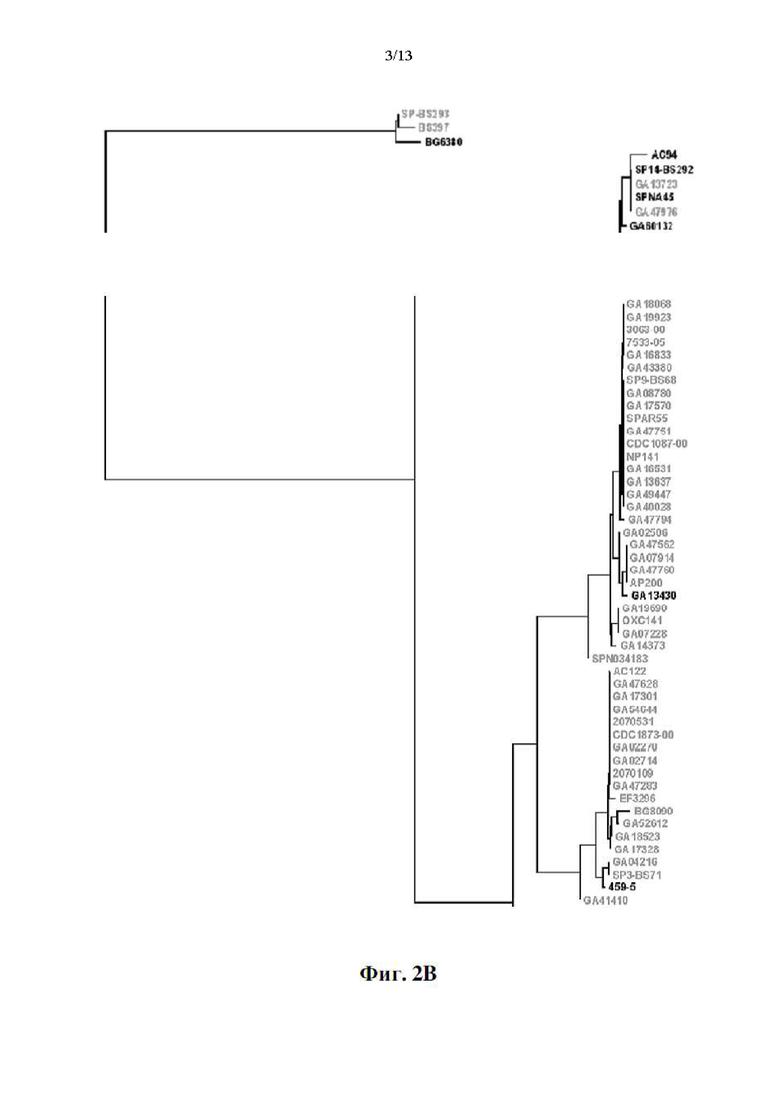
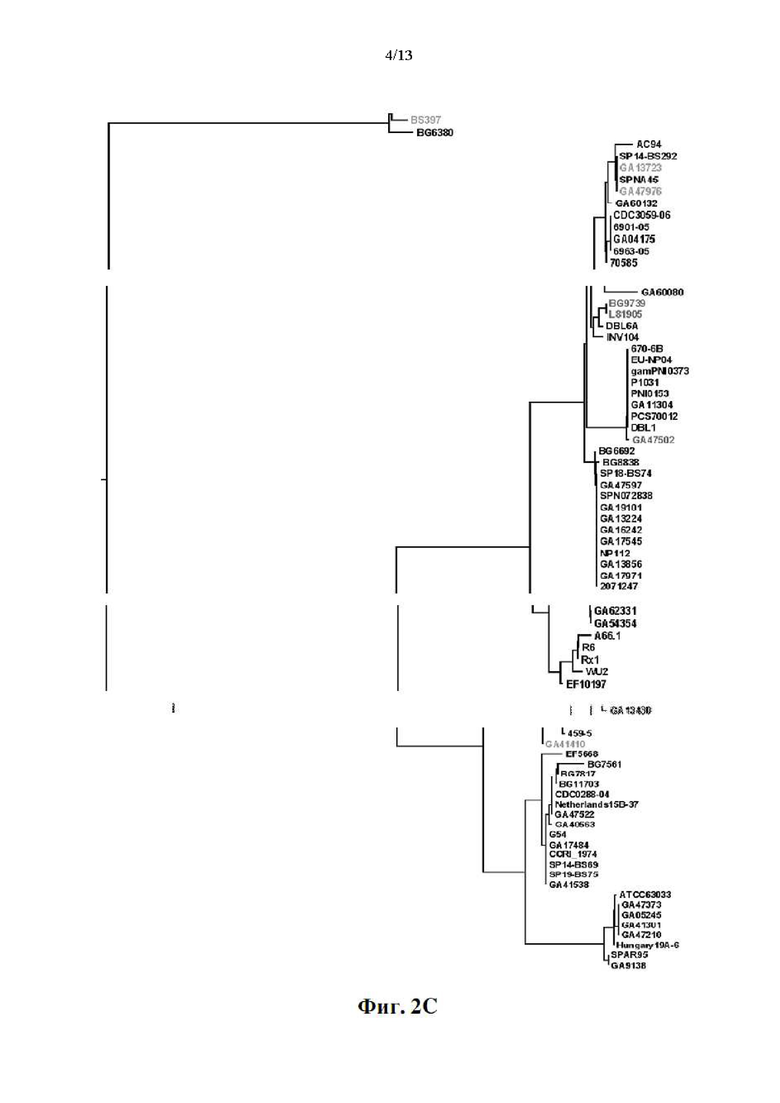

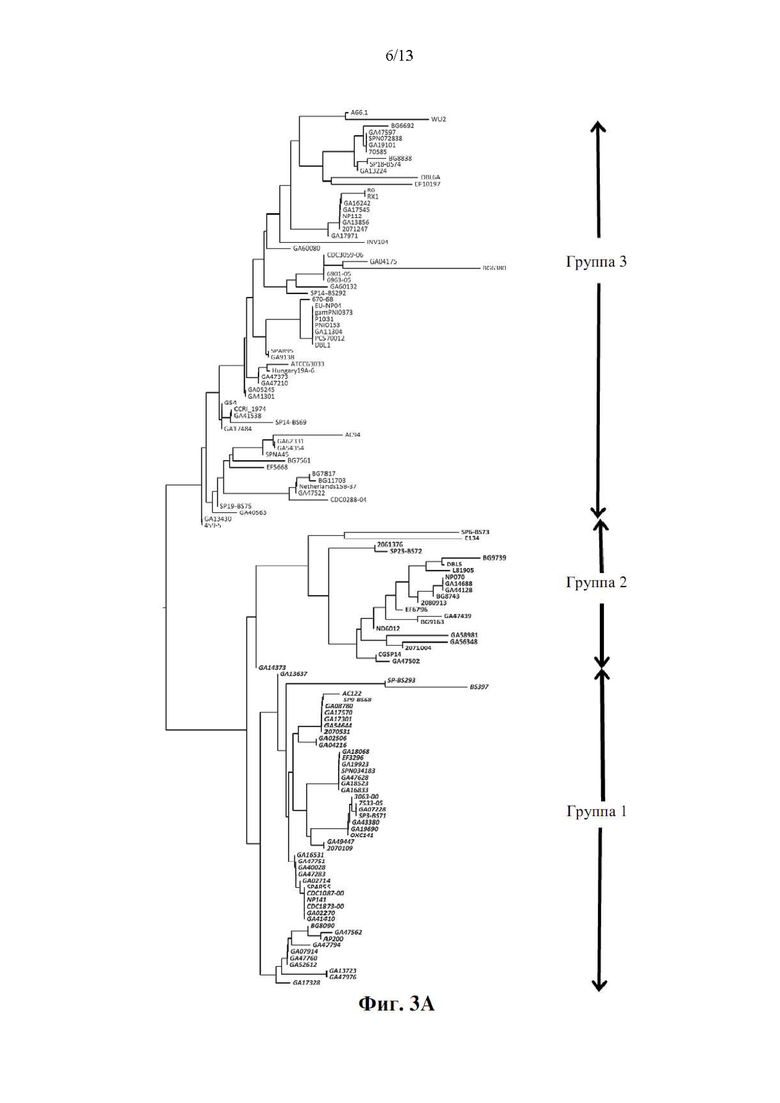
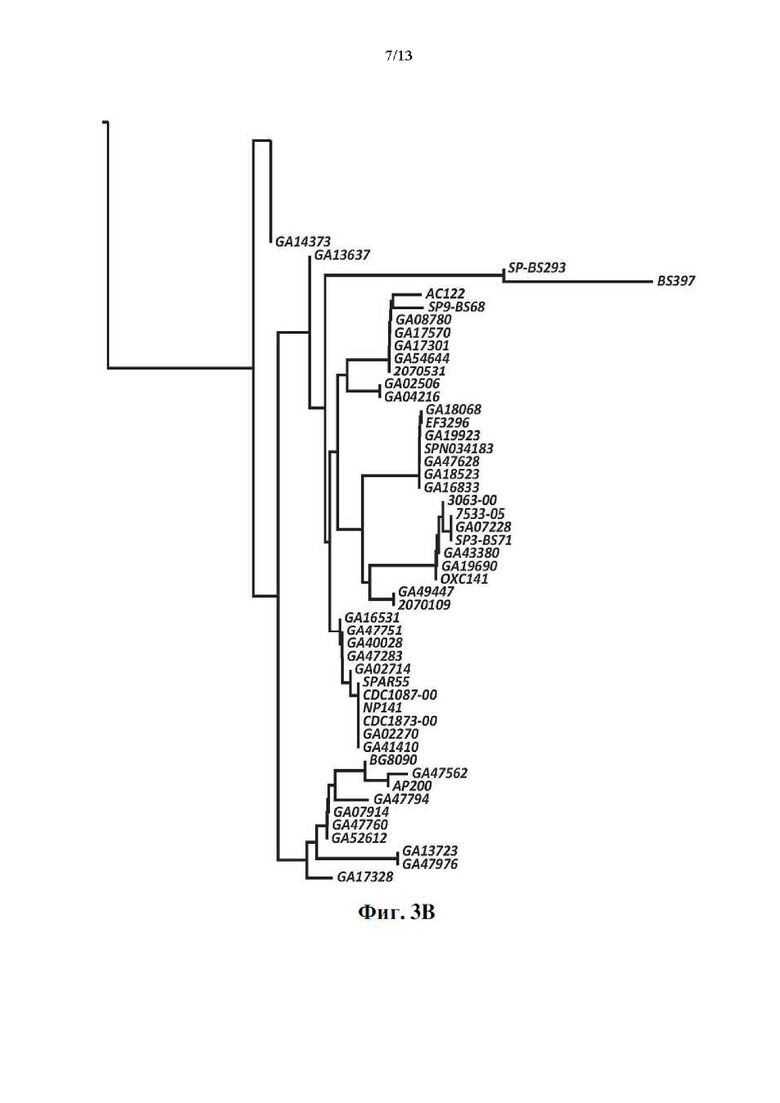
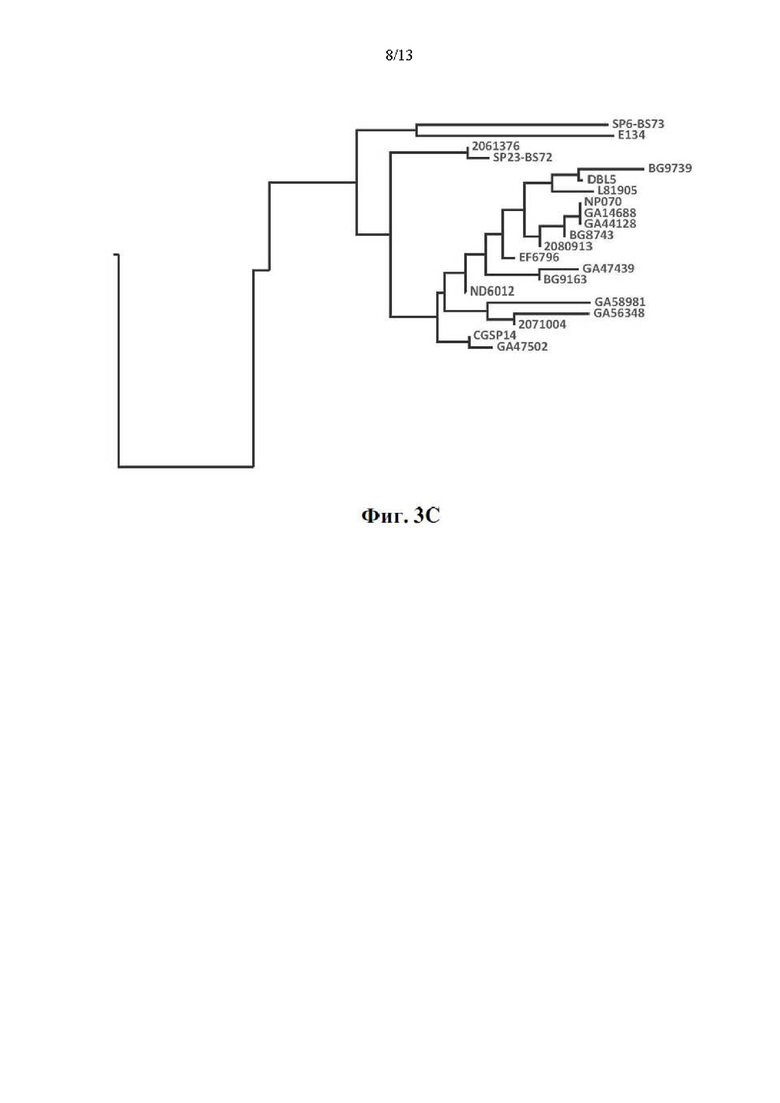
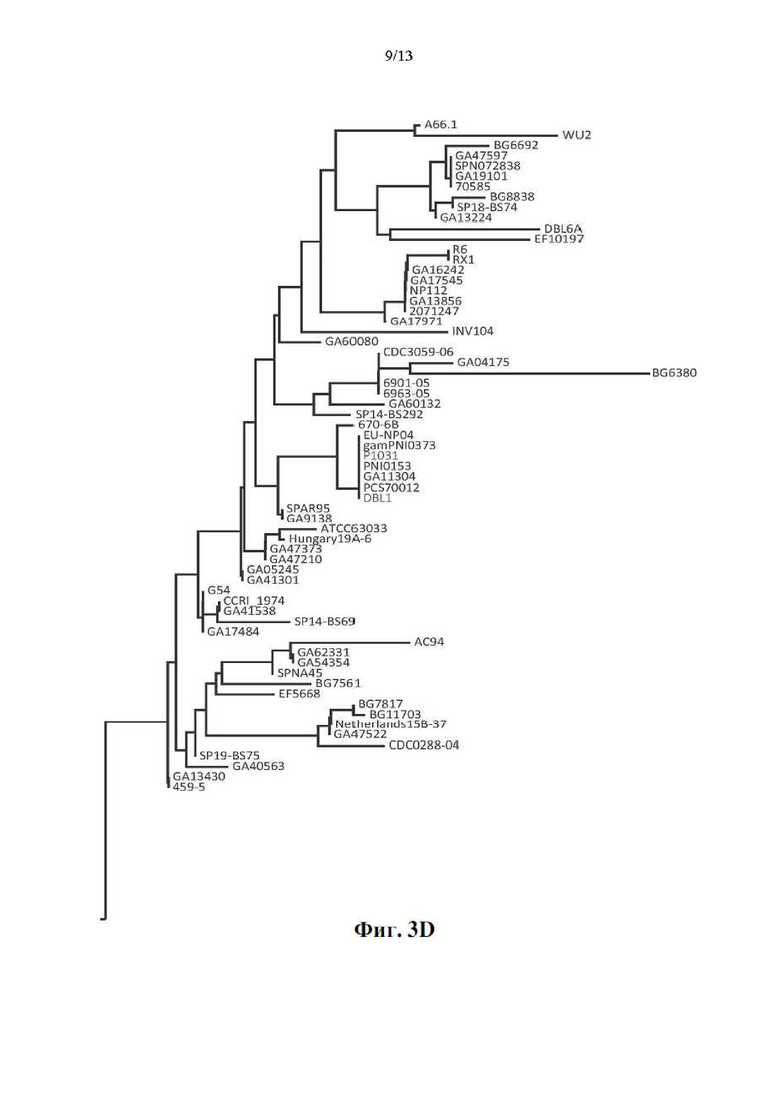
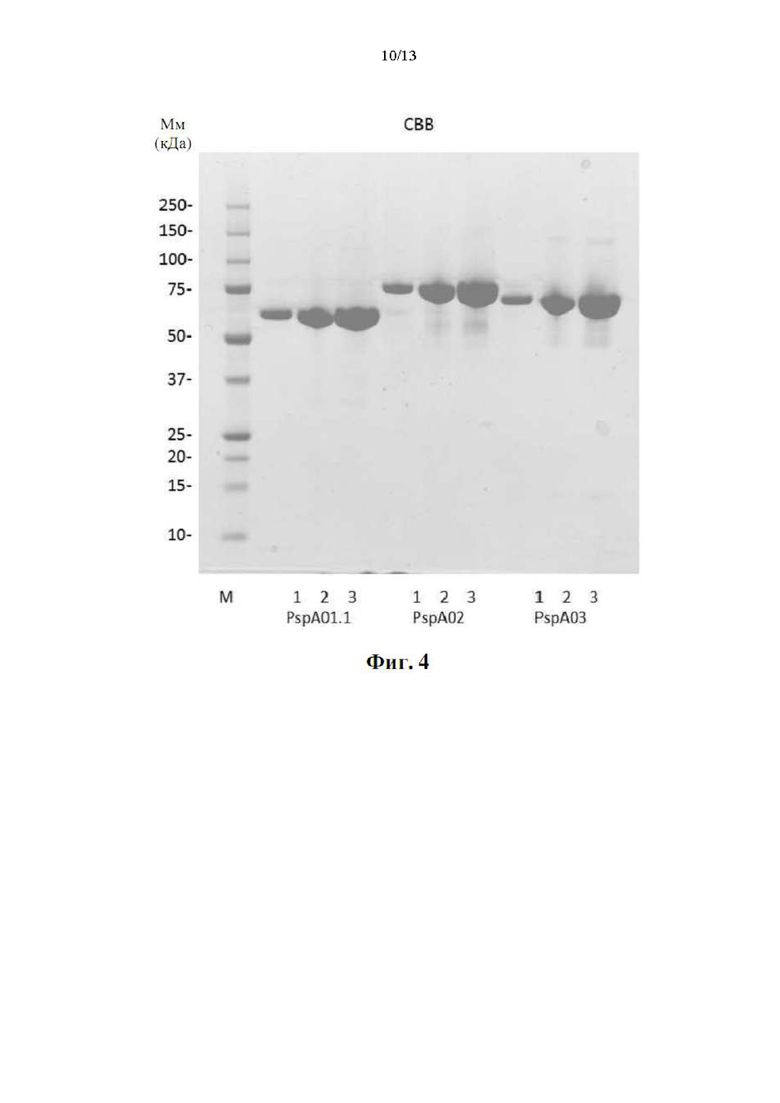
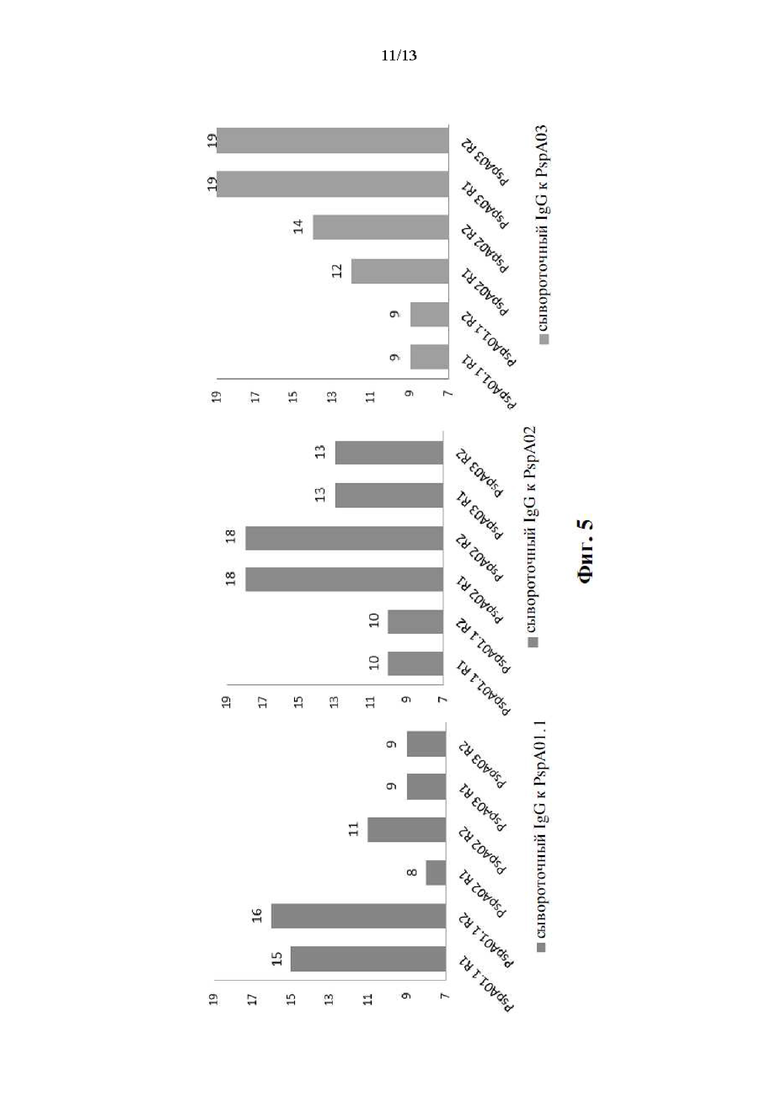
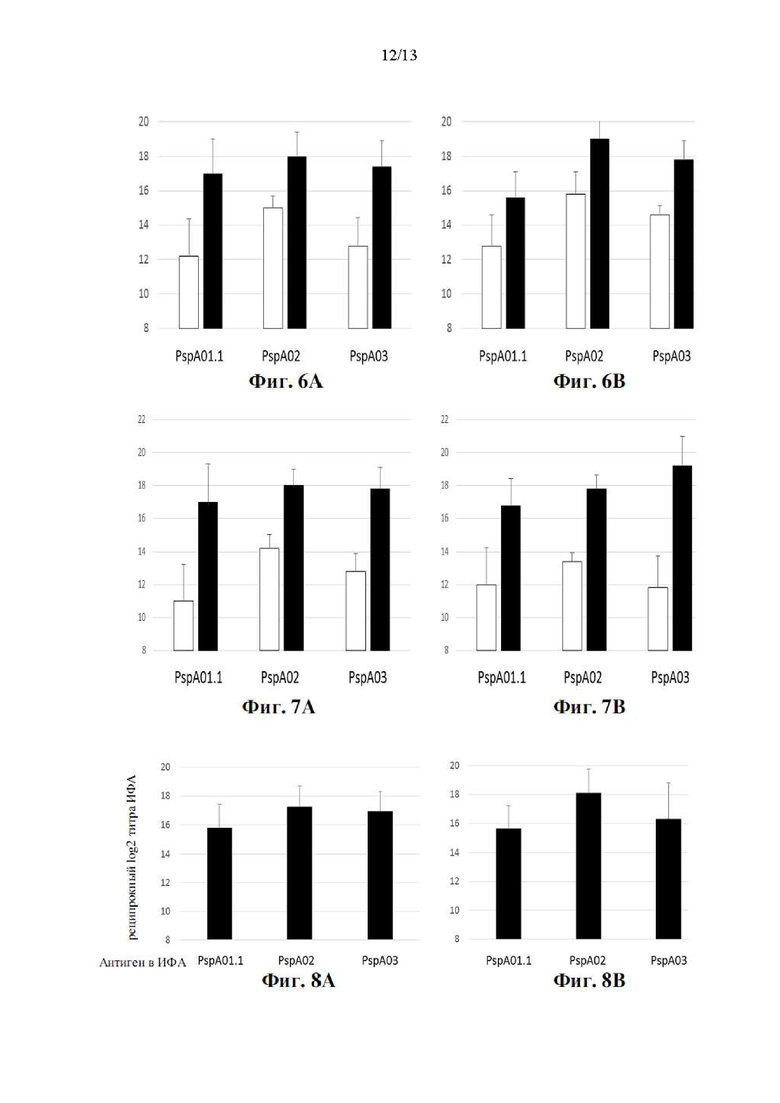
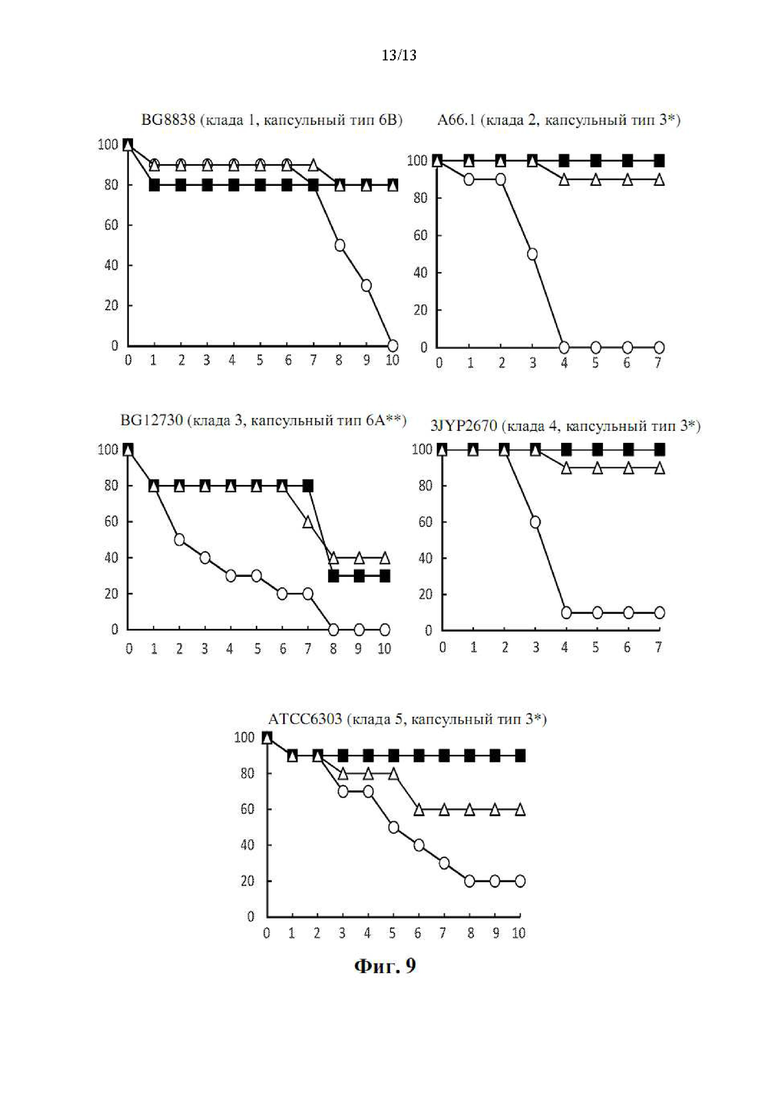
Изобретение относится к биотехнологии. Предложена композиция, являющаяся иммуногенной против пневмококкового заболевания, вызванного Streptococcus pneumoniae, содержащая по меньшей мере одну рекомбинантную конструкцию aHD-PRD, состоящую из альфа-спирального домена (aHD) и богатого пролином домена (PRD) пневмококкового поверхностного белка A Streptococcus pneumoniae (PspA), и по меньшей мере одно фармацевтически приемлемое вспомогательное вещество. Также предложены вакцина для индуцирования иммунного ответа против S. pneumonia, содержащая указанную композицию, рекомбинантная молекула нуклеиновой кислоты, которая кодирует конструкцию aHD-PRD, экспрессионный вектор и клетка-хозяин, содержащие такие молекулы, применение указанной композиции или указанной вакцины для максимизации перекрестной реактивности против патогенных пневмококков и обеспечения защиты от широкого спектра пневмококковых штаммов или серотипов, не включенных в указанную композицию или указанную вакцину. Изобретение обеспечивает максимизацию перекрестной реактивности и обеспечение защиты от широкого спектра пневмококковых серотипов. 7 н. и 5 з.п. ф-лы, 9 ил., 4 табл., 7 пр.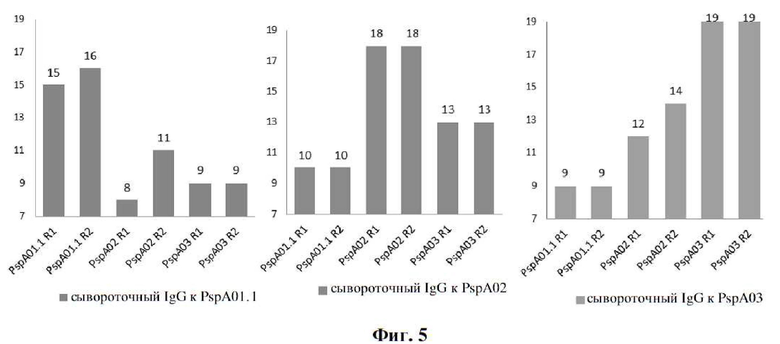
1. Композиция, являющаяся иммуногенной против пневмококкового заболевания, вызванного Streptococcus pneumoniae, содержащая по меньшей мере одну рекомбинантную конструкцию aHD-PRD, состоящую из альфа-спирального домена (aHD) и богатого пролином домена (PRD) пневмококкового поверхностного белка A Streptococcus pneumoniae (PspA), и по меньшей мере одно фармацевтически приемлемое вспомогательное вещество;
причем указанная конструкция aHD-PRD выбрана из группы, состоящей из конструкций, имеющих следующие последовательности:
- SEQ ID NO: 1, где последовательностью aHD является SEQ ID NO: 159, а последовательностью PRD является SEQ ID NO: 12;
- SEQ ID NO: 2, где последовательностью aHD является SEQ ID NO: 159, а последовательностью PRD является SEQ ID NO: 13;
- SEQ ID NO: 158, где последовательностью aHD является SEQ ID NO: 159, а последовательностью PRD является SEQ ID NO: 157;
- SEQ ID NO: 3, где последовательностью aHD является SEQ ID NO: 42, а последовательностью PRD является SEQ ID NO: 14;
- SEQ ID NO: 4, где последовательностью aHD является SEQ ID NO: 60, а последовательностью PRD является SEQ ID NO: 16;
причем указанная композиция является иммуногенной и не встречается в природе.
2. Вакцина для индуцирования иммунного ответа против S. pneumonia, содержащая композицию по п. 1.
3. Вакцина по п. 2, дополнительно содержащая адъювант.
4. Вакцина по п. 2 или 3, составленная для внутримышечного введения.
5. Вакцина по п. 2 или 3, составленная для введения через слизистую оболочку, причем введение через слизистую является интраназальным, пероральным или путем распыления в бронхи легких.
6. Вакцина по п. 2 или 3, содержащая по меньшей мере одну конструкцию aHD-PRD, заключенную в гидрофильный полисахарид для введения через слизистую оболочку, причем гидрофильный полисахарид представляет собой наногель, который содержит несущий катионную холестериновую группу пуллулан (cCHP).
7. Вакцина по п. 2 или 3, дополнительно содержащая по меньшей мере один дополнительный антиген, который усиливает защитный иммунный ответ против S. pneumonia.
8. Рекомбинантная молекула нуклеиновой кислоты, которая кодирует одну из указанных по меньшей мере одной рекомбинантной конструкции aHD-PRD по п. 1, где указанная рекомбинантная молекула нуклеиновой кислоты кодирует конструкцию aHD-PRD, выбранную из группы, состоящей из конструкций, имеющих следующие последовательности:
- SEQ ID NO: 1, где последовательностью aHD является SEQ ID NO: 159, а последовательностью PRD является SEQ ID NO: 12;
- SEQ ID NO: 2, где последовательностью aHD является SEQ ID NO: 159, а последовательностью PRD является SEQ ID NO: 13;
- SEQ ID NO: 158, где последовательностью aHD является SEQ ID NO: 159, а последовательностью PRD является SEQ ID NO: 157;
- SEQ ID NO: 3, где последовательностью aHD является SEQ ID NO: 42, а последовательностью PRD является SEQ ID NO: 14;
- SEQ ID NO: 4, где последовательностью aHD является SEQ ID NO: 60, а последовательностью PRD является SEQ ID NO: 16.
9. Экспрессионный вектор, содержащий рекомбинантную молекулу нуклеиновой кислоты по п. 8.
10. Клетка-хозяин, трансформированная вектором экспрессии по п. 9, для получения рекомбинантной конструкции aHD-PRG.
11. Применение композиции по п. 1 для максимизации перекрестной реактивности против патогенных пневмококков и обеспечения защиты от широкого спектра пневмококковых штаммов или серотипов, не включенных в указанную композицию.
12. Применение вакцины по любому из пп. 2-7 для максимизации перекрестной реактивности против патогенных пневмококков и обеспечения защиты от широкого спектра пневмококковых штаммов или серотипов, не включенных в указанную вакцину.
| US 2015032085 A1, 12.11.2015 | |||
| DANIELS C.C | |||
| ET AL | |||
| The Proline-Rich Region of Pneumococcal Surface Proteins A and C Contains Surface-Accessible Epitopes Common to All Pneumococci and Elicits Antibody-Mediated Protection against Sepsis | |||
| INFECTION AND IMMUNITY, May 2010, p | |||
| Способ изготовления окисных катодов | 1924 |
|
SU2163A1 |
| Парный автоматический сцепной прибор для железнодорожных вагонов | 0 |
|
SU78A1 |
| Кипятильник для воды | 1921 |
|
SU5A1 |
| HOLLINGSHEAD S.K | |||
| ET AL | |||
| Diversity of PspA: mosaic | |||
Авторы
Даты
2023-04-24—Публикация
2017-12-01—Подача