Изобретение относится к области медицинской диагностики, может быть использовано для прогнозирования риска развития сахарного диабета 2 типа у жителей Центральной России.
Сахарный диабет 2 типа представляет собой многофакторное генетически гетерогенное заболевание, формирующееся под воздействием наследственных и средовых факторов риска [A review of current trends with Type 2 diabetes epidemiology, aetiology, pathogenesis, treatments and future perspectives / J. Reed, S. Bain, V. Kanamarlapudi [et al.] // Diabetes, Metabolic Syndrome and Obesity: Targets and Therapy. - 2021. - Vol. 14. - P. 3567-3602]. Установлено, что у больных сахарным диабетом 2 типа имеют место нарушения в системе редокс-гомеостаза, характеризующиеся дефицитом продукции эндогенных антиоксидантов, в частности, глутатиона, и избыточным образованием свободных радикалов [Alnahdi, A. N-acetyl cysteine attenuates oxidative stress and glutathione-dependent redox imbalance caused by high glucose/high palmitic acid treatment in pancreatic Rin-5F cells / A. Alnahdi, A. John, H. Raza // PloS One. - 2019. - Vol. 14, Iss. 12. - Art. e0226696. - URL: https://doi.org/10.1371/journal.pone.0226696; Benáková, Š. Redox homeostasis in pancreatic β-cells: from development to failure / Š. Benáková, B. Holendová, L. Plecitá-Hlavatá // Antioxidants. - 2021. - Vol. 10, Iss. 4. - Art. 526. - URL: https://doi.org/10.3390/antiox10040526]. Данные литературы показывают, что способность поджелудочной железы к синтезу глутатиона значительно ниже, чем в других органах и тканях с высоким уровнем метаболической активности, таких как печень, скелетные мышцы и почки [Neuschwander-Tetri, B. A. Glutathione synthesis in the exocrine pancreas / B. A. Neuschwander-Tetri, M. E. Presti, L. D. Wells // Pancreas. - 1997. - Vol. 14, Iss. 4. - P. 342-349]. Как следствие, содержание глутатиона в поджелудочной железе определяется ассоциированными с мембранами ферментами, такими как гамма-глутамилтрансфераза GGT и аминопептидаза ANPEP, которые катализируют гидролиз глутатиона плазмы до входящих в его состав аминокислот и способствуют их транспортировке внутрь клетки [Githens, S. Glutathione metabolism in the pancreas compared with that in the liver, kidney, and small intestine / S. Githens // International journal of pancreatology. - 1991. - Vol. 8, Iss. 2. - P. 97-109]. По данным транскриптомного анализа GTex Portal, полиморфный вариант rs11073891 ассоциирован с изменением экспрессии гена ANPEP в широком спектре тканей, включая поджелудочную железу [https://www.gtexportal.org].
Известен cпособ прогнозирования риска развития сахарного диабета 2 типа, по патенту на изобретение EA030585B1 (публикация: 31.08.2018), включающий следующие этапы: определяют у пациента клинико-анамнестические и лабораторные данные, представляющие собой индекс массы тела (ИМТ); окружность талии (ОТ); наличие артериальной гипертензии (АГ); наличие сахарного диабета у близких родственников; триглицериды (ТГ); холестерин высокой плотности (ХС ЛВП); систолическое артериальное давление (САД) и/или диастолическое артериальное давление (ДАД); уровень сахара в крови, полученные значения оценивают с использованием балльной шкалы: ИМТ<25 кг/м2 - 0 баллов, 25-30 кг/м2 - 1 балл, >30 кг/м2 - 2 балла; ОТ у мужчин <94 см - 0 баллов, 94-102 см - 2 балла, >102 см - 3 балла; ОТ у женщин <80 см - 0 баллов, 80-88 см - 2 балла, >88 см - 3 балла; наличие АГ: нет - 0 баллов, да - 1 балл; наличие сахарного диабета у близких родственников: нет 0 баллов, да - 2 балла; выявление ТГ>1,7 ммоль/л: нет - 0 баллов, да - 1 балл; выявление ХС ЛВП>1,0 ммоль/л: нет - 1 балл, да - 0 баллов; показания САД>140 мм рт.ст. и/или ДАД>90 мм рт.ст.: нет - 0 баллов, да - 1 балл; уровень сахара в крови >5,6 ммоль/л: нет - 0 баллов, да - 3 балла, суммируют полученные баллы и при сумме баллов <8 прогнозируют низкий, а при сумме баллов >8 - высокий риск развития СД 2 типа у пациента в течение ближайших 10 лет.
Недостаток метода заключается в том, что он не учитывает индивидуальную генетическую предрасположенность к заболеванию и имеет ограничение прогноза риска развития сахарного диабета 2 типа во времени.
Известен способ прогнозирования развития сахарного диабета 2 типа у лиц, проживающих в Башкортостане (патент на изобретение RU 2 688 208 C1, дата публикации 21.05.2019), включающий выделение ДНК из лимфоцитов периферической венозной крови, генотипирование методом полимеразной цепной реакции синтеза ДНК, отличающийся тем, что проводят амплификацию участка rs2107538 гена хемокина CCL5 и участка rs6749704 гена хемокина CCL20 и при выявлении генотипов С/Т или Т/Т полиморфного локуса rs2107538 гена CCL5 или генотипа С/С полиморфного локуса rs6749704 гена CCL20 прогнозируют риск развития сахарного диабета 2 типа у обследуемого.
Недостаток метода заключается в том, что он может быть использован только для жителей Башкортостана и непригоден для прогнозирования риска развития сахарного диабета 2 типа у жителей других регионов России ввиду имеющихся межэтнических генетических различий в частотах минорных аллелей однонуклеотидных полиморфизмов и величин неравновесия по сцеплению между ними.
Известен способ прогнозирования риска развития сахарного диабета 2 типа у больных гипертонической болезнью по патенту на изобретение RU 2521202 (дата публикации 27.06.2014), включающий забор образца периферической венозной крови, выделение ДНК и анализ полиморфизма гена лимфотоксина α (+250G/A Ltα), по результатам которого прогнозируют риск развития сахарного диабета 2 типа у больных гипертонической болезнью: высокий - в случае обнаружения аллеля +250G Ltα, низкий - в случае обнаружения генотипа +250А/A Ltα.
Однако данный способ не пригоден для выявления предрасположенности к развитию сахарного диабета 2 типа у лиц без гипертонической болезни.
Наиболее близок по результату исследования способ ранней генетической диагностики риска развития сахарного диабета 2 типа (патент на изобретение RU2655635C1, дата публикации 29.05.2018), включающий экстракцию ДНК из периферической крови с последующим проведением полимеразной цепной реакции в режиме реального времени, характеризующийся тем, что проводят анализ полиморфизма гена рецептора к инкретинам GLP-1R и прогнозируют пониженный риск развития СД 2 типа в результате выявления генотипа GG полиморфизма rs6923761 гена GLP-1R.
Недостатком описанного способа является малый размер выборки пациентов с сахарным диабетом 2 типа (n=87) и здоровых лиц (n=109) и, как следствие, низкая статистическая мощность исследования.
Технический результат заключается в получении критериев оценки риска развития сахарного диабета 2 типа у жителей Центральной России по данным о генетическом полиморфизме rs11073891 (A>C).
Технический результат достигается тем, что после экстракции ДНК проводят анализ полиморфного варианта гена аминопептидазы ANPEP rs11073891 (А>С) и прогнозируют повышенный риск формирования сахарного диабета 2 типа у жителей Центральной России в случае выявления генотипа rs11073891-А/А, а при обнаружении генотипов rs11073891-А/С или rs11073891-С/С - низкий риск развития сахарного диабета 2 типа.
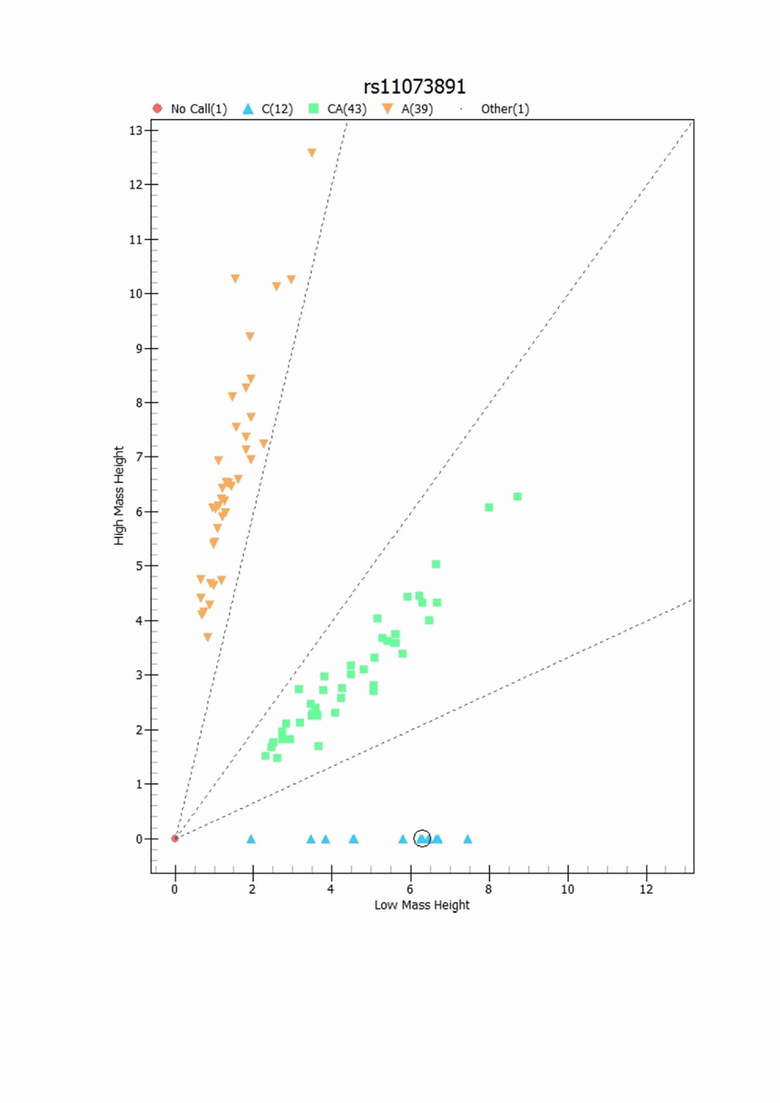
Изобретение поясняется следующей фигурой: дискриминация генотипов по локусу гена ANPEP rs11073891 при генотипировании на основе масс-спектрометрии: генотипы rs11073891-C/С показаны голубым цветом, генотипы rs11073891-A/C показаны зеленым цветом, генотипы rs11073891-A/A показаны оранжевым цветом.
Способ осуществляют следующим образом:
1. Выделение ДНК из периферической венозной крови. На первом этапе к 0,5 мл крови добавляли 0,5 мл PBS и центрифугировали 10 мин при 12 тыс. об/мин. Надосадочную жидкость сливали, добавляли 1 мл PBS и вновь центрифугировали при тех же условиях. Надосадочную жидкость сливали, добавляли 200 мкл ТЕ-буфера, пипетировали до растворения осадка и затем последовательно добавляли 10 мкл 1% раствора додецилсульфата натрия SDS и 5 мкл протеиназы К. Пробирки инкубировали в термостате при t=37°C 12 ч. В ходе второго этапа проводили четыре последовательных центрифугирования с фенолом и хлороформом согласно протоколу методики (10 мин, 8 тыс. об/мин), после чего ДНК осаждали ледяным раствором 95% этилового спирта и центрифугировали 10 мин при 14,3 тыс. об/мин. По испарении спирта ДНК растворяли в 100 мкл деионизированной дистиллированной воды. Получаемый раствор ДНК в воде имел чистоту в диапазоне А260/280=1,5-2,0 и среднюю концентрацию около 180-200 нг/мкл.
Экстракция геномной ДНК из цельной крови колоночным методом проводилась с помощью набора QIAamp DNA blood mini kit (QIAGEN, Германия) на автоматической станции QiaCube (QIAGEN, Германия). Роботизированный протокол продолжительностью 58 минут включал этап лизиса клеток 0,2 мл цельной крови с помощью лизирующего буфера и протеиназы К QIAGEN, инкубирование, перенос лизата в колонку, связывание ДНК с мембраной колонки, центрифугирование, двукратное промывание колонки буфером AW1 и AW2, центрифугирование колонки и, наконец, элюирование очищенной ДНК. Получаемый раствор ДНК в воде имел идеальную чистоту А260/280=1,7-1,9 и среднюю концентрацию около 40-50 нг/мкл. Экстрагированные из крови образцы ДНК хранились в морозильниках Thermo Fisher Scientific (США) при -20°С.
2. Подготовка образцов ДНК к масс-спектрометрическому анализу. Качество выделенной ДНК оценивали по степени чистоты и концентрации раствора на спектрофотометре NanoDrop (Thermo Fisher Scientific, США). Все анализируемые образцы ДНК были разведены деионизированной водой до концентрации 10 нг/мкл при А260/280=1,5-2,0.
3. Анализ полиморфизма гена ANPEP - генотипирование методом матрично-активированной лазерной десорбционно-ионизационной масс-спектрометрии MALDI-TOF. Использовали следующие последовательности праймеров: прямой F: 5`- ACGTTGGATGTAGGGCAGAATAGGACTTGG -3`, обратный R: 5`-ACGTTGGATGTTCCTCCTCTGTGAAGTTTC-3`, праймер удлинения E: 5`-CTCTGTGAAGTTTCAGATCTAA-3`. Для приготовления ПЦР-микса (в расчете на один спектральный чип) в центрифужную микропробирку вносили 80,6 мкл ddH2O, 50,4 мкл 10x буфера, 40,3 мкл MgCl2 (концентрация 25 ммоль/л), 10,1 мкл смеси дНТФ (концентрация 25 ммоль/л), 100,8 мкл смеси ПЦР-праймеров (концентрация 0,5 мкмоль/л) и 20,16 мкл HotStartTaq полимеразы (концентрация 5 ЕД/мкл). Смесь вортексировали и раскапывали в 96-луночный ПЦР-планшет по 3 мкл в лунку, после чего с помощью восьмиканального дозатора вносили по 2 мкл ДНК (концентрация 10 нг/мкл). Планшет заклеивали, центрифугировали 20 сек при 1000 об/мин и загружали в термоциклер CFX96 Bio-Rad на 125 мин при следующем режиме: денатурация 2 мин при 95°С, амплификация 44 цикла, состоящая из денатурации 30 сек при 95°С, отжига 30 сек при 56°С и элонгации 60 сек при 72°С. После чего пробы инкубировали 5 мин при 72°С. Не прореагировавшие в ходе ПЦР дНТФ удаляли с помощью реакции SAP (shrimp alkaline phosphatase), в ходе которой щелочная фосфатаза креветки гидролизовала дНТФ до нуклеозидов и фосфатов. Для приготовления SAP-микса в микропробирке смешивали 161,6 мкл ddH2O, 18 мкл 10хTS буфера и 31,7 мкл SAP фермента. Далее вносили по 2 мкл SAP-смеси в каждую лунку, планшет заклеивали, центрифугировали 20 сек при 1000 об/мин и загружали в термоциклер CFX96 Bio-Rad на 55 мин при следующем режиме: 45 мин при 37°С и 10 мин при 85°С. Для проведения третьей реакции iPLEX готовили Е-праймер-микс из расчета 8,8 мкл праймеров Е1-Е9, 11,7 мкл праймеров Е10-Е18, 14,6 мкл праймеров Е19-Е27, 17,5 мкл праймеров Е28-Е35 и 45,1 мкл ddH2O. После масс-спектрометрической оценки интенсивности пиков Е-праймеров в полученной смеси, в микс добавляли Е-праймеры в количествах, необходимых для достижения одинаковой интенсивности сигнала. Для приготовления iPLEX-микса в микропробирке смешивали 65,4 мкл ddH2O, 21,2 мкл iPLEX буфера, 21,2 мкл терминирующей смеси, 99,3 мкл Е-праймер-микса и 4,33 мкл iPLEX-фермента, вортексировали и раскапывали в лунки по 2 мкл. Планшет заклеивали, центрифугировали 20 секунд при 1000 об/мин и загружали в термоциклер CFX96 Bio-Rad на 135 мин при следующем режиме: денатурация 30 сек при 94°С, затем 40 циклов, состоящие из денатурации 5 сек при 94°С, отжига 5 сек при 52°С, элонгации 5 сек при 80°С, с последующим инкубированием в течение 3 мин при 72°С. По завершении реакции iPLEX, планшет охлаждали до +4°С, добавляли по 30 мкл воды во все лунки, центрифугировали 1 мин при 1000 об/мин и загружали в масс-спектрометр. Ввиду того, что небольшие полярные молекулы и положительно заряженные катионы натрия и калия могут образовывать аддукты с олигонуклеотидами и создавать серию контаминантных пиков, ампликоны были подвергнуты роботизированному обессоливанию путем их обработки смолой SpectroCLEAN (Agena Bioscience). Перенос образцов на спектральный чип с матрицей для ионизации осуществлялся в автоматическом режиме на рабочей станции Nanodispenser. Пример кластерного распределения генотипов по SNP rs11073891 в результате масс-спектрометрического анализа на геномном масс-спектрометре MassArray analyzer 4 (Agena Bioscience) показан на фигуре 1. Статистические расчеты проводили с помощью программы SNPStats [https://www.snpstats.net/].
4. Прогнозирование повышенного риска развития сахарного диабета 2 типа в случае выявления генотипа rs11073891-А/А и пониженного риска развития этого заболевания при выявлении генотипов rs11073891-А/С или rs11073891-С/С.
Возможность использования предложенного способа для определения риска развития сахарного диабета 2 типа у жителей Центральной России подтверждает анализ результатов наблюдений 2555 лиц, у 1450 из которых установлен сахарный диабет 2 типа. В исследование включались лица славянской национальности Центральной России. Диагноз СД2 был установлен врачами-эндокринологами ОБУЗ ГК БСМП на основе клинического и лабораторно-инструментального обследования. Установлено, что генотип rs11073891-A/A значимо чаще встречался в группе больных (31,2%) по сравнению с контролем (22,3%) и ассоциировался с повышенным риском развития СД2: OR=1,58, 95% CI=1,32-1,89, P<0,0001 (таблица 1). Генотипы rs11073891-A/С и rs11073891-С/С значимо чаще встречались у здоровых лиц (77,7%) по сравнению пациентами с СД2 (68,8%). Носительство генотипов rs11073891-A/С и rs11073891-С/С ANPEP ассоциировалось с пониженным риском развития сахарного диабета 2 типа: OR=0,63, 95% CI 0,53-0,76, P<0,0001 (таблица 1).
В качестве примеров конкретного применения разработанного способа приведено генетическое обследование лиц славянского происхождения, уроженцев Центральной России и не являющихся родственниками между собой: проведено генетическое обследование по локусу rs11073891 (А>С) гена ANPEP.
Пациент Г., мужчина 46 лет, проходил медосмотр в поликлинике ОБУЗ «Курской городской клинической больницы скорой медицинской помощи» 23.12.2016 г. При анализе крови натощак была выявлена гипергликемия 5,9 ммоль/л, в связи с чем мужчина был направлена на консультацию к эндокринологу. Результаты перорального глюкозотолерантного теста с 75 г глюкозы соответствовали норме, однако в связи с наличием факторов риска сахарного диабета 2 типа, а именно, отягощенной наследственности (сахарным диабетом 2 типа болеет мать), избыточной массы тела, сидячего образа жизни, высококалорийного питания, пациенту было рекомендовано выполнение тестирования для оценки генетического риска развития заболевания. У пациента Г. была взята венозная кровь, при генотипировании полиморфного локуса rs11073891 (А>С) ANPEP был выявлен генотип rs11073891-А/А, что позволило отнести мужчину в группу лиц с высоким риском развития сахарного диабета 2 типа. Тем не менее, профилактические мероприятия по снижению массы тела, коррекции питания и образа жизни мужчиной не проводились. Три года спустя пациент Г. был госпитализирован с жалобами на сухость во рту, жажду и частое мочеиспускание в эндокринологическое отделение ОБУЗ КГКБ СМП, где он находился на стационарном лечении с 04.10.2019 г. по 18.10.2019 г. с диагнозом: сахарный диабет, 2 тип, впервые выявленный, фаза декомпенсации от 04.10.2019 г., фаза компенсации от 18.10.2019 г. Кетоз от 04.10.2019 г. Индивидуальный целевой уровень HbA1c<7,0%. Целевой уровень гликемии плазмы натощак <7,0 ммоль/л, через 2 ч после еды <9,0 ммоль/л. Биохимический анализ крови подтвердил наличие у мужчины сахарного диабета 2 типа: была выявлена гипергликемия натощак 31 ммоль/л и повышенный уровень гликированного гемоглобина 18,9%.
Донор-доброволец К., женщина 46 лет, обратилась в ОБУЗ «Курская областная клиническая станция переливания крови» комитета здравоохранения Курской области 12.07.2016 г. для сдачи крови. Пациентке было предложено принять участие в научном исследовании для выявления генетической предрасположенности к сахарному диабету 2 типа. У женщины была взята венозная кровь, при генотипировании полиморфного локуса rs11073891 (А>С) ANPEP был выявлен генотип rs11073891-А/С, что позволило отнести женщину в группу лиц с низким риском развития сахарного диабета 2 типа. Анализ крови подтвердил факт отсутствия нарушений углеводного обмена: концентрация глюкозы крови натощак 4,2 ммоль/л, гликированный гемоглобин 5,1%, что соответствует норме. Дальнейшее наблюдение не выявило диагноз сахарного диабета 2 типа.
Пациентке В., женщине 52 лет, при прохождении профилактического осмотра на базе поликлиники ОБУЗ «Курской городской клинической больницы скорой медицинской помощи» 27.11.2018 г. было предложено пройти тестирование на предмет предрасположенности к сахарному диабету 2 типа в связи с имеющимися факторами риска - избыточной массой тела, курением и отягощенной наследственностью по диабету (сахарным диабетом 2 типа страдает мать). У женщины была взята венозная кровь, при генотипировании полиморфного варианта rs11073891 (А>С) ANPEP был выявлен генотип rs11073891-С/С, что позволило отнести пациентку в группу лиц с низким риском развития сахарного диабета 2 типа. Дальнейшее наблюдение не выявило диагноз сахарного диабета 2 типа.
Применение данного способа позволит на доклиническом этапе формировать среди жителей Центральной России группы риска и своевременно реализовывать в этих группах необходимые лечебно-профилактические мероприятия по предупреждению развития сахарного диабета 2 типа.
Резюме
Таким образом, полученные данные свидетельствуют о том, что аллель rs11073891-A гена ANPEP является генетическим фактором риска развития сахарного диабета 2 типа (OR=1,38, Р<0,0001) у жителей Центральной России.
Использование предложенного способа позволит прогнозировать развитие сахарного диабета 2 типа у жителей Центральной России, что даст возможность осуществлять мероприятия по профилактике данного заболевания - регулярный контроль уровня глюкозы в крови, нормализацию массы тела, достаточную физическую активность, правильное питание с ежедневным включением в рацион свежих овощей и фруктов и ограничением рафинированных углеводов и жиров.
Изобретение относится к медицине, а именно к медицинской диагностике, и может быть использовано для прогнозирования риска развития сахарного диабета 2 типа у жителей Центральной России. Осуществляют забор образца периферической венозной крови и экстракцию ДНК. Проводят анализ полиморфного варианта гена аминопептидазы ANPEP rs11073891 (А>С). В случае выявления генотипа rs11073891-А/А прогнозируют повышенный риск развития сахарного диабета 2 типа. При обнаружении генотипов rs11073891-А/С или rs11073891-С/С прогнозируют низкий риск развития сахарного диабета 2 типа. Способ обеспечивает получение новых критериев оценки риска развития сахарного диабета 2 типа у жителей Центральной России по данным о генетическом полиморфизме rs11073891 (A>C). 1 ил., 1 табл., 3 пр.
Способ прогнозирования риска развития сахарного диабета 2 типа у жителей Центральной России, включающий забор образца периферической венозной крови, отличающийся тем, что после экстракции ДНК проводят анализ полиморфного варианта гена аминопептидазы ANPEP rs11073891 (А>С) и прогнозируют повышенный риск развития сахарного диабета 2 типа в случае выявления генотипа rs11073891-А/А, а при обнаружении генотипов rs11073891-А/С или rs11073891-С/С – низкий риск развития сахарного диабета 2 типа.
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ САХАРНОГО ДИАБЕТА ВТОРОГО ТИПА У БОЛЬНЫХ ГИПЕРТОНИЧЕСКОЙ БОЛЕЗНЬЮ | 2013 |
|
RU2521202C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ САХАРНОГО ДИАБЕТА 2 ТИПА У НАСЕЛЕНИЯ БАШКОРТОСТАНА | 2018 |
|
RU2688208C1 |
| СПОСОБ РАННЕЙ ГЕНЕТИЧЕСКОЙ ДИАГНОСТИКИ РИСКА РАЗВИТИЯ САХАРНОГО ДИАБЕТА 2 ТИПА | 2017 |
|
RU2655635C1 |
| WO 2011115955 A1, 22.09.2011 | |||
| LIGTHART S | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Erasmus University Rotterdam | |||
| Способ восстановления спиралей из вольфрамовой проволоки для электрических ламп накаливания, наполненных газом | 1924 |
|
SU2020A1 |
| Способ приготовления консистентных мазей | 1912 |
|
SU350A1 |
Авторы
Даты
2023-09-18—Публикация
2023-03-06—Подача