Изобретение относится к области медицинской диагностики, может быть использовано для прогнозирования риска развития диабетической нефропатии у пациентов Центральной России с сахарным диабетом 2 типа и нормальной массой тела.
Дефицит эндогенно синтезирующихся антиоксидантов, таких как глутатион, играет важную роль в развитии сахарного диабета 2 типа и его микрососудистых осложнений, в частности, диабетической нефропатии [Oxidative stress and inflammation in renal and cardiovascular complications of diabetes / A. Charlton, J. Garzarella, K. A. Jandeleit-Dahm, J. C. Jha // Biology. - 2021. - Vol. 10, Iss. 1. - Art. 18. - URL: https://doi.org/10.3390/biology10010018 (date of the application: 23.06.2023)]. Фермент аминопептидаза, кодируемая геном ANPEP, катализирует расщепление конъюгатов глутатиона на составляющие их аминокислоты с целью последующего транспорта аминокислот внутрь клеток и ресинтеза новых копий молекул глутатиона [Hypericum perforatum L. regulates glutathione redox stress and normalizes Ggt1/Anpep signaling to alleviate ovx-induced kidney dysfunction / Y.R. Liu, N.J. Yang, M.L. Zhao [et al.] // Frontiers in Pharmacology. - 2021. - Vol. 12. - Art. 628651. - URL: https://doi.org/10.3389/fphar.2021.628651 (date of the application: 23.06.2023)]. По данным транскриптомного анализа GTex Portal полиморфные варианты rs9920421 и rs4932143 ассоциированы с изменением экспрессии гена ANPEP в широком спектре тканей, включая поджелудочную железу и почки [https://www.gtexportal.org].
Известен способ прогнозирования формирования микрососудистых осложнений сахарного диабета 2 типа с помощью клинико-анамнестических и лабораторных данных (патент на изобретение RU2741715C1, дата публикации 28.01.2021), отличающийся тем, что у больного СД 2 типа определяют возраст, стаж диабета, а также уровни креатинина, ACT, общего холестерина, постпрандиальной гликемии, скорость клубочковой фильтрации, содержание гликированного гемоглобина, индекс атерогенности; при сочетании таких факторов, как возраст старше 57,7 лет, стаж диабета более 10,3 лет, уровень постпрандиальной гликемии более 7,9 ммоль/л, содержание общего холестерина выше 5,05 ммоль/л, прогнозируют развитие микрососудистого осложнения СД 2 типа в виде диабетической ретинопатии; при сочетании факторов - возраст старше 63 лет, стаж диабета больше 8 лет, уровень креатинина более 94,17 мкмл/л, скорость клубочковой фильтрации ниже 77,4 мл/мин/1,73 м2, уровень гликированного гемоглобина (НbА1c) выше 9,58%, показатель индекса атерогенности выше 3,7% и уровень ACT более 21,4 ед/л - прогнозируют развитие микрососудистого осложнения СД 2 типа в виде диабетической нефропатии.
Недостаток метода заключается в том, что не рассматривается связь генетических полиморфизмов и их сочетаний с риском развития диабетической нефропатии у пациентов с сахарным диабетом 2 типа.
Известен способ прогнозирования диабетической нефропатии у больных сахарным диабетом 1 типа (по патенту на изобретение RU2200328C1, дата публикации: 10.03.2003), включающий определение прогностических факторов риска, отличающийся тем, что исследуют исходные значения соотношения систолодиастолических скоростей (Vmax/Vmin) в дуговых почечных артериях, гликозилированного гемоглобина (HbAlC) в %, диастолического артериального давления (АДд) в мм рт. ст., триглицеридов (ТГ) сыворотки крови в ммоль/л, решают дискриминантное уравнение: Д= -207,116•Vmax/Vmin-28,659•HbА1С-3,068•АДд-20,079•ТГ и при величине Д меньше -844,07 прогнозируют развитие диабетической нефропатии в течение года.
Недостаток метода заключается в том, что он разработан пациентов с сахарным диабетом 1 типа и не может быть использован для прогнозирования риска развития диабетической нефропатии у пациентов с сахарным диабетом 2 типа.
Известен способ диагностики нарушений компенсации обмена веществ и прогнозирования риска развития осложнений у больных сахарным диабетом 2 типа с помощью оценки апоптоза лимфоцитов по патенту на изобретение РФ №2452965 (дата публикации 10.06.2012), включающий забор периферической венозной крови и определение процентного содержания апоптотических лимфоцитов An+/PI-, при значении содержания лимфоцитов An+/PI- ниже 3,5% диагностируется состояние компенсации углеводного обмена и прогнозируется благоприятное течение заболевания на ближайший год, при содержании лимфоцитов An+/PI- в пределах от 3,5 до 6% диагностируется состояние субкомпенсации и прогнозируется умеренный риск развития осложнений, уровень лимфоцитов An+/PI- выше 6% характеризует состояние декомпенсации и высокий риск развития хронических осложнений сахарного диабета.
Недостаток метода заключается в том, что с его помощью можно спрогнозировать только риск развития осложнений, но невозможно спрогнозировать, какое именно осложнение может быть у конкретного пациента.
Наиболее близок по результату исследования способ прогнозирования риска развития ангиопатии нижних конечностей у больных сахарным диабетом 2-го типа (патент на изобретение RU 2507520, дата публикации 20.02.2014), включающий выделение ДНК из периферической венозной крови, отличающийся тем, что проводят анализ полиморфизма гена фактора некроза опухоли -308G/A TNFα и прогнозируют повышенный риск развития ангиопатии нижних конечностей у больных сахарным диабетом 2-го типа в случае выявления аллеля -308A TNFα.
Однако данный способ не способен выявить предрасположенность к развитию диабетической нефропатии у пациентов с сахарным диабетом 2 типа и нормальной массой тела.
Технический результат заключается в получении критериев оценки риска формирования диабетической нефропатии у пациентов Центральной России с сахарным диабетом 2 типа и нормальной массой тела по данным о генетических полиморфизмах rs9920421 (A>G) и rs4932143 (С>G).
Технический результат достигается тем, что после экстракции ДНК проводят анализ полиморфных вариантов гена аминопетидазы ANPEP rs9920421 (A>G) и rs4932143 (С>G) и прогнозируют повышенный риск формирования диабетической нефропатии у пациентов Центральной России с сахарным диабетом 2 типа и нормальной массой тела в случае выявления сочетания аллеля G rs9920421 с аллелем G rs4932143, а при обнаружении сочетания аллеля А rs9920421 с аллелем С rs4932143 - низкий риск развития диабетической нефропатии у пациентов Центральной России с сахарным диабетом 2 типа и нормальной массой тела.
Изобретение поясняется следующими фигурами:
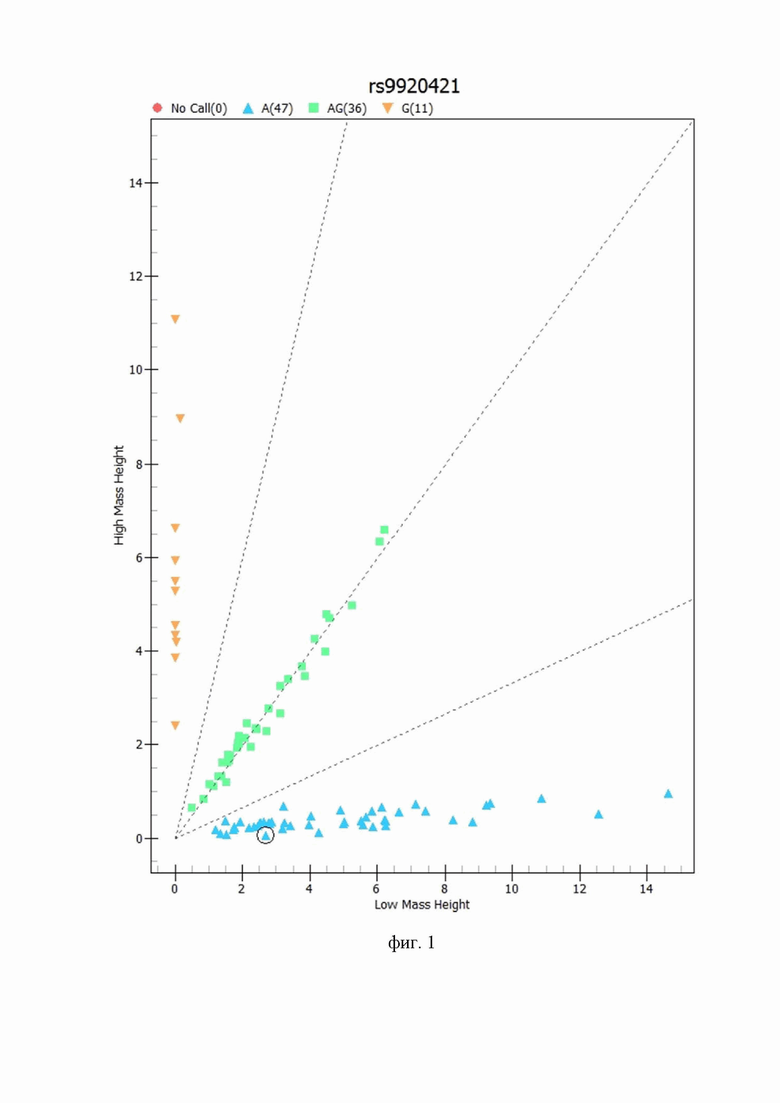
На фиг.1 показана дискриминация аллелей по локусу гена ANPEP rs9920421 при генотипировании на основе масс-спектрометрии: аллель G rs9920421 показан оранжевым цветом, гетерозиготное носительство аллелей A и G rs9920421 показано зеленым цветом, аллель A rs9920421 показан голубым цветом.
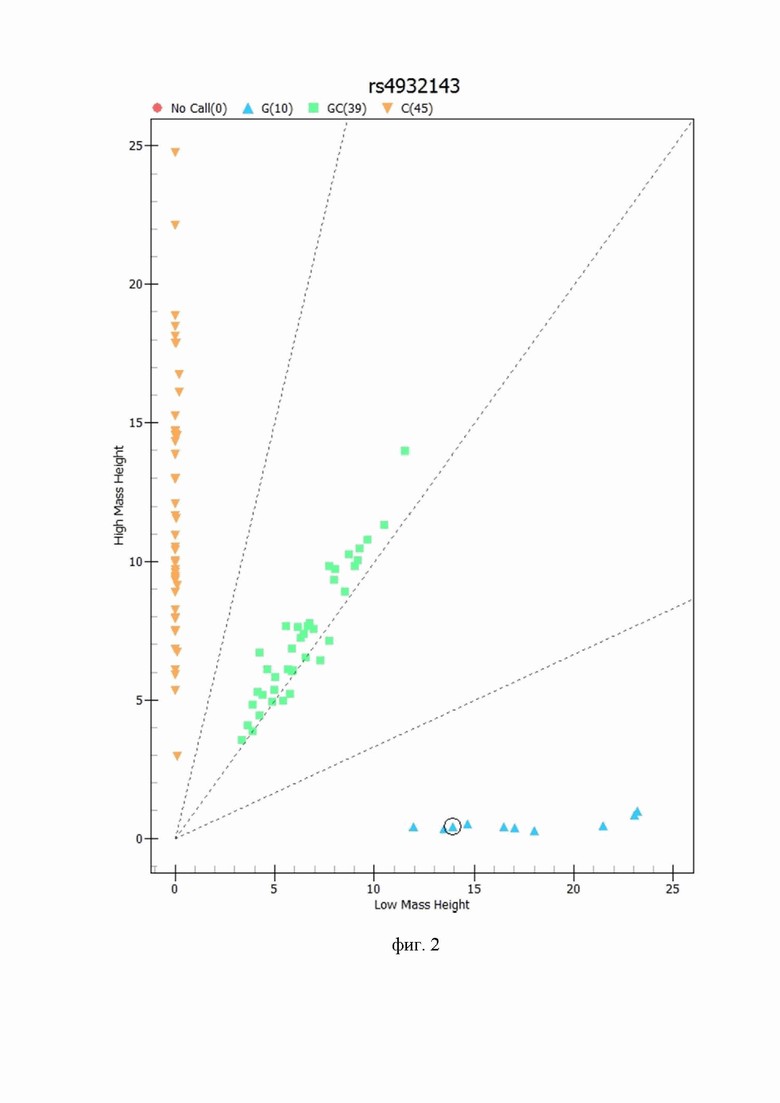
На фиг.2 показана дискриминация аллелей по локусу гена ANPEP rs4932143 при генотипировании на основе масс-спектрометрии: аллель С rs4932143 показан оранжевым цветом, гетерозиготное носительство аллелей С и G rs4932143 показано зеленым цветом, аллель G rs4932143 показан голубым цветом.
Способ осуществляют следующим образом:
1. Выделение ДНК из периферической венозной крови. На первом этапе к 0,5 мл крови добавляли 0,5 мл PBS и центрифугировали 10 мин при 12 тыс. об/мин. Надосадочную жидкость сливали, добавляли 1 мл PBS и вновь центрифугировали при тех же условиях. Надосадочную жидкость сливали, добавляли 200 мкл ТЕ-буфера, пипетировали до растворения осадка и затем последовательно добавляли 10 мкл 1% раствора додецилсульфата натрия SDS и 5 мкл протеиназы К. Пробирки инкубировали в термостате при t=37°C 12 ч. В ходе второго этапа проводили четыре последовательных центрифугирования с фенолом и хлороформом согласно протоколу методики (10 мин, 8 тыс. об/мин), после чего ДНК осаждали ледяным раствором 95% этилового спирта и центрифугировали 10 мин при 14,3 тыс. об/мин. По испарении спирта ДНК растворяли в 100 мкл деионизированной дистиллированной воды. Получаемый раствор ДНК в воде имел чистоту в диапазоне А260/280=1,5-2,0 и среднюю концентрацию около 180-200 нг/мкл.
Экстракция геномной ДНК из цельной крови колоночным методом проводилась с помощью набора QIAamp DNA blood mini kit (QIAGEN, Германия) на автоматической станции QiaCube (QIAGEN, Германия). Роботизированный протокол продолжительностью 58 минут включал этап лизиса клеток 0,2 мл цельной крови с помощью лизирующего буфера и протеиназы К QIAGEN, инкубирование, перенос лизата в колонку, связывание ДНК с мембраной колонки, центрифугирование, двукратное промывание колонки буфером AW1 и AW2, центрифугирование колонки и, наконец, элюирование очищенной ДНК. Получаемый раствор ДНК в воде имел идеальную чистоту А260/280=1,7-1,9 и среднюю концентрацию около 40-50 нг/мкл. Экстрагированные из крови образцы ДНК хранились в морозильниках Thermo Fisher Scientific (США) при -20°С.
2. Подготовка образцов ДНК к масс-спектрометрическому анализу. Качество выделенной ДНК оценивали по степени чистоты и концентрации раствора на спектрофотометре NanoDrop (Thermo Fisher Scientific, США). Все анализируемые образцы ДНК были разведены деионизированной водой до концентрации 10 нг/мкл при А260/280=1,5-2,0.
3. Анализ полиморфизмов гена ANPEP - генотипирование методом матрично-активированной лазерной десорбционно-ионизационной масс-спектрометрии MALDI-TOF. Использовали следующие последовательности праймеров для генотипирования по локусу rs9920421: прямой F: 5`-ACGTTGGATGCCTCAGATCTGCATGAAACG-3`, обратный R: 5`-ACGTTGGATGATTTCAGTGACCACTCAGCC-3`, праймер удлинения E: 5`- CTACTGGCTGCCTACA-3`. Для генотипирования по локусу rs4932143 использовали следующие последовательности праймеров: прямой F: 5`-ACGTTGGATGACAGGCCTCATCTCTGACTC-3`, обратный R: 5`-ACGTTGGATGAACATTCCTTCCGAGGCAAC-3`, праймер удлинения E: 5`-GCAACAGCCACATCT-3`. Для приготовления ПЦР-микса (в расчете на один спектральный чип) в центрифужную микропробирку вносили 80,6 мкл ddH2O, 50,4 мкл 10x буфера, 40,3 мкл MgCl2 (концентрация 25 ммоль/л), 10,1 мкл смеси дНТФ (концентрация 25 ммоль/л), 100,8 мкл смеси ПЦР-праймеров (концентрация 0,5 мкмоль/л) и 20,16 мкл HotStartTaq полимеразы (концентрация 5 ЕД/мкл). Смесь вортексировали и раскапывали в 96-луночный ПЦР-планшет по 3 мкл в лунку, после чего с помощью восьмиканального дозатора вносили по 2 мкл ДНК (концентрация 10 нг/мкл). Планшет заклеивали, центрифугировали 20 сек при 1000 об/мин и загружали в термоциклер CFX96 Bio-Rad на 125 мин при следующем режиме: денатурация 2 мин при 95°С, амплификация 44 цикла, состоящая из денатурации 30 сек при 95°С, отжига 30 сек при 56°С и элонгации 60 сек при 72°С. После чего пробы инкубировали 5 мин при 72°С. Не прореагировавшие в ходе ПЦР дНТФ удаляли с помощью реакции SAP (shrimp alkaline phosphatase), в ходе которой щелочная фосфатаза креветки гидролизовала дНТФ до нуклеозидов и фосфатов. Для приготовления SAP-микса в микропробирке смешивали 161,6 мкл ddH2O, 18 мкл 10хTS буфера и 31,7 мкл SAP фермента. Далее вносили по 2 мкл SAP-смеси в каждую лунку, планшет заклеивали, центрифугировали 20 сек при 1000 об/мин и загружали в термоциклер CFX96 Bio-Rad на 55 мин при следующем режиме: 45 мин при 37°С и 10 мин при 85°С. Для проведения третьей реакции iPLEX готовили Е-праймер-микс из расчета 8,8 мкл праймеров Е1-Е9, 11,7 мкл праймеров Е10-Е18, 14,6 мкл праймеров Е19-Е27, 17,5 мкл праймеров Е28-Е35 и 45,1 мкл ddH2O. После масс-спектрометрической оценки интенсивности пиков Е-праймеров в полученной смеси, в микс добавляли Е-праймеры в количествах, необходимых для достижения одинаковой интенсивности сигнала. Для приготовления iPLEX-микса в микропробирке смешивали 65,4 мкл ddH2O, 21,2 мкл iPLEX буфера, 21,2 мкл терминирующей смеси, 99,3 мкл Е-праймер-микса и 4,33 мкл iPLEX-фермента, вортексировали и раскапывали в лунки по 2 мкл. Планшет заклеивали, центрифугировали 20 секунд при 1000 об/мин и загружали в термоциклер CFX96 Bio-Rad на 135 мин при следующем режиме: денатурация 30 сек при 94°С, затем 40 циклов, состоящие из денатурации 5 сек при 94°С, отжига 5 сек при 52°С, элонгации 5 сек при 80°С, с последующим инкубированием в течение 3 мин при 72°С. По завершении реакции iPLEX, планшет охлаждали до +4°С, добавляли по 30 мкл воды во все лунки, центрифугировали 1 мин при 1000 об/мин и загружали в масс-спектрометр. Ввиду того, что небольшие полярные молекулы и положительно заряженные катионы натрия и калия могут образовывать аддукты с олигонуклеотидами и создавать серию контаминантных пиков, ампликоны были подвергнуты роботизированному обессоливанию путем их обработки смолой SpectroCLEAN (Agena Bioscience). Перенос образцов на спектральный чип с матрицей для ионизации осуществлялся в автоматическом режиме на рабочей станции Nanodispenser. Примеры кластерного распределения генотипов в результате масс-спектрометрического анализа на геномном масс-спектрометре MassArray analyzer 4 (Agena Bioscience) по SNPs rs9920421 и rs4932143 показаны на фигурах 1 и 2, соответственно. Статистические расчеты проводили с помощью программы SNPStats ( E., Valls, J., Iniesta, R., & Moreno, V. (2006). SNPStats: a web tool for the analysis of association studies. Bioinformatics, 22(15), 1928-1929).
E., Valls, J., Iniesta, R., & Moreno, V. (2006). SNPStats: a web tool for the analysis of association studies. Bioinformatics, 22(15), 1928-1929).
4. Прогнозирование повышенного риска формирования диабетической нефропатии у пациентов Центральной России с сахарным диабетом 2 типа и нормальной массой тела в случае выявления сочетания аллеля G rs9920421 с аллелем G rs4932143 и пониженного риска развития этого осложнения сахарного диабета 2 типа при выявлении сочетания аллеля А rs9920421 с аллелем С rs4932143.
Возможность использования предложенного способа для определения риска развития диабетической нефропатии у пациентов с сахарным диабетом 2 типа с нормальной массой тела подтверждает анализ результатов наблюдений 156 пациентов с СД2, у 35 из которых установлена диабетическая нефропатия. В исследование включались лица славянской национальности Центральной России с нормальной массой тела, то есть с индексом массы тела от 18,5 до 25 кг/м2. Диагноз СД2 был установлен врачами-эндокринологами ОБУЗ «Курская городская клиническая больница скорой медицинской помощи» на основе клинического и лабораторно-инструментального обследования. Установлены различия в распространенности сочетания аллеля G rs9920421 с аллелем G rs4932143 между больными сахарным диабетом 2 типа с диабетической нефропатией (32,86%) и больными сахарным диабетом 2 типа без диабетической нефропатии (21,07%) на фоне нормальной массы тела. Эта комбинация аллельных вариантов является фактором риска формирования диабетической нефропатии у пациентов с сахарным диабетом 2 типа и нормальной массой тела: OR=1,94, 95% CI 1,04-3,63, P=0,04 (таблица 1).
Распределение и анализ ассоциаций гаплотипов ANPEP c риском развития диабетической нефропатии у пациентов с сахарным диабетом 2 типа и нормальной массой тела
H
H - гаплотипы. СД2 - сахарный диабет 2 типа; ДНФ - диабетическая нефропатия.
В качестве примеров конкретного применения разработанного способа приведено генетическое обследование русских пациентов, уроженок Центральной России и не являющихся родственниками между собой: проведено генетическое обследование по локусам rs9920421 (A>G) и rs4932143 (С>G) гена ANPEP.
Пациентка Г., 63 года, находилась на стационарном лечении в ОБУЗ КГКБ СМП г. Курска с 30.08.2017 по 20.09.2017. Диагноз: сахарный диабет, 2 тип, фаза декомпенсации от 30.08.2017, фаза компенсации от 19.09.2017. Рецидивирующие тяжелые гипогликемические состояния. Кетонурия от 14.09.17. Индивидуальный целевой уровень HbA1c<7,5%. Целевой уровень гликемии плазмы натощак <7,5 ммоль/л, через 2 ч после еды <10,0 ммоль/л. У пациентки была взята венозная кровь, при генотипировании полиморфных локусов rs9920421 (A>G) и rs4932143 (С>G) было выявлено сочетание аллеля G rs9920421 с аллелем G rs4932143, что позволило отнести пациентку в группу больных с высоким риском развития диабетической нефропатии. При повторном обследовании через год у пациентки была выявлена диабетическая нефропатия.
Пациент Д., 53 года, находился на стационарном лечении в ОБУЗ КГКБ СМП г. Курска с 28.08.2019 по 16.09.2019. Диагноз: сахарный диабет, 2 тип, фаза декомпенсации от 28.08.2019, фаза компенсации от 16.09.2019. Кетонурия от 28.08.2019. Индивидуальный целевой уровень HbA1c<7,0%. Целевой уровень гликемии плазмы натощак <7,0 ммоль/л, через 2 ч после еды <9,0 ммоль/л. У пациента была взята венозная кровь, при генотипировании полиморфных локусов rs9920421 (A>G) и rs4932143 (С>G) было выявлено сочетание аллеля А rs9920421 с аллелем С rs4932143, что позволило отнести пациента в группу больных с низким риском развития диабетической нефропатии. Дальнейшее наблюдение не выявило у пациента диабетической нефропатии.
Пациентка А., 57 лет, находилась на стационарном лечении в ОБУЗ КГКБ СМП г. Курска с 01.04.19 по 12.04.19. Диагноз: сахарный диабет, 2 тип, впервые выявленный, фаза декомпенсации от 01.04.19, фаза компенсации от 12.04.19. Кетоацидотическая прекома от 01.04.2019. Индивидуальный целевой уровень HbA1c<7,5%. Целевой уровень гликемии плазмы натощак <7,5 ммоль/л, через 2 ч после еды <10,0 ммоль/л. У пациентки А. была взята венозная кровь, при генотипировании полиморфных локусов rs9920421 (A>G) и rs4932143 (С>G) было выявлено сочетание аллеля А rs9920421 с аллелем С rs4932143, что позволило отнести пациентку в группу больных с низким риском развития диабетической нефропатии. Дальнейшее наблюдение не выявило у пациентки диабетической нефропатии.
Применение данного способа позволит на доклиническом этапе формировать среди пациентов с сахарным диабетом 2 типа нормальной массы тела группы риска и своевременно реализовывать в этих группах необходимые лечебно-профилактические мероприятия по предупреждению развития диабетической нефропатии.
Резюме
Таким образом, полученные с помощью генетико-статистического анализа данные свидетельствуют о том, что сочетание аллеля G rs9920421 с аллелем G rs4932143 гена ANPEP является генетическим фактором риска развития диабетической нефропатии у пациентов с сахарным диабетом 2 типа и нормальной массой тела (OR=1,94).
Использование предложенного способа позволит прогнозировать развитие диабетической нефропатии у пациентов с сахарным диабетом 2 типа и нормальной массой тела, что даст возможность осуществлять мероприятия по профилактике диабетической нефропатии - диспансерное наблюдение, регулярный контроль уровня глюкозы в крови, достаточную физическую активность, правильное питание с ежедневным включением в рацион свежих овощей и фруктов и ограничением рафинированных углеводов и жиров.
Изобретение относится к медицине, а именно к медицинской диагностике, и может быть использовано для прогнозирования риска развития диабетической нефропатии у пациентов с сахарным диабетом 2 типа и нормальной массой тела. Осуществляют забор образца периферической венозной крови и экстракцию ДНК. Проводят анализ полиморфных вариантов гена аминопетидазы ANPEP rs9920421 (A>G) и rs4932143 (С>G). В случае выявления сочетания аллеля G rs9920421 с аллелем G rs4932143 прогнозируют повышенный риск формирования диабетической нефропатии. При обнаружении сочетания аллеля А rs9920421 с аллелем С rs4932143 прогнозируют низкий риск. Способ обеспечивает получение новых критериев оценки риска формирования диабетической нефропатии у пациентов Центральной России с сахарным диабетом 2 типа и нормальной массой тела по данным о генетических полиморфизмах rs9920421 (A>G) и rs4932143 (С>G). 2 ил., 1 табл., 3 пр.
Способ прогнозирования риска развития диабетической нефропатии у пациентов с сахарным диабетом 2 типа и нормальной массой тела, включающий забор образца периферической венозной крови, отличающийся тем, что после экстракции ДНК проводят анализ полиморфных вариантов гена аминопетидазы ANPEP rs9920421 (A>G) и rs4932143 (С>G) и прогнозируют повышенный риск формирования диабетической нефропатии у пациентов Центральной России с сахарным диабетом 2 типа и нормальной массой тела в случае выявления сочетания аллеля G rs9920421 с аллелем G rs4932143, а при обнаружении сочетания аллеля А rs9920421 с аллелем С rs4932143 – низкий риск развития диабетической нефропатии у пациентов Центральной России с сахарным диабетом 2 типа и нормальной массой тела.
| СПОСОБ РАННЕГО ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ ДИАБЕТИЧЕСКОЙ НЕФРОПАТИИ У ПАЦИЕНТОВ С САХАРНЫМ ДИАБЕТОМ 1 ТИПА | 2022 |
|
RU2793531C1 |
| US 20140038203 A1, 06.02.2014 | |||
| КОРВЯКОВА Я.Е | |||
| и др | |||
| Электрическая трубчатая печь | 1930 |
|
SU25653A1 |
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Т | |||
| Торфодобывающая машина с вращающимся измельчающим орудием | 1922 |
|
SU87A1 |
Авторы
Даты
2023-12-11—Публикация
2023-07-06—Подача