Изобретение относится к области медицинской диагностики, может быть использовано для прогнозирования риска развития сахарного диабета 2 типа у мужчин.
Исследования последних лет показали, что нарушения окислительно-восстановительного баланса, с формированием окислительного стресса, являются ведущим механизмом развития сахарного диабета 2 типа [Gerber PA, Rutter GA. The Role of Oxidative Stress and Hypoxia in Pancreatic Beta-Cell Dysfunction in Diabetes Mellitus. Antioxid Redox Signal. 2017 Apr 1;26(10):501-518. doi: 10.1089/ars.2016.6755; Singh A, Kukreti R, Saso L, Kukreti S. Mechanistic Insight into Oxidative Stress-Triggered Signaling Pathways and Type 2 Diabetes. Molecules. 2022 Jan 30;27(3):950. doi: 10.3390/molecules27030950]. Ген GPX3, расположенный на пятой хромосоме (5q33.1), кодирует фермент глутатионпероксидазу 3, которая катализирует расщепление перекиси водорода и других перекисных соединений с помощью молекулы восстановленного глутатиона и защищает клетки от повреждения в условиях окислительного стресса [Qi X, Ng KT, Shao Y, Li CX, Geng W, Ling CC, Ma YY, Liu XB, Liu H, Liu J, Yeung WH, Lo CM, Man K. The Clinical Significance and Potential Therapeutic Role of GPx3 in Tumor Recurrence after Liver Transplantation. Theranostics. 2016 Aug 8;6(11):1934-46. doi: 10.7150/thno.16023.]. Согласно ресурса eQTLGen phase I [https://www.eqtlgen.org/cis-eqtls.html], полиморфный вариант rs870406 (G>A) гена GPX3 ассоциирован со значимым снижением экспрессии гена в крови и потому может рассматриваться как потенциальный генетический маркер предрасположенности к сахарному диабету 2 типа.
Известен cпособ прогнозирования риска развития сахарного диабета 2 типа, по патенту на изобретение EA201501035A (публикация: 18.11.2015), включающий следующие этапы: определение у пациента клинико-анамнестических данных: индекс массы тела (ИМТ), окружность талии (ОТ), наличие артериальной гипертензии (АГ), наличие сахарного диабета у близких родственников и лабораторных данных: выявление триглицеридов (ТГ) >1,7 ммоль/л, холестерина высокой плотности (ХС ЛВП) >1,0 ммоль/л, показаний САД > 140 и/или ДАД > 90 мм рт. ст., уровня сахара в крови > 5.6 ммоль/л; оценивают с использованием бальной шкалы: ИМТ < 25 кг/м2 - 0 баллов, 25-30 кг/м2 - 1 балл, >30 кг/м2 - 2 балла; ОТ у мужчин <94 см - 0 баллов, 94-102 см - 2 балла, >10 2 см - 3 балла; ОТ у женщин < 80 см - 0 баллов, 80-88 см - 2 балла, > 88 см - 3 балла; наличие АГ: нет - 0 баллов, да - 1 балл; выявление ТГ > 1,7 ммоль/л: да - 1 балл, нет - 0 баллов; выявление ХС ЛВП >1,0 ммоль/л: да - 0 баллов, нет - 1 балл; показания САД >140 и/или ДАД >90 мм.рт.ст.: нет - 0 баллов, да - 1 балл; уровень сахара в крови >5.6 ммоль/л: нет - 0 баллов, да - 3 балла, полученные баллы суммируют и при сумме баллов < 8 баллов судят о низком риске, а при сумме баллов > 8 баллов судят о высоком риске развития СД 2 типа у пациента в течение ближайших 10 лет.
Недостаток метода заключается в том, что он не учитывает индивидуальную генетическую предрасположенность к заболеванию и имеет ограничение прогноза риска развития сахарного диабета 2 типа во времени.
Известен способ прогнозирования риска развития сахарного диабета 2 типа у больных метаболическим синдромом по патенту на изобретение RU2580632C1 (дата публикации 10.04.2016), включающий определение: содержания аспартатаминотрансферазы в сыворотке крови (x1,ед/л), конечного систолического объема левого желудочка по данным эхокардиографии (x2,мл), конечного диастолического объема левого желудочка по данным эхокардиографии (x3,см), содержания аланинаминотрансферазы в сыворотке крови (х4,ед/л), систолического артериального давления (х5,мм рт.ст.), размера левого предсердия по данным эхокардиографии (x6,см), содержания триглицеридов в сыворотке крови (х7,ммоль/л), содержания кортизола в сыворотке крови (x8,нмоль/л), содержания сахара в сыворотке крови через два часа после приема пищи (х9,моль/л), возраста больного (х10,лет), индекса массы тела больного (x11,кг/м2), наличия у больного отягощенной наследственности по сахарному диабету второго типа (x12=1, если наследственность отягощена, и x12=0, если наследственность не отягощена) с последующим расчетом стратификационного показателя риска G(x)=0,27x1+0,28x2+5,03x3+0,25х4+0,12х5+1,93x6-3,13х7+0,28x8+1,05x9+ 0,17x10+0,06x11+0,59x12, по величине которого риск развития сахарного диабета второго типа прогнозируют как: «высокий», если G(x) превышает 88,1, и «незначительный» в противном случае.
Однако данный способ не пригоден для выявления предрасположенности к развитию сахарного диабета 2 типа у лиц без метаболического синдрома.
Наиболее близок по результату исследования способ прогнозирования риска развития сахарного диабета 2 типа у жителей Центральной России на основе генотипирования полиморфизма rs11073891 гена ANPEP (патент на изобретение RU2803636C1, дата публикации 18.09.2023), включающий забор образца периферической венозной крови и экстракцию ДНК с последующим анализом полиморфного варианта гена аминопептидазы ANPEP rs11073891 (А>С). Прогнозируют повышенный риск развития сахарного диабета 2 типа в случае выявления генотипа rs11073891-А/А, а при обнаружении генотипов rs11073891-А/С или rs11073891-С/С - низкий риск развития сахарного диабета 2 типа.
Однако данный способ не учитывает пол пациентов.
Технический результат заключается в получении критериев оценки риска развития сахарного диабета 2 типа у мужчин по данным о генетическом полиморфизме rs870406 (G>A) гена GPX3.
Технический результат достигается тем, что после экстракции ДНК проводят анализ полиморфного варианта rs870406 (G>A) гена GPX3 и прогнозируют повышенный риск развития сахарного диабета 2 типа в случае выявления генотипа rs870406-A/A, а при обнаружении генотипа rs870406-G/G или rs870406-G/A - низкий риск развития сахарного диабета 2 типа у мужчин.
Способ осуществляют следующим образом:
1. Выделение ДНК из периферической венозной крови. На первом этапе к 0,5 мл крови добавляли 0,5 мл PBS и центрифугировали 10 мин при 12 тыс. об/мин. Надосадочную жидкость сливали, добавляли 1 мл PBS и вновь центрифугировали при тех же условиях. Надосадочную жидкость сливали, добавляли 200 мкл ТЕ-буфера, пипетировали до растворения осадка и затем последовательно добавляли 10 мкл 1% раствора додецилсульфата натрия SDS и 5 мкл протеиназы К. Пробирки инкубировали в термостате при t=37°C 12 ч. В ходе второго этапа проводили четыре последовательных центрифугирования с фенолом и хлороформом согласно протоколу методики (10 мин, 8 тыс. об/мин), после чего ДНК осаждали ледяным раствором 95% этилового спирта и центрифугировали 10 мин при 14,3 тыс. об/мин. По испарении спирта ДНК растворяли в 100 мкл деионизированной дистиллированной воды. Получаемый раствор ДНК в воде имел чистоту в диапазоне А260/280=1,5-2,0 и среднюю концентрацию около 180-200 нг/мкл. Экстрагированные из крови образцы ДНК хранились в морозильниках Thermo Fisher Scientific (США) при -20°С.
2. Подготовка образцов ДНК к генотипированию. Качество выделенной ДНК оценивали по степени чистоты и концентрации раствора на спектрофотометре NanoDrop (Thermo Fisher Scientific, США). Все анализируемые образцы ДНК были разведены деионизированной водой до концентрации 10 нг/мкл при А260/280=1,5-2,0.
3. Анализ полиморфизма rs870406 (G>A) гена GPX3 - генотипирование методом матрично-активированной лазерной десорбционно-ионизационной масс-спектрометрии MALDI-TOF. Использовали следующие последовательности праймеров: прямой F: 5`- ACGTTGGATGGAATGACTAAGGGAGGAAGG-3`, обратный R: 5`- ACGTTGGATGCGGAGGTGACATAGATGTAG-3`, праймер удлинения E: 5`- ggGATGTAGCAAGGCGAC-3`. Для приготовления ПЦР-микса (в расчете на один спектральный чип) в центрифужную микропробирку вносили 80,6 мкл ddH2O, 50,4 мкл 10x буфера, 40,3 мкл MgCl2 (концентрация 25 ммоль/л), 10,1 мкл смеси дНТФ (концентрация 25 ммоль/л), 100,8 мкл смеси ПЦР-праймеров (концентрация 0,5 мкмоль/л) и 20,16 мкл HotStartTaq полимеразы (концентрация 5 ЕД/мкл). Смесь вортексировали и раскапывали в 96-луночный ПЦР-планшет по 3 мкл в лунку, после чего с помощью восьмиканального дозатора вносили по 2 мкл ДНК (концентрация 10 нг/мкл). Планшет заклеивали, центрифугировали 20 сек при 1000 об/мин и загружали в термоциклер CFX96 Bio-Rad на 125 мин при следующем режиме: денатурация 2 мин при 95°С, амплификация 44 цикла, состоящая из денатурации 30 сек при 95°С, отжига 30 сек при 56°С и элонгации 60 сек при 72°С. После чего пробы инкубировали 5 мин при 72°С. Не прореагировавшие в ходе ПЦР дНТФ удаляли с помощью реакции SAP (shrimp alkaline phosphatase), в ходе которой щелочная фосфатаза креветки гидролизовала дНТФ до нуклеозидов и фосфатов. Для приготовления SAP-микса в микропробирке смешивали 161,6 мкл ddH2O, 18 мкл 10хTS буфера и 31,7 мкл SAP фермента. Далее вносили по 2 мкл SAP-смеси в каждую лунку, планшет заклеивали, центрифугировали 20 сек при 1000 об/мин и загружали в термоциклер CFX96 Bio-Rad на 55 мин при следующем режиме: 45 мин при 37°С и 10 мин при 85°С. Для проведения третьей реакции iPLEX готовили Е-праймер-микс из расчета 8,8 мкл праймеров Е1-Е9, 11,7 мкл праймеров Е10-Е18, 14,6 мкл праймеров Е19-Е27, 17,5 мкл праймеров Е28-Е35 и 45,1 мкл ddH2O. После масс-спектрометрической оценки интенсивности пиков Е-праймеров в полученной смеси, в микс добавляли Е-праймеры в количествах, необходимых для достижения одинаковой интенсивности сигнала. Для приготовления iPLEX-микса в микропробирке смешивали 65,4 мкл ddH2O, 21,2 мкл iPLEX буфера, 21,2 мкл терминирующей смеси, 99,3 мкл Е-праймер-микса и 4,33 мкл iPLEX-фермента, вортексировали и раскапывали в лунки по 2 мкл. Планшет заклеивали, центрифугировали 20 секунд при 1000 об/мин и загружали в термоциклер CFX96 Bio-Rad на 135 мин при следующем режиме: денатурация 30 сек при 94°С, затем 40 циклов, состоящие из денатурации 5 сек при 94°С, отжига 5 сек при 52°С, элонгации 5 сек при 80°С, с последующим инкубированием в течение 3 мин при 72°С. По завершении реакции iPLEX, планшет охлаждали до +4°С, добавляли по 30 мкл воды во все лунки, центрифугировали 1 мин при 1000 об/мин и загружали в масс-спектрометр. Ввиду того, что небольшие полярные молекулы и положительно заряженные катионы натрия и калия могут образовывать аддукты с олигонуклеотидами и создавать серию контаминантных пиков, ампликоны были подвергнуты роботизированному обессоливанию путем их обработки смолой SpectroCLEAN (Agena Bioscience). Перенос образцов на спектральный чип с матрицей для ионизации осуществлялся в автоматическом режиме на рабочей станции Nanodispenser. Статистические расчеты проводили с помощью программы PLINK ( E., Valls, J., Iniesta, R., & Moreno, V. (2006). SNPStats: a web tool for the analysis of association studies. Bioinformatics, 22(15), 1928-1929).
E., Valls, J., Iniesta, R., & Moreno, V. (2006). SNPStats: a web tool for the analysis of association studies. Bioinformatics, 22(15), 1928-1929).
4. Прогнозирование повышенного риска развития сахарного диабета 2 типа у мужчин в случае выявления генотипа rs870406-A/A и пониженного риска развития этого заболевания при выявлении генотипов rs870406-G/G или rs870406-G/A.
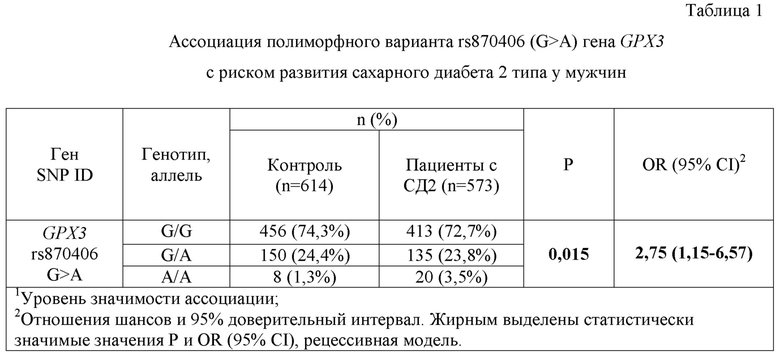
Возможность использования предложенного способа для определения риска развития сахарного диабета 2 типа у мужчин подтверждает анализ результатов наблюдений 1182 мужчин, у 568 из которых установлен сахарный диабет 2 типа. В исследование включались лица славянской национальности Центральной России. Диагноз СД2 был установлен врачами-эндокринологами ОБУЗ ГК БСМП на основе клинического и лабораторно-инструментального обследования. Установлено, что носительство генотипа rs870406-A/A (OR=2,75, 95% CI 1,15-6,57, P=0,015) ассоциировалось с повышенным риском развития сахарного диабета 2 типа (таблица 1).
В качестве примеров конкретного применения разработанного способа приведено генетическое обследование мужчин славянского происхождения, уроженцев Центральной России и не являющихся родственниками между собой: проведено генетическое обследование по локусу rs870406 (G>A) гена GPX3.
Донор-доброволец С.А., мужчина 59 лет, обратился в ОБУЗ «Курская областная клиническая станция переливания крови» комитета здравоохранения Курской области 06.11.2015 г. для сдачи крови. Пациенту было предложено принять участие в научном исследовании для выявления генетической предрасположенности к сахарному диабету 2 типа. У мужчины была взята венозная кровь, при генотипировании полиморфного локуса rs870406 (G>A) гена GPX3 был выявлен генотип rs870406-А/А гена GPX3, что позволило отнести мужчину в группу лиц с высоким риском развития сахарного диабета 2 типа. Тем не менее, профилактические мероприятия по увеличению физической активности и формированию приверженности к здоровому питанию с целью нормализации массы тела мужчиной не проводились. С жалобами на сухость во рту, жажду и общую слабость 24.03.2018 г. пациент С.А. был доставлен бригадой скорой медицинской помощи в эндокринологическое отделение ОБУЗ КГКБ СМП г. Курска, где получал стационарное лечение по 04.04.2018 г. При поступлении концентрация глюкозы крови составила 12,9 ммоль/л, гликированный гемоглобин 9,1%. Клинический диагноз: сахарный диабет, 2 тип, впервые выявленный, фаза декомпенсации от 24.03.2018 г., фаза компенсации от 04.04.2018 г. Индивидуальный целевой уровень HbA1c<7,5%. Целевой уровень гликемии плазмы натощак <7,5 ммоль/л, через 2 ч после еды <10,0 ммоль/л.
Донор-доброволец З.А., мужчина 56 лет, обратился в ОБУЗ «Курская областная клиническая станция переливания крови» комитета здравоохранения Курской области 12.10.2018 г. для сдачи крови. Пациенту было предложено принять участие в научном исследовании для выявления генетической предрасположенности к сахарному диабету 2 типа. У мужчины была взята венозная кровь, при генотипировании полиморфного локуса rs870406 (G>A) гена GPX3 был выявлен генотип rs870406-G/А гена GPX3, что позволило отнести мужчину в группу лиц с низким риском развития сахарного диабета 2 типа. Анализ крови подтвердил факт отсутствия нарушений углеводного обмена: концентрация глюкозы крови натощак 4,0 ммоль/л, гликированный гемоглобин 5,1%, что соответствует норме. Дальнейшее наблюдение не выявило диагноз сахарного диабета 2 типа.
Донор-доброволец Б.М., мужчина 55 лет, обратился в ОБУЗ «Курская областная клиническая станция переливания крови» комитета здравоохранения Курской области 15.08.2019 г. для сдачи крови. Пациенту было предложено принять участие в научном исследовании для выявления генетической предрасположенности к сахарному диабету 2 типа. У мужчины была взята венозная кровь, при генотипировании полиморфного локуса rs870406 (G>A) гена GPX3 был выявлен генотип rs870406-G/G гена GPX3, что позволило отнести мужчину в группу лиц с низким риском развития сахарного диабета 2 типа. Анализ крови подтвердил факт отсутствия нарушений углеводного обмена: концентрация глюкозы крови натощак 3,7 ммоль/л, гликированный гемоглобин 5,0%, что соответствует норме. Дальнейшее наблюдение не выявило диагноз сахарного диабета 2 типа.
Применение данного способа позволит на доклиническом этапе формировать среди мужчин группы риска и своевременно реализовывать в этих группах необходимые лечебно-профилактические мероприятия по предупреждению развития сахарного диабета 2 типа.
Резюме
Таким образом, полученные данные свидетельствуют о том, что носительство генотипа rs870406-A/A GPX3 является генетическим фактором риска развития сахарного диабета 2 типа (OR=2,75, Р=0,015) у мужчин.
Использование предложенного способа позволит прогнозировать развитие сахарного диабета 2 типа у мужчин, что даст возможность осуществлять мероприятия по профилактике данного заболевания - регулярный контроль уровня глюкозы в крови, нормализацию массы тела, достаточную физическую активность, правильное питание с ежедневным включением в рацион свежих овощей и фруктов и ограничением рафинированных углеводов и жиров.
Изобретение относится к медицине, а именно к клинической лабораторной диагностике, и может быть использовано для прогнозирования риска развития сахарного диабета 2 типа у мужчин. Осуществляют забор образца периферической венозной крови. После экстракции ДНК проводят анализ полиморфного варианта rs870406 (G>A) гена GPX3. В случае выявления генотипа rs870406-A/A прогнозируют повышенный риск развития сахарного диабета 2 типа. При обнаружении генотипов rs870406-G/G или rs870406-G/A прогнозируют низкий риск развития сахарного диабета 2 типа. Способ обеспечивает получение новых критериев оценки риска развития сахарного диабета 2 типа у мужчин на основе генотипирования полиморфного варианта rs870406 (G>A) гена GPX3. 1 табл., 3 пр.
Способ прогнозирования риска развития сахарного диабета 2 типа у мужчин, включающий забор образца периферической венозной крови, отличающийся тем, что после экстракции ДНК проводят анализ полиморфного варианта rs870406 (G>A) гена GPX3 и прогнозируют повышенный риск развития сахарного диабета 2 типа в случае выявления генотипа rs870406-A/A, а при обнаружении генотипов rs870406-G/G или rs870406-G/A – низкий риск развития сахарного диабета 2 типа у мужчин.
| Способ прогнозирования риска развития сахарного диабета 2 типа у лиц с ожирением и/или предиабетом | 2022 |
|
RU2801174C1 |
| Способ оценки риска возникновения сахарного диабета 2 типа на основании средней скорректированной фазы сна по Мюнхенскому тесту | 2022 |
|
RU2786822C1 |
| KR 100902282 B1, 10.06.2009 | |||
| LIU D | |||
| et al | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Diab Vasc Dis Res | |||
| Способ получения цианистых соединений | 1924 |
|
SU2018A1 |
| Способ получения цианистых соединений | 1924 |
|
SU2018A1 |
Авторы
Даты
2025-03-25—Публикация
2024-10-31—Подача