Изобретение относится к области органической химии, а именно способу получения метил 1-{[2-(2-хлоробензоил)гидразинилиден](2-хлорофенил)метил}циклоалкан-1-карбоксилатов 1а, б формулы:

Данные соединения могут быть применены в медицине, фармакологии, ветеринарии.
Известны структурные аналоги заявляемых соединений, обладающие биологической активностью [J.P.M.  R.F.M. Frade, F.M.F. Santos, J.A.S. Coelho, C.A.M. Afonso, P.M.P. Gois, A.F. Trindade /NHC catalysed direct addition of HMF to diazo compounds: synthesis of acyl hydrazones with antitumor activity // RSC Adv. - 2014. - Vol. 4. - №55. - P. 29352-29356. DOI: 10.1039/c4ra03710 с]. Синтез структурных аналогов осуществляется по следующей схеме:
R.F.M. Frade, F.M.F. Santos, J.A.S. Coelho, C.A.M. Afonso, P.M.P. Gois, A.F. Trindade /NHC catalysed direct addition of HMF to diazo compounds: synthesis of acyl hydrazones with antitumor activity // RSC Adv. - 2014. - Vol. 4. - №55. - P. 29352-29356. DOI: 10.1039/c4ra03710 с]. Синтез структурных аналогов осуществляется по следующей схеме:

К недостаткам данного способа относится невозможность получения 1-{[2-(2-хлоробензоил)гидразинилиден](2-хлорофенил)метил}циклоалкан-1-карбоксилатов. Также способ синтеза структурных аналогов предполагает необходимость работы в инертной атмосфере аргона.
Задачей изобретения является разработка простого способа синтеза неописанных в литературе 1-{[2-(2-хлоробензоил)гидразинилиден](2-хлорофенил)метил}циклоалкан-1-карбоксилатов 1а, б.
Поставленная задача достигается путем кипячения 2,5-ди(2-хлорфенил)-1,3,4-оксадиазола 2 с метиловыми эфирами 1-бромциклоалканкарбоновых кислот 3а, б и цинком в среде толуола с последующей обработкой реакционной массы и выделением целевых продуктов 1а, б.
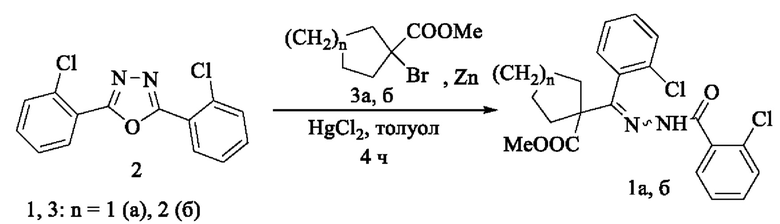
Из патентной и технической литературы не были выявлены способы получения, имеющие сходные признаки с заявленным способом, а именно, не использовались исходные продукты, растворитель, в котором проходит реакция, на основании чего можно сделать вывод о соответствии заявленного технического решения критерию «новизна» и «изобретательский уровень».
Изобретение иллюстрируется следующими примерами.
Пример 1. 1-{[2-(2-Хлоробензоил)гидразинилиден](2-хлорофенил)метил}циклопентан-1-карбоксилат 1а.
К смеси 2,0 г измельченного в мелкую стружку цинка, каталитического количества сулемы, 2 г (0,0069) моль 2,5-бис(2-хлорфенил)-1,3,4-оксадиазола 2, 20 мл безводного толуола и 2 мл ГМФТА добавляли по каплям при кипячении и перемешивании смесь 3.13 г (0,0151 моль) метил 1-бромциклопентанкарбоксилата 3а в 10 мл безводного толуола. Затем реакционную смесь кипятили 4 ч, охлаждали, декантировали с избытка цинка, гидролизовали 5%-ным раствором уксусной кислоты, органический слой отделяли, из водного слоя продукты реакции дважды экстрагировали толуолом. После сушки органической фазы безводным сульфатом натрия толуол отгоняли, продукт дважды перекристаллизовывали из этанола. Выход 2.33 г (81%), т.пл. 144-145°С.
Выделенное соединение 1а представляет собой белое кристаллическое вещество, легкорастворимое в хлороформе, ДМСО, ДМФА, растворимое в ацетоне, труднорастворимое в спирте, алканах и ароматических углеводородах, нерастворимое в воде. Устойчиво при хранении в обычных условиях.
ИК спектр соединения (1а) снят в виде пасты в вазелиновом масле (ν, см-1): 3152 (NH), 1734, 1725, 1676, 1663(СО), 1621 (C=N).
Спектр ЯМР 1Н соединения (1а) снят в растворе CDCl3 при частоте 400 МГц δ, м.д.: 1.46-1.58 м (2Н), 1.65-1.84-2.57 м (2Н), 1.90-2.15 м (3Н), 2.22-2.55 м (1H) [(СН2)4], 3.49 с (2.1Н, МеО), 3.71 с (0.9Н, МеО), 7.15-7.85 м [8Н, 2 (2-ClC6H4)], 8.18 с (0.7Н, NH), 8.89 с (0.3Н, NH).
Спектр ЯМР 13С соединения (1а) снят в растворе CDCl3 при частоте 100 МГц δ, м.д.: 24.1, 24.2, 24.6, 34.0, 34.4, 35.2, 36.0, 52.2, 52.5, 62.4, 126.4, 127.4, 127.9, 129.0, 129.4, 129.7, 130.6, 130.7, 131.5, 132.0, 133.0, 135.2, 151.3, 155.3, 169.4, 174.3, 174.3.
Соединение (1a) C21H20Cl2N2O3. Найдено, %: С 60.26; Н 4.64; N 6.49. Вычислено, %: С 60.15; Н 4.81; N 6.68.
Пример 2. 1-{[2-(2-Хлоробензоил)гидразинилиден](2-хлорофенил)метил}циклогексан-1-карбоксилат 1б.
К смеси 2,0 г измельченного в мелкую стружку цинка, каталитического количества сулемы, 2 г (0,0069) моль 2,5-бис(2-хлорфенил)-1,3,4-оксадиазола 2, 20 мл безводного толуола и 2 мл ГМФТА добавляли по каплям при кипячении и перемешивании смесь 3.34 г (0,0151 моль) метил 1-бромциклогексанкарбоксилата 3б в 10 мл безводного толуола. Затем реакционную смесь кипятили 4 ч, охлаждали, декантировали с избытка цинка, гидролизовали 5%-ным раствором уксусной кислоты, органический слой отделяли, из водного слоя продукты реакции дважды экстрагировали толуолом. После сушки органической фазы безводным сульфатом натрия толуол отгоняли, продукт дважды перекристаллизовывали из этанола. Выход 93 (%),т.пл. 120-122°С.
Выделенное соединение 1б белое кристаллическое вещество, легкорастворимое в хлороформе, ДМСО, ДМФА, растворимое в ацетоне, труднорастворимое в спирте, алканах и ароматических углеводородах, нерастворимое в воде. Устойчиво при хранении в обычных условиях.
ПК спектр соединения (1б) снят в виде пасты в вазелиновом масле (см-1): 3164 (NH), 1738, 1673, 1665 (СО), 1615 (C=N).
Спектр ЯМР 1Н соединения (3б) снят в растворе CDCl3 при частоте 400 МГц δ, м.д.: 0.94-1.82 м (8Н), 2.01-2.57-2.40 м (2Н) [(СН2)5], 3.36 с (2.1Н, МеО), 3.63 с (0.9Н, МеО), 7.02 дд (1H, J 7.4 Гц, 1.9 Гц) 7.22-7.78 м [7Н, 2 (2-ClC6H4)], 8.06 с (0.7Н, NH), 8.80 с (0.3Н, NH).
Спектр ЯМР 13С соединения (1б) снят в растворе CDCl3 при частоте 100 МГц δ, м.д.: 23.0, 23.1, 25.1, 32.1, 32.3, 33.2, 51.7, 55.5, 126.3, 127.5, 128.8, 129.2, 129.9, 130.4, 130.6, 131.3, 131.4, 131.9, 132.8, 135.0, 152.7, 169.3, 172.8.
Соединение (1б) C22H22Cl2N2O3. Найдено, %: С 61.16; Н 5.24; N 6.39. Вычислено, %: С 60.98; Н 5.12; N 6.46.
Пример 3. Исследование соединений (1а, б) на наличие антиоксидантной активности.
Антиоксидантная активность изучалась спектрофотометрическим методом по способности растворов исследуемых веществ улавливать ярко окрашенные радикалы 2,2-дифенил-1-пикрилгидразила (DPPH) [Methods for Antioxidant Capacity Estimation of Wheat and Wheat-Based Food Products / J. Moore, L. Yu // Wheat Antioxidants - Wiley, 2007. - 118-172. DOI: 10.1002/9780470228333.CH9; Wheat Antioxidants (ed. Liangli Yu). Wiley. 2007. DOI: 10.1002/9780470228333].
Фотометрический DPPH реагент содержал 0.2 мМ раствор DPPH в метаноле. Растворы (концентрация 15 мкмоль/мл) исследуемых соединений и эталонов (агидол-1, аскорбиновая кислота) в ДМСО в количестве 100 мкл добавлялись к DPPH реагенту (100 мкл) в лунки 96-луночного планшета. Реакционная смесь выдерживалась при 20°С в течение 20 мин. в темноте. Оптическую плотность реакционных смесей измеряли при 517 нм. Калибровка проводилась по свежеприготовленному раствору DPPH в смеси ДМСО-метанол, 1 к 1. Убыль радикала рассчитывали по формуле:
Убыль радикала (%)=[(А0-A1)/A0]⋅100, где А0 поглощение раствора DPPH без исследуемого образца, A1 поглощение раствора DPPH в присутствии исследуемого образца.
Результаты исследований приведены в Таблице 1.

В результате исследования выявлено, что соединения (1а, б) проявляют умеренную антиоксидантную активность в отношении свободного радикала DPPH.
Изобретение относится к области органической химии, а именно способу получения метил 1-{[2-(2-хлоробензоил)гидразинилиден](2-хлорофенил)метил}циклоалкан-1-карбоксилатов формулы 1а, б, обладающих антиоксидантной активностью, которые могут быть применены в качестве лекарственных препаратов в фармакологии. Способ заключается во взаимодействии 2,5-ди(2-хлорфенил)-1,3,4-оксадиазола 2 с метиловыми эфирами 1-бромциклоалканкарбоновых кислот 3а, б и цинком в среде толуола с последующей обработкой реакционной массы и выделением целевых продуктов, по схеме:
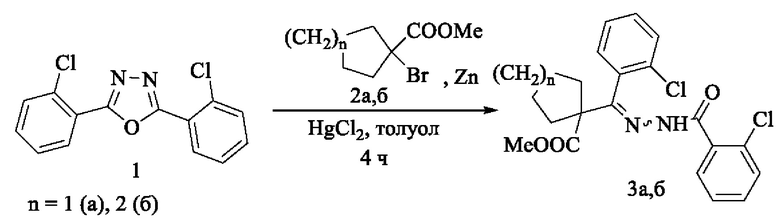
Техническим результатом изобретения является предоставление простого способа синтеза метил 1-{[2-(2-хлоробензоил)гидразинилиден](2-хлорофенил)метил}циклоалкан-1-карбоксилатов 1а, б. 1 табл., 3 пр.
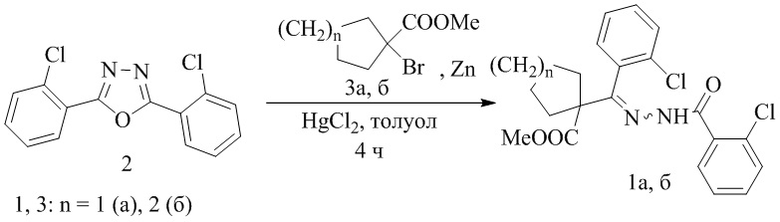
Способ получения метил 1-{[2-(2-хлоробензоил)гидразинилиден](2-хлорофенил)метил}циклоалкан-1-карбоксилатов 1а, б, при котором 2,5-ди(2-хлорфенил)-1,3,4-оксадиазол 2 подвергают взаимодействию с метиловыми эфирами 1-бромциклоалканкарбоновых кислот 3а, б и цинком в среде толуола при кипячении в течение 4 часов с последующей обработкой реакционной массы и выделением целевых продуктов, по следующей схеме:
| J.P.M | |||
| Antônio et al | |||
| / NHC catalysed direct addition of HMF to diazo compounds: synthesis of acyl hydrazones with antitumor activity / RSC Adv | |||
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| - Vol | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Устройство двукратного усилителя с катодными лампами | 1920 |
|
SU55A1 |
| - P | |||
| Устройство для кинопроекции и киносъемки с непрерывным движением ленты и прерывистым источником света | 1930 |
|
SU29352A1 |
| CN 111423339 A, 17.07.2020 | |||
| Sevim Rollas, Sevgi Karakuş /The synthesis and biological activities of 3-acyl- 2,3-dihydro-1,3,4-oxadiazole / | |||
Авторы
Даты
2023-12-05—Публикация
2023-05-03—Подача