ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННУЮ ЗАЯВКУ
Настоящая заявка испрашивает приоритет по предварительной заявке на патент США 62/848,983, поданной 16 мая 2019 года, и предварительной заявке на патент США 62/975,966, поданной 13 февраля 2020 года, содержание каждой из которых включено посредством отсылок во всей своей полноте, и по каждой из которых испрашивается приоритет.
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
Настоящая заявка содержит Список последовательностей, который был представлен в формате ASCII по системе EFS-Web и настоящим включен посредством отсылки во всей своей полноте. Копия ASCII, созданная 13 мая 2020 года, названа 0727341041SL_ST25.TXT и имеет размер 144318 байтов.
1. ВВЕДЕНИЕ
Настоящее изобретение относится к способам и композициям для усиления иммунного ответа в отношении рака и патогенов. Оно относится к химерным антигенным рецепторам (CAR), которые специфично взаимодействуют с мезотелином человека, а также к иммунореактивным клеткам, включающим такие CAR-рецепторы. Раскрытые в настоящем документе мезотелин-направленные CAR-рецепторы обладают улучшенными иммуноактивирующими свойствами, включая противоопухолевую активность, и в то же время обладают свойствами, позволяющими свести к минимуму CAR-индуцированную токсичность и иммуногенность.
2. УРОВЕНЬ ТЕХНИКИ
Клеточная иммунотерапия - это терапия с лечебным потенциалом для лечения рака. T-клетки и другие иммунные клетки могут быть модифицированы для направленного взаимодействия с опухолевыми антигенами посредством введения генетического материала, кодирующего искусственные или синтетические рецепторы антигена, называемые химерными антигенными рецепторами (CAR), специфичными к выбранным антигенам. Адресная T-клеточная терапия с применением CAR-рецепторов недавно продемонстрировала клинический успех при лечении некоторых гемобластозов. Однако перенос терапии CAR-экспрессирующими T-клетками на солидные опухоли создает несколько препятствий, которые необходимо преодолеть для достижения клинического эффекта. Злокачественные клетки приспосабливаются к созданию иммуносупрессивного микроокружения для своей защиты от иммунного распознавания и уничтожения. Такое микроокружение опухоли представляет сложность для применения способов лечения, включающих стимуляцию иммунного ответа, таких как адресная терапия T-клетками. Солидные опухоли также могут быть ограничены в анатомических компартментах, которые препятствуют эффективной миграции T-клеток, не имеют достаточной экспрессии агонистических костимулирующих лигандов и/или экспрессируют негативные регуляторы функции T-клеток. Таким образом, для успешного устранения солидных опухолей требуется эффективная инфильтрация опухоли и преодоление индуцированной опухолью иммуносупрессии. Кроме того, солидные опухоли создают проблему для выбора оптимальных иммунных мишеней - антигенов, направленное взаимодействие с которыми позволит активным T-клетками уничтожать опухоль с минимальным или переносимым токсическим действием в отношении неопухолевых тканей.
Таким образом, существуют потребности в новых терапевтических стратегиях конструирования CAR-рецепторов для лечения онкологических заболеваний, в особенности солидных опухолей, где такие стратегии способны индуцировать активное уничтожение опухоли с минимальной токсичностью и иммуногенностью.
3. СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В настоящем изобретении предложены полипептидные композиции, включающие: (a) химерный антигенный рецептор (CAR), который специфично взаимодействует с мезотелином (например, мезотелином человека); и (b) доминантно-негативная форма белка программируемой смерти 1 (PD-1 DN); иммунореактивные клетки, включающие такие полипептидные композиции, и применение этих полипептидных композиций и иммунореактивных клеток, например, для лечения онкологических заболеваний.
В настоящем изобретении предложены полипептидные композиции. В некоторых вариантах осуществления полипептидная композиция включает: i) химерный антигенный рецептор (CAR) и ii) доминантно-негативную форму белка программируемой смерти 1 (PD-1 DN), где CAR включает: (a) внеклеточный антигенсвязывающий домен и (b) внутриклеточный сигнальный домен, включающий модифицированный полипептид CD3ζ, включающий вариант ITAM2 и вариант ITAM3, где каждый вариант ITAM2 и вариант ITAM3 включает две мутации с потерей функции.
В некоторых вариантах осуществления внеклеточный антигенсвязывающий домен включает: вариабельную область тяжелой цепи, включающую CDR1, включающую аминокислотную последовательность, представленную в SEQ ID NO: 76, CDR2, включающую аминокислотную последовательность, представленную в SEQ ID NO: 77, и CDR3, включающую аминокислотную последовательность, представленную в SEQ ID NO: 78 SEQ; и вариабельную область легкой цепи, включающую CDR1, включающую аминокислотную последовательность, представленную в SEQ ID NO: 79, CDR2, включающую аминокислотную последовательность, представленную в SEQ ID NO: 80, и CDR3, включающую аминокислотную последовательность, представленную в SEQ ID NO: 81.
В некоторых вариантах осуществления PD-1 DN включает: (a) по меньшей мере, часть внеклеточного домена белка программируемой смерти 1 (PD-1), включающую лигандсвязывающую область, и (b) первый трансмембранный домен.
В некоторых вариантах осуществления первый трансмембранный домен PD-1 DN включает полипептид CD8, полипептид CD28, полипептид CD3ζ, полипептид CD4, полипептид 4-1BB, полипептид OX40, полипептид CD166, полипептид CD166, полипептид CD8a, полипептид CD8b, полипептид ICOS, полипептид ICAM-1, полипептид CTLA-4, полипептид CD27, пептид CD40/My88, пептид NKGD2 или их комбинацию. В некоторых вариантах осуществления первый трансмембранный домен PD-1 DN включает полипептид CD8. В некоторых вариантах осуществления полипептид CD8, содержащийся в первом трансмембранном домене PD-1 DN, включает аминокислоты 137-207 из SEQ ID NO: 86. В некоторых вариантах осуществления PD-1 DN не имеет внутриклеточного домена. В некоторых вариантах осуществления PD-1 DN включает аминокислоты 21-165 из SEQ ID NO: 48 и аминокислоты 137-207 из SEQ ID NO: 86.
В некоторых вариантах осуществления внеклеточный антигенсвязывающий домен CAR специфично связывается с мезотелином человека со значением EC50 от приблизительно 1 нМ до приблизительно 25 нМ. В некоторых вариантах осуществления внеклеточный антигенсвязывающий домен CAR специфично связывается с мезотелином человека со значением EC50 приблизительно 20 нМ.
В некоторых вариантах осуществления внеклеточный антигенсвязывающий домен CAR включает одноцепочечный вариабельный фрагмент (scFv), Fab, который необязательно является сшитым, или F(ab)2. В некоторых вариантах осуществления внеклеточный антигенсвязывающий домен CAR включает человеческий scFv. В некоторых вариантах осуществления внеклеточный антигенсвязывающий домен CAR распознает мезотелин человека с уровнем экспрессии мезотелина приблизительно 1000 или больше связывающих сайтов мезотелина/клетка.
В некоторых вариантах осуществления вариабельная область тяжелой цепи включает аминокислотную последовательность, которая по меньшей мере приблизительно на 80%, по меньшей мере приблизительно на 81%, по меньшей мере приблизительно на 82%, по меньшей мере приблизительно на 83%, по меньшей мере приблизительно на 84%, по меньшей мере приблизительно на 85%, по меньшей мере приблизительно на 86%, по меньшей мере приблизительно на 87%, по меньшей мере приблизительно на 88%, по меньшей мере приблизительно на 89%, по меньшей мере приблизительно на 90%, по меньшей мере приблизительно на 91%, по меньшей мере приблизительно на 92%, по меньшей мере приблизительно на 93%, по меньшей мере приблизительно на 94%, по меньшей мере приблизительно на 95%, по меньшей мере приблизительно на 96%, по меньшей мере приблизительно на 97%, по меньшей мере приблизительно на 98%, по меньшей мере приблизительно на 99% или по меньшей мере приблизительно на 100% гомологична или идентична аминокислотной последовательности, представленной в SEQ ID NO: 82. В некоторых вариантах осуществления вариабельная область тяжелой цепи включает аминокислотную последовательность, представленную в SEQ ID NO: 82.
В некоторых вариантах осуществления вариабельная область легкой цепи включает аминокислотную последовательность, которая по меньшей мере приблизительно на 80%, по меньшей мере приблизительно на 81%, по меньшей мере приблизительно на 82%, по меньшей мере приблизительно на 83%, по меньшей мере приблизительно на 84%, по меньшей мере приблизительно на 85%, по меньшей мере приблизительно на 86%, по меньшей мере приблизительно на 87%, по меньшей мере приблизительно на 88%, по меньшей мере приблизительно на 89%, по меньшей мере приблизительно на 90%, по меньшей мере приблизительно на 91%, по меньшей мере приблизительно на 92%, по меньшей мере приблизительно на 93%, по меньшей мере приблизительно на 94%, по меньшей мере приблизительно на 95%, по меньшей мере приблизительно на 96%, по меньшей мере приблизительно на 97%, по меньшей мере приблизительно на 98%, по меньшей мере приблизительно на 99% или по меньшей мере приблизительно на 100% гомологична или идентична аминокислотной последовательности, представленной в SEQ ID NO: 83. В некоторых вариантах осуществления вариабельная область легкой цепи включает аминокислотную последовательность, представленную в SEQ ID NO: 83.
В некоторых вариантах осуществления вариабельная область тяжелой цепи включает аминокислотную последовательность, которая по меньшей мере приблизительно на 80%, по меньшей мере приблизительно на 81%, по меньшей мере приблизительно на 82%, по меньшей мере приблизительно на 83%, по меньшей мере приблизительно на 84%, по меньшей мере приблизительно на 85%, по меньшей мере приблизительно на 86%, по меньшей мере приблизительно на 87%, по меньшей мере приблизительно на 88%, по меньшей мере приблизительно на 89%, по меньшей мере приблизительно на 90%, по меньшей мере приблизительно на 91%, по меньшей мере приблизительно на 92%, по меньшей мере приблизительно на 93%, по меньшей мере приблизительно на 94%, по меньшей мере приблизительно на 95%, по меньшей мере приблизительно на 96%, по меньшей мере приблизительно на 97%, по меньшей мере приблизительно на 98%, по меньшей мере приблизительно на 99% или по меньшей мере приблизительно на 100% гомологична или идентична аминокислотной последовательности, представленной в SEQ ID NO: 82, и вариабельная область легкой цепи включает аминокислотную последовательность, которая по меньшей мере приблизительно на 80%, по меньшей мере приблизительно на 81%, по меньшей мере приблизительно на 82%, по меньшей мере приблизительно на 83%, по меньшей мере приблизительно на 84%, по меньшей мере приблизительно на 85%, по меньшей мере приблизительно на 86%, по меньшей мере приблизительно на 87%, по меньшей мере приблизительно на 88%, по меньшей мере приблизительно на 89%, по меньшей мере приблизительно на 90%, по меньшей мере приблизительно на 91%, по меньшей мере приблизительно на 92%, по меньшей мере приблизительно на 93%, по меньшей мере приблизительно на 94%, по меньшей мере приблизительно на 95%, по меньшей мере приблизительно на 96%, по меньшей мере приблизительно на 97%, по меньшей мере приблизительно на 98%, по меньшей мере приблизительно на 99% или по меньшей мере приблизительно на 100% гомологична или идентична аминокислотной последовательности, представленной в SEQ ID NO: 83. В некоторых вариантах осуществления вариабельная область тяжелой цепи включает аминокислотную последовательность, представленную в SEQ ID NO: 82, а вариабельная область легкой цепи включает аминокислотную последовательность, представленную в SEQ ID NO: 83.
В некоторых вариантах осуществления внеклеточный антигенсвязывающий домен CAR включает линкер между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи.
В некоторых вариантах осуществления лидерная последовательность, ковалентно связана с N-концом внеклеточного антигенсвязывающего домена. В некоторых вариантах осуществления лидерная последовательность включает полипептид CD8. В некоторых вариантах осуществления полипептид CD8 состоит из аминокислотной последовательности, представленной в SEQ ID NO: 71. В некоторых вариантах осуществления по меньшей мере часть внеклеточного домена PD-1 включает аминокислоты 21-165 из SEQ ID NO: 48.
В некоторых вариантах осуществления каждая из мутаций с потерей функции в модифицированном полипептиде CD3ζ CAR присутствует в положении остатка аминокислоты тирозина. В некоторых вариантах осуществления вариант ITAM2 включает или состоит из аминокислотной последовательности, представленной в SEQ ID NO: 29. В некоторых вариантах осуществления вариант ITAM3 включает или состоит из аминокислотной последовательности, представленной в SEQ ID NO: 33. В некоторых вариантах осуществления модифицированный полипептид CD3ζ включает нативный ITAM1. В некоторых вариантах осуществления нативный ITAM1 включает или состоит из аминокислотной последовательности, представленной в SEQ ID NO: 23. В некоторых вариантах осуществления модифицированный полипептид CD3ζ включает или состоит из аминокислотной последовательности, представленной в SEQ ID NO: 35.
В некоторых вариантах осуществления CAR включает или состоит из аминокислотной последовательности, представленной в SEQ ID NO: 56.
В некоторых вариантах осуществления CAR дополнительно включает второй трансмембранный домен. В некоторых вариантах осуществления второй трансмембранный домен CAR включает полипептид CD8, полипептид CD28, полипептид CD3ζ, полипептид CD4, полипептид 4-1BB, полипептид OX40, полипептид CD166, полипептид CD166, полипептид CD8a, полипептид CD8b, полипептид ICOS, полипептид ICAM-1, полипептид CTLA-4, полипептид CD27, пептид CD40/My88, пептид NKGD2 или их комбинацию. В некоторых вариантах осуществления второй трансмембранный домен CAR включает полипептид CD28
В некоторых вариантах осуществления внутриклеточный сигнальный домен CAR дополнительно включает костимулирующий сигнальный домен. В некоторых вариантах осуществления, костимулирующая сигнализация область включает полипептид CD28, полипептид 4-1BB, полипептид OX40, полипептид ICOS, полипептид DAP-10, полипептид CD27, полипептид CD40/My88, полипептид NKGD2 или их комбинации. В некоторых вариантах осуществления, костимулирующая сигнализация область включает полипептид CD28.
В настоящем изобретении предложены иммунореактивные клетки, включающие полипептидную композицию, раскрытую в настоящем документе. В некоторых вариантах осуществления PD-1 DN и/или CAR экспрессирован рекомбинантно. В некоторых вариантах осуществления PD-1 DN и/или CAR экспрессируется с вектора. В некоторых вариантах осуществления иммунореактивная клетка выбрана из группы, состоящей из T-клетки, естественной киллерной (NK) клетки, плюрипотентной стволовой клетки, из которой могут дифференцироваться лимфоидные клетки. В некоторых вариантах осуществления плюрипотентная стволовая клетка является эмбриональной стволовой клеткой или индуцированными плюрипотентными стволовыми клетками. В некоторых вариантах осуществления иммунореактивная клетка является T-клеткой. В некоторых вариантах осуществления T-клетка выбрана из группы, состоящей из цитотоксического T-лимфоцита (CTL), регуляторной T-клетки и естественной киллерной Т (NKT) клетки. В некоторых вариантах осуществления иммунореактивная клетка является аутологичной. В некоторых вариантах осуществления иммунореактивная клетка является аллогенной.
В настоящем изобретении также предложены композиции, включающие иммунореактивную клетку, раскрытую в настоящем документе. В некоторых вариантах осуществления композиция является фармацевтической композицией, дополнительно включающей фармацевтически приемлемое вспомогательное вещество. В некоторых вариантах осуществления фармацевтическая композиция включает от приблизительно 104 до 106 иммунореактивных клеток. В некоторых вариантах осуществления фармацевтическая композиция включает по меньшей мере приблизительно 105 иммунореактивных клеток. В некоторых вариантах осуществления фармацевтическая композиция включает приблизительно 105 иммунореактивных клеток. В некоторых вариантах осуществления фармацевтическая композиция предназначена для предупреждения и/или лечения неоплазии у субъекта, лечения субъекта, имеющего рецидив неоплазии, снижения опухолевой нагрузки у субъекта, увеличения или продления выживаемости субъекта, имеющего неоплазию, предупреждения и/или лечения воспалительного заболевания у субъекта, и/или предотвращения отторжения трансплантата у субъекта, который является реципиентом трансплантата органа.
Кроме того, в настоящем изобретении предложены композиции нуклеиновых кислот, включающие полинуклеотид, кодирующий полипептидную композицию, раскрытую в настоящем документе. В некоторых вариантах осуществления полинуклеотид включает нуклеотидную последовательность, представленную в SEQ ID NO: 123. В некоторых вариантах осуществления полинуклеотид включает нуклеотидную последовательность, представленную в SEQ ID NO: 124. В настоящем изобретении также предложены векторы, включающие раскрытые в настоящем документе композиции нуклеиновых кислот. В некоторых вариантах осуществления вектор является ретровирусным вектором. В некоторых вариантах осуществления ретровирусный вектор является γ-ретровирусным вектором или лентивирусным вектором.
В настоящем изобретении предложены способы получения иммунореактивной клетки, раскрытой в настоящем документе. В некоторых вариантах осуществления способ включает введение в иммунореактивную клетку раскрытой в настоящем документе полипептидной композиции, раскрытой в настоящем документе композиции нуклеиновой кислоты или раскрытого в настоящем документе вектора.
В настоящем изобретении предложены наборы, включающие раскрытую в настоящем документе полипептидную композицию, раскрытую в настоящем документе композицию нуклеиновой кислоты, раскрытый в настоящем документе вектор, раскрытую в настоящем документе иммунореактивную клетку или раскрытую в настоящем документе фармацевтическую композицию. В некоторых вариантах осуществления набор дополнительно включает письменные инструкции по лечению и/или предупреждению опухоли.
Кроме того, в настоящем изобретении предложены различные способы применения описанной выше иммунореактивной клетки. Например, в настоящем изобретении предложены способы снижения опухолевой нагрузки у субъекта, где способ включает введение субъекту эффективного количества иммунореактивных клеток или фармацевтической композиции, раскрытой в настоящем документе. В некоторых вариантах осуществления способ снижает количество опухолевых клеток, уменьшает размер опухоли и/или устраняет опухоль у субъекта.
В настоящем изобретении также предложены способы увеличения или продления выживаемости субъекта, имеющего неоплазию, где способ включает введение субъекту эффективного количества раскрытой в настоящем документе иммунореактивной клетки или раскрытой в настоящем документе фармацевтической композиции.
В некоторых вариантах осуществления опухоль или неоплазия является солидной опухолью. В некоторых вариантах осуществления солидная опухоль выбрана из группы, состоящей из мезотелиомы, рака легкого, рака поджелудочной железы, рака яичника, рака молочной железы, рака толстой кишки, плевральной опухоли, глиобластомы, рака пищевода, рака желудка, синовиальной саркомы, карциномы тимуса, карциномы эндометрия, рака желудка, холангиокарциномы, рака шейки матки, рака слюнных желез и их комбинации.
В настоящем изобретении предложены способы лечения субъекта, имеющего рецидив неоплазии, где способ включает введение субъекту эффективного количества иммунореактивных клеток или фармацевтической композиции, раскрытой в настоящем документе. В некоторых вариантах осуществления субъект получал иммунотерапию до указанного введения иммунореактивных клеток или композиции.
Кроме того, в настоящем изобретении предложены способы повышения продукции иммуноактивирующего цитокина в ответ на раковую клетку или патоген у субъекта. В некоторых вариантах осуществления способ включает введение субъекту эффективного количества иммунореактивных клеток или фармацевтической композиции, раскрытой в настоящем документе. В некоторых вариантах осуществления иммуноактивирующий цитокин выбран из группы, состоящей из гранулоцитарно-макрофагального колониестимулирующего фактора (ГМ-КСФ), IFN-α, IFN-β, IFN-γ, ФНО-α, IL-2, IL-3, IL-6, IL-11, IL-7, IL-12, IL-15, IL-21, регуляторный фактор интерферона 7 (IRF7) и их комбинаций.
В соответствии с раскрытым в настоящем документе изобретением, различные вышеописанные способы могут включать введение по меньшей мере одного иммуномодулирующего средства. В некоторых вариантах осуществления по меньшей мере одно иммуномодулирующее средство выбрано из группы, состоящей из иммуностимулирующих средств, блокаторов иммунных контрольных точек, радиотерапевтических средств, химиотерапевтических средств и их комбинаций. В некоторых вариантах осуществления иммуностимулирующие средства выбраны из группы, состоящей из IL-12, агонистического костимулирующего моноклонального антитела и их комбинаций. В некоторых вариантах осуществления иммуностимулирующим средством является IL-12. В некоторых вариантах осуществления агонистическое костимулирующее моноклональное антитело выбрано из группы, состоящей из антитела против 4-1BB, антитела против OX40, антитела против ICOS и их комбинаций. В некоторых вариантах осуществления агонистическое костимулирующее моноклональное антитело является антителом против 4-1BB. В некоторых вариантах осуществления блокаторы иммунных контрольных точек выбран из группы, состоящей из антител против PD-L1, антител против CTLA-4, антител против PD-1, антител против LAG3, антител против B7-H3, антител против TIM3 и их комбинаций. В некоторых вариантах осуществления блокатор иммунной контрольной точки является антителом против PD-L1 или антителом против PD-1. В некоторых вариантах осуществления субъектом является человек.
В некоторых вариантах осуществления иммунореактивную клетку вводят субъекту плеврально или внутриплеврально.
В настоящем изобретении также предложен способ предупреждения и/или лечения воспалительного заболевания у субъекта. В некоторых вариантах осуществления способ включает введение субъекту раскрытой в настоящем документе иммунореактивной клетки или фармацевтической композиции. В некоторых вариантах осуществления иммунореактивная клетка является иммуноингибирующей клеткой. В некоторых вариантах осуществления иммуноингибирующая клетка является регуляторной T-клеткой. В некоторых вариантах осуществления воспалительным заболеванием является панкреатит. В некоторых вариантах осуществления субъектом является человек. В некоторых вариантах осуществления субъектом является реципиент трансплантат органа. В некоторых вариантах осуществления субъектом является реципиент трансплантата поджелудочной железы.
В настоящем изобретении также предложен способ предотвращения отторжения трансплантата у субъекта, который является реципиентом трансплантата органа. В некоторых вариантах осуществления способ включает введение субъекту раскрытой в настоящем документе иммунореактивной клетки или фармацевтической композиции. В некоторых вариантах осуществления иммунореактивная клетка является иммуноингибирующей клеткой. В некоторых вариантах осуществления иммуноингибирующая клеткой является регуляторной T-клеткой. В некоторых вариантах осуществления субъектом является человек. В некоторых вариантах осуществления субъектом является реципиент трансплантата поджелудочной железы.
4. КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Следующее подробное описание, представленное в качестве примера, но не предназначенное для ограничния раскрытого в настоящем документе изобретения конкретными описанными вариантами осуществления, может быть понято в сочетании с прилагаемыми чертежами.
На Фигуре 1 изображена полипептидная композиция в соответствии с некоторыми вариантами осуществления раскрытого в настоящем документе изобретения. Полипептидная композиция включает CAR, включающий scFv против мезотелина (MSLN), трансмембранный домен CD28, цитоплазматический сигнальный домен CD28, сигнальный домен CD3дзета (например, включающий вариант ITAM2 и вариант ITAM3). CAR слит с PD1DNR (и сигнальным доменом PD-1) через расщепляемый пептид P2A. SP: сигнальный пептид; scFv: одноцепочечный вариабельный фрагмент; ТМ: трансмембранный домен; cyt: цитозольный домен; DNR: доминантно-негативный рецептор; LTR: длинный концевой повтор.
На Фигуре 2 изображены различные конструкции, раскрытые в Примере 2.
На Фигурах 3A-3D показана продукция вируса в линии клеток-продуцентов RD114. Клетки RD114 трансдуцировали различными разведениями вирусного супернатанта H29 (неразведенный, 1:2 и 1:4) и окрашивали на экспрессию CAR с помощью проточной цитометрии с использованием антитела против Fab. Пустые RD114 служили в качестве отрицательного контроля. На Фигуре 3A показаны пустые RD114 (в качестве отрицательного контроля). На Фигуре 3B показан неразведенный супернатант. На Фигуре 3C показан супернатант в разведении 1:2; и на Фигуре 3D показан супернатант в разведении 1:4.
На Фигурах 4A-4E показана трансдукция человеческих T-клеток M28z1XX-P2A-PD1DNR - донором H116-2. ФГА-активированные T-клетки трансдуцировали различными концентрациями вирусного супернатанта RD114 (на Фигуре 4A показано разведение 1:2, на Фигуре 4B показано разведение 1:5, на Фигуре 4C показано разведение 1:7, на Фигуре 4D показано разведение 1:15 и на Фигуре 4E показаны нетрансдуцированные ("UT") клетки) и окрашивали на экспрессию CAR антителом против Fab и на PD1DNR антителом против PD1 с помощью проточной цитометрии.
На Фигурах 5A-5E показана трансдукция человеческих T-клеток M28z1XX-P2A-PD1DNR - донором H18. ФГА-активированные T-клетки трансдуцировали различными концентрациями вирусного супернатанта RD114 (на Фигуре 5A показано разведение 1:2, на Фигуре 5B показано разведение 1:5, на Фигуре 5C показано разведение 1:10, на Фигуре 5D показано разведение 1:15 и на Фигуре 5E показаны нетрансдуцированные ("UT") клетки) и окрашивали на экспрессию CAR антителом против Fab и на PD1DNR антителом против PD1 с помощью проточной цитометрии.
На Фигурах 6A-6F показана трансдукция человеческих T-клеток M28z1XX-P2A-PD1DNR - донором H19. ФГА-активированные T-клетки трансдуцировали различными концентрациями вирусного супернатанта RD114 (На Фигуре 6A показано разведение 1:2, на Фигуре 6B показано разведение 1:5, на Фигуре 6C показано разведение 1:7; на Фигуре 6D показано разведение 1:10, на Фигуре 6E показано разведение 1:15 и на Фигуре 6F показаны нетрансдуцированные ("UT") клетки) и окрашивали на экспрессию CAR антителом против Fab и на PD1DNR антителом против PD1 с помощью проточной цитометрии.
На Фигурах 7A-7C показана корреляция числа копий вектора (VCN) со средней интенсивностью флуоресценции (MFI). ФГА-активированные T-клетки трансдуцировали различными концентрациями вирусного супернатанта RD114 и окрашивали на экспрессию CAR антителом против Fab и с помощью проточноцитометрического анализа. Геномную ДНК трансдуцированных T-клеток выделяли и определяли число копий вектора как VCN/мкг ДНК с помощью кПЦР. MFI CAR-положительных клеток коррелировали с VCN/мкг ДНК для трех разных доноров. На Фигуре 7A показан донор H19; на Фигуре 7B показан донор H18 и на Фигуре 7C показан донор H116-2.
На Фигуре 8 показана цитотоксичность для трансдуцированных T-клеток от 3 разных доноров. Клетки-мишени с высоким уровнем MSLN (MGM) культивировали совместно с M28z1xx-PD1DNR CAR T-клетками разных доноров при разном отношении E:T при использовании анализа на основе электрического сопротивления. M28z1xx-PD1DNR CAR T-клетка опосредовала цитолиз клеток MGM при отношении E:T 1:1. M28z1xx-PD1DNR CAR T-клетки убивали клетки-мишени с высоким уровнем MSLN.
На Фигуре 9 показан пример измерения цитотоксичности на основе электрического сопротивления (eCTL).
На Фигуре 10 показаны параметры сравнительного анализа различных конструкций с помощью eCTL.
На Фигурах 11A-11E показана экспрессия MSLN и PD-L1 линий клеток-мишеней. Линии клеток мезотелиомы (MGM (показанная на Фигуре 11A), MGM-PDL1 (показанная на Фигуре 11B) и MSTOG (показанная на Фигуре 11C)) и рака легкого (A549GM (показанная на Фигуре 11D) и A549G (показанная на Фигуре 11e)) оценивали на экспрессию MSLN и PD-L1 с помощью проточной цитометрии. MGM, MGM-PDL1 и A549GM повышенно экспрессировали MSLN; клетки MGM-PDL1 дополнительно показали оверэкспрессию PD-L1.
На Фигурах 12A-12E показана экспрессия CAR и PD-1 в трансдуцированных T-клетках. Человеческие T-клетки, трансдуцированные M28z (как показано на Фигуре 12A), M28z1xx (как показано на Фигуре 12B), M28z-PD1DNR (как показано на Фигуре 12C) и M28z1xx-PD1DNR (как показано на Фигуре 12D), анализировали на экспрессию CAR при окрашивании антителом против myc и на экспрессию PD1/PD1DNR при окрашивании антителом против PD1 с помощью проточной цитометрии. На Фигуре 12E показаны нетрансдуцированные ("UT") T-клетки.
На Фигурах 13A-13C показан сравнительный анализ противоопухолевой эффективности CAR T-клеток, несущих 1XX домен и PD1DNR, в отношении опухолевых клеток с высоким уровнем MSLN (MGM). Клетки-мишени с высоким уровнем MSLN (MGM) совместно культивировали с одним из M28z, M28z1xx, M28z-PD1DNR, M28z1XX-PD1DNR или с нетрансдуцированными T-клетками при указанных отношениях E:T. Противоопухолевую эффективность оценивали с помощью анализа на основе электрического сопротивления. На Фигуре 13A показано отношение E:T приблизительно 3:1. На Фигуре 13B показано отношение E:T приблизительно 1:1. На Фигуре 13C показано отношение E:T приблизительно 0,33:1.
На Фигуре 14 показан сравнительный анализ цитотоксичности CAR T-клеток, несущих 1xx домен и PD1DNR, в отношении опухолевых клеток с высоким уровнем MSLN (MGM). Клетки-мишени с высоким уровнем MSLN (MGM), меченые хромом-51, совместно культивировали с одним из M28z, M28z1xx, M28z-PD1DNR, M28z1xx-PD1DNR или с нетрансдуцированными T-клетками при указанном отношении E:T в течение 18 часов. Цитотоксичность определяли по высвобождению хрома-51 CTL.
На Фигурах 15A-15C показан сравнительный анализ противоопухолевой эффективности CAR T-клеток, несущих 1xx домен и PD1DNR, в отношении MSLN-отрицательных опухолевых клеток (MSTOG). MSLN-отрицательные клетки-мишени (MSTOG) совместно культивировали с одним из M28z, M28z1xx, M28z-PD1DNR, M28z1xx-PD1DNR или с нетрансдуцированными T-клетками при указанных отношениях E:T. Противоопухолевую эффективность оценивали с помощью анализа на основе электрического сопротивления. На Фигуре 15A показано отношение E:T приблизительно 3:1. На Фигуре 15B показано отношение E:T приблизительно 1:1. На Фигуре 15C показано отношение E:T приблизительно 0,33:1.
На Фигуре 16 показан сравнительный анализ цитотоксичности CAR T-клеток, несущих 1XX домен и PD1DNR, в отношении MSLN-отрицательных опухолевых клеток (MSTOG). MSLN-отрицательные клетки-мишени (MSTOG), меченые хромом-51, совместно культивировали с одним из M28z, M28z1XX, M28z-PD1DNR, M28z1XX-PD1DNR или с нетрансдуцированными T-клетками при указанном отношении E:T в течение 18 часов. Цитотоксичность определяли по высвобождению хрома-51 CTL.
На Фигурах 17A-17C показан сравнительный анализ противоопухолевой эффективности CAR T-клеток, несущих 1XX домен и PD1DNR, в отношении опухолевых клеток с высоким уровнем MSLN и оверэкспрессией PDL1. Клетки-мишени с высоким уровнем MSLN и оверэкспрессией PDL1 (MGM-PDL1) совместно культивировали с одним из M28z, M28z1XX, M28z-PD1DNR, M28z1XX-PD1DNR или с нетрансдуцированными T-клетками при указанных отношениях E:T. Противоопухолевую эффективность оценивали с помощью анализа на основе электрического сопротивления. На Фигуре 17A показано отношение E:T приблизительно 3:1. На Фигуре 17B показано отношение E:T приблизительно 1:1. На Фигуре 17C показано отношение E:T приблизительно 0,33:1.
На Фигурах 18A-18C показан сравнительный анализ противоопухолевой эффективности CAR T-клеток, несущих 1xx домен и PD1DNR, в отношении опухолевых клеток с высоким уровнем MSLN (A549GM). Клетки-мишени с высоким уровнем MSLN (A549GM) совместно культивировали с одним из M28z, M28z1xx, M28z-PD1DNR, M28z1xx-PD1DNR или с нетрансдуцированными T-клетками при указанных отношениях E:T. Противоопухолевую эффективность оценивали с помощью анализа на основе электрического сопротивления. На Фигуре 18A показано отношение E:T приблизительно 10:1. На Фигуре 18B показано отношение E:T приблизительно 5:1. На Фигуре 18C показано отношение E:T приблизительно 2:1.
На Фигурах 19A-19C показан сравнительный анализ противоопухолевой эффективности CAR T-клеток, несущих 1xx домен и PD1DNR, в отношении опухолевых клеток с низким уровнем MSLN (A549G). Клетки-мишени с низким уровнем MSLN (A549G) совместно культивировали с одним из M28z, M28z1xx, M28z-PD1DNR, M28z1xx-PD1DNR или с нетрансдуцированными T-клетками при указанных отношениях E:T. Противоопухолевую эффективность оценивали с помощью анализа на основе электрического сопротивления. На Фигуре 19A показано отношение E:T приблизительно 10:1. На Фигуре 19B показано отношение E:T приблизительно 5:1. На Фигуре 19C показано отношение E:T приблизительно 2:1.
На Фигурах 20A-20D показаны результаты различного лечения в исследовании in vivo. На Фигуре 20A показана сравнительная in vivo эффективность CAR T-клеток - M28z, M28z с антителом PD-1 и M28z с PD1DNR. На Фигуре 20B показана сравнительная in vivo эффективность M28z и M28z1XX+PD1DNR CAR T-клеток. На Фигуре 20C показана визуализация опухолевой нагрузки, демонстрирующая системный противоопухолевый иммунитет после повторного введения опухолей. На Фигуре 20D показано иммунофлуоресцентное окрашивание ex vivo ортотопических опухолей MPM, демонстрирующее инфильтрацию CAR T-клеток.
На Фигуре 21 показана структура и компоненты M28z1XXPD1DNR CAR. В отличие от M28z, M28z1XXPD1DNR CAR T-клетки несут мутантный сигнальный домен CD3ζ с одним функциональным ITAM и коэкспрессируют PD1DNR, который состоит из трансмембранного и шарнирного доменов CD8 и не имеет внутриклеточного сигнального домена PD-1, присутствующего в эндогенном PD1.
На Фигуре 22 показана структура векторов CAR T-клеток.
На Фигуре 23 показана экспрессия мезотелина (MSLN), PD-L1 и GFP на линиях опухолевых клеток. Опухолевые клетки MGM, MGM-PDL1 и MSTOG исследовали на экспрессию мезотелина (панели слева), PD-L1 (средние панели) и GFP (панели справа) с помощью проточной цитометрии. Показаны графики плотности, демонстрирующие относительную интенсивность экспрессии в зависимости от площади бокового рассеяния (ось Y).
На Фигурах 24A-24D показана модель ортотопической MPM на мышах. На Фигуре 24A показана макроскопическая картина человеческой MPM (верхняя панель слева), воспроизведенной в модели MPM на мышах (верхняя панель справа), с охватом опухолью сердца, легких и структур средостения, и опухоль, внедрившаяся в грудную стенку (нижняя панель). На Фигуре 24B показана обширная васкуляризация опухоли, демонстрируемая иммунофлуоресценцией CD34. На Фигуре 24C показано, что прогрессирование опухолевой нагрузки, наблюдаемое с помощью BLI, коррелирует с измерениями объема опухоли с помощью МРТ в соответствующих точках времени. На Фигуре 24D показано прогрессирование опухолевой нагрузки, наблюдаемое с помощью последовательных BLI и МРТ.
На Фигурах 25A-25C показана экспрессия мезотелина в человеческих тканях с помощью иммуногистохимического анализа. На Фигуре 25A показана экспрессия мезотелина в MPM по сравнению с нормальной плеврой и перикардом. На Фигуре 25B показана экспрессия мезотелина в аденокарциноме легкого по сравнению с нормальной тканью легкого. На Фигуре 25C показана экспрессия мезотелина в трижды негативном раке молочной железы по сравнению с нормальной тканью молочных желез.
На Фигуре 26 показано, что экспрессию M28z1XXPD1DNR можно титровать с использованием различных разведений вирусного супернатанта. Человеческие T-клетки трансдуцировали различными разведениями вирусного супернатанта, кодирующего M28z1XXPD1DNR (левые панели) или mycM28z1XXPD1DNR (средние панели). Экспрессию CAR (ось Y) и PD1 (ось X) жизнеспособных CD3-положительных клеток оценивали с помощью проточной цитометрии. Представленные результаты получены у 1 донора, репрезентативного для 3 разных доноров.
На Фигуре 27 показано, что экспрессия CAR, измеренная по MFI, коррелирует с VCN. Человеческие T-клетки, полученные от 3 разных доноров, трансдуцировали разными разведениями ретровирусного супернатанта, кодирующего либо M28z1XXPD1DNR, либо mycM28z1XXPD1DNR. Значения MFI CAR-положительных T-клеток (определенные с помощью проточной цитометрии) наносили на график в зависимости от VCN (определенного с помощью кПЦР). Значение R2 было получено из линейно-регрессионного анализа (черная линия).
На Фигурах 28A-28D показана экспрессия PD-1 и PD1DNR в mycM28z1XXPD1DNR и mycM28z CAR T-клетках. На Фигуре 28A показан процента поверхностной экспрессии CAR на mycM28z и mycM28z1XXPD1DNR CAR T-клетках. На Фигуре 28B показан процент CD3-положительных клеток, положительных на поверхностную экспрессию PD-1. На Фигуре 28C показаны MFI экспрессии PD-1 на поверхности CD3-положительных клеток. На Фигуре 28D показана относительная экспрессия мРНК внеклеточного и внутриклеточного домена PD1, показанная как кратное изменение по сравнению с экспрессией нетрансдуцированных T-клеток.
На Фигуре 29 показано, что M28z1XXPD1DNR-экспрессирующие T-клетки с или без myc-метки демонстрируют идентичную противоопухолевую эффективность in vitro. Человеческие T-клетки, полученные от 3 разных доноров, трансдуцировали либо с M28z1XXPD1DNR (красный), либо mycM28z1XXPD1DNR (зеленый) (диапазон трансдукции, 37%-63%) и совместно культивировали с клетками MGM (зеленый; стрелка указывает время добавления T-клеток). Противоопухолевую эффективность обеих конструкций сравнивали при указанных отношениях E:T с помощью анализа цитотоксичности на основе электрического сопротивления.
На Фигуре 30 показано, что mycM28z1XXPD1DNR CAR T-клетки опосредуют антигенспецифический HLA-независимый лизис опухоли. Человеческие T-клетки, трансдуцированные mycM28z1XXPD1DNR (синий) или mycM28z (красный), совместно культивировали с одними из опухолевых клеток MGM, MGM-PDL1 или MSTOG при указанных отношениях E:T. Цитотоксичность CAR T-клеток оценивали с помощью анализа высвобождения 51Cr после 18 ч совместного культивирования. Нетрансдуцированные (оранжевый) T-клетки служили в качестве контроля.
На Фигуре 31 показано накопление mycM28z1XXPD1DNR CAR T-клеток при стимуляции мезотелин-экспрессирующими опухолевых клетками. Человеческие T-клетки, трансдуцированные mycM28z1XXPD1DNR (синий) или mycM28z (красный), неоднократно подвергали контакту с клетками-мишенями MGM или MGM-PDL1 в течение 48 ч при отношении E:T 1:1. Накопление CAR T-клеток количественно определяли при подсчете абсолютного количества CAR T-клеток после каждой стимуляции антигеном.
На Фигуре 32 показано, что mycM28z1XXPD1DNR CAR T-клетки демонстрировали аналогичную цитотоксичность, как mycM28z CAR T-клетки при первоначальной стимуляции антигеном. Человеческие T-клетки, трансдуцированные mycM28z1XXPD1DNR (синий) или mycM28z (красный), совместно культивировали с 51Cr-меченными клетками-мишенями MGM или MGM-PDL1 при указанных отношениях E:T. Цитотоксичность оценивали после 18 ч с помощью анализа высвобождения 51Cr. Нетрансдуцированные T-клетки (оранжевый) служили в качестве контроля.
На Фигуре 33 показано, что mycM28z1XXPD1DNR CAR T-клетки сохраняли противоопухолевая эффективность при повторной стимуляции антигеном. Человеческие T-клетки, трансдуцированные mycM28z1XXPD1DNR (синий) или mycM28z (красный), повторно подвергали контакту с клетками-мишенями MGM (панели слева) или MGM-PDL1 (панели справа) в течение 48 ч при отношении E:T 3:1 в ходе 4 стимуляций, с 2 последующими дополнительными стимуляциями при отношении E:T 1:1. Цитотоксичность CAR T-клеток оценивали с помощью анализа высвобождения 51Cr в ходе четвертой и седьмой стимуляции антигеном при указанных отношениях E:T, после 18 ч совместного культивирования.
На Фигуре 34 показано, что mycM28z1XXPD1DNR CAR T-клетки секретировали эффекторные цитокины при стимуляции антигеном. Человеческие T-клетки, трансдуцированные mycM28z1XXPD1DNR (синий) или mycM28z (красный), повторно подвергали контакту с клетками-мишенями MGM (верхний ряд) или MGM-PDL1 (нижний ряд) в течение 48 ч при отношении E:T 1:1. Бесклеточный супернатант собирали через 24 ч после первой, третьей и шестой стимуляции антигеном, и оценивали секрецию эффекторных цитокинов с помощью анализа Luminex.
На Фигуре 35 показано, что внутриплевральное введение однократной низкой дозы 3×104 mycM28z1XXPD1DNR CAR T-клеток демонстрирует противоопухолевую эффективность in vivo. Самки мышей NSG, несущие ортотопическую опухоль MGM, получали однократную внутриплевральную дозу либо P28z CAR T-клеток (n=6, красный столбец), либо mycM28z1XXPD1DNR CAR T-клеток (n=10, синий столбец). Опухолевую нагрузку измеряли с помощью BLI. Указанная точка времени представляет день 15 после введения CAR T-клеток, когда мыши, получавшие P28z CAR T-клетки, начали погибать. Статистическую значимость определяли при использовании непарного t-критерия Стьюдента (2-стороннего). ***p<0,001.
На Фигурах 36A-36D показано, что внутриплеврально введенные mycM28z1XXPD1DNR CAR T-клетки демонстрировали противоопухолевую эффективность in vivo и увеличивали выживаемость. На Фигуре 3A показаны серии снимков BLI опухолей MGM-PDL1 опухоленесущих самок мышей NSG, получавших однократную дозу mycM28z (1×105) или mycM28z1XXPD1DNR (1×105 или 5×104) CAR T-клеток (n=7-8). Показаны 4 мыши в каждой группе лечения в вентральном положении. На Фигуре 36B показаны соответствующие серии снимков BLI опухолей (среднее дорсальных и вентральных), показывающие опухолевую нагрузку каждой мыши, подвергнутой лечению. На Фигуре 36C показаны соответствующий вес мышей после лечения. На Фигуре 36D показан анализ выживаемости Каплана-Мейера, в котором сравнивали эффективность mycM28z и mycM28z1XXPD1DNR CAR T-клеток in vivo. Кривую выживаемости анализировали с использованием логрангового критерия. *p<0,05, **p<0,01.
На Фигуре 37 показано обнаружение mycM28z1XXPD1DNR CAR T-клеток в первичной опухоли мышей после внутриплеврального лечения. Плевральная опухоль MGM мышей, получавших 5×105 нетрансдуцированных T-клеток (слева), mycM28z CAR T-клеток (середина) или mycM28z1XXPD1DNR CAR T-клеток (справа). Опухолевую ткань собирали через 3 дня после внутриплевральной инъекции T-клеток, фиксировали и окрашивали ex vivo на опухолевый мезотелин (зеленый), человеческие CD45-положительные клетки (красный) и DAPI (ядро клетки, синий) с помощью иммунофлуоресценции.
На Фигурах 38A и 38B показано, что mycM28z1XXPD1DNR CAR T-клетки препятствовали повторному приживлению опухоли при повторном введении опухоли in vivo. На Фигуре 38A показана схема, иллюстрирующая эксперимент по повторному введению опухоли: через 68 дней после внутриплеврального введения mycM28z или mycM28z1XXPD1DNR CAR T-клеток (однократной дозы 1×105 CAR T-клеток) и после плевральной эрадикации опухолевых клеток MGM-PDL1 (инокулируемая доза 8×105), мышей внутрибрюшинно повторно заражали 10 раз повышаемыми дозами (от 2×106 до 11×106) опухолевых клеток MGM каждые 4-8 дней. На Фигуре 38B показаны серии снимков BLI, демонстрирующие опухолевую нагрузку после однократной внутриплевральной дозы mycM28z (2 мыши, красные линии) или mycM28z1XXPD1DNR (3 мыши, черные линии) CAR T-клеток и повторного введения опухоли, начиная в день лечения 68. Черные стрелки указывают точки времени повторного внутрибрюшинного заражения опухолями с повышаемыми дозами.
На Фигурах 39A-39C показано, что M28z1XXPD1DNR CAR T-клетки, изготовленные при использовании запасов векторов для клинического исследования, обладают противоопухолевой эффективностью in vivo и продлевают выживаемость. На Фигуре 39A показаны серии снимков BLI опухолей MGM у опухоленесущих самок мышей NSG, получавших 6×104 (n=8) или 2×105 (n=10) M28z1XXPD1DNR CAR T-клеток, изготовленных в CTCEF при использовании вирусного супернатанта для клинического исследования. На Фигуре 39B показан соответствующий вес мышей после лечения. На Фигуре 39C показан анализ выживаемости Каплана-Мейера.
На Фигуре 40 показаны средние массы тела при промежуточном умерщвлении самцов мышей. Показаны группы 1 (контроль без опухоли), 3 (контроль растворителем) и 5 (исследуемый препарат).
На Фигуре 41 показаны средние массы тела при промежуточном умерщвлении самок мышей. Показаны группы 2 (контроль без опухоли), 4 (контроль) и 6 (исследуемый препарат).
На Фигуре 42 показаны средние массы тела при окончательном умерщвлении самцов мышей. Показаны группы 7 (контроль без опухоли), 9 (контроль растворителем) и 11 (исследуемый препарат).
На Фигуре 43 показано средние массы тела при окончательном умерщвлении самок мышей. Показаны группы 8 (контроль без опухоли), 10 (контроль растворителем) и 12 (исследуемый препарат).
На Фигуре 44 показана идентификация человеческих T-клеток в опухолях мышей, получавших CAR T-клетки и получавших растворитель. Клетки внутриплевральной опухолевой ткани, полученные от мышей, получавших CAR T-клетки и получавших растворитель, окрашивали DAPI, конъюгатами антитела против CD45 человека АФЦ/CY7 и антитела против CD3 человека ФЭ/CY7 для обнаружения жизнеспособных T-клеток человека с помощью проточной цитометрии. Показаны диаграммы плотности экспрессии CD3 человека (ось X) и экспрессии CD45 человека (ось Y) в DAPI-отрицательных (живых) одиночных клетках. Гейт указывает клетки, положительно окрашенные на CD45 человека и CD3 человека, представляющие человеческие T-клетки.
На Фигуре 45 показана идентификация человеческих T-клеток в селезенке мышей, получавших CAR T-клетки и получавших растворитель. Клетки ткани селезенки, полученные у мышей, получавших CAR T-клетки и получавших растворитель, окрашивали DAPI, конъюгатами антитела против CD45 человека АФЦ/CY7 и антитела против CD3 человека ФЭ/CY7, для обнаружения жизнеспособных человеческих T-клеток с помощью проточной цитометрии. Показаны диаграммы плотности экспрессии CD3 человека (Ось X) и экспрессии CD45 человека (Ось Y) в DAPI-отрицательных (живых) одиночных клетках. Гейт указывает клетки, положительно окрашенные на CD45 человека и CD3 человека, представляющие человеческие T-клетки.
На Фигуре 46 показана BLI самцов мышей.
На Фигуре 47 показана BLI самок мышей.
5. ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В настоящем изобретении предложены полипептидные композиции, включающие химерный антигенный рецептор (CAR), направленно взаимодействующий с мезотелином и доминантно-негативной формой белка программируемой смерти 1 (PD-1 DN), и иммунореактивные клетки (например, T-клетки или NK-клетки) включающие полипептидные композиции. В настоящем изобретении также предложены способы применения такой полипептидной композиции для индукции и/или усиления иммунного ответа иммунореактивной клетки на антиген-мишень, и/или лечения и/или предупреждения неоплазий или других заболеваний/нарушений, где желательно уменьшение истощения иммунных клеток.
Постоянный контакт антигена с T-клетками, например, при раке, приводит к измененному состоянию дифференцировки T-клеток, называемому истощением, которое делает CAR T-клетки дисфункциональными (Youngblood et al., Int Immunol.2010; 22(10): 797-803; Wherry et al., Nat Rev Immunol.2015; 15(8): 486-499). Предыдущие исследования показали, что потенциал активации CAR связан с тремя ITAM (1-2-3), присутствующими в цитоплазматическом домене CD3ζ (Acuto et al., Nat Rev Immunol. 2003; 3(12): 939-951; Love et al., Cold Spring Harb Perspect Biol. 2010; 2(6): a002485). Недавние исследования показали, что такой потенциал активации CAR можно регулировать путем мутации мотивов ITAM, уменьшая тем самым их функциональность. Важно отметить, что было показано, что путем введения точечных мутаций во второе и третье положения мотивов ITAM (1-X-X; в настоящем документе обозначено как "1XX") домена CD3ζ, направление дифференцировки CAR T-клеток было изменено с истощающего терминального состояния на сбалансированное эффекторное состояние и состояние памяти в присутствии высокой антигенной стимуляции (Feucht et al., Nat Med. 2019; 25(1): 82-88).
Еще один барьер, с которым CAR T-клетки сталкиваются в микроокружении солидной опухоли - ингибирование их цитолитической активности, опосредуемое PD1, ингибирующим рецептором, который экспрессируется при антиген-опосредованной активации T-клеток. Кроме того, опухолевые клетки усиливают экспрессию коингибирующих лигандов, таких как PD-L1, после воздействия секретируемых T-клетками проапоптотических цитокинов (McGray et al., Mol Ther. 2014; 22(1): 206-218; Spranger et al., Sci Transl Med. 2013; 5(200): 200ra116; Moon et al., Clin Cancer Res. 2014; 20(16): 4262-4273). Чтобы преодолеть этот барьер, авторы изобретения объединили мезотелин-специфичные CAR T-клетки с блокирующими PD1 антителами для спасения истощенных CAR T-клеток, восстанавливая противоопухолевую эффективность CAR T-клеток в ортотопической модели на мышах (Cherkassky et al., J Clin Invest. 2016; 126(8): 3130-3144; Grosser et al., Cancer Cell. 2019; 36(5): 471-482). Чтобы избежать повторного введения доз блокаторов контрольной точки PD1 и ассоциированными с ними клинических побочных эффектов, авторы изобретения продемонстрировали, что применение естественной для клетки стратегии блокады контрольной точки PD1, при которой PD1DNR котрансдуцируют в T-клетку вместе с CAR второго поколения, в конечном счете делает трансдуцированные клетки устойчивыми к опосредованному опухолевым PD-L1 ингибированию в микроокружении солидной опухоли (Cherkassky et al., J Clin Invest. 2016; 126(8): 3130-3144; Grosser et al., Cancer Cell. 2019; 36(5): 471-482).
Следовательно, для разработки CAR T-клеток с улучшенным терапевтическим профилем, функциональным персистированием и устойчивостью к опосредованному опухолью ингибированию, авторы изобретения включили компоненты 1XX и PD1DNR в конструкцию вектора CAR второго поколения, что позволяет этим клеткам эффективно функционировать в крайне иммуносупрессивном микроокружении солидных опухолей.
В целях ясности раскрытия изобретения, но не ограничения, подробное описание разделено на следующие подразделы:
5.1. Определения;
5.2. Полипептидные композиции;
5.2.1. PD-1 DN;
5.2.2. Мезотелин-направленные CAR-рецепторы; и
5.2.3. Иллюстративные полипептидные композиции;
5.3. Иммунореактивные клетки;
5.4. Композиции нуклеиновых кислот и векторы;
5.5. Полипептиды и аналоги;
5.6. Фармацевтические композиции и введение;
5.7. Составы;
5.8. Способы лечения; и
5.9. Наборы
5.1. Определения
Если не определено иное, все технические и научные термины, используемые в настоящем документе, имеют значение, которое обычно известно специалисту в данной области.
При использовании в настоящем документе термин "приблизительно" или "примерно" означает в пределах допустимого диапазона ошибок для конкретного значения, как определено специалистом в данной области техники, которое будет частично зависеть от того, как измеряют или определяют значение, т.е. от ограничений системы измерения. Например, "приблизительно" может означать в пределах 3 или больше 3 стандартных отклонений в соответствии с практикой в данной области. В альтернативе "приблизительно" может означать диапазон до 20%, например, до 10%, до 5% или до 1% от данного значения. В альтернативе, в частности в отношении биологических систем или процессов, термин может означать в пределах порядка величины, например, в пределах 5-кратного или 2-кратного значения.
Под "иммунореактивной клеткой" подразумевается клетка, которая функционирует в иммунном ответе, или ее предшественник или потомство.
Под "активирует иммунореактивную клетку" подразумевается индукция передачи сигналов или изменений экспрессии белка в клетке, приводящие к инициации иммунного ответа. Например, когда цепи CD3 группируются в ответ на связывание лиганда и иммунорецепторные тирозиновые ингибирующие мотивы (ITAM), формируется каскад передачи сигнала. В некоторых вариантах осуществления, при связывании химерного антигенного рецептора (CAR) с антигеном происходит образование иммунологического синапса, который включает кластеризацию многих молекул вблизи от связанного рецептора (например, CD4 или CD8, CD3γ/δ/ε/ζ и т.д.). Такая кластеризация мембраносвязанных сигнальных молекул позволяет фосфорилироваться мотивам ITAM, содержащимся в цепях CD3. Это фосфорилирование, в свою очередь, инициирует путь активации T-клеток, в конечном счете, активируя факторы транскрипции, такие как NF-κB и AP-1. Эти факторы транскрипции индуцируют глобальную экспрессию генов T-клетки с повышением продукции IL-2 для пролиферации и экспрессии основных белков-регуляторов T-клеток, чтобы инициировать опосредованный T-клетками иммунный ответ.
Под "стимулирует иммунореактивную клетку" подразумевается сигнал, приводящий к стойкому и долговременному иммунному ответу. В различных вариантах осуществления это происходит после активации иммунореактивной клетки (например, T-клетки) или одновременно опосредуется через рецепторы, включающие, без ограничения, CD28, CD137 (4-1BB), OX40, CD40 и ICOS. Получение множества костимулирующих сигналов может быть важным для создания стойкого и долгосрочного иммунного ответа, опосредованного T-клетками. T-клетки могут быстро переходить в ингибированное состояние и переставать реагировать на антиген. Хотя эффекты этих костимулирующих сигналов могут варьировать, они обычно приводят к повышенной экспрессии генов с формированием долгоживущих, пролиферативных и антиапоптотических T-клеток, которые эффективно отвечают на антиген до полной и устойчивой эрадикации.
При использовании в настоящем документе термин "антитело" означает не только интактные молекулы антител, но также фрагменты молекул антител, которые сохраняют способность связывать иммуноген. Такие фрагменты также хорошо известны в уровне техники и регулярно применяются как in vitro, так и in vivo. Таким образом, при использовании в настоящем документе термин "антитело" означает не только интактные молекулы иммуноглобулинов, но и хорошо известные активные фрагменты F(ab')2 и Fab. F(ab')2 и Fab-фрагменты, в которых отсутствует Fc-фрагмент интактного антитела, быстрее выводятся из циркулирующей крови и могут иметь меньшее неспецифическое связывание с тканью, чем интактное антитело (Wahl et al., J. Nucl. Med 24: 316-325 (1983)). При использовании в настоящем документе антитела включают цельные нативные антитела, биспецифичные антитела; химерные антитела; Fab, Fab', одноцепочечные фрагменты V-области (scFv), слитые полипептиды и нестандартные антитела. В некоторых вариантах осуществления антитело представляет собой гликопротеин, включающий по меньшей мере две тяжелые (H) цепи и две легкие (L) цепи, соединенные дисульфидными связями. Каждая тяжелая цепь состоит из вариабельной области тяжелой цепи (сокращенно именуемой в настоящем документе как VH) и константной области тяжелой цепи (CH). Константная область тяжелой цепи состоит из трех доменов, CH1, CH2 и CH3. Каждая легкая цепь состоит из вариабельной области легкой цепи (сокращенно именуемой в настоящем документе как VL) и константной области легкой цепи CL. Константная область легкой цепи состоит из одного домена, CL. Области VH и VL могут быть дополнительно подразделены на области гипервариабельности, называемые областями, определяющими комплементарность (CDR), которые чередуются с более консервативными областями, называемыми каркасными областями (FR). Каждая VH и VL состоит из трех CDR-областей и четырех FR-областей, расположенных от N-конца к C-концу в следующем порядке: FR1, CDR1, FR2, CDR2, FR3, CDR3, FR4. Вариабельные области тяжелой и легкой цепей содержат связывающий домен, который взаимодействует с антигеном. Константные области антител могут опосредовать связывание иммуноглобулина с тканями или факторами хозяина, включая различные клетки иммунной системы (например, эффекторные клетки) и первый компонент (C1q) классической системы комплемента.
При использовании в настоящем документе "CDR-области" определены как аминокислотные последовательности определяющих комплементарность областей антитела, которые представляют собой гипервариабельные области тяжелой и легкой цепей иммуноглобулина. См., например, Kabat et al., Sequences of Proteins of Immunological Interest, 4th U.S. Department of Health and Human Services, National Institutes of Health (1987). Как правило, антитела содержат в вариабельной области три CDR или CDR-области тяжелой цепи и три CDR или CDR-области легкой цепи. CDR-области обеспечивают большинство контактных остатков для связывания антитела с антигеном или эпитопом. В некоторых вариантах осуществления границы CDR-областей определены при использовании системы Кэбата (Kabat, EA, et al. (1991) Sequences of Proteins of Immunological Interest, Fifth Edition, US Department of Health and Human Services, NIH Publication No. 91-3242). В некоторых вариантах осуществления CDR-области идентифицированы в соответствии с системой Кэбата.
При использовании в настоящем документе термин "одноцепочечный вариабельный фрагмент" или "scFv" представляет собой слитый белок вариабельных областей тяжелой (VH) и легкой цепей (VL) иммуноглобулина, ковалентно связанных с образованием гетеродимера VH::VL. Либо VH и VL соединены непосредственно, либо соединены линкером, кодирующим пептид (например, из 10, 15, 20, 25 аминокислот), который соединяет N-конец VH с C-концом VL или C-конец VH с N-концом VL. Линкер обычно богат глицином для гибкости, а также серином или треонином для растворимости. "Линкер", при использовании в настоящем документе, должен означать функциональную группу (например, химическую или полипептидную), которая ковалентно соединяет два или больше полипептидов или нуклеиновых кислот, в результате чего они связываются друг с другом. При использовании в настоящем документе термин "пептидный линкер" относится к одной или больше аминокислотам, используемым для соединения двух белков друг с другом (например, для соединения VH и VL доменов). В некоторых вариантах осуществления линкер содержит или состоит из аминокислотной последовательности, указанной в SEQ ID NO: 66, которая представлена ниже:
GGGGSGGGGSGGGGS [SEQ ID NO: 66].
Примерная нуклеотидная последовательность, кодирующая аминокислотную последовательность SEQ ID NO: 66, представлена в SEQ ID NO: 50, которая приведена ниже:
GGAGGTGGAGGCTCAGGAGGAGGAGGCAGTGGAGGTGGTGGGTCA [SEQ ID NO: 50].
Примерная нуклеотидная последовательность, кодирующая аминокислотную последовательность SEQ ID NO: 66, представлена в SEQ ID NO: 51, которая приведена ниже.
GGTGGAGGCGGTTCAGGCGGAGGTGGCTCTGGCGGTGGCGGATCA [SEQ ID NO: 51]
Несмотря на удаление константных областей и введение линкера, белки scFv сохраняют специфичность исходного иммуноглобулина. Антитела из полипептида одиночной цепи Fv могут быть экспрессированы с нуклеиновой кислоты, включающей последовательности, кодирующие VH и VL, как описано в Huston, et al. (Proc. Nat. Acad. Sci. USA, 85: 5879-5883, 1988). См., также, патенты США 5,091,513, 5,132,405 и 4,956,778; и патентные публикации США 20050196754 и 20050196754. Были описаны антагонистические scFv-фрагменты, обладающие ингибирующей активностью (см., например, Zhao et al., Hyrbidoma (Larchmt) 2008 27(6): 455-51; Peter et al., J Cachexia Sarcopenia Muscle 2012 August 12; Shieh et al., J Imunol2009 183(4): 2277-85; Giomarelli et al., Thromb Haemost 2007 97(6): 955-63; Fife eta., J Clin Invst 2006 116(8): 2252-61; Brocks et al., Immunotechnology 1997 3(3): 173-84; Moosmayer et al., Ther Immunol 1995 2(10: 31-40). Было описаны агонистические scFv-фрагменты, обладающие стимулирующей активностью (см., например, Peter et al., J Bioi Chern 2003 25278(38): 36740-7; Xie et al., Nat Biotech 1997 15(8): 768-71; Ledbetter et al., Crit Rev Immunol1997 17(5-6): 427-55; Ho et al., BioChim Biophys Acta 2003 1638(3): 257-66).
При использовании в настоящем документе "F(ab)" относится к фрагменту структуры антитела, который связывается с антигеном, но является моновалентным и не имеет Fc-части, например, антитело при расщеплении ферментом папаином дает два F(ab)-фрагмента и Fc-фрагмент (например, константную область (H) тяжелой цепи; Fc-область, не связывается с антигеном).
При использовании в настоящем документе "F(ab')2" относится к фрагменту антитела, образующемуся при расщеплении пепсином цельных IgG антител, причем такой фрагмент содержит две антигенсвязывающих (ab') (двухвалентных) области, где каждая (ab') область включает две отдельных аминокислотных цепи, часть H-цепи и легкую (L) цепь, соединенные S-S связью, для связывания антигена, и где оставшиеся части H-цепей соединены друг с другом. "F(ab')2" фрагмент может быть разделен на два отдельных Fab'-фрагмента.
При использовании в настоящем документе термин "вектор" относится к любому генетическому элементу, такому как плазмида, фаг, транспозон, космида, хромосома, вирус, вирион и т.д., который способен к репликации при соединении с нужными элементами регуляции и который может переносить последовательности генов в клетки. Таким образом, термин включает клонирующие и экспрессионные носители, а также вирусные векторы и плазмидные векторы.
При использовании в настоящем документе термин "вектор экспрессии" относится к последовательности рекомбинантной нуклеиновой кислоты, то есть молекуле рекомбинантной ДНК, содержащей нужную кодирующую последовательность и соответствующие последовательности нуклеиновых кислот, необходимые для экспрессии функционально связанной кодирующей последовательности в конкретном организме-хозяине. Последовательности нуклеиновых кислот, необходимые для экспрессии в прокариотах, обычно включают в себя промотор, оператор (необязательно) и сайт связывания рибосомы, часто вместе с другими последовательностями. Как известно, эукариотические клетки используют промоторы, энхансеры и сигналы терминации и полиаденилирования.
При использовании в настоящем документе термин "аффинность" означает величину силы связывания. Аффинность может зависеть от близости стереохимического соответствия между паратопами антител и антигенными детерминантами, от размера области контакта между ними и/или от распределения заряженных и гидрофобных групп. Способы расчета аффинности антитела к антигену известны в уровне техники, включая, без ограничения, различные эксперименты по связыванию антигена, например, функциональные анализы (например, анализ с помощью проточной цитометрии).
Термин "химерный антигенный рецептор" или "CAR" при использовании в настоящем документе относится к молекуле, включающей внеклеточный антигенсвязывающий домен, который слит с внутриклеточным сигнальным доменом, который способен активировать или стимулировать иммунореактивную клетку, и трансмембранным доменом. В некоторых вариантах осуществления внеклеточный антигенсвязывающий домен CAR включает scFv. scFv может быть получен при слиянии вариабельных областей тяжелой и легкой цепей антитела. В альтернативе или дополнительно, scFv может быть получен из Fab-фрагментов (а не из антитела, например, получен из Fab-библиотек). В некоторых вариантах осуществления scFv слит с трансмембранным доменом, а затем с внутриклеточным сигнальным доменом. В некоторых вариантах осуществления CAR выбран так, чтобы обладать высокой аффинностью связывания с антигеном.
При использовании в настоящем документе термин "молекулы нуклеиновых кислот" включает любую молекулу нуклеиновой кислоты, кодирующую представляющий интерес полипептид или его фрагмент. Такие молекулы нуклеиновых кислот не должны быть обязательно на 100% гомологичными или идентичными эндогенной последовательности нуклеиновой кислоты, а могут демонстрировать существенную идентичность.
Под "по существу идентичной" или "по существу гомологичной" подразумевается аминокислотная последовательность или молекула нуклеиновой кислоты, демонстрирующая по меньшей мере приблизительно 50% гомологию или идентичность референсной аминокислотной последовательности (например, любой из аминокислотных последовательностей, описанных в настоящем документе) или референсной последовательности нуклеиновой кислоты (например, любой из последовательностей нуклеиновых кислот, описанных в настоящем документе). В некоторых вариантах осуществления такая последовательность по меньшей мере приблизительно на 60%, по меньшей мере приблизительно на 65%, по меньшей мере приблизительно на 70%, по меньшей мере приблизительно на 75%, по меньшей мере приблизительно на 80%, по меньшей мере приблизительно на 85%, по меньшей мере приблизительно на 90%, по меньшей мере приблизительно на 95%, по меньшей мере приблизительно на 99% или по меньшей мере приблизительно на 100% гомологична или идентична последовательности референсной аминокислоты или референсной нуклеиновой кислоты, используемой для сравнения.
Идентичность последовательностей может быть измерена при использовании программ для анализа последовательностей (например, пакета программ Sequence Analysis Software Package разработки Genetics Computer Group, University of Wisconsin Biotechnology Center, 1710 University Avenue, Madison, Wis. 53705, программ BLAST, BESTFIT, GAP или PILEUP/PRETTYBOX). Такие программы сравнивают идентичные или похожие последовательности, присваивая степени гомологии различным заменам, делециям и/или другим модификациям. Консервативные замены обычно включают замены в следующих группах: глицин, аланин; валин, изолейцин, лейцин; аспарагиновая кислота, глутаминовая кислота, аспарагин, глутамин; серин, треонин; лизин, аргинин; и фенилаланин, тирозин. В примерном подходе к определению степени идентичности может использоваться программа BLAST, где оценка вероятностей в пределах от e-3 до e-100 указывает на близкородственную последовательность.
При использовании в настоящем документе процент гомологии между двумя аминокислотными последовательностями эквивалентен проценту идентичности между двумя последовательностями. Процент идентичности между двумя последовательностями является функцией количества идентичных положений в последовательностях (т.е. % гомологии=количество идентичных положений/общее количество положений ×100), с учетом количества пропусков и длины каждого пропуска, который нужно ввести для оптимального выравнивания двух последовательностей. Сравнение последовательностей и определение процента идентичности между двумя последовательностями может быть выполнено при использовании математического алгоритма.
Процент гомологии между двумя аминокислотными последовательностями может быть определен при использовании алгоритма Ю. Мейерса и У. Миллера (E. Meyers and W. Miller, Comput. Appl. Biosci., 4: 11-17 (1988)), который был включен в программу ALIGN (версии 2.0), с использованием таблицы весов замен остатков PAM120, штрафа за длину пропуска, равного 12, и штрафа за пропуск, равного 4. Кроме того, процент гомологии между двумя аминокислотными последовательностями может быть определен при использовании алгоритма Нидлмана и Вунша (Needleman and Wunsch, J. Mol. Biol. 48: 444-453 (1970)), который был включен в программу GAP в пакете программ GCG (доступна на сайте www.gcg.com), с использованием либо матрицы Blossum 62, либо матрицы PAM250, и веса пропуска 16, 14 , 12, 10, 8, 6 или 4 и веса длины 1, 2, 3, 4, 5 или 6.
Дополнительно или альтернативно, аминокислотные последовательности раскрытого в настоящем документе изобретения могут дополнительно применяться в качестве "запрашиваемой последовательности" для выполнения поиска в общедоступных базах данных, например, для идентификации связанных последовательностей. Такой поиск можно выполнить с помощью программы XBLAST (версии 2.0), описанной в публикации Altschul, et al. (1990) J. Mol. Biol. 215: 403-10. Поиск белков в BLAST можно выполнять при использовании программы XBLAST с параметрами score=50, wordlength=3, с получением аминокислотных последовательностей, гомологичных указанным последовательностям (например, последовательностям вариабельной области тяжелой и легкой цепей scFv m903, m904, m905, m906 и m900), раскрытых в настоящем документе. Для получения выравниваний с пропусками в целях сравнения можно использовать Gapped BLAST, как описано в публикации Altschul et al., (1997) Nucleic Acids Res. 25(17): 3389-3402. При использовании программ BLAST и Gapped BLAST можно использовать параметры по умолчанию соответствующих программ (например, XBLAST и NBLAST). Термин "конститутивная экспрессия" или "конститутивно экспрессируемый" при использовании в настоящем документе относится к экспрессии или экспрессии при любых физиологических условиях.
Под "заболеванием" подразумевается любое состояние, заболевание или нарушение, которое повреждает или нарушает нормальную функцию клетки, ткани или органа, например, неоплазия и заражение клетки патогеном.
Под "эффективным количеством" подразумевается количество, достаточное, чтобы произвести терапевтический эффект. В некоторых вариантах осуществления "эффективное количество" является количеством, достаточным для остановки, улучшения или ингибирования продолжающейся пролиферации, роста или метастазирования (например, инвазии или миграции) неоплазии.
Под "модулировать" подразумевается положительное или отрицательное изменение. Примеры модуляции включают приблизительно 1%, приблизительно 2%, приблизительно 5%, приблизительно 10%, приблизительно 25%, приблизительно 50%, приблизительно 75% или приблизительно 100% изменение.
Под "увеличением" подразумевается положительное изменение по меньшей мере на приблизительно 5%. Изменение может составить приблизительно 5%, приблизительно 10%, приблизительно 25%, приблизительно 30%, приблизительно 50%, приблизительно 75%, приблизительно 100% или больше.
Под "уменьшением" подразумевается отрицательное изменение по меньшей мере на приблизительно 5%. Изменение может составить приблизительно 5%, приблизительно 10%, приблизительно 25%, приблизительно 30%, приблизительно 50%, приблизительно 75% или даже приблизительно 100%.
Под "выделенной клеткой" подразумевается клетка, отделенная от молекулярных и/или клеточных компонентов, которые обычно сопровождают клетку.
Термины "выделенный", "очищенный" или "биологически чистый" относятся к материалу, который в различной степени освобожден от компонентов, которые обычно сопровождают его в естественном состоянии. "Выделять" означает степень отделения от источника или окружающей среды. "Очищать" означает более высокую степень разделения, чем выделение. "Очищенный" или "биологически чистый" белок в достаточной степени свободен от других материалов, при этом какие-либо примеси не оказывают существенного влияния на биологические свойства белка и не вызывают других неблагоприятных последствий. Иными словами нуклеиновая кислота или пептид являются очищенными, если они по существу не содержат клеточного материала, вирусного материала или культуральной среды при получении с применением методов рекомбинантных ДНК или химических предшественников или других химических реагентов при химическом синтезе. Чистоту и гомогенность обычно определяют с помощью методов аналитической химии, например, электрофореза в полиакриламидном геле или высокоэффективной жидкостной хроматографии. Термин "очищенный" может означать, что нуклеиновая кислота или белок дают по существу одну полосу в электрофоретическом геле. В случае белка, который может быть подвергнут модификациям, например фосфорилированию или гликозилированию, различные модификации могут приводить к разным выделенным белкам, которые могут быть очищены отдельно.
Под "неоплазией" подразумевается заболевание, характеризующееся патологической пролиферацией клетки или ткани и ее последующей миграцией или инвазией в другие ткани или органы. Неопластический рост обычно является неконтролируемым и прогрессирующим и происходит в условиях, которые не вызывают или могут вызвать остановку размножения нормальных клеток. Неоплазия может поражать различные типы клеток, тканей или органов, включая, помимо прочего, орган, выбранный из группы, состоящей из мочевого пузыря, кости, головного мозга, молочной железы, хряща, глии, пищевода, фаллопиевой трубы, желчного пузыря, сердца, кишечника, почки, печени, легкого, лимфатического узла, нервной ткани, яичников, поджелудочной железы, предстательной железы, скелетных мышц, кожи, спинного мозга, селезенки, желудка, яичек, тимуса, щитовидной железы, трахеи, мочеполовых путей, мочеточника, уретры, матки и влагалища, или ткань или клетку такого типа. Неоплазии включают злокачественные опухоли, такие как саркомы, карциномы или плазмоцитомы (злокачественную опухоль из плазматических клеток). В некоторых вариантах осуществления неоплазия представляет собой солидную опухоль. Неоплазия может быть первичной опухолью или первичным раком. Кроме того, неоплазия может иметь метастатический статус.
При использовании в настоящем документе термин "консервативная модификация последовательности" относится к модификации аминокислоты, которая не оказывает значительного влияния или не изменяет характеристики связывания раскрытого в настоящем изобретении мезотелин-направленного CAR (например, внеклеточного антигенсвязывающего домена CAR), включающего аминокислотную последовательность. Консервативные модификации могут включать аминокислотные замены, добавления и делеции. Модификации могут быть введены во внеклеточный антигенсвязывающий домен раскрытого в настоящем изобретении CAR с помощью стандартных методов, известных в данной области, таких как сайт-направленный мутагенез и ПЦР-опосредованный мутагенез. Аминокислоты могут быть подразделены на группы в соответствии с их физико-химическими свойствами, такими как заряд и полярность. Консервативные аминокислотные замены - это замены, при которых аминокислотный остаток заменяется аминокислотой из той же группы. Например, аминокислоты можно классифицировать по заряду: положительно заряженные аминокислоты включают лизин, аргинин, гистидин, отрицательно заряженные аминокислоты включают аспарагиновую кислоту, глутаминовую кислоту, аминокислоты с нейтральным зарядом включают аланин, аспарагин, цистеин, глутамин, глицин, изолейцин, лейцин, метионин, фенилаланин, пролин, серин, треонин, триптофан, тирозин и валин. Кроме того, аминокислоты можно классифицировать по полярности: полярные аминокислоты включают аргинин (основный полярный), аспарагин, аспарагиновую кислоту (кислотную полярную), глутаминовую кислоту (кислотную полярную), глутамин, гистидин (основный полярный), лизин (основный полярный), серин, треонин и тирозин; неполярные аминокислоты включают аланин, цистеин, глицин, изолейцин, лейцин, метионин, фенилаланин, пролин, триптофан и валин. Таким образом, один или больше аминокислотных остатков в CDR-области могут быть заменены другими аминокислотными остатками из той же группы, и измененное антитело могут тестировать на сохранность функции (то есть функции, указанные в пунктах (c)-(l) выше) с использованием функциональных анализов, описанных в настоящем документе. В некоторых вариантах осуществления измению подвергают не больше одного, не больше двух, не больше трех, не больше четырех, не больше пяти остатков в указанной последовательности или CDR-области.
Под "сигнальной последовательностью" или "лидерной последовательностью" подразумевается пептидная последовательность (например, 5, 10, 15, 20, 25 или 30 аминокислот) присутствующая на N-конце синтезируемых белков, которая направляет их попадание в секреторный путь. Примеры лидерных последовательностей включают, без ограничения перечисленными, сигнальную последовательность IL-2 человека (например, MYRMQLLSCIALSLALVTNS [SEQ ID NO: 67]), сигнальную последовательность IL-2 мыши (например, MYSMQLASCVTLTLVLLVNS [SEQ ID NO: 68]); лидерную последовательность каппа человека (например, METPAQLLFLLLLWLPDTTG [SEQ ID NO: 69]), лидерную последовательность каппа мыши (например, METDTLLLWVLLLWVPGSTG [SEQ ID NO: 70]); лидерную последовательность CD8 человека (например, MALPVTALLLPLALLLHAARP [SEQ ID NO: 71]); усеченный сигнальный пептид CD8 человека (например, MALPVTALLLPLALLLHA [SEQ ID NO: 72]); сигнальную последовательность альбумина человека (например, MKWVTFISLLFSSAYS [SEQ ID NO: 73]); и сигнальную последовательность пролактина человека (например, MDSKGSSQKGSRLLLLLVVSNLLLCQGVVS [SEQ ID NO: 74]).
В некоторых вариантах осуществления CAR включает сигнальный пептид CD8 на N-конце, например, сигнальный пептид соединен с внеклеточным антигенсвязывающим доменом CAR. В некоторых вариантах осуществления сигнальный пептид CD8 включает или состоит из аминокислотной последовательности, представленной в SEQ ID NO: 71.
Примерный нуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 71, представлен в SEQ ID NO: 125. SEQ ID NO: 125 представлена ниже.
ATGGCCCTGCCAGTAACGGCTCTGCTGCTGCCACTTGCTCTGCTCCTCCATGCAGCCAGGCCT [SEQ ID NO: 125]
Термины "включает", "включающий" должны иметь широкое значение, присвоенное им в Патентном праве США, и могут означать "включает в себя", "включающий в себя" и т.п.
При использовании в настоящем документе "лечение" относится к клиническому вмешательству в попытке изменить течение заболевания у индивида или клетки, подвергаемых лечению, и может быть проведено либо для профилактики, либо в течение клинической патологии. Терапевтические эффекты лечения включают, без ограничения, предотвращение возникновения или рецидива заболевания, облегчение симптомов, уменьшение любых прямых или косвенных патологических последствий заболевания, предотвращение метастазов, снижение скорости прогрессирования заболевания, улучшение или облегчение патологического состояния и ремиссию или улучшенный прогноз. Посредством предотвращения прогрессирования заболевания или нарушения, лечение может предотвращать ухудшение вследствие нарушения у пораженного субъекта или субъекта с диагнозом, или субъекта, подозреваемого на наличие нарушения, однако лечение также может предотвращать появление нарушения или симптома нарушения у субъекта, подвергающегося риску возникновения заболевания или подозреваемого на наличие заболевания.
"Индивид" или "субъект" в настоящем документе является позвоночным, таким как человек или животное, не относящееся к человеку, например, млекопитающее. Млекопитающие включают, без ограничения ими, человека, приматов, сельскохозяйственных животных, спортивных животных, грызунов и домашних животных. Неограничивающие примеры животных, не относящихся к человеку, включают грызунов, таких как мыши, крысы, хомяки и морские свинки; кроликов; собак; кошек; овец; свиней; коз; крупный рогатый скот; лошадей; и не относящихся к человеку приматов, таких как человекообразные обезьяны и обезьяны. Термин "иммунодефицитный" при использовании в настоящем документе относится к субъекту, который имеет иммунодефицит. Субъект очень уязвим к оппортунистическим инфекциям, инфекциям, вызываемых организмами, которые обычно не вызывают заболевания у человека со здоровой иммунной системой, но могут поражать людей с плохо функционирующей или подавленной иммунной системой.
Другие аспекты раскрытого в настоящем документе изобретения описаны ниже и входят в объем раскрытого в настоящем документе изобретения.
5.2. Полипептидные композиции
В настоящем изобретении предложены полипептидные композиции, включающие мезотелин-направленный химерный антигенный рецептор (CAR) и доминантно-негативную форму белка программируемой смерти 1 (PD-1 DN).
5.2.1. Доминантно-негативная форма белка программируемой смерти 1 (PD-1 DN)
Доминантно-негативная форма белка программируемой смерти 1 (называемый "PD-1 DN") может повышать терапевтическую эффективность иммунореактивной клетки, включающей CAR. В некоторых вариантах осуществления PD-1 DN включает: (a) по меньшей мере часть внеклеточного домена белка программируемой смерти 1 (PD-1), включающую лигандсвязывающую область, и (b) трансмембранный домен.
В некоторых вариантах осуществления иммунореактивная клетка, такая как T-клетка или ее клетка-предшественник, модифицирована для экспрессии доминантно-негативной формы (DN-формы) PD-1.
Злокачественные клетки адаптируются, чтобы генерировать иммуносупрессивное микроокружение, которое защищает клетки от иммунного распознавания и элиминирования (Sharpe et al., Dis. Model Mech. 2015; 8: 337-350). Иммуносупрессивное микроокружение накладывает ограничения на способы иммунотерапии. Раскрытое в настоящем документе изобретение решает проблему такого ограничения путем экспрессии в иммунореактивной клетке или ее клетке-предшественнике DN-формы ингибитора клеточно-опосредованного иммунного ответа. Детали DN-форм ингибиторов клеточно-опосредованного иммунного ответа раскрыты в заявках WO2017/040945 и WO2017/100428, содержание каждой из которых включено в настоящий документ во всей своей полноте.
Белок программируемой гибели клеток 1 (PD-1) является негативным иммунным регулятором активированных T-клеток при взаимодействии со своими соответствующими лигандами, PD-L1 и PD-L2, экспрессируемыми на эндогенных макрофагах и дендритных клетках. PD-1 представляет собой мембранный белок I типа из 268 аминокислот. PD-1 имеет два лиганда, PD-L1 и PD-L2, которые являются членами семейства B7. Структура белка включает внеклеточный домен IgV, после которого расположена трансмембранная область и внутриклеточный хвост. Внутриклеточный хвост содержит два сайта фосфорилирования, локализованные в иммунорецепторном тирозиновом ингибиторном мотиве и иммунорецепторном тирозиновом переключающем мотиве. PD-1 негативно регулирует сигналы TCR. Фосфатазы SHP-1 и SHP-2 связываются с цитоплазматическим хвостом PD-1 при связывании лиганда. Апрегуляция PD-L1 является одним из механизмов, который опухолевые клетки используют для уклонения от иммунной системы хозяина. В доклинических и клинических испытаниях блокада PD-1 антагонистическими антителами индуцировала противоопухолевые ответы, опосредуемые эндогенной иммунной системой хозяина.
В некоторых вариантах осуществления полипептид PD-1 состоит из аминокислотной последовательности с номером в GenBank NP_005009.2 (SEQ ID NO: 48) или ее фрагмента. В некоторых вариантах осуществления аминокислоты 1-20 SEQ ID NO: 48 представляют собой сигнальный пептид (или пептидный сигнал) PD-1. В некоторых вариантах осуществления аминокислоты 21-170 SEQ ID NO: 48 представляют собой внеклеточный домен PD-1. В некоторых вариантах осуществления аминокислоты 171-191 SEQ ID NO: 48 представляют собой трансмембранный домен PD-1. В некоторых вариантах осуществления аминокислоты 192-288 SEQ ID NO: 48 представляют собой внутриклеточный домен PD-1. SEQ ID NO: 48 приведена ниже:
MQIPQAPWPV VWAVLQLGWR PGWFLDSPDR PWNPPTFSPA LLVVTEGDNA TFTCSFSNTS ESFVLNWYRM SPSNQTDKLA AFPEDRSQPG QDCRFRVTQL PNGRDFHMSV VRARRNDSGT YLCGAISLAP KAQIKESLRA ELRVTERRAE VPTAHPSPSP RPAGQFQTLV VGVVGGLLGS LVLLVWVLAV ICSRAARGTI GARRTGQPLK EDPSAVPVFS VDYGELDFQW REKTPEPPVP CVPEQTEYAT IVFPSGMGTS SPARRGSADG PRSAQPLRPE DGHCSWPL [SEQ ID NO: 48]
В некоторых вариантах осуществления внеклеточный домен PD-1 включает лигандсвязывающий домен (называемый "внеклеточным лигандсвязывающим доменом"). В некоторых вариантах осуществления внеклеточный лигандсвязывающий домен PD-1 слит с одной или больше гетерологичными полипептидными последовательностями, то есть PD-1 DN представляет собой химерную последовательность. Например, внеклеточный лигандсвязывающий домен PD-1 может быть слит на его N-конце с сигнальным пептидом, который необязательно является гетерологичным сигнальным пептидом, включающим различные сигнальные пептиды, описанные в настоящем документе. Кроме того, PD-1 DN может включать трансмембранный домен, который необязательно является гетерологичным трансмембранным доменом, включающим любой из различных трансмембранных доменов, описанных в настоящем документе.
В некоторых вариантах осуществления PD-1 DN включает внеклеточный домен полипептида PD-1 (например, аминокислоты 21-170 в SEQ ID NO: 48) или его лигандсвязывающую часть (например, аминокислоты 21-165 в SEQ ID NO: 48). Клетка, экспрессирующая такой PD-1 DN, может быть неспособна или может обладать сниженной способностью к передаче сигнала в пути иммунной контрольной точки PD-1. В некоторых вариантах осуществления PD-1 DN является делеционным мутантом, состоящим из делеции внутриклеточного домена (например, PD-1 DN не имеет аминокислот 192-288 в SEQ ID NO: 48), или его частью. PD-1, состоящий из делеции внутриклеточного домена, может имеет сниженный или ингибированный путь иммунной контрольной точки, опосредуемый PD-1.
В некоторых вариантах осуществления PD-1 DN включает внеклеточный лигандсвязывающий домен PD-1. В некоторых вариантах осуществления PD-1 DN включает внеклеточный лигандсвязывающий домен полипептида PD-1 и трансмембранный домен полипептида PD-1. В некоторых вариантах осуществления PD-1 DN включает или состоит из аминокислотной последовательности, представленной в SEQ ID NO: 58 (или аминокислот 21-165 в SEQ ID NO: 48). SEQ ID NO: 58 приведена ниже.
PGWFLDSPDR PWNPPTFSPA LLVVTEGDNA TFTCSFSNTS ESFVLNWYRM SPSNQTDKLA AFPEDRSQPG QDCRFRVTQL PNGRDFHMSV VRARRNDSGT YLCGAISLAP KAQIKESLRA ELRVTERRAE VPTAHPSPSP RPAGQ [SEQ ID NO: 58]
Примерная нуклеотидная последовательность, кодирующая SEQ ID NO: 58 (или аминокислоты 21-165 в SEQ ID NO: 48), представлена в SEQ ID NO: 59, которая приведена ниже.
CCAGGATGGTTCTTAGACTCCCCAGACAGGCCCTGGAACCCCCCCACCTTCTCCCCAGCCCTGCTCGTGGTGACCGAAGGGGACAACGCCACCTTCACCTGCAGCTTCTCCAACACATCGGAGAGCTTCGTGCTAAACTGGTACCGCATGAGCCCCAGCAACCAGACGGACAAGCTGGCCGCTTTCCCCGAGGACCGCAGCCAGCCCGGCCAGGACTGCCGCTTCCGTGTCACACAACTGCCCAACGGGCGTGACTTCCACATGAGCGTGGTCAGGGCCCGGCGCAATGACAGCGGCACCTACCTCTGTGGGGCCATCTCCCTGGCCCCCAAGGCGCAGATCAAAGAGAGCCTGCGGGCAGAGCTCAGGGTGACAGAGAGAAGGGCAGAAGTGCCCACAGCCCACCCCAGCCCCTCACCCAGGCCAGCCGGCCAG [SEQ ID NO: 59]
В некоторых вариантах осуществления PD-1 DN дополнительно включает сигнальный пептид, например, PD-1 DN включает внеклеточный лигандсвязывающий домен полипептида PD-1, трансмембранный домен полипептида PD-1 и сигнальный пептид полипептида PD-1. В некоторых вариантах осуществления сигнальный пептид включает или состоит из аминокислот 1-20 в SEQ ID NO: 48. Примерная нуклеотидная последовательность, кодирующая аминокислоты 1-20 в SEQ ID NO: 48, представлена в SEQ ID NO: 60, которая приведена ниже.
ATGCAGATCCCACAGGCGCCCTGGCCAGTCGTCTGGGCGGTGCTACAACTGGGCTGGCGG [SEQ ID NO: 60]
В некоторых вариантах осуществления PD-1 DN включает или состоит из аминокислот 1-165 в SEQ ID NO: 48.
Примерная нуклеотидная последовательность, кодирующая аминокислоты 1-165 в SEQ ID NO: 48, представлена в SEQ ID NO: 61, которая приведена ниже.
ATGCAGATCCCACAGGCGCCCTGGCCAGTCGTCTGGGCGGTGCTACAACTGGGCTGGCGGCCAGGATGGTTCTTAGACTCCCCAGACAGGCCCTGGAACCCCCCCACCTTCTCCCCAGCCCTGCTCGTGGTGACCGAAGGGGACAACGCCACCTTCACCTGCAGCTTCTCCAACACATCGGAGAGCTTCGTGCTAAACTGGTACCGCATGAGCCCCAGCAACCAGACGGACAAGCTGGCCGCTTTCCCCGAGGACCGCAGCCAGCCCGGCCAGGACTGCCGCTTCCGTGTCACACAACTGCCCAACGGGCGTGACTTCCACATGAGCGTGGTCAGGGCCCGGCGCAATGACAGCGGCACCTACCTCTGTGGGGCCATCTCCCTGGCCCCCAAGGCGCAGATCAAAGAGAGCCTGCGGGCAGAGCTCAGGGTGACAGAGAGAAGGGCAGAAGTGCCCACAGCCCACCCCAGCCCCTCACCCAGGCCAGCCGGCCAG [SEQ ID NO: 61]
В некоторых вариантах осуществления PD-1 DN включает или состоит из аминокислот 21-151 в SEQ ID NO: 48. В некоторых вариантах осуществления PD-1 DN включает или состоит из аминокислот 1-151 в SEQ ID NO: 48. В некоторых вариантах осуществления PD-1 DN включает или состоит из аминокислот 21-151 в SEQ ID NO: 48. В некоторых вариантах осуществления PD-1 DN включает или состоит из аминокислотной последовательности, начинающейся с аминокислоты 21 в SEQ ID NO: 48 до аминокислоты между аминокислотами 151-165 в SEQ ID NO: 48.
В некоторых вариантах осуществления PD-1 DN дополнительно включает полипептид CD8. В некоторых вариантах осуществления PD-1 DN включает внеклеточный домен PD-1 или его часть (например, внеклеточный лигандсвязывающий домен) слитый с трансмембранным доменом и/или шарнирным доменом CD8. В некоторых вариантах осуществления PD-1 DN включает трансмембранный домен CD8 (например, аминокислоты 183-203 в SEQ ID NO: 86). Такие варианты осуществления являются репрезентативными для химерной формы DN, включающей трансмембранный домен из другого (гетерологичного) полипептида. Как описано выше, PD-1 DN, включающий гетерологичный домен, такой как трансмембранный домен, необязательно может включать дополнительную последовательность из гетерологичного полипептида. В некоторых вариантах осуществления PD-1 DN включает дополнительную последовательность из гетерологичного полипептида с N-конца трансмембранного домена. В некоторых вариантах осуществления PD-1 DN включает шарнирный домен CD8. В некоторых вариантах осуществления гетерологичная последовательность включает дополнительную N-концевую последовательность полипептида CD8 (например, аминокислоты 137-182 (или необязательно начинающуюся с аминокислот 138 или 139) из SEQ ID NO: 86). В некоторых вариантах осуществления PD-1 DN включает дополнительную последовательность из гетерологичного полипептида с C-конца трансмембранного домена CD8. В некоторых вариантах осуществления дополнительная C-концевая последовательность представляет собой аминокислоты 204-209 из SEQ ID NO: 86.
В некоторых вариантах осуществления PD-1 DN включает трансмембранный домен полипептида CD8 (например, аминокислоты 183-203 из SEQ ID NO: 86), шарнирный домен полипептида CD8 (например, аминокислоты 137-182 из SEQ ID NO: 86), и дополнительную C-концевую последовательность полипептида CD8 (например, аминокислоты 204-207 из SEQ ID NO: 86). В некоторых вариантах осуществления PD-1 DN включает полипептид CD8, состоящий из аминокислот 137-207 из SEQ ID NO: 86.
Примерная нуклеотидная последовательность, кодирующая аминокислоты 137-207 из SEQ ID NO: 86, представлена в SEQ ID NO: 62, которая приведена ниже:
CCCACCACGACGCCAGCGCCGCGACCACCAACCCCGGCGCCCACGATCGCGTCGCAGCCCCTGTCCCTGCGCCCAGAGGCGTGCCGGCCAGCGGCGGGGGGCGCAGTGCACACGAGGGGGCTGGACTTCGCCTGTGATATCTACATCTGGGCGCCCCTGGCCGGGACTTGTGGGGTCCTTCTCCTGTCACTGGTTATCACCCTTTACTGCAAC [SEQ ID NO: 62]
В некоторых вариантах осуществления PD-1 DN включает трансмембранный домен полипептида CD8 (например, аминокислоты 183-203 из SEQ ID NO: 86), шарнирный домен полипептида CD8 (например, аминокислоты 137-182 из SEQ ID NO: 86) и дополнительную C-концевую последовательность полипептида CD8 (например, аминокислоты 204-209 из SEQ ID NO: 86). В некоторых вариантах осуществления PD-1 DN включает полипептид CD8, состоящий из аминокислот 137-209 из SEQ ID NO: 86.
Примерная нуклеотидная последовательность, кодирующая аминокислоты 137-209 из SEQ ID NO: 86, представлена в SEQ ID NO: 63, которая приведена ниже:
CCCACCACGACGCCAGCGCCGCGACCACCAACCCCGGCGCCCACGATCGCGTCGCAGCCCCTGTCCCTGCGCCCAGAGGCGTGCCGGCCAGCGGCGGGGGGCGCAGTGCACACGAGGGGGCTGGACTTCGCCTGTGATATCTACATCTGGGCGCCCCTGGCCGGGACTTGTGGGGTCCTTCTCCTGTCACTGGTTATCACCCTTTACTGCAACCACAGG [SEQ ID NO: 63]
В некоторых вариантах осуществления PD-1 DN включает аминокислотную последовательность, представленную в SEQ ID NO: 49, которая приведена ниже.
MQIPQAPWPVVWAVLQLGWRPGWFLDSPDRPWNPPTFSPALLVVTEGDNA
TFTCSFSNTSESFVLNWYRMSPSNQTDKLAAFPEDRSQPGQDCRFRVTQL
PNGRDFHMSVVRARRNDSGTYLCGAISLAPKAQIKESLRAELRVTERRAE
VPTAHPSPSPRPAGQAAAPTTTPAPRPPTPAPTIASQPLSLRPEACRPAA
GGAVHTRGLDFACDIYIWAPLAGTCGVLLLSLVITLYCN [SEQ ID NO: 49]
Примерная нуклеотидная последовательность, кодирующая аминокислотную последовательность, представленную в SEQ ID NO: 49, представлена в SEQ ID NO: 64, которая приведена ниже:
ATGCAGATCCCACAGGCGCCCTGGCCAGTCGTCTGGGCGGTGCTACAACTGGGCTGGCGGCCAGGATGGTTCTTAGACTCCCCAGACAGGCCCTGGAACCCCCCCACCTTCTCCCCAGCCCTGCTCGTGGTGACCGAAGGGGACAACGCCACCTTCACCTGCAGCTTCTCCAACACATCGGAGAGCTTCGTGCTAAACTGGTACCGCATGAGCCCCAGCAACCAGACGGACAAGCTGGCCGCTTTCCCCGAGGACCGCAGCCAGCCCGGCCAGGACTGCCGCTTCCGTGTCACACAACTGCCCAACGGGCGTGACTTCCACATGAGCGTGGTCAGGGCCCGGCGCAATGACAGCGGCACCTACCTCTGTGGGGCCATCTCCCTGGCCCCCAAGGCGCAGATCAAAGAGAGCCTGCGGGCAGAGCTCAGGGTGACAGAGAGAAGGGCAGAAGTGCCCACAGCCCACCCCAGCCCCTCACCCAGGCCAGCCGGCCAGGCGGCCGCACCCACCACGACGCCAGCGCCGCGACCACCAACCCCGGCGCCCACGATCGCGTCGCAGCCCCTGTCCCTGCGCCCAGAGGCGTGCCGGCCAGCGGCGGGGGGCGCAGTGCACACGAGGGGGCTGGACTTCGCCTGTGATATCTACATCTGGGCGCCCCTGGCCGGGACTTGTGGGGTCCTTCTCCTGTCACTGGTTATCACCCTTTACTGCAAC [SEQ ID NO: 64]
В некоторых вариантах осуществления PD-1 DN включает аминокислотную последовательность, представленную в SEQ ID NO: 118, которая приведена ниже.
MQIPQAPWPVVWAVLQLGWRPGWFLDSPDRPWNPPTFSPALLVVTEGDNA
TFTCSFSNTSESFVLNWYRMSPSNQTDKLAAFPEDRSQPGQDCRFRVTQL
PNGRDFHMSVVRARRNDSGTYLCGAISLAPKAQIKESLRAELRVTERRAE
VPTAHPSPSPRPAGQAAAPTTTPAPRPPTPAPTIASQPLSLRPEACRPAA
GGAVHTRGLDFACDIYIWAPLAGTCGVLLLSLVITLYCNHR [SEQ ID NO: 118]
Примерная нуклеотидная последовательность, кодирующая аминокислотную последовательность, представленную в SEQ ID NO: 118, представлена в SEQ ID NO: 119, которая приведена ниже:
ATGCAGATCCCACAGGCGCCCTGGCCAGTCGTCTGGGCGGTGCTACAACTGGGCTGGCGGCCAGGATGGTTCTTAGACTCCCCAGACAGGCCCTGGAACCCCCCCACCTTCTCCCCAGCCCTGCTCGTGGTGACCGAAGGGGACAACGCCACCTTCACCTGCAGCTTCTCCAACACATCGGAGAGCTTCGTGCTAAACTGGTACCGCATGAGCCCCAGCAACCAGACGGACAAGCTGGCCGCTTTCCCCGAGGACCGCAGCCAGCCCGGCCAGGACTGCCGCTTCCGTGTCACACAACTGCCCAACGGGCGTGACTTCCACATGAGCGTGGTCAGGGCCCGGCGCAATGACAGCGGCACCTACCTCTGTGGGGCCATCTCCCTGGCCCCCAAGGCGCAGATCAAAGAGAGCCTGCGGGCAGAGCTCAGGGTGACAGAGAGAAGGGCAGAAGTGCCCACAGCCCACCCCAGCCCCTCACCCAGGCCAGCCGGCCAGGCGGCCGCACCCACCACGACGCCAGCGCCGCGACCACCAACCCCGGCGCCCACGATCGCGTCGCAGCCCCTGTCCCTGCGCCCAGAGGCGTGCCGGCCAGCGGCGGGGGGCGCAGTGCACACGAGGGGGCTGGACTTCGCCTGTGATATCTACATCTGGGCGCCCCTGGCCGGGACTTGTGGGGTCCTTCTCCTGTCACTGGTTATCACCCTTTACTGCAACCACAGG [SEQ ID NO: 119]
В некоторых вариантах осуществления трансмембранный домен PD-1 DN включает гидрофобную альфа-спираль, которая охватывает, по меньшей мере, часть мембраны. Различные трансмембранные домены приводят к различной стабильности рецептора. В соответствии с раскрытым в настоящем документе изобретением, трансмембранный домен PD-1 DN может включать нативный или модифицированный трансмембранный домен любого полипептида, раскрытого в настоящем документе, например, любой трансмембранный домен, который может содержаться в химерном антигенном рецепторе. В некоторых вариантах осуществления трансмембранный домен является полипептидом CD8, полипептидом CD28, полипептидом CD3ζ, полипептидом CD40, полипептидом 4-1BB, полипептидом OX40, полипептидом CD84, полипептидом CD166, полипептидом CD8a, полипептидом CD8b, полипептидом ICOS, полипептидом ICAM-1, полипептидом CTLA-4, полипептидом CD27, пептидом CD40/My88, пептидом NKGD2, синтетическим полипептидом (не основанным на белке, ассоциированном с иммунным ответом) или их комбинацией. В некоторых вариантах осуществления трансмембранный домен является полипептидом CD8. Детали этих трансмембранных доменов будут описаны в разделе ниже.
5.2.2. Мезотелин-направленный химерный антигенный рецептор (CAR)
Раскрытая в настоящем документе полипептидная композиция включает CAR, который специфично взаимодействует с мезотелином, например, мезотелином человека.
CAR-рецепторы представляют собой сконструированные рецепторы, которые передают или придают представляющую интерес специфичность иммунной эффекторной клетке. CAR-рецепторы могут использоваться для переноса специфичности моноклонального антитела T-клетке; с переносом их кодирующей последовательности, опосредуемым ретровирусными векторами.
Существует три поколения CAR-рецепторов. CAR-рецепторы "первого поколения", как правило, состоят из внеклеточного антигенсвязывающего домена (например, scFv), который слит с трансмембранным доменом, который слит цитоплазматическим/внутриклеточным сигнальным доменом. CAR-рецепторы "первого поколения" могут обеспечивать распознавание антигена de novo и вызывать активацию и CD4+ и CD8+ T-клеток через их сигнальный домен CD3ζ цепи в одной слитой молекуле, независимой от HLA-опосредованного презентирования антигена. В CAR-рецепторах "второго поколения" внутриклеточные сигнальные домены различных костимулирующих молекул (например, CD28, 4-1BB, ICOS, OX40, CD27, CD40/My88 и NKGD2) добавлены к цитоплазматическому хвосту CAR, с передачей дополнительных сигналов T-клетке. CAR-рецепторы "второго поколения" включают рецепторы, которые обеспечивают и костимуляцию (например, CD28 или 4-1BB), и активацию (CD3ζ). CAR-рецепторы "третьего поколения" включают рецепторы, которые обеспечивают множественную костимуляцию (например, CD28 и 4-1BB) и активацию (CD3ζ). В некоторых вариантах осуществления CAR представляет собой CAR второго поколения. В некоторых вариантах осуществления CAR включает внеклеточный антигенсвязывающий домен, который связывается с антигеном, трансмембранный домен и внутриклеточный сигнальный домен, где внутриклеточный сигнальный домен включает костимулирующий сигнальный домен. В некоторых вариантах осуществления CAR дополнительно включает шарнирную/спейсерную область.
5.2.2.1. Внеклеточный антигенсвязывающий домен CAR-рецептора
Внеклеточный антигенсвязывающий домен CAR специфично связывается с мезотелином, например, мезотелином человека. В некоторых вариантах осуществления внеклеточным антигенсвязывающим доменом является scFv. В некоторых вариантах осуществления scFv является человеческим scFv. В некоторых вариантах осуществления scFv является гуманизированным scFv. В некоторых вариантах осуществления scFv является мышиным scFv. В некоторых вариантах осуществления внеклеточный антигенсвязывающий домен CAR представляет собой Fab, который необязательно является сшитым. В некоторых вариантах осуществления внеклеточный антигенсвязывающий домен CAR представляет собой F(ab)2. В некоторых вариантах осуществления любая из предыдущих молекул может содержаться в слитом белке с гетерологичной последовательностью, образуя внеклеточный антигенсвязывающий домен. В некоторых вариантах осуществления scFv идентифицируют путем скрининга фаговой библиотеки scFv с использованием слитого белка антигена-Fc. scFv может быть получен из мыши, несущей гены VL и/или VH человека. scFv также может быть заменен тяжелой цепью верблюдового (например, VHH верблюда, ламы и т.д.) или частичным природным лигандом рецептора клеточной поверхности.
Мезотелин - иммуногенный поверхностный антиген клетки, который повышенно экспрессируется в солидных злокачественных опухолях. Мезотелин участвует в пролиферации, адгезии, инвазии, клеточной сигнализации и метастазировании. Исследования показали, что растворимый в сыворотке крови родственный мезотелину пептид, секретируемый мезотелин-экспрессирующими опухолями, можно измерять у человека и у мышей, при этом было показано, что он коррелирует с ответом на терапию и прогнозом. В нормальных тканях мезотелин экспрессируется только в плевре, перикарде и брюшиной полости на низких уровнях. Рекомбинантный иммунотоксин SS1P против мезотелина показал специфичность in vivo и значимую противоопухолевую активность у пациентов. В иследовании вакцины против рака поджелудочной железы пациенты с преимуществом в выживаемости имели устойчивые ответы CD8+ T-клеток на мезотелин, ассоциированные с поствакцинальной реакцией гиперчувствительности замедленного типа. Было показано, что специфические эпитопы T-клеток, происходящие из мезотелина, активируют T-клетки человека с эффективным лизисом человеческих опухолей, экспрессирующих мезотелин. Таким образом, имеются данные, убедительно подтверждающие, что адоптивная иммунотерапия, направленная на мезотелин, может специфично воздействовать на мезотелин-экспрессирующие опухоли.
В некоторых вариантах осуществления CAR связывается с мезотелином человека. В некоторых вариантах осуществления мезотелин человека включает или состоит из аминокислотной последовательности под номером NCBI: AAV87530.1 (SEQ ID NO: 75) или ее фрагмента.
SEQ ID NO: 75 приведена ниже:
MALPTARPLL GSCGTPALGS LLFLLFSLGW VQPSRTLAGE TGQEAAPLDG VLANPPNISS LSPRQLLGFP CAEVSGLSTE RVRELAVALA QKNVKLSTEQ LRCLAHRLSE PPEDLDALPL DLLLFLNPDA FSGPQACTHF FSRITKANVD LLPRGAPERQ RLLPAALACW GVRGSLLSEA DVRALGGLAC DLPGRFVAES AEVLLPRLVS CPGPLDQDQQ EAARAALQGG GPPYGPPSTW SVSTMDALRG LLPVLGQPII RSIPQGIVAA WRQRSSRDPS WRQPERTILR PRFRREVEKT ACPSGKKARE IDESLIFYKK WELEACVDAA LLATQMDRVN AIPFTYEQLD VLKHKLDELY PQGYPESVIQ HLGYLFLKMS PEDIRKWNVT SLETLKALLE VNKGHEMSPQ VATLIDRFVK GRGQLDKDTL DTLTAFYPGY LCSLSPEELS SVPPSSIWAV RPQDLDTCDP RQLDVLYPKA RLAFQNMNGS EYFVKIQSFL GGAPTEDLKA LSQQNVSMDL ATFMKLRTDA VLPLTVAEVQ KLLGPHVEGL KAEERHRPVR DWILRQRQDD LDTLGLGLQG GIPNGYLVLD LSVQEALSGT PCLLGPGPVL TVLALLLAST LA [SEQ ID NO: 75]
В некоторых вариантах осуществления внеклеточный антигенсвязывающий домен CAR (реализованный, например, в scFv или его аналоге) связывается с мезотелином человека со значением EC50 от приблизительно 1 нМ до приблизительно 25 нМ, при измерении с помощью твердофазного иммуноферментного анализа (ИФА). В некоторых вариантах осуществления внеклеточный антигенсвязывающий домен CAR имеет значение EC50 приблизительно 20 нМ при измерении с помощью ИФА. В некоторых вариантах осуществления внеклеточный антигенсвязывающий домен CAR включает антитело против мезотелина или его антигенсвязывающую часть, описанную в патенте США 8,357,783, который включен в настоящий документ посредством отсылки во всей своей полноте. В некоторых вариантах осуществления внеклеточный антигенсвязывающий домен CAR получен из вариабельной области тяжелой цепи и вариабельной области легкой цепи антитела, которое связывается с мезотелином человека, например, антитела m912, как раскрыто в публикации Feng et al., Mol. Cancer Therapy (2009); 8(5): 1113-1118, которая включена в настоящий документ посредством отсылки во всей своей полноте. Антитело m912 выделяли из библиотеки Fab человека путем пэннинга против рекомбинантного мезотелина. В некоторых вариантах осуществления внеклеточный антигенсвязывающий домен CAR получен из Fab (например, из библиотеки Fab человека или мыши).
Связывание внеклеточного антигенсвязывающего домена (вариант осуществления, например, в scFv или его аналоге) CAR-рецептора можно подтвердить, например, с помощью иммуноферментного анализа (ИФА), радиоиммуноанализа (РИА), FACS-анализа, биоанализа (например, ингибирования роста) или Вестерн-блоттинга. Каждый из этих анализов обычно обнаруживает присутствие комплексов белка-антитела, представляющих особый интерес, при использовании меченого реагента (например, антитела или scFv), специфичного к представляющему интерес комплексу. Например, scFv может быть помечен радиоактивной меткой и использован в радиоиммуноанализе (РИА) (см., например, публикацию Weintraub, B., Principles of Radioimmunoassays, Seventh Training Course on Radioligand Assay Techniques, The Endocrine Society, March, 1986, которая включена в настоящий документ посредством отсылки). Радиоактивный изотоп можно детектировать при использовании таких средств, как счетчик γ-излучения или сцинтилляционный счетчик, или с помощью авторадиографии. В некоторых вариантах осуществления мезотелин-направленный внеклеточный антигенсвязывающий домен помечен флуоресцентным маркером. Неограничивающие примеры флуоресцентных маркеров включают зеленый флуоресцентный белок (GFP), синий флуоресцентный белок (например, EBFP, EBFP2, Azurite и mKalama1), голубой флуоресцентный белок (например, ECFP, Cerulean и CyPet) и желтый флуоресцентный белок (например, YFP, Citrine, Venus и YPet). В некоторых вариантах осуществления мезотелин-направленный scFv человека помечен GFP.
В некоторых вариантах осуществления внеклеточный антигенсвязывающий домен CAR связывается с мезотелином человека при уровне мезотелина приблизительно 1000 или больше связывающих сайтов мезотелина/клетка. В некоторых вариантах осуществления внеклеточный антигенсвязывающий домен CAR связывается с мезотелином человека при уровне мезотелина от приблизительно 1000 до приблизительно 50000 связывающих сайтов мезотелина/клетка. В некоторых вариантах осуществления внеклеточный антигенсвязывающий домен CAR не связывается с мезотелином человека при уровне экспрессии мезотелина меньше 1000 связывающих сайтов мезотелина/клетка, например, мезотелином человека, эспрессируемым в нормальных тканях, например, нормальных тканях плевры, перикарда и брюшной полости. В некоторых вариантах осуществления внеклеточный антигенсвязывающий домен CAR не связывается с мезотелином человека при уровне экспрессии мезотелина больше 50000 связывающих сайтов мезотелина/клетка. В некоторых вариантах осуществления человеческий scFV, содержащийся в CAR, связывается с мезотелином человека при уровне экспрессии мезотелина от приблизительно 1000 до приблизительно 50000 связывающих сайтов мезотелина/клетка. В некоторых вариантах осуществления человеческий scFV, содержащийся в CAR, не связывается с мезотелином человека при уровне экспрессии мезотелина больше 50000 или меньше 1000 связывающих сайтов мезотелина/клетка.
В некоторых вариантах осуществления внеклеточный антигенсвязывающий домен CAR (например, scFv) включает вариабельную область тяжелой цепи (VH), включающую CDR1, включающую или состоящую из аминокислотной последовательности, представленной в SEQ ID NO: 76, или ее консервативной модификации, CDR2, включающую или состоящую из аминокислотной последовательности, представленной в SEQ ID NO: 77, или ее консервативной модификации, и CDR3, включающую или состоящую из аминокислотной последовательности, представленной в SEQ ID NO: 78, или ее консервативной модификации. В некоторых вариантах осуществления VH включает CDR1, включающую или состоящую из аминокислотной последовательности, представленной в SEQ ID NO: 76, CDR2, включающую или состоящую из аминокислотной последовательности, представленной в SEQ ID NO: 77, и CDR3, включающую или состоящую из аминокислотной последовательности, представленной в SEQ ID NO: 78.
В некоторых вариантах осуществления внеклеточный антигенсвязывающий домен CAR (например, scFv) включает вариабельную область легкой цепи (VL), включающую CDR1, включающую или состоящую из аминокислотной последовательности, представленной в SEQ ID NO: 79, или ее консервативной модификации, CDR2, включающую или состоящую из аминокислотной последовательности, представленной в SEQ ID NO: 80, или ее консервативной модификации, и CDR3, включающую или состоящую из аминокислотной последовательности, представленной в SEQ ID NO: 81, или ее консервативной модификации. В некоторых вариантах осуществления VL включает CDR1, включающую или состоящую из аминокислотной последовательности, представленной в SEQ ID NO: 79, CDR2, включающую или состоящую из аминокислотной последовательности, представленной в SEQ ID NO: 80, и CDR3, включающую или состоящую из аминокислотной последовательности, представленной в SEQ ID NO: 81.
В некоторых вариантах осуществления VH включает CDR1, включающую или состоящую из аминокислотной последовательности, представленной в SEQ ID NO: 76, или ее консервативной модификации, CDR2, включающую или состоящую из аминокислотной последовательности, представленной в SEQ ID NO: 77, или ее консервативной модификации, и CDR3, включающую или состоящую из аминокислотной последовательности, представленной в SEQ ID NO: 78, ее консервативной модификации; и VL включает CDR1, включающую или состоящую из аминокислотной последовательности, представленной в SEQ ID NO: 79, или ее консервативной модификации, CDR2, включающую или состоящую из аминокислотной последовательности, представленной в SEQ ID NO: 80, или ее консервативной модификации, и CDR3, включающую или состоящую из аминокислотной последовательности, представленной в SEQ ID NO: 81, или ее консервативной модификации. В некоторых вариантах осуществления VH включает CDR1, включающую или состоящую из аминокислотной последовательности, представленной в SEQ ID NO: 76, CDR2, включающую или состоящую из аминокислотной последовательности, представленной в SEQ ID NO: 77, и CDR3, включающую или состоящую из аминокислотной последовательности, представленной в SEQ ID NO: 78; и VL включает CDR1, включающую или состоящую из аминокислотной последовательности, представленной в SEQ ID NO: 79, CDR2, включающую или состоящую из аминокислотной последовательности, представленной в SEQ ID NO: 80, и CDR3, включающую или состоящую из аминокислотной последовательности, представленной в SEQ ID NO: 81. В некоторых вариантах осуществления CDR-области идентифицированы согласно системе нумерации Кэбата.
В некоторых вариантах осуществления вариабельная область тяжелой цепи (VH) включает аминокислотную последовательность, представленную в SEQ ID NO: 82. В некоторых вариантах осуществления вариабельная область легкой цепи (VL) включает аминокислотную последовательность, представленную в SEQ ID NO: 83. В некоторых вариантах осуществления VH включает аминокислотную последовательность, представленную в SEQ ID NO: 82, а VL включает аминокислотную последовательность, представленную в SEQ ID NO: 83, необязательно с (iii) линкерной последовательностью, например линкерным пептидом, между VH и VL. В некоторых вариантах осуществления линкер включает или состоит из аминокислотной последовательности, представленной в SEQ ID NO: 66. В некоторых вариантах осуществления VH включает аминокислотную последовательность, которая по меньшей мере приблизительно на 80% (например, по меньшей мере приблизительно на 85%, по меньшей мере приблизительно на 90% или по меньшей мере приблизительно на 95%) гомологична или идентична аминокислотной последовательности, представленной в SEQ ID NO: 82. Например, VH включает аминокислотную последовательность, которая приблизительно на 80%, приблизительно на 81%, приблизительно на 82%, приблизительно на 83%, приблизительно на 84%, приблизительно на 85%, приблизительно на 86%, приблизительно на 87%, приблизительно на 88%, приблизительно 89%, приблизительно на 90%, приблизительно на 91%, приблизительно на 92%, приблизительно на 93%, приблизительно на 94%, приблизительно на 95%, приблизительно на 96%, приблизительно на 97%, приблизительно на 98%, приблизительно на 99% или приблизительно на 100% гомологична или идентична аминокислотной последовательности, представленной в SEQ ID NO: 82. В некоторых вариантах осуществления VH включает аминокислотную последовательность, представленную в SEQ ID NO: 82. В некоторых вариантах осуществления VL включает аминокислотную последовательность, которая по меньшей мере приблизительно на 80% (например, по меньшей мере приблизительно на 85%, по меньшей мере приблизительно на 90% или по меньшей мере приблизительно на 95%) гомологична или идентична аминокислотной последовательности, представленной в SEQ ID NO: 83. Например, VL включает аминокислотную последовательность, которая приблизительно на 80%, приблизительно на 81%, приблизительно на 82%, приблизительно на 83%, приблизительно на 84%, приблизительно на 85%, приблизительно на 86%, приблизительно на 87%, приблизительно на 88%, приблизительно на 89%, приблизительно на 90%, приблизительно на 91%, приблизительно на 92%, приблизительно на 93%, приблизительно на 94%, приблизительно на 95%, приблизительно на 96%, приблизительно на 97%, приблизительно на 98%, приблизительно на 99% или приблизительно на 100% гомологична или идентична аминокислотной последовательности, представленной в SEQ ID NO: 83. В некоторых вариантах осуществления VL включает аминокислотную последовательность, представленную в SEQ ID NO: 83. В некоторых вариантах осуществления VH включает аминокислотную последовательность, которая по меньшей мере приблизительно на 80% (например, по меньшей мере приблизительно на 85%, по меньшей мере приблизительно на 90% или по меньшей мере приблизительно на 95%) гомологична или идентична аминокислотной последовательности, представленной в SEQ ID NO: 82, и VL включает аминокислотную последовательность, которая по меньшей мере приблизительно на 80% (например, по меньшей мере приблизительно на 85%, по меньшей мере приблизительно на 90% или по меньшей мере приблизительно на 95%) гомологична или идентична аминокислотной последовательности, представленной в SEQ ID NO: 83. В некоторых вариантах осуществления VH включает аминокислотную последовательность, представленную в SEQ ID NO: 82, а VL включает аминокислотную последовательность, представленную в SEQ ID NO: 83.
Примерная последовательность нуклеиновой кислоты, кодирующая аминокислотную последовательность SEQ ID NO: 82, представлена в SEQ ID NO: 52.
Примерная последовательность нуклеиновой кислоты, кодирующая аминокислотную последовательность SEQ ID NO: 83, представлена в SEQ ID NO: 53.
В некоторых вариантах осуществления внеклеточный антигенсвязывающий домен CAR (например, scFv) включает аминокислотную последовательность, которая по меньшей мере приблизительно на 80%, по меньшей мере приблизительно на 80%, по меньшей мере приблизительно на 85%, по меньшей мере приблизительно на 90% или по меньшей мере приблизительно на 95% (например, приблизительно на 81%, приблизительно на 82%, приблизительно на 83%, приблизительно на 84%, приблизительно на 85%, приблизительно на 86%, приблизительно на 87%, приблизительно на 88%, приблизительно на 89%, приблизительно на 90%, приблизительно на 91%, приблизительно на 92%, приблизительно на 93%, приблизительно на 94%, приблизительно на 95%, приблизительно на 96%, приблизительно на 97%, приблизительно на 98% или приблизительно на 99%) гомологична или идентична аминокислотной последовательности, представленной в SEQ ID NO: 84. В некоторых вариантах осуществления внеклеточный антигенсвязывающий домен CAR (например, scFv) включает или состоит из аминокислотной последовательности, представленной в SEQ ID NO: 84. В некоторых вариантах осуществления внеклеточный антигенсвязывающий домен CAR (например, scFv) специфично связывается с полипептидом мезотелина человека (например, полипептидом мезотелина человека, включающим аминокислотную последовательность, представленную в SEQ ID NO: 75).
Примерная нуклеотидная последовательность, кодирующая аминокислотную последовательность SEQ ID NO: 84, представлена в SEQ ID NO: 85.
В некоторых вариантах осуществления scFv является человеческим scFv.
Последовательности SEQ ID NO: 52, 53 и 76-85 приведены ниже:
CAGGTTCAGCTTCAGGAGAGTGGCCCAGGCCTGGTGAAGCCAAGTGAGACTCTCAGCTTGACTTGCACAGTTTCTGGAGGCAGTGTCTCCTCAGGCAGCTATTATTGGTCCTGGATTCGGCAGCCCCCTGGGAAAGGCCTGGAGTGGATTGGGTACATATATTACAGTGGCAGCACAAATTACAATCCATCCCTGAAGTCTCGAGTAACTATCAGTGTGGACACAAGCAAGAATCAGTTTTCACTCAAACTGTCTTCTGTGACTGCTGCTGACACTGCTGTTTATTATTGTGCCAGGGAGGGGAAAAATGGGGCATTTGATATTTGGGGTCAGGGCACAATGGTGACAGTCAGCTCT [SEQ ID NO: 52]
CGCCATCAGATGACTCAGTCCCCCTCCAGTCTTTCTGCCTCAGTTGGGGATAGAGTGACCATCACATGCAGAGCAAGTCAGAGCATATCATCCTATCTGAACTGGTACCAGCAGAAGCCAGGGAAAGCCCCCAAATTGCTGATTTATGCAGCCTCAAGTCTCCAGAGTGGGGTGCCAAGCAGGTTCTCAGGCAGTGGCAGTGGGACAGATTTCACATTGACAATCAGCTCCCTCCAACCTGAAGATTTTGCCACCTACTATTGCCAGCAATCCTACAGCACGCCCCTGACTTTTGGAGGTGGCACAAAGGTAGAGATCAAGAGGACT [SEQ ID NO: 53]
GGSVSSGSYY [SEQ ID NO: 76]
IYYSGST [SEQ ID NO: 77]
AREGKNGAFDIW [SEQ ID NO: 78]
QSISSY [SEQ ID NO: 79]
AASS [SEQ ID NO: 80]
QQSYSTPLTF [SEQ ID NO: 81]
QVQLQESGPGLVKPSETLSLTCTVSGGSVSSGSYYWSWIRQPPGKGLEWIGYIYYSGSTNYNPSLKSRVTISVDTSKNQFSLKLSSVTAADTAVYYCAREGKNGAFDIWGQGTMVTVSS [SEQ ID NO: 82]
RHQMTQSPSSLSASVGDRVTITCRASQSISSYLNWYQQKPGKAPKLLIYAASSLQSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQSYSTPLTFGGGTKVEIKRT [SEQ ID NO: 83]
QVQLQESGPGLVKPSETLSLTCTVSGGSVSSGSYYWSWIRQPPGKGLEWIGYIYYSGSTNYNPSLKSRVTISVDTSKNQFSLKLSSVTAADTAVYYCAREGKNGAFDIWGQGTMVTVSSGGGGSGGGGSGGGGSRHQMTQSPSSLSASVGDRVTITCRASQSISSYLNWYQQKPGKAPKLLIYAASSLQSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQSYSTPLTFGGGTKVEIKRT [SEQ ID NO: 84]
CAGGTTCAGCTTCAGGAGAGTGGCCCAGGCCTGGTGAAGCCAAGTGAGACTCTCAGCTTGACTTGCACAGTTTCTGGAGGCAGTGTCTCCTCAGGCAGCTATTATTGGTCCTGGATTCGGCAGCCCCCTGGGAAAGGCCTGGAGTGGATTGGGTACATATATTACAGTGGCAGCACAAATTACAATCCATCCCTGAAGTCTCGAGTAACTATCAGTGTGGACACAAGCAAGAATCAGTTTTCACTCAAACTGTCTTCTGTGACTGCTGCTGACACTGCTGTTTATTATTGTGCCAGGGAGGGGAAAAATGGGGCATTTGATATTTGGGGTCAGGGCACAATGGTGACAGTCAGCTCTGGAGGTGGAGGCTCAGGAGGAGGAGGCAGTGGAGGTGGTGGGTCACGCCATCAGATGACTCAGTCCCCCTCCAGTCTTTCTGCCTCAGTTGGGGATAGAGTGACCATCACATGCAGAGCAAGTCAGAGCATATCATCCTATCTGAACTGGTACCAGCAGAAGCCAGGGAAAGCCCCCAAATTGCTGATTTATGCAGCCTCAAGTCTCCAGAGTGGGGTGCCAAGCAGGTTCTCAGGCAGTGGCAGTGGGACAGATTTCACATTGACAATCAGCTCCCTCCAACCTGAAGATTTTGCCACCTACTATTGCCAGCAATCCTACAGCACGCCCCTGACTTTTGGAGGTGGCACAAAGGTAGAGATCAAGAGGACT [SEQ ID NO: 85]
В некоторых вариантах осуществления вариабельная область тяжелой цепи включает аминокислотную последовательность, которая по меньшей мере приблизительно на 80%, по меньшей мере приблизительно на 80%, по меньшей мере приблизительно на 85%, по меньшей мере приблизительно на 90% или по меньшей мере приблизительно на 95% (например, приблизительно на 81%, приблизительно на 82%, приблизительно на 83%, приблизительно на 84%, приблизительно на 85%, приблизительно на 86%, приблизительно на 87%, приблизительно на 88%, приблизительно на 89%, приблизительно на 90%, приблизительно на 91%, приблизительно на 92%, приблизительно на 93%, приблизительно на 94%, приблизительно на 95%, приблизительно на 96%, приблизительно на 97%, приблизительно на 98% или приблизительно на 99%) гомологична или идентична аминокислотной последовательности, представленной в SEQ ID NO: 36, которая приведена ниже.
QVQLQESGPGLVKPSETLSLTCTVSGGSVSSGSYYWSWIRQPPGKGLE WIGYIYYSGSTNYNPSLKSRVTISVDTSKNQFSLKLSSVTAADTAVYY CAREGKNGAFDIWGQGTMVTVSSASTKGPSVFPLAPSSKSTSGGTAAL GCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPS SSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTSGQAG [SEQ ID NO: 36]
Примерная последовательность нуклеиновой кислоты, кодирующая аминокислотную последовательность SEQ ID NO: 36, представлена в SEQ ID NO: 37, которая приведена ниже.
caggtgcagctgcaggagtccggcccaggactggtgaagccttcggagaccctgtccctc 60
acctgcactgtctctggtggctccgtcagcagtggtagttactactggagctggatccgg 120
cagcccccagggaagggactggagtggattgggtatatctattacagtgggagcaccaac 180
tacaacccctccctcaagagtcgagtcaccatatcagtagacacgtccaagaaccagttc 240
tccctgaagctgagctctgtgaccgctgcggacacggccgtgtattactgtgcgagagag 300
gggaagaatggggcttttgatatctggggccaagggacaatggtcaccgtctcttcagcc 360
tccaccaagggcccatcggtcttccccctggcaccctcctccaagagcacctctgggggc 420
acagcggccctgggctgcctggtcaaggactacttccccgaaccggtgacggtgtcgtgg 480
aactcaggcgccctgaccagcggcgtgcacaccttcccggctgtcctacagtcctcagga 540
ctctactccctcagcagcgtggtgaccgtgccctccagcagcttgggcacccagacctac 600
atctgcaacgtgaatcacaagcccagcaacaccaaggtggacaagaaagttgagcccaaa 660
tcttgtgacaaaactagtggccaggccggccac 693 [SEQ ID NO: 37]
В некоторых вариантах осуществления, вариабельная область легкой цепи включает аминокислотную последовательность, которая по меньшей мере приблизительно на 80%, по меньшей мере приблизительно на 80%, по меньшей мере приблизительно на 85%, по меньшей мере приблизительно на 90% или по меньшей мере приблизительно на 95% (например, приблизительно на 81%, приблизительно на 82%, приблизительно на 83%, приблизительно на 84%, приблизительно на 85%, приблизительно на 86%, приблизительно на 87%, приблизительно на 88%, приблизительно на 89%, приблизительно на 90%, приблизительно на 91%, приблизительно на 92%, приблизительно на 93%, приблизительно на 94%, приблизительно на 95%, приблизительно на 96%, приблизительно на 97%, приблизительно на 98% или приблизительно на 99%) гомологична или идентична аминокислотной последовательности, представленной в SEQ ID NO: 38, которая приведена ниже.
DIQMTQSPSSLSASVGDRVTITCRASQSISSYLNWYQQKPGKAPKLLIYAASSLQSGVPSGFSGSGSGTDFTLTISSLQPEDFATYYCQQSYSTPLTFGGGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC [SEQ ID NO: 38]
Примерная последовательность нуклеиновой кислоты, кодирующая аминокислотную последовательность SEQ ID NO: 38, представлена в SEQ ID NO: 39, которая приведена ниже.
gacatccagatgacccagtctccatcctccctgtctgcatctgtaggagacagagtcacc 60
atcacttgccgggcaagtcagagcattagcagctatttaaattggtatcagcagaaacca 120
gggaaagcccctaagctcctgatctatgctgcatccagtttgcaaagtggggtcccatca 180
gggttcagtggcagtggatctgggacagatttcactctcaccatcagcagtctgcaacct 240
gaagattttgcaacttactactgtcaacagagttacagtaccccgctcactttcggcgga 300
gggaccaaggtggagatcaaacgaactgtggctgcaccatctgtcttcatcttcccgcca 360
tctgatgagcagttgaaatctggaactgcctctgttgtgtgcctgctgaataacttctat 420
cccagagaggccaaagtacagtggaaggtggataacgccctccaatcgggtaactcccag 480
gagagtgtcacagagcaggacagcaaggacagcacctactgcctcagcagcaccctgacg 540
ctgagcaaagcagactacgagaaacacaaactctacgcctgcgaagtcacccatcagggc 600
ctgagctcgcccgtcacaaagagcttcaacaggggagagt [SEQ ID NO: 39]
В некоторых вариантах осуществления вариабельная область легкой цепи включает аминокислотную последовательность, которая по меньшей мере приблизительно на 80%, по меньшей мере приблизительно на 80%, по меньшей мере приблизительно на 85%, по меньшей мере приблизительно на 90% или по меньшей мере приблизительно на 95% (например, приблизительно на 81%, приблизительно на 82%, приблизительно на 83%, приблизительно на 84%, приблизительно на 85%, приблизительно на 86%, приблизительно на 87%, приблизительно на 88%, приблизительно на 89%, приблизительно на 90%, приблизительно на 91%, приблизительно на 92%, приблизительно на 93%, приблизительно на 94%, приблизительно на 95%, приблизительно на 96%, приблизительно на 97%, приблизительно на 98% или приблизительно на 99%) гомологична или идентична аминокислотной последовательности, представленной в SEQ ID NO: 40, которая приведена ниже.
RHQMTQSPSSLSASVGDRVTITCRASQSISSYLNWYQQKPGKAPKLLIYAASSLQSGVPSGFSGSGSGTDFTLTISSLQPEDFATYYCQQSYSTPLTFGGGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC [SEQ ID NO: 40]
В некоторых вариантах осуществления вариабельная область тяжелой цепи включает аминокислотную последовательность, которая по меньшей мере приблизительно на 80%, по меньшей мере приблизительно на 80%, по меньшей мере приблизительно на 85%, по меньшей мере приблизительно на 90% или по меньшей мере приблизительно на 95% (например, приблизительно на 81%, приблизительно на 82%, приблизительно на 83%, приблизительно на 84%, приблизительно на 85%, приблизительно на 86%, приблизительно на 87%, приблизительно на 88%, приблизительно на 89%, приблизительно на 90%, приблизительно на 91%, приблизительно на 92%, приблизительно на 93%, приблизительно на 94%, приблизительно на 95%, приблизительно на 96%, приблизительно на 97%, приблизительно на 98% или приблизительно на 99%) гомологична или идентична аминокислотной последовательности, представленной в SEQ ID NO: 41, которая приведена ниже.
QVQLQESGPGLVKPSETLSLTCTVSGGSVSSGSYYWSWIRQPPGKGLEWIGYIYYSGSTNYNPSLKSRVTISVDTSKNQFSLKLSSVTAADTAVYYCAREGKNGAFDIWGQGTMVTVSSS [SEQ ID NO: 41]
В некоторых вариантах осуществления вариабельная область легкой цепи включает аминокислоты 1-107 из SEQ ID NO: 38. В некоторых вариантах осуществления вариабельная область легкой цепи включает аминокислоты 1-107 из SEQ ID NO: 40.
В некоторых вариантах осуществления внеклеточный антигенсвязывающий домен CAR (например, scFv) включает аминокислотную последовательность, которая по меньшей мере приблизительно на 80%, по меньшей мере приблизительно на 80%, по меньшей мере приблизительно на 85%, по меньшей мере приблизительно на 90% или по меньшей мере приблизительно на 95% (например, приблизительно на 81%, приблизительно на 82%, приблизительно на 83%, приблизительно на 84%, приблизительно на 85%, приблизительно на 86%, приблизительно на 87%, приблизительно на 88%, приблизительно на 89%, приблизительно на 90%, приблизительно на 91%, приблизительно на 92%, приблизительно на 93%, приблизительно на 94%, приблизительно на 95%, приблизительно на 96%, приблизительно на 97%, приблизительно на 98% или приблизительно на 99%) гомологична или идентична аминокислотной последовательности, представленной в SEQ ID NO: 42, которая приведена ниже.
QVQLQESGPGLVKPSETLSLTCTVSGGSVSSGSYYWSWIRQPPGKGLEWIGYIYYSGSTNYNPSLKSRVTISVDTSKNQFSLKLSSVTAADTAVYYCAREGKNGAFDIWGQGTMVTVSSSGGGGSGGGGSGGGGSRHQMTQSPSSLSASVGDRVTITCRASQSISSYLNWYQQKPGKAPKLLIYAASSLQSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQSYSTPLTFGGGTKVEIKGQAGHHHHHHGDYKDDDDKG [SEQ ID NO: 42]
Примерная последовательность нуклеиновой кислоты, кодирующая аминокислотную последовательность SEQ ID NO: 42, представлена в SEQ ID NO: 45, которая приведена ниже.
atggccttaccagtgaccgccttgctcctgccgctggccttgctgctccacgccgccaggccgcaggtgcagctgcaggagtccggcccaggactggtgaagccttcggagaccctgtccctcacctgcactgtctctggtggctccgtcagcagtggtagttactactggagctggatccggcagcccccagggaagggactggagtggattgggtatatctattacagtgggagcaccaactacaacccctccctcaagagtcgagtcaccatatcagtagacacgtccaagaaccagttctccctgaagctgagctctgtgaccgctgcggacacggccgtgtattactgtgcgagagaggggaagaatggggcttttgatatctggggccaagggacaatggtcaccgtctcttcaggtggaggcggttcaggcggaggtggctctggcggtggcggatcacgacatcagatgacccagtctccatcctccctgtctgcatctgtaggagacagagtcaccatcacttgccgggcaagtcagagcattagcagctatttaaattggtatcagcagaaaccagggaaagcccctaagctcctgatctatgctgcatccagtttgcaaagtggggtcccatcaaggttcagtggcagtggatctgggacagatttcactctcaccatcagcagtctgcaacctgaagattttgcaacttactactgtcaacagagttacagtaccccgctcactttcggcggagggaccaaggtggagatcaaacggactgcggccgca [SEQ ID NO: 45]
Примерная последовательность нуклеиновой кислоты, кодирующая аминокислотную последовательность SEQ ID NO: 42, представлена в SEQ ID NO: 46, которая приведена ниже. Последовательность нуклеиновой кислоты, представленная в SEQ ID NO: 46, синтетически оптимизирована по использованию кодонов, что может повысить экспрессию CAR.
ATGGCGCTGCCGGTGACCGCGCTGCTGCTGCCGCTGGCGCTGCTGCTGCATGCGGCGCGCCCGCAGGTGCAGCTGCAGGAAAGCGGCCCGGGCCTGGTGAAACCGAGCGAAACCCTGAGCCTGACCTGCACCGTGAGCGGCGGCAGCGTGAGCAGCGGCAGCTATTATTGGAGCTGGATTCGCCAGCCGCCGGGCAAAGGCCTGGAATGGATTGGCTATATTTATTATAGCGGCAGCACCAACTATAACCCGAGCCTGAAAAGCCGCGTGACCATTAGCGTGGATACCAGCAAAAACCAGTTTAGCCTGAAACTGAGCAGCGTGACCGCGGCGGATACCGCGGTGTATTATTGCGCGCGCGAAGGCAAAAACGGCGCGTTTGATATTTGGGGCCAGGGCACCATGGTGACCGTGAGCAGCGGCGGCGGCGGCAGCGGCGGCGGCGGCAGCGGCGGCGGCGGCAGCCGCCATCAGATGACCCAGAGCCCGAGCAGCCTGAGCGCGAGCGTGGGCGATCGCGTGACCATTACCTGCCGCGCGAGCCAGAGCATTAGCAGCTATCTGAACTGGTATCAGCAGAAACCGGGCAAAGCGCCGAAACTGCTGATTTATGCGGCGAGCAGCCTGCAGAGCGGCGTGCCGAGCCGCTTTAGCGGCAGCGGCAGCGGCACCGATTTTACCCTGACCATTAGCAGCCTGCAGCCGGAAGATTTTGCGACCTATTATTGCCAGCAGAGCTATAGCACCCCGCTGACCTTTGGCGGCGGCACCAAAGTGGAAATTAAACGCACCGCGGCGGCG [SEQ ID NO: 46]
Примерная последовательность нуклеиновой кислоты, кодирующая аминокислотную последовательность SEQ ID NO: 42, представлена в SEQ ID NO: 47, которая приведена ниже. Последовательность нуклеиновой кислоты, представленная в SEQ ID NO: 47, синтетически оптимизирована по использованию кодонов, что может повысить экспрессию CAR.
atggccCTCCCGGTAACGGCTCTGCTGCTTCCACTCGCACTGCTCTTGCATGCTGCCAGACCACAGGTCCAGCTGCAGGAGAGTGGGCCTGGACTGGTTAAGCCGAGTGAGACACTTTCCTTGACGTGCACTGTGAGCGGGGGAAGTGTGTCCTCAGGTAGTTATTACTGGTCCTGGATTCGCCAGCCACCAGGAAAGGGACTGGAGTGGATAGGTTATATCTATTATTCTGGCAGCACTAATTACAATCCTTCTCTCAAAAGTAGGGTGACAATTTCAGTGGATACTTCCAAAAATCAGTTTAGTCTGAAGCTCAGCTCTGTGACAGCTGCTGATACTGCAGTTTACTACTGCGCCAGGGAGGGGAAGAATGGCGCCTTCGATATTTGGGGACAGGGCACTATGGTGACTGTATCAAGCGGAGGCGGTGGCAGCGGCGGGGGAGGGAGTGGAGGCGGCGGGTCTCGACATCAGATGACACAGAGCCCATCATCACTTAGCGCCAGCGTTGGCGACCGGGTTACGATAACATGCAGGGCTTCCCAATCTATCAGTTCTTATCTGAACTGGTATCAGCAGAAACCAGGTAAGGCCCCCAAGCTGCTCATCTACGCAGCCTCATCCCTGCAGAGCGGCGTCCCTAGTCGATTTTCCGGTAGTGGGTCAGGGACAGATTTTACCCTGACTATCAGTTCACTGCAGCCCGAGGACTTCGCGACATACTATTGCCAACAGTCCTATAGTACACCCTTGACATTTGGCGGCGGGACTAAAGTAGAAATTAAACGCACCgcggccgca [SEQ ID NO: 47]
Аминокислотные последовательности VH и/или VL, состоящие из последовательности, по меньшей мере приблизительно на 80%, по меньшей мере приблизительно на 80%, по меньшей мере приблизительно на 85%, по меньшей мере приблизительно на 90% или по меньшей мере приблизительно на 95% (например, приблизительно на 81%, приблизительно на 82%, приблизительно на 83%, приблизительно на 84%, приблизительно на 85%, приблизительно на 86%, приблизительно на 87%, приблизительно на 88%, приблизительно на 89%, приблизительно на 90%, приблизительно на 91%, приблизительно на 92%, приблизительно на 93%, приблизительно на 94%, приблизительно на 95%, приблизительно на 96%, приблизительно на 97%, приблизительно на 98% или приблизительно на 99%) гомологичной или идентичной определенной последовательности (например, SEQ ID NO: 82, SEQ ID NO: 83, SEQ ID NO: 36, SEQ ID NO: 38, SEQ ID NO: 40, SEQ ID NO: 41 или SEQ ID NO: 42), могут включать замены (например, консервативные замены), вставки или делеции по сравнению с указанной последовательностью(ями), но при этом сохранять способность связываться с антигеном-мишенью (например, мезотелином). В некоторых вариантах осуществления в общей сложности 1-10 аминокислот заменены, вставлены и/или удалены в определенной последовательности (например, SEQ ID NO: 82, SEQ ID NO: 83, SEQ ID NO: 36, SEQ ID NO: 38, SEQ ID NO: 40, SEQ ID NO: 41 или SEQ ID NO: 42). В некоторых вариантах осуществления замены, вставки или делеции присутствуют в областях за пределами CDR-областей (например, в FR-областях) внеклеточного антигенсвязывающего домена. В некоторых вариантах осуществления внеклеточный антигенсвязывающий домен включает последовательность VH и/или VL, выбранную из группы, состоящей из SEQ ID NO: 82 и 83, включая посттрансляционные модификации такой последовательности (SEQ ID NO: 82 и 83).
5.2.2.2. Трансмембранный домен CAR
В некоторых вариантах осуществления CAR включает трансмембранный домен. В некоторых вариантах осуществления трансмембранный домен CAR включает гидрофобную альфа-спираль, которая охватывает по меньшей мере часть мембраны. Различные трансмембранные домены обеспечивают разную стабильность рецептора. После распознавания антигена рецепторы образуют кластер, и сигнал передается клетке. В соответствии с раскрытым в настоящем документе изобретением трансмембранный домен CAR может включать нативный или модифицированный трансмембранный домен полипептида CD8, полипептида CD28, полипептида CD3ζ, полипептида CD40, полипептида 4-1BB, полипептида OX40, полипептида CD84, полипептида CD166, полипептида CD8a, полипептида CD8b, полипептида ICOS, полипептида ICAM-1, полипептида CTLA-4, полипептида CD27, пептида CD40/My88, пептида NKGD2, синтетического полипептида (не на основе белка, ассоциированного с иммунным ответом) или их комбинацию.
CD8
В некоторых вариантах осуществления трансмембранный домен включает полипептид CD8 (например, трансмембранный домен CD8 или его часть). В некоторых вариантах осуществления трансмембранный домен включает трансмембранный домен CD8 человека или его часть. В некоторых вариантах осуществления полипептид CD8 включает или состоит из аминокислотной последовательности, которая по меньшей мере приблизительно на 80%, по меньшей мере приблизительно на 85%, по меньшей мере приблизительно на 90%, по меньшей мере приблизительно на 95%, по меньшей мере приблизительно на 96%, по меньшей мере приблизительно на 97%, по меньшей мере приблизительно на 98%, по меньшей мере приблизительно на 99% или по меньшей мере приблизительно на 100% гомологична или идентична последовательности под номером NCBI: NP_001139345.1 (SEQ ID NO: 86), или ее фрагмента, и/или необязательно может включать до одной или до двух, или до трех консервативных аминокислотных замен. В некоторых вариантах осуществления полипептид CD8 включает или состоит из аминокислотной последовательности, которая является непрерывной частью SEQ ID NO: 86, которая имеет длину по меньшей мере приблизительно 20 или по меньшей мере приблизительно 30, или по меньшей мере приблизительно 40, или по меньшей мере приблизительно 50, или по меньшей мере приблизительно 60 или по меньшей мере приблизительно 70, и до приблизительно 235 аминокислот. В некоторых вариантах осуществления полипептид CD8 включает или состоит из аминокислотной последовательности аминокислот 1-235, 1-50, 50-100, 100-150, 150-200, 137-209 или 200-235 из SEQ ID NO: 86. В некоторых вариантах осуществления CAR раскрытого в настоящем документе изобретения включает трансмембранный домен, включающий полипептид CD8, включающий или состоящий из аминокислотной последовательности аминокислот 137-209 из SEQ ID NO: 86. В некоторых вариантах осуществления трансмембранный домен CAR включает полипептид CD8, включающий или состоящий из аминокислот 137-207 из SEQ ID NO: 86.
MALPVTALLLPLALLLHAARPSQFRVSPLDRTWNLGETVELKCQVLLSNPTSGCSWLFQPRGAAASPTFLLYLSQNKPKAAEGLDTQRFSGKRLGDTFVLTLSDFRRENEGYYFCSALSNSIMYFSHFVPVFLPAKPTTTPAPRPPTPAPTIASQPLSLRPEACRPAAGGAVHTRGLDFACDIYIWAPLAGTCGVLLLSLVITLYCNHRNRRRVCKCPRPVVKSGDKPSLSARYV [SEQ ID NO: 86]
В некоторых вариантах осуществления трансмембранный домен включает трансмембранный домен CD8 мыши или его часть. В некоторых вариантах осуществления полипептид CD8 включает или состоит из аминокислотной последовательности, которая по меньшей мере приблизительно на 80%, по меньшей мере приблизительно на 85%, по меньшей мере приблизительно на 90%, по меньшей мере приблизительно на 95%, по меньшей мере приблизительно на 96%, по меньшей мере приблизительно на 97%, по меньшей мере приблизительно на 98%, по меньшей мере приблизительно на 99% или по меньшей мере приблизительно на 100% гомологична или идентична последовательности под номером NCBI: AAA92533.1 (SEQ ID NO: 87), или ее фрагменту, и/или может необязательно включать до одной или до двух, или до трех консервативных аминокислотных замен. В некоторых вариантах осуществления полипептид CD8 включает или состоит из аминокислотной последовательности, которая является непрерывной частью SEQ ID NO: 87, которая имеет длину по меньшей мере приблизительно 20 или по меньшей мере приблизительно 30, или по меньшей мере приблизительно 40, или по меньшей мере приблизительно 50, или по меньшей мере приблизительно 60, или по меньшей мере приблизительно 70, или по меньшей мере приблизительно 100, или по меньшей мере приблизительно 200 и до 247 аминокислот. В некоторых вариантах осуществления полипептид CD8 включает или состоит из аминокислотной последовательности аминокислот 1-247, 1-50, 50-100, 100-150, 150-200, 151-219 или 200-247 из SEQ ID NO: 87. В некоторых вариантах осуществления трансмембранный домен CAR включает полипептид CD8, который включает или состоит из аминокислот 151-219 из SEQ ID NO: 87.
1 MASPLTRFLS LNLLLMGESI ILGSGEAKPQ APELRIFPKK MDAELGQKVD LVCEVLGSVS
61 QGCSWLFQNS SSKLPQPTFV VYMASSHNKI TWDEKLNSSK LFSAVRDTNN KYVLTLNKFS
121 KENEGYYFCS VISNSVMYFS SVVPVLQKVN STTTKPVLRT PSPVHPTGTS QPQRPEDCRP
181 RGSVKGTGLD FACDIYIWAP LAGICVAPLL SLIITLICYH RSRKRVCKCP RPLVRQEGKP
241 RPSEKIV [SEQ ID NO: 87]
В некоторых вариантах осуществления полипептид CD8 включает или состоит из аминокислотной последовательности, представленной в SEQ ID NO: 88, которая приведена ниже:
STTTKPVLRTPSPVHPTGTSQPQRPEDCRPRGSVKGTGLDFACDIYIWAPLAGICVALLLSLIITLICY [SEQ ID NO: 88]
Примерная нуклеотидная последовательность, кодирующая аминокислотную последовательность SEQ ID NO: 88, представлена в SEQ ID NO: 89, которая приведена ниже.
TCTACTACTACCAAGCCAGTGCTGCGAACTCCCTCACCTGTGCACCCTACCGGGACATCTCAGCCCCAGAGACCAGAAGATTGTCGGCCCCGTGGCTCAGTGAAGGGGACCGGATTGGACTTCGCCTGTGATATTTACATCTGGGCACCCTTGGCCGGAATCTGCGTGGCCCTTCTGCTGTCCTTGATCATCACTCTCATCTGCTAC [SEQ ID NO: 89]
CD28
В некоторых вариантах осуществления трансмембранный домен CAR включает полипептид CD28 (например, трансмембранный домен CD28 или его часть). В некоторых вариантах осуществления трансмембранный домен включает трансмембранный домен CD28 человека или его часть. В некоторых вариантах осуществления полипептид CD28 включает или состоит из аминокислотной последовательности, которая по меньшей мере приблизительно на 80%, по меньшей мере приблизительно на 85%, по меньшей мере приблизительно на 90%, по меньшей мере приблизительно на 95%, по меньшей мере приблизительно на 96%, по меньшей мере приблизительно на 97%, по меньшей мере приблизительно на 98%, по меньшей мере приблизительно на 99% или по меньшей мере приблизительно на 100% гомологична или идентична последовательности под номером NCBI: NP_006130 (SEQ ID NO: 90), или ее фрагменту, и/или необязательно может включать до одной или до двух, или до трех консервативных аминокислотных замен. В некоторых вариантах осуществления полипептид CD28 включает или состоит из аминокислотной последовательности, которая является непрерывной частью SEQ ID NO: 90, которая имеет длину по меньшей мере приблизительно 20, по меньшей мере приблизительно 25 или по меньшей мере приблизительно 30, или по меньшей мере приблизительно 40, или по меньшей мере приблизительно 50, и до приблизительно 220 аминокислот. В некоторых вариантах осуществления полипептид CD28 включает или состоит из аминокислотной последовательности аминокислот 1-220, 1-50, 50-100, 100-150, 114-220, 153-179, 150-200 или 200-220 из SEQ ID NO: 90. В некоторых вариантах осуществления трансмембранный домен CAR включает полипептид CD28, включающий или состоящий из SEQ ID NO: 92 (или аминокислот 153-179 из SEQ ID NO: 90). Примерная последовательность нуклеиновой кислоты, кодирующая аминокислотную последовательность SEQ ID NO: 92 или аминокислоты 153-179 из SEQ ID NO: 90, представлена в SEQ ID NO: 93. В некоторых вариантах осуществления трансмембранный домен CAR включает полипептид CD28, включающий или состоящий из аминокислотной последовательности аминокислот 114-220 из SEQ ID NO: 90. Примерная нуклеотидная последовательность, кодирующая аминокислотную последовательность SEQ ID NO: 92 (или аминокислоты 153-179 из SEQ ID NO: 90), представлена в SEQ ID NO: 91. SEQ ID NO: 90-93 приведены ниже:
1 MLRLLLALNL FPSIQVTGNK ILVKQSPMLV AYDNAVNLSC KYSYNLFSRE FRASLHKGLD
61 SAVEVCVVYG NYSQQLQVYS KTGFNCDGKL GNESVTFYLQ NLYVNQTDIY FCKIEVMYPP
121 PYLDNEKSNG TIIHVKGKHL CPSPLFPGPS KPFWVLVVVG GVLACYSLLV TVAFIIFWVR
181 SKRSRLLHSD YMNMTPRRPG PTRKHYQPYA PPRDFAAYRS [SEQ ID NO: 90]
ttttgggtgctggtggtggttggtggagtcctggcttgctatagcttgctagtaacagtggcctttattattttctgggtg [SEQ ID NO: 91]
FWVLVVVGGV LACYSLLVTV AFIIFWV [SEQ ID NO: 92].
TTTTGGGTGCTGGTGGTGGTTGGTGGAGTCCTGGCTTGCTATAGCTTGCTAGTAACAGTGGCCTTTATTATTTTCTGGGTG [SEQ ID NO: 93]
В некоторых вариантах осуществления трансмембранный домен включает трансмембранный домен CD28 мыши или его часть. В некоторых вариантах осуществления полипептид CD28 включает или состоит из аминокислотной последовательности, которая по меньшей мере приблизительно на 80%, по меньшей мере приблизительно на 85%, по меньшей мере приблизительно на 90%, по меньшей мере приблизительно на 95%, по меньшей мере приблизительно на 96%, по меньшей мере приблизительно на 97%, по меньшей мере приблизительно на 98%, по меньшей мере приблизительно на 99% или по меньшей мере приблизительно на 100% гомологична или идентична последовательности под номером NCBI: NP_031668.3 (SEQ ID NO: 97) или ее фрагменту, и/или необязательно может включать до одной или до двух, или до трех консервативных аминокислотных замен. В некоторых вариантах осуществления полипептид CD28 включает или состоит из аминокислотной последовательности, которая является непрерывной частью SEQ ID NO: 97, которая имеет длину по меньшей мере приблизительно 20 или по меньшей мере приблизительно 30, или по меньшей мере приблизительно 40, или по меньшей мере приблизительно 50 и до 218 аминокислот. В некоторых вариантах осуществления полипептид CD28 включает или состоит из аминокислотной последовательности аминокислот 1-218, 1-50, 50-100, 100-150, 114-220, 150-200, 151-177 или 200-218 из SEQ ID NO: 97. В некоторых вариантах осуществления трансмембранный домен CAR включает полипептид CD28, включающий или состоящий из аминокислот 151-177 из SEQ ID NO: 97.
SEQ ID NO: 97 приведена ниже:
1 MTLRLLFLAL NFFSVQVTEN KILVKQSPLL VVDSNEVSLS CRYSYNLLAK EFRASLYKGV
61 NSDVEVCVGN GNFTYQPQFR SNAEFNCDGD FDNETVTFRL WNLHVNHTDI YFCKIEFMYP
121 PPYLDNERSN GTIIHIKEKH LCHTQSSPKL FWALVVVAGV LFCYGLLVTV ALCVIWTNSR
181 RNRLLQSDYM NMTPRRPGLT RKPYQPYAPA RDFAAYRP [SEQ ID NO: 97]
CD84
В некоторых вариантах осуществления трансмембранный домен CAR включает нативный или модифицированный трансмембранный домен полипептида CD84 или его часть. Полипептид CD84 может иметь аминокислотную последовательность, которая по меньшей мере приблизительно на 80%, по меньшей мере приблизительно на 85%, по меньшей мере приблизительно на 90%, по меньшей мере приблизительно на 95%, по меньшей мере приблизительно на 96%, по меньшей мере приблизительно на 97%, по меньшей мере приблизительно на 98%, по меньшей мере приблизительно на 99% или по меньшей мере приблизительно на 100% гомологична или идентична последовательности под номером NCBI: NP_001171808.1 (SEQ ID NO: 1) или ее фрагменту, и/или необязательно может включать до одной или до двух, или до трех консервативных аминокислотных замен. В некоторых вариантах осуществления полипептид CD84 включает или состоит из аминокислотной последовательности, которая является непрерывной частью SEQ ID NO: 1, которая имеет длину по меньшей мере приблизительно 20 или по меньшей мере приблизительно 30, или по меньшей мере приблизительно 40 или по меньшей мере приблизительно 50 и до приблизительно 345 аминокислот. В некоторых вариантах осуществления полипептид CD84 включает или состоит из аминокислотной последовательности аминокислот 1-345, 1-50, 50-100, 100-150, 150-200, 226-250, 250-300 или 300-345 из SEQ ID NO: 1. В некоторых вариантах осуществления трансмембранный домен CAR включает или состоит полипептида CD84, включающего или состоящего из аминокислот 226-250 из SEQ ID NO: 1.
SEQ ID NO: 1 приведена ниже:
1 maqhhlwill lclqtwpeaa gkdseiftvn gilgesvtfp vniqeprqvk iiawtsktsv
61 ayvtpgdset apvvtvthrn yyerihalgp nynlvisdlr medagdykad intqadpytt
121 tkrynlqiyr rlgkpkitqs lmasvnstcn vtltcsveke eknvtynwsp lgeegnvlqi
181 fqtpedqelt ytctaqnpvs nnsdsisarq lcadiamgfr thhtgllsvl amffllvlil
241 ssvflfrlfk rrqgrifpeg sclntftknp yaaskktiyt yimasrntqp aesriydeil
301 qskvlpskee pvntvysevq fadkmgkast qdskppgtss yeivi [SEQ ID NO: 1]
Примерная нуклеотидная последовательность, кодирующая аминокислоты 226-250 из SEQ ID NO: 1, представлена в SEQ ID NO: 2, которая приведена ниже.
TTGCTGAGCGTGCTGGCTATGTTCTTTCTGCTTGTTCTCATTCTGTCTTCAGTGTTTTTGTTCCGTTTGTTCAAG [SEQ ID NO: 2]
CD166
В некоторых вариантах осуществления трансмембранный домен CAR включает нативный или модифицированный трансмембранный домен полипептида CD166 или его часть. Полипептид CD166 может иметь аминокислотную последовательность, которая по меньшей мере приблизительно на 80%, по меньшей мере приблизительно на 85%, по меньшей мере приблизительно на 90%, по меньшей мере приблизительно на 95%, по меньшей мере приблизительно на 96%, по меньшей мере приблизительно на 97%, по меньшей мере приблизительно на 98%, по меньшей мере приблизительно на 99% или по меньшей мере приблизительно на 100% гомологична или идентична последовательности под номером NCBI: NP_001618.2 (SEQ ID NO: 3) или ее фрагменту, и/или необязательно может включать до одной или до двух, или до трех консервативных аминокислотных замен. В некоторых вариантах осуществления полипептид CD166 включает или состоит из аминокислотной последовательности, которая является непрерывной частью SEQ ID NO: 3, которая имеет длину по меньшей мере приблизительно 20 или по меньшей мере приблизительно 30, или по меньшей мере приблизительно 40, или по меньшей мере приблизительно 50, по меньшей мере приблизительно 100 и до приблизительно 583 аминокислот. В некоторых вариантах осуществления полипептид CD166 включает или состоит из аминокислотной последовательности аминокислот 1-583, 1-50, 50-100, 100-150, 150-200, 200-300, 300-400, 400-500, 528-549 или 500-583 из SEQ ID NO: 3. В некоторых вариантах осуществления полипептид CD166, содержащийся в трансмембранном домене раскрытого в настоящем документе CAR-рецептора, включает или состоит из аминокислотной последовательности аминокислот 528-553 из SEQ ID NO: 3. В некоторых вариантах осуществления полипептид CD166, содержащийся в трансмембранном домене CAR, включает или состоит из аминокислотной последовательности аминокислот 528-549 из SEQ ID NO: 3.
SEQ ID NO: 3 приведена ниже:
1 MESKGASSCR LLFCLLISAT VFRPGLGWYT VNSAYGDTII IPCRLDVPQN LMFGKWKYEK
61 PDGSPVFIAF RSSTKKSVQY DDVPEYKDRL NLSENYTLSI SNARISDEKR FVCMLVTEDN
121 VFEAPTIVKV FKQPSKPEIV SKALFLETEQ LKKLGDCISE DSYPDGNITW YRNGKVLHPL
181 EGAVVIIFKK EMDPVTQLYT MTSTLEYKTT KADIQMPFTC SVTYYGPSGQ KTIHSEQAVF
241 DIYYPTEQVT IQVLPPKNAI KEGDNITLKC LGNGNPPPEE FLFYLPGQPE GIRSSNTYTL
301 TDVRRNATGD YKCSLIDKKS MIASTAITVH YLDLSLNPSG EVTRQIGDAL PVSCTISASR
361 NATVVWMKDN IRLRSSPSFS SLHYQDAGNY VCETALQEVE GLKKRESLTL IVEGKPQIKM
421 TKKTDPSGLS KTIICHVEGF PKPAIQWTIT GSGSVINQTE ESPYINGRYY SKIIISPEEN
481 VTLTCTAENQ LERTVNSLNV SAISIPEHDE ADEISDENRE KVNDQAKLIV GIVVGLLLAA
541 LVAGVVYWLY MKKSKTASKH VNKDLGNMEE NKKLEENNHK TEA [SEQ ID NO: 3]
Примерная нуклеотидная последовательность, кодирующая аминокислоты 528-553 из SEQ ID NO: 3, представлена в SEQ ID NO: 4, которая приведена ниже.
CTAATTGTGGGAATCGTTGTTGGTCTCCTCCTTGCTGCCCTTGTTGCTGGTGTCGTCTACTGGCTGTACATGAAGAAG [SEQ ID NO: 4]
CD8a
В некоторых вариантах осуществления трансмембранный домен CAR включает нативный или модифицированный трансмембранный домен полипептида CD8a или его часть. Полипептид CD8a может иметь аминокислотную последовательность, которая по меньшей мере приблизительно на 80%, по меньшей мере приблизительно на 85%, по меньшей мере приблизительно на 90%, по меньшей мере приблизительно на 95%, по меньшей мере приблизительно на 96%, по меньшей мере приблизительно на 97%, по меньшей мере приблизительно на 98%, по меньшей мере приблизительно на 99% или по меньшей мере приблизительно на 100% гомологична или идентична последовательности, состоящей из номера NCBI: NP_001139345.1 (SEQ ID NO: 5) или ее фрагментов, и/или необязательно может включать до одной или до двух, или до трех консервативных аминокислотных замен. В некоторых вариантах осуществления полипептид CD8a включает или состоит из аминокислотной последовательности, которая является непрерывной частью SEQ ID NO: 5, которая имеет длину по меньшей мере приблизительно 20 или по меньшей мере приблизительно 30, или по меньшей мере приблизительно 40, или по меньшей мере приблизительно 50 и до приблизительно 235 аминокислот. В некоторых вариантах осуществления полипептид CD8a включает или состоит из аминокислотной последовательности аминокислот 1-235, 1-50, 50-100, 100-150, 183-207, 150-200 или 200-235 из SEQ ID NO: 5. В некоторых вариантах осуществления трансмембранный домен CAR включает полипептид CD8a, включающий или состоящий из аминокислот 183-207 из SEQ ID NO: 5. SEQ ID NO: 5 приведена ниже:
1 MALPVTALLL PLALLLHAAR PSQFRVSPLD RTWNLGETVE LKCQVLLSNP TSGCSWLFQP
61 RGAAASPTFL LYLSQNKPKA AEGLDTQRFS GKRLGDTFVL TLSDFRRENE GYYFCSALSN
121 SIMYFSHFVP VFLPAKPTTT PAPRPPTPAP TIASQPLSLR PEACRPAAGG AVHTRGLDFA
181 CDIYIWAPLA GTCGVLLLSL VITLYCNHRN RRRVCKCPRP VVKSGDKPSL SARYV
[SEQ ID NO: 5]
Примерная нуклеотидная последовательность, кодирующая аминокислоты 183-207 из SEQ ID NO: 5, представлена в SEQ ID NO: 6, которая приведена ниже.
atctacatctgggcgcccttggccgggacttgtggggtccttctcctgtcactggttatcaccctttactgcaac [SEQ ID NO: 6]
CD8b
В некоторых вариантах осуществления трансмембранный домен CAR включает нативный или модифицированный трансмембранный домен полипептида CD8b или его часть. Полипептид CD8b может иметь аминокислотную последовательность, которая по меньшей мере приблизительно на 80%, по меньшей мере приблизительно на 85%, по меньшей мере приблизительно на 90%, по меньшей мере приблизительно на 95%, по меньшей мере приблизительно на 96%, по меньшей мере приблизительно на 97%, по меньшей мере приблизительно на 98%, по меньшей мере приблизительно на 99% или по меньшей мере приблизительно на 100% гомологична или идентична последовательности под номером NCBI: NP_742099.1 (SEQ ID NO: 7), или ее фрагментам, и/или могут необязательно включать до одной или до двух, или до трех консервативных аминокислотных замен. В некоторых вариантах осуществления полипептид CD8b включает или состоит из аминокислотной последовательности, которая является непрерывной частью SEQ ID NO: 7, которая имеет длину по меньшей мере приблизительно 20 или по меньшей мере приблизительно 30, или по меньшей мере приблизительно 40, или по меньшей мере приблизительно 50 и до приблизительно 221 аминокислоты. В некоторых вариантах осуществления полипептид CD8b включает или состоит из аминокислотной последовательности аминокислот 1-221, 1-50, 50-100, 100-150, 171-195, 150-200 или 200-221 из SEQ ID NO: 7. В некоторых вариантах осуществления трансмембранный домен CAR включает полипептид CD8b, включающий или состоящий из аминокислот 171-195 из SEQ ID NO: 7. SEQ ID NO: 7 приведена ниже:
1 MRPRLWLLLA AQLTVLHGNS VLQQTPAYIK VQTNKMVMLS CEAKISLSNM RIYWLRQRQA
61 PSSDSHHEFL ALWDSAKGTI HGEEVEQEKI AVFRDASRFI LNLTSVKPED SGIYFCMIVG
121 SPELTFGKGT QLSVVDFLPT TAQPTKKSTL KKRVCRLPRP ETQKGPLCSP ITLGLLVAGV
181 LVLLVSLGVA IHLCCRRRRA RLRFMKQLRL HPLEKCSRMD Y [SEQ ID NO: 7]
Примерная нуклеотидная последовательность, кодирующая аминокислоты 171-195 из SEQ ID NO: 7, представлена в SEQ ID NO: 8, которая приведена ниже.
ATCACCCTTGGCCTGCTGGTGGCTGGCGTCCTGGTTCTGCTGGTTTCCCTGGGAGTGGCCATCCACCTGTGCTGC [SEQ ID NO: 8]
ICOS
В некоторых вариантах осуществления трансмембранный домен CAR включает нативный или модифицированный трансмембранный домен полипептида ICOS или его часть. Полипептид ICOS может иметь аминокислотную последовательность, которая по меньшей мере приблизительно на 80%, по меньшей мере приблизительно на 85%, по меньшей мере приблизительно на 90%, по меньшей мере приблизительно на 95%, по меньшей мере приблизительно на 96%, по меньшей мере приблизительно на 97%, по меньшей мере приблизительно на 98%, по меньшей мере приблизительно на 99% или по меньшей мере приблизительно на 100% гомологична или идентична последовательности под номером NCBI: NP_036224.1 (SEQ ID NO: 9) или ее фрагменту, и/или необязательно может включать до одной или до двух, или до трех консервативных аминокислотных замен. В некоторых вариантах осуществления полипептид ICOS включает или состоит из аминокислотной последовательности, которая является непрерывной частью SEQ ID NO: 9, которая имеет длину по меньшей мере приблизительно 20 или по меньшей мере приблизительно 30, или по меньшей мере приблизительно 40, или по меньшей мере приблизительно 50 и до приблизительно 199 аминокислот. В некоторых вариантах осуществления полипептид ICOS включает или состоит из аминокислотной последовательности аминокислот 1-199, 1-50, 50-100, 100-150, 141-165 или 150-199 из SEQ ID NO: 9. В некоторых вариантах осуществления трансмембранный домен CAR включает полипептид ICOS, включающий или состоящий из аминокислот 141-165 из SEQ ID NO: 9. SEQ ID NO: 9 приведена ниже:
1 MKSGLWYFFL FCLRIKVLTG EINGSANYEM FIFHNGGVQI LCKYPDIVQQ FKMQLLKGGQ
61 ILCDLTKTKG SGNTVSIKSL KFCHSQLSNN SVSFFLYNLD HSHANYYFCN LSIFDPPPFK
121 VTLTGGYLHI YESQLCCQLK FWLPIGCAAF VVVCILGCIL ICWLTKKKYS SSVHDPNGEY
181 MFMRAVNTAK KSRLTDVTL [SEQ ID NO: 9]
Примерная нуклеотидная последовательность, кодирующая аминокислоты 141-165 из SEQ ID NO: 9, представлена в SEQ ID NO: 10, которая приведена ниже.
TTCTGGTTACCCATAGGATGTGCAGCCTTTGTTGTAGTCTGCATTTTGGGATGCATACTTATTTGTTGGCTTACA [SEQ ID NO: 10]
CTLA-4
В некоторых вариантах осуществления трансмембранный домен CAR включает нативный или модифицированный трансмембранный домен полипептида CTLA-4 или его часть. Полипептид CTLA-4 может иметь аминокислотную последовательность, которая по меньшей мере приблизительно на 80%, по меньшей мере приблизительно на 85%, по меньшей мере приблизительно на 90%, по меньшей мере приблизительно на 95%, по меньшей мере приблизительно на 96%, по меньшей мере приблизительно на 97%, по меньшей мере приблизительно на 98%, по меньшей мере приблизительно на 99% или по меньшей мере приблизительно на 100% гомологична или идентична последовательности под номером NCBI: NP_005205.2 (SEQ ID NO: 11) или ее фрагменту, и/или необязательно может включать до одной или до двух, или до трех консервативных аминокислотных замен. В некоторых вариантах осуществления полипептид CTLA-4 включает или состоит из аминокислотной последовательности, которая является непрерывной частью SEQ ID NO: 11, которая имеет длину по меньшей мере приблизительно 20 или по меньшей мере приблизительно 30, или по меньшей мере приблизительно 40 или по меньшей мере приблизительно 50 и до приблизительно 223 аминокислот. В некоторых вариантах осуществления полипептид CTLA-4 включает или состоит из аминокислотной последовательности аминокислот 1-223, 1-50, 50-100, 100-150, 162-186, 150-200 или 200-223 из SEQ ID NO: 11. В некоторых вариантах осуществления трансмембранный домен CAR включает полипептид CTLA-4, включающий или состоящий из аминокислот 162-186 из SEQ ID NO: 11. SEQ ID NO: 11 приведена ниже:
1 MACLGFQRHK AQLNLATRTW PCTLLFFLLF IPVFCKAMHV AQPAVVLASS RGIASFVCEY
61 ASPGKATEVR VTVLRQADSQ VTEVCAATYM MGNELTFLDD SICTGTSSGN QVNLTIQGLR
121 AMDTGLYICK VELMYPPPYY LGIGNGTQIY VIDPEPCPDS DFLLWILAAV SSGLFFYSFL
181 LTAVSLSKML KKRSPLTTGV YVKMPPTEPE CEKQFQPYFI PIN [SEQ ID NO: 11]
Примерная нуклеотидная последовательность, кодирующая аминокислоты 162-186 из SEQ ID NO: 11, представлена в SEQ ID NO: 12, которая приведена ниже.
TTCCTCCTCTGGATCCTTGCAGCAGTTAGTTCGGGGTTGTTTTTTTATAGCTTTCTCCTCACAGCTGTTTCTTTG [SEQ ID NO: 12]
ICAM-1
В некоторых вариантах осуществления трансмембранный домен CAR включает нативный или модифицированный трансмембранный домен полипептида ICAM-1 или его часть. Полипептид ICAM-1 может иметь аминокислотную последовательность, которая по меньшей мере приблизительно на 80%, по меньшей мере приблизительно на 85%, по меньшей мере приблизительно на 90%, по меньшей мере приблизительно на 95%, по меньшей мере приблизительно на 96%, по меньшей мере приблизительно на 97%, по меньшей мере приблизительно на 98%, по меньшей мере приблизительно на 99% или по меньшей мере приблизительно на 100% гомологична или идентична последовательности под номером NCBI: NP_000192.2 (SEQ ID NO: 13) или ее фрагменту, и/или необязательно может включать до одной или до двух, или до трех консервативных аминокислотных замен. В некоторых вариантах осуществления полипептид ICAM-1 включает или состоит из аминокислотной последовательности, которая является непрерывной частью SEQ ID NO: 13, которая имеет длину по меньшей мере приблизительно 20 или по меньшей мере приблизительно 30, или по меньшей мере приблизительно 40, или по меньшей мере приблизительно 50 и до приблизительно 220 аминокислот. В некоторых вариантах осуществления полипептид ICAM-1 включает или состоит из аминокислотной последовательности аминокислот 1-532, 1-50, 50-100, 100-150, 150-200, 200-300, 300-400, 481-507, 400-500 или 500-532 из SEQ ID NO: 13. В некоторых вариантах осуществления трансмембранный домен CAR включает полипептид ICAM-1, включающий или состоящий из аминокислот 481-507 из SEQ ID NO: 13. SEQ ID NO: 13 приведена ниже:
1 MAPSSPRPAL PALLVLLGAL FPGPGNAQTS VSPSKVILPR GGSVLVTCST SCDQPKLLGI
61 ETPLPKKELL LPGNNRKVYE LSNVQEDSQP MCYSNCPDGQ STAKTFLTVY WTPERVELAP
121 LPSWQPVGKN LTLRCQVEGG APRANLTVVL LRGEKELKRE PAVGEPAEVT TTVLVRRDHH
181 GANFSCRTEL DLRPQGLELF ENTSAPYQLQ TFVLPATPPQ LVSPRVLEVD TQGTVVCSLD
241 GLFPVSEAQV HLALGDQRLN PTVTYGNDSF SAKASVSVTA EDEGTQRLTC AVILGNQSQE
301 TLQTVTIYSF PAPNVILTKP EVSEGTEVTV KCEAHPRAKV TLNGVPAQPL GPRAQLLLKA
361 TPEDNGRSFS CSATLEVAGQ LIHKNQTREL RVLYGPRLDE RDCPGNWTWP ENSQQTPMCQ
421 AWGNPLPELK CLKDGTFPLP IGESVTVTRD LEGTYLCRAR STQGEVTRKV TVNVLSPRYE
481 IVIITVVAAA VIMGTAGLST YLYNRQRKIK KYRLQQAQKG TPMKPNTQAT PP [SEQ ID NO: 13]
Примерная нуклеотидная последовательность, кодирующая аминокислоты 481-507 из SEQ ID NO: 13, представлена в SEQ ID NO: 14, которая приведена ниже.
ATTGTCATCATCACTGTGGTAGCAGCCGCAGTCATAATGGGCACTGCAGGCCTCAGCACGTACCTCTATAACCGCCAGCGG [SEQ ID NO: 14]
5.2.2.3. Шарнирная/спейсерная область CAR
В некоторых вариантах осуществления CAR включает шарнирную/спейсерную область, которая соединяет внеклеточный антигенсвязывающий домен с трансмембранным доменом. Шарнирная/спейсерная область может быть достаточно гибкой, чтобы позволять антигенсвязывающему домену ориентироваться в различных направлениях, облегчая распознавание антигена. В некоторых вариантах осуществления шарнирная/спейсерная область CAR может включать нативную или модифицированную шарнирную область полипептида CD8, полипептида CD28, полипептида CD3ζ, полипептида CD40, полипептида 4-1BB, полипептида OX40, полипептида CD84, полипептида CD166, полипептида CD8a, полипептида CD8b, полипептида ICOS, полипептида ICAM-1, полипептида CTLA-4, полипептида CD27, пептида CD40/My88, пептида NKGD2, синтетического полипептида (не на основе белка, ассоциированного с иммунным ответом) или их комбинации. Шарнирная/спейсерная область может быть шарнирной областью из IgG1 или CH2CH3 областью иммуноглобулина и частями CD3, частью полипептида CD28 (например, частью SEQ ID NO: 90), частью полипептида CD8 (например, частью SEQ ID NO: 86 или частью SEQ ID NO: 87), вариантом любого из предыдущих, который по меньшей мере приблизительно на 80%, по меньшей мере приблизительно на 85%, по меньшей мере приблизительно на 90%, по меньшей мере приблизительно на 95% или по меньшей мере приблизительно на 100% гомологичен или идентичен им, или синтетической спейсерной последовательностью.
CD28
В некоторых вариантах осуществления шарнирная/спейсерная область CAR включает нативную или модифицированную шарнирную область полипептида CD28 или ее часть, как описано в настоящем документе. В некоторых вариантах осуществления шарнирная/спейсерная область CAR включает полипептид CD28, включающий или состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 15 (или аминокислот 114-152 из SEQ ID NO: 90). SEQ ID NO: 15 приведена ниже.
IEVMYPPPYLDNEKSNGTIIHVKGKHLCPSPLFPGPSKP [SEQ ID NO: 15]
Примерная нуклеотидная последовательность, кодирующая аминокислотную последовательность SEQ ID NO: 15 (или аминокислоты 114-152 из SEQ ID NO: 90), представлена в SEQ ID NO: 54, которая приведена ниже.
attgaagttatgtatcctcctccttacctagacaatgagaagagcaatggaaccattatccatgtgaaagggaaacacctttgtccaagtcccctatttcccggaccttctaagccc [SEQ ID NO: 54]
CD84
В некоторых вариантах осуществления шарнирная/спейсерная область CAR включает нативную или модифицированную шарнирную область полипептида CD84 или ее часть, как описано в настоящем документе. В некоторых вариантах осуществления шарнирная/спейсерная область CAR включает полипептид CD84, включающий или состоящий из аминокислот 187-225 из SEQ ID NO: 1. Примерная нуклеотидная последовательность, кодирующая аминокислоты 187-225 из SEQ ID NO: 1, представлена в SEQ ID NO: 16, которая приведена ниже.
CAAGAGCTGACTTACACGTGTACAGCCCAGAACCCTGTCAGCAACAATTCTGACTCCATCTCTGCCCGGCAGCTCTGTGCAGACATCGCAATGGGCTTCCGTACTCACCACACCGGG [SEQ ID NO: 16]
CD166
В некоторых вариантах осуществления шарнирная/спейсерная область CAR включает нативную или модифицированную шарнирную область полипептида CD166 или ее часть, как описано в настоящем документе. В некоторых вариантах осуществления шарнирная/спейсерная область CAR включает полипептид CD166, включающий или состоящий из аминокислот 489-527 из SEQ ID NO: 3. Примерная нуклеотидная последовательность, кодирующая аминокислоты 489-527 из SEQ ID NO: 3, представлена в SEQ ID NO: 17, которая приведена ниже.
ACCAACTGGAGAGAACAGTAAACTCCTTGAATGTCTCTGCTATAAGTATTCCAGAACACGATGAGGCAGACGAGATAAGTGATGAAAACAGAGAAAAGGTGAATGACCAGGCAAAA [SEQ ID NO: 17]
В некоторых вариантах осуществления шарнирная/спейсерная область CAR включает полипептид CD166, включающий или состоящий из аминокислот 484-527 из SEQ ID NO: 3. В некоторых вариантах осуществления шарнирная/спейсерная область CAR включает полипептид CD166, включающий или состоящий из аминокислот 506-527 из SEQ ID NO: 3. В некоторых вариантах осуществления шарнирная/спейсерная область CAR включает полипептид CD166, включающий или состоящий из аминокислот 517-527 из SEQ ID NO: 3. В некоторых вариантах осуществления шарнирная/спейсерная область CAR включает полипептид CD166, включающий или состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 109 или SEQ ID NO: 110. SEQ ID NO: 109 и 110 приведены ниже.
NQLERTVNSLNVPAISIPEHDEADEISDENREKVNDQAK [SEQ ID NO: 109]
AAANQLERTVNSLNVSAISIPEHDEADEISDENREKVNDQAK [SEQ ID NO: 110]
В некоторых вариантах осуществления полипептид CD166, содержащийся в шарнирной/спейсерной области и трансмембранном домене CAR, включает или состоит из аминокислотной последовательности, представленной в SEQ ID NO: 111, SEQ ID NO: 112, SEQ ID NO: 113, SEQ ID NO: 114, SEQ ID NO: 115, SEQ ID NO: 116 или SEQ ID NO: 117. SEQ ID NO: 111-117 приведены ниже.
PEHDEADEISDENREKVNDQAKLIVGIVVGLLLAALVAGVVYWLYMKK [SEQ ID NO: 111]
ENREKVNDQAKLIVGIVVGLLLAALVAGVVYWLYMKK [SEQ ID NO: 112]
NQLERTVNSLNVPAISIPEHDEADEISDENREKVNDQAKLIVGIVVGLLLAALVAGVVYWLYMKK [SEQ ID NO: 113]
TCTAENQLERTVNSLNVSAISIPEHDEADEISDENREKVNDQAKLIVGIVVGLLLAALVAGVVYWL [SEQ ID NO: 114]
PEHDEADEISDENREKVNDQAKLIVGIVVGLLLAALVAGVVYWL [SEQ ID NO: 115]
NQLERTVNSLNVSAISIPEHDEADEISDENREKVNDQAKLIVGIVVGLLLAALVAGVVYWL [SEQ ID NO: 116]
AAANQLERTVNSLNVSAISIPEHDEADEISDENREKVNDQAKLIVGIVVGLLLAALVAGVVYWLYMKK [SEQ ID NO: 117]
CD8a
В некоторых вариантах осуществления шарнирная/спейсерная область CAR включает нативную или модифицированную шарнирную область полипептида CD8a или ее часть, как описано в настоящем документе. В некоторых вариантах осуществления шарнирная/спейсерная область CAR включает полипептид CD8a, включающий или состоящий из аминокислот 137-182 из SEQ ID NO: 5. Примерная нуклеотидная последовательность, кодирующая аминокислоты 137-182 из SEQ ID NO: 5, представлена в SEQ ID NO: 18, которая приведена ниже.
cccaccacgacgccagcgccgcgaccaccaacaccggcgcccaccatcgcgtcgcagcccctgtccctgcgcccagaggcgtgccggccagcggcggggggcgcagtgcacacgagggggctggacttcgcctgtgat [SEQ ID NO: 18]
CD8b
В некоторых вариантах осуществления шарнирная/спейсерная область CAR включает нативную или модифицированную шарнирную область полипептида CD8b, как описано в настоящем документе. В некоторых вариантах осуществления полипептид CD8b, содержащийся в шарнирной/спейсерной области CAR, включает или состоит из аминокислот 132-170 из SEQ ID NO: 7. Примерная нуклеотидная последовательность, кодирующая аминокислоты 132-170 из SEQ ID NO: 7, представлена в SEQ ID NO: 19, которая приведена ниже.
CTGAGTGTGGTTGATTTCCTTCCCACCACTGCCCAGCCCACCAAGAAGTCCACCCTCAAGAAGAGAGTGTGCCGGTTACCCAGGCCAGAGACCCAGAAGGGCCCACTTTGTAGCCCC [SEQ ID NO: 19]
ICOS
В некоторых вариантах осуществления шарнирная/спейсерная область CAR включает нативную или модифицированную шарнирную область полипептида ICOS или ее часть, как описано в настоящем документе. В некоторых вариантах осуществления шарнирная/спейсерная область CAR включает полипептид ICOS, включающий или состоящий из аминокислот 102-140 из SEQ ID NO: 9. Примерная нуклеотидная последовательность, кодирующая аминокислоты 102-140 из SEQ ID NO: 9, представлена в SEQ ID NO: 20, которая приведена ниже.
tctcatgccaactattacttctgcaacctatcaatttttgatcctcctccttttaaagtaactcttacaggaggatatttgcatatttatgaatcacaactttgttgccagctgaag [SEQ ID NO: 20]
CTLA-4
В некоторых вариантах осуществления шарнирная/спейсерная область CAR включает нативную или модифицированную шарнирную область полипептида CTLA-4 или ее часть, как описано в настоящем документе. В некоторых вариантах осуществления шарнирная/спейсерная область CAR включает полипептид CTLA-4, включающий или состоящий из аминокислот 123-161 из SEQ ID NO: 11. Примерная нуклеотидная последовательность, кодирующая аминокислоты 123-161 из SEQ ID NO: 11, представлена в SEQ ID NO: 21, которая приведена ниже.
GACACGGGACTCTACATCTGCAAGGTGGAGCTCATGTACCCACCGCCATACTACCTGGGCATAGGCAACGGAACCCAGATTTATGTAATTGATCCAGAACCGTGCCCAGATTCTGAC [SEQ ID NO: 21]
ICAM-1
В некоторых вариантах осуществления шарнирная/спейсерная область CAR включает нативную или модифицированную шарнирную область полипептида ICAM-1 или ее часть, как описано в настоящем документе. В некоторых вариантах осуществления шарнирная/спейсерная область CAR включает полипептид ICAM-1, включающий или состоящий из аминокислот 442-480 из SEQ ID NO: 13. Примерная нуклеотидная последовательность, кодирующая аминокислоты 442-480 из SEQ ID NO: 13, представлена в SEQ ID NO: 22, которая приведена ниже.
GGGGAATCAGTGACTGTCACTCGAGATCTTGAGGGCACCTACCTCTGTCGGGCCAGGAGCACTCAAGGGGAGGTCACCCGCAAGGTGACCGTGAATGTGCTCTCCCCCCGGTATGAG [SEQ ID NO: 22]
В некоторых вариантах осуществления мезотелин-направленный CAR включает шарнирную/спейсерную область. В некоторых вариантах осуществления шарнирная/спейсерная область расположена между внеклеточным антигенсвязывающим доменом и трансмембранным доменом. В некоторых вариантах осуществления шарнирная/спейсерная область включает полипептид CD8, полипептид CD28, полипептид CD3ζ, полипептид CD4, полипептид 4-1BB, полипептид OX40, полипептид CD166, полипептид CD8a, полипептид CD8b, полипептид ICOS, полипептид ICAM-1, полипептид CTLA-4, полипептид CD27, пептид CD40/My88, пептид NKGD2, синтетический полипептид (не на основе белка, ассоциированного с иммунным ответом) или их комбинацию. В некоторых вариантах осуществления трансмембранный домен включает полипептид CD8, полипептид CD28, полипептид CD3ζ, полипептид CD4, полипептид 4-1BB, полипептид OX40, полипептид CD166, полипептид CD8a, полипептид CD8b, полипептид ICOS, полипептид ICAM-1, полипептид CTLA-4, полипептид CD27, пептид CD40/My88, пептид NKGD2, синтетический полипептид (не на основе белка, ассоциированного с иммунным ответом) или их комбинацию.
В некоторых вариантах осуществления трансмембранный домен и шарнирная/спейсерная область происходят из одной и той же молекулы. В некоторых вариантах осуществления трансмембранный домен и шарнирная/спейсерная область происходят из разных молекул. В некоторых вариантах осуществления шарнирная/спейсерная область CAR включает полипептид CD28, и трансмембранный домен CAR включает полипептид CD28. В некоторых вариантах осуществления шарнирная/спейсерная область CAR включает полипептид CD28, и трансмембранный домен CAR включает полипептид CD28. В некоторых вариантах осуществления шарнирная/спейсерная область CAR включает полипептид CD84, и трансмембранный домен CAR включает полипептид CD84. В некоторых вариантах осуществления шарнирная/спейсерная область CAR включает полипептид CD166, и трансмембранный домен CAR включает полипептид CD166. В некоторых вариантах осуществления шарнирная/спейсерная область CAR включает полипептид CD8a, и трансмембранный домен CAR включает полипептид CD8a. В некоторых вариантах осуществления шарнирная/спейсерная область CAR включает полипептид CD8b, и трансмембранный домен CAR включает полипептид CD8b. В некоторых вариантах осуществления шарнирная/спейсерная область CAR включает полипептид CD28, а трансмембранный домен CAR включает полипептид ICOS.
5.2.2.4. Внутриклеточный сигнальный домен CAR
A. CD3ζ
В некоторых вариантах осуществления CAR-рецептор включает внутриклеточный сигнальный домен. В некоторых вариантах осуществления внутриклеточный сигнальный домен CAR включает полипептид CD3ζ, который может активировать или стимулировать клетку (например, клетку лимфоидной линии дифференцировки, например, T-клетку). CD3ζ дикого типа ("нативный") включает три иммунорецепторых тирозиновых активирующих мотива ("ITAM") (например, ITAM1, ITAM2 и ITAM3), три области с богатым основными остатками участком (BRS) (BRS1, BRS2 и BRS3), и передает сигнал активации в клетку (например, клетку лимфоидной линии дифференцировки, например, T-клетку) после связывания антигена. Внутриклеточный сигнальный домен нативной CD3ζ-цепи является основным передатчиком сигналов от эндогенных TCR-рецепторов.
В некоторых вариантах осуществления внутриклеточный сигнальный домен CAR включает нативный полипептид CD3ζ. В некоторых вариантах осуществления нативный полипептид CD3ζ включает или состоит из аминокислотной последовательности, которая по меньшей мере приблизительно на 80%, по меньшей мере приблизительно на 85%, по меньшей мере приблизительно на 90%, по меньшей мере приблизительно на 95%, по меньшей мере приблизительно на 96%, по меньшей мере приблизительно на 97%, по меньшей мере приблизительно на 98%, по меньшей мере приблизительно на 99% или по меньшей мере приблизительно на 100% гомологична или идентична последовательности под номером NCBI: NP_932170 (SEQ ID NO: 94) или ее фрагменту. В некоторых вариантах осуществления нативный полипептид CD3ζ включает или состоит из аминокислотной последовательности, которая является непрерывной частью SEQ ID NO: 94, которая имеет длину по меньшей мере приблизительно 20 или по меньшей мере приблизительно 30, или по меньшей мере приблизительно 40, или по меньшей мере приблизительно 50, или по меньшей мере приблизительно 100, или по меньшей мере приблизительно 110 и до приблизительно 164 аминокислот. В некоторых вариантах осуществления нативный полипептид CD3ζ включает или состоит из аминокислотной последовательности аминокислот 1-50, 50-100, 100-150, 50-164, 55-164 или 150-164 из SEQ ID NO: 94. В некоторых вариантах осуществления нативный полипептид CD3ζ включает или состоит из аминокислотной последовательности аминокислот 52-164 из SEQ ID NO: 94.
SEQ ID NO: 94 приведена ниже:
1 MKWKALFTAA ILQAQLPITE AQSFGLLDPK LCYLLDGILF IYGVILTALF LRVKFSRSAD
61 APAYQQGQNQ LYNELNLGRR EEYDVLDKRR GRDPEMGGKP QRRKNPQEGL YNELQKDKMA
121 EAYSEIGMKG ERRRGKGHDG LYQGLSTATK DTYDALHMQA LPPR [SEQ ID NO: 94]
В некоторых вариантах осуществления полипептид CD3ζ включает или состоит из аминокислотной последовательности, которая по меньшей мере приблизительно на 80%, по меньшей мере приблизительно на 85%, по меньшей мере приблизительно на 90%, по меньшей мере приблизительно на 95%, по меньшей мере приблизительно на 96%, по меньшей мере приблизительно на 97%, по меньшей мере приблизительно на 98%, по меньшей мере приблизительно на 99% или по меньшей мере приблизительно на 100% гомологична или идентична аминокислотной последовательности, представленной в SEQ ID NO: 95, или ее фрагменту, и/или необязательно может включать до одной или до двух, или до трех консервативных аминокислотных замен. SEQ ID NO: 95 приведена ниже:
RVKFSRSADA PAYQQGQNQL YNELNLGRRE EYDVLDKRRG RDPEMGGKPR RKNPQEGLYN
ELQKDKMAEA YSEIGMKGER RRGKGHDGLY QGLSTATKDT YDALHMQALP PR [SEQ ID NO: 95]
Примерная нуклеотидная последовательность, кодирующая аминокислотную последовательность SEQ ID NO: 95, представлена в SEQ ID NO: 96, которая приведена ниже.
AGAGTGAAGTTCAGCAGGAGCGCAGACGCCCCCGCGTACCAGCAGGGCCAGAACCAGCTCTATAACGAGCTCAATCTAGGACGAAGAGAGGAGTACGATGTTTTGGACAAGAGACGTGGCCGGGACCCTGAGATGGGGGGAAAGCCGAGAAGGAAGAACCCTCAGGAAGGCCTGTACAATGAACTGCAGAAAGATAAGATGGCGGAGGCCTACAGTGAGATTGGGATGAAAGGCGAGCGCCGGAGGGGCAAGGGGCACGATGGCCTTTACCAGGGTCTCAGTACAGCCACCAAGGACACCTACGACGCCCTTCACATGCAGGCCCTGCCCCCTCGC [SEQ ID NO: 96]
В некоторых вариантах осуществления внутриклеточный сигнальный домен CAR включает модифицированный полипептид CD3ζ. В некоторых вариантах осуществления внутриклеточный сигнальный домен CAR включает модифицированный полипептид CD3ζ человека. В некоторых вариантах осуществления модифицированный полипептид CD3ζ включает или состоит из аминокислотной последовательности, которая по меньшей мере приблизительно на 80%, по меньшей мере приблизительно на 85%, по меньшей мере приблизительно на 90%, по меньшей мере приблизительно на 95%, по меньшей мере приблизительно на 96%, по меньшей мере приблизительно на 97%, по меньшей мере приблизительно на 98%, по меньшей мере приблизительно на 99% или по меньшей мере приблизительно на 100% гомологична или идентична аминокислотной последовательности, представленной в SEQ ID NO: 35, или ее фрагменту, и/или необязательно может включать до одной или до двух, или до трех консервативных аминокислотных замен. SEQ ID NO: 35 приведена ниже:
RVKFSRSADA PAYQQGQNQL YNELNLGRRE EYDVLDKRRG RDPEMGGKPR RKNPQEGLFN
ELQKDKMAEA FSEIGMKGER RRGKGHDGLF QGLSTATKDT FDALHMQALP PR [SEQ ID NO: 35]
Примерная нуклеотидная последовательность, кодирующая аминокислотную последовательность SEQ ID NO: 35, представлена в SEQ ID NO: 55, которая приведена ниже.
agagtgaagttcagcaggagcgcagacgcccccgcgtaccagcagggccagaaccagctctataacgagctcaatctaggacgaagagaggagtacgatgttttggacaagagacgtggccgggaccctgagatggggggaaagccgagaaggaagaaccctcaggaaggcctgtTcaatgaactgcagaaagataagatggcggaggcctTcagtgagattgggatgaaaggcgagcgccggaggggcaaggggcacgatggcctttTccaggggctcagtacagccaccaaggacacctTcgacgcccttcacatgcaggccctgccccctcgc [SEQ ID NO: 55]
В некоторых вариантах осуществления модифицированный полипептид CD3ζ включает один, два или три варианта ITAM. В некоторых вариантах осуществления модифицированный полипептид CD3ζ включает нативный ITAM1. В некоторых вариантах осуществления нативный ITAM1 включает или состоит из аминокислотной последовательности, представленной в SEQ ID NO: 23.
QNQLYNELNLGRREEYDVLDKR [SEQ ID NO: 23]
Примерная последовательность нуклеиновой кислоты, кодирующая аминокислотную последовательность SEQ ID NO: 23, представлена в SEQ ID NO: 24, которая приведена ниже.
cagaaccagctctataacgagctcaatctaggacgaagagaggagtacgatgttttggacaagaga [SEQ ID NO: 24]
В некоторых вариантах осуществления модифицированный полипептид CD3ζ включает вариант ITAM1, включающий одну или больше мутаций с потерей функции. В некоторых вариантах осуществления вариант ITAM1 включает или состоит из двух мутаций с потерей функции. В некоторых вариантах осуществления каждая из одной или больше (например, двух) мутаций с потерей функции включает или состоит из мутации остатка тирозина в ITAM1. В некоторых вариантах осуществления вариант ITAM1 (например, вариант, состоящий из двух мутаций с потерей функции) включает или состоит из аминокислотной последовательности, представленной в SEQ ID NO: 25, которая приведена ниже.
QNQLFNELNLGRREEFDVLDKR [SEQ ID NO: 25]
Примерная последовательность нуклеиновой кислоты, кодирующая аминокислотную последовательность SEQ ID NO: 25, представлена в SEQ ID NO: 26, которая приведена ниже.
cagaaccagctctTtaacgagctcaatctaggacgaagagaggagtTcgatgttttggacaagaga [SEQ ID NO: 26]
В некоторых вариантах осуществления модифицированный полипептид CD3ζ включает нативный ITAM2. В некоторых вариантах осуществления нативный ITAM2 включает или состоит из аминокислотной последовательности, представленной в SEQ ID NO: 27, которая приведена ниже.
QEGLYNELQKDKMAEAYSEIGMK [SEQ ID NO: 27]
Примерная последовательность нуклеиновой кислоты, кодирующая аминокислотную последовательность SEQ ID NO: 27, представлена в SEQ ID NO: 28, которая приведена ниже.
caggaaggcctgtacaatgaactgcagaaagataagatggcggaggcctacagtgagattgggatgaaa [SEQ ID NO: 28]
В некоторых вариантах осуществления модифицированный полипептид CD3ζ включает вариант ITAM2, включающий одну или больше мутаций с потерей функции. В некоторых вариантах осуществления вариант ITAM2 включает или состоит из двух мутаций с потерей функции. В некоторых вариантах осуществления каждая из одной или больше (например, двух) мутаций с потерей функции включает или состоит из мутации остатка тирозина в ITAM2. В некоторых вариантах осуществления вариант ITAM2 (например, вариант, состоящий из двух мутаций с потерей функции) включает или состоит из аминокислотной последовательности, представленной в SEQ ID NO: 29, которая приведена ниже.
QEGLFNELQKDKMAEAFSEIGMK [SEQ ID NO: 29]
Примерная последовательность нуклеиновой кислоты, кодирующая аминокислотную последовательность SEQ ID NO: 29, представлена в SEQ ID NO: 30, которая приведена ниже.
caggaaggcctgtTcaatgaactgcagaaagataagatggcggaggcctTcagtgagattgggatgaaa [SEQ ID NO: 30]
В некоторых вариантах осуществления модифицированный полипептид CD3ζ включает нативный ITAM3. В некоторых вариантах осуществления нативный ITAM3 включает или состоит из аминокислотной последовательности, представленной в SEQ ID NO: 31, которая приведена ниже.
HDGLYQGLSTATKDTYDALHMQ [SEQ ID NO: 31]
Примерная последовательность нуклеиновой кислоты, кодирующая аминокислотную последовательность SEQ ID NO: 31, представлена в SEQ ID NO: 32, которая приведена ниже.
cacgatggcctttaccagggtctcagtacagccaccaaggacacctacgacgcccttcacatgcag [SEQ ID NO: 32]
В некоторых вариантах осуществления модифицированный полипептид CD3ζ включает вариант ITAM3, включающий одну или больше мутаций с потерей функции. В некоторых вариантах осуществления вариант ITAM3 включает или состоит из двух мутаций с потерей функции. В некоторых вариантах осуществления каждая из одной или больше (например, двух) мутаций с потерей функции включает или состоит из мутации остатка тирозина в ITAM3. В некоторых вариантах осуществления вариант ITAM3 (например, вариант, состоящий из двух мутаций с потерей функции) включает или состоит из аминокислотной последовательности, представленной в SEQ ID NO: 33, которая приведена ниже.
HDGLFQGLSTATKDTFDALHMQ [SEQ ID NO: 33]
Примерная последовательность нуклеиновой кислоты, кодирующая аминокислотную последовательность SEQ ID NO: 33, представлена в SEQ ID NO: 34, которая приведена ниже.
cacgatggcctttTccaggggctcagtacagccaccaaggacacctTcgacgcccttcacatgcag [SEQ ID NO: 34]
В некоторых вариантах осуществления внутриклеточный сигнальный домен CAR включает модифицированный полипептид CD3ζ, включающий вариант ITAM1, включающий или состоящий из одной или больше мутаций с потерей функции, варианта ITAM2, включающий или состоящий из одной или больше мутаций с потерей функции, и/или вариант ITAM3, включающий или состоящий из одной или больше мутаций с потерей функции, или их комбинацию.
В некоторых вариантах осуществления внутриклеточный сигнальный домен CAR включает модифицированный полипептид CD3ζ, включающий вариант ITAM2, включающий или состоящий из одной или больше (например, двух) мутаций с потерей функции, и вариант ITAM3, включающий или состоящий из одной или больше (например, двух) мутаций с потерей функции. В некоторых вариантах осуществления внутриклеточный сигнальный домен CAR включает модифицированный полипептид CD3ζ, включающий нативный ITAM1, вариант ITAM2, включающий или состоящий из двух мутаций с потерей функции, и вариант ITAM3, включающий или состоящий из двух мутаций с потерей функции. В некоторых вариантах осуществления внутриклеточный сигнальный домен CAR включает модифицированный полипептид CD3ζ, включающий нативный ITAM1, состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 23, вариант ITAM2, состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 29, и вариант ITAM3, состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 33 (например, в конструкции, обозначенной "1XX"). В некоторых вариантах осуществления модифицированный полипептид CD3ζ включает или состоит из аминокислотной последовательности, представленной в SEQ ID NO: 35.
В некоторых вариантах осуществления внутриклеточный сигнальный домен CAR включает модифицированный полипептид CD3ζ, включающий вариант ITAM1, включающий или состоящий из одной или больше (например, двух) мутаций с потерей функции, и вариант ITAM3, включающий или состоящий из одной или больше (например, двух) мутаций с потерей функции. В некоторых вариантах осуществления внутриклеточный сигнальный домен CAR включает модифицированный полипептид CD3ζ, включающий вариант ITAM1, включающий или состоящий из двух мутаций с потерей функции, нативный ITAM2 и варианта ITAM3, включающий или состоящий из двух мутаций с потерей функции. В некоторых вариантах осуществления внутриклеточный сигнальный домен CAR включает модифицированный полипептид CD3ζ, включающий вариант ITAM1, состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 25, нативный ITAM2, состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 27, и вариант ITAM3, состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 33 (например, в конструкции, обозначенной "X2X").
В некоторых вариантах осуществления внутриклеточный сигнальный домен CAR включает модифицированный полипептид CD3ζ, включающий вариант ITAM1, включающий или состоящий из одной или больше (например, двух) мутаций с потерей функции, и вариант ITAM2, включающий или состоящий из одной или больше (например, двух) мутаций с потерей функции. В некоторых вариантах осуществления внутриклеточный сигнальный домен CAR включает модифицированный полипептид CD3ζ, включающий или состоящий из варианта ITAM1, включающего две мутации с потерей функции, варианта ITAM2, включающего или состоящего из двух мутаций с потерей функции, и нативного ITAM3. В некоторых вариантах осуществления внутриклеточный сигнальный домен CAR включает модифицированный полипептид CD3ζ, включающий вариант ITAM1, состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 25, вариант ITAM2, состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 29, и нативный ITAM3, состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 31 (например, в конструкции, обозначенной "XX3").
В некоторых вариантах осуществления внутриклеточный сигнальный домен CAR включает модифицированный полипептид CD3ζ, включающий вариант ITAM1, включающий одну или больше (например, две) мутации с потерей функции. В некоторых вариантах осуществления внутриклеточный сигнальный домен CAR включает модифицированный полипептид CD3ζ, включающий вариант ITAM1, включающий или состоящий из двух мутаций с потерей функции, нативный ITAM2 и нативный ITAM3. В некоторых вариантах осуществления внутриклеточный сигнальный домен CAR включает модифицированный полипептид CD3ζ, включающий вариант ITAM1, состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 25, нативный ITAM2, состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 27, и нативный ITAM3, состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 31 (например, в конструкции, обозначенной "X23").
В некоторых вариантах осуществления внутриклеточный сигнальный домен CAR включает модифицированный полипептид CD3ζ, включающий нативный ITAM1, нативный ITAM2 и вариант ITAM3, включающий одну или больше (например, две) мутации с потерей функции. В некоторых вариантах осуществления внутриклеточный сигнальный домен CAR включает модифицированный полипептид CD3ζ, включающий нативный ITAM1, нативный ITAM2 и вариант ITAM1, включающий или состоящий из двух мутаций с потерей функции. В некоторых вариантах осуществления внутриклеточный сигнальный домен CAR включает модифицированный полипептид CD3ζ, включающий нативный ITAM1, состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 23, нативный ITAM2, состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 27, и вариант ITAM3, состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 33 (например, в конструкции, обозначенной "12X").
В некоторых вариантах осуществления внутриклеточный сигнальный домен CAR включает модифицированный полипептид CD3ζ, включающий нативный ITAM1, вариант ITAM2, включающий одну или больше (например, две) мутаций с потерей функции, и нативный ITAM3. В некоторых вариантах осуществления внутриклеточный сигнальный домен CAR включает модифицированный полипептид CD3ζ, включающий нативный ITAM1, вариант ITAM2, включающий или состоящий из двух мутаций с потерей функции, и нативный ITAM3. В некоторых вариантах осуществления внутриклеточный сигнальный домен CAR включает модифицированный полипептид CD3ζ, включающий нативный ITAM1, состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 23, вариант ITAM2, состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 29, и нативный вариант ITAM3, состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 31 (например, в конструкции, обозначенной "1X3").
В некоторых вариантах осуществления внутриклеточный сигнальный домен CAR включает модифицированный полипептид CD3ζ, включающий делецию одного или двух ITAM. В некоторых вариантах осуществления модифицированный полипептид CD3ζ включает или состоит из делеции ITAM1 и ITAM2, например, модифицированный полипептид CD3ζ включает нативный ITAM3 или вариант ITAM3, и не включает ITAM1 или ITAM2. В некоторых вариантах осуществления модифицированный полипептид CD3ζ включает нативный ITAM3, состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 31, и не включает ITAM1 (нативный или модифицированный) или ITAM2 (нативный или модифицированный) (например, в конструкции, обозначенной "D12").
В некоторых вариантах осуществления модифицированный полипептид CD3ζ включает или состоит из делеции ITAM2 и ITAM3, например, модифицированный полипептид CD3ζ включает нативный ITAM1 или вариант ITAM1, и не включает ITAM2 или ITAM3. В некоторых вариантах осуществления модифицированный полипептид CD3ζ включает нативный ITAM1, состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 23, и не включает ITAM2 (нативный или модифицированный) или ITAM3 (нативный или модифицированный) (например, в конструкции, обозначенной "D23").
В некоторых вариантах осуществления модифицированный полипептид CD3ζ включает или состоит из делеции ITAM1 и ITAM3, например, модифицированный полипептид CD3ζ включает нативный ITAM2 или вариант ITAM2, и не включает ITAM1 или ITAM3. В некоторых вариантах осуществления модифицированный полипептид CD3ζ включает нативный ITAM2, состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 27, и не включает ITAM1 (нативный или модифицированный) или ITAM3 (нативный или модифицированный) (например, в конструкции, обозначенной "D13").
В некоторых вариантах осуществления модифицированный полипептид CD3ζ включает или состоит из делеции ITAM1, например, модифицированный полипептид CD3ζ включает нативный ITAM2 или вариант ITAM2, и нативный ITAM3 или вариант ITAM3, и не включает ITAM1 (нативный или модифицированный).
В некоторых вариантах осуществления модифицированный полипептид CD3ζ включает или состоит из делеции ITAM2, например, модифицированный полипептид CD3ζ включает нативный ITAM1 или вариант ITAM1, и нативный ITAM3 или вариант ITAM3, и не включает ITAM2 (нативный или модифицированный).
В некоторых вариантах осуществления модифицированный полипептид CD3ζ включает или состоит из делеции ITAM3, например, модифицированный полипептид CD3ζ включает нативный ITAM1 или вариант ITAM1, и нативный ITAM2 или вариант ITAM2, и не включает ITAM3 (нативный или модифицированный).
B. Костимулирующая сигнальная область
В некоторых вариантах осуществления внутриклеточный сигнальный домен CAR дополнительно включает по меньшей мере костимулирующую сигнальную область. В некоторых вариантах осуществления костимулирующая сигнальная область включает по меньшей мере часть костимулирующей молекулы, которая может обеспечивать оптимальную активацию лимфоцитов.
При использовании в настоящем документе "костимулирующие молекулы" относятся к поверхностным молекулам клеток за исключением рецепторов антигенов или их лигандов, которые требуются для эффективного ответа лимфоцитов на антиген. Неограничивающие примеры костимулирующих молекул включают CD28, 4-1BB, OX40, ICOS, DAP-10, CD27, CD40 и NKGD2. Костимулирующая молекула может связываться с костимулирующим лигандом, который представляет собой белок, экспрессирующийся на поверхности клеток, который после связывания со своим рецептором производит костимулирующий ответ, т.е. внутриклеточный ответ, который вызывает стимуляцию, когда антиген связывается со своей молекулой CAR. Костимулирующие лиганды включают, без ограничения, CD80, CD86, CD70, OX40L и 4-1BBL. В качестве одного примера, лиганд 4-1BB (т.е. 4-1BBL) может связываться с 4-1BB (также известным как "CD137"), обеспечивая внутриклеточный сигнал, который в сочетании с сигналом CAR индуцирует эффекторную функцию CAR+ T-клетки. CAR-рецепторы, включающие внутриклеточный сигнальный домен, включающий костимулирующую сигнальную область, включающую 4-1BB, ICOS или DAP-10, раскрыты в U.S. 7,446,190, который включен в настоящий документ посредством отсылки во всей своей полноте.
В некоторых вариантах осуществления внутриклеточный сигнальный домен CAR включает костимулирующую сигнальную область, включающую полипептид CD28 (например, внутриклеточный домен CD28 или его часть). В некоторых вариантах осуществления костимулирующая сигнальная область включает внутриклеточный домен CD28 человека или его часть. В некоторых вариантах осуществления костимулирующая сигнальная область включает полипептид CD28, включающий или состоящий из аминокислот 180-220 из SEQ ID NO: 90.
В некоторых вариантах осуществления костимулирующая сигнальная область включает полипептид CD28, включающий или состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 101 (или аминокислоты 180-220 из SEQ ID NO: 90). SEQ ID NO: 101 приведена ниже.
RSKRSRLLHS DYMNMTPRRP GPTRKHYQPY APPRDFAAYR S [SEQ ID NO: 101]
Примерная нуклеотидная последовательность, кодирующая аминокислотную последовательность SEQ ID NO: 101 (или аминокислоты 180-220 из SEQ ID NO: 90), представлена в SEQ ID NO: 102, которая приведена ниже.
AGGAGTAAGAGGAGCAGGCTCCTGCACAGTGACTACATGAACATGACTCCCCGCCGCCCCGGGCCCACCCGCAAGCATTACCAGCCCTATGCCCCACCACGCGACTTCGCAGCCTATCGCTCC [SEQ ID NO: 102]
В некоторых вариантах осуществления костимулирующая сигнальная область включает полипептид CD28, включающий или состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 108 (или аминокислоты 180-219 из SEQ ID NO: 90). SEQ ID NO: 108 приведена ниже.
RSKRSRLLHS DYMNMTPRRP GPTRKHYQPY APPRDFAAYR K [SEQ ID NO: 108]
В некоторых вариантах осуществления костимулирующая сигнальная область включает внутриклеточный домен CD28 мыши или его часть. В некоторых вариантах осуществления костимулирующая сигнальная область включает или состоит из аминокислот 178-218 из SEQ ID NO: 97.
Примерная нуклеотидная последовательность, кодирующая аминокислоты 178-218 из SEQ ID NO: 97, представлена в SEQ ID NO: 98, которая приведена ниже.
aat agtagaagga acagactcct tcaaagtgac tacatgaaca tgactccccg gaggcctggg ctcactcgaa agccttacca gccctacgcc cctgccagag actttgcagc gtaccgcccc [SEQ ID NO: 98]
В некоторых вариантах осуществления костимулирующая сигнальная область включает или состоит из полипептида CD28, включающего или состоящего из аминокислотной последовательности, представленной в SEQ ID NO: 99. SEQ ID NO: 99 приведена ниже:
NSRRNRLLQS DYMNMTPRRP GLTRKPYQPY APARDFAAYR P [SEQ ID NO: 99].
Примерная последовательность нуклеиновой кислоты, кодирующая аминокислотную последовательность SEQ ID NO: 99, представлена в SEQ ID NO: 100, которая приведена ниже.
AATAGTAGAAGGAACAGACTCCTTCAAAGTGACTACATGAACATGACTCCCCGGAGGCCTGGGCTCACTCGAAAGCCTTACCAGCCCTACGCCCCTGCCAGAGACTTTGCAGCGTACCGCCCC [SEQ ID NO: 100]
В некоторых вариантах осуществления костимулирующая сигнальная область включает часть первой костимулирующей молекулы и часть второй костимулирующей молекулы, например, внутриклеточный домен CD28 и внутриклеточный домен 4-1BB или внутриклеточный домен CD28 и внутриклеточный домен OX40.
В некоторых вариантах осуществления костимулирующая сигнальная область включает полипептид 4-1BB (например, внутриклеточный домен 4-1BB или его часть). В некоторых вариантах осуществления костимулирующая сигнальная область включает внутриклеточный домен 4-1BB человека или его часть. 4-1BB может действовать в качестве лиганда фактора некроза опухоли (ФНО) и обладать стимулирующей активностью. В некоторых вариантах осуществления полипептид 4-1BB включает или состоит из аминокислотной последовательности, которая по меньшей мере приблизительно на 80%, по меньшей мере приблизительно на 85%, по меньшей мере приблизительно на 90%, по меньшей мере приблизительно на 95%, по меньшей мере приблизительно на 96%, по меньшей мере приблизительно на 97%, по меньшей мере приблизительно на 98%, по меньшей мере приблизительно на 99% или по меньшей мере приблизительно на 100% гомологична или идентична последовательности под номером NCBI: NP_001552.2 (SEQ ID NO: 103) или ее фрагменту, и/или необязательно может включать до одной или до двух, или до трех консервативных аминокислотных замен. В некоторых вариантах осуществления полипептид 4-1BB включает или состоит из аминокислотной последовательности, которая является непрерывной частью SEQ ID NO: 103, которая имеет длину по меньшей мере приблизительно 20, по меньшей мере приблизительно 25 или по меньшей мере приблизительно 30, или по меньшей мере приблизительно 40, или по меньшей мере приблизительно 50 и до приблизительно 255 аминокислот. В некоторых вариантах осуществления полипептид 4-1BB включает или состоит из аминокислотной последовательности аминокислот 1-255, 1-50, 50-100, 100-150, 150-200, 214-255 или 200-255 из SEQ ID NO: 103. В некоторых вариантах осуществления костимулирующая сигнальная область включает полипептид 4-1BB, включающий или состоящий из SEQ ID NO: 104 (или аминокислоты 214-255 из SEQ ID NO: 103). SEQ ID NO: 103 и 104 приведены ниже:
1 MGNSCYNIVA TLLLVLNFER TRSLQDPCSN CPAGTFCDNN RNQICSPCPP NSFSSAGGQR
61 TCDICRQCKG VFRTRKECSS TSNAECDCTP GFHCLGAGCS MCEQDCKQGQ ELTKKGCKDC
121 CFGTFNDQKR GICRPWTNCS LDGKSVLVNG TKERDVVCGP SPADLSPGAS SVTPPAPARE
181 PGHSPQIISF FLALTSTALL FLLFFLTLRF SVVKRGRKKL LYIFKQPFMR PVQTTQEEDG
241 CSCRFPEEEE GGCEL [SEQ ID NO: 103]
KRGRKKLLYI FKQPFMRPVQ TTQEEDGCSC RFPEEEEGGC EL [SEQ ID NO: 104].
Примерная нуклеотидная последовательность, кодирующая аминокислотную последовательность SEQ ID NO: 104 (или аминокислоты 214-255 из SEQ ID NO: 103), представлена в SEQ ID NO: 105, которая приведена ниже.
AAACGGGGCAGAAAGAAACTCCTGTATATATTCAAACAACCATTTATGAGACCAGTACAAACTACTCAAGAGGAAGATGGCTGTAGCTGCCGATTTCCAGAAGAAGAAGAAGGAGGATGTGAACTG [SEQ ID NO: 105]
В некоторых вариантах осуществления костимулирующая сигнальная область включает полипептид OX40 (например, внутриклеточный домен OX40 или его часть). В некоторых вариантах осуществления костимулирующая сигнальная область включает внутриклеточный домен человеческого OX40 или его часть. В некоторых вариантах осуществления полипептид OX40 включает или состоит из аминокислотной последовательности, которая по меньшей мере приблизительно на 80%, по меньшей мере приблизительно на 85%, по меньшей мере приблизительно на 90%, по меньшей мере приблизительно на 95%, по меньшей мере приблизительно на 96%, по меньшей мере приблизительно на 97%, по меньшей мере приблизительно на 98%, по меньшей мере приблизительно на 99% или по меньшей мере приблизительно на 100% гомологична или идентична последовательности под номером NCBI: NP_003318.1 (SEQ ID NO: 106) или ее фрагменту, и/или необязательно может включать до одной или до двух, или до трех консервативных аминокислотных замен. В некоторых вариантах осуществления полипептид OX40 включает или состоит из аминокислотной последовательности, которая является непрерывной частью SEQ ID NO: 106, которая имеет длину по меньшей мере приблизительно 20, по меньшей мере приблизительно 25 или по меньшей мере приблизительно 30, или по меньшей мере приблизительно 40, или по меньшей мере приблизительно 50 и до приблизительно 277 аминокислот. В некоторых вариантах осуществления полипептид OX40 включает или состоит из аминокислотной последовательности аминокислот 1-277, 1-50, 50-100, 100-150, 150-200 или 200-277 из SEQ ID NO: 106. SEQ ID NO: 106 приведена ниже.
1 MCVGARRLGR GPCAALLLLG LGLSTVTGLH CVGDTYPSND RCCHECRPGN GMVSRCSRSQ
61 NTVCRPCGPG FYNDVVSSKP CKPCTWCNLR SGSERKQLCT ATQDTVCRCR AGTQPLDSYK
121 PGVDCAPCPP GHFSPGDNQA CKPWTNCTLA GKHTLQPASN SSDAICEDRD PPATQPQETQ
181 GPPARPITVQ PTEAWPRTSQ GPSTRPVEVP GGRAVAAILG LGLVLGLLGP LAILLALYLL
241 RRDQRLPPDA HKPPGGGSFR TPIQEEQADA HSTLAKI [SEQ ID NO: 106]
В некоторых вариантах осуществления костимулирующая сигнальная область включает полипептид ICOS (например, внутриклеточный домен ICOS или его часть). В некоторых вариантах осуществления костимулирующая сигнальная область включает внутриклеточный домен ICOS человека или его часть. В некоторых вариантах осуществления полипептид ICOS включает или состоит из аминокислотной последовательности, которая по меньшей мере приблизительно на 80%, по меньшей мере приблизительно на 85%, по меньшей мере приблизительно на 90%, по меньшей мере приблизительно на 95%, по меньшей мере приблизительно на 96%, по меньшей мере приблизительно на 97%, по меньшей мере приблизительно на 98%, по меньшей мере приблизительно на 99% или по меньшей мере приблизительно на 100% гомологична или идентична последовательности под номером NCBI: NP_036224 (SEQ ID NO: 65) или ее фрагменту, и/или необязательно может включать до одной или до двух, или до трех консервативных аминокислотных замен. В некоторых вариантах осуществления полипептид ICOS включает или состоит из аминокислотной последовательности, которая является непрерывной частью SEQ ID NO: 65, которая имеет длину по меньшей мере приблизительно 20, по меньшей мере приблизительно 25 или по меньшей мере приблизительно 30, или по меньшей мере приблизительно 40, или по меньшей мере приблизительно 50 и до приблизительно 199 аминокислот. В некоторых вариантах осуществления полипептид ICOS включает или состоит из аминокислотной последовательности аминокислот 1-199, 1-50, 50-100, 100-150 или 150-199 из SEQ ID NO: 65. SEQ ID NO: 65 приведена ниже.
1 MKSGLWYFFL FCLRIKVLTG EINGSANYEM FIFHNGGVQI LCKYPDIVQQ FKMQLLKGGQ
61 ILCDLTKTKG SGNTVSIKSL KFCHSQLSNN SVSFFLYNLD HSHANYYFCN LSIFDPPPFK
121 VTLTGGYLHI YESQLCCQLK FWLPIGCAAF VVVCILGCIL ICWLTKKKYS SSVHDPNGEY
181 MFMRAVNTAK KSRLTDVTL [SEQ ID NO: 65]
В некоторых вариантах осуществления раскрытый в настоящем документе мезотелин-направленный CAR дополнительно включает индуцируемый промотор для экспрессии последовательностей нуклеиновых кислот в клетках человека. Промоторы для применения в экспрессии генов CAR могут быть конститутивным промотором, таким как промотор убиквитина C (UbiC).
В некоторых вариантах осуществления сайты мутации и/или соединение между доменами/мотивами/областями CAR, полученного из разных белков, являются деиммунизированными. Иммуногенность соединений между разными фрагментами CAR может быть предсказана с помощью сервера NetMHC 4.0. Для каждого пептида, содержащего по меньшей мере одну аминокислоту из следующего фрагмента, может быть предсказана аффинность связывания с HLA A, B и C, для всех аллелей. Индекс иммуногенности каждого пептида может быть установлен для каждого пептида. Индекс иммуногенности может быть вычислен при использовании следующей формулы: Индекс иммуногенности=[(50-аффинность связывания)*частота HLA]n. n является числом прогноза для каждого пептида.
5.2.2.5. Иллюстративные CAR-рецепторы
В некоторых вариантах осуществления мезотелин-направленный CAR включает:
(a) внеклеточный антигенсвязывающий домен, включающий VH, включающую CDR1, состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 76, CDR2, состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 77, и CDR3, состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 78; и VL, включающую CDR1, состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 79, CDR2, состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 80, и CDR3, состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 81;
(b) трансмембранный домен, включающий полипептид CD28 (например, трансмембранный домен CD28 человека или его часть);
(c) шарнирную/спейсерную область CD28 (например, шарнирную/спейсерную область CD28 человека или его часть); и
(d) внутриклеточный сигнальный домен, включающий: (i) модифицированный полипептид CD3ζ (например, модифицированный человеческий полипептид CD3ζ), включающий нативный ITAM1, вариант ITAM2, состоящий из двух мутаций с потерей функции, и вариант ITAM3, состоящий из двух мутаций с потерей функции, и (ii) костимулирующую сигнальную область, включающую полипептид CD28 (например, человеческий полипептид CD28, например, внутриклеточный домен CD28 человека или его часть).
В некоторых вариантах осуществления трансмембранный домен включает полипептид CD28, состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 92 (или аминокислоты 153-179 из SEQ ID NO: 90).
В некоторых вариантах осуществления шарнирная/спейсерная область CD28 состоит из аминокислотной последовательности, представленной в SEQ ID NO: 15 (или аминокислот 114-152 из SEQ ID NO: 90).
В некоторых вариантах осуществления модифицированный CD3ζ полипептид состоит из аминокислотной последовательности, представленной в SEQ ID NO: 35.
В некоторых вариантах осуществления костимулирующая сигнальная область включает полипептид CD28, состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 101 (или аминокислот 180-220 из SEQ ID NO: 90).
В некоторых вариантах осуществления CAR включает аминокислотную последовательность, которая по меньшей мере приблизительно на 80%, по меньшей мере приблизительно на 85%, по меньшей мере приблизительно на 90%, по меньшей мере приблизительно на 95%, по меньшей мере приблизительно на 96%, по меньшей мере приблизительно на 97%, по меньшей мере приблизительно на 98%, по меньшей мере приблизительно на 99% или по меньшей мере приблизительно на 100% гомологична или идентична аминокислотной последовательности, представленной в SEQ ID NO: 56. В некоторых вариантах осуществления CAR включает аминокислотную последовательность, представленную в SEQ ID NO: 56. SEQ ID NO: 56 приведена ниже.
QVQLQESGPGLVKPSETLSLTCTVSGGSVSSGSYYWSWIRQPPGKGLEWIGYIYYSGSTNYNPSLKSRVTISVDTSKNQFSLKLSSVTAADTAVYYCAREGKNGAFDIWGQGTMVTVSSGGGGSGGGGSGGGGSRHQMTQSPSSLSASVGDRVTITCRASQSISSYLNWYQQKPGKAPKLLIYAASSLQSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQSYSTPLTFGGGTKVEIKRTAAAIEVMYPPPYLDNEKSNGTIIHVKGKHLCPSPLFPGPSKPFWVLVVVGGVLACYSLLVTVAFIIFWVRSKRSRLLHSDYMNMTPRRPGPTRKHYQPYAPPRDFAAYRSRVKFSRSADAPAYQQGQNQLYNELNLGRREEYDVLDKRRGRDPEMGGKPRRKNPQEGLFNELQKDKMAEAFSEIGMKGERRRGKGHDGLFQGLSTATKDTFDALHMQALPPR [SEQ ID NO: 56]
Примерная нуклеотидная последовательность, кодирующая аминокислотную последовательность SEQ ID NO: 56, представлена в SEQ ID NO: 57, которая приведена ниже.
CAGGTTCAGCTTCAGGAGAGTGGCCCAGGCCTGGTGAAGCCAAGTGAGACTCTCAGCTTGACTTGCACAGTTTCTGGAGGCAGTGTCTCCTCAGGCAGCTATTATTGGTCCTGGATTCGGCAGCCCCCTGGGAAAGGCCTGGAGTGGATTGGGTACATATATTACAGTGGCAGCACAAATTACAATCCATCCCTGAAGTCTCGAGTAACTATCAGTGTGGACACAAGCAAGAATCAGTTTTCACTCAAACTGTCTTCTGTGACTGCTGCTGACACTGCTGTTTATTATTGTGCCAGGGAGGGGAAAAATGGGGCATTTGATATTTGGGGTCAGGGCACAATGGTGACAGTCAGCTCTGGAGGTGGAGGCTCAGGAGGAGGAGGCAGTGGAGGTGGTGGGTCACGCCATCAGATGACTCAGTCCCCCTCCAGTCTTTCTGCCTCAGTTGGGGATAGAGTGACCATCACATGCAGAGCAAGTCAGAGCATATCATCCTATCTGAACTGGTACCAGCAGAAGCCAGGGAAAGCCCCCAAATTGCTGATTTATGCAGCCTCAAGTCTCCAGAGTGGGGTGCCAAGCAGGTTCTCAGGCAGTGGCAGTGGGACAGATTTCACATTGACAATCAGCTCCCTCCAACCTGAAGATTTTGCCACCTACTATTGCCAGCAATCCTACAGCACGCCCCTGACTTTTGGAGGTGGCACAAAGGTAGAGATCAAGAGGACTGCGGCCGCAATTGAAGTTATGTATCCTCCTCCTTACCTAGACAATGAGAAGAGCAATGGAACCATTATCCATGTGAAAGGGAAACACCTTTGTCCAAGTCCCCTATTTCCCGGACCTTCTAAGCCCTTTTGGGTGCTGGTGGTGGTTGGTGGAGTCCTGGCTTGCTATAGCTTGCTAGTAACAGTGGCCTTTATTATTTTCTGGGTGAGGAGTAAGAGGAGCAGGCTCCTGCACAGTGACTACATGAACATGACTCCCCGCCGCCCCGGGCCCACCCGCAAGCATTACCAGCCCTATGCCCCACCACGCGACTTCGCAGCCTATCGCTCCAGAGTGAAGTTCAGCAGGAGCGCAGACGCCCCCGCGTACCAGCAGGGCCAGAACCAGCTCTATAACGAGCTCAATCTAGGACGAAGAGAGGAGTACGATGTTTTGGACAAGAGACGTGGCCGGGACCCTGAGATGGGGGGAAAGCCGAGAAGGAAGAACCCTCAGGAAGGCCTGTTCAATGAACTGCAGAAAGATAAGATGGCGGAGGCCTTCAGTGAGATTGGGATGAAAGGCGAGCGCCGGAGGGGCAAGGGGCACGATGGCCTTTTCCAGGGGCTCAGTACAGCCACCAAGGACACCTTCGACGCCCTTCACATGCAGGCCCTGCCCCCTCGC [SEQ ID NO: 57]
В некоторых вариантах осуществления CAR дополнительно включает лидерную последовательность CD8. В некоторых вариантах осуществления лидерная последовательность CD8 включает или состоит из аминокислотной последовательности, представленной в SEQ ID NO: 71.
Примерная нуклеотидная последовательность, кодирующая аминокислотную последовательность SEQ ID NO: 71, представлена в SEQ ID NO: 120, которая приведена ниже.
ATGGCCCTGCCAGTAACGGCTCTGCTGCTGCCACTTGCTCTGCTCCTCCATGCAGCCAGGCCT [SEQ ID NO: 120]
В некоторых вариантах осуществления CAR включает аминокислотную последовательность, которая по меньшей мере приблизительно на 80%, по меньшей мере приблизительно на 85%, по меньшей мере приблизительно на 90%, по меньшей мере приблизительно на 95%, по меньшей мере приблизительно на 96%, по меньшей мере приблизительно на 97%, по меньшей мере приблизительно на 98%, по меньшей мере приблизительно на 99% или по меньшей мере приблизительно на 100% гомологична или идентична аминокислотной последовательности, представленной в SEQ ID NO: 43, которая приведена ниже. В некоторых вариантах осуществления CAR включает или состоит из аминокислотной последовательности, представленной в SEQ ID NO: 43. SEQ ID NO: 43 включает лидерную последовательность CD8, которая состоит из аминокислотной последовательности, представленной в SEQ ID NO: 71. SEQ ID NO: 43 приведена ниже:
MALPVTALLLPLALLLHAARPQVQLQESGPGLVKPSETLSLTCTVSGGSVSSGSYYWSWI
RQPPGKGLEWIGYIYYSGSTNYNPSLKSRVTISVDTSKNQFSLKLSSVTAADTAVYYCAR
EGKNGAFDIWGQGTMVTVSSGGGGSGGGGSGGGGSRHQMTQSPSSLSASVGDRVTITCRA
SQSISSYLNWYQQKPGKAPKLLIYAASSLQSGVPSRFSGSGSGTDFTLTISSLQPEDFAT
YYCQQSYSTPLTFGGGTKVEIKRTAAAIEVMYPPPYLDNEKSNGTIIHVKGKHLCPSPLF
PGPSKPFWVLVVVGGVLACYSLLVTVAFIIFWVRSKRSRLLHSDYMNMTPRRPGPTRKHY
QPYAPPRDFAAYRSRVKFSRSADAPAYQQGQNQLYNELNLGRREEYDVLDKRRGRDPEMG
GKPRRKNPQEGLFNELQKDKMAEAFSEIGMKGERRRGKGHDGLFQGLSTATKDTFDALHM
QALPPR [SEQ ID NO: 43]
Примерная нуклеотидная последовательность, кодирующая аминокислотную последовательность SEQ ID NO: 43, представлена в SEQ ID NO: 44, которая приведена ниже.
ATGGCCCTGCCAGTAACGGCTCTGCTGCTGCCACTTGCTCTGCTCCTCCATGCAGCCAGGCCTCAGGTTCAGCTTCAGGAGAGTGGCCCAGGCCTGGTGAAGCCAAGTGAGACTCTCAGCTTGACTTGCACAGTTTCTGGAGGCAGTGTCTCCTCAGGCAGCTATTATTGGTCCTGGATTCGGCAGCCCCCTGGGAAAGGCCTGGAGTGGATTGGGTACATATATTACAGTGGCAGCACAAATTACAATCCATCCCTGAAGTCTCGAGTAACTATCAGTGTGGACACAAGCAAGAATCAGTTTTCACTCAAACTGTCTTCTGTGACTGCTGCTGACACTGCTGTTTATTATTGTGCCAGGGAGGGGAAAAATGGGGCATTTGATATTTGGGGTCAGGGCACAATGGTGACAGTCAGCTCTGGAGGTGGAGGCTCAGGAGGAGGAGGCAGTGGAGGTGGTGGGTCACGCCATCAGATGACTCAGTCCCCCTCCAGTCTTTCTGCCTCAGTTGGGGATAGAGTGACCATCACATGCAGAGCAAGTCAGAGCATATCATCCTATCTGAACTGGTACCAGCAGAAGCCAGGGAAAGCCCCCAAATTGCTGATTTATGCAGCCTCAAGTCTCCAGAGTGGGGTGCCAAGCAGGTTCTCAGGCAGTGGCAGTGGGACAGATTTCACATTGACAATCAGCTCCCTCCAACCTGAAGATTTTGCCACCTACTATTGCCAGCAATCCTACAGCACGCCCCTGACTTTTGGAGGTGGCACAAAGGTAGAGATCAAGAGGACTGCGGCCGCAATTGAAGTTATGTATCCTCCTCCTTACCTAGACAATGAGAAGAGCAATGGAACCATTATCCATGTGAAAGGGAAACACCTTTGTCCAAGTCCCCTATTTCCCGGACCTTCTAAGCCCTTTTGGGTGCTGGTGGTGGTTGGTGGAGTCCTGGCTTGCTATAGCTTGCTAGTAACAGTGGCCTTTATTATTTTCTGGGTGAGGAGTAAGAGGAGCAGGCTCCTGCACAGTGACTACATGAACATGACTCCCCGCCGCCCCGGGCCCACCCGCAAGCATTACCAGCCCTATGCCCCACCACGCGACTTCGCAGCCTATCGCTCCAGAGTGAAGTTCAGCAGGAGCGCAGACGCCCCCGCGTACCAGCAGGGCCAGAACCAGCTCTATAACGAGCTCAATCTAGGACGAAGAGAGGAGTACGATGTTTTGGACAAGAGACGTGGCCGGGACCCTGAGATGGGGGGAAAGCCGAGAAGGAAGAACCCTCAGGAAGGCCTGTTCAATGAACTGCAGAAAGATAAGATGGCGGAGGCCTTCAGTGAGATTGGGATGAAAGGCGAGCGCCGGAGGGGCAAGGGGCACGATGGCCTTTTCCAGGGGCTCAGTACAGCCACCAAGGACACCTTCGACGCCCTTCACATGCAGGCCCTGCCCCCTCGC [SEQ ID NO: 44]
5.2.3. Иллюстративные полипептидные композиции
В некоторых вариантах осуществления полипептидная композиция включает мезотелин-направленный CAR, включающий или состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 56, и PD-1 DN, включающий или состоящий из аминокислот 21-165 из SEQ ID NO: 48.
В некоторых вариантах осуществления полипептидная композиция включает мезотелин-направленный CAR, включающий или состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 56, и PD-1 DN, включающий или состоящий из аминокислот 1-165 из SEQ ID NO: 48.
В некоторых вариантах осуществления полипептидная композиция включает мезотелин-направленный CAR, включающий или состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 56, и PD-1 DN, включающий или состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 49.
В некоторых вариантах осуществления полипептидная композиция включает мезотелин-направленный CAR, включающий или состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 56, и PD-1 DN, включающий или состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 118.
В некоторых вариантах осуществления полипептидная композиция включает мезотелин-направленный CAR, включающий или состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 56, и лидерную последовательность CD8, включающую или состоящую из аминокислотной последовательности, представленной в SEQ ID NO: 71, и PD-1 DN, включающий или состоящий из аминокислот 21-165 из SEQ ID NO: 48.
В некоторых вариантах осуществления полипептидная композиция включает мезотелин-направленный CAR, включающий или состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 56, и лидерную последовательность CD8, включающую или состоящую из аминокислотной последовательности, представленной в SEQ ID NO: 71, и PD-1 DN, включающий или состоящий из аминокислот 1-165 из SEQ ID NO: 48.
В некоторых вариантах осуществления полипептидная композиция включает мезотелин-направленный CAR, включающий или состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 56, и лидерную последовательность CD8, включающую или состоящую из аминокислотной последовательности, представленной в SEQ ID NO: 71, и PD-1 DN, включающий или состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 49.
В некоторых вариантах осуществления полипептидная композиция включает мезотелин-направленный CAR, включающий или состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 56, и лидерную последовательность CD8, включающую или состоящую из аминокислотной последовательности, представленной в SEQ ID NO: 71, и PD-1 DN, включающий или состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 118.
5.3. Иммунореактивные клетки
В настоящем изобретении обеспечивает иммунореактивные клетки, включающие полипептидную композицию, раскрытую в настоящем документе. В некоторых вариантах осуществления CAR способен активировать иммунореактивную клетку. В некоторых вариантах осуществления полипептидная композиция способна стимулировать противоопухолевый эффект иммунореактивной клетки. Иммунореактивные клетки могут быть трансдуцированы полипептидной композицией, при этом такие клетки будут коэкспрессировать CAR и PD-1 DN.
Иммунореактивные клетки раскрытого в настоящем документе изобретения могут быть клетками лимфоидной линии дифференцировки. Лимфоидная линия дифференцировки, включающая B, T и естественный киллерные (NK) клетки, обеспечивает продукцию антител, регуляцию клеточной иммунной системы, обнаружение чужеродных агентов в крови, обнаружение клеток, чужеродных для хозяина, и т.п. Неограничивающие примеры иммунореактивных клеток лимфоидной линии дифференцировки включают T-клетки, естественные киллерные (NK) клетки, эмбриональные стволовые клетки и плюрипотентные стволовые клетки (например, клетки, из которых могут дифференцироваться лимфоидные клетки). T-клетки могут быть лимфоцитами, которые созревают в тимусе, и в основном отвечают за клеточный иммунитет. T-клетки входят в адаптивную иммунную систему. T-клетки раскрытого в настоящем документе изобретения могут представлять собой T-клетки любого типа, в том числе, без ограничения перечисленными, Т-хелперы, цитотоксические T-клетки, T-клетки памяти (включая T-клетки центральной памяти, подобные стволовым клеткам T-клетки памяти (или подобные стволовым T-клетки памяти), и два типа T-клеток эффекторной памяти: например, клетки TEM и клетки TEMRA, регуляторные T-клетки (также известный как супрессорные T-клетки), естественные киллерные T-клетки, ассоциированные со слизистой оболочкой инвариантные T-клетки и γδ T-клетки. Цитотоксические T-клетки (CTL или киллерные T-клетки) представляют собой субпопуляцию T-лимфоцитов, способных вызывать гибель инфицированных соматических или опухолевых клеток. Собственные T-клетки пациента могут быть генетически модифицированы для направленного взаимодействия со специфическими антигенами посредством введения антигенраспознающего рецептора, например, CAR или TCR. В некоторых вариантах осуществления иммунореактивной клеткой является T-клетка. T-клетка может быть CD4+ T-клеткой или CD8+ T-клеткой. В некоторых вариантах осуществления T-клетка является CD4+ T-клеткой. В некоторых вариантах осуществления T-клетка является CD8+ T-клеткой.
Естественные киллерные (NK) клетки могут быть лимфоцитами, которые являются частью клеточного иммунитета и участвуют во врожденном иммунном ответе. NK-клетки не требуют предшествующей активации для проявления своего цитотоксического эффекта в отношении клеток-мишеней.
Типы лимфоцитов человека согласно раскрытому в настоящем документе изобретению включают, без ограничения, периферические донорские лимфоциты, например, раскрытые в публикации Sadelain, M., et al. 2003 Nat Rev Cancer 3: 35-45 (в которой раскрыты периферические донорские лимфоциты, генетически модифицированные для экспрессии CAR-рецепторов), в публикации Morgan, R.A., et al. 2006 Science 314: 126-129 (в которой раскрыты периферические донорские лимфоциты, генетически модифицированные для экспрессии T-клеточного рецепторного комплекса, распознающего полноразмерные опухолевые антигены и включающего α и β гетеродимер), в публикациях Panelli, M.C., et al. 2000 J Immunol 164: 495-504; Panelli, M.C., et al. 2000 J Immunol 164: 4382-4392 (в которых раскрыты культуры лимфоцитов, полученных из инфильтрирующих опухоль лимфоцитов (TIL) в образцах биопсии опухолей), и в публикациях Dupont, J., et al. 2005 Cancer Res 65: 5417-5427; Papanicolaou, G.A., et al. 2003 Blood 102: 2498-2505 (в которых раскрыты антигенспецифичные лейкоциты периферической крови, селективно размноженные in vitro при использовании искусственных антигенпрезентирующих клеток (иАПК) или активированных дендритных клеток). Иммунореактивные клетки (например, T-клетки) могут быть аутологичными, неаутологичными (например, аллогенными) или могут быть получены in vitro из модифицированных прогениторных или стволовых клеток.
В некоторых вариантах осуществления раскрытая в настоящем документе иммунореактивная клетка включает мезотелин-направленный CAR, включающий или состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 56, и PD-1 DN, включающий или состоящий из аминокислот 1-165 из SEQ ID NO: 48.
В некоторых вариантах осуществления раскрытые в настоящем документе иммунореактивные клетки, включающие один или больше полипептидов CAR и/или PD-1/DN согласно раскрытому в настоящем документе изобретению, являются аллогенными или аутологичными ВЭБ-сенсибилизированными цитотоксическими T-лимфоцитами (CTL). Например, получение ВЭБ-чувствительных цитотоксических T-клеток может включать выделение МКПК у ВЭБ-серопозитивного аутологичного или аллогеннного донора и их обогащения T-клетками путем элиминирования моноцитов и NK-клеток. ВЭБ-сенсибилизированные цитотоксические T-клетки также могут быть получены при контакте донорских МКПК или очищенных донорских T-клеток с клетками "стимуляторами", которые экспрессируют один или более антигенов ВЭБ и презентируют антиген(ы) ВЭБ нестимулированным T-клеткам, вызывая в результате стимуляцию и экспансию ВЭБ-сенсибилизированных CTL. В частности, в некоторых вариантах осуществления такие способы включают получение образца клеток (например, МКПК) у субъекта, включающих CD3+ клетки, и контакт указанных CD3+ клеток с антигеном и/или антиген-презентирующими стимулирующими клетками. В некоторых вариантах осуществления CD3+ T-клетки выделяют из образца до контакта с антигеном при использовании способа, известного в данной области (например, позитивного отбора CD3+ клеток из образца и/или негативного отбора путем элиминирования нежелательных клеток или компонентов из образца). В некоторых вариантах осуществления такие способы включают отбор с помощью сортировки клеток с активированной флуоресценцией (FACS), с использованием гранул против CD3 (например, магнитных гранул), адгезии к пластику, элиминирования NK-клеток с использованием антител против CD56, элютриации и/или комбинаций этого. Антигены ВЭБ включают, например, латентный мембранный белок (LMP) и белки ядерных антигенов ВЭБ (EBNA), такие как LMP-1, LMP-2A и LMP-2B, и EBNA-1, EBNA-2, EBNA-3A, EBNA-3B, EBNA-3C и EBNA-LP. Цитотоксические T-клетки, которые включают T-клеточный рецептор(ы), которые распознают один или больше ВЭБ-специфических антигенов, считаются "сенсибилизированными" таким антигеном(ами) ВЭБ и поэтому называются в настоящем документе "ВЭБ-сенсибилизированными цитотоксическими T-клетками". Известные способы создания популяций аллогенных или аутологичных ВЭБ-специфичных цитотоксических T-клеток, которые могут включать один или больше раскрытых в настоящем документе полипептидов CAR, описаны, например, в публикациях Barker et al., Blood 116(23): 5045-49 (2010); Doubrovina et al., Blood 119(11): 2644-56 (2012); Koehne et al., Blood 99(5): 1730-40 (2002); и Smith et al., Cancer Res. 72(5): 1116-25 (2012), которые включены в настоящее описание посредством отсылок. Аналогичным образом, цитотоксические T-клетки можно "сенсибилизировать" к другим вирусным антигенам, включая цитомегаловирус (ЦМВ), папилломавирус (например, ВПЧ), аденовирус, полиомавирус (например, BKV, JCV и вирус клеток Меркеля), ретровирус (например, HTLV-I, также включая лентивирус, такой как ВИЧ), пикорнавирус (например, вирус гепатита А), гепаднавирус (например, вирус гепатита B), гепацивирус (например, вирус гепатита С), дельтавирус (например, вирус гепатита D), гепевирус (например, вирус гепатита E) и т.п. В некоторых вариантах осуществления антиген-мишень происходит из онковируса. В некоторых вариантах осуществления T-клетки, используемые для создания раскрытых в настоящем документе CAR-T-клеток, являются полифункциональными T-клетками, например, такими T-клетками, которые способны индуцировать множество функций иммунных эффекторов, что обеспечивает более эффективный иммунный ответ против патогена, чем у клеток, которые продуцируют, например, только один иммунный эффектор (например, один биомаркер, такой как цитокин или CD107a). Менее полифункциональные, монофункциональные или даже "истощенные" T-клетки могут доминировать в иммунных ответах во время хронических инфекций, оказывая тем самым отрицательное влияние на защиту от вирус-ассоциированных осложнений. В некоторых вариантах осуществления раскрытые в настоящем документе CAR-T-клетки являются полифункциональными. В некоторых вариантах осуществления по меньшей мере около 50% T-клеток, используемых для создания раскрытых в настоящем документе CAR-T-клеток, являются CD4+ T-клетками. В некоторых таких вариантах осуществления T-клетки меньше чем приблизительно на 50% являются CD4+ T-клетками. В некоторых вариантах осуществления T-клетки преимущественно являются CD4+ T-клетками.
В некоторых вариантах осуществления по меньшей мере приблизительно 50% T-клеток, используемых для создания раскрытых в настоящем документе CAR-T-клеток, являются CD8+ T-клетками. В некоторых таких вариантах осуществления T-клетки меньше чем приблизительно на 50% являются CD8+ T-клетками. В некоторых вариантах осуществления T-клетки преимущественно являются CD8+ T-клетками. В некоторых вариантах осуществления T-клетки (например, сенсибилизированные T-клетки и/или CAR-T-клетки, описанные в настоящем документе) хранятся в клеточной библиотеке или банке до введения субъекту.
Раскрытая в настоящем документе иммунореактивная клетка может дополнительно включать по меньшей мере один экзогенный костимулирующий лиганд, при этом иммунореактивная клетка коэкспрессирует или в ней индуцирована коэкспрессия мезотелин-специфичного CAR и по меньшей мере одного экзогенного костимулирующего лиганда. Взаимодействие между мезотелин-специфичным CAR и по меньшей мере одним костимулирующим лигандом предоставляет неантигенспецифичный сигнал, важный для полной активации иммунореактивной клетки (например, T-клетки). Костимулирующие лиганды включают, без ограничения, представителей суперсемейства фактора некроза опухоли (ФНО) и лиганды суперсемейства иммуноглобулинов (Ig). ФНО представляет собой цитокин, участвующий в системном воспалении, и который стимулирует ответ острой фазы. Его основная роль заключается в регуляции иммунных клеток. Члены суперсемейства ФНО обладают рядом общих признаков. Большинство представителей суперсемейства ФНО синтезируется в виде трансмембранных белков II типа (с внеклеточным C-концом), содержащих короткий цитоплазматический сегмент и относительно длинную внеклеточную область. Представители суперсемейства ФНО включают, без ограничения перечисленными, фактор роста нервов (NGF), CD40L (CD40L)/CD154, CD137L/4-1BBL, ФНО-α, CD134L/OX40L/CD252, CD27L/CD70, лиганд Fas (FasL), CD30L/CD153, фактора некроза опухоли бета (ФНОβ)/лимфотоксин-альфа (LTα), лимфотоксин-бета (LTβ), CD257/фактор активации B-клеток (BAFF)/Blys/THANK/Tall-1, лиганд глюкокортикоид-индуцируемого рецептора ФНО (GITRL) и ФНО-родственный апоптоз-индуцирующий лиганд (TRAIL), LIGHT (TNFSF14). Суперсемейство иммуноглобулинов (Ig) является многочисленной группой поверхностных и растворимых клеточных белков, которые участвуют в процессах распознавания, связывания или адгезии клеток. Эти белки обладают сходными структурными особенностями с иммуноглобулинами - они содержат иммуноглобулиновый домен (сгиб). Лиганды суперсемейства иммуноглобулинов включают, без ограничения перечисленными, CD80 и CD86, оба лиганда CD28, PD-L1/(B7-H1), которые являются лигандами PD-1.
В некоторых вариантах осуществления по меньшей мере один костимулирующий лиганд выбран из группы, состоящей из 4-1BBL, CD80, CD86, CD70, OX40L, CD48, TNFRSF14, PD-L1 и их комбинаций. В некоторых вариантах осуществления костимулирующим лигандом является 4-1BBL. 4-1BBL может быть ковалентно соединен с 5'-концом внеклеточного антигенсвязывающего домена мезотелин-направленного CAR. В альтернативе 4-1BBL может быть ковалентно соединен с 3'-концом внутриклеточного сигнального домена мезотелин-направленного CAR.
Кроме того, раскрытая в настоящем документе иммунореактивная клетка может дополнительно включать по меньшей мере один экзогенный цитокин, при этом иммунореактивная клетка коэкспрессирует или в ней индуцирована коэкспрессия мезотелин-специфичного CAR и по меньшей мере одного экзогенного цитокина. В некоторых вариантах осуществления по меньшей мере один экзогенный цитокин выбран из группы, состоящей из IL-2, IL-3, IL-6, IL-7, IL-11, IL-12, IL-15, IL-17 и IL-21. В некоторых вариантах осуществления по меньшей мере один экзогенный цитокин включает IL-12. В некоторых вариантах осуществления иммунореактивная клетка коэкспрессирует мезотелин-направленный CAR и экзогенный IL-12. IL-12 может быть ковалентно соединен с 3'-концом внутриклеточного сигнального домена мезотелин-направленного CAR.
Кроме того, иммунореактивные клетки могут экспрессировать второй CAR, который связывается со вторым антигеном, который является мезотелином, или антигеном, отличным от мезотелина. CAR-рецепторы, которые могут применяться в качестве второго CAR в комбинации с мезотелин-специфичным CAR в раскрытом в настоящем документе изобретении, включают CAR-рецепторы, описанные в публикации Sadelain, et al., "The Basic Principles of Chimeric Antigen Receptor Design". Cancer Discovery, OF1-11, (2013), Chicaybam, et al., (2011), Brentjens et al. Nature Medicine 9: 279-286 (2003), и U.S. 7,446,190, которые включены в настоящий документ посредством отсылок во всей своей полноте, например, CD19-направленные CAR-рецепторы (см. U.S. 7,446,190; U.S. 2013/0071414), HER2-направленные CAR-рецепторы (см. Ahmed, et al., Clin Cancer Res., 2010), MUC16-направленные CAR-рецепторы (см. Chekmasova, et al., 2011), простат-специфический мембранный антиген (ПСМА)-направленные CAR-рецепторы (например, Zhong, et al., Molecular Therapy, 18(2): 413-420 (2010), которые включены в настоящий документ посредством отсылок во всей своей полноте. Иммунореактивные клетки, экспрессирующие два или больше антиген-распознающих рецепторов (например, CAR-рецепторов), описаны в заявке WO 2014/055668, которая полностью включена в настоящий документ посредством отсылки.
Второй антиген может быть опухолевым антигеном или антигеном патогена. Любой подходящий опухолевый антиген (антигенный пептид) подходит для применения в связанных с опухолью вариантах осуществления, описанных в настоящем документе. Источники опухолевого антигена включают, без ограничения, раковые белки. Второй антиген может экспрессироваться в виде пептида или интактного белка или его части. Интактный белок или его часть могут быть нативными или мутантными. Подходящие вторые антигены включают, без ограничения, простат-специфический мембранный антиген (ПСМА) и антиген стволовых клеток простаты (PCSA). В некоторых вариантах осуществления опухолевым антигеном может быть карбоангидраза IX (CAIX), раковоэмбриональный антиген (РЭА), CD5, CD7, CD10, CD19, CD20, CD22, CD30, CD33, CD34, CD38, CD41, CD44, CD49f, CD56, CD74, CD123, CD133, CD138, антиген инфицированной цитомегаловирусом (ЦМВ) клетки (например, антиген клеточной поверхности), эпителиальный гликопротеин 2 (EGP 2), эпителиальный гликопротеин-40 (EGP-40), молекула адгезии эпителиальных клеток (EpCAM), рецепторные тирозин-протеинкиназы ErbB2, Erb-B3, Erb-B4, фолатсвязывающий белок (FBP), фетальный ацетилхолиновый рецептор (AChR), рецептор фолата a, ганглиозид G2 (GD2), ганглиозид G3 (GD3), рецептор эпидермального фактора роста 2 человека (HER-2), обратная транскриптаза теломеразы человека (hTERT), субъединица рецептора интерлейкина-13 альфа-2 (IL-13Rα2), κ-легкая цепь, рецептор со вставкой киназного домена (KDR), Льюис A (CA19.9), Льюис Y (LeY), молекула клеточной адгезии L1 (L1CAM), семейство антигенов меланомы A, 1 (MAGE-AI), Муцин 16 (Muc-16), Муцин 1 (Muc-1), лиганды NKG2D, раково-тестикулярный антиген NY-ESO-1, офетальный антиген (h5T4), антиген стволовых клеток простаты (PSCA), простат-специфический мембранный антиген (ПСМА), опухолевый гликопротеин 72 (TAG-72), фактор роста эндотелия сосудов R2 (VEGF-R2), белок опухоли Вильмса (WT-1), трансмембранный рецептор тирозин-протеинкиназы 1 типа (ROR1) или их комбинация.
Подходящие антигены патогенов для применения при лечении инфекции, вызванной патогенном, или другого инфекционного заболевания, например у субъекта с ослабленным иммунитетом включают, без ограничения, вирусные антигены, присутствующие в цитомегаловирусе (ЦМВ), вирусе Эпштейна-Барр (ВЭБ), вирусе иммунодефицита человека (ВИЧ) и вирусе гриппа. Иммунореактивные клетки, включающие второй CAR, направленно взаимодействующий с вирусным антигеном, могут применяться для лечения вирусных заболеваний. В некоторых вариантах осуществления мезотелин-направленный CAR и второй CAR, который связывается с антигеном ЦМВ, коэкспрессируются в иммунореактивных клетках (например, цитотоксических T-лимфоцитах) и могут применяться для лечения ЦМВ.
Мезотелин-специфичные или мезотелин-направленные человеческие лимфоциты, которые могут применяться в способах раскрытого в настоящем документе изобретения, включают, без ограничения, периферические донорские лимфоциты, например, описанные в публикации в публикации Sadelain, M., et al. 2003 Nat Rev Cancer 3: 35-45 (в которой раскрыты периферические донорские лимфоциты, генетически модифицированные для экспрессии CAR-рецепторов), в публикации Morgan, R.A., et al. 2006 Science 314: 126-129 (в которой раскрыты периферические донорские лимфоциты, генетически модифицированные для экспрессии T-клеточного рецепторного комплекса, распознающего полноразмерные опухолевые антигены и включающего α и β-гетеродимер), в публикациях Panelli, M.C., et al. 2000 J Immunol 164: 495-504; Panelli, M.C., et al. 2000 J Immunol 164: 4382-4392 (в которых раскрыты культуры лимфоцитов, полученных из инфильтрирующих опухоль лимфоцитов (TIL) в образцах биопсии опухолей), и в публикациях Dupont, J., et al. 2005 Cancer Res 65: 5417-5427; Papanicolaou, G.A., et al. 2003 Blood 102: 2498-2505 (в которых раскрыты антигенспецифичные лейкоциты периферической крови, селективно размноженные in vitro при использовании искусственных антигенпрезентирующих клеток (иАПК) или активированных дендритных клеток). Иммунореактивные клетки (например, T-клетки) могут быть аутологичными, неаутологичными (например, аллогенными) или могут быть получены in vitro из модифицированных прогениторных или стволовых клеток.
Могут использоваться анализы для сравнения влияния передачи костимулирующих сигналов на усиление пролиферации эффекторной функции и накопления T-клеток, трансдуцированных мезотелин-направленным CAR, при повторной (еженедельной) стимуляции антигеном. Лимфоциты периферической крови (PBL) могут быть получены у здоровых добровольцев в соответствии с протоколом, одобренным IRB, и трансдуцированы. Эффективность переноса генов можно контролировать с помощью FACS анализа для количественного определения доли GFP+ (трансдуцированных) T-клеток и/или с помощью количественной ПЦР. При использовании хорошо отработанной системы сокультивирования (Gade, T.P., et al.Cancer Res.65, 9080-9088 (2005); Gong, M.C., et al. Neoplasia. 1, 123-127 (1999); Latouche, J.B. & Sadelain, M. Nat.Biotechnol. 18, 405-409 (2000)) можно определить, могут ли фибробластные ААРС, экспрессирующие мезотелин (в сравнении с контролями по мезотелину), направлять высвобождение цитокинов из трансдуцированных T-клеток (анализ LUMINEX клеточного супернатанта на IL-2, IL -4, IL-10, IFN-γ, ФНО-α и ГМ-КСФ), пролиферацию T-клеток (при мечении CFSE) и выживаемость T-клеток (при окрашивании аннексином V). Можно оценить влияние CD80 и/или 4-1BBL на выживаемость, пролиферацию и эффективность T-клеток. T-клетки могут быть подвергнуты повторной стимуляции мезотелин+ клетками-мишенями (MSLN+) и определению, остались ли пролиферация T-клеток и цитокиновый ответ аналогичными или уменьшились при повторной стимуляции. Анализы цитотоксичности с различными соотношениями E:T можно проводить при использовании анализов высвобождения хрома. Статистический анализ может быть необязательно выполнен с использованием двухфакторного дисперсионного анализа с последующими процедурами попарного множественного сравнения, в котором данные могут быть выражены как среднее ±SEM. Субтипы CD4 и CD8 T-клеток (активированные эффекторные, центральной памяти, эффекторной памяти) могут быть идентифицированы для определения, какие условия являются благоприятными для поддержания или экспансии фенотипа центральной памяти.
В некоторых вариантах осуществления раскрытая в настоящем документе иммунореактивная клетка (например, T-клетка) экспрессирует от приблизительно 1 до приблизительно 4, от приблизительно 2 до приблизительно 4, от приблизительно 3 до приблизительно 4, от приблизительно 1 до приблизительно 2, от приблизительно 1 до приблизительно 3 или от приблизительно 2 до приблизительно 3 копий вектора/клетка мезотелин-направленного CAR. Например, раскрытая в настоящем документе иммунореактивная клетка (например, T-клетка) экспрессирует приблизительно 1, приблизительно 2, приблизительно 3 или приблизительно 4 копий вектора/клетка мезотелин-направленного CAR. В некоторых вариантах осуществления раскрытая в настоящем документе иммунореактивная клетка (например, T-клетка) экспрессирует от приблизительно 3 до приблизительно 4 копий вектора/клетка мезотелин-направленного CAR. В некоторых вариантах осуществления цитотоксичность и продукция цитокинов иммунореактивной клетки (например, T-клетки) пропорциональны уровню экспрессии мезотелин-специфичного CAR в клетке. Например, чем выше уровень экспрессии CAR в иммунореактивной клетке, тем выше цитотоксичность и продукция цитокинов, которую демонстрирует иммунореактивная клетка. Иммунореактивная клетка (например, T-клетка), имеющая высокий уровень экспрессии мезотелин-CAR-рецептора, может вызвыать антиген-специфическую продукцию или секрецию цитокина и/или демонстрировать цитотоксичность для ткани или клетки, имеющей низкий уровень экспрессии мезотелина, например, приблизительно 2000 или меньше, приблизительно 1000 или меньше, приблизительно 900 или меньше, приблизительно 800 или меньше, приблизительно 700 или меньше, приблизительно 600 или меньше, приблизительно 500 или меньше, приблизительно 400 или меньше, приблизительно 300 или меньше, приблизительно 200 или меньше, приблизительно 100 или меньше связывающих сайтов мезотелина/клетка. Дополнительно или альтернативно, цитотоксичность и продукция цитокинов раскрытой в настоящем документе иммунореактивной клетки (например, T-клетки) пропорциональны уровню экспрессии человеческого мезотелина в ткани-мишени или клетке-мишени. Например, чем выше уровень экспрессии человеческого мезотелин в мишени, тем выше цитотоксичность и продукция цитокинов, которую демонстрирует иммунореактивная клетка.
В некоторых вариантах осуществления клетки-мишени являются гетерогенными MSLN-экспрессирующими клетками, которые представляют собой популяцию клеток, включающих клетки с низкой экспрессией MSLN и клетки с высокой экспрессией MSLN. Раскрытая в настоящем документе иммунореактивная клетка может демонстрировать повышенную цитотоксичность и противоопухолевую активность в отношении клеток с низкой экспрессией MSLN (например, приблизительно 2000 или меньше, приблизительно 1000 или меньше, приблизительно 900 или меньше, приблизительно 800 или меньше, приблизительно 700 или меньше, приблизительно 600 или меньше, приблизительно 500 или меньше, приблизительно 400 или меньше, приблизительно 300 или меньше, приблизительно 200 или меньше или приблизительно 100 или меньше связывающих сайтов MSLN/клетка) в присутствии клеток с высокой экспрессией MSLN. В некоторых вариантах осуществления, даже в присутствии клеток с высокой экспрессией MSLN, иммунореактивная клетка не демонстрирует повышенную цитотоксичность или неспецифичный киллинг в отношении MSLN-отрицательных клеток. Таким образом, иммунореактивная клетка может демонстрировать повышенную цитотоксичность и противоопухолевую активность в отношении клеток с низкой экспрессией MSLN в присутствии клеток с высокой экспрессией MSLN, сохраняя при этом безопасность в отношении MSLN-отрицательных клеток.
В некоторых вариантах осуществления иммунореактивная клетка может экспрессировать одну или больше молекул адгезии, которые могут повышать авидность MSLN-специфичного CAR, в особенности если CAR является низкоаффинным CAR. Неограничивающие примеры молекул адгезии включают CD2 и VLA-4. CD2, экспрессируемый на иммунореактивной клетке, может связываться с CD58, экспрессируемым на клетке-мишени (например, раковой клетке). VLA-4, экспрессируемый на иммунореактивной клетке, может связываться с VCAM-1 на клетке-мишени (например, раковой клетке).
Неочищенный источник CTL может быть любым известным в уровне техники, таким как костный мозг, эмбриональный, неонатальный или взрослый или другой источник гемопоэтических клеток, например, эмбриональная печень, периферическая кровь или пуповинная кровь. Различные методы могут применяться для разделения клеток. Например, методы негативного отбора позволяют первоначально удалять клетки кроме CTL. МАт особенно полезны для идентификации маркеров, связанных с конкретными линиями и/или стадиями дифференцировки клеток как для позитивных, так и для негативных отборов.
Большая часть терминально дифференцированных клеток может быть первоначально удалена при относительно грубом разделении. Например, разделение с помощью магнитных гранул может использоваться первоначально для удаления большого количества нерелевантных клеток. В некоторых вариантах осуществления по меньшей мере приблизительно 80%, обычно по меньшей мере 70% от общего количества гемопоэтических клеток будут удалять до выделения клеток.
Процедуры разделения включают, без ограничения, центрифугирование в градиенте плотности; возврат в исходное состояние; связывание с частицами, которые изменяют плотность клеток; разделение в магнитном поле с помощью магнитных гранул, покрытых антителами; аффинная хроматография; цитотоксические средства, соединенные или используемые вместе с мАт, в том числе, без ограничения перечисленными, комплемент и цитотоксины; а также пэннинг с антителом, прикрепленным к твердой матрице, например пластине, чипу, элютриацию или любую другую удобную методику.
Методы разделения и анализа включают, без ограничения, проточную цитометрию, которая может иметь различную степень сложности, например, множество цветовых каналов, каналы детектирования малоуглового и тупоугольного светорассеяния, каналы сопротивления.
Клетки могут быть отобраны от мертвых клеток при использовании красителей, связывающихся с мертвыми клетками, таких как йодистый пропидий (PI). В некоторых вариантах осуществления клетки собирают в среде, содержащей 2% фетальной телячьей сыворотки (FCS) или 0,2% бычьего сывороточного альбумина (BSA), или любой другой подходящей, например стерильной изотонической, среде.
5.4. Композиции нуклеиновых кислот и векторы
В настоящем изобретении предложены композиции нуклеиновых кислот, кодирующих полипептидные композиции, раскрытые в настоящем документе (например, раскрытые в Разделе 5.2). В некоторых вариантах осуществления композиция нуклеиновой кислоты включает полинуклеотид, кодирующий полипептидную композицию, раскрытую в настоящем документе (например, раскрытую в Разделе 5.2). Также предложены векторы, включающие такие композиции нуклеиновых кислот, и клетки, включающие такие композиции нуклеиновых кислот или векторы.
В некоторых вариантах осуществления композиция нуклеиновой кислоты дополнительно включает промотор, функционально связанный с полипептидной композицией. В некоторых вариантах осуществления промотор является эндогенным или экзогенным. В некоторых вариантах осуществления экзогенный промотор выбран из промотора фактора элонгации (EF)-1, промотора ЦМВ, промотора SV40, промотора PGK и промотора металлотионеина. В некоторых вариантах осуществления промотор является индуцируемым промотором. В некотором варианте осуществления индуцируемый промотор выбран из промотора транскрипционного элемента ответа (TRE) NFAT, промотора CD69, промотора CD25 и промотора IL-2.
Композиции нуклеиновых кислот могут вводить субъектам и/или доставлять в клетки с помощью известных способов, или как описано в настоящем документе.
Генетическая модификация иммунореактивной клетки (например, T-клетки или NK-клетки) может быть выполнена путем трансдукции по существу гомогенной композиции клеток конструкцией рекомбинантной ДНК. В некоторых вариантах осуществления ретровирусный вектор (гамма-ретровирусный или лентивирусный) используют для введения конструкции ДНК в клетку. Например, полинуклеотид, кодирующий антигенраспознающий рецептор, может быть клонирован в ретровирусный вектор, и экспрессия может направляться с его эндогенного промотора, из ретровирусного длинного концевого повтора, или с промотора, специфического для данного типа представляющей интерес клетки-мишени. Также могут использоваться невирусные векторы.
Для первоначальной генетической модификации иммунореактивной клетки, с целью введения антигенраспознающего рецептора (например, CAR или TCR), для трансдукции обычно используют ретровирусный вектор, однако могут использовать любой другой подходящий вирусный вектор или невирусную систему доставки. CAR и PD-1 DN могут быть сконструированы в одной мультицистронной кассете экспрессии, в нескольких кассетах экспрессии одного вектора, или в нескольких векторах. Примеры элементов, которые создают полицистронную кассету экспрессии, включают, без ограничения, различные вирусные и невирусные участки внутренней посадки рибосомы (IRES, например, IRES FGF-1, IRES FGF-2, IRES VEGF, IRES IGF-II, IRES NF-κB, IRES RUNX1, IRES p53, IRES вируса гепатита A, IRES вируса гепатита C, IRES пестивируса, IRES афтовируса, IRES пикорнавируса, IRES полиовируса и IRES вируса энцефаломиокардита), а также расщепляемые линкеры (например, 2А пептиды, например, P2A, T2A, E2A и F2A пептиды). В некоторых вариантах осуществления P2A пептид включает или состоит из аминокислотной последовательности, представленной в SEQ ID NO: 107, которая приведена ниже:
GSGATNFSLLKQAGDVEENPGPM [SEQ ID NO: 107]
В некоторых вариантах осуществления P2A пептид включает или состоит из аминокислотной последовательности, представленной в SEQ ID NO: 121, которая приведена ниже:
ATNFSLLKQAGDVEENPGP [SEQ ID NO: 121]
Примерная нуклеотидная последовательность, кодирующая аминокислотную последовательность SEQ ID NO: 121, представлена в SEQ ID NO: 122, которая приведена ниже:
GCAACAAACTTCTCACTACTCAAACAAGCAGGTGACGTGGAGGAGAATCCCGGCCCA [SEQ ID NO: 122]
Комбинации ретровирусного вектора и соответствующей пакующей линии также являются подходящими, если капсидные белки будут функциональными для инфицирования клеток человека. Известны различные линии клеток, продуцирующих амфотропные вирусы, в том числе, без ограничения перечисленными, PA12 (Miller, et al. (1985) Mol. Cell. Biol. 5: 431-437); PA317 (Miller, et al. (1986) Mol. Cell. Biol. 6: 2895-2902); и CRIP (Danos, et al. (1988) Proc. Natl. Acad. Sci. USA 85: 6460-6464). Также подходят неамфотропные частицы, например частицы, псевдотипированные гликопротеинами оболочки VSVG, RD114 или GALV, а также любые другие частицы, известные в данной области.
Возможные способы трансдукции также включают прямое совместное культивирование клеток с клетками-продуцентами, например, способом Bregni, et al. (1992) Blood 80: 1418-1422, или культивирование только с вирусным супернатантом или концентрированными стоковыми растворами векторов с соответствующими факторами роста и поликатионами или без них, например, способом Xu, et al. (1994) Exp. Hemat. 22: 223-230; и Hughes et al. (1992) J. Clin. Invest. 89: 1817.
Для модификации иммунореактивной клетки могут использоваться другие трансдуцирующие вирусные векторы. В некоторых вариантах осуществления выбранный вектор демонстрирует высокую эффективность инфекции и стабильную интеграцию и экспрессию (см., например, Cayouette et al., Human Gene Therapy 8: 423-430, 1997; Kido et al., Current Eye Research 15: 833-844, 1996; Bloomer et al., Journal of Virology 71: 6641-6649, 1997; Naldini et al., Science 272: 263-267, 1996; и Miyoshi et al., Proc. Natl. Acad. Sci. U.S.A. 94: 10319, 1997). Другие вирусные векторы, которые могут использоваться, включают, например, аденовирусные, лентивирусные векторы и векторы на основе аденоассоциированного вируса, вирус осповакцины, вирус папилломы крупного рогатого скота или вирус герпеса, такой как вирус Эпштейна-Барр (также см., например, векторы в Miller, Human Gene Therapy 15-14, 1990; Friedman, Science 244: 1275-1281, 1989; Eglitis et al., BioTechniques 6: 608-614, 1988; Tolstoshev et al., Current Opinion in Biotechnology 1: 55-61, 1990; Sharp, The Lancet 337: 1277-1278, 1991; Cornetta et al., Nucleic Acid Research and Molecular Biology 36: 311-322, 1987; Anderson, Science 226: 401-409, 1984; Moen, Blood Cells 17: 407-416, 1991; Miller et al., Biotechnology 7: 980-990, 1989; LeGal La Salle et al., Science 259: 988-990, 1993; и Johnson, Chest 107: 77S-83S, 1995). Ретровирусные векторы особенно хорошо отработаны и применяются в клинических условиях (Rosenberg et al., N. Engl. J. Med 323: 370, 1990; Anderson et al., Патент США 5,399,346).
В некоторых вариантах осуществления вектор, кодирующий раскрытую в настоящем документе полипептидную композицию, является ретровирусным вектором, например, SGF γ-ретровирусным вектором, который может быть ретровирусным вектором на основе вируса мышиного лейкоза Молони. В некоторых вариантах осуществления вектор включает или состоит из нуклеотидной последовательности, представленной в SEQ ID NO: 123, которая приведена ниже:
ATGGCCCTGCCAGTAACGGCTCTGCTGCTGCCACTTGCTCTGCTCCTCCATGCAGCCAGGCCTCAGGTTCAGCTTCAGGAGAGTGGCCCAGGCCTGGTGAAGCCAAGTGAGACTCTCAGCTTGACTTGCACAGTTTCTGGAGGCAGTGTCTCCTCAGGCAGCTATTATTGGTCCTGGATTCGGCAGCCCCCTGGGAAAGGCCTGGAGTGGATTGGGTACATATATTACAGTGGCAGCACAAATTACAATCCATCCCTGAAGTCTCGAGTAACTATCAGTGTGGACACAAGCAAGAATCAGTTTTCACTCAAACTGTCTTCTGTGACTGCTGCTGACACTGCTGTTTATTATTGTGCCAGGGAGGGGAAAAATGGGGCATTTGATATTTGGGGTCAGGGCACAATGGTGACAGTCAGCTCTGGAGGTGGAGGCTCAGGAGGAGGAGGCAGTGGAGGTGGTGGGTCACGCCATCAGATGACTCAGTCCCCCTCCAGTCTTTCTGCCTCAGTTGGGGATAGAGTGACCATCACATGCAGAGCAAGTCAGAGCATATCATCCTATCTGAACTGGTACCAGCAGAAGCCAGGGAAAGCCCCCAAATTGCTGATTTATGCAGCCTCAAGTCTCCAGAGTGGGGTGCCAAGCAGGTTCTCAGGCAGTGGCAGTGGGACAGATTTCACATTGACAATCAGCTCCCTCCAACCTGAAGATTTTGCCACCTACTATTGCCAGCAATCCTACAGCACGCCCCTGACTTTTGGAGGTGGCACAAAGGTAGAGATCAAGAGGACTgcggccgcaattgaagttatgtatcctcctccttacctagacaatgagaagagcaatggaaccattatccatgtgaaagggaaacacctttgtccaagtcccctatttcccggaccttctaagcccttttgggtgctggtggtggttggtggagtcctggcttgctatagcttgctagtaacagtggcctttattattttctgggtgaggagtaagaggagcaggctcctgcacagtgactacatgaacatgactccccgccgccccgggcccacccgcaagcattaccagccctatgccccaccacgcgacttcgcagcctatcgctccagagtgaagttcagcaggagcgcagacgcccccgcgtaccagcagggccagaaccagctctataacgagctcaatctaggacgaagagaggagtacgatgttttggacaagagacgtggccgggaccctgagatggggggaaagccgagaaggaagaaccctcaggaaggcctgtTcaatgaactgcagaaagataagatggcggaggcctTcagtgagattgggatgaaaggcgagcgccggaggggcaaggggcacgatggcctttTccaggggctcagtacagccaccaaggacacctTcgacgcccttcacatgcaggccctgccccctcgcGGATCTGGAGCAACAAACTTCTCACTACTCAAACAAGCAGGTGACGTGGAGGAGAATCCCGGCCCAATGCAGATCCCACAGGCGCCCTGGCCAGTCGTCTGGGCGGTGCTACAACTGGGCTGGCGGCCAGGATGGTTCTTAGACTCCCCAGACAGGCCCTGGAACCCCCCCACCTTCTCCCCAGCCCTGCTCGTGGTGACCGAAGGGGACAACGCCACCTTCACCTGCAGCTTCTCCAACACATCGGAGAGCTTCGTGCTAAACTGGTACCGCATGAGCCCCAGCAACCAGACGGACAAGCTGGCCGCTTTCCCCGAGGACCGCAGCCAGCCCGGCCAGGACTGCCGCTTCCGTGTCACACAACTGCCCAACGGGCGTGACTTCCACATGAGCGTGGTCAGGGCCCGGCGCAATGACAGCGGCACCTACCTCTGTGGGGCCATCTCCCTGGCCCCCAAGGCGCAGATCAAAGAGAGCCTGCGGGCAGAGCTCAGGGTGACAGAGAGAAGGGCAGAAGTGCCCACAGCCCACCCCAGCCCCTCACCCAGGCCAGCCGGCCAGGCGGCCGCACCCACCACGACGCCAGCGCCGCGACCACCAACCCCGGCGCCCACGATCGCGTCGCAGCCCCTGTCCCTGCGCCCAGAGGCGTGCCGGCCAGCGGCGGGGGGCGCAGTGCACACGAGGGGGCTGGACTTCGCCTGTGATATCTACATCTGGGCGCCCCTGGCCGGGACTTGTGGGGTCCTTCTCCTGTCACTGGTTATCACCCTTTACTGCAACCACAGGCGGATCCAATAAcagccactcgaggatccGGATTAGTCCAATTTGTTAAAGACAGGATATCAGTGGTCCAGGCTCTAGTTTTGACTCAACAATATCACCAGCTGAAGCCTATAGAGTACGAGCCATAGATAAAATAAAAGATTTTATTTAGTCTCCAGAAAAAGGGGGGAATGAAAGACCCCACCTGTAGGTTTGGCAAGCTAGCTTAAGTAACGCCATTTTGCAAGGCATGGAAAAATACATAACTGAGAATAGAGAAGTTCAGATCAAGGTCAGGAACAGATGGAACAGCTGAATATGGGCCAAACAGGATATCTGTGGTAAGCAGTTCCTGCCCCGGCTCAGGGCCAAGAACAGATGGAACAGCTGAATATGGGCCAAACAGGATATCTGTGGTAAGCAGTTCCTGCCCCGGCTCAGGGCCAAGAACAGATGGTCCCCAGATGCGGTCCAGCCCTCAGCAGTTTCTAGAGAACCATCAGATGTTTCCAGGGTGCCCCAAGGACCTGAAATGACCCTGTGCCTTATTTGAACTAACCAATCAGTTCGCTTCTCGCTTCTGTTCGCGCGCTTCTGCTCCCCGAGCTCAATAAAAGAGCCCACAACCCCTCACTCGGGGCGCCAGTCCTCCGATTGACTGAGTCGCCCGGGTACCCGTGTATCCAATAAACCCTCTTGCAGTTGCATCCGACTTGTGGTCTCGCTGTTCCTTGGGAGGGTCTCCTCTGAGTGATTGACTACCCGTCAGCGGGGGTCTTTCACACATGCAGCATGTATCAAAATTAATTTGGTTTTTTTTCTTAAGTATTTACATTAAATGGCCATAGTACTTAAAGTTACATTGGCTTCCTTGAAATAAACATGGAGTATTCAGAATGTGTCATAAATATTTCTAATTTTAAGATAGTATCTCCATTGGCTTTCTACTTTTTCTTTTATTTTTTTTTGTCCTCTGTCTTCCATTTGTTGTTGTTGTTGTTTGTTTGTTTGTTTGTTGGTTGGTTGGTTAATTTTTTTTTAAAGATCCTACACTATAGTTCAAGCTAGACTATTAGCTACTCTGTAACCCAGGGTGACCTTGAAGTCATGGGTAGCCTGCTGTTTTAGCCTTCCCACATCTAAGATTACAGGTATGAGCTATCATTTTTGGTATATTGATTGATTGATTGATTGATGTGTGTGTGTGTGATTGTGTTTGTGTGTGTGACTGTGAAAATGTGTGTATGGGTGTGTGTGAATGTGTGTATGTATGTGTGTGTGTGAGTGTGTGTGTGTGTGTGTGCATGTGTGTGTGTGTGACTGTGTCTATGTGTATGACTGTGTGTGTGTGTGTGTGTGTGTGTGTGTGTGTGTGTGTGTGTGTGTTGTGAAAAAATATTCTATGGTAGTGAGAGCCAACGCTCCGGCTCAGGTGTCAGGTTGGTTTTTGAGACAGAGTCTTTCACTTAGCTTGGAATTCactggccgtcgttttacaacgtcgtgactgggaaaaccctggcgttacccaacttaatcgccttgcagcacatccccctttcgccagctggcgtaatagcgaagaggcccgcaccgatcgcccttcccaacagttgcgcagcctgaatggcgaatggcgcctgatgcggtattttctccttacgcatctgtgcggtatttcacaccgcatatggtgcactctcagtacaatctgctctgatgccgcatagttaagccagccccgacacccgccaacacccgctgacgcgccctgacgggcttgtctgctcccggcatccgcttacagacaagctgtgaccgtctccgggagctgcatgtgtcagaggttttcaccgtcatcaccgaaacgcgcgatgacgaaagggcctcgtgatacgcctatttttataggttaatgtcatgataataatggtttcttagacgtcaggtggcacttttcggggaaatgtgcgcggaacccctatttgtttatttttctaaatacattcaaatatgtatccgctcatgagacaataaccctgataaatgcttcaataatattgaaaaaggaagagtatgagtattcaacatttccgtgtcgcccttattcccttttttgcggcattttgccttcctgtttttgctcacccagaaacgctggtgaaagtaaaagatgctgaagatcagttgggtgcacgagtgggttacatcgaactggatctcaacagcggtaagatccttgagagttttcgccccgaagaacgttttccaatgatgagcacttttaaagttctgctatgtggcgcggtattatcccgtattgacgccgggcaagagcaactcggtcgccgcatacactattctcagaatgacttggttgagtactcaccagtcacagaaaagcatcttacggatggcatgacagtaagagaattatgcagtgctgccataaccatgagtgataacactgcggccaacttacttctgacaacgatcggaggaccgaaggagctaaccgcttttttgcacaacatgggggatcatgtaactcgccttgatcgttgggaaccggagctgaatgaagccataccaaacgacgagcgtgacaccacgatgcctgtagcaatggcaacaacgttgcgcaaactattaactggcgaactacttactctagcttcccggcaacaattaatagactggatggaggcggataaagttgcaggaccacttctgcgctcggcccttccggctggctggtttattgctgataaatctggagccggtgagcgtgggtctcgcggtatcattgcagcactggggccagatggtaagccctcccgtatcgtagttatctacacgacggggagtcaggcaactatggatgaacgaaatagacagatcgctgagataggtgcctcactgattaagcattggtaactgtcagaccaagtttactcatatatactttagattgatttaaaacttcatttttaatttaaaaggatctaggtgaagatcctttttgataatctcatgaccaaaatcccttaacgtgagttttcgttccactgagcgtcagaccccgtagaaaagatcaaaggatcttcttgagatcctttttttctgcgcgtaatctgctgcttgcaaacaaaaaaaccaccgctaccagcggtggtttgtttgccggatcaagagctaccaactctttttccgaaggtaactggcttcagcagagcgcagataccaaatactgtccttctagtgtagccgtagttaggccaccacttcaagaactctgtagcaccgcctacatacctcgctctgctaatcctgttaccagtggctgctgccagtggcgataagtcgtgtcttaccgggttggactcaagacgatagttaccggataaggcgcagcggtcgggctgaacggggggttcgtgcacacagcccagcttggagcgaacgacctacaccgaactgagatacctacagcgtgagcattgagaaagcgccacgcttcccgaagggagaaaggcggacaggtatccggtaagcggcagggtcggaacaggagagcgcacgagggagcttccagggggaaacgcctggtatctttatagtcctgtcgggtttcgccacctctgacttgagcgtcgatttttgtgatgctcgtcaggggggcggagcctatggaaaaacgccagcaacgcggcctttttacggttcctggccttttgctggccttttgctcacatgttctttcctgcgttatcccctgattctgtggataaccgtattaccgcctttgagtgagctgataccgctcgccgcagccgaacgaccgagcgcagcgagtcagtgagcgaggaagcggaagagcgcccaatacgcaaaccgcctctccccgcgcgttggccgattcattaatgcagctggcacgacaggtttcccgactggaaagcgggcagtgagcgcaacgcaattaatgtgagttagctcactcattaggcaccccaggctttacactttatgcttccggctcgtatgttgtgtggaattgtgagcggataacaatttcacacaggaaacagctatgaccatgattacgccAAGCTTTGCTCTTAGGAGTTTCCTAATACATCCCAAACTCAAATATATAAAGCATTTGACTTGTTCTATGCCCTAGGGGGCGGGGGGAAGCTAAGCCAGCTTTTTTTAACATTTAAAATGTTAATTCCATTTTAAATGCACAGATGTTTTTATTTCATAAGGGTTTCAATGTGCATGAATGCTGCAATATTCCTGTTACCAAAGCTAGTATAAATAAAAATAGATAAACGTGGAAATTACTTAGAGTTTCTGTCATTAACGTTTCCTTCCTCAGTTGACAACATAAATGCGCTGCTGAGCAAGCCAGTTTGCATCTGTCAGGATCAATTTCCCATTATGCCAGTCATATTAATTACTAGTCAATTAGTTGATTTTTATTTTTGACATATACATGTGAATGAAAGACCCCACCTGTAGGTTTGGCAAGCTAGCTTAAGTAACGCCATTTTGCAAGGCATGGAAAAATACATAACTGAGAATAGAAAAGTTCAGATCAAGGTCAGGAACAGATGGAACAGCTGAATATGGGCCAAACAGGATATCTGTGGTAAGCAGTTCCTGCCCCGGCTCAGGGCCAAGAACAGATGGAACAGCTGAATATGGGCCAAACAGGATATCTGTGGTAAGCAGTTCCTGCCCCGGCTCAGGGCCAAGAACAGATGGTCCCCAGATGCGGTCCAGCCCTCAGCAGTTTCTAGAGAACCATCAGATGTTTCCAGGGTGCCCCAAGGACCTGAAATGACCCTGTGCCTTATTTGAACTAACCAATCAGTTCGCTTCTCGCTTCTGTTCGCGCGCTTATGCTCCCCGAGCTCAATAAAAGAGCCCACAACCCCTCACTCGGGGCGCCAGTCCTCCGATTGACTGAGTCGCCCGGGTACCCGTGTATCCAATAAACCCTCTTGCAGTTGCATCCGACTTGTGGTCTCGCTGTTCCTTGGGAGGGTCTCCTCTGAGTGATTGACTACCCGTCAGCGGGGGTCTTTCATTTGGGGGCTCGTCCGGGATCGGGAGACCCCTGCCCAGGGACCACCGACCCACCACCGGGAGGTAAGCTGGCCAGCAACTTATCTGTGTCTGTCCGATTGTCTAGTGTCTATGACTGATTTTATGCGCCTGCGTCGGTACTAGTTAGCTAACTAGCTCTGTATCTGGCGGACCCGTGGTGGAACTGACGAGTTCGGAACACCCGGCCGCAACCCTGGGAGACGTCCCAGGGACTTCGGGGGCCGTTTTTGTGGCCCGACCTGAGTCCTAAAATCCCGATCGTTTAGGACTCTTTGGTGCACCCCCCTTAGAGGAGGGATATGTGGTTCTGGTAGGAGACGAGAACCTAAAACAGTTCCCGCCTCCGTCTGAATTTTTGCTTTCGGTTTGGGACCGAAGCCGCGCCGCGCGTCTTGTCTGCTGCAGCATCGTTCTGTGTTGTCTCTGTCTGACTGTGTTTCTGTATTTGTCTGAAAATATGGGCCCGGGCTAGcctgttaccactCCCTTAAGTTTGACCTTAGGTCACTGGAAAGATGTCGAGCGGATCGCTCACAACCAGTCGGTAGATGTCAAGAAGAGACGTTGGGTTACCTTCTGCTCTGCAGAATGGCCAACCTTTAACGTCGGATGGCCGCGAGACGGCACCTTTAACCGAGACCTCATCACCCAGGTTAAGATCAAGGTCTTTTCACCTGGCCCGCATGGACACCCAGACCAGGTccccTACATCGTGACCTGGGAAGCCTTGGCTTTTGACCCCCCTCCCTGGGTCAAGCCCTTTGTACACCCTAAGCCTCCGCCTCCTCTTCCTCCATCCGCCCCGTCTCTCCCCCTTGAACCTCCTCGTTCGACCCCGCCTCGATCCTCCCTTTATCCAGCCCTCACTCCTTCTCTAGGCGCCCCCATATGGCCATATGAGATCTTATATGGGGCACCCCCGCCCCTTGTAAACTTCCCTGACCCTGACATGACAAGAGTTACTAACAGCCCCTCTCTCCAAGCTCACTTACAGGCTCTCTACTTAGTCCAGCACGAAGTCTGGAGACCTCTGGCGGCAGCCTACCAAGAACAACTGGACCGACCGGTGGTACCTCACCCTTACCGAGTCGGCGACACAGTGTGGGTCCGCCGACACCAGACTAAGAACCTAGAACCTCGCTGGAAAGGACCTTACACAGTCCTGCTGACCACCCCCACCGCCCTCAAAGTAGACGGCATCGCAGCTTGGATACACGCCGCCCACGTGAAGGCTGCCGACCCCGGGGGTGGACCATCCTCTAGACTGCC [SEQ ID NO: 123]
В некоторых вариантах осуществления вектор включает или состоит из нуклеотидной последовательности, представленной в SEQ ID NO: 124, которая приведена ниже:
ATGGCCCTGCCAGTAACGGCTCTGCTGCTGCCACTTGCTCTGCTCCTCCATGCAGCCAGGCCTCAGGTTCAGCTTCAGGAGAGTGGCCCAGGCCTGGTGAAGCCAAGTGAGACTCTCAGCTTGACTTGCACAGTTTCTGGAGGCAGTGTCTCCTCAGGCAGCTATTATTGGTCCTGGATTCGGCAGCCCCCTGGGAAAGGCCTGGAGTGGATTGGGTACATATATTACAGTGGCAGCACAAATTACAATCCATCCCTGAAGTCTCGAGTAACTATCAGTGTGGACACAAGCAAGAATCAGTTTTCACTCAAACTGTCTTCTGTGACTGCTGCTGACACTGCTGTTTATTATTGTGCCAGGGAGGGGAAAAATGGGGCATTTGATATTTGGGGTCAGGGCACAATGGTGACAGTCAGCTCTGGAGGTGGAGGCTCAGGAGGAGGAGGCAGTGGAGGTGGTGGGTCACGCCATCAGATGACTCAGTCCCCCTCCAGTCTTTCTGCCTCAGTTGGGGATAGAGTGACCATCACATGCAGAGCAAGTCAGAGCATATCATCCTATCTGAACTGGTACCAGCAGAAGCCAGGGAAAGCCCCCAAATTGCTGATTTATGCAGCCTCAAGTCTCCAGAGTGGGGTGCCAAGCAGGTTCTCAGGCAGTGGCAGTGGGACAGATTTCACATTGACAATCAGCTCCCTCCAACCTGAAGATTTTGCCACCTACTATTGCCAGCAATCCTACAGCACGCCCCTGACTTTTGGAGGTGGCACAAAGGTAGAGATCAAGAGGACTgcggccgcaattgaagttatgtatcctcctccttacctagacaatgagaagagcaatggaaccattatccatgtgaaagggaaacacctttgtccaagtcccctatttcccggaccttctaagcccttttgggtgctggtggtggttggtggagtcctggcttgctatagcttgctagtaacagtggcctttattattttctgggtgaggagtaagaggagcaggctcctgcacagtgactacatgaacatgactccccgccgccccgggcccacccgcaagcattaccagccctatgccccaccacgcgacttcgcagcctatcgctccagagtgaagttcagcaggagcgcagacgcccccgcgtaccagcagggccagaaccagctctataacgagctcaatctaggacgaagagaggagtacgatgttttggacaagagacgtggccgggaccctgagatggggggaaagccgagaaggaagaaccctcaggaaggcctgtTcaatgaactgcagaaagataagatggcggaggcctTcagtgagattgggatgaaaggcgagcgccggaggggcaaggggcacgatggcctttTccaggggctcagtacagccaccaaggacacctTcgacgcccttcacatgcaggccctgccccctcgcGGATCTGGAGCAACAAACTTCTCACTACTCAAACAAGCAGGTGACGTGGAGGAGAATCCCGGCCCAATGCAGATCCCACAGGCGCCCTGGCCAGTCGTCTGGGCGGTGCTACAACTGGGCTGGCGGCCAGGATGGTTCTTAGACTCCCCAGACAGGCCCTGGAACCCCCCCACCTTCTCCCCAGCCCTGCTCGTGGTGACCGAAGGGGACAACGCCACCTTCACCTGCAGCTTCTCCAACACATCGGAGAGCTTCGTGCTAAACTGGTACCGCATGAGCCCCAGCAACCAGACGGACAAGCTGGCCGCTTTCCCCGAGGACCGCAGCCAGCCCGGCCAGGACTGCCGCTTCCGTGTCACACAACTGCCCAACGGGCGTGACTTCCACATGAGCGTGGTCAGGGCCCGGCGCAATGACAGCGGCACCTACCTCTGTGGGGCCATCTCCCTGGCCCCCAAGGCGCAGATCAAAGAGAGCCTGCGGGCAGAGCTCAGGGTGACAGAGAGAAGGGCAGAAGTGCCCACAGCCCACCCCAGCCCCTCACCCAGGCCAGCCGGCCAGGCGGCCGCACCCACCACGACGCCAGCGCCGCGACCACCAACCCCGGCGCCCACGATCGCGTCGCAGCCCCTGTCCCTGCGCCCAGAGGCGTGCCGGCCAGCGGCGGGGGGCGCAGTGCACACGAGGGGGCTGGACTTCGCCTGTGATATCTACATCTGGGCGCCCCTGGCCGGGACTTGTGGGGTCCTTCTCCTGTCACTGGTTATCACCCTTTACTGCAACCACAGGCGGATCCAATAAcagccactcgaggatccGGATTAGTCCAATTTGTTAAAGACAGGATATCAGTGGTCCAGGCTCTAGTTTTGACTCAACAATATCACCAGCTGAAGCCTATAGAGTACGAGCCATAGATAAAATAAAAGATTTTATTTAGTCTCCAGAAAAAGGGGGGAATGAAAGACCCCACCTGTAGGTTTGGCAAGCTAGCTTAAGTAACGCCATTTTGCAAGGCATGGAAAAATACATAACTGAGAATAGAGAAGTTCAGATCAAGGTCAGGAACAGATGGAACAGCTGAATATGGGCCAAACAGGATATCTGTGGTAAGCAGTTCCTGCCCCGGCTCAGGGCCAAGAACAGATGGAACAGCTGAATATGGGCCAAACAGGATATCTGTGGTAAGCAGTTCCTGCCCCGGCTCAGGGCCAAGAACAGATGGTCCCCAGATGCGGTCCAGCCCTCAGCAGTTTCTAGAGAACCATCAGATGTTTCCAGGGTGCCCCAAGGACCTGAAATGACCCTGTGCCTTATTTGAACTAACCAATCAGTTCGCTTCTCGCTTCTGTTCGCGCGCTTCTGCTCCCCGAGCTCAATAAAAGAGCCCACAACCCCTCACTCGGGGCGCCAGTCCTCCGATTGACTGAGTCGCCCGGGTACCCGTGTATCCAATAAACCCTCTTGCAGTTGCATCCGACTTGTGGTCTCGCTGTTCCTTGGGAGGGTCTCCTCTGAGTGATTGACTACCCGTCAGCGGGGGTCTTTCACATGCAGCATGTATCAAAATTAATTTGGTTTTTTTTCTTAAGTATTTACATTAAATGGCCATAGTACTTAAAGTTACATTGGCTTCCTTGAAATAAACATGGAGTATTCAGAATGTGTCATAAATATTTCTAATTTTAAGATAGTATCTCCATTGGCTTTCTACTTTTTCTTTTATTTTTTTTTGTCCTCTGTCTTCCATTTGTTGTTGTTGTTGTTTGTTTGTTTGTTTGTTGGTTGGTTGGTTAATTTTTTTTTAAAGATCCTACACTATAGTTCAAGCTAGACTATTAGCTACTCTGTAACCCAGGGTGACCTTGAAGTCATGGGTAGCCTGCTGTTTTAGCCTTCCCACATCTAAGATTACAGGTATGAGCTATCATTTTTGGTATATTGATTGATTGATTGATTGATGTGTGTGTGTGTGATTGTGTTTGTGTGTGTGAtTGTGtAtATGTGTGTATGGtTGTGTGTGAtTGTGTGTATGTATGTtTGTGTGTGAtTGTGTGTGTGTGatTGTGCATGTGTGTGTGTGTGAtTGTGTtTATGTGTATGAtTGTGTGTGTGTGTGTGTGTGTGTGTGTGTGTGTGTGTGTGTGTGTGTTGTGtAtAtATATTTATGGTAGTGAGAGgCAACGCTCCGGCTCAGGTGTCAGGTTGGTTTTTGAGACAGAGTCTTTCACTTAGCTTGGAATTCactggccgtcgttttacaacgtcgtgactgggaaaaccctggcgttacccaacttaatcgccttgcagcacatccccctttcgccagctggcgtaatagcgaagaggcccgcaccgatcgcccttcccaacagttgcgcagcctgaatggcgaatggcgcctgatgcggtattttctccttacgcatctgtgcggtatttcacaccgcatatggtgcactctcagtacaatctgctctgatgccgcatagttaagccagccccgacacccgccaacacccgctgacgcgccctgacgggcttgtctgctcccggcatccgcttacagacaagctgtgaccgtctccgggagctgcatgtgtcagaggttttcaccgtcatcaccgaaacgcgcgagacgaaagggcctcgtgatacgcctatttttataggttaatgtcatgataataatggtttcttagacgtcaggtggcacttttcggggaaatgtgcgcggaacccctatttgtttatttttctaaatacattcaaatatgtatccgctcatgagacaataaccctgataaatgcttcaataatattgaaaaaggaagagtatgagtattcaacatttccgtgtcgcccttattcccttttttgcggcattttgccttcctgtttttgctcacccagaaacgctggtgaaagtaaaagatgctgaagatcagttgggtgcacgagtgggttacatcgaactggatctcaacagcggtaagatccttgagagttttcgccccgaagaacgttttccaatgatgagcacttttaaagttctgctatgtggcgcggtattatcccgtattgacgccgggcaagagcaactcggtcgccgcatacactattctcagaatgacttggttgagtactcaccagtcacagaaaagcatcttacggatggcatgacagtaagagaattatgcagtgctgccataaccatgagtgataacactgcggccaacttacttctgacaacgatcggaggaccgaaggagctaaccgcttttttgcacaacatgggggatcatgtaactcgccttgatcgttgggaaccggagctgaatgaagccataccaaacgacgagcgtgacaccacgatgcctgtagcaatggcaacaacgttgcgcaaactattaactggcgaactacttactctagcttcccggcaacaattaatagactggatggaggcggataaagttgcaggaccacttctgcgctcggcccttccggctggctggtttattgctgataaatctggagccggtgagcgtgggtctcgcggtatcattgcagcactggggccagatggtaagccctcccgtatcgtagttatctacacgacggggagtcaggcaactatggatgaacgaaatagacagatcgctgagataggtgcctcactgattaagcattggtaactgtcagaccaagtttactcatatatactttagattgatttaaaacttcatttttaatttaaaaggatctaggtgaagatcctttttgataatctcatgaccaaaatcccttaacgtgagttttcgttccactgagcgtcagaccccgtagaaaagatcaaaggatcttcttgagatcctttttttctgcgcgtaatctgctgcttgcaaacaaaaaaaccaccgctaccagcggtggtttgtttgccggatcaagagctaccaactctttttccgaaggtaactggcttcagcagagcgcagataccaaatactgtTcttctagtgtagccgtagttaggccaccacttcaagaactctgtagcaccgcctacatacctcgctctgctaatcctgttaccagtggctgctgccagtggcgataagtcgtgtcttaccgggttggactcaagacgatagttaccggataaggcgcagcggtcgggctgaacggggggttcgtgcacacagcccagcttggagcgaacgacctacaccgaactgagatacctacagcgtgagcTAtgagaaagcgccacgcttcccgaagggagaaaggcggacaggtatccggtaagcggcagggtcggaacaggagagcgcacgagggagcttccagggggaaacgcctggtatctttatagtcctgtcgggtttcgccacctctgacttgagcgtcgatttttgtgatgctcgtcaggggggcggagcctatggaaaaacgccagcaacgcggcctttttacggttcctggccttttgctggccttttgctcacatgttctttcctgcgttatcccctgattctgtggataaccgtattaccgcctttgagtgagctgataccgctcgccgcagccgaacgaccgagcgcagcgagtcagtgagcgaggaagcggaagagcgcccaatacgcaaaccgcctctccccgcgcgttggccgattcattaatgcagctggcacgacaggtttcccgactggaaagcgggcagtgagcgcaacgcaattaatgtgagttagctcactcattaggcaccccaggctttacactttatgcttccggctcgtatgttgtgtggaattgtgagcggataacaatttcacacaggaaacagctatgaccatgattacgccAAGCTTTGCTCTTAGGAGTTTCCTAATACATCCCAAACTCAAATATATAAAGCATTTGACTTGTTCTATGCCCTAGGGGGCGGGGGGAAGCTAAGCCAGCTTTTTTTAACATTTAAAATGTTAATTCCATTTTAAATGCACAGATGTTTTTATTTCATAAGGGTTTCAATGTGCATGAATGCTGCAATATTCCTGTTACCAAAGCTAGTATAAATAAAAATAGATAAACGTGGAAATTACTTAGAGTTTCTGTCATTAACGTTTCCTTCCTCAGTTGACAACATAAATGCGCTGCTGAGAAGCCAGTTTGCATCTGTCAGGATCAATTTCCCATTATGCCAGTCATATTAATTACTAGTCAATTAGTTGATTTTTATTTTTGACATATACATGTGAAAGACCCCACCTGTAGGTTTGGCAAGCTAGCTTAAGTAACGCCATTTTGCAAGGCATGGAAAAATACATAACTGAGAATAGAAAAGTTCAGATCAAGGTCAGGAACAGATGGAACAGCTGAATATGGGCCAAACAGGATATCTGTGGTAAGCAGTTCCTGCCCCGGCTCAGGGCCAAGAACAGATGGAACAGCTGAATATGGGCCAAACAGGATATCTGTGGTAAGCAGTTCCTGCCCCGGCTCAGGGCCAAGAACAGATGGTCCCCAGATGCGGTCCAGCCCTCAGCAGTTTCTAGAGAACCATCAGATGTTTCCAGGGTGCCCCAAGGACCTGAAATGACCCTGTGCCTTATTTGAACTAACCAATCAGTTCGCTTCTCGCTTCTGTTCGCGCGCTTcTGCTCCCCGAGCTCAATAAAAGAGCCCACAACCCCTCACTCGGcGCGCCAGTCCTCCGATTGACTGAGTCGCCCGGGTACCCGTGTATCCAATAAACCCTCTTGCAGTTGCATCCGACTTGTGGTCTCGCTGTTCCTTGGGAGGGTCTCCTCTGAGTGATTGACTACCCGTCAGCGGGGGTCTTTCATTTGGGGGCTCGTCCGGGATCGGGAGACCCCTGCCCAGGGACCACCGACCCACCACCGGGAGGTAAGCTGGCCAGCAACTTATCTGTGTCTGTCCGATTGTCTAGTGTCTATGACTGATTTTATGCGCCTGCGTCGGTACTAGTTAGCTAACTAGCTCTGTATCTGGCGGACCCGTGGTGGAACTGACGAGTTCGGAACACCCGGCCGCAACCCTGGGAGACGTCCCAGGGACTTCGGGGGCCGTTTTTGTGGCCCGACCTGAGTCCTAAAATCCCGATCGTTTAGGACTCTTTGGTGCACCCCCCTTAGAGGAGGGATATGTGGTTCTGGTAGGAGACGAGAACCTAAAACAGTTCCCGCCTCCGTCTGAATTTTTGCTTTCGGTTTGGGACCGAAGCCGCGCCGCGCGTCTTGTCTGCTGCAGCATCGTTCTGTGTTGTCTCTGTCTGACTGTGTTTCTGTATTTGTCTGAAAATATGGGCCCGGGCTAGcctgttaccactCCCTTAAGTTTGACCTTAGGTCACTGGAAAGATGTCGAGCGGATCGCTCACAACCAGTCGGTAGATGTCAAGAAGAGACGTTGGGTTACCTTCTGCTCTGCAGAATGGCCAACCTTTAACGTCGGATGGCCGCGAGACGGCACCTTTAACCGAGACCTCATCACCCAGGTTAAGATCAAGGTCTTTTCACCTGGCCCGCATGGACACCCAGACCAGGTccccTACATCGTGACCTGGGAAGCCTTGGCTTTTGACCCCCCTCCCTGGGTCAAGCCCTTTGTACACCCTAAGCCTCCGCCTCCTCTTCCTCCATCCGCCCCGTCTCTCCCCCTTGAACCTCCTCGTTCGACCCCGCCTCGATCCTCCCTTTATCCAGCCCTCACTCCTTCTCTAGGCGCCCCCATATGGCCATATGAGATCTTATATGGGGCACCCCCGCCCCTTGTAAACTTCCCTGACCCTGACATGACAAGAGTTACTAACAGCCCCTCTCTCCAAGCTCACTTACAGGCTCTCTACTTAGTCCAGCACGAAGTCTGGAGACCTCTGGCGGCAGCCTACCAAGAACAACTGGACCGACCGGTGGTACCTCACCCTTACCGAGTCGGCGACACAGTGTGGGTCCGCCGACACCAGACTAAGAACCTAGAACCTCGCTGGAAAGGACCTTACACAGTCCTGCTGACCACCCCCACCGCCCTCAAAGTAGACGGCATCGCAGCTTGGATACACGCCGCCCACGTGAAGGCTGCCGACCCCGGGGGTGGACCATCCTCTAGACTGCC [SEQ ID NO: 124]
Для генетической модификации иммунореактивной клетки также могут использоваться невирусные подходы. Например, молекула нуклеиновой кислоты может быть введена в иммунореактивную клетку путем введения нуклеиновой кислоты в присутствии липофекции (Feigner et al., Proc. Natl. Acad. Sci. U.S.A. 84: 7413, 1987; Ono et al., Neuroscience Letters 17: 259, 1990; Brigham et al., Am. J. Med. Sci. 298: 278, 1989; Staubinger et al., Methods in Enzymology 101: 512, 1983), асиалоорозомукоид-полилизин конъюгирования (Wu et al., Journal of Biological Chemistry 263: 14621, 1988; Wu et al., Journal of Biological Chemistry 264: 16985, 1989) или с помощью микроинъекции в хирургических условиях (Wolff et al., Science 247: 1465, 1990). Другие невирусные способы переноса генов включают трансфекцию in vitro с использованием фосфата кальция, DEAE-декстрана, электропорации и слияние протопластов. Липосомы также могут потенциально применяться для доставки ДНК в клетку. Трансплантация нормальных генов в пораженные ткани субъекта также может осуществляться путем переноса нормальной нуклеиновой кислоты в клетки культивируемого типа ex vivo (например, в аутологичную или гетерологичную первичную клетку или ее потомство), после чего клетку (или ее потомство) вводят в ткань-мишень или вводят системно. Рекомбинантные рецепторы также могут быть созданы или получены при использовании транспозаз или направленных нуклеаз (например, цинк-пальцевых нуклеаз, мегануклеаз или TALE-нуклеаз, CRISPR). Транзиентная экспрессия может быть достигнута с помощью электропорации РНК.
Для экспрессии полипептидной композиции могут использоваться любые методы адресного редактирования генома. В некоторых вариантах осуществления система CRISPR используется для экспрессии полипептидной композиции, раскрытой в настоящем документе. В некоторых вариантах осуществления для экспрессии полипептидной композиции, раскрытой в настоящем документе, используются цинк-пальцевые нуклеазы. В некоторых вариантах осуществления для экспрессии полипептидной композиции, раскрытой в настоящем документе, используется система TALEN.
Система регулярно расположенных кластерами коротких палиндромных повторов (CRISPR) представляет собой инструмент редактирования генома, открытый в прокариотических клетках. При использовании для редактирования генома такая система включает Cas9 (белок, способный модифицировать ДНК, используя crРНК в качестве гида), CRISPR РНК (crРНК, содержит РНК, используемую нуклеазой Cas9 для ее направления к правильному участку ДНК хозяина, вместе с областью, которая связывается с tracrРНК (обычно в форме шпильки), образуя активный комплекс с Cas9), трансактивирующей crРНК (tracrРНК, связывается с crРНК и образует активный комплекс с Cas9) и необязательным участком матрицы репарации ДНК (ДНК, которая направляет процесс клеточной репарации, обеспечивая вставку определенной последовательности ДНК). В CRISPR/Cas9 часто используется плазмида для трансфекции клеток-мишеней. CrРНК нужно создавать для каждого конкретного применения, поскольку она представляет собой последовательность, которую Cas9 использует для идентификации и прямого связывания с ДНК-мишенью в клетке. Матрица репарации, несущая кассету экспрессии CAR, также должна быть сконструирована для каждого конкретного применения, поскольку она должна перекрываться с последовательностями по обе стороны от разреза и кодировать последовательность вставки. Множество crРНК и tracrРНК могут быть упакованы вместе, формируя единую направляющую РНК (sgРНК). Такая sgРНК может быть соединена с геном Cas9 и превращена в плазмиду для трансфекции в клетки.
Цинк-пальцевая нуклеаза (ZFN) представляет собой искусственную рестриктазу, созданную путем объединения ДНК-связывающего домена цинкового пальца с ДНК-расщепляющим доменом. Домен цинкового пальца может быть сконструирован для направленного воздействия на определенные последовательности ДНК, что позволяет цинк-пальцевой нуклеазе направленно воздействовать на требуемые последовательности в геномах. ДНК-связывающие домены отдельных ZFN обычно содержат множество отдельных повторов цинковых пальцев, и каждый может распознавать множество пар оснований. Наиболее распространенный метод создания нового домена цинкового пальца состоит в комбинировании "модулей" цинковых пальцев меньшего размера, которые обладают известной специфичностью. Наиболее распространенным расщепляющим доменом в ZFN является неспецифичный расщепляющий домен из эндонуклеазы рестрикции II типа FokI. При использовании эндогенного аппарата гомологичной рекомбинации (HR) и гомологичной ДНК-матрицы, несущей кассету экспрессии CAR, ZFN можно использовать для вставки кассеты экспрессии CAR в геном. При расщеплении последовательности-мишени ZFN-нуклеазами, аппарат HR ищет гомологию между поврежденной хромосомой и гомологичной ДНК-матрицей, а затем копирует последовательность матрицы между двумя разорванными концами хромосомы, в результате чего гомологичная ДНК-матрица интегрируется в геном.
Нуклеазы на основе подобных активаторам транскрипции эффекторов (TALEN) представляют собой рестриктазы, которые могут быть сконструированы, чтобы разрезать определенные последовательности ДНК. Система TALEN работает практически по тому же принципу, что и ZFN. Их создают путем объединения ДНК-связывающего домена подобных активаторам транскрипции эффекторов с ДНК-расщепляющим доменом. Подобные активаторам транскрипции эффекторы (TALE) состоят из повторяющихся мотивов длиной 33-34 аминокислоты с двумя вариабельными положениями, которые способны надежно распознавать определенные нуклеотиды. При сборке наборов таких TALE-эффекторов ДНК-связывающий домен TALE может быть сконструирован так, чтобы связывать нужную последовательность ДНК и, таким образом, направлять нуклеазу для разреза в определенных местах генома. Экспрессия кДНК для применения в способах терапии полинуклеотидами, может быть направлена с любого подходящего промотора (например, промоторов цитомегаловируса человека (ЦМВ), вируса обезьян 40 (SV40) или металлотионеиона) и может регулироваться любым подходящим регуляторным элементом или интроном млекопитающих (например, структурой энхансер/промотор/интрон фактора элонгации 1α). Например, при необходимости можно использовать энхансеры, которые, как известно, предпочтительно направляют экспрессию генов в конкретных типах клеток, регулируя экспрессию нуклеиновой кислоты. Используемые энхансеры могут включать, без ограничения, энхансеры, которые характеризуются как тканеспецифические или клеточноспецифические энхансеры. В альтернативе, если в качестве терапевтической конструкции используют геномный клон, регуляция может быть опосредована родственными регуляторными последовательностями или, при необходимости, регуляторными последовательностями, полученными из гетерологичного источника, включая любой из промоторов или регуляторных элементов, описанных выше.
Способы доставки средств/систем редактирования генома могут изменяться в зависимости от необходимости. В некоторых вариантах осуществления компоненты выбранного способа редактирования генома доставляют в виде конструкций ДНК в одной или больше плазмидах. В некоторых вариантах осуществления компоненты доставляются при помощи вирусных векторов. Общие способы доставки включают, помимо прочего, электропорацию, микроинъекцию, генную пушку, импалефекцию, гидростатическое давление, непрерывную инфузию, обработку ультразвуком, магнитофекцию, аденоассоциированные вирусы, псевдотипирование вирусных векторов белками оболочки, репликационно-компетентные векторы, цис- и транс-действующие элементы, вирус простого герпеса и химические носители (например, олигонуклеотиды, липоплексы, полимерсомы, полиплексы, дендримеры, неорганические наночастицы и проникающие в клетки пептиды).
5.5. Полипептиды и аналоги
Также раскрытое в настоящем документе изобретение включает полипептид, раскрытый в настоящем документе (например, мезотелин, CD28, CD8, CD3ζ и PD-1 DN, и т.д.), или его фрагменты, которые модифицированы способами, которые улучшают их противоопухолевую активность при экспрессии в иммунореактивной клетке. В настоящем изобретении предложены способы оптимизации аминокислотной последовательности или последовательности нуклеиновой кислоты путем изменения последовательности. Такие изменения могут включать некоторые мутации, делеции, вставки или посттрансляционные модификации. Настоящее изобретение дополнительно включает аналоги любого полипептида, раскрытого в настоящем документе (в том числе, но без ограничения, мезотелин, CD28, CD8, CD3ζ и PD-1 DN). Аналоги могут отличаться от полипептида, раскрытого в настоящем документе, различиями в аминокислотной последовательности и/или посттрансляционными модификациями. Аналоги могут демонстрировать по меньшей мере приблизительно 85%, приблизительно 90%, приблизительно 91%, приблизительно 92%, приблизительно 93%, приблизительно 94%, приблизительно 95%, приблизительно 96%, приблизительно 97%, приблизительно 98%, приблизительно 99% или больше гомологии ко всей или части аминокислотной последовательности согласно раскрытому в настоящем документе изобретению. Длина сравнения последовательности составляет по меньшей мере 5, 10, 15 или 20 аминокислотных остатков, например, по меньшей мере 25, 50 или 75 аминокислотных остатков, или больше 100 аминокислотных остатков. Опять же, в иллюстративном подходе к определению степени идентичности может использоваться программа BLAST с оценкой вероятности от e-3 до e-100, указывающей на близкородственную последовательность. Модификации включают химическую дериватизацию полипептидов in vivo и in vitro, например, ацетилирование, карбоксилирование, фосфорилирование или гликозилирование; такие модификации могут происходить во время синтеза или процессинга полипептида или после обработки выделенными модифицирующими ферментами. Аналоги также могут отличаться от полипептидов изменениями в первичной последовательности. Такие изменения включают генетические варианты, природные и индуцированные (например, полученные в результате случайного мутагенеза под воздействием излучения или этанметилсульфоната, или в результате сайт-специфического мутагенеза, как описано в справочнике Sambrook, Fritsch and Maniatis, Molecular Cloning: A Laboratory Manual (2d ed.), CSH Press, 1989, или Ausubel et al., выше). Также включены циклизованные пептиды, молекулы и аналоги, которые содержат остатки, отличные от L-аминокислот, например, D-аминокислоты или не встречающиеся в природе или синтетические аминокислоты, например, β- или γ-аминокислоты.
В дополнение к полноразмерным полипептидам в изобретении, раскрытом в настоящем документе, также предложены фрагменты любого из полипептидов или пептидных доменов, раскрытых в настоящем документе. При использовании в настоящем описании термин "фрагмент" означает по меньшей мере 5, 10, 13 или 15 аминокислот. В некоторых вариантах осуществления фрагмент включает по меньшей мере 20 последовательных аминокислот, по меньшей мере 30 последовательных аминокислот или по меньшей мере 50 последовательных аминокислот. В некоторых вариантах осуществления фрагмент включает по меньшей мере 60-80, 100, 200, 300 или больше последовательных аминокислот. Фрагменты могут быть получены способами, известными специалистам в данной области, или могут образоваться в результате нормального процессинга белков (например, удаления аминокислот из синтезируемого полипептида, которые не требуются для биологической активности, или удаления аминокислот в результате событий альтернативного сплайсинга мРНК или альтернативного процессинга белка).
Небелковые аналоги имеют химическую структуру, служащую для имитации функциональной активности белка, раскрытого в настоящем документе. Такие аналоги могут проявлять физиологическую активность исходного полипептида. Способы конструирования аналогов хорошо известны в данной области, и синтез аналогов может быть осуществлен согласно таким способам путем такой модификации химических структур, чтобы получаемые в результате аналоги обладали более высокой антинеопластической активностью, чем исходный полипептид, при экспрессии в иммунореактивной клетке. Такие химические модификации включают, без ограничения, замещение альтернативных R-групп и изменение степени насыщения конкретных атомов углерода по сравнению с исходным полипептидом. В некоторых вариантах осуществления белковые аналоги относительно устойчивы к деградации in vivo, что обеспечивает более длительное терапевтическое действие при введении. Анализы для измерения функциональной активности включают, без ограничения, анализы, описанные в Примерах ниже.
В соответствии с раскрытым в настоящем документе изобретением полинуклеотиды, кодирующие внеклеточный антигенсвязывающий домен, который специфично связывается с мезотелином человека (например, scFv, Fab или (Fab)2), CD3ζ, CD8, CD28, 4-1BB, 4-1BBL и IL-12, могут быть модифицированы путем оптимизации кодонов. Оптимизация кодонов может изменять как природные, так и рекомбинантные последовательности генов, с получением максимально возможных уровней продуктивности в любой конкретной системе экспрессии. Факторы, которые влияют на различные стадии экспрессии белка, включают адаптируемость кодонов, структуру мРНК и различные цис-элементы в транскрипции и трансляции. Любые подходящие методы или технологии оптимизации кодонов, которые известны специалистам в данной области, могут использоваться для модификации полинуклеотидов раскрытого в настоящем документе изобретения, в том числе, но без ограничения, OptimumGene™, оптимизация Encor и Blue Heron.
Оптимизация кодонов может быть выполнена на основе четырех различных алгоритмов (например, алгоритмов Blue Heron и Encore). Последовательности, оптимизированные по кодонам, полученные в результате применения всех четырех алгоритмов, смешивают и удаляют все CPG и BamH1 для оптимального клонирования. В некоторых вариантах осуществления кодон-оптимизированная нуклеотидная последовательность приблизительно на 70% гомологична исходной последовательности до оптимизации кодонов. Для получения эффективной экспрессии в иммунореактивной клетке (например, первичных T-клетках человека), кодон-оптимизированную нуклеотидную последовательность лигируют с лидерной последовательностью CD8, например, полинуклеотидом, кодирующим SEQ ID NO: 71. Лидерная последовательность CD8 обеспечивает оптимальное отщепление сигнальной последовательности, предшествующей тяжелой цепи scFv (QVQL). Оптимизация кодонов оптимизирует экспрессию мезотелин-специфичного CAR в иммунореактивной клетке, например первичных человеческих T-клетках множества доноров, с хорошей эффективностью трансдукции. Множество копий CAR векторов в T-клетках множества доноров тестируют на функциональную эффективность, специфичность и чувствительность против множества клеток гемобластных и солидных злокачественных опухолей с различной экспрессией мезотелина. Кодон-оптимизированный мезотелин-направленный CAR с числом копий вектора 1-4 (более конкретно, приблизительно 3-4) обеспечивает очень эффективное цитотоксическое действие против мишеней с высокой экспрессией мезотелина, но при этом с минимальной реактивностью против мишеней с низкой экспрессией мезотелина, т.е. нормальной ткани. Вышеописанные средства генной инженерии при создании специфичного к мезотелину CAR-рецептора, который является реактивным против раковых клеток, экспрессирующих высокие уровни мезотелина, при щадящем воздействии на нормальную ткань, экспрессирующую низкие уровни мезотелина, оптимальны для применения в качестве клинического вектора для терапии рака с гарантией безопасности.
5.6. Фармацевтические композиции и введение
В раскрытом в настоящем документе изобретении предложены композиции, включающие раскрытые в настоящем документе клетки (например, как раскрыто в Разделе 5.3). Количество клеток, содержащихся в композициях, может изменяться в зависимости от цели применения композиции, и/или размера, возраста, пола, веса и состояния субъекта, который получает композицию. В некоторых вариантах осуществления композиция включает от приблизительно 104 до приблизительно 1010, от приблизительно 104 до приблизительно 106, от приблизительно 105 до приблизительно 106, от приблизительно 105 до приблизительно 107, от приблизительно 105 до приблизительно 109 или от приблизительно 106 до приблизительно 108 раскрытых в настоящем документе иммунореактивных клеток. В некоторых вариантах осуществления композиция включает по меньшей мере приблизительно 1×105, по меньшей мере приблизительно 5×105, по меньшей мере приблизительно 1×106, по меньшей мере приблизительно 1×107, по меньшей мере приблизительно 1×108 раскрытых в настоящем документе иммунореактивных клеток. В некоторых вариантах осуществления композиция включает приблизительно 1×105 раскрытых в настоящем документе клеток.
Композиции, включающие раскрытые в настоящем документе иммунореактивные клетки, могут быть предоставлены системно или непосредственно субъекту для индукции и/или усиления иммунного ответа на антиген, и/или лечения и/или предотвращения опухоли, патогенной инфекции или инфекционного заболевания, воспалительного заболевания или отторжения трансплантата. В некоторых вариантах осуществления раскрытые в настоящем документе иммунореактивные клетки или включающие их композиции непосредственно вводят в орган, представляющий интерес (например, орган, пораженный неоплазией). Также раскрытые в настоящем документе иммунореактивные клетки или включающие их композиции предоставляют опосредованно в орган, представляющий интерес, например, при введении в сердечно-сосудистую систему (например, сосудистая сеть опухоли). Средства, вызывающие экспансию и дифференцировку, можно предоставить до, во время или после введения клеток или композиций для увеличения продукции T-клеток, NK-клеток или CTL-клеток in vitro или in vivo.
Раскрытые в настоящем документе иммунореактивные клетки могут вводить в любой физиологически приемлемой среде, обычно внутрисосудистым путем, хотя их можно также вводить в кость или другой удобный участок, где клетки могут найти подходящее место для регенерации и дифференцировки (например, тимус). Обычно будет вводить по меньшей мере приблизительно 1×105 клеток, достигая в конечном счете приблизительно 1×1010 или больше. Раскрытые в настоящем документе иммунореактивные клетки могут включать очищенную популяцию клеток. Специалисты в данной области с легкостью сумеют определить процент раскрытых в настоящем документе иммунореактивных клеток в популяции при использовании различных известных методов, таких как сортировка клеток с активированной флуоресценцией (FACS). Подходящие границы дипазонов чистоты в популяциях, включающих раскрытые в настоящем документе иммунореактивные клетки, составляют от приблизительно 50% до приблизительно 55%, от приблизительно 5% до приблизительно 60% и от приблизительно 65% до приблизительно 70%. В некоторых вариантах осуществления чистота составляет от приблизительно 70% до приблизительно 75%, от приблизительно 75% до приблизительно 80% или от приблизительно 80% до приблизительно 85%. В некоторых вариантах осуществления чистота составляет от приблизительно 85% до приблизительно 90%, от приблизительно 90% до приблизительно 95% и от приблизительно 95% до приблизительно 100%. Дозы могут быть с легкостью скорректированы специалистами (например, уменьшение чистоты может потребовать увеличения дозы). Клетки могут вводить путем инъекции, с помощью катетера и т.п.
Раскрытые в настоящем документе композиции могут быть фармацевтическими композициями, включающими раскрытые в настоящем документе иммунореактивные клетки или их предшественники и фармацевтически приемлемый носитель. Введение может быть аутологичным или гетерологичным. Например, иммунореактивные клетки или предшественники могут быть получены у одного субъекта и введены тому же субъекту или другому совместимому субъекту. Полученные из периферической крови иммунореактивные клетки или их потомство (например, полученные in vivo, ex vivo или in vitro) может вводить путем локализованной инъекции, в том числе путем введения через катетер, путем системной инъекции, локализованной инъекции, внутривенной инъекции или парентерального введения. При введении терапевтической композиции согласно настоящему изобретению (например, фармацевтической композиции, включающей раскрытую в настоящем документе иммунореактивную клетку), она может быть приготовлена в стандартной форме для инъекций (раствора, суспензии, эмульсии).
5.7. Составы
Композиции, включающие раскрытые в настоящем документе иммунореактивные клетки, могут быть удобно представлены в виде стерильных жидких препаратов, например, изотоничных водных растворов, суспензий, эмульсий, дисперсий или вязких композиций, которые могут быть забуферены до выбранного pH. Жидкие препараты обычно легче приготавливать, чем гели, другие вязкие композиции и твердые композиции. Кроме того, жидкие композиции немного более удобны для введения, в особенности путем инъекции. С другой стороны, вязкие композиции могут быть приготовлены в соответствующем диапазоне вязкости, чтобы обеспечить более длительные периоды контакта с конкретными тканями. Жидкие и вязкие композиции могут включать носители, которые могут быть растворителем или дисперсионной средой, содержащей воду, солевой раствор, фосфатно-солевой буфер, многоатомный спирт (например, глицерин, пропиленгликоль, жидкий полиэтиленгликоль и т.п.) и их подходящие смеси.
Стерильные растворы для инъекций могут быть приготовлены путем включения генетически модифицированных иммунореактивных клеток в требуемом количестве подходящего растворителя, с разными количествами других ингредиентов при необходимости. Такие композиции могут присутствовать в смеси с подходящим носителем, разбавителем или вспомогательным веществом, таким как стерильная вода, физиологический раствор, глюкоза, декстроза и т.п. Композиции также могут быть лиофилизированными. Композиции могут содержать вспомогательные вещества, такие как увлажняющие, диспергирующие или эмульгирующие вещества (например, метилцеллюлозу), pH-буферные вещества, желатинизирующие или повышающие вязкость добавки, консерванты, корригенты, красители и т.п., в зависимости от требуемого пути введения и препарата. В стандартных текстах, таких как справочник "REMINGTON'S PHARMACEUTICAL SCIENCE", 17th edition, 1985, включенный в настоящее описание посредством отсылки, можно найти сведения по приготовлению подходящих препаратов без излишнего экспериментирования.
Могут быть добавлены различные добавки, которые повышают стабильность и стерильность композиций, включая противомикробные консерванты, антиоксиданты, хелатообразующие и буферные вещества. Предотвращение действия микроорганизмов может быть обеспечено различными противобактериальными и противогрибковыми средствами, например, парабенами, хлорбутанолом, фенолом, сорбиновой кислотой и т.п. Пролонгированное всасывание инъекционной фармацевтической формы можно обеспечивать при использовании веществ, задерживающих всасывание, например, моностеарата алюминия и желатина. Однако согласно раскрытому в настоящем документе изобретению любая используемая среда, разбавитель или добавка должны быть совместимыми с генетически модифицированными иммунореактивными клетками или их предшественниками.
Композиции могут быть изотоническими, т.е. они могут иметь такое же осмотическое давление, как кровь и слезная жидкость. Требуемая изотоничность композиций может быть достигнута при использовании хлорида натрия или других фармацевтически приемлемых веществ, таких как декстроза, борная кислота, тартрат натрия, пропиленгликоль или другие неорганические или органические растворенные вещества. Хлорид натрия является особенно предпочтительным в случае буферов, содержащих ионы натрия.
Вязкость композиции при необходимости можно поддерживать на выбранном уровне при использовании фармацевтически приемлемого загустителя. Например, метилцеллюлоза легко и экономически доступна и с ней легко работать. Другие подходящие загустители включают, например, ксантановую камедь, карбоксиметилцеллюлозу, гидроксипропилцеллюлозу, карбомер и т.п. Концентрация загустителя может зависеть от выбранного средства. Важным моментом является использование такого количества, которое позволит получить выбранную вязкость. Очевидно, выбор подходящих носителей и других добавок будет зависеть от точного пути введения и природы конкретной лекарственной формы, например, жидкой лекарственной формы (например, независимо от того, требуется ли изготавливать композицию в форме раствора, суспензии, геля или другой жидкой формы, такой как форма замедленного высвобождения или форма, заполненная жидкостью).
Вводимое количество клеток будет изменяться в зависимости от субъекта, подвергаемого лечению. В некоторых вариантах осуществления субъекту-человеку вводят от приблизительно 104 до приблизительно 1010, от приблизительно 105 до приблизительно 109, от приблизительно 104 до приблизительно 106, от приблизительно 105 до приблизительно 106, от приблизительно 105 до приблизительно 107 или от приблизительно 106 до приблизительно 108 раскрытых в настоящем документе иммунореактивных клеток. Более эффективные клетки могут вводить в еще меньшем количестве. В некоторых вариантах осуществления субъекту-человеку вводят по меньшей мере приблизительно 1×105, по меньшей мере приблизительно 1×106, по меньшей мере приблизительно 1×107, 1×108, по меньшей мере приблизительно 2×108, по меньшей мере приблизительно 3×108, по меньшей мере приблизительно 4×108 или по меньшей мере приблизительно 5×108 раскрытых в настоящем документе иммунореактивных клеток. Точное определение того, что считается эффективной дозой, может быть основано на факторах, исндивидуальных для каждого субъекта, включая размер, возраст, пол, вес и состояние конкретного субъекта. Дозы могут быть с легкостью установлены специалистами в данной области из настоящего описания и доступных знаний. В некоторых вариантах осуществления субъекту вводят приблизительно 1×105 клеток, раскрытых в настоящем документе.
Специалист в данной области легко сумеет определить количество клеток и необязательных добавок, наполнителей и/или носителя в композициях и вводимых в способах. Как правило, любые добавки (в дополнение к активной клетке(ам) и/или средству(ам)) присутствуют в количестве от 0,001 до 50% (по весу) раствора в фосфатно-солевом буфере, и активный ингредиент присутствует в количестве порядка микрограммов или миллиграммов, таком как от приблизительно 0,0001 до приблизительно 5 вес. %, предпочтительно от приблизительно 0,0001 до приблизительно 1 вес. %, еще более предпочтительно от приблизительно 0,0001 до приблизительно 0,05 вес. % или от приблизительно 0,001 до приблизительно 20 вес. %, от приблизительно 0,01 до приблизительно 10 вес. % или от приблизительно 0,05 до приблизительно 5 вес. %. В случае любой композиции, вводимой животному или человеку, могут быть определены следующие показатели: токсичность, например, при определении летальной дозы (LD) и LD50 в подходящей модели на животных, например, грызунах, таких как мыши; и доза композиции(й), концентрация компонентов в ней и время введения композиции(й), которые вызывают соответствующий ответ. Такие определения не требуют проведения излишних экспериментов исходя из знаний, доступных специалисту в данной области, приведенных в настоящем описании, а также цитируемых в нем документах. Кроме того, время последовательных введений может быть установлено без проведения излишних экспериментов.
5.8. Способы лечения
Иммунореактивные клетки и включающие их композиции согласно раскрытому в настоящем документе изобретению могут применяться для лечения и/или предупреждения опухоли, вызванной патогеном инфекции, инфекционного заболевания, воспалительного заболевания или отторжения трансплантата. Такие иммунореактивные клетки могут вводить субъекту (например, субъекту человеку), нуждающемуся в лечении или предупреждении солидной опухоли (например, мезотелиомы, рака легкого, рака поджелудочной железы, рака яичника, рака молочной железы, рака толстой кишки, плевральной опухоли, глиобластомы, рака пищевода, рака желудка, синовиальной саркомы, карциномы тимуса, карциномы эндометрия, рака желудка и/или холангиокарциномы). В некоторых вариантах осуществления иммунореактивной клеткой является T-клетка. T-клетка может быть CD4+ T-клеткой или CD8+ T-клеткой. В некоторых вариантах осуществления T-клетка является CD4+ T-клеткой.
В настоящем изобретении предложены способы индукции и/или усиления иммунного ответа у нуждающегося в этом субъекта. Раскрытые в настоящем документе иммунореактивные клетки и включающие их композиции могут применяться для лечения и/или предупреждения неоплазии у субъекта. Раскрытые в настоящем документе иммунореактивные клетки и включающие их композиции могут применяться для продления выживаемости субъекта, страдающего от неоплазии. Раскрытые в настоящем документе иммунореактивные клетки и включающие их композиции могут также применяться для лечения и/или предупреждения вызванной патогеном инфекции или другого инфекционного заболевания у субъекта, такого как субъект-человек с ослабленным иммунитетом. Такие способы включают введение раскрытых в настоящем документе иммунореактивных клеток или включающей их композиции (например, фармацевтической композиции) в количестве, эффективном для достижения требуемого эффекта, будь то облегчение существующего состояния или предотвращение рецидива. В случае лечения вводимое количество является количеством, эффективным для достижения требуемого эффекта. Эффективное количество может быть предоставлено в одном или серии введений. Эффективное количество может быть предоставлено в виде болюса или непрерывной перфузии.
"Эффективное количество" (или "терапевтически эффективное количество") является количеством, достаточным для получения полезного или требуемого клинического результата при лечении. Эффективное количество могут вводить субъекту в виде одной или больше доз. Что касается лечения, то эффективное количество является количеством, которое является достаточным для облегчения, ослабления, стабилизации, реверсии или замедления прогрессирования заболевания, или иного уменьшения патологических последствий заболевания. Эффективное количество обычно определяет лечащий врач в индивидуальном порядке, и это находится в рамках компетенции специалиста в данной области. Обычно при определении соответствующей дозы учитывают несколько факторов с целью достижения эффективного количества. Такие факторы включают возраст, пол и вес субъекта, состояние, подвергаемое лечению, тяжесть состояния, а также форму и эффективную концентрацию вводимых иммунореактивных клеток.
В случае адоптивной иммунотерапии с применением антигенспецифичных T-клеток обычно производят инфузию доз клеток в диапазоне от приблизительно 106 до приблизительно 1010 (например, 109). Однако благодаря высокой эффективности раскрытых в настоящем документе полипептидных композиций для достижения необходимых эффектов требуется меньшее количество раскрытых в настоящем документе клеток. Например, приблизительно 1×105 клеток, раскрытых в настоящем документе, достаточно для достижения необходимых эффектов.
После введения иммунореактивных клеток субъекту и последующей дифференцировки индуцируют иммунореактивные клетки, которые специфично направлены против конкретного антигена (например, мезотелина человека). "Индукция" T-клеток может включать инактивацию антигенспецифичных T-клеток, например, в результате удаления или анергии. Инактивация особенно применима для установления и восстановления толерантности, например, при аутоиммунных нарушениях. Иммунореактивные клетки согласно раскрытому в настоящем документе изобретению можно вводить любыми способами, известными в данной области, включая, без ограничения перечисленными, плевральное введение, внутривенное введение, подкожное введение, внутриузловое введение, внутриопухолевое введение, интратекальное введение, внутриплевральное введение, внутрибрюшинное введение и непосредственное введение в тимус. В некоторых вариантах осуществления иммунореактивные клетки и/или включающие их композиции вводят плеврально нуждающемуся субъекту. В некоторых вариантах осуществления иммунореактивные клетки и/или включающие их композиции вводят внутриплеврально нуждающемуся субъекту.
В настоящем изобретении предложены различные способы применения иммунореактивных клеток (например, T-клеток). Например, в настоящем изобретении предложены способы снижения опухолевой нагрузки у субъекта. В некоторых вариантах осуществления способ снижения опухолевой нагрузки включает введение эффективного количества раскрытых в настоящем документе иммунореактивных клеток или включающей их композиции субъекту. Раскрытая в настоящем документе иммунореактивная клетка может снижать количество опухолевых клеток, уменьшать размер опухоли и/или устранять опухоль у субъекта. Опухоль может быть солидной опухолью. Неограничивающие примеры солидной опухоли включают мезотелиому, рак легкого, рак поджелудочной железы, рак яичника, рак молочной железы, рак толстой кишки, плевральную опухоль, глиобластому, рак пищевода, рак желудка, синовиальную саркому, карциному тимуса, карциному эндометрия, рак желудка и холангиокарциному.
В настоящем изобретении также предложены способы увеличения или продления выживаемости субъекта, имеющего неоплазию. В некоторых вариантах осуществления способ увеличения или продления выживаемости субъекта, имеющего неоплазию, включает введение эффективного количества раскрытых в настоящем документе иммунореактивных клеток или включающей их композиции субъекту. Способ может вызвать снижение или устранение опухолевой нагрузки у субъекта. Кроме того, в настоящем изобретении предложены способы усиления иммунного ответа у субъекта, включающие введение раскрытой в настоящем документе иммунореактивной клетки или включающей ее композиции субъекту. В настоящем изобретении также предложены способы лечения и/или предупреждения опухоли у субъекта, включающие введение раскрытой в настоящем документе иммунореактивной клетки или включающей ее композиции субъекту.
В некоторых вариантах осуществления неоплазия является солидной опухолью. Неоплазия может быть первичной опухолью или первичным раком. Кроме того, неоплазия может иметь метастатический статус.
Злокачественные опухоли, рост которых может быть замедлен с применением иммунореактивных клеток согласно раскрытому в настоящем документе изобретению, включают злокачественные опухоли, типично чувствительные к иммунотерапии. Неограничивающие примеры злокачественных опухолей для лечения включают мезотелиому, рак легкого (например, немелкоклеточный рак легкого), рак поджелудочной железы, рак яичника, рак молочной железы (например, метастатический рак молочной железы, метастатический трижды негативный рак молочной железы), рак толстой кишки, плевральную опухоль, глиобластому, рак пищевода, рак желудка, синовиальную саркому, карциному тимуса, карциному эндометрия, рак желудка, холангиокарциному, рак шейки матки и рак слюнной железы. Кроме того, раскрытое в настоящем документе изобретение включает рефрактерные или рецидивирующие злокачественные опухоли, рост которых может быть замедлен с применением иммунореактивных клеток согласно раскрытому в настоящем документе изобретению.
Примеры других неоплазий или злокачественных опухолей, которые можно лечить с применением способов согласно раскрытому в настоящем документе изобретению, включают рак костей, рак кишечника, рак печени, рак кожи, рак головы или шеи, меланому (кожную или внутриглазную злокачественную меланому), рак почки, (например, светлоклеточную карциному), рак горла, рак предстательной железы (например, гормонорезистентную аденокарциному предстательной железы), гемобластозы (например, лейкозы, лимфомы и миеломы), рак матки, рак прямой кишки, рак анальной области, рак мочевого пузыря, рак головного мозга, рак желудка, рак яичка, карциному фаллопиевой трубы, карциному эндометрия, карциному шейки матки, карциному влагалища, карциному вульвы, лейкозы (например, острый лейкоз, острый лимфолейкоз, острый миелоцитарный лейкоз, острый миелобластный лейкоз, острый промиелоцитарный лейкоз, острый миеломоноцитарный лейкоз, острый моноцитарный лейкоз, острый эритролейкоз, хронический лейкоз, хронический миелоцитарный лейкоз, хронический лимфоцитарный лейкоз), истинную полицитемию, лимфому (болезнь Ходжкина, неходжкинскую лимфому), рак тонкой кишки, рак эндокринной системы, рак щитовидной железы, рак паращитовидной железы, рак надпочечника, саркому мягких тканей, рак уретры, рак полового члена, солидные опухоли у детей, лимфоцитарную лимфому, рак мочевого пузыря, рак почки или мочеточника, рак почечной лоханки, неоплазию центральной нервной системы (ЦНС), первичную лимфому ЦНС, опухолевый ангиогенез, опухоль оси позвоночника, глиому ствола головного мозга, аденому гипофиза, саркому Капоши, эпидермоидный рак, плоскоклеточный рак, T-клеточную лимфому, онкологические заболевания, вызванные факторами внешней среды, в том числе вызванные асбестом, включая макроглобулинемию Вальденстрема, болезнь тяжелых цепей и солидные опухоли, такие как саркомы и карциномы (например, фибросаркому, миксосаркому, липосаркому, хондросаркому, остеогенную саркому, хордому, ангиосаркому, эндотелиосаркому, лимфангиосаркому, лимфангиоэндотелиосаркому, синовиому, мезотелиому, опухоль Юинга, лейомиосаркому, рабдомиосаркому, плоскоклеточную карциному, базально-клеточную карциному, аденокарциному, карциному потовых желез, карциному сальных желез, папиллярную карциному, папиллярные аденокарциномы, цистаденокарциному, медуллярную карциному, бронхогенную карциному, гепатому, карциному желчных протоков, хориокарциному, семиному, эмбриональную карциному, опухоль Вильмса, рак шейки матки, рак слюнной железы, рак матки, рак яичка, карциному мочевого пузыря, эпителиальную карциному, глиому, астроцитому, медуллобластому, краниофарингиома, эпендимома, пинеалома, гемангиобластома, невриному слухового нерва, олигоденроглиому, шванному, менингиому, меланому, нейробластому и ретинобластому).
Кроме того, в настоящем изобретении предложены способы увеличения продукции иммуноактивирующего цитокина в ответ на раковую клетку или патоген у субъекта. В некоторых вариантах осуществления способ включает введение раскрытой в настоящем документе иммунореактивной клетки или включающей ее композиции субъекту. Иммуноактивирующим цитокином может быть гранулоцитарно-макрофагальный колониестимулирующий фактор (ГМ-КСФ), IFN-α, IFN-β, IFN-γ, ФНО-α, IL-2, IL-3, IL-6, IL-11, IL-7, IL-12, IL-15, IL-21, регуляторный фактор интерферона 7 (IRF7) и их комбинации. В некоторых вариантах осуществления иммунореактивные клетки увеличивают продукцию ГМ-КСФ, IFN-γ и/или ФНО-α.
В изобретении, раскрытом в настоящем документе, предложены терапии, которые особенно полезны для лечения солидных опухолей (например, мезотелиомы, рака легкого, рака поджелудочной железы, рака яичника, рака молочной железы, рака толстой кишки, плевральной опухоли, глиобластомы, рака пищевода, рака желудка, синовиальной саркомы, карциномы тимуса, карциномы эндометрия, рака желудка и холангиокарциномы). Солидные опухоли могут быть первичными опухолями или опухолями в метастатическом состоянии. Некоторые солидные опухоли представляют собой гетерогенные MSLN-экспрессирующие опухоли, например, рак молочной железы (например, ТНРМЖ), рак легкого, рак яичника, рак поджелудочной железы, рак пищевода, рак толстой кишки, рак желудка и злокачественную мезотелиому плевры (MPM). Гетерогенные MSLN-экспрессирующие клетки (например, опухолевые клетки), представляют собой популяцию клеток, включающую клетки с низким уровнем экспрессии MSLN и клетки с высоким уровнем экспрессии MSLN. Раскрытая в настоящем документе иммунореактивная клетка может демонстрировать повышенную цитотоксичность и противоопухолевую активность в отношении клеток с низкой экспрессией MSLN (например, приблизительно 2000 или меньше, приблизительно 1000 или меньше, приблизительно 900 или меньше, приблизительно 800 или меньше, приблизительно 700 или меньше, приблизительно 600 или меньше, приблизительно 500 или меньше, приблизительно 400 или меньше, приблизительно 300 или меньше, приблизительно 200 или меньше, или приблизительно 100 или меньше связывающих сайтов MSLN/клетка) в присутствии клеток с высоким уровнем экспрессии MSLN. В некоторых вариантах осуществления даже в присутствии клеток с высокой экспрессией MSLN иммунореактивные клетки не демонстрируют повышенную цитотоксичность или неспецифический цитолиз MSLN-отрицательных клеток. Таким образом, иммунореактивная клетка может демонстрировать повышенную цитотоксичность и противоопухолевую активность в отношении клеток с низким уровнем экспрессии MSLN в присутствии клеток с высоким уровнем экспрессии MSLN, при этом сохраняя безопасность для MSLN-отрицательных клеток.
Кроме того, в изобретении, раскрытом в настоящем документе, предложены способы лечения субъектов с вызванной патогеном инфекцией (например, вирусной инфекцией, бактериальной инфекцией, грибковой инфекцией, паразитарной инфекцией или протозойной инфекцией). Раскрытое в настоящем документе изобретение особенно полезно для усиления иммунного ответа у субъекта с иммунодефицитом. Примеры вирусных инфекций, восприимчивых к лечению с применением способа изобретения, включают, без ограничения перечисленными, инфекции, вызванные цитомегаловирусом (ЦМВ), вирусом Эпштейна-Барр (ВЭБ), вирусом иммунодефицита человека (ВИЧ) и вирусом гриппа. Таким образом, в настоящем изобретении предложен способ лечения или предупреждения вызванной патогеном инфекции у субъекта, включающий введение эффективного количества раскрытых в настоящем документе иммунореактивных клеток или включающей их композиции.
В соответствии с раскрытым в настоящем документе изобретением различные вышеописанные способы могут включать введение по меньшей мере одного иммуномодулирующего средства. Неограничивающие примеры иммуномодулирующих средств включают иммуностимулирующие средства, блокаторы иммунных контрольных точек, радиотерапевтические средства и химиотерапевтические средства. В некоторых вариантах осуществления иммуномодулирующее средство является иммуностимулирующим средством. Неограничивающие примеры иммуностимулирующих средств включают IL-12 и агонистические костимулирующие моноклональные антитела. В некоторых вариантах осуществления иммуностимулирующим средством является IL-12. В некоторых вариантах осуществления раскрытые в настоящем документе иммунореактивные клетки или включающая их композиция в комбинации с антителом против IL-12 могут применяться для лечения рака молочной железы (РМЖ), например, метастатического трижды-негативного рака молочной железы (ТНРМЖ). Неограничивающие примеры агонистических костимулирующих моноклональных антител включают антитела против 4-1BB, антитела против OX40 и антитела против ICOS. В некоторых вариантах осуществления агонистическое костимулирующее моноклональное антитело является антителом против 4-1BB.
В некоторых вариантах осуществления раскрытые в настоящем документе иммунореактивные клетки или включающая их композиция не только могут демонстрировать опухоленаправленную адоптивную T-клеточную терапию, но могут также усиливать функцию T-клеток посредством создания улучшенных антигенных рецепторов и посредством вмешательства в микроокружение хозяина путем иммуномодуляции с использованием IL-12. Из всех иммунотерапевтических подходов, IL-12, многофункциональный цитокин, считается одним из наиболее многообещающих подходов для лечения РМЖ (Boggio, K., et al., Cancer Res 60, 359-364 (2000); Czerniecki, BJ et al., Cancer Res 67, 1842-1852 (2007); Nanni, P. et al., J Exp Med 194, 1195-1205 (2001)). IL-12 считается главным регулятором адаптивного клеточного иммунитета 1 типа, важнейшего пути, участвующего в противоопухолевых ответах (Del Vecchio, M., et al., Clin Cancer Res 13, 4677-4685 (2007)). IL-12 модулирует противоопухолевые ответы на различных уровнях, включая поляризацию CD4 T-клеток в направлении Th1 фенотипа (Wesa, et al., J Immunother 30, 75-82 (2007)), усиление эффекторных функций T и NK-клеток (Curtsinger et al., J Exp Med 197, 1141-1151 (2003)), ремоделирование врожденного иммунного ответа (Chmielewski et al., Cancer Res 71, 5697-5706 (2011)) и регуляцию ангиогенеза опухоли (Voest et al., J Natl Cancer Inst 87, 581-586 (1995)). Иммуномодулирующие и антиангиогенные функции IL-12 предоставили основу для применения этого цитокина в комбинации с иммунореактивной клеткой раскрытого в настоящем документе изобретения для лечения рака, например, РМЖ (например, ТНРМЖ). В 148 клинических исследованиях, включающих введение IL-12 пациентам с онкологическими заболеваниями (о 36 из которых сообщали недавно), успешные исследования фазы II внутрибрюшинного (Lenzi et al. Clin.Cancer Res. 8, 3686-3695 (2002)) или подкожного (Mahviet et al. Cancer Gene Ther. 14, 717-723 (2007); Kang et al., Hum. Gen Ther. 12, 671-684 (2001)). введения IL-12 показали, что паракринная секреция IL-12, генерируемая переносом гена, может индуцировать иммунитет против опухоли локально и в удаленном участке. Хотя в нескольких исследованиях задокументировали противоопухолевую эффективность IL-12 в доклинических моделях рака молочной железы (РМЖ) (Boggio et al. Cancer Res 60, 359-364 (2000); Nanniet al. J Exp Med 194, 1195-1205 (2001)), значимое токсическое действие, возникающее в результате введения рекомбинантного человеческого IL-12, наблюдаемое в нескольких клинических исследованиях с распространенными злокачественными опухолями, препятствует его клиническому применению. Для преодоления этого ограничения некоторыми группами было продемонстрировано, что внутриопухолевая доставка IL-12 с применением аденовирусных векторов вызывает регрессию опухоли и активацию T-клеток в доклинических моделях РМЖ (Gyorffy et al. J Immunol 166, 6212-6217 (2001); Bramson et al., Hum Gene Ther 7, 1995-2002 (1996)). Позже Sabel et al. использовали микросферы полимолочной кислоты для высвобождения IL-12 в опухоль и обнаружили, что противоопухолевый ответ опосредован в первую очередь NK-клетками (Sabel et al. Breast Cancer Res Treat 122, 325-336 (2010)). В других исследованиях использовали мезенхимальные стромальные клетки для локальной доставки IL-12 в РМЖ у мышей (Eliopoulos et al. Cancer Res 68, 4810-4818 (2008)). Исследование I фазы паклитаксела и трастузумаба в комбинации с IL-12 у пациентов с HER2/neu-экспрессирующими злокачественными опухолями показало впечатляющую синергию между IL-12 и трастузумабом в отношении стимуляции секреции цитокинов NK-клетками (Bekaii-Saabet al. Cancer Therapeutics 8, 2983-2991 (2009)). Следовательно, IL-12 может иметь большие перспективы в качестве противоопухолевого средства, и его применение в качестве костимулятора в подходе адоптивной T-клеточной терапии вполне оправдано.
В некоторых вариантах осуществления иммуномодулирующее средство является блокатором иммунной контрольной точки. Неограничивающие примеры блокаторов иммунной контрольной точки включает антитела против PD-L1, антитела против CTLA-4, антитела против PD-1, антитела против LAG3, антитела против B7-H3 и антитела против TIM3. В некоторых вариантах осуществления блокатором иммунной контрольной точки является антитело против PD-L1. В некоторых вариантах осуществления иммунореактивная клетка согласно раскрытому в настоящем документе изобретению или включающей ее композиции в комбинации с антителом против PD-L1, может применяться для лечения рака молочной железы (РМЖ), например, ТНРМЖ.
Лиганд белка программируемой клеточной смерти 1 (PD-L1/B7-H4/CD274) представляет собой ингибирующий сигнал, обычно экспрессируемый в активно воспаленных тканях, служащий петлей отрицательной обратной связи для ограничения активации T-клеток. Экспрессия PD-L1 обычно отсутствует в невоспаленных здоровых тканях (включая молочную железу (Dong et al. Nature Medicine 8, 793-800 (2002))), но вместо этого наиболее распространена в раковых тканях, особенно в раковых тканях с воспалительным инфильтратом (Spranger et al. Science translational medicine 5, 200ra116 (2013)). Такая связь с воспалением, вероятно, связана с апрегуляцией PD-L1 при воздействии на опухолевые клетки секретируемых T-клетками цитокинов, вырабатываемых при активации T-клеток. Этот профиль экспрессии наблюдается в РМЖ, при этом 50-75% образцов РМЖ характеризуются положительным окрашиванием на PD-L1, и экспрессия в значительной степени связана с тяжелым лимфоцитарным инфильтратом (Brown et al. Journal of Immunology 170, 1257-1266 (2003); Ghebeh et al. Neoplasia 8, 190-198 (2006); Ghebeh et al. BMC Cancer 8, 57 (2008)). РМЖ-инфильтрирующие T-клетки также экспрессировали PD-L1 у 54% пациентов (Ghebeh et al., BCM Cancer 8, 57 (2008)). РМЖ также может изначально экспрессировать PD-L1, вторично по отношению к онкогенной сигнализации. Активация пути PI(3)K приводит к апрегуляции белка PD-L1 в клетках РМЖ, при этом активация PI(3)K в опухолях пациентов в значительной степени коррелирует с экспрессией PD-L1 (Crane et al. Oncogen 28, 306-312 (2009)). Экспрессия PD-1 активированными T-клетками в пространственном и временном отношении связывает лиганд с экспрессией рецептора в иммуносупрессивном микроокружении опухоли (TME). Экспрессия PD-L1 в тканях РМЖ позволяет предположить, что он является иммунотерапевтической мишенью у таких пациентов. Эффективность блокады PD-L1/PD-1 в различных доклинических моделях рака (включая молочную железу (Ge et al. Cancer letter 336, 253-259 (2013))) проложила путь к иследованиям I фазы с применением PD-L1- или PD-1-специфичных антител у пациентов с запущенным раком. Исследование I фазы (с применением антитела к PD-1) продемонстрировало эффективность только у PD-L1+ пациентов (Topalian et al., New England Journal of Medicine 366, 2443-2454 (2012)). Генетически модифицированные T-клетки предоставляют уникальные преимущества для преодоления коингибирующих контрольных точек и типичного отсутствия костимуляции, обнаруживаемого в TME. CAR-экспрессирующие T-клетки фактически созданы для оптимизации их костимулирующих требований для поддержки экспансии, выживания и функции T-клеток.
В некоторых вариантах осуществления иммуномодулирующее средство является радиотерапевтическим средством. Локализованная, созданная при воздействии радиации иммунологическая среда не только может обеспечить предварительные условия для улучшения приживления направленных T-клеток в опухоли (исключая тем самым необходимость в применении схем системной лимфодеплеции), но также и иммунологические ответы, возникающие в результате комбинации лучевой терапии и адаптивной T-клеточной терапии, также повышают абскопальную противоопухолевую эффективность. В радиационно-резистентных опухолях костимулирующая сигнализация 4-1BB в CAR T-клетках может преодолевать иммуноингибирование. В некоторых вариантах осуществления иммуномодулирующее средство представляет собой химиотерапевтические средства, включающие, без ограничения, цисплатин. Индуцированная цисплатином секреция хемокинов и цитокинов может способствовать MSLN-направленным и эндогенным T-клеточным ответам.
Исследования показали, что пациенты с аденокарциномой легкого (LAC) и злокачественной мезотелиомой плевры (MPM), у которых присутствует высокий уровень цитотоксических инфильтрирующих опухоль лимфоцитов (cTIL) и низкие уровни регуляторных T-клеток (Treg), имеют лучший прогноз и более длительную выживаемость без прогрессирования (Servais, et al., Clin Cancer Res (May 1, 2012); 18: 2478-2489; Kachala et al., Clin Cancer Res (2013); 20(4); 1020-8). Адоптивная T-клеточная терапия с применением MSLN-направленного CAR может использоваться для стимуляции cTIL при LAC и MPM. Servais (2012) и Kachala (2013) сообщали, что MSLN повышенно экспрессируется и способствует агрессивности LAC и MPM, оправдывая выбор MSLN в качестве мишени CAR T-клеточной терапии. Более высокий процент TIL после терапии цисплатином и лучевой терапии был ассоциирован с улучшенными результатами лечения как в моделях на мышах, так и у пациентов.
Индуцированная цисплатином и лучевой терапией опухолевая и абскопальная иммуномодуляция может обеспечивать прекондиционирование, необходимое для лучшего приживления адоптивно перенесенных T-клеток; стратегии T-клеточной костимуляции для использования опухолевой и стромальной иммуномодуляции могут усиливать противоопухолевую эффективность как эндогенных, так и адоптивно перенесенных T-клеток.
Кроме того, различные вышеописанные способы применения иммунореактивных клеток (например, T-клеток), экспрессирующих мезотелин-специфичный CAR, например, для лечения рака у субъекта или для снижения опухолевой нагрузки у субъекта, можно комбинировать с модуляцией антигена раковых клеток. Иммунореактивные клетки (например, T-клетки), экспрессирующие мезотелин-специфичный CAR, могут направленно взаимодействовать и уничтожать MSLN, экспрессируемый на мембране (называемый "MSLN клеточной мембраны") опухолевой или раковой клетки, но не цитоплазматический MSLN. Некоторые опухоли или раковые опухоли (например, рак легкого и мезотелиома) имеют низкое содержание MSLN клеточной мембраны, но высокое содержание цитоплазматического MSLN. Модуляция антигена раковой клетки может повышать экспрессию MSLN клеточной мембраны в опухолевой или раковой клетке, что может сделать опухолевую или раковую клетку более вероятной мишенью CAR-экспрессирующей иммунореактивной клетки, и, таким образом, более восприимчивой к цитолизу, вызванному иммунореактивной клеткой. В некоторых вариантах осуществления модуляцией антигена раковой клетки является радиация.
В иммунореактивные клетки (например, T-клетки) могут быть введены другие модификации для предотвращения или минимизации рисков иммунологических осложнений (известных как "злокачественная трансформация T-клеток"), например, реакции трансплантат против хозяина (РТПХ), или случаев, когда здоровые ткани экспрессируют те же антигены-мишени, что и опухолевые клетки, что приводит к результатам, подобным РТПХ. Возможным решением этой проблемы является введение суицидального гена в CAR-экспрессирующие T-клетки. Подходящие суицидальные гены включают, без ограничения перечисленными, тимидинкиназу вируса простого герпеса (hsv-tk), индуцируемый суицидальный ген Каспазы 9 (iCasp-9) и усеченный полипептид рецептора эпидермального фактора роста человека (EGFRt). В некоторых вариантах осуществления суицидальный ген представляет собой полипептид EGFRt. Полипептид EGFRt может обеспечивать элиминирование T-клеток при введении моноклонального антитела против EGFR (например, цетуксимаба). EGFRt может быть ковалентно присоединен к 3'-концу внутриклеточного сигнального домена мезотелин-направленного CAR. Суицидальный ген может быть введен в вектор, содержащий нуклеиновые кислоты, кодирующие раскрытые в настоящем документе мезотелин-специфичные CAR-рецепторы. В этом случае введение пролекарства, созданного для активации суицидального гена (например, пролекарства (например, AP1903), которое может активировать iCasp-9) во время злокачественной трансформации T-клеток (например, РТПХ), инициирует апоптоз в активированных суицидальным геном CAR-экспрессирующих T-клетках.
Кроме того, в настоящем изобретении предложен способ предупреждения и/или лечения воспалительного заболевания у субъекта. В некоторых вариантах осуществления способ включает введение раскрытой в настоящем документе иммунореактивной клетки или включающей ее композиции субъекту. В некоторых вариантах осуществления иммунореактивная клетка является иммуноингибирующей клеткой. В некоторых вариантах осуществления иммуноингибирующая клетка является регуляторной T-клеткой. В некоторых вариантах осуществления воспалительное заболевание является панкреатитом. В некоторых вариантах осуществления субъектом является человек. В некоторых вариантах осуществления субъектом является реципиент трансплантата органа, например, реципиент трансплантата поджелудочной железы.
Кроме того, в настоящем изобретении предложен способ предотвращения отторжения трансплантата у субъекта, который является реципиентом трансплантата органа. В некоторых вариантах осуществления способ включает введение раскрытой в настоящем документе иммунореактивной клетки или включающей ее композиции субъекту. В некоторых вариантах осуществления иммунореактивная клетка является иммуноингибирующей клеткой. В некоторых вариантах осуществления иммуноингибирующая клетка является регуляторной T-клеткой. В некоторых вариантах осуществления субъектом является человек. В другом варианте осуществления субъектом является реципиент трансплантата поджелудочной железы.
Раскрытый в настоящем документе мезотелин-направленный CAR может быть трансдуцирован в иммуноингибирующую клетку, например, регуляторную T-клетку. Трансдуцированную иммуноингибирующую клетку могут вводить субъекту (например, человеку), имеющему воспалительные патологии или воспалительное заболевание. В некоторых вариантах осуществления воспаленный участок или участок воспалительного заболевания имеет высокий уровень экспрессии мезотелина, распознаваемого раскрытым в настоящем документе MSLN-CAR. Воспалительное заболевание может быть тяжелым, например, острым панкреатитом. Кроме того, трансдуцированную иммуноингибирующую клетку могут вводить субъекту, который является реципиентом трансплантата органа.
Кроме того, раскрытый в настоящем документе мезотелин-направленный CAR, а также второй CAR, направленный против антигена MHC, могут быть совместно трансдуцированы в иммуноингибирующую клетку (например, регуляторную T-клетку), в результате чего иммуноингибирующая клетка сможет специфично собраться на участке пересаженной поджелудочной железы. В некоторых вариантах осуществления субъект MHC класса I получает трансплантат поджелудочной железы от донора MHC класса II; регуляторные T-клетки реципиента трансдуцируют раскрытым в настоящем документе MSLN-специфичным CAR и вторым CAR, направленным против антигена MHC класса II, и, таким образом, трансдуцированные регуляторные T-клетки реципиента собираются/объединяют на участке пересаженной поджелудочной железы и избегают отторжения трансплантата или органа.
Подходящие для терапии люди-субъекты, как правило, включают две группы лечения, которые можно различать по клиническим критериям. Субъекты с "распространенным заболеванием" или "высокой опухолевой нагрузкой" являются субъектами, которые несут клинически измеряемую опухоль. Клинически измеряемая опухоль является опухолью, которая может быть обнаружена по опухолевой массе (например, с помощью пальпации, компьютерной томографии, сонограммы, маммограммы или рентгеновского исследования; положительные биохимические или гистопатологические маркеры сами по себе недостаточны для идентификации этой популяции). Фармацевтическую композицию вводят таким субъектам чтобы вызвать противоопухолевый эффект с целью облегчения их состояния. В идеальном случае в результате этого происходит уменьшение массы опухоли, однако эффективность составляет любое клиническое улучшение. Клиническое улучшение включает снижение риска или скорости прогрессирования, или уменьшение патологических последствий опухоли.
Вторая группа подходящих субъектов известна в искусстве как "адъювантная группа". Это лица, имевшие в анамнезе неоплазию, но демонстрировавшие ответ на другую схему терапии. Предыдущая терапия может включать, без ограничения, хирургическую резекцию, лучевую терапию и традиционную химиотерапию. В результате у таких лиц отсутствует опухоль, поддающаяся клиническому измерению. Однако существуют подозрения, что они подвержены риску прогрессирования заболевания либо вблизи от исходного участка локализации опухоли, либо из-за метастазов. Эту группу можно разделить на лиц с высоким и низким риском. Такое разделение производится на основе признаков, наблюдаемых до или после первоначального лечения. Эти признаки известны в области медицины и соответствующим образом определены для каждой определенной неоплазии. Признаки, типичные для подгрупп высокого риска, включают пациентов, у которых опухоль распространилась в близлежащие ткани, или у которых наблюдается поражение лимфатических узлов.
Другая группа имеет генетическую предрасположенность к неоплазии, но еще не демонстрировала клинических признаков неоплазии. Например, женщины с положительным тестом на генетическую мутацию, связанную с раком молочной железы, но все еще в детородном возрасте могут пожелать получить одну или больше иммунореактивных клеток, описанных в настоящем документе, для профилактического лечения с целью предотвращения возникновения неоплазии до того момента, пока они не будут подходить для проведения превентивной хирургической операции.
Вследствие поверхностной экспрессии CAR-рецептора против мезотелина и PD-1 DN, который усиливает противоопухолевое действие иммунореактивной клетки, адоптивно перенесенные Т- или NK-клетки обладают повышенной и селективной цитолитической активностью на участке локализации опухоли. Кроме того, после их локализации в опухоли или вирусной инфекции и их пролиферации, T-клетки превращают опухоль или вирусную инфекцию в среду с высокой проницаемостью для широкого спектра иммунных клеток, участвующих в физиологическом противоопухолевом или противовирусном ответе (инфильтрирующих опухоли лимфоцитов, NK-, NKT-клеток, дендритных клеток и макрофагов).
Кроме того, в настоящем изобретении предложены способы лечения и/или предупреждения вызванной патогеном инфекции (например, вирусной инфекции, бактериальной инфекции, грибковой инфекции, паразитарной инфекции или протозойной инфекции) у субъекта, например, у субъекта с иммунодефицитом. Способ может включать введение эффективного количества раскрытых в настоящем документе иммунореактивных клеток или включающей их композиции субъекту, имеющему инфекцию, вызванную патогеном. Примеры вирусных инфекций, восприимчивых к лечению, включают, без ограничения, инфекции, вызванные цитомегаловирусом (ЦМВ), вирусом Эпштейна-Барр (ВЭБ), вирусом иммунодефицита человека (ВИЧ) и вирусом гриппа.
В иммунореактивные клетки (например, T-клетки) могут быть введены другие модификации для предотвращения или минимизации рисков иммунологических осложнений (известных как "злокачественная трансформация T-клеток"), например, реакции трансплантат против хозяина (РТПХ), или случаев, когда здоровые ткани экспрессируют те же антигены-мишени, что и опухолевые клетки, что приводит к результатам, подобным РТПХ. Возможным решением этой проблемы является введение суицидального гена в CAR-экспрессирующие T-клетки. Подходящие суицидальные гены включают, без ограничения перечисленными, тимидинкиназу вируса простого герпеса (hsv-tk), индуцируемый суицидальный ген Каспазы 9 (iCasp-9) и усеченный полипептид рецептора эпидермального фактора роста человека (EGFRt). В некоторых вариантах осуществления суицидальный ген представляет собой полипептид EGFRt. Полипептид EGFRt может обеспечивать элиминирование T-клеток при введении моноклонального антитела против EGFR (например, цетуксимаба). EGFRt может быть ковалентно присоединен перед антигенраспознающим рецептором раскрытого в настоящем документе CAR-рецептора. Суицидальный ген может быть введен в вектор, включающий нуклеиновые кислоты, кодирующие раскрытый в настоящем документе CAR-рецептор. В этом случае введение пролекарства, созданного для активации суицидального гена (например, пролекарства (например, AP1903), которое может активировать iCasp-9) во время злокачественной трансформации T-клеток (например, РТПХ), инициирует апоптоз в активированных суицидальным геном CAR-экспрессирующих T-клетках. Включение суицидального гена в раскрытый в настоящем документе CAR повышает уровень безопасности благодаря способности элиминировать большую часть CAR T-клеток в очень короткое время. Раскрытая в настоящем документе иммунореактивная клетка (например, T-клетка), в которую включен суицидальный ген, может быть преимущественно элиминирована напосредственно после инфузии CAR T-клеток или устранена при ранних признаках токсических явлений.
5.9. Наборы
В изобретении, раскрытом в настоящем документе, предложены наборы для индукции и/или усиления иммунного ответа, и/или лечения и/или предупреждения опухоли или вызванной патогеном инфекции у субъекта. В некоторых вариантах осуществления набор включает эффективное количество раскрытых в настоящем документе иммунореактивных клеток или включающей их фармацевтической композиции. В некоторых вариантах набор включает стерильный контейнер; такими контейнерами могут быть коробки, ампулы, бутылки, флаконы, пробирки, мешки, саше, блистерные упаковки или другие подходящие формы контейнеров, известные в данной области. Такие емкости могут быть изготовлены из пластика, стекла, ламинированной бумаги, металлической фольги или других материалов, подходящих для хранения лекарственных препаратов. В некоторых вариантах осуществления набор включает выделенную молекулу нуклеиновой кислоты, кодирующую CAR против мезотелина, и выделенную молекулу нуклеиновой кислоты, кодирующую PD-1 DN в экспрессируемой форме, которые необязательно могут содержаться в одном и том же или разных векторах.
При необходимости иммунореактивные клетки и/или молекулы нуклеиновых кислот поставляют вместе с инструкциями по введению клеток или молекул нуклеиновых кислот субъекту, имеющему или подвергающемуся риску развития неоплазии или вызванной патогеном инфекции, или иммунного нарушения. Инструкции, как правило, содержат информацию о применении композиции для лечения и/или предупреждения неоплазии или вызванной патогеном инфекции. В некоторых вариантах осуществления инструкции включают по меньшей мере одно из следующего: описание терапевтического средства; схему применения для лечения или предупреждения неоплазии, вызванной патогеном инфекции или иммунного нарушения, или их симптомов; меры предосторожности; предупреждения; показания; противопоказания; информацию о передозировке; нежелательные реакции; фармакологию у животных; клинические исследования и/или ссылки. Инструкции могут быть напечатаны непосредственно на контейнере (если имеется) или представлены в виде этикетки на контейнере, или в виде отдельного листка, брошюры, карточки или папки, поставляемой в контейнере или вместе с ним.
6. ПРИМЕРЫ
При практическом осуществлении настоящего изобретения используются, если не указано иное, стандартные методы молекулярной биологии (включая методы рекомбинации), микробиологии, клеточной биологии, биохимии и иммунологии, которые находятся в рамках компетенции специалиста в данной области. Такие способы полностью описаны в литературе, например, в "Molecular Cloning: A Laboratory Manual", second edition (Sambrook, 1989); "Oligonucleotide Synthesis" (Gait, 1984); "Animal Cell Culture" (Freshney, 1987); "Methods in Enzymology" "Handbook of Experimental Immunology" (Weir, 1996); "Gene Transfer Vectors for Mammalian Cells" (Miller and Calos, 1987); "Current Protocols in Molecular Biology" (Ausubel, 1987); "PCR: The Polymerase Chain Reaction", (Mullis, 1994); "Current Protocols in Immunology" (Coligan, 1991). Указанные методы могут применяться для получения полинуклеотидов и полипептидов, раскрытых в настоящем документе, и, в таком качестве, могут рассматриваться при осуществлении и практической реализации раскрытого в настоящем документе изобретения. Особенно полезные методы для конкретных вариантов осуществления будут обсуждаться в разделах, следующих ниже.
Следующие примеры используются для предоставления специалистам в данной области полного раскрытия и описания того, как надлежит осуществлять и применять раскрытые в настоящем документе клетки и композиции, и не предназначены для ограничения объема того, что авторы считают своим изобретением.
Пример 1
Были создана раскрытая в настоящем документе полипептидная композиция. Полипептидная композиция включает: (i) CAR, который связывается с мезотелином человека, и (ii) доминантно-негативную форму белка программируемой смерти 1 (PD-1 DN), как показано на Фигуре 1. Мезотелин-направленный CAR включает: (a) сигнальный пептид CD8 (например, сигнальный пептид CD8, состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 71), (b) внеклеточный антигенсвязывающий домен, который представляет собой scFv, включающий VH, включающую CDR1, состоящую из аминокислотной последовательности, представленной в SEQ ID NO: 76, CDR2, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 77, и CDR3, имеющей аминокислотную последовательность, представленную в SEQ ID NO: 78; и VL, включающую CDR1, состоящую из аминокислотной последовательности, представленной в SEQ ID NO: 79, CDR2, состоящкй из аминокислотной последовательности, представленной в SEQ ID NO: 80, и CDR3, состоящкй из аминокислотной последовательности, представленной в SEQ ID NO: 81, (c) трансмембранный домен, который включает полипептид CD28 (например, полипептид CD28, состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 92 (или аминокислот 153-179 из SEQ ID NO: 90)), (d) шарнирную/спейсерную область CD28 (например, полипептид CD28, состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 15 (или аминокислоты 114-152 из SEQ ID NO: 90)), и (e) внутриклеточный сигнальный домен, включающий модифицированный полипептид CD3ζ, состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 35, и костимулирующую сигнальную область, включающую полипептид CD28 (например, полипептид CD28, состоящий из аминокислотной последовательности, представленной в SEQ ID NO: 101 (или аминокислот 180-220 из SEQ ID NO: 90)). PD-1 DN включает сигнальный пептид PD-1, состоящий из аминокислот 1-20 из SEQ ID NO: 48, внеклеточный домен PD-1, состоящий из аминокислот 21-165 из SEQ ID NO: 48, и полипептид CD8, состоящий из аминокислот 137-207 из SEQ ID NO: 86. Полипептидная композиция также включает P2A пептид, имеющий аминокислотную последовательность, представленную в SEQ ID NO: 121, и расположенный между CAR и PD-1 DN, как показано на Фигуре 1. Полипептидная композиция обозначена как "M28z1XXPD1DNR".
CAR, содержащийся в полипептидной конструкции, имеет аминокислотную последовательность, представленную в SEQ ID NO: 56. Примерная нуклеотидная последовательность, кодирующая полипептидную конструкцию, представлена в SEQ ID NO: 123. Другая примерная нуклеотидная последовательность, кодирующая полипептидную композицию, представлена в SEQ ID NO: 124.
Пример 2
Исследовали активности M28z1XX-P2A-PD1DNR, имеющего структуру полипептидной композиции, как описано в Примере 1. Структуры альтернативной и контрольной конструкций сравнивали с M28z1XX-P2A-PD1DNR, как показано на Фигуре 2.
Вирусные векторы, включающие CAR конструкции, получали в линии клеток-продуцентов RD114, как показано на Фигурах 3A-3D. Клетки RD114 трансдуцировали различными разведениями вирусного супернатанта H29 (неразведенный, 1:2 и 1:4) и окрашивали на экспрессию CAR с помощью проточной цитометрии при использовании антитела против Fab. Пустой RD114 служил в качестве отрицательного контроля. Человеческие T-клетки успешны трансдуцировали M28z1XX-P2A-PD1DNR, как показано на Фигурах 4A-4E, 5A-5E и 6A-6F. ФГА-активированные T-клетки трансдуцировали различными концентрациями вирусного супернатанта RD114 и окрашивали на экспрессию CAR при окраске антителом против Fab и PD1DNR при окраске антителом против PD1 с помощью проточной цитометрии. Исследовали наличие корреляции числа копий вектора (VCN) со средней интенсивностью флуоресценции (MFI). ФГА-активированные T-клетки трансдуцировали различными концентрациями вирусного супернатанта RD114 и окрашивали на экспрессию CAR при окраске антителом против Fab и с помощью анализа методом проточной цитометрии. Геномную ДНК трансдуцированных T-клеток выделяли и определяли число копий вектора как VCN/мкг ДНК с помощью кПЦР. Как показано на Фигурах 7A-7C, MFI CAR-положительных клеток коррелировала с VCN/мкг ДНК для всех трех протестированных доноров. Отношения трансдукции человеческих CD4+ и CD8+ T-клеток показаны в Таблице 1.
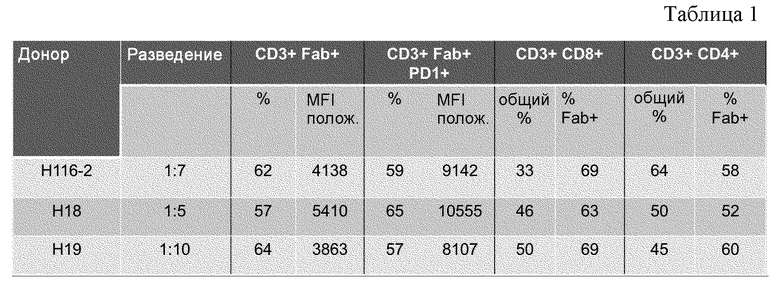
Затем исследовали цитолитические эффекты CAR T-клеток M28z1xx-PD1DNR. Клетки-мишени с высоким уровнем MSLN (MGM) культивировали совместно с M28z1XX-PD1DNR CAR T-клетками от разных доноров при различных отношениях E:T с использованием онализа на основе сопротивления. Результаты показаны на Фигуре 8. Как показано на Фигуре 8, T-клетки, трансдуцированные M28z1XX-PD1DNR CAR, продемонстрировали эффективную цитотоксичность для всех трех протестированных разных доноров. Эффекторная цитотоксичность присутствовала при нескольких отношениях E:T (данные не показаны).
Выводы:
Векторы M28z1xx-PD1DNR были успешно получены в клетках RD114. Стабильные линии клеток-продуцентов были успешно получены для всех конструкций. Вирусные векторы титровали с получением показателя трансдукции ~40-60% в T-клетках нескольких доноров. CD4 и CD8 T-клетки успешно трансдуцировали для экспрессии CAR и PD1DNR. Наблюдали корреляцию между числом копий вектора и трансдукцией.
Пример 3
В этом примере описан сравнительный анализ различных конструкций, включая M28z1XX-PD1DNR. Цитотоксичность измеряли с помощью анализа сопротивления. Принцип измерения цитотоксичности по электрическому сопротивлению (eCTL) показан на Фигуре 9. Параметры сравнительного анализа показаны на Фигуре 10, включая конструкции CAR, доноров, мишени CAR и отношения E:T. Измеряли экспрессию MSLN и PD-L1 в линиях клеток-мишеней. Линии клеток мезотелиомы (MGM, MGM-PDL1 и MSTOG) и рака легкого (A549GM и A549G) оценивали на экспрессию MSLN и PD-L1 с помощью проточной цитометрии. Результаты показаны на Фигурах 11A-11E. MGM, MGM-PDL1 и A549GM повышенно экспрессируют MSLN. Клетки MGM-PDL1 дополнительно экспрессировали PD-L1.
Также измеряли экспрессию CAR и PD1 в трансдуцированных T-клетках. Человеческие T-клетки, трансдуцированные M28z, M28z1xx, M28z-PD1DNR или M28z1xx-PD1DNR, исследовали на экспрессию CAR при окраске антителом к myc и экспрессию PD1/PD1DNR при окраске антителом к PD1 с использованием проточной цитометрии. Результаты показаны на Фигурах 12A-12E.
Проводили сравнительный анализ противоопухолевой эффективности CAR T-клеток, экспрессирующих M28z, M28z1xx, M28z-PD1DNR или M28z1xx-PD1DNR, против опухолевых клеток с высоким уровнем MSLN (MGM). Клетки-мишени MSLN (MGM) культивировали совместно либо с M28z, M28z1xx, M28z-PD1DNR, M28z1XX-PD1DNR, либо с нетрансдуцированными T-клетками при различных соотношениях E:T. Противоопухолевую эффективность оценивали с помощью анализа на основе сопротивления. Результаты показаны на Фигурах 13A-13C. Кроме того, клетки-мишени с высоким содержанием MSLN (MGM), меченные хромом-51, культивировали совместно с M28z, M28z1xx, M28z-PD1DNR, M28z1xx-PD1DNR или нетрансдуцированными T-клетками при различном соотношении E:T в течение 18 часов. Цитотоксичность определяли по высвобождению хрома-51 CTL. Результаты показаны на Фигуре 14.
Затем проводили сравнительный анализ с измерением противоопухолевой эффективности CAR T-клеток, экспрессирующих M28z, M28z1xx, M28z-PD1DNR или M28z1xx-PD1DNR, против MSLN-отрицательных опухолевых клеток (MSTOG). MSLN-отрицательные клетки-мишени (MSTOG) культивировали совместно с M28z, M28z1xx, M28z-PD1DNR, M28z1xx-PD1DNR или нетрансдуцированными T-клетками при указанных соотношениях E:T. Противоопухолевую эффективность оценивали с помощью анализа на основе сопротивления. Результаты показаны на Фигурах 15A-15C. Кроме того, MSLN-отрицательные клетки-мишени (MSTOG), меченные хромом-51, культивировали совместно с M28z, M28z1XX, M28z-PD1DNR, M28z1XX-PD1DNR или нетрансдуцированными T-клетками при различном соотношении E:T в течение 18 часов. Цитотоксичность определяли по высвобождению хрома-51 CTL. Результаты показаны на Фигуре 16.
Кроме того, проводили сравнительный анализ противоопухолевой эффективности CAR T-клеток, экспрессирующих M28z, M28z1xx, M28z-PD1DNR или M28z1xx-PD1DNRag, по сравнению с опухолевыми клетками с высоким уровнем MSLN, повышенно экспрессирующими PDL1. Клетки-мишени с высоким уровнем MSLN и оверэкспрессией PDL1 (MGM-PDL1) культивировали совместно с M28z, M28z1XX, M28z-PD1DNR, M28z1XX-PD1DNR или нетрансдуцированными T-клетками при различных соотношениях E:T. Противоопухолевую эффективность оценивали с помощью анализа на основе сопротивления. Результаты показаны на Фигурах 19A-19C. Аналогичным образом проводили сравнительный анализ противоопухолевой эффективности CAR T-клеток, экспрессирующих M28z, M28z1xx, M28z-PD1DNR или M28z1xx-PD1DNRag, против опухолевых клеток с высоким уровнем MSLN (A549GM), результаты показаны на Фигурах 18A-18C; а также проводили сравнительный анализ противоопухолевой эффективности CAR T-клеток, экспрессирующих M28z, M28z1xx, M28z-PD1DNR или M28z1xx-PD1DNR, против опухолевых клеток с низким уровнем MSLN (A549G), результаты показаны на Фигурах 19A-19C.
Выводы:
Конструкции M28z1xx-PD1DNR вызывали лизис MSLN+ клеток-мишеней с зависимостью от отношения E:T, причем результаты воспроизводились с разными донорами T-клеток при различных формах рака (линия клеток рака легкого и мезотелиомы). Специфическое цитотоксическое действие коррелировало с уровнями экспрессии MSLN, и было эффективным против MSLN+ клеток-мишеней с высокой экспрессией PD-L1.
Пример 4 - Регионарная доставка мезотелин-направленных CAR T-клеток для клинического применения с блокадой собственной контрольной точки PD-1 клеток: Переход к исследованию фазы I
Краткое описание: В данном примере представлены подтверждения доклинической безопасности и улучшенной противоопухолевой эффективности M28z1XXPD1DNR CAR T-клеток для клинического применения.
Методы: Сравнительную цитотоксичность, пролиферацию и секрецию цитокинов человеческими T-клетками, модифицированными для экспрессии M28z или M28z1XXPD1DNR CAR, оценивали с помощью анализов высвобождения хрома, накопление и анализа Luminex, соответственно. Противоопухолевую эффективность однократной дозы (1×105 CAR T-клеток; E:T 1:1000) внутриплеврально введенных M28z или M28z1XXPD1DNR CAR T-клеток исследовали на NSG мышах с ортотопической мезотелиомой плевры с помощью серийной визуализации биолюминесценции и сравнения выживаемости. После устранения опухоли функциональное персистирование CAR T-клеток тестировали при повторном заражении опухолью (возрастающие дозы от 2×106 до 11×106 опухолевых клеток).
Результаты: In vitro, и M28z, и M28z1XXPD1DNR CAR T-клетки проявляли антигенспецифическую цитотоксичность, накопление и секрецию эффекторных цитокинов (см. Таблицу 2). In vivo, однократная доза M28z1XXPD1DNR CAR T-клеток приводила к устранению опухоли, увеличению выживаемости и устойчивости к повторному приживлению опухоли после 10 повторных заражений опухолью (см. Таблицу 2) по сравнению с однократной дозой M28z CAR T-клеток.
Выводы: Данные по безопасности, устранению опухоли и функциональному персистированию CAR T-клеток без использования антител против PD1 обосновывают начало фазы I клинического исследования внутриплеврального введения M28z1XXPD1DNR CAR T-клеток у пациентов с мезотелиомой плевры.
Пример 5 - CAR T-клетка следующего поколения с блокадой собственного PD-1 клетки: Клиническое обоснование, разработка протокола доклинического и клинического исследования
Злокачественная мезотелиома плевры (MPM) представляет собой рак с низкой мутационной нагрузкой и низкой экспрессией PDL1 с разочаровывающими ответами на антитела против PD1. В ходе продолжающегося исследования фазы I/II (NCT02414269, n=41) была установлена безопасность и противоопухолевая эффективность при внутриплевральном введении T-клеток с мезотелин-направленным химерным антигенным рецептором (M28z CAR) с последующим введением антитела PD-1. CAR T-клетки с применением стратегии блокады антителами собственного PD1 клетки безопасны и могут обеспечивать противоопухолевую эффективность против опухоли как с низким, так и с высоким уровнем PDL1 без необходимости повторного введения антитела против PD1.
Краткое описание: В данном примере предоставлены подтверждения доклинической безопасности и повышенной противоопухолевой эффективности M28z1XXPD1DNR CAR T-клеток для клинического применения.
Методы: M28z и M28z1XXPD1DNR (модифицированный CD3z домен с доминантно-негативным рецептором PD-1) CAR для клинического применения трансдуцировали в несколько донорских T-клеток в качестве эффекторов, а в качестве мишеней использовали клетки MPM с низким и высоким уровнем PDL1. При различных соотношениях E:T сравнительную противоопухолевую эффективность in vitro и in vivo оценивали на мышах с ортотопической MPM. Системный противоопухолевый иммунитет проверяли путем повторного заражения опухолью на удаленном участке.
Результаты: In vitro, не было отмечено значимых различий между M28z и M28z1XXPD1DNR CAR (антигенспецифическая цитотоксичность, накопление и секреция эффекторных цитокинов). In vivo, однократная доза (1×105 CAR T-клеток) вводимых внутриплеврально M28z CAR T-клеток, либо с повторным введением антитела против PD1, либо с собственным PD1DNR клетки, приводила к сравнимому устранению опухоли, увеличению выживаемости с набором веса. См. Фигуру 20A и Таблицу 3. У мышей с ортотопической MPM однократная низкая доза (1×105 CAR T-клеток) M28z1XXPD1DNR CAR T-клеток приводила к устранению плевральной опухоль, продемонстрировав повышенный системный иммунитет по сравнению с M28z CAR T-клетками благодаря устойчивости к повторным заражениям опухолью на удаленном участке брюшной полости без каких-либо токсических явлений (PD1DNR связывается с мышиным PDL1/2). См. Фигуры 20B и 20C. Собранные опухоли демонстрируют повышенную и более глубокую инфильтрацию CAR T-клеток по сравнению с нетрансдуцированными T-клетками. См. Фигуру 20D.
Выводы: Однократное внутриплевральное введение низких доз M28z1XXPD1DNR CAR T-клеток демонстрирует выполнимость, безопасность, устранение опухоли, функциональную устойчивость и системный противоопухолевый иммунитет.
Потенциальные дозы
Направленная терапия
Однократная
Да
Многократные
Нет
Чувствительность к антигенам
Множественная
Множественная
Пример 6
1. Краткое описание
Злокачественная мезотелиома плевры (MPM) представляет собой редкую и смертельную злокачественную опухоль, связанную с воздействием асбеста. MPM - регионарно агрессивное первичное злокачественное новообразование плевры, характеризуемое инвазией в жизненно важные органы или грудную стенку (Carbone et al., CA Cancer J Clin. 2019; 69(5): 402-429). Большинство пациентов (60-70%) на момент обращения имеют локорегионарно распространенное заболевание и неоперабельны (Nelson et al., J Clin Oncol. 2017; 35(29): 3354-3362; Flores et al., J Thorac Oncol. 2007; 2(10): 957-965). Даже при успешном завершении комбинации химиотерапии, агрессивной хирургической резекции и лучевой терапии средняя выживаемость пациентов после лечения составляет всего 9-17 месяцев (Flores et al., J Thorac Oncol. 2007; 2(10): 957-965). С 2003 года не было новых одобренных FDA методов лечения MPM (Tsao et al., J Thorac Oncol. 2018; 13(11): 1655-1667). В настоящее время стандартом первой линии системного лечения пациентов с MPM является цисплатин с пеметрекседом, исходя из средней общей выживаемости 12,1 месяца по сравнению с 9,3 месяца для одного цисплатина (Vogelzang et al., J Clin Oncol. 2003; 21(14): 2636-2644). Поскольку пациенты с MPM имеют низкую мутационную нагрузку опухоли и низкую экспрессию лиганда программируемой смерти 1 (PD-L1), их ответ на ингибиторы иммунных контрольных точек ограничен, и при этом сохраняется огромная неудовлетворенная потребность (Yarchoan et al., JCI Insight. 2019; 4(6); Forde et al., Curr Treat Options Oncol.2019; 20(2): 18). Локальный характер, потенциальная доступность и относительное отсутствие метастазов делают MPM подходящим кандидатом для регионарной направленной терапии (Nelson et al., J Clin Oncol. 2017; 35(29): 3354-3362).
В данном примере описаны доклинические исследования, проведенные в поддержку клинического применения внутриплевральной дозы T-клеток с химерным антигенным рецептором (CAR) M28z1XXPD1DNR, нового исследуемого препарата для лечения пациентов с диагнозом (гистологически или цитологически задокументированным) MPM, которые прошли по меньшей мере одну химиотерапевтическую схему, и у которых документально подтверждено наличие опухоли.
Это одноцентровое исследование фазы I с максимальным числом участников 36, разработанное для оценки безопасности, требуемой дозы и эффективности таргетинга генетически направленных аутологичных M28z1XXPD1DNR CAR T-клеток после предварительного лечения циклофосфамидом. В этом исследовании было запланировано 5 уровней доз: 1×106, 3×106, 6×106, 1×107 и 3×107 M28z1XXPD1DNR CAR T-клеток/кг при условии отсутствия дозолимитирующих токсических явлений. M28z1XXPD1DNR CAR T-клетки вводят путем инфузии через постоянный плевральный катетер. Перед лечением пациентов подвергают скринингу на экспрессию мезотелина с помощью иммуногистохимического анализа образцов биопсии опухоли и/или уровней растворимых родственных мезотелину пептидов в крови.
M28z1XXPD1DNR CAR T-клетки представляют собой аутологичные T-клетки, трансдуцированные ex vivo стоковым супернатантом гамма-ретровирусного вектора, полученным из главного банка вектор-продуцирующих клеток, 293VEC GALV SFG M28z1XXPD1DNR. Основные компоненты CAR, кодируемые в векторе, являются следующими:
1) человеческий scFv против мезотелина для направленного взаимодействия с опухолями, экспрессирующими мезотелин,
2) Костимулирующий домен CD28 человека для передачи сигналов выживания и пролиферации T-клеток,
3) Точечно-мутантный человеческий CD3ζ с одним функциональным иммунорецепторным тирозиновым активирующим мотивом (ITAM) для калиброванной активации T-клеток, и
4) Доминантно-негативный рецептор белка программируемой клеточной смерти 1 (PD1) (PD1DNR) для защиты T-клеток от перехода в состояние дисфункции или истощения при воздействии антигена (см. Фигуру 21).
Мезотелин - поверхностный антиген раковых клеток, который повышенно экспрессируется в большинстве форм MPM, рака легкого, трижды негативного рака молочной железы, рака поджелудочной железы и рака яичника, а также в некоторых формах рака пищевода (Pastan et al., Cancer Res. 2014; 74(11): 2907-2912; Kachala et al., Clin Cancer Res. 2014; 20(4): 1020-1028; Tang et al., Anticancer Agents Med Chem. 2013; 13(2): 276-280; Servais et al., Clin Cancer Res. 2012; Kelly et al., Mol Cancer Ther. 2012; 11(3): 517-525; Tchou et al., Breast Cancer Res Treat. 2012; 133(2): 799-804). Авторы изобретения ранее продемонстрировали, что оверэкспрессия мезотелина способствует агрессивности аденокарцином легкого (n=1200) (Kachala et al., Clin Cancer Res. 2014; 20(4): 1020-1028), MPM (n=250) (Servais et al., Clin Cancer Res. 2012; Kelly et al., Mol Cancer Ther. 2012; 11(3): 517-525), а также трижды негативного рака молочной железы (n=250) (Tozbikian et al., PLoS One.2014; 9(12): e114900). Помимо того, что экспрессия мезотелина в опухолях относительно высока по сравнению с нормальными тканями, он также экспрессируется на очень низких уровнях на нормальных мезотелиальных поверхностях брюшинной полости, плевры и перикарда (Villena-Vargas et al., Ann Cardiothorac Surg. 2012; 1(4): 466-471), что делает его идеальной мишенью для терапии с применением CAR T-клеток против солидных опухолей. Биологическая функция мезотелина недостаточно исследована и изучается.
Ранее мезотелин-направленные CAR T-клетки вводили внутривенно людям (3×108 клеток/м2 или 4,8×107 клеток/доза) в клиническом исследовании, проведенном в Пенсильванском университете (NCT01355965), где CAR включает мышиный scFv. Сообщали, что анафилактическая реакция, отмеченная у 1 пациента, была вызвана ответами против мышиных антител, которые вырабатывались против гуманизированной части мышиного scFv в конструкции CAR, используемой в этом исследовании (Beatty et al., Cancer Immunol Res. 2014). В то же время, в недавнем исследовании фазы I (NCT02414269), проведенном в лаборатории авторов изобретения, внутриплеврально вводили мезотелин-направленные CAR T-клетки (до 6×107 CAR T-клеток/кг), которые состояли из полностью человеческого scFv, полученного из библиотеки Fab человека (Feng et al., Mol Cancer Ther. 2009). На данный момент 40 пациентов прошли курс лечения, при этом дозолимитирующих токсических эффектов не наблюдали. Предварительную эффективность в этом исследовании наблюдали в когорте пациентов (n=18), которые получали CAR T-клеточную терапию с последующим введением минимум 3 доз пембролизумаба (антитело против PD1) с дополнительным трехмесячным периодом наблюдения. Важно отметить, что 83% пациентов в этой когорте не потребовали нового или дополнительного лечения через 6 месяцев, при этом половина пациентов не получала дополнительного лечения в течение 18 месяцев. Кроме того, у большинства пациентов CAR T-клетки были обнаружены в периферической крови через >100 дней после внутриплеврального введения, что указывает на персистирование этих клеток в организме пациента.
В поддержку первого клинического исследования у человека фармакологическая программа для M28z1XXPD1DNR CAR T-клеток состоит из серии исследований ортогональной in vitro специфичности, цитотоксичности, накопления и секреции цитокинов, а также исследований опухолевой эффективности и выживаемости in vivo на мышах, результаты которые предлагают эффективную дозу для перевода в клиническое применение. В Таблице 4 представлена общая информация о проведенных доклинических фармакологических и токсикологических исследованиях, а также их основные результаты.
- Отсутствие экспрессии мезотелина в нормальной ткани легкого и молочной железы
- трансдукция CAR оптимизирована до 35%-70% для сохранения VCN≤5
- Повторная стимуляция антигеном: Цитотоксичность сохранялась для mycM28z1XXPD1DNR, но снижалась для mycM28z CAR T-клеток
- Секреция эффекторных цитокинов снижалась при повторной стимуляции антигеном
- Мыши, получавшие mycM28z1XXPD1DNR (доза 5×104 и 1×105) CAR T-клетки, оставались без опухоли до завершения исследования (день 68; медианная выживаемость, не достигнута в сравнении с 50 днями у мышей, получавших 1×105 mycM28z CAR T-клеток)
- Набор веса и отсутствие токсического действия у мышей, получавших mycM28z1XXPD1DNR CAR T-клетки
- mycM28z CAR T-клетки стали дисфункциональными при повторной антигенной стимуляции
- Токсические явления не наблюдали
- Отсутствие значимых клинических признаков
- Отсутствие значимого различия в массе тела по сравнению с контролями без опухоли
- Гистопатология: Отсутствие результатов микроскопических исследования, связанных с острыми или отложенными токсическими явлениями
- Гематология: Самки мышей, умерщвленные в день исследования 15, имели высокое среднее % значение моноцитов; отсутствие корреляции с результатами микроскопических исследований.
- Клиническая биохимия: Самцы мышей, умерщвленные в день исследования 14, имели низкое среднее значение общего белка; отсутствие корреляции с результатами микроскопических исследований.
- Однократное ортотопическое введение 1×105 mycM28z1XXPD1DNR CAR T-клеток в ксенотрансплантатной модели мезотелиомы хорошо переносилось.
Для облегчения обнаружения CAR T-клеток в доклинических исследованиях, были созданы CAR T-клетки, содержащие метку myc на N-конце мезотелин-специфичного scFv (mycM28z1XXPD1DNR). Для оценки соответствия между mycM28z1XXPD1DNR и M28z1XXPD1DNR CAR T-клетками, сравнивали эффективность трансдукции вирусных супернатантов и наблюдали постоянную, зависимую от концентрации экспрессию компонентов вектора между двумя конструкциями. Кроме того, CAR и PD1DNR экспрессировались пропорционально в каждой трансдуцированной клетке из-за присутствия саморасщепляющегося P2A пептида, который эффективно опосредует экспрессию бицистронного трансгена. При сравнении процента трансдуцированных клеток, экспрессирующих CAR, с числом вставок копий вектора в геном T-клеток, наблюдали положительную линейную зависимость между разведением вирусного супернатанта, используемого для трансдукции, и итоговым числом копий вектора (VCN). На основании этих наблюдений было определено, что диапазон 35-70% T-клеток, экспрессирующих CAR, обеспечивает оптимальную эффективность трансдукции, которая: (1) поддерживает низкое соотношение VCN:клеток и (2) снижает риск инсерционного мутагенеза, который обычно растет с высоким соотношением VCN:клетка.
Для подтверждения экспрессии PD1DNR и ее дифференцирования от эндогенного аналога, проводили анализа проточной цитометрии и кПЦР для измерения и сравнения экспрессии белка на поверхности клеток и экспрессии внутриклеточной мРНК PD1, соответственно, в T-клетках, трансдуцированных mycM28z1XXPD1DNR и mycM28z. На уровне белка клеточной поверхности, по сравнению с mycM28z CAR T-клетками, mycM28z1XXPD1DNR CAR T-клетки демонстрировали 2-кратное увеличение процента клеток с положительной окраской на PD1, и 3-кратное увеличение средней интенсивности флуоресценции (MFI), демонстрируемое PD1-положительными клетками. На уровне мРНК, по сравнению с нетрансдуцированными T-клетками, mycM28z CAR T-клетки демонстрировали 4-кратное увеличение как внеклеточных, так и внутриклеточных доменов PD1, тогда как mycM28z1XXPD1DNR CAR T-клетки демонстрировали 157-кратное увеличение внеклеточного домена PD1 и только 2-кратное увеличение внутриклеточного домена PD1. Такая экспрессия внеклеточного домена PD1, повышенная на порядки, указывает на высокую экспрессию PD1DNR, что служит для борьбы с ингибированием контрольной точки.
Наконец, для исключения любого возможного взаимодействия myc-метки (используемой в доклинических исследованиях) с нарушением функции CAR, противоопухолевую эффективность mycM28z1XXPD1DNR и M28z1XXPD1DNR CAR T-клеток сравнивали с использованием анализа цитотоксичности на основе электрического сопротивления, который не обнаружил различий в кинетике и общем цитолизе мезотелин-положительных опухолевых клеток 3 разных доноров, что подтверждает, что myc-метка не влияет на функцию CAR.
Затем исследовали специфичность, цитотоксичность, накопление и секрецию цитокинов mycM28z1XXPD1DNR CAR T-клеток. В анализе цитотоксичности с высвобождением 51Cr, mycM28z1XXPD1DNR CAR T-клетки демонстрировали антигенспецифическую и независимую от человеческого лейкоцитарного антигена (HLA) цитотоксичность в отношении мезотелин-положительных опухолевых клеток, как с конститутивной экспрессией, так и с оверэкспрессией PD-L1. Неспецифическую цитотоксичность в отношении мезотелин-отрицательных опухолевых клеток не наблюдали. mycM28z1XXPD1DNR CAR T-клетки не проявляли какой-либо цитотоксичности в отношении мишеней с оверэкспрессией PD-L1 в отсутствие экспрессии мезотелинового антигена. При проведении анализа с повторной стимуляцией антигеном (антигенный стресс-тест) отмечали увеличение экспансии до 622 раз как mycM28z1XXPD1DNR, так и mycM28z CAR T-клеток в течение периода, включающего 6 антигенных стимуляций. В точках времени, в которых проводили анализ, конструкции демонстрировали аналогичную цитотоксичность после первой стимуляции антигеном и сохраняли аналогичную цитотоксичность до четвертой стимуляции антигеном. Когда соотношение эффектор-мишень (E:T) дополнительно уменьшали для увеличения антигенного стресса, mycM28z1XXPD1DNR CAR T-клетки сохраняли цитотоксичность лучше, чем mycM28z CAR T-клетки при седьмой стимуляции антигеном. Однако в ходе анализа секреция эффекторных цитокинов (IL-2, IFN-γ и ФНО-α) постепенно снижалась как у mycM28z1XXPD1DNR, так и у mycM28z CAR T-клеток, что указывает на профиль безопасности обеих конструкций.
Опухолевые клетки MPM, котрансдуцированные с люциферазой светляка (ffLuc), вводили внутриплеврально для приживления опухолей, представляющих модель ортотопического рака MPM. Для неинвазивного контроля роста опухоли мышам-опухоленосителям внутрибрюшинно вводили люциферин в дозе 150 мг/кг и визуализировали в системе визуализации IVIS Spectrum (PerkinElmer, Waltham, MA) через 15 минут при использовании протокола, оптимизированного для количественного мониторинга регрессии или прогрессирования плевральной опухоли, который был ранее опубликован лабораторией авторов изоборетения (Servais et al., Curr Protoc Pharmacol. 2011; Chapter 14: Unit 14 21).
В первоначальном эксперименте, проведенном для исследования противоопухолевой активности CAR T-клеток in vivo, мышам NSG с ортотопическими опухолями вводили однократную внутриплевральную дозу 3×104 mycM28z1XXPD1DNR CAR T-клеток и сравнивали с мышами, получавшими однократную внутриплевральную дозу контрольных CAR T-клеток, специфичных к простатическому специфическому мембранному антигену (P28z). Через пятнадцать дней мыши, получавшие CAR T-клетки mycM28z1XXPD1DNR, показали значимое снижение опухолевой нагрузки (p=0,0002), тогда как у мышей, получавших P28z CAR T-клетками, развивалась агония из-за высокой опухолевой нагрузки.
Во втором исследовании in vivo мышей с ортотопическими опухолями делили на 3 группы, каждая из которых получала однократную внутриплевральную дозу 1×105 или 5×104 mycM28z1XXPD1DNR CAR T-клеток или 1×105 mycM28z CAR T-клеток. Серийная визуализация опухолей показала снижение опухолевой нагрузки уже через 5 дней после введения CAR T-клеток с полным устранением опухоли, определяемым по снижению сигнала визуализации биолюминесценции (BLI) до исходного уровня, примерно в день 19 у мышей, получавших 1×105 mycM28z1XXPD1DNR CAR T-клеток, и приблизительно в день 26 у мышей, получавших 1×105 mycM28z CAR T-клеток. Мыши, получавшие любую дозу mycM28z1XXPD1DNR CAR T-клеток, оставались без опухолей до завершения исследования (68 дней). Медианная выживаемость составила 50 дней у мышей, получавших 1×105 mycM28z CAR T-клеток; медианная выживаемость не была достигнута у мышей, получавших любую дозу mycM28z1XXPD1DNR CAR T-клеток (>68 дней; p=0,0085-0,0427). Иммунофлуоресцентная визуализация опухолей плевры ex vivo показала, что mycM28z1XXPD1DNR CAR T-клетки окружают периферию опухоли с высокой плотностью и проникают в паренхиму опухоли через 3 дня после регионарной доставки. Эти результаты воспроизводили с использованием T-клеток нескольких доноров с различным процентом CD4 и CD8 T-клеток, трансдуцированных mycM28z1XXPD1DNR CAR.
Чтобы исследовать функциональное персистирование mycM28z1XXPD1DNR CAR T-клеток, мышей с ортотопическим MPM, которые получали однократную внутриплевральную дозу 1×105 mycM28z1XXPD1DNR или mycM28z CAR T-клеток, повторно заражали повышаемыми дозами (от 2×106 до 11×106 клеток/доза) мезотелин-положительных опухолевых клеток, вводимых внутрибрюшинно (повторное введение клеток более целесообразно производить в брюшную полость, чем в плевральную полость) каждые 4-8 дней, до 10 раз. Сигнал BLI у мышей, получавших mycM28z1XXPD1DNR CAR T-клетки, достигал пиковой интенсивности вскоре после каждого повторного заражения опухолью и возвращался к исходному уровню во все точки времени после повторного заражения. В отличие от этого, мыши, получавшие mycM28z CAR T-клетки, показали аналогичную тенденцию до 5 повторных заражений опухоли, но не смогли контролировать восстановление опухоли после введения более высоких доз опухоли в поздние точки времени при повторном заражении опухоли (от 6 до 10), что привело к рецидиву опухоли и агональному состоянию. mycM28z1XXPD1DNR CAR T-клетки препятствовали формированию внутрибрюшинной опухоли в течение 10 повторных заражений, даже через >126 дней после однократной внутриплевральной дозы 1×105 CAR T-клеток, без каких-либо явных признаков токсического действия. В условиях высокого антигенного стресса mycM28z1XXPD1DNR CAR T-клетки демонстрировали превосходное функциональное персистирование и повышенную противоопухолевую эффективность по сравнению с mycM28z CAR T-клетками in vivo. Для подтверждения, что эта повышенная эффективность не была вызвана реакцией трансплантат против хозяина, которая обычно наблюдается у мышей NSG, которым вводят CAR T-клетки, в этот момент времени вводили не экспрессирующие антиген мишени, что приводило к повышению сигнала BLI опухолей без противоопухолевого ответа, подтверждая, что наблюдаемая противоопухолевая эффективность была антигенспецифической.
Для подтверждения противоопухолевой эффективности криоконсервированных T-клеток, трансдуцированных кодирующим M28z1XXPD1DNR CAR вирусным супернатантом, полученным для применения в клинических исследованиях, M28z1XXPD1DNR CAR T-клетки, созданные в Лаборатории клеточной терапии и клеточной инженерии (CTCEF) Мемориального онкологического центра им. Слоуна-Кеттеринга (MSK), размораживали (жизнеспособность: 88% после размораживания) и вводили мышам внутриплеврально с ортотопическими MPM в дозе 6×104 и 2×105 CAR T-клеток/мышь. Регрессию и устранению опухоли наблюдали после введения обеих доз, при этом 100% мышей выживали до конца периода наблюдения (день 70), тогда как у мышей, не получавших лечения, опухоль прогрессировала, вызвав смерть ко дню 19. Криоконсервированные CAR T-клетки продемонстрировали высокую жизнеспособность после размораживания и были эффективны без каких-либо признаков токсического действия.
При проведении вышеописанных экспериментов по исследованию эффективности у мышей не наблюдали токсических явлений, при этом вес животных оставался стабильным в течение всего исследования.
В разделе 3 данного Примера (озаглавленном "Доклиническая токсикология") описано исследование, проведенное на мышах с целью специфической оценки потенциальной токсичности mycM28z1XXPD1DNR CAR T-клеток в мышиной модели ортотопической MPM. Смертность, тяжесть патологии, вес, клинические признаки, общий анализ крови и клиническую биохимию, результаты макроскопической аутопсии и гистопатологического исследования оценивали у 96 (48 самцов и 48 самок) мышей NSG, несущих 8-дневную ортотопическую мезотелиому, которые были случайным образом распределены для группы контроля и лечения. Дозу 1×105 CAR T-клеток/мышь или контрольную среду (5×106 CAR T-клеток/кг) вводили однократно посредством ортотопической инъекции. В день 2 и 14 после введения CAR T-клеток или среды (промежуточное и окончательное умерщвление соответственно) мышам давали наркоз для вскрытия и оценки показателей общего анализа и клинической биохимии крови. День 14 выбрали в качестве момента для умерщвления, поскольку опухоль либо значительно регрессировала, либо была устранена к этому моменту времени (что подтверждалось данными BLI или аутопсии из предыдущих экспериментов). Выполнение умерщвления и вскрытия в этот момент времени позволяет исследовать любые целевые, внеопухолевые эффекты (scFv, используемый в настоящем CAR, реагирует с мезотелином мыши) (Feng et al., Mol Cancer Ther. 2009) в отношении нормальных тканей, в частности плевры, брюшной полости и перикарда, с низкими уровнями экспрессии мезотелина после пиковой экспансии CAR T-клеток при отсутствии опухолевой нагрузки с высокой экспрессией антигена.
У животных в этом исследовании не наблюдали смертности или тяжелой патологии, за исключением 2 животных из контрольной группы, получавших среду, которые были подвергнуты отдельному умерщвлению из-за тяжелого состояния и затрудненного дыхания через 20-22 дня после введения опухоли. Предыдущая работа в лаборатории авторов изобретения показала, что контрольные животные, которым вводили среду, могут погибать из-за опухолевой нагрузки примерно через 20-22 дня после введения опухоли (Servais et al., Clin Cancer Res. 2012; Servais et al., Curr Protoc Pharmacol. 2011; Chapter 14: Unit14 21; Adusumilli et al., Sci Transl Med. 2014; 6(261): 261ra151; Cherkassky et al., J Clin Invest. 2016; 126(8): 3130-3144; Servais et al., PLoS One. 2011; 6(10): e26722). Поэтому умерщвления этих животных были незапланированными, но не неожиданными. Смертность или патология не были связаны с CAR T-клетками. Животные, которые получали контрольную среду, демонстрировали прогрессирующее снижение массы тела в течение периода исследования и значимое различие в весе по сравнению с контрольными мышами без опухолей, и мышами, получавшими mycM28z1XXPD1DNR CAR T-клетки. Это было связано с увеличением опухолевой нагрузки у контрольных животных, получавших среду. У мышей, получавших mycM28z1XXPD1DNR CAR T-клетки, не наблюдали никаких значимых клинических признаков. У одной мыши, получавшей исследуемый препарат, наблюдали легкое шелушение кожи, которое объяснялось раздражением, вызванным хирургическими зажимами, поскольку никакие другие животные не были затронуты, и активность животных была нормальной. Мыши выглядели нормальными на протяжении всего периода наблюдения.
Самки мышей, получавших mycM28z1XXPD1DNR CAR T-клетки, которые были умерщвлены через 14 дней после введения CAR T-клеток, имели высокое среднее процентное значение моноцитов (среднее, 18,44%, n=5) (p≤0,0001) по сравнению с контрольными мышами с опухолями, которым вводили среду (среднее, 3,34%, n=5). Диапазон референсных значений, установленный для процента моноцитов, составляет 0,9-18%. Однако это не совпадало с данными микроскопического исследования. Никаких других значимых или аномальных результатов по оцениваемым гематологическим показателям не наблюдали. Любые различия между группами, получавшими исследуемый препарат, и группами, получавшими соответствующую среду, находились в пределах нормальных референсных диапазонов или не были биологически значимыми или статистически значимыми.
Самцы мышей, получавших mycM28z1XXPD1DNR CAR T-клетки, которые были умерщвлены через 14 дней после введения CAR T-клеток, имели низкое среднее значение общего белка (в среднем 3,83 г/дл, n=5) (p=0,0022) по сравнению с контрольными мышами с опухолями, которые получали среду (в среднем 4,68 г/дл, n=4). Диапазон референсных значений, установленный для общего белка, составляет 4,1-6,4 г/дл. Однако это не совпадало с данными микроскопического исследования. Никаких других побочных эффектов в отношении параметров клинической биохимии при введении исследуемого препарата не наблюдали. Любые различия между группами, получавшими исследуемый препарат, и соответствующими группами, получавшими среду, находились в пределах нормальных референсных диапазонов или не были биологически значимыми или статистически значимыми.
Обзор результатов гистопатологических исследований показал, что в дни промежуточного и окончательного умерщвления не было обнаружено результатов микроскопических исследований, связанных с острой или отсроченной токсичностью в результате введения mycM28z1XXPD1DNR CAR T-клеток. Результаты микроскопических исследований животных в группах CAR-T-клеток промежуточного умерщвления включали присутствие смешанной клеточной инфильтрации в ксенотрансплантатах опухолей. Посчитали, что это связано с введением исследуемого препарата, но не с каким-либо токсическим действием исследуемого препарата. Было установлено, что любые другие наблюдаемые результаты возникали спорадически, с такой же частотой, что и у контрольных животных, или были распространенными для используемых видов/штаммов.
mycM28z1XXPD1DNR CAR T-клетки были обнаружены в опухоли и селезенке через 8 дней после внутриплеврального введения, при этом BLI показала, что через 2 недели опухолевая нагрузка значительно снижалась у мышей, получавших CAR T-клетки, что подтверждает не только успешное введение, но и фармакологическую активность исследуемого препарата. Уровни цитокинов в плазме мышей, полученные в тот же момент времени, показали несколько более высокие уровни IL-4 у мышей, получавших CAR T-клетки, чем у мышей, получавших контрольную среду. Уровни IL-10, IL-6, KC/GRO и ФНО-α в целом были низкими и значимо не отличались у мышей, получавших CAR T-клетки, и мышей, получавших контрольную среду. IFN-γ, IL-12p70, IL-1β, IL-2 и IL-5 не были обнаружены (ниже предела количественного определения).
В заключение следует отметить, что данные показывают, что M28z1XXPD1DNR CAR T-клетки хорошо переносятся. Доза 1×105 клеток/мышь в 5 раз превышает начальную дозу для пациентов (1×106 клеток/кг в расчете на массу тела), соответствуя 5×106 клеток/кг. M28z1XXPD1DNR CAR T-клетки содержат такой же антигеннаправляющий фрагмент, что и M28z CAR T-клетки, для которых уже доступны данные по безопасности применения у пациентов (n=50). В настоящем клиническом исследовании (IND16354) авторы не наблюдали какого-либо дозолимитирующего токсического действия и внеопухолевого токсического действия при внутриплевральном введении до 6×107 M28z CAR T-клеток/кг в комбинации с антителом-блокатором контрольной точки PD1, вводимым через 3 недели после введения CAR T-клеток. Четыре пациента получали вторую дозу внутриплевральных T-клеток M28z CAR после нескольких доз антитела против PD1 (период вымывания - 4 недели) без наблюдаемой токсичности. В совокупности все доступные данные доклинических и клинических исследований обоснованно указывают на то, что предложенная начальная доза и способ введения M28z1XXPD1DNR CAR T-клеток не несут неприемлемого риска для наших пациентов.
2. Доклиническая фармакология
A. Методы
CAR-векторы. Векторы, используемые в доклинических исследованиях, представлены в Таблице 5.
Конструкции мезотелиннаправленных CAR содержат мезотелин-специфичный scFv (клон m912) (Feng et al., Mol Cancer Ther. 2009), слитый с костимулирующим доменом CD28 и сигнальным доменом CD3ζ (M28z). В цепь CD3ζ вводили мутации в два из трех ее ITAM мотивов, в результате чего остался один функциональный ITAM (обозначенный 1XX) (Feucht et al., Nat Med. 2019; 25(1): 82-88). CAR сливали с PD1DNR через сайт P2A из тешовируса свиней 1. PD1DNR состоит из сигнального пептида PD1 и внеклеточного домена PD1, слитых с трансмембранным и шарнирным доменами CD8 (Cherkassky et al., J Clin Invest. 2016; 126(8): 3130-3144). Этот рецептор-ловушка не содержит сигнального домена PD1, что обеспечивает блокаду внутренней контрольной точки T-клеток. Для облегчения обнаружения CAR, myc-метка (с аминокислотной последовательностью EQKLISEEDL ×2) была слита с N-концом scFv в конструкциях mycM28z и mycM28z1XXPD1DNR. Чтобы исключить какой-либо потенциальный риск иммуногенности у человека, конструкция M28z1XXPD1DNR для клинического применения не содержит myc-метку. Кроме того, экспрессия белка оптимизирована по кодонам, чтобы избежать какой-либо иммуногенности в конструкции CAR и PD1DNR. Подробная структура конструкций, используемых в доклинических исследованиях, представлена на Фигуре 22.
Экспрессия CAR-конструкций находится под контролем длинного концевого повтора (LTR) вируса мышиного лейкоза Молони из ретровирусного SFG вектора (Riviere et al., Proc Natl Acad Sci US A. 1995; 92(15): 6733-6737). Экспрессия CAR и PD1DNR направляется ретровирусным LTR.
Все CAR-векторы трансфицировали в линии упаковывающих клеток 293T H29, и вирусный супернатант, продуцируемый этими клетками, использовали для трансдукции и создания стабильных линий клеток 293T RD114.
CAR T-клетки. Первичные Т-лимфоциты человека выделяли из крови здоровых добровольцев-доноров в соответствии с протоколом, одобренным наблюдательным советом центра. Активированные фитогемагглютинином мононуклеарные клетки периферической крови (МКПК) выделяли с помощью центрифугирования при низкой плотности в среде для разделения лимфоцитов Lymphocyte Separation Medium (Corning, New York, NY). Через два дня после выделения, МКПК трансдуцировали вирусным супернатантом, содержащим векторы mycM28z, mycM28z1XXPD1DNR или M28z1XXPD1DNR, путем спинокуляции при 1800 g в течение 60 минут при 24°C в 6-луночных культуральных планшетах, покрытых 15 мкг/мл RetroNectin (Takara, Shiga, Japan). После спинокуляции трансдуцированные МКПК поддерживали в RPMI-1640 с добавкой 10% фетальной бычьей сыворотки (FBS), 2 мМ L-глутамина, 100 ед/мл пенициллина, 100 мкг/мл стрептомицина и 20 ед/мл IL-2. Эффективность трансдукции определяли с помощью проточного цитометрического анализа экспрессии myc-метки на scFv меченых CAR-рецепторов или при окрашивании антителом против IgG человека, специфичным к F(ab')2 фрагменту, для обнаружения экспрессии scFv немеченного CAR из M28z1XXPD1DNR. CAR T-клетки тестировали на жизнеспособность >70%, чистоту T-клеток >95% с помощью окрашивания антителом против CD3 человека, эффективность трансдукции 35-70% с помощью проточной цитометрии и экспрессию CD4/CD8. Характеристики T-клеток, используемых в доклинических исследованиях, представлены в Таблице 6.
Опухолевые клетки. Клетки из клеточной линии мезотелиомы плевры человека MSTO-211H (ATCC CRL-2081) генетически модифицировали и использовали для исследований in vitro и in vivo (Таблица 7).
MSTO-211H представляет собой линию раковых клеток MPM двухфазного типа, в которой отсутствует экспрессия эндогенных костимулирующих лигандов CD80/86. Клетки MSTO-211H подвергали ретровирусной трансдукции для экспрессии GFP и белка ffLuc, обозначив MSTOG, что позволило неинвазивно проводить BLI in vivo, с использованием ретровирусных SFG векторов, сконструированных в MSK. Среду, содержащую отфильтрованный вирус, добавляли к клеткам, пермеабилизованным при использовании 8 мкг/мл полибрена (Sigma-Aldrich, St. Louis, MO). Через 24 часа клетки повторно заражали свежесобранным вирусом. Эти клетки трансдуцировали с использованием варианта человеческого мезотелина 1 (выделенного из линии клеток рака яичника человека [OVCAR-3]), субклонированного в ретровирусный SFG вектор, с получением мезотелин+ MSTO- клеток 211H, обозначенных MGM. Аналогичным образом клетки MGM трансдуцировали PD-L1 (кДНК OriGene, субклонированный в вектор SFG), получив в результате MGM-PDL1. Опухолевые клетки поддерживали в среде RPMI-1640 с 10% FBS, 2 мМ L-глутамина, 100 ед/мл пенициллина и 100 мкг/мл стрептомицина в термостате с регулиремой влажностью и 5% CO2 при 37°C. Наблюдали линейную корреляцию между количеством опухолевых клеток, экспрессирующих люциферазу, и числом фотонов BLI in vitro (коэффициент корреляции Пирсона r=0,999, p<0,0001, данные не показаны). Относительные уровни экспрессии трансдуцированных белков показаны на Фигуре 23.
Проточная цитометрия. Проточную цитометрию проводили с использованием проточного цитофлуориметра Attune NxT (ThermoScientific, Waltham, MA) или BD LSRFortessa (BD Biosciences, San Jose, CA). Экспрессию человеческого мезотелина на поверхности опухолевых клеток детектировали с помощью конъюгированного с фикоэритрином крысиного IgG2a антитела против мезотелина человека (R&D Systems, Minneapolis, MN). Экспрессию человеческого PD-L1 на поверхности опухолевых клеток детектировали с использованием конъюгированного с фикоэритрином-цианином 7 мышиного IgG1 против человеческого PD-L1 (BD Biosciences). Человеческие T-клетки анализировали на предмет экспрессии на их клеточной поверхности человеческого CD3 при использовании конъюгированного с аллофикоцианином-цианином 7 мышиного IgG2a антитела против CD3 человека или конъюгированного с фикоэритрином-цианином 7 мышиного IgG1 антитела против CD3 человека (BioLegend, San Diego, CA) и CD4 человека или CD8 человека при использовании конъюгированного с флуоресцеинизотиоцианатом мышиного IgG1 антитела против CD4 человека (BioLegend) или конъюгированного с Alexa Fluor 488 мышиного IgG1 антитела против CD8 человека (BioLegend), соответственно. Экспрессию CAR на клеточной поверхности определяли количественно при использовании конъюгированного с фикоэритрином антитела против myc-метки (Cell Signaling Technology, Danvers, MA) или конъюгированного с Alexa Fluor 647 F(ab')2-фрагментом специфичного козьего антитела против человеческого F(ab')2 (Jackson ImmunoResearch, West Grove, PA). Экспрессию PD1 на клеточной поверхности CAR T-клеток анализировали с помощью конъюгированного с Brilliant Violet 711 мышиного IgG1 антитела против PD1 человека (BioLegend). Для обнаружения ex vivo человеческих T-клеток обработанную ткань мыши окрашивали конъюгированным с фикоэритрином-цианином 7 мышиным IgG1 антителом против CD3 человека и конъюгированным с аллофикоцианином-цианином 7 мышиным IgG1 антителом против CD45 человека (BioLegend). Дифференцирование живых клеток и мертвых клеток проводили при окрашивании клеток либо 4',6-диамидино-2-фенилиндолом (DAPI, ThermoFisher Scientific, Waltham, MA), либо eFluor 506 (ThermoFisher Scientific). Анализ данных проводили при использовании программы FCS Express (De Novo Software, Pasadena, CA) и FlowJo (BD Biosciences). В Таблице 8 представлены антитела, используемые для проточной цитометрии.
Определение VCN. Суммарную геномную ДНК из CAR T-клеток выделяли при использовании набора Miniprep Kit (Qiagen, Hilden, Germany). ПЦР-праймеры и зонды TaqMan использовали для обнаружения SFG и гена домашнего хозяйства альбумина (ALB). Последовательности зонда и праймеров на SFG человека:
Последовательность зонда: 5'-VIC-AGGACCTTACACAGTCCTGCTGAC-TAMRA-3' [SEQ ID NO: 126]
Последовательность прямого праймера: 5'-AGAACCTAGAACCTCGCTGGA-3' [SEQ ID NO: 127]
Последовательность обратного праймера: 5'-CTGCGATGCCGTCTACTTTG-3' [SEQ ID NO: 128]
Последовательности зонда и праймеров на ALB человека:
Последовательность зонда: 5'-VIC-TGCTGAAACATTCACCTTCCATGCAGA-TAMRA-3' [SEQ ID NO: 129]
Последовательность прямого праймера: 5'-TGAAACATACGTTCCCAAAGAGTTT-3' [SEQ ID NO: 130]
Последовательность обратного праймера: 5'-CTCTCCTTCTCAGAAAGTGTGCATAT-3' [SEQ ID NO: 131]
Реакция амплификации (25 мкл) содержала 5 мкл (150 мкг) геномной ДНК и 12,5 мкл смеси TaqMan Fast Advanced Master Mix (ThermoFisher Scientific), 0,8 мкл праймеров (прямого и обратного), 0,2 мкл зонда TaqMan и 5,7 мкл дистиллированной воды. Условия кПЦР были следующими: 50°C (2 мин), 95°C (20 мин), затем 42 цикла при 95°C (15 сек) и 60°C (1 мин), с использованием системы ПЦР в реальном времени QuantStudio 7-Flex (ThermoFisher Scientific). Все измерения ПЦР проводили в трех повторностях. Отношение VCN на клетку вычисляли как (среднее количество SFG/среднее количество ALB)*2. Средние количества экстраполировали из стандартных кривых SFG и ALB.
Определение экспрессии мРНК PD1. Суммарную РНК из CAR T-клеток выделяли при использовании набора Miniprep (Qiagen) и подвергали реакции обратной транскрипции при использовании набора для обратной транскрипции High-Capacity cDNA Reverse Transcription Kit (ThermoFisher Scientific). Анализ SYBR Green использовали для обнаружения внеклеточных и внутриклеточных доменов PDCD1 человека. Для нормализации использовали глицеральдегид-3-фосфатдегидрогеназу человека (GAPDH). Использовали следующие праймеры.
Последовательности праймеров к GAPDH:
Последовательность прямого праймера: 5'-GAAGGTGAAGGTCGGAGT-3' [SEQ ID NO: 132]
Последовательность обратного праймера: 5'-CATGGGTGGAATCATATTGGAA-3' [SEQ ID NO: 133]
Последовательности праймеров к внеклеточному домену PD-1 (Yoon et al., Science. 2015; 349(6247): 1261669):
Последовательность прямого праймера: 5'-CCAGGATGGTTCTTAGACTCCC-3' [SEQ ID NO: 134]
Последовательность обратного праймера: 5'-TTTAGCACGAAGCTCTCCGAT-3' [SEQ ID NO: 135]
Последовательности праймеров к внеклеточному домену PD-1 (Hsu et al., J Immunol. 2016; 197(5): 1884-1892):
Последовательность прямого праймера: 5'-ACGAGGGACAATAGGAGCCA-3' [SEQ ID NO: 136]
Последовательность обратного праймера: 5'-GGCATACTCCGTCTGCTCAG-3' [SEQ ID NO: 137]
кДНК разбавляли в 5 раз для последующего анализа кПЦР. Реакция амплификации (20 мкл) содержала кДНК из 200 нг суммарной РНК и 10 мкл смеси QuantiTect SYBR Green PCR Mix (Qiagen), 4 мкл праймеров (прямого и обратного, по 200 нМ) и дистиллированную воду. Условия кПЦР были следующими: 95°C (15 мин), 95°C (20 мин), затем 45 циклов при 94°C (15 сек), 60°C (30 сек), 72°C (30 сек) и 50°C (20 секунд для сбора данных) при использовании системы ПЦР в реальном времени QuantStudio 7 Flex (ThermoFisher Scientific). Все измерения ПЦР проводили в трех повторностях. Все праймеры синтезировали в Integrated DNA Technologies (Coralville, IA) и вычисляли значения эффективности амплификации (E). Относительную экспрессию генов-мишеней нормализовали по референсной группе в виде отношения согласно формуле Пфаффля (Pfaffl, Nucleic Acids Res. 2001; 29(9): e45):
Относительный коэффициент=(Eмишень)ΔCtмишень (контроль-образец)/(Eреф)ΔCtреф (контроль-образец)
Мишень=внеклеточный/внутриклеточный домен PD1; Реф=GAPDH; контроль=нетрансдуцированные T-клетки.
Анализ цитотоксичности 51Cr. Цитотоксичность mycM28z1XXPD1DNR CAR T-клеток по сравнению с mycM28z T-клетками определяли с помощью стандартного анализа высвобождения 51Cr. В 96-луночных круглодонных планшетах от 5×105 до 1×106 общих T-клеток в 200 мкл RPMI с 10% FBS, 2 мМ L-глутамина, 100 ед/мл пенициллина и 100 мкг/мл стрептомицина серийно разводили 1:2 в 100 мкл среды. Клетки-мишени инкубировали с 75 мкКи 51Cr на 1×106 клеток в течение 2 ч и ресуспендировали до конечной концентрации 5×103 клеток/100 мкл. После 3 промывок средой, 100 мкл клеток-мишеней добавляли к T-клеткам в трех повторностях и инкубировали в течение 4-18 ч в инкубаторе с регулируемой влажностью и 5% CO2 при 37°C. Супернатанты собирали, сеяли в 96-луночные планшеты Lumina (PerkinElmer) и измеряли на PerkinElmer TopCount. Спонтанное высвобождение 51Cr оценивали в клетках-мишенях, инкубированных только со средой, и максимальное высвобождение 51Cr определяли с клетками-мишенями, инкубированными в 100 мкл 0,2% Triton X-100. Процент специфичного лизиса вычисляли следующим образом: [(экспериментальное число отсчетов в минуту (имп/мин)-спонтанное высвобождение имп/мин)/(общее число имп/мин-спонтанное высвобождение имп/мин)]+/-стандартная ошибка среднего, и анализировали с использованием Microsoft Excel (Microsoft, Redmond, WA) или GraphPad Prism (GraphPad Software, La Jolla, CA).
Анализ электрического сопротивления. Индуцированный CAR T-клетками лизис клеток-мишеней in vitro оценивали в реальном времени с помощью клеточного анализатора xCELLigence Real Time Cell Analysis (ACEA Biosciences, San Diego, CA). Сначала 50 мкл RPMI с 10% FBS, 2 мМ L-глутамина, 100 ед/мл пенициллина и 100 мкг/мл стрептомицина в качестве культуральной среды для клеток-мишеней и эффекторных клеток добавляли в 96-луночный микротитровальный планшет, покрытый золотыми микроэлектродами (ACEA Biosciences) для измерения фонового сопротивления. Затем 10000 клеток-мишеней сеяли в 100 мкл среды на лунку и контролировали адгезию клеток-мишеней в течение 24-34 ч перед добавлением CAR T-клеток в 50 мкл среды в трех повторностях при соотношении E:T 1:1-1:3. Для оценки изменений сопротивления в результате индуцированного CAR T-клетками лизиса и отделения клеток-мишеней регистрировали данные каждые 15 мин в инкубаторе с регулируемой влажностью и 5% CO2 при 37°C в течение до 4 дней после добавления эффекторных клеток.
Повторная антигенная стимуляция. Для исследования противоопухолевой эффективности CAR T-клеток при повторной стимуляции антигеном in vitro, 3,3×105-1×106 T-клеток, трансдуцированных mycM28z1XXPD1DNR или mycM28z в качестве контроля, совместно культивировали с 3,3×105 облученных клеток-мишеней (соотношение E:T от 1:1 до 3:1) в 1 мл RPMI с 10% FBS, 2 мМ L-глутамина, 100 ед/мл пенициллина и 100 мкг/мл стрептомицина в 24-луночных планшетах для культур клеток. После 48 ч совместного культивирования T-клетки объединяли в пулы, подсчитывали, анализировали на экспрессию CAR с помощью проточной цитометрии и повторно сеяли при том же соотношении Е:Т с облученными клетками-мишенями в 6 циклах повторного контакта с антигеном. После 1, 3 и 6 циклов контакта с антигеном оценивали цитотоксичность CAR T-клеток с помощью анализов высвобождения 51Cr и сопротивления.
Накопление. Накопление оценивали при совместном культивировании 3,3×105 T-клеток, трансдуцированных mycM28z1XXPD1DNR или mycM28z в качестве контроля, с 3,3×105 облученных клеток-мишеней (соотношение E:T, 1:1) в 1 мл RPMI с 10% FBS, 2 мМ L-глутамином, 100 ед/мл пенициллина и 100 мкг/мл стрептомицина в 24-луночных планшетах для культур клеток. После 48 ч совместного культивирования T-клетки объединяли, подсчитывали, анализировали на предмет их экспрессии CAR с помощью проточной цитометрии и повторно сеяли при том же соотношении Е:Т с облученными клетками-мишенями до 6 циклов повторного контакта с антигеном. Количество CAR T-клеток после каждого цикла стимуляции антигеном использовали для определения накопления CAR T-клеток с течением времени по абсолютному количеству T-клеток.
Количественное определение цитокинов. Анализы высвобождения цитокинов проводили путем совместного культивирования 3,3×105 T-клеток, трансдуцированных mycM28z1XXPD1DNR или mycM28z в качестве контроля, с 3,3×103 клеток-мишеней (соотношение E:T, 1:1) в RPMI с 10% FBS, 2 мМ L-глутамином, 100 ед/мл пенициллина и 100 мкг/мл стрептомицина в 24-луночных планшетах для культур клеток. После 48 ч совместного культивирования T-клетки объединяли в пулы, подсчитывали, анализировали на предмет их экспрессии CAR с помощью проточной цитометрии и повторно сеяли при том же соотношении Е:Т с облученными клетками-мишенями до 6 циклов повторного контакта с антигеном. Для количественного определения цитокинов супернатанты собирали через 24 часа после сокультивирования для повторных стимуляций антигеном 1, 3 и 6 и центрифугировали при 800 g в течение 10 мин при комнатной температуре для удаления клеток и дебриса. Уровни цитокинов определяли в двух повторностях при использовании Human Cytokine Magnetic 30-plex Panel (Invitrogen, Carlsbad, CA) и системы MAGPIX (Luminex, Austin, TX) в соответствии с инструкциями производителей.
Ортотопическая мышиная модель. Модели ортотопических опухолей считаются более значимыми в клиническом отношении и лучше подходят для прогнозирования эффективности лекарственных препаратов, нежели стандартные подкожные модели. Благодаря тому, что опухолевые клетки имплантируют непосредственно в орган происхождения, эти опухоли намного лучше отражают исходную ситуацию (например, микроокружение), чем традиционные модели опухолей с подкожными ксенотрансплантатами. Комбинация опухолевых клеток, трансфицированных геном люциферазы, вместе с ортотопической имплантацией этих клеток позволяет неинвазивно визуализировать рост опухоли, распределение опухоли и рост метастазов.
Для создания ортотопической модели использовали самок и самцов мышей NOD/SCID гамма возрастом 6-10 недель (The Jackson Laboratory, Bar Harbor, ME). Все процедуры выполняли в соответствии с утвержденными протоколами Комитета по уходу и использованию животных центра (IACUC). Мышам делали анестезию ингиляцией изофлурана и кислорода. Для приживления ортотопических опухолей MPM выполняли прямую внутриплевральную инъекцию мезотелин-экспрессирующих клеток (8×105 опухолевых клеток) в 200 мкл бессывороточной среды через правый торакальный разрез. Опухоль приживалась у >95% мышей после инокуляции через 8-12 дней после инъекции. В случае агонии мышей умерщвляли в соответствии с рекомендациями IACUC.
Данная модель воспроизводит микроокружение опухоли человека, поскольку она отражает общий вид и гистопатологический профиль MPM (см. Фигуру 24A). Кроме того, обширная лимфоваскуляризация опухолей MPM в настоящей модели на мышах (см. Фигуру 24B) характерна для MPM человека.
BLI - чувствительный метод in vivo, который позволяет обнаруживать всего 1×103 опухолевых клеток в плевральном пространстве. Стандартизация и чувствительность основаны на собственных экспериментах авторов изобретения (Kachala et al., Clin Cancer Res. 2014; 20(4): 1020-1028; Servais et al., Clin Cancer Res. 2012; Servais et al., Curr Protoc Pharmacol. 2011; Глава 14: Unit14 21; Servais et al., PLoS One.2011; 6(10): e26722; Servais et al., J Mol Med (Berl). 2011; 89(8): 753-769). Наблюдали сильную зависимость между BLI сигналом опухоли и объемом опухоли плевры, определенным с помощью магнитно-резонансной томографии (МРТ), золотого стандарта для оценки объема опухоли (r=0,86, p<0,0001, с поправкой на внутреннюю кластеризацию у мышей; Фигуры 24C и 24D). Полученные результаты количественной BLI объясняются тем, что опухоль растет вдоль грудной стенки в виде утолщения плевральной выстилки, минимизируя глубину опухоли (Фигура 24A). Таким образом, BLI в модели ортотопического рака плевры может давать точную количественную оценку опухолевой нагрузки, обеспечивая тем самым сопоставимый стандарт для неинвазивной серийной оценки эффективности биомаркеров у живых мышей. При использовании иммуногистохимического анализа и проточной цитометрии наблюдали, что экспрессия мезотелина поддерживается в ортотопической модели MPM даже на поздних стадиях заболевания (данные не показаны).
Обработка тканей мыши. Мышей умерщвляли CO2, опухоль плевры и селезенку собирали в коническую пробирку объемом 50 мл охлаждаемой льдом RPMI-1640. Для обработки ткань измельчали через клеточное сито с ячейками 40 мкм и центрифугировали при 450 g в течение 5 мин при 4°C. Если осадок клеток выглядел кровянистым, его ресуспендировали в 2 мл буфера для лизиса ACK (Lonza, Basel, Switzerland) и инкубировали в течение 5 минут при комнатной температуре. После дополнительной стадии центрифугирования при 450 g в течение 5 минут при 4°C осадок клеток ресуспендировали в PBS с 5% бычьего сывороточного альбумина для промывки и окраски антителами для непосредственного использования в проточной цитометрии.
Иммунофлуоресценция. Самкам мышей NSG с вживленной опухолью плевры MGM вводили 5×105 mycM28z1XXPD1DNR CAR T-клеток, mycM28z CAR T-клеток или нетрансдуцированных T-клеток. Через три дня после инъекции мышей умерщвляли, выделяли плевральные опухоли, фиксировали в 4% параформальдегиде в течение ночи при комнатной температуре и обрабатывали для заливки парафином с использованием гистологического процессора Leica ASP6025 (Leica Biosystems, Wetzlar, Germany). Свеженарезанные 5 мкм парафиновые срезы окрашивали для последовательной двойной иммунофлуоресценции на Leica Bond RX (Leica Biosystems) с использованием 1,25 мкг/мл клона мышиного моноклонального антитела к CD45 2B11+PD7/26 (Dako) в течение 1 часа с детектированием 10 мин тирамидом Alexa Fluor 594 1:200 (Life Technologies, Carlsbad, CA) на Leica Bond по методике F, затем 0,03 мкг/мл кроличьего моноклонального клона D9R5G к мезотелину (Cell Signaling) в течение 1 ч с детектированием 10 мин тирамидом Alexa Fluor 488 1:200 (Life Technologies) на Leica Bond по методике F. Срезы предварительно обрабатывали буфером Leica Bond ER2 (Leica Biosystems) в течение 20 мин при 100°C перед каждым окрашиванием. После окрашивания срезы заключали в среду Mowiol для цифрового сканирования на мультиспектральном микроскопе Vectra 3.0 (Perkin Elmer) при использовании 20× объектива.
Гистологическое исследование опухолей и иммуноокрашивание. Гистопатологическую оценку опухолей проводили после окрашивания гематоксилином и эозином образцов ткани, залитых в парафин и фиксированных 4% параформальдегидом. Иммуногистохимический анализ на человеческий мезотелин проводили с мышиным IgG антителом против человеческого мезотелина (1:100; Vector Labs, Burlingame, CA) при использовании платформы Ventana. Оценку мезотелина проводил не ознакомленный с клиническими данными лаборант следующим образом: 0 (отсутствие окраски), 1 (слабая экспрессия), 2 (умеренная экспрессия) и 3 (сильная экспрессия). Распределение мезотелин-положительных опухолевых клеток по сравнению со всеми опухолевыми клетками, обнаруженными в одном образце, оценивали как 0 (отсутствуют), 1 (1-50%) и 2 (51-100%).
МРТ. МРТ проводили при использовании сканера Bruker 4.7T USR (Bruker Biospin, Ettlingen, Germany), оборудованного градиентной катушкой 400 мТ/м и изготовленным по индивидуальному заказу резонатором типа "птичья клетка" с внутренним диаметром 32 мм. Снимки МРТ грудной клетки в аксиальной проекции были получены с использованием быстрой последовательности спин-эхо RARE [время повтора (TR)=1,7 сек, время эхо-сигнала (TE)=40 мсек и 12 средних значений], запускаемой дыханием животного, чтобы уменьшить артефакты движения, вызванные дыханием. Толщина среза составляла 0,7 мм, а разрешение изображения в плоскости составляло 117×156 мм. Объемы опухоли (мм3) измеряли путем отслеживания границ опухоли в каждом срезе с помощью программы Bruker ParaVision Xtip (Bruker Biospin), а затем вычисляли по площадям областей опухолей в каждом срезе.
BLI. BLI использовали для неинвазивной визуализации опухолевой нагрузки. Мышам внутрибрюшинно вводили D-люциферин в дозе 150 мг/кг. Биолюминесценцию опухоли измеряли через 15 мин у мышей в дорсальном и вентральном положениях при использовании системы визуализации in vivo IVIS Spectrum (PerkinElmer). Средний общий поток в дорсальном и вентральном положениях был представлен как сигнал BLI в фотонах в секунду.
Количественное определение цитокинов в образцах плазмы крови мышей. Уровни цитокинов в плазме у подгруппы мышей из токсикологического исследования определяли количественно с использованием 10-плексного анализа V-Plex Mouse Proinflamasted Panel 1 (Meso Scale Diagnostics, Rockville, MD). Проводили анализ на следующие цитокины: IFN-γ, IL-1β, IL-2, IL-4, IL-5, IL-6, IL-10, IL-12p70, KC/GRO и ФНО-α. При возможности 60 мкл плазмы разбавляли в 2 раза и наносили в дублирующие лунки. Результаты (n=2 на образец) представлены в пикограммах на миллилитр плазмы. Количественное определение цитокинов выполняли в Лаборатории иммунного мониторинга при MSK.
B. Исследования тканевого мезотелина человека и in vitro CAR T-клеток
B.1. Экспрессия мезотелина в опухолевых и нормальных тканях
В опубликованных исследованиях наблюдали очень низкую экспрессию мезотелина в нормальной плевре, брюшной полости и перикарде. Обширные исследования тканей MPM, аденокарциномы легкого и трижды негативного рака молочной железы человека наряду с контрольными нормальными тканями проводили с помощью иммуногистохимического анализа мезотелина (Kachala et al., Clin Cancer Res. 2014; 20(4): 1020-1028; Servais et al., Clin Cancer Res.2012; Rizket al., Cancer Epidemiol Biomarkers Prev. 2012; 21(3): 482-486). Как показано на Фигурах 25A-25C, мезотелин повышенно экспрессируется в MPM человека и карциноме легкого по сравнению с нормальными тканями (см. Фигуру 25A). Мезотелин повышенно экспрессировался в 69% аденокарцином легкого без экспрессии в нормальных легких (см. Фигуру 25B). Аналогично, мезотелин не экспрессируется в нормальной ткани молочной железы, но повышенно экспрессируется в тройном негативном раке молочной железы (см. Фигуру 25C).
B2. Трансдукция T-клеток человека с использованием M28z1XXPD1DNR
Вирусный супернатант, кодирующий M28z1XXPD1DNR или mycM28z1XXPD1DNR, полученный из стабильных клеточных линий 293T RD114, титровали для оценки эффективности трансдукции человеческих T-клеток с помощью проточной цитометрии. T-клетки успешно трансдуцировали CAR и PD1DNR с донор-зависимыми уровнями поверхностной экспрессии в диапазоне от 32% до 73% CAR и от 22% до 64% PD1 (включая экспрессию PD1DNR и эндогенного PD1) для тестируемых разведений вирусного супернатанта (см. Фигуру 26). CAR и PD1DNR экспрессировались пропорционально из-за экспрессии бицистронного трансгена, опосредованной саморасщепляющимся P2A пептидом.
В.3. Число копий вектора (VCN)
После успешной трансдукции человеческих T-клеток с испльзованием M28z1XXPD1DNR на следующем этапе исследовали взаимосвязь между экспрессией CAR и интеграцией копий вектора в геном T-клеток. Тесная взаимосвязь между MFI CAR-положительных клеток и VCN была обнаружена у нескольких доноров и разведений вирусного супернатанта, кодирующего M28z1XXPD1DNR или mycM28z1XXPD1DNR, с получением значений R2 в диапазоне от 0,89 до 0,99 (см. Фигуру 27). Было обнаружено, что эффективность трансдукции и VCN зависят от донора, но высокие VCN (>5/клетка) наблюдали, в частности, при эффективности трансдукции >70%, а низкие VCN (<1/клетка) наблюдали, в частности, при эффективности трансдукции <35% (данные не показаны). Чтобы избежать высокого риска инсерционного мутагенеза и гарантировать эффективную трансдукцию T-клеток, титровали вирусные супернатанты для всех конструкций, чтобы получить эффективность трансдукции в диапазоне 35-70% для всех последующих экспериментов in vitro и in vivo.
В.4. M28z1XXPD1DNR CAR T-клетки оверэкспрессируют внеклеточный домен PD1
Человеческие T-клетки, трансдуцированные M28z1XXPD1DNR, экспрессируют PD1DNR, рецептор-ловушку, который не содержит внутриклеточный сигнальный домен PD1. Относительную поверхностную экспрессию белка PD1 и экспрессию мРНК в mycM28z1XXPD1DNR CAR T-клетках и mycM28z CAR T-клетках исследовали с помощью проточной цитометрии и кПЦР, соответственно. При сравнимом уровне экспрессии CAR на поверхности (64-70%, см. Фигуру 28A), окрашивание PD1 на клеточной поверхности привело к обнаружению более высоких уровней PD1 как по процентам положительных клеток (в 2 раза), так и по интенсивности (в 3,4 раза) на mycM28z1XXPD1DNR CAR T-клетках в сравнении с mycM28z CAR T-клетками (см. Фигуры 28B и 28C). Обнаружение экспрессии PD1 на клеточной поверхности было ограничено внеклеточным доменом, который присутствовал в PD1DNR, а также эндогенном PD1. Следовательно, хотя более высокая поверхностная экспрессия внеклеточного домена PD1 была вызвана и свидетельствовала об экспрессии PD1DNR, дифференцировать PD1DNR и эндогенный PD1 на уровне клеточной поверхности было невозможно.
Для дальнейшего исследования различий в экспрессии PD1DNR и эндогенного PD1 исследовали относительную экспрессию мРНК с помощью кПЦР. Чтобы отличить экспрессию PD1DNR и эндогенного PD1, были подобраны праймеры, специфичные к внеклеточному и внутриклеточному доменам PD1, а также измеряли экспрессию мРНК внеклеточного и внутриклеточного доменов PD1 mycM28z1XXPD1DNR и mycM28z CAR T-клеток по сравнению с нетрансдуцированными T-клетками. mycM28z CAR T-клетки не экспрессируют PD1DNR и, следовательно, экспрессируют только эндогенный PD1 при эквимолярном соотношении внеклеточного домена к внутриклеточному. Тогда как экспрессия внутриклеточного домена была исключительной только в случае эндогенного PD1, внеклеточный домен экспрессировался как PD1DNR, так и эндогенным PD1. Было обнаружено, что mycM28z CAR T-клетки экспрессировали в 4 раза более высокие уровни внеклеточных и внутриклеточных доменов PD1 по сравнению с нетрансдуцированными T-клетками. Однако mycM28z1XXPD1DNR CAR T-клетки демонстрировали 157-кратную апрегуляцию внеклеточного домена PD1; нетрансдуцированные T-клетки демонстрировали только двукратную апрегуляцию внутриклеточного домена PD1 (см. Фигуру 28D).
Таким образом, эти данные подтверждают, что PD1DNR повышенно экспрессируется как на уровне мРНК, так и на уровне белка в сравнении с эндогенным PD1 в mycM28z1XXPD1DNR CAR T-клетках. Это открытие дает основание для блокады собственной контрольной точки T-клеток.
В.5. Функциональное сравнение CAR T-клеток M28z1XXPD1DNR с myc-меткой и без нее
Для облегчения обнаружения экспрессии CAR, M28z1XXPD1DNR CAR T-клетки были созданы с myc-меткой, слитой с N-концом scFv против мезотелина, что привело к получению mycM28z1XXPD1DNR. Чтобы исключить любое возможное взаимодействие myc-метки с функцией CAR, проводили прямое сравнение противоопухолевой эффективности M28z1XXPD1DNR (без метки) и mycM28z1XXPD1DNR CAR T-клеток. Человеческие T-клетки, полученные у 3 независимых доноров, трансдуцированные как M28z1XXPD1DNR, так и mycM28z1XXPD1DNR, при аналогичных уровнях трансдукции (37-63%, как определено с помощью проточной цитометрии с клетками, окрашенными козьим F(ab')2 фрагментом, специфичным против человеческого F(ab')2) не демонстрировали различий в кинетике и общем лизисе клеток-мишеней MGM при различных соотношениях E:T (см. Фигуру 29).
В.6. mycM28z1XXPD1DNR CAR T-клетки опосредуют антигенспецифичный, HLA-независимый лизис опухоли
Цитотоксическую активность mycM28z1XXPD1DNR в сравнении с mycM28z CAR T-клетками определяли против панели линий опухолевых клеток, включая клетки мезотелиомы человека (MSTO-211H) с (GM) и без (G) экспрессии мезотелина, а также с конститутивной экспрессией PD-L1, с помощью анализа высвобождения 51Cr. mycM28z1XXPD1DNR CAR T-клетки эффективно лизировали мишени MGM и MGM-PDL1, как и mycM28z CAR T-клетки, при совместном культивировании в течение 18 часов с мезотелин-экспрессирующими опухолевыми клетками при различиных соотношениях E:T, как показано в результатах анализа цитотоксичности ниже (см. Фигуру 30). Неспецифический лизис либо mycM28z1XXPD1DNR, либо mycM28z CAR T-клетками в отношении опухолевых клеток MSTOG, отрицательных на мезотелин, не наблюдали. Нетрансдуцированные T-клетки не показали уничтожения ни одной из мишеней. Эти результаты подтверждают, что M28z1XXPD1DNR CAR T-клетки убивают клетки-мишени мезотелин-специфическим и HLA-независимым образом.
В.7. mycM28z1XXPD1DNR CAR T-клетки накапливаются
Для исследования, поддерживают ли mycM28z1XXPD1DNR CAR T-клетки накопление T-клеток при повторной антигенной стимуляции мезотелин-экспрессирующими опухолевыми клетками с индуцируемой экспрессией PD-L1 (MGM) или конститутивной экспрессией PD-L1 (MGM-PDL1), экспансию mycM28z1XXPD1DNR CAR T-клеток определяли количественно и сравнивали с экспансией mycM28z CAR T-клеток. В течение 6 повторных стимуляций антигеном mycM28z1XXPD1DNR CAR T-клетки размножились до 622 раз, аналогично mycM28z CAR T-клеткам (см. Фигуру 31).
В.8. Противоопухолевая эффективность mycM28z1XXPD1DNR CAR T-клеток при повторной антигенной стимуляции
При первом контакте с антигеном, mycM28z1XXPD1DNR CAR T-клетки демонстрировали E:T-зависимую цитотоксичность в отношении клеток-мишеней MGM и MGM-PDL1, но не проявляли различий в цитотоксичности по сравнению с mycM28z CAR T-клетками (см. Фигуру 32). Для исследования цитотоксической способности mycM28z1XXPD1DNR и mycM28z CAR T-клеток во время постоянного контакта с антигеном (или высокого антигенного стресса), CAR T-клетки многократно совместно культивировали с облученными клетками-мишенями MGM или MGM-PDL1 каждые 48 ч при соотношении E:T 3:1 в течение 4 циклов. В конце третьего цикла образец CAR T-клеток подвергали четвертой стимуляции антигеном в анализе цитотоксичности 51Cr. mycM28z1XXPD1DNR и mycM28z CAR T-клетки продемонстрировали сравнимую цитотоксичность во время четвертой стимуляции антигеном (см. Фигуру 33).
Затем для дальнейшего усиления антигенного стресса, имитирующего высокую опухолевую нагрузку при солидных опухолях, CAR T-клетки совместно культивировали с клетками-мишенями при соотношении E:T 1:1 в пятом и шестом циклах антигенной стимуляции. В конце шестого цикла собирали еще один образец CAR T-клеток и подвергали седьмому циклу антигенной стимуляции в анализе цитотоксичности 51Cr. Цитотоксичность при седьмой антигенной стимуляции у mycM28z CAR T-клеток против обеих линий клеток-мишеней была существенно снижена. Напротив, mycM28z1XXPD1DNR CAR T-клетки сохраняли цитотоксичность по отношению к клеткам-мишеням. mycM28z1XXPD1DNR CAR T-клетки по сравнению с mycM28z CAR T-клетками продемонстрировали лучшее уничтожение опухолевых клеток с клетками-мишенями с высокой конститутивной экспрессией PD-L1 (см. Фигуру 33), хотя цитотоксичность была снижена по сравнению с первой и четвертой антигенными стимуляциями. В совокупности эти данные показывают, что mycM28z CAR T-клетки достигают состояния истощения при длительном воздействии антигена, тогда как mycM28z1XXPD1DNR CAR T-клетки способны поддерживать противоопухолевую активность даже в условиях высокого антигенного стресса. Наблюдаемые эффекты зависели от биологических параметров, таких как донор, соотношение E:T и время совместного культивирования между опухолью и CAR T-клетками.
В.9. Мишень-стимулируемое высвобождение цитокинов mycM28z1XXPD1DNR CAR T-клетками
Секрецию эффекторных цитокинов mycM28z1XXPD1DNR и mycM28z CAR T-клетками при повторной антигенной стимуляции оценивали с помощью анализа Luminex. Как mycM28z1XXPD1DNR, так и mycM28z CAR T-клетки секретировали высокие уровни IL-2, IFN-γ и ФНО-α после первой антигенной стимуляции. Однако секреция эффекторных цитокинов обоими CAR T-клетками снижалась при повторной стимуляции антигеном (см. Фигуру 34).
C. Исследования in vivo
С.1. Противоопухолевая эффективность mycM28z1XXPD1DNR CAR T-клеток, визуализируемая опухолевыми клетками ffLuc
При использовании ортотопической модели проводили серию экспериментов на мышах in vivo для изучения специфичности и эффективности mycM28z1XXPD1DNR CAR T-клеток путем измерения опухолевой нагрузки и выживаемости животных. Серийную BLI использовали для подтверждения приживления опухоли, для выравнивания опухолевой нагрузки между группами вмешательства до начала терапии T-клетками, а затем для измерения ответа на терапию.
Для исследования противоопухолевой эффективности mycM28z1XXPD1DNR CAR T-клеток, однократную низкую дозу 3×104 CAR T-клеток вводили внутриплеврально самкам мышей NSG через 13 дней после инокуляции ортотопической опухоли MGM. Низкую дозу специально выбрали для имитации высокой антигенной нагрузки опухоли, с которой сталкиваются CAR T-клетки. По сравнению с контрольными мышами, получавшими P28z CAR T-клетки, мыши, получавшие одну дозу mycM28z1XXPD1DNR CAR T-клеток, показали значительное снижение опухолевой нагрузки через 15 дней после введения T-клеток (p=0,0002) (см. Фигуру 35). На 15 день после лечения, мыши, которым вводили P28z CAR T-клетки, начали агонизировать, как и ожидали, из-за высокой опухолевой нагрузки, тогда как у мышей, которым вводили mycM28z1XXPD1DNR CAR T-клетки, никаких признаков токсического действия не наблюдали.
Наблюдая за эффективностью и ерадикацией опухоли при однократной дозе 3×104 mycM28z1XXPD1DNR CAR T-клеток/мышь (что соответствует 1,2×106-1,5×106 клеток/кг; при весе мыши 20-25 г), авторы изобретения решили повысить уровень дозы в 3-4 раза для изучения токсического действия у мышей (описано в Разделе 3 этого Примера (под заголовком "Доклиническая токсикология")).
В последующем эксперименте самкам мышей NSG с прижившейся плевральной опухолью MGM-PDL1 через 11 дней после инокуляции опухоли делали однократное внутриплевральное введение 1×105 или 5×104 mycM28z1XXPD1DNR CAR T-клеток на мышь (соотношение E:T, 1:1000-1:2000; от 2,5×106 до 5×106 клеток/кг; средний вес мыши 20 г) или 1×105 mycM28z CAR T-клеток/мышь в качестве контроля. Отношения E:T вычисляли на основе количественной оценки опухолевой нагрузки, как описано ранее (Servais et al., Curr Protoc Pharmacol. 2011; Глава 14: Unit14 21; Servais et al., PLoS One. 2011; 6(10): e26722).
Серийная визуализация опухоли с D-люциферином (люциферин для ffluc) показала снижение опухолевой нагрузки согласно BLI уже через 5 дней после введения CAR T-клеток с полным устранением опухоли (фоновый сигнал BLI) примерно в день 19 у мышей, получавших 1×105 mycM28z1XXPD1DNR CAR T-клеток, и примерно в день 26 у мышей, получавших 1×105 mycM28z CAR T-клеток (см. Фигуры 36A и 36B). Необработанные мыши погибали через 9-12 дней после начала лечения (см. Фигуру 36B). Эрадикация опухоли поддерживалась mycM28z1XXPD1DNR CAR T-клетками (доза 1×105 и 5×104) до завершения исследования на день 68. Однако у мышей, получавших mycM28z CAR T-клетки, умерщвленных до 68 дня из-за состояния агонии и потери веса, вскрытие показало присутствие опухоли. Мыши, получавшие любую дозу mycM28z1XXPD1DNR CAR T-клеток, набирали вес линейно в течение всего исследования, тогда как мыши, получавшие mycM28z CAR T-клетки, теряли вес к концу исследования (см. Фигуру 36C). Медианная выживаемость составляла 12 дней у необработанных мышей и 50 дней у мышей, получавших 1×105 mycM28z CAR T-клеток; медианная выживаемость не была достигнута у мышей, получавших какую-либо дозу mycM28z1XXPD1DNR CAR T-клеток (см. Фигуру 36D). Выживаемость была значительно увеличена у мышей, получавших mycM28z1XXPD1DNR CAR T-клетки, по сравнению с мышами, получавшими mycM28z CAR T-клетки (p=0,0085 для 5×104 mycM28z1XXPD1DNR и p=0,0427 для 1×105 mycM28z1XXPD1DNR по сравнению с 1×105 mycM28 CAR T-клеток). У мышей, получавших mycM28z1XXPD1DNR CAR T-клетки, явных клинических признаков токсического действия не наблюдали.
С.2. Обнаружение mycM28z1XXPD1DNR CAR T-клеток в первичной опухоли
В подгруппе мышей после интраплевральной инъекции 5×105 mycM28z1XXPD1DNR CAR T-клеток, mycM28z CAR T-клеток или нетрансдуцированных T-клеток мышам NSG, несущим плевральную опухоль MGM, опухоль плевры извлекали в течение 3 дней после инъекции и исследовали на инфильтрацию человеческими T-клетками при окраске на CD45 человека и мезотелин опухоли человека с помощью иммунофлуоресценции.
У мышей, получавших нетрансдуцированные T-клетки, только несколько нетрансдуцированных T-клеток были обнаружены в периферии и паренхиме опухоли, тогда как mycM28z1XXPD1DNR CAR T-клетки и mycM28z CAR T-клетки были обнаружены в более высокой плотности в перитуморальной области и на границе между опухолью и перитуморальной областью (см. Фигуру 37). Эти данные позволяют предположить, что регионарно (внутриплеврально) вводимые мезотелин-направленные T-клетки концентрируются в перитуморальной области и инфильтрируют с периферии опухоли в опухоль.
С.3. Противоопухолевая активность mycM28z1XXPD1DNR CAR T-клеток при повторном заражении опухолью in vivo
Для исследования функционального персистирования mycM28z1XXPD1DNR CAR T-клеток, мышей с плевральной опухолью MGM-PDL1 (n=5), получавших однократную внутриплевральную дозу 1×105 mycM28z1XXPD1DNR или mycM28z CAR T-клеток, повторно заражали внутрибрюшинно повышаемыми дозами опухолевых клеток MGM. Повторное заражение начинали через 68 дней после внутриплеврального введения T-клеток и после устранения опухоли плевры с начальной повторной дозой 2×106 опухолевых клеток. Дозу опухоли повышали до 11×106 опухолевых клеток в течение 10 повторных заражений каждые 4-8 дней (см. Фигуру 38A). Повторное заражение опухолью было связано с усилением сигнала BLI вскоре после каждого введения опухоли, после которого следовало снижение BLI, что указывает на регрессию опухоли, опосредованную T-клетками (см. Фигуру 38B). Пиковые сигналы BLI повышались после последующего увеличения доз опухолевых клеток, при этом мыши, получавшие mycM28z CAR T-клетки, демонстрировали значительно более высокое увеличение сигнала BLI по сравнению с мышами, получавшими такую же дозу mycM28z1XXPD1DNR CAR T-клеток. В частности, сигнал BLI у мышей, обработанных mycM28z1XXPD1DNR CAR T-клетками, достигал пика вскоре после каждого повторного заражения опухолью, но возвращался к исходному сигналу BLI даже при максимальной дозе повторного заражения (см. Фигуру 38B). Напротив, мыши, получавшие mycM28z CAR T-клетки, показали снижение сигнала BLI после начального увеличения BLI до 5 повторных заражений опухолью, однако, в конечном счете, они теряли способность контролировать повторное приживление опухоли после более высоких доз опухоли, что привело к постоянному повышению сигнала BLI и опухолевой нагрузки и агональному состоянию. mycM28z1XXPD1DNR CAR T-клетки препятствовали приживлению внутрибрюшинной опухоли в течение 10 повторных заражений, даже через >126 дней после однократной внутриплевральной дозы 1×105 CAR T-клеток, без каких-либо явных клинических признаков токсичности. Эти данные показывают, что mycM28z1XXPD1DNR CAR T-клетки способны контролировать опухоль не только локально в плевральном пространстве, но также и в удаленных частях тела. In vivo, mycM28z1XXPD1DNR CAR T-клетки оставались функциональными при длительном контакте с антигеном в результате повторной антигенной стимуляции, и долгое время персистировали, тогда как mycM28z CAR T-клетки становились дисфункциональными при повторной антигенной стимуляции, что указывает на превосходное функциональное персистирование и повышенную долговременную противоопухолевую активность mycM28z1XXPD1DNR CAR T-клеток. Было подтверждено, что такая повышенная эффективность не вызвана реакцией трансплантат против хозяина. Вводили мишени, не экспрессирующие антиген, и отметили усиление BLI опухоли без противоопухолевого ответа, подтверждая, что противоопухолевая эффективность является антигенспецифической.
С.4. Противоопухолевая эффективность M28z1XXPD1DNR T-клеток для клинического применения
Цель данного исследования состояла в подтверждении противоопухолевой эффективности криоконсервированных M28z1XXPD1DNR CAR T-клеток, которые были созданы в Лаборатории клеточной терапии и клеточной инженерии MSK (CTCEF). Перед внутриплевральной инъекцией аликвоты криоконсервированных M28z1XXPD1DNR CAR T-клеток размораживали в RPMI-1640 с 10% FBS, два раза промывали в RPMI-1640 без FBS и ресуспендировали в RPMI-1640 без FBS в качестве среды для инъекции. Жизнеспособность CAR T-клеток после размораживания и перед инъекцией определяли как 88% при окрашивании акридиновым оранжевым/йодистым пропидием. CAR T-клетки вводили внутриплеврально самкам мышей NSG, несущих плевральные опухоли MGM, в дозе 6×104 или 2×105 жизнеспособных CAR T-клеток/мышь (n=8-10). Серийная BLI опухолей обнаружила устранение опухолей на 16 день у мышей, получавших 2×105 CAR T-клеток (см. Фигуру 39A). У мышей, которым вводили 6×104 CAR T-клеток, наблюдали регрессию и устранение опухолей в день 29 (см. Фигуру 39A). Никакой потери веса не наблюдалось ни в одной из групп лечения, тогда как необработанные мыши с опухолью теряли вес и погибали в течение 19 дней после начала лечения (см. Фигуры 39B и 39C). У мышей, получавших CAR T-клетки, токсическое действие не наблюдали, и 100% обработанных мышей оставались живыми в конце периода наблюдения (день 70, см. Фигуру 39C). Это исследование подтвердило, что криоконсервированные M28z1XXPD1DNR CAR T-клетки, полученные с использованием исходных векторов, полученных для предполагаемого клинического исследования, продемонстрировали высокую жизнеспособность после размораживания, демонстрировали противоопухолевую эффективность in vivo и хорошо переносились мышами.
3. Доклиническая токсикология
A. Краткое описание доклинических исследований безопасности
Связывание и активность M28z1XXPD1DNR CAR T-клетками специфичны в отношении мезотелина человека, поэтому не существует идеальных фармакологически релевантных видов, на которых можно было бы проводить доклинические исследования безопасности. Кроме того, вариабельность профилей экспрессии антигенов-мишеней и различия в механизмах выведения и иммуногенности человеческих полипептидов, таких как CAR, у иммунокомпетентных мышей, препятствуют применению животных для прогнозирования токсического действия CAR T-клеток у человека. Поскольку M28z1XXPD1DNR CAR T-клетки обладают релевантным фармакодинамическим эффектом (цитокины, накопление, регрессия опухоли) в ортотопической модели на мышах с иммунодефицитом, экспрессирующих мезотелин человека, провели исследование безопасности на этой ксеногенной модели. Это было исследование по стандартам надлежащей лабораторной практики (GLP), проведенное в центре MSK в Центральной лаборатории оценки противоопухолевой активности. В этом разделе обсуждается схема, методы и результаты данного исследования.
Выбранная доза CAR T-клеток для этого исследования составляла 1×105 mycM28z1XXPD1DNR CAR T-клеток. Эта доза была выбрана потому, что она в 3-4 раза выше, чем минимальная испытанная эффективная доза (3×104 mycM28z1XXPD1DNR CAR T-клеток) для лечения ортотопических опухолей мезотелиомы в нашей доклинической модели на мышах. Важно отметить, что выбранная доза CAR T-клеток (1×105 клеток/мышь или 5×106 клеток/кг) в 5 раз выше, чем начальная доза, предложенная в текущем исследовании (1×106 клеток/кг). В опубликованных авторами изобретения исследованиях было показано, что мезотелин-направленный CAR с PD1DNR (Cherkassky et al., J Clin Invest. 2016; 126(8): 3130-3144) при дозе от 40000 до 50000 CAR T-клеток устраняет высокую плевральную опухолевую нагрузку у мышей с ортотопической мезотелиомой плевры.
CAR T-клетки доставляли однократно путем внутриплевральной инъекции мышам NSG, несущим ксенотрансплантаты мезотелиомы в плевральной полости. В отличие от других средств, таких как антитела, для которых внутриплевральное введение изначально ограничено плевральной полостью, было показано, что у мышей, как и у человека, внутриплеврально введенные CAR T-клетки циркулируют системно в течение одного или двух дней и не ограничиваются плевральной полостью (Adusumilli et al., Sci Transl Med. 2014; 6(261): 261ra151; Cherkassky et al., J Clin Invest. 2016; 126(8): 3130-3144; Adusumilli et al., Cancer Res. 2019; 79(13)). В частности, авторы изобретения наблюдали, что у мышей, как и у человека, внутриплеврально введенные CAR T-клетки активируются антигеном и пролиферируют в 5-10 раз выше, чем первоначально введенная доза, в течение короткого периода времени (Adusumilli et al., Sci Transl Med. 2014; 6(261): 261ra151; Cherkassky et al., J Clin Invest. 2016; 126(8): 3130-3144), поэтому фактическое количество CAR T-клеток, протестированное в данном исследовании, в 5-10 раз превышает первоначально введенную дозу в течение короткого периода времени.
При оценке безопасности M28z1XXPD1DNR CAR T-клеток при медицинском применении важны следующие факторы.
1. Предыдущий опыт медицинского применения CAR T-клеток показывает, что превышение фармакодинамического эффекта является основной причиной нежелательных явлений, которые можно контролировать и сдерживать. В клиническом исследовании фазы I, проведенном авторами изобретения, не было сообщений о побочных эффектах, связанных с внеопухолевой токсичностью мезотелин-направленных CAR T-клеток (Adusumilli et al., Cancer Res.2019; 79(13)).
2. В исследованиях in vitro было обнаружено, что фармакологическая активность mycM28z1XXPD1DNR CAR T-клеток коррелирует с экспрессией мезотелина на поверхности клетки-мишени.
3. В созданной авторами изобретения ортотопической модели MPM специфическая цитотоксичность и повышенная выживаемость наблюдались после однократной внутриплевральной инъекции mycM28z1XXPD1DNR CAR T-клеток мышам, несущим опухоли MPM. Без лечения mycM28z1XXPD1DNR CAR T-клетками эти мыши погибли бы в течение 20-22 дней после имплантации опухоли. В течение 7 дней опухолевая нагрузка существенно снижалась, а у животных выздоровление сохранялось после 68 дней; Напротив, у необработанных контрольных животных медианная выживаемость составляла 12 дней, а у получавших mycM28z контрольных животных медианная выживаемость составляла 50 дней.
Смертность и тяжесть заболевания, вес, клинические признаки, гематология и клиническая биохимия, макроскопические результаты вскрытия и гистопатологические данные оценивали у 96 (48 самцов и 48 самок) мышей NSG (Jackson Laboratory) с 8-дневными ортотопическими опухолями MGM, случайным образом распределенных в группы контроля и лечения. Была выбрана доза 1×105 клеток/мышь (приблизительно 5×106 клеток/кг) в RPMI-1640, что соответствует по меньшей мере приблизительно 3-4-кратной минимальной эффективной дозе, определенной в контрольных экспериментах in vitro и in vivo на этой модели (3×104 клеток/мышь). Доза и режим вскрытия были выбраны рационально: (а) хотя более высокая начальная тестовая доза может позволить исследовать любые немедленные нежелательные эффекты от введения дозы (такие эффекты не наблюдались в текущих клинических исследованиях), биология и фармакология не отражают функциональное персистирование и пролиферацию mycM28z1XXPD1DNR CAR T-клеток (т.е. в микроокружении солидной опухоли важно обеспечить, чтобы относительно большее количество CAR T-клеток присутствовало в опухоли/теле в течение длительного периода времени, чем при кратковременной кинетике эрадикации опухоли, вызванной высокой дозой), и (b) день 14 был выбран, потому что опухоль либо в значительной степени регрессировала, либо была устранена в этот момент времени (как подтверждали данные BLI или вскрытия из предыдущих экспериментов) (Adusumilli et al., Sci Transl Med. 2014; 6(261): 261ra151; Cherkassky et al., J Clin Invest. 2016; 126(8): 3130-3144). Умерщвление и вскрытие в этот момент времени позволяют исследовать любые целевые внеопухолевые эффекты (scFv, используемый в настоящем CAR, реагирует с мезотелином мыши) (Feng et al., Mol Cancer Ther. 2009) в отношении нормальных тканей, в частности плевры, брюшной полости и перикарда, с низкими уровнями экспрессии мезотелина после пиковой экспансии CAR T-клеток при отсутствии опухолевой нагрузки с высокой экспрессией мезотелина.
mycM28z1XXPD1DNR CAR T-клетки или контрольную среду вводили однократно путем ортотопической инъекции в день исследования 1 (самцам мышей) или день исследования 2 (самкам мышей). Всех животных наблюдали на предмет смертности и тяжести заболевания два раза в неделю до -8 дня исследования с последующим ежедневным мониторингом (рабочие дни) до 1 дня исследования. После введения дозы животных наблюдали ежедневно до конца исследования (день 15 исследования). Массу тела регистрировали два раза в неделю до -8 дня исследования с последующим ежедневным мониторингом (рабочие дни) до дня 1 исследования. После введения дозы массу тела регистрировали ежедневно до конца исследования (день 15 исследования). Клинические признаки регистрировали два раза в неделю до 1 дня исследования с последующим ежедневным мониторингом с 1-го по 15-й день исследования. В день 2 исследования (промежуточное умерщвление самцов мышей), день 3 исследования (промежуточное умерщвление самок мышей), день 14 исследования (заключительное умерщвление самцов мышей) и день 15 исследования (заключительное умерщвление самок мышей) мышам давали наркоз изофлураном и забирали кровь для исследований гематологии и клинической биохимии. Для макроскопического и полного вскрытия ткани собирали и фиксировали в формалине. Во время вскрытия ткани не отбрасывали. Во время вскрытия макроскопическое исследование каждого животного проводили члены Центральной лаборатории оценки противоопухолевой активности. Любые макроскопические поражения или другие отклонения от нормы регистрировали с использованием стандартной терминологии и предоставляли лаборанту для сопоставления с результатами микроскопического исследования. Для гистопатологического анализа все ткани вскрытых животных сохраняли в формалине. По истечении не менее 24 часов в фиксаторе, ткани обрабатывали и заливали парафином. Затем парафиновые блоки разрезали на срезы толщиной 4 мкм. Затем полученные неокрашенные слайды окрашивали гематоксилином и эозином. Затем слайды отправляли в HSRL для анализа сертифицированным врачом-лаборантом. Поражения регистрировали с использованием морфологических диагнозов в соответствии со стандартной номенклатурой. В дни исследования 9 (самцы мышей) и 10 (самки мышей) у подгруппы мышей собирали плазму крови, а оценку цитокинов проводили в Центральной лаборатории иммунного мониторинга в MSK (не GLP). Кроме того, селезенку и опухоль извлекали у подгруппы мышей для идентификации mycM28z1XXPD1DNR CAR T-клеток с помощью проточной цитометрии (не GLP). В дни исследования -1/1, 7/8 и 14/15 подгруппу животных визуализировали с использованием люциферина (дорсально/вентрально) для оценки опухолевой нагрузки и эффективности исследуемого препарата.
Смертность или тяжесть заболевания животных в этом исследовании не наблюдали, за исключением 2 контрольных животных в когорте визуализации, которые были подвергнуты выборочному умерщвлению из-за тяжелого состояния и затрудненного дыхания в дни исследования 12 и 14 (дни 20-22 после введения опухоли). Предыдущая работа в лаборатории авторов изобретения показала, что контрольные животные могут погибать из-за опухолевой нагрузки примерно через 20-22 дня после введения опухоли (Servais et al., Clin Cancer Res.2012; Servais et al., Curr Protoc Pharmacol. 2011; Глава 14: Unit14 21; Adusumilli et al., Sci Transl Med.2014; 6(261): 261ra151; Cherkassky et al., J Clin Invest. 2016; 126(8): 3130-3144; Servais et al., PLoS One. 2011; 6(10): e26722). Поэтому эти умерщвления были незапланированными, но не неожиданными. Смертность или тяжесть заболевания при введении исследуемого препарата не отслеживали.
Животные, получавшие контрольную среду, показали прогрессирующее снижение массы тела во время исследования и значительную разницу в весе по сравнению с контрольными мышами, не получавшими опухоли, и мышами, получавшими mycM28z1XXPD1DNR CAR T-клетки. Это было связано с увеличением опухолевой нагрузки у контрольных животных.
У мышей, получавших mycM28z1XXPD1DNR CAR T-клетки, значимых клинических признаков не наблюдали. У одной мыши, получавшей исследуемый препарат, наблюдали легкое шелушение, которое связывали с раздражением, вызванным хирургическими зажимами, поскольку никакие другие животные не пострадали, и активность животных была нормальной. Мыши выглядели нормальными на протяжении всего периода наблюдения.
Самки мышей, получавшие mycM28z1XXPD1DNR CAR T-клетки, в группе 12 (окончательное умерщвление в день 15 исследования) имели высокое среднее процентное значение моноцитов (среднее, 18,44%, n=5) (p≤0,0001) по сравнению с группой 10 (опухоль с контролем средой) (среднее, 3,34%, n=5). Референсный диапазон, установленный для процента моноцитов, составляет 0,9-18%. Однако это не коррелировало с данными микроскопических исследований. Других значимых или аномальных результатов при оценке показателей общего анализа крови не наблюдали. Любые различия между группами, получавшими исследуемый препарат, и группами, получавшими соответствующую среду, находились в пределах нормальных референсных диапазонов или не были биологически релевантными или статистически значимыми.
Самцы мышей, получавшие mycM28z1XXPD1DNR CAR T-клетки в группе 11 (окончательное умерщвление в день 14 исследования), имели низкое среднее значение общего белка (среднее, 3,83 г/дл, n=5) (p=0,0022) по сравнению с группой 9 (опухоль с контролем средой) (среднее, 4,68 г/дл, n=4). Референсный диапазон, установленный для общего белка, составляет 4,1-6,4 г/дл. Однако это не коррелировало с данными микроскопических исследований. Никаких других побочных эффектов в отношении показателей клинической биохимии при введении исследуемого препарата не наблюдали. Любые различия между группами, получавшими исследуемый препарат, и группами, получавшими соответствующую среду, находились в пределах нормальных референсных диапазонов или не были биологически релевантными или статистически значимыми.
Во время вскрытия опухолевую ткань не собирали, но наблюдали у многих животных при промежуточном умерщвлении, как и предполагалось. Во время окончательной умерщвления опухолевая нагрузка была заметна у контрольных животных, получавших только среду, однако в большинстве случаев у животных, получавших исследуемый препарат, наблюдались незначительные опухолевые очаги или они полностью отсутствовали. Макроскопические наблюдения при вскрытии отдельных животных включали покрытую пятнами печень, уменьшенную селезенку, синий семенной пузырек, темно-зеленый желчный пузырь, синий желчный пузырь, маслянистую почку, пузырь в печени и белое пятно на селезенке. Ни один из этих результатов не коррелировал с результатами микроскопических исследований. Небольшая селезенка ожидается у мышей фенотипа NSG вследствие деплеции лимфоцитов.
Обзор результатов гистопатологических исследований показал отсутствие микроскопических данных в дни промежуточного (день 2/3 исследования) и окончательного (день 14/15 исследования) умерщвления, связанных с острой или отсроченной токсичностью в результате введения исследуемого препарата. Результаты микроскопических исследований животных в группах 5 и 6 (исследуемый образец; промежуточное умерщвление) включали наличие смешанной клеточной инфильтрации в ксенотрансплантатных опухолях в легких. Считалось, что это связано с введением исследуемого препарата, но не связано с какой-либо токсичностью исследуемого препарата. Этот результат подтверждался при отдельном исследовании с помощью иммунофлуоресцентного окрашивания mycM28z1XXPD1DNR CAR T-клеток в первичной опухоли у мышей, получавших интраплевральную терапию (см. Раздел 2.C.2 этого Примера). Было установлено, что любые другие наблюдаемые результаты возникали спорадически, с такой же частотой, что и в контроле, или были обычными для используемых видов/штаммов.
In vivo, BLI в день -1/1 исследования показала успешное введение опухоли у всех животных в каждой группе. После введения контрольной среды опухолевая нагрузка у животных в группах самцов и самок мышей увеличивалась в каждой точке времени при проведении измерения, при этом двум животным потребовалось досрочное проведение визуализационного обследования из-за тяжелого состояния. После введения исследуемого препарата опухолевая нагрузка у животных в группах самцов и самок мышей увеличивалась через 1 неделю после инъекции; однако через 2 недели нагрузка существенно снизилась. Человеческие T-клетки были обнаружены в ткани селезенки и опухоли через 8 дней после внутриплеврального введения у мышей, получавших mycM28z1XXPD1DNR CAR T-клетки, но не у мышей, получавших среду. Уровни цитокинов в плазме мышей, полученные в той же точке времени, показали несколько повышенные уровни IL-4 у мышей, получавших CAR T-клетки, по сравнению с мышами, получавшими контрольную среду. Уровни IL-10, IL-6, KC/GRO и ФНО-α обычно были низкими и не демонстрировали значимых различий между мышами, получавшими CAR T-клетки, и мышами, получавшими контрольную среду. IFN-γ, IL-12p70, IL-1β, IL-2 и IL-5 не обнаруживали (ниже предела количественного определения).
Целью данного исследования состояла в оценке острой и отсроченной токсичности mycM28z1XXPD1DNR CAR T-клеток у мышей NSG после однократной ортотопической инъекции. В ходе исследования собирали и анализировали данные по массе тела, клиническим признакам, общему анализу крови, клинической биохимии и гистопатологическим данным. Результаты этого исследования показывают, что однократное ортотопическое введение 1×105 mycM28z1XXPD1DNR CAR T-клеток в модели ксенотрансплантата мезотелиомы хорошо переносится.
Б. Методы
Система тестирования. Эксперименты проводили на самцах и самках мышей NSG возрастом 6-8 недель из Jackson Laboratory. Мыши в группах опухоли получали 800000 клеток MGM/мышь посредством внутриплевральной инъекции в день 1 исследования (самцы мышей) и день 2 исследования (самки мышей). Предполагали, что у этих мышей симптомы плеврального заболевания разовьются примерно через 5-20 дней после инъекции.
Исследуемый препарат. Исследуемый препарат (mycM28z1XXPD1DNR CAR T-клетки) был приготовлен авторами изобретения в MSK. МКПК от здорового донора размораживали 11.05.2019 и трансдуцировали 11.07.2019 ретровирусными частицами, кодирующими mycM28z1XXPD1DNR. Перед инъекцией трансдуцированные МКПК поддерживали в среде RPMI-1640 с 10% FBS, 100 ед/мл пенициллина, 100 мкг/мл стрептомицина и 20 ед/мл IL-2. В дни инъекции 13.11.2019 (самцы мышей) и 14.11.2019 (самки мышей) трансдуцированные клетки объединяли в пулы, анализировали с помощью проточной цитометрии на экспрессию CD3 и CAR, промывали и ресуспендировали в среде (RPMI-1640 без FBS и без фенолового красного) и держали во льду до инъекции.
mycM28z1XXPD1DNRCAR T-клетки ресуспендировали в носителе до конечной концентрации 5×105 жизнеспособных CAR T-клеток/мл. Измеряли жизнеспособность клеток. Затем приготовленный раствор переносили в виварий во льду для немедленного применения. Исследуемый препарат, готовый к применению и хранящийся во льду, считался стабильным в этих условиях на протяжении всего периода исследования. Приготовление препарата CAR T-клеток проводили в лаборатории авторов изобретения в ламинарном боксе при комнатной температуре в асептических условиях. Жизнеспособность и экспрессию CAR определяли до и после введения дозы.
Среда. В качестве среды, используемой при изготовлении композиций CAR T-клеток и для введения контрольной группе, использовали стерильную среду RPMI-1640 без FBS и без фенолового красного (GIBCO, номер по кат. 32404, номер партии 2099376). Среду переносили в виварий во льду для немедленного применения. Среда, готовая к применению и хранящаяся во льду, считалась стабильной в этих условиях на протяжении всего периода исследования, что подтверждалось сертификатом анализа от производителя. Приготовление среды осуществляли в лаборатории авторов изобретения в ламинарном боксе при комнатной температуре в асептических условиях.
Схема исследования. Все когорты были рандомизированы в группы исследования перед днем 1 исследования. По прибытии животных случайным образом отбирали из транспортировочных клеток и помещали в соответствующие группы лечения, как показано в Таблице 9 ниже. Мышей идентифицировали при помощи ушного перфоратора.
Мыши в группах опухоли получали 8×105 клеток MGM посредством ортотопической инъекции в плевру за 8 дней до введения исследуемого препарата. mycM28z1XXPD1DNR CAR T-клетки или контрольную среду вводили аналогичным образом посредством ортотопической инъекции один раз в день 1 исследования (самцы мышей) или день 2 исследования (самки мышей). Опухолевые клетки, среду и исследуемый препарат вводили в объеме инъекции 200 мкл/мышь.
Группа
Опухоль - Контрольная среда: Мыши с опухолью MGM+RPMI1640
Опухоль - Исследуемый препарат: Мыши с опухолью MGM+1×105 mycM28z1XXPD1DNR CAR T-клеток
Клинические признаки и показатели массы тела регистрировали на протяжении всего исследования для оценки патологии, и острую и отсроченную токсичность оценивали через 1 и 14 дней после введения дозы, соответственно. Данные общего анализа крови, клинической биохимии и гистопатологических исследований собирали и оценивали в ранних и поздних точках времени для определения переносимости исследуемого препарата.
Оцениваемые параметры.
Смертность и тяжесть заболевания. Всех животных наблюдали на предмет смертности и тяжести заболевания два раза в неделю до дня -8 исследования с последующим ежедневным наблюдением (в рабочие дни) до дня 1 исследования. После введения дозы животных наблюдали ежедневно до конца исследования (день 15 исследования).
Масса тела. Массу тела регистрировали два раза в неделю перед днем -8 исследования с последующим ежедневным мониторированием (рабочие дни) до дня 1 исследования. После введения дозы массу тела регистрировали ежедневно до конца исследования (день 15 исследования).
Клинические признаки. Клинические признаки регистрировали два раза в неделю перед днем 1 исследования с последующим ежедневным мониторированием с 1 по 15 день исследования.
Общий анализ крови. В день 2 исследования (группы самцов 1, 3, 5), день 3 исследования (группы самок 2, 4, 6), день 14 исследования (группы самцов 7, 9, 11) и день 15 исследования (группы самок 8, 10, 12) мышам давали наркоз изофлураном и забирали цельную кровь в пробирку с ЭДТА для следующих измерений, как показано в Таблице 10:
Клиническая биохимия. В день 2 исследования (группы самцов 1, 3, 5), день 3 исследования (группы самок 2, 4, 6), день 14 исследования (группы самцов 7, 9, 11) и день 15 исследования (группы самок 8, 10, 12) мышам давали наркоз изофлураном. Цельную кровь забирали в пробирку для отделения сыворотки. Сыворотку отделяли и исследовали путем следующих измерений, как показано в Таблице 11:
Вскрытие. В день 2 исследования (группы самцов 1, 3, 5), день 3 исследования (группы самок 2, 4, 6), день 14 исследования (группы самцов 7, 9, 11) и день 15 исследования (группы самок 8, 10, 12) мышей усыпляли путем ингаляции CO2. Проводили общее вскрытие животных в группах 1, 2, 7 и 8, и полное вскрытие животных в группах 3-6 и 9-12. Ткани собирали и фиксировали в формалине. Во время вскрытия никакие ткани не отбрасывали.
Наблюдения общей патологии. Во время вскрытия макроскопические исследования каждого животного были проведены членами Центральной лаборатории оценки противоопухолевой активности. Любые макроскопические поражения или другие патологические результаты регистрировали с помощью стандартной терминологии и предоставляли лаборанту для сравнения с результатами микроскопического исследования.
Гистопатология. Все ткани вскрытых животных консервировали в формалине. По меньшей мере, после 24 ч в фиксаторе, ткани, перечисленные в Таблице 12, обрабатывали и заливали в парафин (ткани, обозначенные звездочкой, перед заливкой сначала декальцинировали). Парафиновые блоки затем нарезали на срезы толщиной 4 мкм. Полученные неокрашенные слайды затем окрашивали гематоксилином и эозином. Затем слайды отправляли в HSRL для экспертизы сертифицированным врачом-лаборантом. Очаги регистрировали с помощью морфологических диагнозов согласно стандартизированной номенклатуре.
Анализ цитокинов (не GLP). В дни 9 исследования (самцы мышей) и 10 (самки мышей) кровь забирали у мышей в группах 13, 15 (самцы), 14 и 16 (самки) в пробирки с ЭДТА. Плазму отделяли и замораживали. Оценку цитокинови проводили в Центральной лаборатории иммунного мониторинга в MSK (не GLP).
Исследования токсикокинетики: Идентификация CAR T-клеток с помощью проточной цитометрии (не GLP). В дни 9 исследования (самцы мышей) и 10 (самки мышей) кровь забирали у мышей в группах 13, 15 (самцы), 14 и 16 (самки). Выполняли общее вскрытие всех животных, при этом ткань опухоли и селезенки помещали в среду RPMI. Образцы были немедленно предоставлены авторам изобретения для идентификации mycM28z1XXPD1DNR CAR T-клеток с помощью проточной цитометрии (не GLP).
Визуализация биолюминесценции. В дни -1/1, 7/8 и 14/15 исследования в группах 17-20 животных визуализировали при использовании люциферина (дорсально/вентрально) для оценки опухолевой нагрузки и эффективности исследуемого препарата.
Статистические методы. Групповые средние и стандартные отклонения вычисляли по массе тела, показателям общего анализа крови и клинической биохимии. Для общего анализа крови и клинической биохимии в каждой точке времени вычисляли различие в процентах между средним значением для групп, получавших исследуемый препарат, и соответствующих групп, получавших среду. Статистическую значимость этих различий анализировали с использованием непарного t-критерия и считали статистически значимой при p<0,05. Статистический анализ проводили с использованием программы для доклинических лабораторных информационных систем Ascentos версии 1.3.4, разработанной в PDS Life Sciences (Mt. Arlington, NJ). Обзор клинических данных проводили путем оценки индивидуальных значений потенциальных выбросов при использовании 1,5×IQR критерия и референсных диапазонов параметров, установленных в лаборатории. Любые значения, определенные как выбросы, удаляли из статистического анализа.
C. Результаты
С.1. Смертность и тяжесть заболевания
Предыдущая работа авторов изобретения показала, что контрольные животные могут погибать из-за опухолевой нагрузки примерно через 20-22 дня после введения опухоли. Два контрольных животных в когорте визуализации (86 [группа 17] и 88 [группа 19]) были подвергнуты выборочному умерщвлению в дни исследования 12 и 14 из-за патологии и затрудненного дыхания. Макроскопическое вскрытие каждого животного после умерщвления показало значимую опухолевую нагрузку в грудной полости, окружающей легкие и сердце. Обоим животным вводили контрольную среду, и они демонстрировали патологию в пределах ожидаемого окна. Таким образом, хотя эти умерщвления были незапланированными, они не были неожиданными. Никакой другой смертности или патологии у животных в этом исследовании не наблюдали.
С.2. Масса тела
Сводные данные по средней массе тела в каждой группе показаны на Фигурах 40-43. Животные в группе 9 (контрольная среда) показали прогрессирующее снижение массы тела во время исследования и значимое различие в весе по сравнению с контрольными животными без опухолей (группа 7) и животными в группе исследуемого препарата (группа 11) в день 14 исследования. Это объясняется увеличением опухолевой нагрузки у контрольных животных (см. Фигуру 42). Аналогичным образом, животные в группе 10 (контрольная среда) продемонстрировали значимое различие по массе тела в сравнении с группой 8 (контрольная среда без опухоли) и группой 12 (исследуемый препарат), начиная со дня 13 исследования и до конца исследования (см. Фигуру 43). Это также связано с опухолевой нагрузкой. Все животные показали снижение массы тела на следующий день после хирургической операции (день 2 для самцов мышей и день 3 для самок мышей), что связывали с операцией. Контрольные мыши без опухолей и мыши, получавшие mycM28z1XXPD1DNR CAR T-клетки, восстановили свой первоначальный вес до операции в течение 2-3 дней после операции и постепенно прибавляли в весе в течение оставшейся части исследования, тогда как у мышей, получавших среду, восстановление массы тела после операции было незначительным или отсутствовало, и постепенно животные теряли вес с одновременным увеличением опухолевой нагрузки (см. Фигуру 42 и 43).
С.3. Клинические признаки
Животные в группе 17 (контрольная среда) демонстрировали признаки выпадения волос (85, 87) и шелушения (87), что связывали с агрессивным животным в клетке. После того, как животных разделили, признаки уменьшились, что указывало на то, что наблюдения были связаны с борьбой животных. У животного 86 наблюдали затрудненное дыхание и снижение активности на день 12 исследования, что было связано с опухолевой нагрузкой и привело к выборочному умерщвлению. У животного 93 (группа 19, исследуемый препарат) наблюдали легкое шелушение; однако это было связано с раздражением, вызванным хирургическими зажимами, поскольку никакое другое животное в клетке не пострадало, и активность животных была нормальной. У животного 88 (группа 18, контрольная среда) наблюдали покраснение глаз за 2 дня до выборочного умерщвления. Этот клинический признак мог быть ранним признаком дискомфорта животного перед выборочным умерщвлением из-за опухолевой нагрузки.
Никаких других значимых клинических признаков во время этого исследования не наблюдали - мыши казались нормальными на протяжении всего периода наблюдения.
С.4. Общий анализ крови
Группа 12 (самки мышей, исследуемый препарат) имела высокое среднее процентное значение моноцитов (среднее, 18,44%, n=5) (p=≤0,0001) по сравнению с группой 10 (опухоль с контрольной средой) (среднее значение, 3,34%, n=5) . Референсный диапазон, установленный для процента моноцитов, составляет 0,9-18%. Однако это не коррелировало с данными микроскопического исследования.
Никаких других значимых или аномальных результатов для оцениваемых параметров общего анализа крови не наблюдали. Любые различия между группами, получавшими исследуемый препарат, и группами, получавшими соответствующий носитель, находились в пределах нормальных референсных диапазонов или не были биологически релевантными или статистически значимыми.
C.5. Клиническая биохимия
Группа 11 (самцы мышей, исследуемый препарат) имела низкое среднее значение общего белка (среднее, 3,83 г/дл, n=5) (p=0,0022) по сравнению с группой 9 (опухоли с контрольной средой) (среднее, 4,68 г/дл, n=4). Референсный диапазон, установленный для общего белка, составляет 4,1-6,4 г/дл. Однако это не коррелировало с данными микроскопического исследования.
Никаких других побочных эффектов в отношении показателей клинической биохимии при введении исследуемого препарата не наблюдали. Любые различия между группами, получавшими исследуемый препарат, и группами, получавшими соответствующую среду, находились в пределах нормальных референсных диапазонов или не были биологически релевантными или статистически значимыми.
С.6. Наблюдения макроскопической патологии
Во время вскрытия опухолевую ткань не собирали, но наблюдали у многих животных при промежуточном умерщвлении, как и предполагалось. Во время окончательного умерщвления опухолевая нагрузка была видна у животных, получавших контрольную среду, но в большинстве случаев у животных, получавших исследуемый препарат, наблюдали незначительные опухолевые очаги, или они отсутствовали. Дополнительные результаты, полученные во время вскрытия, подробно описаны в Таблице 13 ниже.
(номер группы)
32 (G5 - Исследуемый препарат)
59 (G10 - Контрольная среда)
60 (G10 - Контрольная среда)
71 (G12 - Исследуемый препарат)
16 (G3 - Контрольная среда)
25 (G4 - Контрольная среда)
30 (G5 - Исследуемый препарат)
34 (G5 - Исследуемый препарат)
40 (G6 - Исследуемый препарат)
45 (G6 - Исследуемый препарат)
56 (G9 - Контрольная среда)
58 (G10 - Контрольная среда)
59 (G10 - Контрольная среда)
60 (G10 - Контрольная среда)
65 (G11 - Исследуемый препарат)
71 (G12 - Исследуемый препарат)
71 (G12 - Исследуемый препарат)
Никаких других макроскопических наблюдений при вскрытии не было отмечено.
C.7. Гистопатология
Обзор результатов гистопатологических исследований показал, что в дни промежуточного (день 2) и окончательного (день 14) умерщвления не было никаких результатов микроскопических исследований, связанных с ранней или поздней токсичностью в результате введения исследуемого препарата.
Результаты микроскопического исследования у животных в группах 5 и 6 (исследуемый препарат) включали присутствие смешанного клеточного инфильтрата в ксенотрансплантатах опухолей в легких. Посчитали, что это связано с введением исследуемого препарата, но не связано с какой-либо токсичностью исследуемого препарата. Этот результат был подтвержден в отдельном исследовании с помощью иммунофлуоресцентного окрашивания mycM28z1XXPD1DNR CAR T-клеток в первичной опухоли мышей, подвергнутых интраплевральному лечению (см. Раздел 2.C.2 данного Примера).
Было установлено, что любые другие наблюдаемые результаты возникали спорадически, с такой же частотой, что и в контроле, или были обычными для используемых видов/штаммов.
С.8. Анализ цитокинов
Уровни цитокинов в плазме, собранной в группах 13-16 (через 8 дней после введения исследуемого препарата/носителя), измеряли для изучения токсичности mycM28z1XXPD1DNR CAR T-клеток по сравнению с контрольной средой в отношении экспрессии периферических цитокинов у обработанных мышей. Были проанализированы следующие цитокины: IFN-γ, IL-1β, IL-2, IL-4, IL-5, IL-6, IL-10, IL-12p70, KC/GRO и ФНО-α.
Результаты этого анализа продемонстрировали неопределяемые уровни IFN-γ, IL-12p70, IL-1β, IL-2 и IL-5 (ниже предела количественного определения) у всех животных, независимо от того, получали ли они CAR T-клетки или контрольную среду. IL-4 был обнаружен в низких уровнях и был единственным цитокином, который показал несколько более высокие уровни у мышей, получавших CAR T-клетки, чем у мышей, получавших контрольную среду. Уровни всех остальных цитокинов, которые были обнаружены выше предела количественного определения, таких как IL-10, IL-6, KC/GRO и ФНО-α, обычно были низкими и существенно не отличались у мышей, получавших CAR T-клетки, и мышей, получавших контрольную среду.
С.9. Идентификация mycM28z1XXPD1DNR CAR T-клеток в опухоли и селезенке
Для подтверждения инъекции mycM28z1XXPD1DNR CAR T-клеток, группы 13-16 умерщвляли через 8 дней после введения тестируемого препарата/среды. Селезенку и опухоль выделяли, обрабатывали и окрашивали на человеческие T-клетки (CD45+ CD3+) с помощью проточной цитометрии. Человеческие T-клетки были обнаружены в опухоли и ткани селезенки у всех мышей, получавших mycM28z1XXPD1DNR CAR T-клетки, но не у мышей, получавших среду (см. Фигуры 44 и 45).
С.10. Биолюминесцентная визуализация
Оптическую BLI всего тела (IVIS) проводили у мышей в группах 17-20 для обеспечения качественной оценки нагрузки опухолей MGM. Изображения, полученные в день -1/1 исследования, показали успешное введение опухоли всем животным в каждой группе. После введения контрольной среды опухолевая нагрузка у животных в группах 17 (самцы мышей) и 18 (самки мышей) увеличивалась в каждый момент измерения, при этом двум животным потребовалась досрочная визуализация из-за тяжелого состояния. После введения исследуемого препарата опухолевая нагрузка у животных в группах 19 (самцы мышей) и 20 (самки мышей) увеличивалась через 1 неделю после инъекции; однако через 2 недели нагрузка значительно снизилась. Результаты визуализации самцов и самок мышей показаны на Фигурах 46 и 47 соответственно.
D. Обсуждение
Для определения противоопухолевой эффективности M28z1XXPD1DNR CAR T-клеток in vitro и in vivo были проведены обширные фармакологические исследования. Было показано, что mycM28z1XXPD1DNR CAR T-клетки убивают клетки-мишени мезотелин-зависимым и HLA-независимым образом, накапливают и секретируют эффекторные цитокины при стимуляции антигеном. Сложный антигенный стресс-тест с использованием повторной антигенной стимуляции показал, что mycM28z1XXPD1DNR CAR T-клетки способны сохранять цитотоксичность дольше, чем mycM28z CAR T-клетки, в ходе анализа. In vivo, повторная стимуляция антигеном показала более высокую функциональную устойчивость mycM28z1XXPD1DNR CAR T-клеток по сравнению с mycM28z CAR T-клетками, что привело к последовательной регрессии опухоли в течение серии из 10 повторных заражений опухолью с повышаемыми дозами опухоли у мышей, получавших mycM28z1XXPD1DNR CAR T-клетки, но в конечном итоге у мышей, которым вводили mycM28z CAR T-клетки, опухоли прогрессировали и рецидивировали.
Фармакологические исследования на животных более релевантны для изучения противоопухолевой эффективности CAR T-клеток, поскольку они охватывают важные аспекты фармакологии и фармакокинетики, которые невозможно изучить в анализах in vitro. Такие факторы, как путь введения, миграция к участку локализации опухоли, хоуминг в лимфоидные органы, системная циркуляция, персистирование in vivo и, несмотря на ограничения, связанные с использованием линии мышей с иммунодефицитом, взаимодействие с иммунным микроокружением опухоли, в конечном итоге модулируют противоопухолевую эффективность. Авторы изобретения разработали трансляционно-релевантную ортотопическую модель мезотелиомы плевры на мышах, которая напоминает болезнь человека (Servais et al., Clin Cancer Res. 2012). Авторы изобретения показали, что регионарное (внутриплевральное) введение T-клеток в значительной степени подавляет не только плевральное заболевание, но и диссеминированные очаги опухоли (Adusumilli et al., Sci Transl Med. 2014; 6(261): 261ra151). Что еще более важно, результаты, наблюдаемые в текущих клинических исследованиях (IND 16354), отражают первоначальные наблюдения авторов на ортотопической модели MPM на мышах, подтверждая достоверность модели с точки зрения клинической релевантности (Adusumilli et al., Cancer Res. 2019; 79(13)). В этом исследовании полную эрадикацию опухоли наблюдали при введении однократной низкой дозы 3×104 mycM28z1XXPD1DNR CAR T-клеток, доставленных регионарно, и не наблюдали никаких признаков целевых внеопухолевых токсических эффектов. Исследование токсичности одной ортотопической дозы 1×105 mycM28z1XXPD1DNR CAR T-клеток в ксенотрансплантатной модели мезотелиомы на мышах с 2-недельным периодом восстановления подтвердило, что mycM28z1XXPD1DNR CAR T-клетки хорошо переносились. Не было обнаружено значимых результатов по смертности, клиническим наблюдениям, изменениям массы тела и макроскопическим исследованиям. Микроскопическое исследование выявило смешанный клеточный инфильтрат в ксенотрансплантатах опухолей, который не наблюдали у мышей, которым вводили среду, но указывает на фармакологию mycM28z1XXPD1DNR CAR T-клеток. Самцы мышей, получавшие лечение, имели низкое среднее значение общего белка, а самки мышей, получавшие лечение, демонстрировали высокий средний процент моноцитов в точке времени 2 недели, но ни один из этих показателей не коррелировал с какими-либо данными микроскопических исследований.
Применение CAR T-клеток, в том числе мезотелин-направленных CAR T-клеток, оценивали у человека, и, как сообщали, они были безопасными, с определенными, поддающимися коррекции побочными эффектами, такими как лихорадка, озноб, миалгии, гиперчувствительность и анафилаксия из-за воспаления, вызванного T-клетками. Риск репликационно-компетентных ретровирусов будет сведен к минимуму за счет всестороннего тестирования продукта. Кроме того, T-клетки пациента будут тестировать каждые 12 недель в течение до 2 лет или до прогрессирования заболевания. Пациентов будут наблюдать на предмет выживаемости в течение 15 лет после введения CAR T-клеток.
Комбинированная оценка этих данных использовалась для установления безопасной начальной дозы для медицинского применения и для поддержки схемы с повышением дозы.
Варианты осуществления раскрытого в настоящем документе изобретения
Из представленного выше описания будет очевидно, что в изобретение, раскрытое в настоящем документе, могут быть внесены изменения и модификации для его адаптации к различным применениям и условиям. Такие варианты осуществления также включены в объем следующей формулы изобретения.
Перечисление списка элементов в любом определении переменной в настоящем документе включает определения этой переменной как любого отдельного элемента или комбинации (или субкомбинации) перечисленных элементов. Описание варианта осуществления в настоящем документе включает этот вариант осуществления как любой отдельный вариант осуществления или в комбинации с любыми другими вариантами осуществления или их частями.
Все патенты и публикации, указанные в этом описании, включены в настоящий документ посредством отсылки в той степени, как если бы каждый независимый патент и публикация были специально и индивидуально указаны как включенные посредством отсылки.
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> МЕМОРИАЛ СЛОАН-КЕТТЕРИНГ КЭНСЕР СЕНТЕР
<120> МЕЗОТЕЛИНОВЫЕ CAR-РЕЦЕПТОРЫ И ИХ ПРИМЕНЕНИЕ
<130> 072734.1041
<150> US 62/848,983
<151> 2019-05-16
<150> US 62/975,966
<151> 2020-02-13
<160> 137
<170> PatentIn version 3.5
<210> 1
<211> 345
<212> БЕЛОК
<213> Homo sapiens
<400> 1
Met Ala Gln His His Leu Trp Ile Leu Leu Leu Cys Leu Gln Thr Trp
1 5 10 15
Pro Glu Ala Ala Gly Lys Asp Ser Glu Ile Phe Thr Val Asn Gly Ile
20 25 30
Leu Gly Glu Ser Val Thr Phe Pro Val Asn Ile Gln Glu Pro Arg Gln
35 40 45
Val Lys Ile Ile Ala Trp Thr Ser Lys Thr Ser Val Ala Tyr Val Thr
50 55 60
Pro Gly Asp Ser Glu Thr Ala Pro Val Val Thr Val Thr His Arg Asn
65 70 75 80
Tyr Tyr Glu Arg Ile His Ala Leu Gly Pro Asn Tyr Asn Leu Val Ile
85 90 95
Ser Asp Leu Arg Met Glu Asp Ala Gly Asp Tyr Lys Ala Asp Ile Asn
100 105 110
Thr Gln Ala Asp Pro Tyr Thr Thr Thr Lys Arg Tyr Asn Leu Gln Ile
115 120 125
Tyr Arg Arg Leu Gly Lys Pro Lys Ile Thr Gln Ser Leu Met Ala Ser
130 135 140
Val Asn Ser Thr Cys Asn Val Thr Leu Thr Cys Ser Val Glu Lys Glu
145 150 155 160
Glu Lys Asn Val Thr Tyr Asn Trp Ser Pro Leu Gly Glu Glu Gly Asn
165 170 175
Val Leu Gln Ile Phe Gln Thr Pro Glu Asp Gln Glu Leu Thr Tyr Thr
180 185 190
Cys Thr Ala Gln Asn Pro Val Ser Asn Asn Ser Asp Ser Ile Ser Ala
195 200 205
Arg Gln Leu Cys Ala Asp Ile Ala Met Gly Phe Arg Thr His His Thr
210 215 220
Gly Leu Leu Ser Val Leu Ala Met Phe Phe Leu Leu Val Leu Ile Leu
225 230 235 240
Ser Ser Val Phe Leu Phe Arg Leu Phe Lys Arg Arg Gln Gly Arg Ile
245 250 255
Phe Pro Glu Gly Ser Cys Leu Asn Thr Phe Thr Lys Asn Pro Tyr Ala
260 265 270
Ala Ser Lys Lys Thr Ile Tyr Thr Tyr Ile Met Ala Ser Arg Asn Thr
275 280 285
Gln Pro Ala Glu Ser Arg Ile Tyr Asp Glu Ile Leu Gln Ser Lys Val
290 295 300
Leu Pro Ser Lys Glu Glu Pro Val Asn Thr Val Tyr Ser Glu Val Gln
305 310 315 320
Phe Ala Asp Lys Met Gly Lys Ala Ser Thr Gln Asp Ser Lys Pro Pro
325 330 335
Gly Thr Ser Ser Tyr Glu Ile Val Ile
340 345
<210> 2
<211> 75
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 2
ttgctgagcg tgctggctat gttctttctg cttgttctca ttctgtcttc agtgtttttg 60
ttccgtttgt tcaag 75
<210> 3
<211> 583
<212> БЕЛОК
<213> Homo sapiens
<400> 3
Met Glu Ser Lys Gly Ala Ser Ser Cys Arg Leu Leu Phe Cys Leu Leu
1 5 10 15
Ile Ser Ala Thr Val Phe Arg Pro Gly Leu Gly Trp Tyr Thr Val Asn
20 25 30
Ser Ala Tyr Gly Asp Thr Ile Ile Ile Pro Cys Arg Leu Asp Val Pro
35 40 45
Gln Asn Leu Met Phe Gly Lys Trp Lys Tyr Glu Lys Pro Asp Gly Ser
50 55 60
Pro Val Phe Ile Ala Phe Arg Ser Ser Thr Lys Lys Ser Val Gln Tyr
65 70 75 80
Asp Asp Val Pro Glu Tyr Lys Asp Arg Leu Asn Leu Ser Glu Asn Tyr
85 90 95
Thr Leu Ser Ile Ser Asn Ala Arg Ile Ser Asp Glu Lys Arg Phe Val
100 105 110
Cys Met Leu Val Thr Glu Asp Asn Val Phe Glu Ala Pro Thr Ile Val
115 120 125
Lys Val Phe Lys Gln Pro Ser Lys Pro Glu Ile Val Ser Lys Ala Leu
130 135 140
Phe Leu Glu Thr Glu Gln Leu Lys Lys Leu Gly Asp Cys Ile Ser Glu
145 150 155 160
Asp Ser Tyr Pro Asp Gly Asn Ile Thr Trp Tyr Arg Asn Gly Lys Val
165 170 175
Leu His Pro Leu Glu Gly Ala Val Val Ile Ile Phe Lys Lys Glu Met
180 185 190
Asp Pro Val Thr Gln Leu Tyr Thr Met Thr Ser Thr Leu Glu Tyr Lys
195 200 205
Thr Thr Lys Ala Asp Ile Gln Met Pro Phe Thr Cys Ser Val Thr Tyr
210 215 220
Tyr Gly Pro Ser Gly Gln Lys Thr Ile His Ser Glu Gln Ala Val Phe
225 230 235 240
Asp Ile Tyr Tyr Pro Thr Glu Gln Val Thr Ile Gln Val Leu Pro Pro
245 250 255
Lys Asn Ala Ile Lys Glu Gly Asp Asn Ile Thr Leu Lys Cys Leu Gly
260 265 270
Asn Gly Asn Pro Pro Pro Glu Glu Phe Leu Phe Tyr Leu Pro Gly Gln
275 280 285
Pro Glu Gly Ile Arg Ser Ser Asn Thr Tyr Thr Leu Thr Asp Val Arg
290 295 300
Arg Asn Ala Thr Gly Asp Tyr Lys Cys Ser Leu Ile Asp Lys Lys Ser
305 310 315 320
Met Ile Ala Ser Thr Ala Ile Thr Val His Tyr Leu Asp Leu Ser Leu
325 330 335
Asn Pro Ser Gly Glu Val Thr Arg Gln Ile Gly Asp Ala Leu Pro Val
340 345 350
Ser Cys Thr Ile Ser Ala Ser Arg Asn Ala Thr Val Val Trp Met Lys
355 360 365
Asp Asn Ile Arg Leu Arg Ser Ser Pro Ser Phe Ser Ser Leu His Tyr
370 375 380
Gln Asp Ala Gly Asn Tyr Val Cys Glu Thr Ala Leu Gln Glu Val Glu
385 390 395 400
Gly Leu Lys Lys Arg Glu Ser Leu Thr Leu Ile Val Glu Gly Lys Pro
405 410 415
Gln Ile Lys Met Thr Lys Lys Thr Asp Pro Ser Gly Leu Ser Lys Thr
420 425 430
Ile Ile Cys His Val Glu Gly Phe Pro Lys Pro Ala Ile Gln Trp Thr
435 440 445
Ile Thr Gly Ser Gly Ser Val Ile Asn Gln Thr Glu Glu Ser Pro Tyr
450 455 460
Ile Asn Gly Arg Tyr Tyr Ser Lys Ile Ile Ile Ser Pro Glu Glu Asn
465 470 475 480
Val Thr Leu Thr Cys Thr Ala Glu Asn Gln Leu Glu Arg Thr Val Asn
485 490 495
Ser Leu Asn Val Ser Ala Ile Ser Ile Pro Glu His Asp Glu Ala Asp
500 505 510
Glu Ile Ser Asp Glu Asn Arg Glu Lys Val Asn Asp Gln Ala Lys Leu
515 520 525
Ile Val Gly Ile Val Val Gly Leu Leu Leu Ala Ala Leu Val Ala Gly
530 535 540
Val Val Tyr Trp Leu Tyr Met Lys Lys Ser Lys Thr Ala Ser Lys His
545 550 555 560
Val Asn Lys Asp Leu Gly Asn Met Glu Glu Asn Lys Lys Leu Glu Glu
565 570 575
Asn Asn His Lys Thr Glu Ala
580
<210> 4
<211> 78
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 4
ctaattgtgg gaatcgttgt tggtctcctc cttgctgccc ttgttgctgg tgtcgtctac 60
tggctgtaca tgaagaag 78
<210> 5
<211> 235
<212> БЕЛОК
<213> Homo sapiens
<400> 5
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Ser Gln Phe Arg Val Ser Pro Leu Asp Arg Thr
20 25 30
Trp Asn Leu Gly Glu Thr Val Glu Leu Lys Cys Gln Val Leu Leu Ser
35 40 45
Asn Pro Thr Ser Gly Cys Ser Trp Leu Phe Gln Pro Arg Gly Ala Ala
50 55 60
Ala Ser Pro Thr Phe Leu Leu Tyr Leu Ser Gln Asn Lys Pro Lys Ala
65 70 75 80
Ala Glu Gly Leu Asp Thr Gln Arg Phe Ser Gly Lys Arg Leu Gly Asp
85 90 95
Thr Phe Val Leu Thr Leu Ser Asp Phe Arg Arg Glu Asn Glu Gly Tyr
100 105 110
Tyr Phe Cys Ser Ala Leu Ser Asn Ser Ile Met Tyr Phe Ser His Phe
115 120 125
Val Pro Val Phe Leu Pro Ala Lys Pro Thr Thr Thr Pro Ala Pro Arg
130 135 140
Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg
145 150 155 160
Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly
165 170 175
Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr
180 185 190
Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Asn His
195 200 205
Arg Asn Arg Arg Arg Val Cys Lys Cys Pro Arg Pro Val Val Lys Ser
210 215 220
Gly Asp Lys Pro Ser Leu Ser Ala Arg Tyr Val
225 230 235
<210> 6
<211> 75
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 6
atctacatct gggcgccctt ggccgggact tgtggggtcc ttctcctgtc actggttatc 60
accctttact gcaac 75
<210> 7
<211> 221
<212> БЕЛОК
<213> Homo sapiens
<400> 7
Met Arg Pro Arg Leu Trp Leu Leu Leu Ala Ala Gln Leu Thr Val Leu
1 5 10 15
His Gly Asn Ser Val Leu Gln Gln Thr Pro Ala Tyr Ile Lys Val Gln
20 25 30
Thr Asn Lys Met Val Met Leu Ser Cys Glu Ala Lys Ile Ser Leu Ser
35 40 45
Asn Met Arg Ile Tyr Trp Leu Arg Gln Arg Gln Ala Pro Ser Ser Asp
50 55 60
Ser His His Glu Phe Leu Ala Leu Trp Asp Ser Ala Lys Gly Thr Ile
65 70 75 80
His Gly Glu Glu Val Glu Gln Glu Lys Ile Ala Val Phe Arg Asp Ala
85 90 95
Ser Arg Phe Ile Leu Asn Leu Thr Ser Val Lys Pro Glu Asp Ser Gly
100 105 110
Ile Tyr Phe Cys Met Ile Val Gly Ser Pro Glu Leu Thr Phe Gly Lys
115 120 125
Gly Thr Gln Leu Ser Val Val Asp Phe Leu Pro Thr Thr Ala Gln Pro
130 135 140
Thr Lys Lys Ser Thr Leu Lys Lys Arg Val Cys Arg Leu Pro Arg Pro
145 150 155 160
Glu Thr Gln Lys Gly Pro Leu Cys Ser Pro Ile Thr Leu Gly Leu Leu
165 170 175
Val Ala Gly Val Leu Val Leu Leu Val Ser Leu Gly Val Ala Ile His
180 185 190
Leu Cys Cys Arg Arg Arg Arg Ala Arg Leu Arg Phe Met Lys Gln Leu
195 200 205
Arg Leu His Pro Leu Glu Lys Cys Ser Arg Met Asp Tyr
210 215 220
<210> 8
<211> 75
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 8
atcacccttg gcctgctggt ggctggcgtc ctggttctgc tggtttccct gggagtggcc 60
atccacctgt gctgc 75
<210> 9
<211> 199
<212> БЕЛОК
<213> Homo sapiens
<400> 9
Met Lys Ser Gly Leu Trp Tyr Phe Phe Leu Phe Cys Leu Arg Ile Lys
1 5 10 15
Val Leu Thr Gly Glu Ile Asn Gly Ser Ala Asn Tyr Glu Met Phe Ile
20 25 30
Phe His Asn Gly Gly Val Gln Ile Leu Cys Lys Tyr Pro Asp Ile Val
35 40 45
Gln Gln Phe Lys Met Gln Leu Leu Lys Gly Gly Gln Ile Leu Cys Asp
50 55 60
Leu Thr Lys Thr Lys Gly Ser Gly Asn Thr Val Ser Ile Lys Ser Leu
65 70 75 80
Lys Phe Cys His Ser Gln Leu Ser Asn Asn Ser Val Ser Phe Phe Leu
85 90 95
Tyr Asn Leu Asp His Ser His Ala Asn Tyr Tyr Phe Cys Asn Leu Ser
100 105 110
Ile Phe Asp Pro Pro Pro Phe Lys Val Thr Leu Thr Gly Gly Tyr Leu
115 120 125
His Ile Tyr Glu Ser Gln Leu Cys Cys Gln Leu Lys Phe Trp Leu Pro
130 135 140
Ile Gly Cys Ala Ala Phe Val Val Val Cys Ile Leu Gly Cys Ile Leu
145 150 155 160
Ile Cys Trp Leu Thr Lys Lys Lys Tyr Ser Ser Ser Val His Asp Pro
165 170 175
Asn Gly Glu Tyr Met Phe Met Arg Ala Val Asn Thr Ala Lys Lys Ser
180 185 190
Arg Leu Thr Asp Val Thr Leu
195
<210> 10
<211> 75
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 10
ttctggttac ccataggatg tgcagccttt gttgtagtct gcattttggg atgcatactt 60
atttgttggc ttaca 75
<210> 11
<211> 223
<212> БЕЛОК
<213> Homo sapiens
<400> 11
Met Ala Cys Leu Gly Phe Gln Arg His Lys Ala Gln Leu Asn Leu Ala
1 5 10 15
Thr Arg Thr Trp Pro Cys Thr Leu Leu Phe Phe Leu Leu Phe Ile Pro
20 25 30
Val Phe Cys Lys Ala Met His Val Ala Gln Pro Ala Val Val Leu Ala
35 40 45
Ser Ser Arg Gly Ile Ala Ser Phe Val Cys Glu Tyr Ala Ser Pro Gly
50 55 60
Lys Ala Thr Glu Val Arg Val Thr Val Leu Arg Gln Ala Asp Ser Gln
65 70 75 80
Val Thr Glu Val Cys Ala Ala Thr Tyr Met Met Gly Asn Glu Leu Thr
85 90 95
Phe Leu Asp Asp Ser Ile Cys Thr Gly Thr Ser Ser Gly Asn Gln Val
100 105 110
Asn Leu Thr Ile Gln Gly Leu Arg Ala Met Asp Thr Gly Leu Tyr Ile
115 120 125
Cys Lys Val Glu Leu Met Tyr Pro Pro Pro Tyr Tyr Leu Gly Ile Gly
130 135 140
Asn Gly Thr Gln Ile Tyr Val Ile Asp Pro Glu Pro Cys Pro Asp Ser
145 150 155 160
Asp Phe Leu Leu Trp Ile Leu Ala Ala Val Ser Ser Gly Leu Phe Phe
165 170 175
Tyr Ser Phe Leu Leu Thr Ala Val Ser Leu Ser Lys Met Leu Lys Lys
180 185 190
Arg Ser Pro Leu Thr Thr Gly Val Tyr Val Lys Met Pro Pro Thr Glu
195 200 205
Pro Glu Cys Glu Lys Gln Phe Gln Pro Tyr Phe Ile Pro Ile Asn
210 215 220
<210> 12
<211> 75
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 12
ttcctcctct ggatccttgc agcagttagt tcggggttgt ttttttatag ctttctcctc 60
acagctgttt ctttg 75
<210> 13
<211> 532
<212> БЕЛОК
<213> Homo sapiens
<400> 13
Met Ala Pro Ser Ser Pro Arg Pro Ala Leu Pro Ala Leu Leu Val Leu
1 5 10 15
Leu Gly Ala Leu Phe Pro Gly Pro Gly Asn Ala Gln Thr Ser Val Ser
20 25 30
Pro Ser Lys Val Ile Leu Pro Arg Gly Gly Ser Val Leu Val Thr Cys
35 40 45
Ser Thr Ser Cys Asp Gln Pro Lys Leu Leu Gly Ile Glu Thr Pro Leu
50 55 60
Pro Lys Lys Glu Leu Leu Leu Pro Gly Asn Asn Arg Lys Val Tyr Glu
65 70 75 80
Leu Ser Asn Val Gln Glu Asp Ser Gln Pro Met Cys Tyr Ser Asn Cys
85 90 95
Pro Asp Gly Gln Ser Thr Ala Lys Thr Phe Leu Thr Val Tyr Trp Thr
100 105 110
Pro Glu Arg Val Glu Leu Ala Pro Leu Pro Ser Trp Gln Pro Val Gly
115 120 125
Lys Asn Leu Thr Leu Arg Cys Gln Val Glu Gly Gly Ala Pro Arg Ala
130 135 140
Asn Leu Thr Val Val Leu Leu Arg Gly Glu Lys Glu Leu Lys Arg Glu
145 150 155 160
Pro Ala Val Gly Glu Pro Ala Glu Val Thr Thr Thr Val Leu Val Arg
165 170 175
Arg Asp His His Gly Ala Asn Phe Ser Cys Arg Thr Glu Leu Asp Leu
180 185 190
Arg Pro Gln Gly Leu Glu Leu Phe Glu Asn Thr Ser Ala Pro Tyr Gln
195 200 205
Leu Gln Thr Phe Val Leu Pro Ala Thr Pro Pro Gln Leu Val Ser Pro
210 215 220
Arg Val Leu Glu Val Asp Thr Gln Gly Thr Val Val Cys Ser Leu Asp
225 230 235 240
Gly Leu Phe Pro Val Ser Glu Ala Gln Val His Leu Ala Leu Gly Asp
245 250 255
Gln Arg Leu Asn Pro Thr Val Thr Tyr Gly Asn Asp Ser Phe Ser Ala
260 265 270
Lys Ala Ser Val Ser Val Thr Ala Glu Asp Glu Gly Thr Gln Arg Leu
275 280 285
Thr Cys Ala Val Ile Leu Gly Asn Gln Ser Gln Glu Thr Leu Gln Thr
290 295 300
Val Thr Ile Tyr Ser Phe Pro Ala Pro Asn Val Ile Leu Thr Lys Pro
305 310 315 320
Glu Val Ser Glu Gly Thr Glu Val Thr Val Lys Cys Glu Ala His Pro
325 330 335
Arg Ala Lys Val Thr Leu Asn Gly Val Pro Ala Gln Pro Leu Gly Pro
340 345 350
Arg Ala Gln Leu Leu Leu Lys Ala Thr Pro Glu Asp Asn Gly Arg Ser
355 360 365
Phe Ser Cys Ser Ala Thr Leu Glu Val Ala Gly Gln Leu Ile His Lys
370 375 380
Asn Gln Thr Arg Glu Leu Arg Val Leu Tyr Gly Pro Arg Leu Asp Glu
385 390 395 400
Arg Asp Cys Pro Gly Asn Trp Thr Trp Pro Glu Asn Ser Gln Gln Thr
405 410 415
Pro Met Cys Gln Ala Trp Gly Asn Pro Leu Pro Glu Leu Lys Cys Leu
420 425 430
Lys Asp Gly Thr Phe Pro Leu Pro Ile Gly Glu Ser Val Thr Val Thr
435 440 445
Arg Asp Leu Glu Gly Thr Tyr Leu Cys Arg Ala Arg Ser Thr Gln Gly
450 455 460
Glu Val Thr Arg Lys Val Thr Val Asn Val Leu Ser Pro Arg Tyr Glu
465 470 475 480
Ile Val Ile Ile Thr Val Val Ala Ala Ala Val Ile Met Gly Thr Ala
485 490 495
Gly Leu Ser Thr Tyr Leu Tyr Asn Arg Gln Arg Lys Ile Lys Lys Tyr
500 505 510
Arg Leu Gln Gln Ala Gln Lys Gly Thr Pro Met Lys Pro Asn Thr Gln
515 520 525
Ala Thr Pro Pro
530
<210> 14
<211> 81
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 14
attgtcatca tcactgtggt agcagccgca gtcataatgg gcactgcagg cctcagcacg 60
tacctctata accgccagcg g 81
<210> 15
<211> 39
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 15
Ile Glu Val Met Tyr Pro Pro Pro Tyr Leu Asp Asn Glu Lys Ser Asn
1 5 10 15
Gly Thr Ile Ile His Val Lys Gly Lys His Leu Cys Pro Ser Pro Leu
20 25 30
Phe Pro Gly Pro Ser Lys Pro
35
<210> 16
<211> 117
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 16
caagagctga cttacacgtg tacagcccag aaccctgtca gcaacaattc tgactccatc 60
tctgcccggc agctctgtgc agacatcgca atgggcttcc gtactcacca caccggg 117
<210> 17
<211> 116
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 17
accaactgga gagaacagta aactccttga atgtctctgc tataagtatt ccagaacacg 60
atgaggcaga cgagataagt gatgaaaaca gagaaaaggt gaatgaccag gcaaaa 116
<210> 18
<211> 138
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 18
cccaccacga cgccagcgcc gcgaccacca acaccggcgc ccaccatcgc gtcgcagccc 60
ctgtccctgc gcccagaggc gtgccggcca gcggcggggg gcgcagtgca cacgaggggg 120
ctggacttcg cctgtgat 138
<210> 19
<211> 117
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 19
ctgagtgtgg ttgatttcct tcccaccact gcccagccca ccaagaagtc caccctcaag 60
aagagagtgt gccggttacc caggccagag acccagaagg gcccactttg tagcccc 117
<210> 20
<211> 117
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 20
tctcatgcca actattactt ctgcaaccta tcaatttttg atcctcctcc ttttaaagta 60
actcttacag gaggatattt gcatatttat gaatcacaac tttgttgcca gctgaag 117
<210> 21
<211> 117
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 21
gacacgggac tctacatctg caaggtggag ctcatgtacc caccgccata ctacctgggc 60
ataggcaacg gaacccagat ttatgtaatt gatccagaac cgtgcccaga ttctgac 117
<210> 22
<211> 117
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 22
ggggaatcag tgactgtcac tcgagatctt gagggcacct acctctgtcg ggccaggagc 60
actcaagggg aggtcacccg caaggtgacc gtgaatgtgc tctccccccg gtatgag 117
<210> 23
<211> 22
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 23
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
1 5 10 15
Asp Val Leu Asp Lys Arg
20
<210> 24
<211> 66
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 24
cagaaccagc tctataacga gctcaatcta ggacgaagag aggagtacga tgttttggac 60
aagaga 66
<210> 25
<211> 22
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 25
Gln Asn Gln Leu Phe Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Phe
1 5 10 15
Asp Val Leu Asp Lys Arg
20
<210> 26
<211> 66
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 26
cagaaccagc tctttaacga gctcaatcta ggacgaagag aggagttcga tgttttggac 60
aagaga 66
<210> 27
<211> 23
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 27
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
1 5 10 15
Tyr Ser Glu Ile Gly Met Lys
20
<210> 28
<211> 69
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 28
caggaaggcc tgtacaatga actgcagaaa gataagatgg cggaggccta cagtgagatt 60
gggatgaaa 69
<210> 29
<211> 23
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 29
Gln Glu Gly Leu Phe Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
1 5 10 15
Phe Ser Glu Ile Gly Met Lys
20
<210> 30
<211> 69
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 30
caggaaggcc tgttcaatga actgcagaaa gataagatgg cggaggcctt cagtgagatt 60
gggatgaaa 69
<210> 31
<211> 22
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 31
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
1 5 10 15
Asp Ala Leu His Met Gln
20
<210> 32
<211> 66
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 32
cacgatggcc tttaccaggg tctcagtaca gccaccaagg acacctacga cgcccttcac 60
atgcag 66
<210> 33
<211> 22
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 33
His Asp Gly Leu Phe Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Phe
1 5 10 15
Asp Ala Leu His Met Gln
20
<210> 34
<211> 66
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 34
cacgatggcc ttttccaggg gctcagtaca gccaccaagg acaccttcga cgcccttcac 60
atgcag 66
<210> 35
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 35
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly
1 5 10 15
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
20 25 30
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
35 40 45
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Phe Asn Glu Leu Gln Lys
50 55 60
Asp Lys Met Ala Glu Ala Phe Ser Glu Ile Gly Met Lys Gly Glu Arg
65 70 75 80
Arg Arg Gly Lys Gly His Asp Gly Leu Phe Gln Gly Leu Ser Thr Ala
85 90 95
Thr Lys Asp Thr Phe Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
100 105 110
<210> 36
<211> 230
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 36
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Val Ser Ser Gly
20 25 30
Ser Tyr Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly Tyr Ile Tyr Tyr Ser Gly Ser Thr Asn Tyr Asn Pro Ser
50 55 60
Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe
65 70 75 80
Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Arg Glu Gly Lys Asn Gly Ala Phe Asp Ile Trp Gly Gln Gly
100 105 110
Thr Met Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr Ser Gly Gln Ala Gly
225 230
<210> 37
<211> 693
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 37
caggtgcagc tgcaggagtc cggcccagga ctggtgaagc cttcggagac cctgtccctc 60
acctgcactg tctctggtgg ctccgtcagc agtggtagtt actactggag ctggatccgg 120
cagcccccag ggaagggact ggagtggatt gggtatatct attacagtgg gagcaccaac 180
tacaacccct ccctcaagag tcgagtcacc atatcagtag acacgtccaa gaaccagttc 240
tccctgaagc tgagctctgt gaccgctgcg gacacggccg tgtattactg tgcgagagag 300
gggaagaatg gggcttttga tatctggggc caagggacaa tggtcaccgt ctcttcagcc 360
tccaccaagg gcccatcggt cttccccctg gcaccctcct ccaagagcac ctctgggggc 420
acagcggccc tgggctgcct ggtcaaggac tacttccccg aaccggtgac ggtgtcgtgg 480
aactcaggcg ccctgaccag cggcgtgcac accttcccgg ctgtcctaca gtcctcagga 540
ctctactccc tcagcagcgt ggtgaccgtg ccctccagca gcttgggcac ccagacctac 600
atctgcaacg tgaatcacaa gcccagcaac accaaggtgg acaagaaagt tgagcccaaa 660
tcttgtgaca aaactagtgg ccaggccggc cac 693
<210> 38
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 38
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Gly Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 39
<211> 640
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 39
gacatccaga tgacccagtc tccatcctcc ctgtctgcat ctgtaggaga cagagtcacc 60
atcacttgcc gggcaagtca gagcattagc agctatttaa attggtatca gcagaaacca 120
gggaaagccc ctaagctcct gatctatgct gcatccagtt tgcaaagtgg ggtcccatca 180
gggttcagtg gcagtggatc tgggacagat ttcactctca ccatcagcag tctgcaacct 240
gaagattttg caacttacta ctgtcaacag agttacagta ccccgctcac tttcggcgga 300
gggaccaagg tggagatcaa acgaactgtg gctgcaccat ctgtcttcat cttcccgcca 360
tctgatgagc agttgaaatc tggaactgcc tctgttgtgt gcctgctgaa taacttctat 420
cccagagagg ccaaagtaca gtggaaggtg gataacgccc tccaatcggg taactcccag 480
gagagtgtca cagagcagga cagcaaggac agcacctact gcctcagcag caccctgacg 540
ctgagcaaag cagactacga gaaacacaaa ctctacgcct gcgaagtcac ccatcagggc 600
ctgagctcgc ccgtcacaaa gagcttcaac aggggagagt 640
<210> 40
<211> 214
<212> БЕЛОК
<213> Homo sapiens
<400> 40
Arg His Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Gly Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 41
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 41
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Val Ser Ser Gly
20 25 30
Ser Tyr Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly Tyr Ile Tyr Tyr Ser Gly Ser Thr Asn Tyr Asn Pro Ser
50 55 60
Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe
65 70 75 80
Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Arg Glu Gly Lys Asn Gly Ala Phe Asp Ile Trp Gly Gln Gly
100 105 110
Thr Met Val Thr Val Ser Ser Ser
115 120
<210> 42
<211> 262
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 42
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Val Ser Ser Gly
20 25 30
Ser Tyr Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly Tyr Ile Tyr Tyr Ser Gly Ser Thr Asn Tyr Asn Pro Ser
50 55 60
Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe
65 70 75 80
Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Arg Glu Gly Lys Asn Gly Ala Phe Asp Ile Trp Gly Gln Gly
100 105 110
Thr Met Val Thr Val Ser Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Arg His Gln Met Thr Gln Ser Pro Ser
130 135 140
Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala
145 150 155 160
Ser Gln Ser Ile Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly
165 170 175
Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly
180 185 190
Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu
195 200 205
Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln
210 215 220
Gln Ser Tyr Ser Thr Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu
225 230 235 240
Ile Lys Gly Gln Ala Gly His His His His His His Gly Asp Tyr Lys
245 250 255
Asp Asp Asp Asp Lys Gly
260
<210> 43
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 43
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly
35 40 45
Ser Val Ser Ser Gly Ser Tyr Tyr Trp Ser Trp Ile Arg Gln Pro Pro
50 55 60
Gly Lys Gly Leu Glu Trp Ile Gly Tyr Ile Tyr Tyr Ser Gly Ser Thr
65 70 75 80
Asn Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr
85 90 95
Ser Lys Asn Gln Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp
100 105 110
Thr Ala Val Tyr Tyr Cys Ala Arg Glu Gly Lys Asn Gly Ala Phe Asp
115 120 125
Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Arg His Gln Met Thr
145 150 155 160
Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile
165 170 175
Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr Leu Asn Trp Tyr Gln
180 185 190
Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala Ser Ser
195 200 205
Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr
210 215 220
Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr
225 230 235 240
Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Leu Thr Phe Gly Gly Gly
245 250 255
Thr Lys Val Glu Ile Lys Arg Thr Ala Ala Ala Ile Glu Val Met Tyr
260 265 270
Pro Pro Pro Tyr Leu Asp Asn Glu Lys Ser Asn Gly Thr Ile Ile His
275 280 285
Val Lys Gly Lys His Leu Cys Pro Ser Pro Leu Phe Pro Gly Pro Ser
290 295 300
Lys Pro Phe Trp Val Leu Val Val Val Gly Gly Val Leu Ala Cys Tyr
305 310 315 320
Ser Leu Leu Val Thr Val Ala Phe Ile Ile Phe Trp Val Arg Ser Lys
325 330 335
Arg Ser Arg Leu Leu His Ser Asp Tyr Met Asn Met Thr Pro Arg Arg
340 345 350
Pro Gly Pro Thr Arg Lys His Tyr Gln Pro Tyr Ala Pro Pro Arg Asp
355 360 365
Phe Ala Ala Tyr Arg Ser Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Phe Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Phe Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Phe
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Phe Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 44
<211> 1458
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 44
atggccctgc cagtaacggc tctgctgctg ccacttgctc tgctcctcca tgcagccagg 60
cctcaggttc agcttcagga gagtggccca ggcctggtga agccaagtga gactctcagc 120
ttgacttgca cagtttctgg aggcagtgtc tcctcaggca gctattattg gtcctggatt 180
cggcagcccc ctgggaaagg cctggagtgg attgggtaca tatattacag tggcagcaca 240
aattacaatc catccctgaa gtctcgagta actatcagtg tggacacaag caagaatcag 300
ttttcactca aactgtcttc tgtgactgct gctgacactg ctgtttatta ttgtgccagg 360
gaggggaaaa atggggcatt tgatatttgg ggtcagggca caatggtgac agtcagctct 420
ggaggtggag gctcaggagg aggaggcagt ggaggtggtg ggtcacgcca tcagatgact 480
cagtccccct ccagtctttc tgcctcagtt ggggatagag tgaccatcac atgcagagca 540
agtcagagca tatcatccta tctgaactgg taccagcaga agccagggaa agcccccaaa 600
ttgctgattt atgcagcctc aagtctccag agtggggtgc caagcaggtt ctcaggcagt 660
ggcagtggga cagatttcac attgacaatc agctccctcc aacctgaaga ttttgccacc 720
tactattgcc agcaatccta cagcacgccc ctgacttttg gaggtggcac aaaggtagag 780
atcaagagga ctgcggccgc aattgaagtt atgtatcctc ctccttacct agacaatgag 840
aagagcaatg gaaccattat ccatgtgaaa gggaaacacc tttgtccaag tcccctattt 900
cccggacctt ctaagccctt ttgggtgctg gtggtggttg gtggagtcct ggcttgctat 960
agcttgctag taacagtggc ctttattatt ttctgggtga ggagtaagag gagcaggctc 1020
ctgcacagtg actacatgaa catgactccc cgccgccccg ggcccacccg caagcattac 1080
cagccctatg ccccaccacg cgacttcgca gcctatcgct ccagagtgaa gttcagcagg 1140
agcgcagacg cccccgcgta ccagcagggc cagaaccagc tctataacga gctcaatcta 1200
ggacgaagag aggagtacga tgttttggac aagagacgtg gccgggaccc tgagatgggg 1260
ggaaagccga gaaggaagaa ccctcaggaa ggcctgttca atgaactgca gaaagataag 1320
atggcggagg ccttcagtga gattgggatg aaaggcgagc gccggagggg caaggggcac 1380
gatggccttt tccaggggct cagtacagcc accaaggaca ccttcgacgc ccttcacatg 1440
caggccctgc cccctcgc 1458
<210> 45
<211> 801
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 45
atggccttac cagtgaccgc cttgctcctg ccgctggcct tgctgctcca cgccgccagg 60
ccgcaggtgc agctgcagga gtccggccca ggactggtga agccttcgga gaccctgtcc 120
ctcacctgca ctgtctctgg tggctccgtc agcagtggta gttactactg gagctggatc 180
cggcagcccc cagggaaggg actggagtgg attgggtata tctattacag tgggagcacc 240
aactacaacc cctccctcaa gagtcgagtc accatatcag tagacacgtc caagaaccag 300
ttctccctga agctgagctc tgtgaccgct gcggacacgg ccgtgtatta ctgtgcgaga 360
gaggggaaga atggggcttt tgatatctgg ggccaaggga caatggtcac cgtctcttca 420
ggtggaggcg gttcaggcgg aggtggctct ggcggtggcg gatcacgaca tcagatgacc 480
cagtctccat cctccctgtc tgcatctgta ggagacagag tcaccatcac ttgccgggca 540
agtcagagca ttagcagcta tttaaattgg tatcagcaga aaccagggaa agcccctaag 600
ctcctgatct atgctgcatc cagtttgcaa agtggggtcc catcaaggtt cagtggcagt 660
ggatctggga cagatttcac tctcaccatc agcagtctgc aacctgaaga ttttgcaact 720
tactactgtc aacagagtta cagtaccccg ctcactttcg gcggagggac caaggtggag 780
atcaaacgga ctgcggccgc a 801
<210> 46
<211> 801
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 46
atggcgctgc cggtgaccgc gctgctgctg ccgctggcgc tgctgctgca tgcggcgcgc 60
ccgcaggtgc agctgcagga aagcggcccg ggcctggtga aaccgagcga aaccctgagc 120
ctgacctgca ccgtgagcgg cggcagcgtg agcagcggca gctattattg gagctggatt 180
cgccagccgc cgggcaaagg cctggaatgg attggctata tttattatag cggcagcacc 240
aactataacc cgagcctgaa aagccgcgtg accattagcg tggataccag caaaaaccag 300
tttagcctga aactgagcag cgtgaccgcg gcggataccg cggtgtatta ttgcgcgcgc 360
gaaggcaaaa acggcgcgtt tgatatttgg ggccagggca ccatggtgac cgtgagcagc 420
ggcggcggcg gcagcggcgg cggcggcagc ggcggcggcg gcagccgcca tcagatgacc 480
cagagcccga gcagcctgag cgcgagcgtg ggcgatcgcg tgaccattac ctgccgcgcg 540
agccagagca ttagcagcta tctgaactgg tatcagcaga aaccgggcaa agcgccgaaa 600
ctgctgattt atgcggcgag cagcctgcag agcggcgtgc cgagccgctt tagcggcagc 660
ggcagcggca ccgattttac cctgaccatt agcagcctgc agccggaaga ttttgcgacc 720
tattattgcc agcagagcta tagcaccccg ctgacctttg gcggcggcac caaagtggaa 780
attaaacgca ccgcggcggc g 801
<210> 47
<211> 801
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 47
atggccctcc cggtaacggc tctgctgctt ccactcgcac tgctcttgca tgctgccaga 60
ccacaggtcc agctgcagga gagtgggcct ggactggtta agccgagtga gacactttcc 120
ttgacgtgca ctgtgagcgg gggaagtgtg tcctcaggta gttattactg gtcctggatt 180
cgccagccac caggaaaggg actggagtgg ataggttata tctattattc tggcagcact 240
aattacaatc cttctctcaa aagtagggtg acaatttcag tggatacttc caaaaatcag 300
tttagtctga agctcagctc tgtgacagct gctgatactg cagtttacta ctgcgccagg 360
gaggggaaga atggcgcctt cgatatttgg ggacagggca ctatggtgac tgtatcaagc 420
ggaggcggtg gcagcggcgg gggagggagt ggaggcggcg ggtctcgaca tcagatgaca 480
cagagcccat catcacttag cgccagcgtt ggcgaccggg ttacgataac atgcagggct 540
tcccaatcta tcagttctta tctgaactgg tatcagcaga aaccaggtaa ggcccccaag 600
ctgctcatct acgcagcctc atccctgcag agcggcgtcc ctagtcgatt ttccggtagt 660
gggtcaggga cagattttac cctgactatc agttcactgc agcccgagga cttcgcgaca 720
tactattgcc aacagtccta tagtacaccc ttgacatttg gcggcgggac taaagtagaa 780
attaaacgca ccgcggccgc a 801
<210> 48
<211> 288
<212> БЕЛОК
<213> Homo sapiens
<400> 48
Met Gln Ile Pro Gln Ala Pro Trp Pro Val Val Trp Ala Val Leu Gln
1 5 10 15
Leu Gly Trp Arg Pro Gly Trp Phe Leu Asp Ser Pro Asp Arg Pro Trp
20 25 30
Asn Pro Pro Thr Phe Ser Pro Ala Leu Leu Val Val Thr Glu Gly Asp
35 40 45
Asn Ala Thr Phe Thr Cys Ser Phe Ser Asn Thr Ser Glu Ser Phe Val
50 55 60
Leu Asn Trp Tyr Arg Met Ser Pro Ser Asn Gln Thr Asp Lys Leu Ala
65 70 75 80
Ala Phe Pro Glu Asp Arg Ser Gln Pro Gly Gln Asp Cys Arg Phe Arg
85 90 95
Val Thr Gln Leu Pro Asn Gly Arg Asp Phe His Met Ser Val Val Arg
100 105 110
Ala Arg Arg Asn Asp Ser Gly Thr Tyr Leu Cys Gly Ala Ile Ser Leu
115 120 125
Ala Pro Lys Ala Gln Ile Lys Glu Ser Leu Arg Ala Glu Leu Arg Val
130 135 140
Thr Glu Arg Arg Ala Glu Val Pro Thr Ala His Pro Ser Pro Ser Pro
145 150 155 160
Arg Pro Ala Gly Gln Phe Gln Thr Leu Val Val Gly Val Val Gly Gly
165 170 175
Leu Leu Gly Ser Leu Val Leu Leu Val Trp Val Leu Ala Val Ile Cys
180 185 190
Ser Arg Ala Ala Arg Gly Thr Ile Gly Ala Arg Arg Thr Gly Gln Pro
195 200 205
Leu Lys Glu Asp Pro Ser Ala Val Pro Val Phe Ser Val Asp Tyr Gly
210 215 220
Glu Leu Asp Phe Gln Trp Arg Glu Lys Thr Pro Glu Pro Pro Val Pro
225 230 235 240
Cys Val Pro Glu Gln Thr Glu Tyr Ala Thr Ile Val Phe Pro Ser Gly
245 250 255
Met Gly Thr Ser Ser Pro Ala Arg Arg Gly Ser Ala Asp Gly Pro Arg
260 265 270
Ser Ala Gln Pro Leu Arg Pro Glu Asp Gly His Cys Ser Trp Pro Leu
275 280 285
<210> 49
<211> 239
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 49
Met Gln Ile Pro Gln Ala Pro Trp Pro Val Val Trp Ala Val Leu Gln
1 5 10 15
Leu Gly Trp Arg Pro Gly Trp Phe Leu Asp Ser Pro Asp Arg Pro Trp
20 25 30
Asn Pro Pro Thr Phe Ser Pro Ala Leu Leu Val Val Thr Glu Gly Asp
35 40 45
Asn Ala Thr Phe Thr Cys Ser Phe Ser Asn Thr Ser Glu Ser Phe Val
50 55 60
Leu Asn Trp Tyr Arg Met Ser Pro Ser Asn Gln Thr Asp Lys Leu Ala
65 70 75 80
Ala Phe Pro Glu Asp Arg Ser Gln Pro Gly Gln Asp Cys Arg Phe Arg
85 90 95
Val Thr Gln Leu Pro Asn Gly Arg Asp Phe His Met Ser Val Val Arg
100 105 110
Ala Arg Arg Asn Asp Ser Gly Thr Tyr Leu Cys Gly Ala Ile Ser Leu
115 120 125
Ala Pro Lys Ala Gln Ile Lys Glu Ser Leu Arg Ala Glu Leu Arg Val
130 135 140
Thr Glu Arg Arg Ala Glu Val Pro Thr Ala His Pro Ser Pro Ser Pro
145 150 155 160
Arg Pro Ala Gly Gln Ala Ala Ala Pro Thr Thr Thr Pro Ala Pro Arg
165 170 175
Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg
180 185 190
Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly
195 200 205
Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr
210 215 220
Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Asn
225 230 235
<210> 50
<211> 45
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 50
ggaggtggag gctcaggagg aggaggcagt ggaggtggtg ggtca 45
<210> 51
<211> 45
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 51
ggtggaggcg gttcaggcgg aggtggctct ggcggtggcg gatca 45
<210> 52
<211> 357
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 52
Cys Ala Gly Gly Thr Thr Cys Ala Gly Cys Thr Thr Cys Ala Gly Gly
1 5 10 15
Ala Gly Ala Gly Thr Gly Gly Cys Cys Cys Ala Gly Gly Cys Cys Thr
20 25 30
Gly Gly Thr Gly Ala Ala Gly Cys Cys Ala Ala Gly Thr Gly Ala Gly
35 40 45
Ala Cys Thr Cys Thr Cys Ala Gly Cys Thr Thr Gly Ala Cys Thr Thr
50 55 60
Gly Cys Ala Cys Ala Gly Thr Thr Thr Cys Thr Gly Gly Ala Gly Gly
65 70 75 80
Cys Ala Gly Thr Gly Thr Cys Thr Cys Cys Thr Cys Ala Gly Gly Cys
85 90 95
Ala Gly Cys Thr Ala Thr Thr Ala Thr Thr Gly Gly Thr Cys Cys Thr
100 105 110
Gly Gly Ala Thr Thr Cys Gly Gly Cys Ala Gly Cys Cys Cys Cys Cys
115 120 125
Thr Gly Gly Gly Ala Ala Ala Gly Gly Cys Cys Thr Gly Gly Ala Gly
130 135 140
Thr Gly Gly Ala Thr Thr Gly Gly Gly Thr Ala Cys Ala Thr Ala Thr
145 150 155 160
Ala Thr Thr Ala Cys Ala Gly Thr Gly Gly Cys Ala Gly Cys Ala Cys
165 170 175
Ala Ala Ala Thr Thr Ala Cys Ala Ala Thr Cys Cys Ala Thr Cys Cys
180 185 190
Cys Thr Gly Ala Ala Gly Thr Cys Thr Cys Gly Ala Gly Thr Ala Ala
195 200 205
Cys Thr Ala Thr Cys Ala Gly Thr Gly Thr Gly Gly Ala Cys Ala Cys
210 215 220
Ala Ala Gly Cys Ala Ala Gly Ala Ala Thr Cys Ala Gly Thr Thr Thr
225 230 235 240
Thr Cys Ala Cys Thr Cys Ala Ala Ala Cys Thr Gly Thr Cys Thr Thr
245 250 255
Cys Thr Gly Thr Gly Ala Cys Thr Gly Cys Thr Gly Cys Thr Gly Ala
260 265 270
Cys Ala Cys Thr Gly Cys Thr Gly Thr Thr Thr Ala Thr Thr Ala Thr
275 280 285
Thr Gly Thr Gly Cys Cys Ala Gly Gly Gly Ala Gly Gly Gly Gly Ala
290 295 300
Ala Ala Ala Ala Thr Gly Gly Gly Gly Cys Ala Thr Thr Thr Gly Ala
305 310 315 320
Thr Ala Thr Thr Thr Gly Gly Gly Gly Thr Cys Ala Gly Gly Gly Cys
325 330 335
Ala Cys Ala Ala Thr Gly Gly Thr Gly Ala Cys Ala Gly Thr Cys Ala
340 345 350
Gly Cys Thr Cys Thr
355
<210> 53
<211> 327
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 53
cgccatcaga tgactcagtc cccctccagt ctttctgcct cagttgggga tagagtgacc 60
atcacatgca gagcaagtca gagcatatca tcctatctga actggtacca gcagaagcca 120
gggaaagccc ccaaattgct gatttatgca gcctcaagtc tccagagtgg ggtgccaagc 180
aggttctcag gcagtggcag tgggacagat ttcacattga caatcagctc cctccaacct 240
gaagattttg ccacctacta ttgccagcaa tcctacagca cgcccctgac ttttggaggt 300
ggcacaaagg tagagatcaa gaggact 327
<210> 54
<211> 117
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 54
attgaagtta tgtatcctcc tccttaccta gacaatgaga agagcaatgg aaccattatc 60
catgtgaaag ggaaacacct ttgtccaagt cccctatttc ccggaccttc taagccc 117
<210> 55
<211> 336
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 55
agagtgaagt tcagcaggag cgcagacgcc cccgcgtacc agcagggcca gaaccagctc 60
tataacgagc tcaatctagg acgaagagag gagtacgatg ttttggacaa gagacgtggc 120
cgggaccctg agatgggggg aaagccgaga aggaagaacc ctcaggaagg cctgttcaat 180
gaactgcaga aagataagat ggcggaggcc ttcagtgaga ttgggatgaa aggcgagcgc 240
cggaggggca aggggcacga tggccttttc caggggctca gtacagccac caaggacacc 300
ttcgacgccc ttcacatgca ggccctgccc cctcgc 336
<210> 56
<211> 465
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 56
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Val Ser Ser Gly
20 25 30
Ser Tyr Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly Tyr Ile Tyr Tyr Ser Gly Ser Thr Asn Tyr Asn Pro Ser
50 55 60
Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe
65 70 75 80
Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Arg Glu Gly Lys Asn Gly Ala Phe Asp Ile Trp Gly Gln Gly
100 105 110
Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Arg His Gln Met Thr Gln Ser Pro Ser Ser
130 135 140
Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser
145 150 155 160
Gln Ser Ile Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys
165 170 175
Ala Pro Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val
180 185 190
Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
195 200 205
Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln
210 215 220
Ser Tyr Ser Thr Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile
225 230 235 240
Lys Arg Thr Ala Ala Ala Ile Glu Val Met Tyr Pro Pro Pro Tyr Leu
245 250 255
Asp Asn Glu Lys Ser Asn Gly Thr Ile Ile His Val Lys Gly Lys His
260 265 270
Leu Cys Pro Ser Pro Leu Phe Pro Gly Pro Ser Lys Pro Phe Trp Val
275 280 285
Leu Val Val Val Gly Gly Val Leu Ala Cys Tyr Ser Leu Leu Val Thr
290 295 300
Val Ala Phe Ile Ile Phe Trp Val Arg Ser Lys Arg Ser Arg Leu Leu
305 310 315 320
His Ser Asp Tyr Met Asn Met Thr Pro Arg Arg Pro Gly Pro Thr Arg
325 330 335
Lys His Tyr Gln Pro Tyr Ala Pro Pro Arg Asp Phe Ala Ala Tyr Arg
340 345 350
Ser Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln
355 360 365
Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu
370 375 380
Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly
385 390 395 400
Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Phe Asn Glu Leu Gln
405 410 415
Lys Asp Lys Met Ala Glu Ala Phe Ser Glu Ile Gly Met Lys Gly Glu
420 425 430
Arg Arg Arg Gly Lys Gly His Asp Gly Leu Phe Gln Gly Leu Ser Thr
435 440 445
Ala Thr Lys Asp Thr Phe Asp Ala Leu His Met Gln Ala Leu Pro Pro
450 455 460
Arg
465
<210> 57
<211> 1395
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 57
caggttcagc ttcaggagag tggcccaggc ctggtgaagc caagtgagac tctcagcttg 60
acttgcacag tttctggagg cagtgtctcc tcaggcagct attattggtc ctggattcgg 120
cagccccctg ggaaaggcct ggagtggatt gggtacatat attacagtgg cagcacaaat 180
tacaatccat ccctgaagtc tcgagtaact atcagtgtgg acacaagcaa gaatcagttt 240
tcactcaaac tgtcttctgt gactgctgct gacactgctg tttattattg tgccagggag 300
gggaaaaatg gggcatttga tatttggggt cagggcacaa tggtgacagt cagctctgga 360
ggtggaggct caggaggagg aggcagtgga ggtggtgggt cacgccatca gatgactcag 420
tccccctcca gtctttctgc ctcagttggg gatagagtga ccatcacatg cagagcaagt 480
cagagcatat catcctatct gaactggtac cagcagaagc cagggaaagc ccccaaattg 540
ctgatttatg cagcctcaag tctccagagt ggggtgccaa gcaggttctc aggcagtggc 600
agtgggacag atttcacatt gacaatcagc tccctccaac ctgaagattt tgccacctac 660
tattgccagc aatcctacag cacgcccctg acttttggag gtggcacaaa ggtagagatc 720
aagaggactg cggccgcaat tgaagttatg tatcctcctc cttacctaga caatgagaag 780
agcaatggaa ccattatcca tgtgaaaggg aaacaccttt gtccaagtcc cctatttccc 840
ggaccttcta agcccttttg ggtgctggtg gtggttggtg gagtcctggc ttgctatagc 900
ttgctagtaa cagtggcctt tattattttc tgggtgagga gtaagaggag caggctcctg 960
cacagtgact acatgaacat gactccccgc cgccccgggc ccacccgcaa gcattaccag 1020
ccctatgccc caccacgcga cttcgcagcc tatcgctcca gagtgaagtt cagcaggagc 1080
gcagacgccc ccgcgtacca gcagggccag aaccagctct ataacgagct caatctagga 1140
cgaagagagg agtacgatgt tttggacaag agacgtggcc gggaccctga gatgggggga 1200
aagccgagaa ggaagaaccc tcaggaaggc ctgttcaatg aactgcagaa agataagatg 1260
gcggaggcct tcagtgagat tgggatgaaa ggcgagcgcc ggaggggcaa ggggcacgat 1320
ggccttttcc aggggctcag tacagccacc aaggacacct tcgacgccct tcacatgcag 1380
gccctgcccc ctcgc 1395
<210> 58
<211> 145
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 58
Pro Gly Trp Phe Leu Asp Ser Pro Asp Arg Pro Trp Asn Pro Pro Thr
1 5 10 15
Phe Ser Pro Ala Leu Leu Val Val Thr Glu Gly Asp Asn Ala Thr Phe
20 25 30
Thr Cys Ser Phe Ser Asn Thr Ser Glu Ser Phe Val Leu Asn Trp Tyr
35 40 45
Arg Met Ser Pro Ser Asn Gln Thr Asp Lys Leu Ala Ala Phe Pro Glu
50 55 60
Asp Arg Ser Gln Pro Gly Gln Asp Cys Arg Phe Arg Val Thr Gln Leu
65 70 75 80
Pro Asn Gly Arg Asp Phe His Met Ser Val Val Arg Ala Arg Arg Asn
85 90 95
Asp Ser Gly Thr Tyr Leu Cys Gly Ala Ile Ser Leu Ala Pro Lys Ala
100 105 110
Gln Ile Lys Glu Ser Leu Arg Ala Glu Leu Arg Val Thr Glu Arg Arg
115 120 125
Ala Glu Val Pro Thr Ala His Pro Ser Pro Ser Pro Arg Pro Ala Gly
130 135 140
Gln
145
<210> 59
<211> 435
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 59
ccaggatggt tcttagactc cccagacagg ccctggaacc cccccacctt ctccccagcc 60
ctgctcgtgg tgaccgaagg ggacaacgcc accttcacct gcagcttctc caacacatcg 120
gagagcttcg tgctaaactg gtaccgcatg agccccagca accagacgga caagctggcc 180
gctttccccg aggaccgcag ccagcccggc caggactgcc gcttccgtgt cacacaactg 240
cccaacgggc gtgacttcca catgagcgtg gtcagggccc ggcgcaatga cagcggcacc 300
tacctctgtg gggccatctc cctggccccc aaggcgcaga tcaaagagag cctgcgggca 360
gagctcaggg tgacagagag aagggcagaa gtgcccacag cccaccccag cccctcaccc 420
aggccagccg gccag 435
<210> 60
<211> 60
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 60
atgcagatcc cacaggcgcc ctggccagtc gtctgggcgg tgctacaact gggctggcgg 60
<210> 61
<211> 495
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 61
atgcagatcc cacaggcgcc ctggccagtc gtctgggcgg tgctacaact gggctggcgg 60
ccaggatggt tcttagactc cccagacagg ccctggaacc cccccacctt ctccccagcc 120
ctgctcgtgg tgaccgaagg ggacaacgcc accttcacct gcagcttctc caacacatcg 180
gagagcttcg tgctaaactg gtaccgcatg agccccagca accagacgga caagctggcc 240
gctttccccg aggaccgcag ccagcccggc caggactgcc gcttccgtgt cacacaactg 300
cccaacgggc gtgacttcca catgagcgtg gtcagggccc ggcgcaatga cagcggcacc 360
tacctctgtg gggccatctc cctggccccc aaggcgcaga tcaaagagag cctgcgggca 420
gagctcaggg tgacagagag aagggcagaa gtgcccacag cccaccccag cccctcaccc 480
aggccagccg gccag 495
<210> 62
<211> 213
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 62
cccaccacga cgccagcgcc gcgaccacca accccggcgc ccacgatcgc gtcgcagccc 60
ctgtccctgc gcccagaggc gtgccggcca gcggcggggg gcgcagtgca cacgaggggg 120
ctggacttcg cctgtgatat ctacatctgg gcgcccctgg ccgggacttg tggggtcctt 180
ctcctgtcac tggttatcac cctttactgc aac 213
<210> 63
<211> 219
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 63
cccaccacga cgccagcgcc gcgaccacca accccggcgc ccacgatcgc gtcgcagccc 60
ctgtccctgc gcccagaggc gtgccggcca gcggcggggg gcgcagtgca cacgaggggg 120
ctggacttcg cctgtgatat ctacatctgg gcgcccctgg ccgggacttg tggggtcctt 180
ctcctgtcac tggttatcac cctttactgc aaccacagg 219
<210> 64
<211> 717
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 64
atgcagatcc cacaggcgcc ctggccagtc gtctgggcgg tgctacaact gggctggcgg 60
ccaggatggt tcttagactc cccagacagg ccctggaacc cccccacctt ctccccagcc 120
ctgctcgtgg tgaccgaagg ggacaacgcc accttcacct gcagcttctc caacacatcg 180
gagagcttcg tgctaaactg gtaccgcatg agccccagca accagacgga caagctggcc 240
gctttccccg aggaccgcag ccagcccggc caggactgcc gcttccgtgt cacacaactg 300
cccaacgggc gtgacttcca catgagcgtg gtcagggccc ggcgcaatga cagcggcacc 360
tacctctgtg gggccatctc cctggccccc aaggcgcaga tcaaagagag cctgcgggca 420
gagctcaggg tgacagagag aagggcagaa gtgcccacag cccaccccag cccctcaccc 480
aggccagccg gccaggcggc cgcacccacc acgacgccag cgccgcgacc accaaccccg 540
gcgcccacga tcgcgtcgca gcccctgtcc ctgcgcccag aggcgtgccg gccagcggcg 600
gggggcgcag tgcacacgag ggggctggac ttcgcctgtg atatctacat ctgggcgccc 660
ctggccggga cttgtggggt ccttctcctg tcactggtta tcacccttta ctgcaac 717
<210> 65
<211> 199
<212> БЕЛОК
<213> Homo sapiens
<400> 65
Met Lys Ser Gly Leu Trp Tyr Phe Phe Leu Phe Cys Leu Arg Ile Lys
1 5 10 15
Val Leu Thr Gly Glu Ile Asn Gly Ser Ala Asn Tyr Glu Met Phe Ile
20 25 30
Phe His Asn Gly Gly Val Gln Ile Leu Cys Lys Tyr Pro Asp Ile Val
35 40 45
Gln Gln Phe Lys Met Gln Leu Leu Lys Gly Gly Gln Ile Leu Cys Asp
50 55 60
Leu Thr Lys Thr Lys Gly Ser Gly Asn Thr Val Ser Ile Lys Ser Leu
65 70 75 80
Lys Phe Cys His Ser Gln Leu Ser Asn Asn Ser Val Ser Phe Phe Leu
85 90 95
Tyr Asn Leu Asp His Ser His Ala Asn Tyr Tyr Phe Cys Asn Leu Ser
100 105 110
Ile Phe Asp Pro Pro Pro Phe Lys Val Thr Leu Thr Gly Gly Tyr Leu
115 120 125
His Ile Tyr Glu Ser Gln Leu Cys Cys Gln Leu Lys Phe Trp Leu Pro
130 135 140
Ile Gly Cys Ala Ala Phe Val Val Val Cys Ile Leu Gly Cys Ile Leu
145 150 155 160
Ile Cys Trp Leu Thr Lys Lys Lys Tyr Ser Ser Ser Val His Asp Pro
165 170 175
Asn Gly Glu Tyr Met Phe Met Arg Ala Val Asn Thr Ala Lys Lys Ser
180 185 190
Arg Leu Thr Asp Val Thr Leu
195
<210> 66
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 66
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1 5 10 15
<210> 67
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 67
Met Tyr Arg Met Gln Leu Leu Ser Cys Ile Ala Leu Ser Leu Ala Leu
1 5 10 15
Val Thr Asn Ser
20
<210> 68
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 68
Met Tyr Ser Met Gln Leu Ala Ser Cys Val Thr Leu Thr Leu Val Leu
1 5 10 15
Leu Val Asn Ser
20
<210> 69
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 69
Met Glu Thr Pro Ala Gln Leu Leu Phe Leu Leu Leu Leu Trp Leu Pro
1 5 10 15
Asp Thr Thr Gly
20
<210> 70
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 70
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly
20
<210> 71
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 71
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro
20
<210> 72
<211> 18
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 72
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala
<210> 73
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 73
Met Lys Trp Val Thr Phe Ile Ser Leu Leu Phe Ser Ser Ala Tyr Ser
1 5 10 15
<210> 74
<211> 30
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 74
Met Asp Ser Lys Gly Ser Ser Gln Lys Gly Ser Arg Leu Leu Leu Leu
1 5 10 15
Leu Val Val Ser Asn Leu Leu Leu Cys Gln Gly Val Val Ser
20 25 30
<210> 75
<211> 622
<212> БЕЛОК
<213> Homo sapiens
<400> 75
Met Ala Leu Pro Thr Ala Arg Pro Leu Leu Gly Ser Cys Gly Thr Pro
1 5 10 15
Ala Leu Gly Ser Leu Leu Phe Leu Leu Phe Ser Leu Gly Trp Val Gln
20 25 30
Pro Ser Arg Thr Leu Ala Gly Glu Thr Gly Gln Glu Ala Ala Pro Leu
35 40 45
Asp Gly Val Leu Ala Asn Pro Pro Asn Ile Ser Ser Leu Ser Pro Arg
50 55 60
Gln Leu Leu Gly Phe Pro Cys Ala Glu Val Ser Gly Leu Ser Thr Glu
65 70 75 80
Arg Val Arg Glu Leu Ala Val Ala Leu Ala Gln Lys Asn Val Lys Leu
85 90 95
Ser Thr Glu Gln Leu Arg Cys Leu Ala His Arg Leu Ser Glu Pro Pro
100 105 110
Glu Asp Leu Asp Ala Leu Pro Leu Asp Leu Leu Leu Phe Leu Asn Pro
115 120 125
Asp Ala Phe Ser Gly Pro Gln Ala Cys Thr His Phe Phe Ser Arg Ile
130 135 140
Thr Lys Ala Asn Val Asp Leu Leu Pro Arg Gly Ala Pro Glu Arg Gln
145 150 155 160
Arg Leu Leu Pro Ala Ala Leu Ala Cys Trp Gly Val Arg Gly Ser Leu
165 170 175
Leu Ser Glu Ala Asp Val Arg Ala Leu Gly Gly Leu Ala Cys Asp Leu
180 185 190
Pro Gly Arg Phe Val Ala Glu Ser Ala Glu Val Leu Leu Pro Arg Leu
195 200 205
Val Ser Cys Pro Gly Pro Leu Asp Gln Asp Gln Gln Glu Ala Ala Arg
210 215 220
Ala Ala Leu Gln Gly Gly Gly Pro Pro Tyr Gly Pro Pro Ser Thr Trp
225 230 235 240
Ser Val Ser Thr Met Asp Ala Leu Arg Gly Leu Leu Pro Val Leu Gly
245 250 255
Gln Pro Ile Ile Arg Ser Ile Pro Gln Gly Ile Val Ala Ala Trp Arg
260 265 270
Gln Arg Ser Ser Arg Asp Pro Ser Trp Arg Gln Pro Glu Arg Thr Ile
275 280 285
Leu Arg Pro Arg Phe Arg Arg Glu Val Glu Lys Thr Ala Cys Pro Ser
290 295 300
Gly Lys Lys Ala Arg Glu Ile Asp Glu Ser Leu Ile Phe Tyr Lys Lys
305 310 315 320
Trp Glu Leu Glu Ala Cys Val Asp Ala Ala Leu Leu Ala Thr Gln Met
325 330 335
Asp Arg Val Asn Ala Ile Pro Phe Thr Tyr Glu Gln Leu Asp Val Leu
340 345 350
Lys His Lys Leu Asp Glu Leu Tyr Pro Gln Gly Tyr Pro Glu Ser Val
355 360 365
Ile Gln His Leu Gly Tyr Leu Phe Leu Lys Met Ser Pro Glu Asp Ile
370 375 380
Arg Lys Trp Asn Val Thr Ser Leu Glu Thr Leu Lys Ala Leu Leu Glu
385 390 395 400
Val Asn Lys Gly His Glu Met Ser Pro Gln Val Ala Thr Leu Ile Asp
405 410 415
Arg Phe Val Lys Gly Arg Gly Gln Leu Asp Lys Asp Thr Leu Asp Thr
420 425 430
Leu Thr Ala Phe Tyr Pro Gly Tyr Leu Cys Ser Leu Ser Pro Glu Glu
435 440 445
Leu Ser Ser Val Pro Pro Ser Ser Ile Trp Ala Val Arg Pro Gln Asp
450 455 460
Leu Asp Thr Cys Asp Pro Arg Gln Leu Asp Val Leu Tyr Pro Lys Ala
465 470 475 480
Arg Leu Ala Phe Gln Asn Met Asn Gly Ser Glu Tyr Phe Val Lys Ile
485 490 495
Gln Ser Phe Leu Gly Gly Ala Pro Thr Glu Asp Leu Lys Ala Leu Ser
500 505 510
Gln Gln Asn Val Ser Met Asp Leu Ala Thr Phe Met Lys Leu Arg Thr
515 520 525
Asp Ala Val Leu Pro Leu Thr Val Ala Glu Val Gln Lys Leu Leu Gly
530 535 540
Pro His Val Glu Gly Leu Lys Ala Glu Glu Arg His Arg Pro Val Arg
545 550 555 560
Asp Trp Ile Leu Arg Gln Arg Gln Asp Asp Leu Asp Thr Leu Gly Leu
565 570 575
Gly Leu Gln Gly Gly Ile Pro Asn Gly Tyr Leu Val Leu Asp Leu Ser
580 585 590
Val Gln Glu Ala Leu Ser Gly Thr Pro Cys Leu Leu Gly Pro Gly Pro
595 600 605
Val Leu Thr Val Leu Ala Leu Leu Leu Ala Ser Thr Leu Ala
610 615 620
<210> 76
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 76
Gly Gly Ser Val Ser Ser Gly Ser Tyr Tyr
1 5 10
<210> 77
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 77
Ile Tyr Tyr Ser Gly Ser Thr
1 5
<210> 78
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 78
Ala Arg Glu Gly Lys Asn Gly Ala Phe Asp Ile Trp
1 5 10
<210> 79
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 79
Gln Ser Ile Ser Ser Tyr
1 5
<210> 80
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 80
Ala Ala Ser Ser
1
<210> 81
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 81
Gln Gln Ser Tyr Ser Thr Pro Leu Thr Phe
1 5 10
<210> 82
<211> 119
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 82
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Val Ser Ser Gly
20 25 30
Ser Tyr Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly Tyr Ile Tyr Tyr Ser Gly Ser Thr Asn Tyr Asn Pro Ser
50 55 60
Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe
65 70 75 80
Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Arg Glu Gly Lys Asn Gly Ala Phe Asp Ile Trp Gly Gln Gly
100 105 110
Thr Met Val Thr Val Ser Ser
115
<210> 83
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 83
Arg His Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg Thr
100 105
<210> 84
<211> 243
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 84
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Val Ser Ser Gly
20 25 30
Ser Tyr Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly Tyr Ile Tyr Tyr Ser Gly Ser Thr Asn Tyr Asn Pro Ser
50 55 60
Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe
65 70 75 80
Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Arg Glu Gly Lys Asn Gly Ala Phe Asp Ile Trp Gly Gln Gly
100 105 110
Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Arg His Gln Met Thr Gln Ser Pro Ser Ser
130 135 140
Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser
145 150 155 160
Gln Ser Ile Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys
165 170 175
Ala Pro Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val
180 185 190
Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
195 200 205
Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln
210 215 220
Ser Tyr Ser Thr Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile
225 230 235 240
Lys Arg Thr
<210> 85
<211> 729
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 85
caggttcagc ttcaggagag tggcccaggc ctggtgaagc caagtgagac tctcagcttg 60
acttgcacag tttctggagg cagtgtctcc tcaggcagct attattggtc ctggattcgg 120
cagccccctg ggaaaggcct ggagtggatt gggtacatat attacagtgg cagcacaaat 180
tacaatccat ccctgaagtc tcgagtaact atcagtgtgg acacaagcaa gaatcagttt 240
tcactcaaac tgtcttctgt gactgctgct gacactgctg tttattattg tgccagggag 300
gggaaaaatg gggcatttga tatttggggt cagggcacaa tggtgacagt cagctctgga 360
ggtggaggct caggaggagg aggcagtgga ggtggtgggt cacgccatca gatgactcag 420
tccccctcca gtctttctgc ctcagttggg gatagagtga ccatcacatg cagagcaagt 480
cagagcatat catcctatct gaactggtac cagcagaagc cagggaaagc ccccaaattg 540
ctgatttatg cagcctcaag tctccagagt ggggtgccaa gcaggttctc aggcagtggc 600
agtgggacag atttcacatt gacaatcagc tccctccaac ctgaagattt tgccacctac 660
tattgccagc aatcctacag cacgcccctg acttttggag gtggcacaaa ggtagagatc 720
aagaggact 729
<210> 86
<211> 235
<212> БЕЛОК
<213> Homo sapiens
<400> 86
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Ser Gln Phe Arg Val Ser Pro Leu Asp Arg Thr
20 25 30
Trp Asn Leu Gly Glu Thr Val Glu Leu Lys Cys Gln Val Leu Leu Ser
35 40 45
Asn Pro Thr Ser Gly Cys Ser Trp Leu Phe Gln Pro Arg Gly Ala Ala
50 55 60
Ala Ser Pro Thr Phe Leu Leu Tyr Leu Ser Gln Asn Lys Pro Lys Ala
65 70 75 80
Ala Glu Gly Leu Asp Thr Gln Arg Phe Ser Gly Lys Arg Leu Gly Asp
85 90 95
Thr Phe Val Leu Thr Leu Ser Asp Phe Arg Arg Glu Asn Glu Gly Tyr
100 105 110
Tyr Phe Cys Ser Ala Leu Ser Asn Ser Ile Met Tyr Phe Ser His Phe
115 120 125
Val Pro Val Phe Leu Pro Ala Lys Pro Thr Thr Thr Pro Ala Pro Arg
130 135 140
Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg
145 150 155 160
Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly
165 170 175
Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr
180 185 190
Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Asn His
195 200 205
Arg Asn Arg Arg Arg Val Cys Lys Cys Pro Arg Pro Val Val Lys Ser
210 215 220
Gly Asp Lys Pro Ser Leu Ser Ala Arg Tyr Val
225 230 235
<210> 87
<211> 247
<212> БЕЛОК
<213> Mus musculus
<400> 87
Met Ala Ser Pro Leu Thr Arg Phe Leu Ser Leu Asn Leu Leu Leu Met
1 5 10 15
Gly Glu Ser Ile Ile Leu Gly Ser Gly Glu Ala Lys Pro Gln Ala Pro
20 25 30
Glu Leu Arg Ile Phe Pro Lys Lys Met Asp Ala Glu Leu Gly Gln Lys
35 40 45
Val Asp Leu Val Cys Glu Val Leu Gly Ser Val Ser Gln Gly Cys Ser
50 55 60
Trp Leu Phe Gln Asn Ser Ser Ser Lys Leu Pro Gln Pro Thr Phe Val
65 70 75 80
Val Tyr Met Ala Ser Ser His Asn Lys Ile Thr Trp Asp Glu Lys Leu
85 90 95
Asn Ser Ser Lys Leu Phe Ser Ala Val Arg Asp Thr Asn Asn Lys Tyr
100 105 110
Val Leu Thr Leu Asn Lys Phe Ser Lys Glu Asn Glu Gly Tyr Tyr Phe
115 120 125
Cys Ser Val Ile Ser Asn Ser Val Met Tyr Phe Ser Ser Val Val Pro
130 135 140
Val Leu Gln Lys Val Asn Ser Thr Thr Thr Lys Pro Val Leu Arg Thr
145 150 155 160
Pro Ser Pro Val His Pro Thr Gly Thr Ser Gln Pro Gln Arg Pro Glu
165 170 175
Asp Cys Arg Pro Arg Gly Ser Val Lys Gly Thr Gly Leu Asp Phe Ala
180 185 190
Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Ile Cys Val Ala Pro
195 200 205
Leu Leu Ser Leu Ile Ile Thr Leu Ile Cys Tyr His Arg Ser Arg Lys
210 215 220
Arg Val Cys Lys Cys Pro Arg Pro Leu Val Arg Gln Glu Gly Lys Pro
225 230 235 240
Arg Pro Ser Glu Lys Ile Val
245
<210> 88
<211> 69
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 88
Ser Thr Thr Thr Lys Pro Val Leu Arg Thr Pro Ser Pro Val His Pro
1 5 10 15
Thr Gly Thr Ser Gln Pro Gln Arg Pro Glu Asp Cys Arg Pro Arg Gly
20 25 30
Ser Val Lys Gly Thr Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp
35 40 45
Ala Pro Leu Ala Gly Ile Cys Val Ala Leu Leu Leu Ser Leu Ile Ile
50 55 60
Thr Leu Ile Cys Tyr
65
<210> 89
<211> 207
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 89
tctactacta ccaagccagt gctgcgaact ccctcacctg tgcaccctac cgggacatct 60
cagccccaga gaccagaaga ttgtcggccc cgtggctcag tgaaggggac cggattggac 120
ttcgcctgtg atatttacat ctgggcaccc ttggccggaa tctgcgtggc ccttctgctg 180
tccttgatca tcactctcat ctgctac 207
<210> 90
<211> 220
<212> БЕЛОК
<213> Homo sapiens
<400> 90
Met Leu Arg Leu Leu Leu Ala Leu Asn Leu Phe Pro Ser Ile Gln Val
1 5 10 15
Thr Gly Asn Lys Ile Leu Val Lys Gln Ser Pro Met Leu Val Ala Tyr
20 25 30
Asp Asn Ala Val Asn Leu Ser Cys Lys Tyr Ser Tyr Asn Leu Phe Ser
35 40 45
Arg Glu Phe Arg Ala Ser Leu His Lys Gly Leu Asp Ser Ala Val Glu
50 55 60
Val Cys Val Val Tyr Gly Asn Tyr Ser Gln Gln Leu Gln Val Tyr Ser
65 70 75 80
Lys Thr Gly Phe Asn Cys Asp Gly Lys Leu Gly Asn Glu Ser Val Thr
85 90 95
Phe Tyr Leu Gln Asn Leu Tyr Val Asn Gln Thr Asp Ile Tyr Phe Cys
100 105 110
Lys Ile Glu Val Met Tyr Pro Pro Pro Tyr Leu Asp Asn Glu Lys Ser
115 120 125
Asn Gly Thr Ile Ile His Val Lys Gly Lys His Leu Cys Pro Ser Pro
130 135 140
Leu Phe Pro Gly Pro Ser Lys Pro Phe Trp Val Leu Val Val Val Gly
145 150 155 160
Gly Val Leu Ala Cys Tyr Ser Leu Leu Val Thr Val Ala Phe Ile Ile
165 170 175
Phe Trp Val Arg Ser Lys Arg Ser Arg Leu Leu His Ser Asp Tyr Met
180 185 190
Asn Met Thr Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln Pro
195 200 205
Tyr Ala Pro Pro Arg Asp Phe Ala Ala Tyr Arg Ser
210 215 220
<210> 91
<211> 81
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 91
ttttgggtgc tggtggtggt tggtggagtc ctggcttgct atagcttgct agtaacagtg 60
gcctttatta ttttctgggt g 81
<210> 92
<211> 27
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 92
Phe Trp Val Leu Val Val Val Gly Gly Val Leu Ala Cys Tyr Ser Leu
1 5 10 15
Leu Val Thr Val Ala Phe Ile Ile Phe Trp Val
20 25
<210> 93
<211> 81
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 93
ttttgggtgc tggtggtggt tggtggagtc ctggcttgct atagcttgct agtaacagtg 60
gcctttatta ttttctgggt g 81
<210> 94
<211> 164
<212> БЕЛОК
<213> Homo sapiens
<400> 94
Met Lys Trp Lys Ala Leu Phe Thr Ala Ala Ile Leu Gln Ala Gln Leu
1 5 10 15
Pro Ile Thr Glu Ala Gln Ser Phe Gly Leu Leu Asp Pro Lys Leu Cys
20 25 30
Tyr Leu Leu Asp Gly Ile Leu Phe Ile Tyr Gly Val Ile Leu Thr Ala
35 40 45
Leu Phe Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr
50 55 60
Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg
65 70 75 80
Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met
85 90 95
Gly Gly Lys Pro Gln Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn
100 105 110
Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met
115 120 125
Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly
130 135 140
Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala
145 150 155 160
Leu Pro Pro Arg
<210> 95
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 95
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly
1 5 10 15
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
20 25 30
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
35 40 45
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
50 55 60
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
65 70 75 80
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
85 90 95
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
100 105 110
<210> 96
<211> 336
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 96
agagtgaagt tcagcaggag cgcagacgcc cccgcgtacc agcagggcca gaaccagctc 60
tataacgagc tcaatctagg acgaagagag gagtacgatg ttttggacaa gagacgtggc 120
cgggaccctg agatgggggg aaagccgaga aggaagaacc ctcaggaagg cctgtacaat 180
gaactgcaga aagataagat ggcggaggcc tacagtgaga ttgggatgaa aggcgagcgc 240
cggaggggca aggggcacga tggcctttac cagggtctca gtacagccac caaggacacc 300
tacgacgccc ttcacatgca ggccctgccc cctcgc 336
<210> 97
<211> 218
<212> БЕЛОК
<213> Mus musculus
<400> 97
Met Thr Leu Arg Leu Leu Phe Leu Ala Leu Asn Phe Phe Ser Val Gln
1 5 10 15
Val Thr Glu Asn Lys Ile Leu Val Lys Gln Ser Pro Leu Leu Val Val
20 25 30
Asp Ser Asn Glu Val Ser Leu Ser Cys Arg Tyr Ser Tyr Asn Leu Leu
35 40 45
Ala Lys Glu Phe Arg Ala Ser Leu Tyr Lys Gly Val Asn Ser Asp Val
50 55 60
Glu Val Cys Val Gly Asn Gly Asn Phe Thr Tyr Gln Pro Gln Phe Arg
65 70 75 80
Ser Asn Ala Glu Phe Asn Cys Asp Gly Asp Phe Asp Asn Glu Thr Val
85 90 95
Thr Phe Arg Leu Trp Asn Leu His Val Asn His Thr Asp Ile Tyr Phe
100 105 110
Cys Lys Ile Glu Phe Met Tyr Pro Pro Pro Tyr Leu Asp Asn Glu Arg
115 120 125
Ser Asn Gly Thr Ile Ile His Ile Lys Glu Lys His Leu Cys His Thr
130 135 140
Gln Ser Ser Pro Lys Leu Phe Trp Ala Leu Val Val Val Ala Gly Val
145 150 155 160
Leu Phe Cys Tyr Gly Leu Leu Val Thr Val Ala Leu Cys Val Ile Trp
165 170 175
Thr Asn Ser Arg Arg Asn Arg Leu Leu Gln Ser Asp Tyr Met Asn Met
180 185 190
Thr Pro Arg Arg Pro Gly Leu Thr Arg Lys Pro Tyr Gln Pro Tyr Ala
195 200 205
Pro Ala Arg Asp Phe Ala Ala Tyr Arg Pro
210 215
<210> 98
<211> 123
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 98
aatagtagaa ggaacagact ccttcaaagt gactacatga acatgactcc ccggaggcct 60
gggctcactc gaaagcctta ccagccctac gcccctgcca gagactttgc agcgtaccgc 120
ccc 123
<210> 99
<211> 41
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 99
Asn Ser Arg Arg Asn Arg Leu Leu Gln Ser Asp Tyr Met Asn Met Thr
1 5 10 15
Pro Arg Arg Pro Gly Leu Thr Arg Lys Pro Tyr Gln Pro Tyr Ala Pro
20 25 30
Ala Arg Asp Phe Ala Ala Tyr Arg Pro
35 40
<210> 100
<211> 123
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 100
aatagtagaa ggaacagact ccttcaaagt gactacatga acatgactcc ccggaggcct 60
gggctcactc gaaagcctta ccagccctac gcccctgcca gagactttgc agcgtaccgc 120
ccc 123
<210> 101
<211> 41
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 101
Arg Ser Lys Arg Ser Arg Leu Leu His Ser Asp Tyr Met Asn Met Thr
1 5 10 15
Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln Pro Tyr Ala Pro
20 25 30
Pro Arg Asp Phe Ala Ala Tyr Arg Ser
35 40
<210> 102
<211> 123
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 102
aggagtaaga ggagcaggct cctgcacagt gactacatga acatgactcc ccgccgcccc 60
gggcccaccc gcaagcatta ccagccctat gccccaccac gcgacttcgc agcctatcgc 120
tcc 123
<210> 103
<211> 255
<212> БЕЛОК
<213> Homo sapiens
<400> 103
Met Gly Asn Ser Cys Tyr Asn Ile Val Ala Thr Leu Leu Leu Val Leu
1 5 10 15
Asn Phe Glu Arg Thr Arg Ser Leu Gln Asp Pro Cys Ser Asn Cys Pro
20 25 30
Ala Gly Thr Phe Cys Asp Asn Asn Arg Asn Gln Ile Cys Ser Pro Cys
35 40 45
Pro Pro Asn Ser Phe Ser Ser Ala Gly Gly Gln Arg Thr Cys Asp Ile
50 55 60
Cys Arg Gln Cys Lys Gly Val Phe Arg Thr Arg Lys Glu Cys Ser Ser
65 70 75 80
Thr Ser Asn Ala Glu Cys Asp Cys Thr Pro Gly Phe His Cys Leu Gly
85 90 95
Ala Gly Cys Ser Met Cys Glu Gln Asp Cys Lys Gln Gly Gln Glu Leu
100 105 110
Thr Lys Lys Gly Cys Lys Asp Cys Cys Phe Gly Thr Phe Asn Asp Gln
115 120 125
Lys Arg Gly Ile Cys Arg Pro Trp Thr Asn Cys Ser Leu Asp Gly Lys
130 135 140
Ser Val Leu Val Asn Gly Thr Lys Glu Arg Asp Val Val Cys Gly Pro
145 150 155 160
Ser Pro Ala Asp Leu Ser Pro Gly Ala Ser Ser Val Thr Pro Pro Ala
165 170 175
Pro Ala Arg Glu Pro Gly His Ser Pro Gln Ile Ile Ser Phe Phe Leu
180 185 190
Ala Leu Thr Ser Thr Ala Leu Leu Phe Leu Leu Phe Phe Leu Thr Leu
195 200 205
Arg Phe Ser Val Val Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe
210 215 220
Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly
225 230 235 240
Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu
245 250 255
<210> 104
<211> 42
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 104
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
1 5 10 15
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
20 25 30
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu
35 40
<210> 105
<211> 126
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 105
aaacggggca gaaagaaact cctgtatata ttcaaacaac catttatgag accagtacaa 60
actactcaag aggaagatgg ctgtagctgc cgatttccag aagaagaaga aggaggatgt 120
gaactg 126
<210> 106
<211> 277
<212> БЕЛОК
<213> Homo sapiens
<400> 106
Met Cys Val Gly Ala Arg Arg Leu Gly Arg Gly Pro Cys Ala Ala Leu
1 5 10 15
Leu Leu Leu Gly Leu Gly Leu Ser Thr Val Thr Gly Leu His Cys Val
20 25 30
Gly Asp Thr Tyr Pro Ser Asn Asp Arg Cys Cys His Glu Cys Arg Pro
35 40 45
Gly Asn Gly Met Val Ser Arg Cys Ser Arg Ser Gln Asn Thr Val Cys
50 55 60
Arg Pro Cys Gly Pro Gly Phe Tyr Asn Asp Val Val Ser Ser Lys Pro
65 70 75 80
Cys Lys Pro Cys Thr Trp Cys Asn Leu Arg Ser Gly Ser Glu Arg Lys
85 90 95
Gln Leu Cys Thr Ala Thr Gln Asp Thr Val Cys Arg Cys Arg Ala Gly
100 105 110
Thr Gln Pro Leu Asp Ser Tyr Lys Pro Gly Val Asp Cys Ala Pro Cys
115 120 125
Pro Pro Gly His Phe Ser Pro Gly Asp Asn Gln Ala Cys Lys Pro Trp
130 135 140
Thr Asn Cys Thr Leu Ala Gly Lys His Thr Leu Gln Pro Ala Ser Asn
145 150 155 160
Ser Ser Asp Ala Ile Cys Glu Asp Arg Asp Pro Pro Ala Thr Gln Pro
165 170 175
Gln Glu Thr Gln Gly Pro Pro Ala Arg Pro Ile Thr Val Gln Pro Thr
180 185 190
Glu Ala Trp Pro Arg Thr Ser Gln Gly Pro Ser Thr Arg Pro Val Glu
195 200 205
Val Pro Gly Gly Arg Ala Val Ala Ala Ile Leu Gly Leu Gly Leu Val
210 215 220
Leu Gly Leu Leu Gly Pro Leu Ala Ile Leu Leu Ala Leu Tyr Leu Leu
225 230 235 240
Arg Arg Asp Gln Arg Leu Pro Pro Asp Ala His Lys Pro Pro Gly Gly
245 250 255
Gly Ser Phe Arg Thr Pro Ile Gln Glu Glu Gln Ala Asp Ala His Ser
260 265 270
Thr Leu Ala Lys Ile
275
<210> 107
<211> 23
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 107
Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val
1 5 10 15
Glu Glu Asn Pro Gly Pro Met
20
<210> 108
<211> 41
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 108
Arg Ser Lys Arg Ser Arg Leu Leu His Ser Asp Tyr Met Asn Met Thr
1 5 10 15
Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln Pro Tyr Ala Pro
20 25 30
Pro Arg Asp Phe Ala Ala Tyr Arg Lys
35 40
<210> 109
<211> 39
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 109
Asn Gln Leu Glu Arg Thr Val Asn Ser Leu Asn Val Pro Ala Ile Ser
1 5 10 15
Ile Pro Glu His Asp Glu Ala Asp Glu Ile Ser Asp Glu Asn Arg Glu
20 25 30
Lys Val Asn Asp Gln Ala Lys
35
<210> 110
<211> 42
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 110
Ala Ala Ala Asn Gln Leu Glu Arg Thr Val Asn Ser Leu Asn Val Ser
1 5 10 15
Ala Ile Ser Ile Pro Glu His Asp Glu Ala Asp Glu Ile Ser Asp Glu
20 25 30
Asn Arg Glu Lys Val Asn Asp Gln Ala Lys
35 40
<210> 111
<211> 48
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 111
Pro Glu His Asp Glu Ala Asp Glu Ile Ser Asp Glu Asn Arg Glu Lys
1 5 10 15
Val Asn Asp Gln Ala Lys Leu Ile Val Gly Ile Val Val Gly Leu Leu
20 25 30
Leu Ala Ala Leu Val Ala Gly Val Val Tyr Trp Leu Tyr Met Lys Lys
35 40 45
<210> 112
<211> 37
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 112
Glu Asn Arg Glu Lys Val Asn Asp Gln Ala Lys Leu Ile Val Gly Ile
1 5 10 15
Val Val Gly Leu Leu Leu Ala Ala Leu Val Ala Gly Val Val Tyr Trp
20 25 30
Leu Tyr Met Lys Lys
35
<210> 113
<211> 65
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 113
Asn Gln Leu Glu Arg Thr Val Asn Ser Leu Asn Val Pro Ala Ile Ser
1 5 10 15
Ile Pro Glu His Asp Glu Ala Asp Glu Ile Ser Asp Glu Asn Arg Glu
20 25 30
Lys Val Asn Asp Gln Ala Lys Leu Ile Val Gly Ile Val Val Gly Leu
35 40 45
Leu Leu Ala Ala Leu Val Ala Gly Val Val Tyr Trp Leu Tyr Met Lys
50 55 60
Lys
65
<210> 114
<211> 66
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 114
Thr Cys Thr Ala Glu Asn Gln Leu Glu Arg Thr Val Asn Ser Leu Asn
1 5 10 15
Val Ser Ala Ile Ser Ile Pro Glu His Asp Glu Ala Asp Glu Ile Ser
20 25 30
Asp Glu Asn Arg Glu Lys Val Asn Asp Gln Ala Lys Leu Ile Val Gly
35 40 45
Ile Val Val Gly Leu Leu Leu Ala Ala Leu Val Ala Gly Val Val Tyr
50 55 60
Trp Leu
65
<210> 115
<211> 44
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 115
Pro Glu His Asp Glu Ala Asp Glu Ile Ser Asp Glu Asn Arg Glu Lys
1 5 10 15
Val Asn Asp Gln Ala Lys Leu Ile Val Gly Ile Val Val Gly Leu Leu
20 25 30
Leu Ala Ala Leu Val Ala Gly Val Val Tyr Trp Leu
35 40
<210> 116
<211> 61
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 116
Asn Gln Leu Glu Arg Thr Val Asn Ser Leu Asn Val Ser Ala Ile Ser
1 5 10 15
Ile Pro Glu His Asp Glu Ala Asp Glu Ile Ser Asp Glu Asn Arg Glu
20 25 30
Lys Val Asn Asp Gln Ala Lys Leu Ile Val Gly Ile Val Val Gly Leu
35 40 45
Leu Leu Ala Ala Leu Val Ala Gly Val Val Tyr Trp Leu
50 55 60
<210> 117
<211> 68
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 117
Ala Ala Ala Asn Gln Leu Glu Arg Thr Val Asn Ser Leu Asn Val Ser
1 5 10 15
Ala Ile Ser Ile Pro Glu His Asp Glu Ala Asp Glu Ile Ser Asp Glu
20 25 30
Asn Arg Glu Lys Val Asn Asp Gln Ala Lys Leu Ile Val Gly Ile Val
35 40 45
Val Gly Leu Leu Leu Ala Ala Leu Val Ala Gly Val Val Tyr Trp Leu
50 55 60
Tyr Met Lys Lys
65
<210> 118
<211> 241
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 118
Met Gln Ile Pro Gln Ala Pro Trp Pro Val Val Trp Ala Val Leu Gln
1 5 10 15
Leu Gly Trp Arg Pro Gly Trp Phe Leu Asp Ser Pro Asp Arg Pro Trp
20 25 30
Asn Pro Pro Thr Phe Ser Pro Ala Leu Leu Val Val Thr Glu Gly Asp
35 40 45
Asn Ala Thr Phe Thr Cys Ser Phe Ser Asn Thr Ser Glu Ser Phe Val
50 55 60
Leu Asn Trp Tyr Arg Met Ser Pro Ser Asn Gln Thr Asp Lys Leu Ala
65 70 75 80
Ala Phe Pro Glu Asp Arg Ser Gln Pro Gly Gln Asp Cys Arg Phe Arg
85 90 95
Val Thr Gln Leu Pro Asn Gly Arg Asp Phe His Met Ser Val Val Arg
100 105 110
Ala Arg Arg Asn Asp Ser Gly Thr Tyr Leu Cys Gly Ala Ile Ser Leu
115 120 125
Ala Pro Lys Ala Gln Ile Lys Glu Ser Leu Arg Ala Glu Leu Arg Val
130 135 140
Thr Glu Arg Arg Ala Glu Val Pro Thr Ala His Pro Ser Pro Ser Pro
145 150 155 160
Arg Pro Ala Gly Gln Ala Ala Ala Pro Thr Thr Thr Pro Ala Pro Arg
165 170 175
Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg
180 185 190
Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly
195 200 205
Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr
210 215 220
Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Asn His
225 230 235 240
Arg
<210> 119
<211> 723
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 119
atgcagatcc cacaggcgcc ctggccagtc gtctgggcgg tgctacaact gggctggcgg 60
ccaggatggt tcttagactc cccagacagg ccctggaacc cccccacctt ctccccagcc 120
ctgctcgtgg tgaccgaagg ggacaacgcc accttcacct gcagcttctc caacacatcg 180
gagagcttcg tgctaaactg gtaccgcatg agccccagca accagacgga caagctggcc 240
gctttccccg aggaccgcag ccagcccggc caggactgcc gcttccgtgt cacacaactg 300
cccaacgggc gtgacttcca catgagcgtg gtcagggccc ggcgcaatga cagcggcacc 360
tacctctgtg gggccatctc cctggccccc aaggcgcaga tcaaagagag cctgcgggca 420
gagctcaggg tgacagagag aagggcagaa gtgcccacag cccaccccag cccctcaccc 480
aggccagccg gccaggcggc cgcacccacc acgacgccag cgccgcgacc accaaccccg 540
gcgcccacga tcgcgtcgca gcccctgtcc ctgcgcccag aggcgtgccg gccagcggcg 600
gggggcgcag tgcacacgag ggggctggac ttcgcctgtg atatctacat ctgggcgccc 660
ctggccggga cttgtggggt ccttctcctg tcactggtta tcacccttta ctgcaaccac 720
agg 723
<210> 120
<211> 63
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 120
atggccctgc cagtaacggc tctgctgctg ccacttgctc tgctcctcca tgcagccagg 60
cct 63
<210> 121
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 121
Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val Glu Glu Asn
1 5 10 15
Pro Gly Pro
<210> 122
<211> 57
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 122
gcaacaaact tctcactact caaacaagca ggtgacgtgg aggagaatcc cggccca 57
<210> 123
<211> 8613
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 123
atggccctgc cagtaacggc tctgctgctg ccacttgctc tgctcctcca tgcagccagg 60
cctcaggttc agcttcagga gagtggccca ggcctggtga agccaagtga gactctcagc 120
ttgacttgca cagtttctgg aggcagtgtc tcctcaggca gctattattg gtcctggatt 180
cggcagcccc ctgggaaagg cctggagtgg attgggtaca tatattacag tggcagcaca 240
aattacaatc catccctgaa gtctcgagta actatcagtg tggacacaag caagaatcag 300
ttttcactca aactgtcttc tgtgactgct gctgacactg ctgtttatta ttgtgccagg 360
gaggggaaaa atggggcatt tgatatttgg ggtcagggca caatggtgac agtcagctct 420
ggaggtggag gctcaggagg aggaggcagt ggaggtggtg ggtcacgcca tcagatgact 480
cagtccccct ccagtctttc tgcctcagtt ggggatagag tgaccatcac atgcagagca 540
agtcagagca tatcatccta tctgaactgg taccagcaga agccagggaa agcccccaaa 600
ttgctgattt atgcagcctc aagtctccag agtggggtgc caagcaggtt ctcaggcagt 660
ggcagtggga cagatttcac attgacaatc agctccctcc aacctgaaga ttttgccacc 720
tactattgcc agcaatccta cagcacgccc ctgacttttg gaggtggcac aaaggtagag 780
atcaagagga ctgcggccgc aattgaagtt atgtatcctc ctccttacct agacaatgag 840
aagagcaatg gaaccattat ccatgtgaaa gggaaacacc tttgtccaag tcccctattt 900
cccggacctt ctaagccctt ttgggtgctg gtggtggttg gtggagtcct ggcttgctat 960
agcttgctag taacagtggc ctttattatt ttctgggtga ggagtaagag gagcaggctc 1020
ctgcacagtg actacatgaa catgactccc cgccgccccg ggcccacccg caagcattac 1080
cagccctatg ccccaccacg cgacttcgca gcctatcgct ccagagtgaa gttcagcagg 1140
agcgcagacg cccccgcgta ccagcagggc cagaaccagc tctataacga gctcaatcta 1200
ggacgaagag aggagtacga tgttttggac aagagacgtg gccgggaccc tgagatgggg 1260
ggaaagccga gaaggaagaa ccctcaggaa ggcctgttca atgaactgca gaaagataag 1320
atggcggagg ccttcagtga gattgggatg aaaggcgagc gccggagggg caaggggcac 1380
gatggccttt tccaggggct cagtacagcc accaaggaca ccttcgacgc ccttcacatg 1440
caggccctgc cccctcgcgg atctggagca acaaacttct cactactcaa acaagcaggt 1500
gacgtggagg agaatcccgg cccaatgcag atcccacagg cgccctggcc agtcgtctgg 1560
gcggtgctac aactgggctg gcggccagga tggttcttag actccccaga caggccctgg 1620
aaccccccca ccttctcccc agccctgctc gtggtgaccg aaggggacaa cgccaccttc 1680
acctgcagct tctccaacac atcggagagc ttcgtgctaa actggtaccg catgagcccc 1740
agcaaccaga cggacaagct ggccgctttc cccgaggacc gcagccagcc cggccaggac 1800
tgccgcttcc gtgtcacaca actgcccaac gggcgtgact tccacatgag cgtggtcagg 1860
gcccggcgca atgacagcgg cacctacctc tgtggggcca tctccctggc ccccaaggcg 1920
cagatcaaag agagcctgcg ggcagagctc agggtgacag agagaagggc agaagtgccc 1980
acagcccacc ccagcccctc acccaggcca gccggccagg cggccgcacc caccacgacg 2040
ccagcgccgc gaccaccaac cccggcgccc acgatcgcgt cgcagcccct gtccctgcgc 2100
ccagaggcgt gccggccagc ggcggggggc gcagtgcaca cgagggggct ggacttcgcc 2160
tgtgatatct acatctgggc gcccctggcc gggacttgtg gggtccttct cctgtcactg 2220
gttatcaccc tttactgcaa ccacaggcgg atccaataac agccactcga ggatccggat 2280
tagtccaatt tgttaaagac aggatatcag tggtccaggc tctagttttg actcaacaat 2340
atcaccagct gaagcctata gagtacgagc catagataaa ataaaagatt ttatttagtc 2400
tccagaaaaa ggggggaatg aaagacccca cctgtaggtt tggcaagcta gcttaagtaa 2460
cgccattttg caaggcatgg aaaaatacat aactgagaat agagaagttc agatcaaggt 2520
caggaacaga tggaacagct gaatatgggc caaacaggat atctgtggta agcagttcct 2580
gccccggctc agggccaaga acagatggaa cagctgaata tgggccaaac aggatatctg 2640
tggtaagcag ttcctgcccc ggctcagggc caagaacaga tggtccccag atgcggtcca 2700
gccctcagca gtttctagag aaccatcaga tgtttccagg gtgccccaag gacctgaaat 2760
gaccctgtgc cttatttgaa ctaaccaatc agttcgcttc tcgcttctgt tcgcgcgctt 2820
ctgctccccg agctcaataa aagagcccac aacccctcac tcggggcgcc agtcctccga 2880
ttgactgagt cgcccgggta cccgtgtatc caataaaccc tcttgcagtt gcatccgact 2940
tgtggtctcg ctgttccttg ggagggtctc ctctgagtga ttgactaccc gtcagcgggg 3000
gtctttcaca catgcagcat gtatcaaaat taatttggtt ttttttctta agtatttaca 3060
ttaaatggcc atagtactta aagttacatt ggcttccttg aaataaacat ggagtattca 3120
gaatgtgtca taaatatttc taattttaag atagtatctc cattggcttt ctactttttc 3180
ttttattttt ttttgtcctc tgtcttccat ttgttgttgt tgttgtttgt ttgtttgttt 3240
gttggttggt tggttaattt ttttttaaag atcctacact atagttcaag ctagactatt 3300
agctactctg taacccaggg tgaccttgaa gtcatgggta gcctgctgtt ttagccttcc 3360
cacatctaag attacaggta tgagctatca tttttggtat attgattgat tgattgattg 3420
atgtgtgtgt gtgtgattgt gtttgtgtgt gtgactgtga aaatgtgtgt atgggtgtgt 3480
gtgaatgtgt gtatgtatgt gtgtgtgtga gtgtgtgtgt gtgtgtgtgc atgtgtgtgt 3540
gtgtgactgt gtctatgtgt atgactgtgt gtgtgtgtgt gtgtgtgtgt gtgtgtgtgt 3600
gtgtgtgtgt gttgtgaaaa aatattctat ggtagtgaga gccaacgctc cggctcaggt 3660
gtcaggttgg tttttgagac agagtctttc acttagcttg gaattcactg gccgtcgttt 3720
tacaacgtcg tgactgggaa aaccctggcg ttacccaact taatcgcctt gcagcacatc 3780
cccctttcgc cagctggcgt aatagcgaag aggcccgcac cgatcgccct tcccaacagt 3840
tgcgcagcct gaatggcgaa tggcgcctga tgcggtattt tctccttacg catctgtgcg 3900
gtatttcaca ccgcatatgg tgcactctca gtacaatctg ctctgatgcc gcatagttaa 3960
gccagccccg acacccgcca acacccgctg acgcgccctg acgggcttgt ctgctcccgg 4020
catccgctta cagacaagct gtgaccgtct ccgggagctg catgtgtcag aggttttcac 4080
cgtcatcacc gaaacgcgcg atgacgaaag ggcctcgtga tacgcctatt tttataggtt 4140
aatgtcatga taataatggt ttcttagacg tcaggtggca cttttcgggg aaatgtgcgc 4200
ggaaccccta tttgtttatt tttctaaata cattcaaata tgtatccgct catgagacaa 4260
taaccctgat aaatgcttca ataatattga aaaaggaaga gtatgagtat tcaacatttc 4320
cgtgtcgccc ttattccctt ttttgcggca ttttgccttc ctgtttttgc tcacccagaa 4380
acgctggtga aagtaaaaga tgctgaagat cagttgggtg cacgagtggg ttacatcgaa 4440
ctggatctca acagcggtaa gatccttgag agttttcgcc ccgaagaacg ttttccaatg 4500
atgagcactt ttaaagttct gctatgtggc gcggtattat cccgtattga cgccgggcaa 4560
gagcaactcg gtcgccgcat acactattct cagaatgact tggttgagta ctcaccagtc 4620
acagaaaagc atcttacgga tggcatgaca gtaagagaat tatgcagtgc tgccataacc 4680
atgagtgata acactgcggc caacttactt ctgacaacga tcggaggacc gaaggagcta 4740
accgcttttt tgcacaacat gggggatcat gtaactcgcc ttgatcgttg ggaaccggag 4800
ctgaatgaag ccataccaaa cgacgagcgt gacaccacga tgcctgtagc aatggcaaca 4860
acgttgcgca aactattaac tggcgaacta cttactctag cttcccggca acaattaata 4920
gactggatgg aggcggataa agttgcagga ccacttctgc gctcggccct tccggctggc 4980
tggtttattg ctgataaatc tggagccggt gagcgtgggt ctcgcggtat cattgcagca 5040
ctggggccag atggtaagcc ctcccgtatc gtagttatct acacgacggg gagtcaggca 5100
actatggatg aacgaaatag acagatcgct gagataggtg cctcactgat taagcattgg 5160
taactgtcag accaagttta ctcatatata ctttagattg atttaaaact tcatttttaa 5220
tttaaaagga tctaggtgaa gatccttttt gataatctca tgaccaaaat cccttaacgt 5280
gagttttcgt tccactgagc gtcagacccc gtagaaaaga tcaaaggatc ttcttgagat 5340
cctttttttc tgcgcgtaat ctgctgcttg caaacaaaaa aaccaccgct accagcggtg 5400
gtttgtttgc cggatcaaga gctaccaact ctttttccga aggtaactgg cttcagcaga 5460
gcgcagatac caaatactgt ccttctagtg tagccgtagt taggccacca cttcaagaac 5520
tctgtagcac cgcctacata cctcgctctg ctaatcctgt taccagtggc tgctgccagt 5580
ggcgataagt cgtgtcttac cgggttggac tcaagacgat agttaccgga taaggcgcag 5640
cggtcgggct gaacgggggg ttcgtgcaca cagcccagct tggagcgaac gacctacacc 5700
gaactgagat acctacagcg tgagcattga gaaagcgcca cgcttcccga agggagaaag 5760
gcggacaggt atccggtaag cggcagggtc ggaacaggag agcgcacgag ggagcttcca 5820
gggggaaacg cctggtatct ttatagtcct gtcgggtttc gccacctctg acttgagcgt 5880
cgatttttgt gatgctcgtc aggggggcgg agcctatgga aaaacgccag caacgcggcc 5940
tttttacggt tcctggcctt ttgctggcct tttgctcaca tgttctttcc tgcgttatcc 6000
cctgattctg tggataaccg tattaccgcc tttgagtgag ctgataccgc tcgccgcagc 6060
cgaacgaccg agcgcagcga gtcagtgagc gaggaagcgg aagagcgccc aatacgcaaa 6120
ccgcctctcc ccgcgcgttg gccgattcat taatgcagct ggcacgacag gtttcccgac 6180
tggaaagcgg gcagtgagcg caacgcaatt aatgtgagtt agctcactca ttaggcaccc 6240
caggctttac actttatgct tccggctcgt atgttgtgtg gaattgtgag cggataacaa 6300
tttcacacag gaaacagcta tgaccatgat tacgccaagc tttgctctta ggagtttcct 6360
aatacatccc aaactcaaat atataaagca tttgacttgt tctatgccct agggggcggg 6420
gggaagctaa gccagctttt tttaacattt aaaatgttaa ttccatttta aatgcacaga 6480
tgtttttatt tcataagggt ttcaatgtgc atgaatgctg caatattcct gttaccaaag 6540
ctagtataaa taaaaataga taaacgtgga aattacttag agtttctgtc attaacgttt 6600
ccttcctcag ttgacaacat aaatgcgctg ctgagcaagc cagtttgcat ctgtcaggat 6660
caatttccca ttatgccagt catattaatt actagtcaat tagttgattt ttatttttga 6720
catatacatg tgaatgaaag accccacctg taggtttggc aagctagctt aagtaacgcc 6780
attttgcaag gcatggaaaa atacataact gagaatagaa aagttcagat caaggtcagg 6840
aacagatgga acagctgaat atgggccaaa caggatatct gtggtaagca gttcctgccc 6900
cggctcaggg ccaagaacag atggaacagc tgaatatggg ccaaacagga tatctgtggt 6960
aagcagttcc tgccccggct cagggccaag aacagatggt ccccagatgc ggtccagccc 7020
tcagcagttt ctagagaacc atcagatgtt tccagggtgc cccaaggacc tgaaatgacc 7080
ctgtgcctta tttgaactaa ccaatcagtt cgcttctcgc ttctgttcgc gcgcttatgc 7140
tccccgagct caataaaaga gcccacaacc cctcactcgg ggcgccagtc ctccgattga 7200
ctgagtcgcc cgggtacccg tgtatccaat aaaccctctt gcagttgcat ccgacttgtg 7260
gtctcgctgt tccttgggag ggtctcctct gagtgattga ctacccgtca gcgggggtct 7320
ttcatttggg ggctcgtccg ggatcgggag acccctgccc agggaccacc gacccaccac 7380
cgggaggtaa gctggccagc aacttatctg tgtctgtccg attgtctagt gtctatgact 7440
gattttatgc gcctgcgtcg gtactagtta gctaactagc tctgtatctg gcggacccgt 7500
ggtggaactg acgagttcgg aacacccggc cgcaaccctg ggagacgtcc cagggacttc 7560
gggggccgtt tttgtggccc gacctgagtc ctaaaatccc gatcgtttag gactctttgg 7620
tgcacccccc ttagaggagg gatatgtggt tctggtagga gacgagaacc taaaacagtt 7680
cccgcctccg tctgaatttt tgctttcggt ttgggaccga agccgcgccg cgcgtcttgt 7740
ctgctgcagc atcgttctgt gttgtctctg tctgactgtg tttctgtatt tgtctgaaaa 7800
tatgggcccg ggctagcctg ttaccactcc cttaagtttg accttaggtc actggaaaga 7860
tgtcgagcgg atcgctcaca accagtcggt agatgtcaag aagagacgtt gggttacctt 7920
ctgctctgca gaatggccaa cctttaacgt cggatggccg cgagacggca cctttaaccg 7980
agacctcatc acccaggtta agatcaaggt cttttcacct ggcccgcatg gacacccaga 8040
ccaggtcccc tacatcgtga cctgggaagc cttggctttt gacccccctc cctgggtcaa 8100
gccctttgta caccctaagc ctccgcctcc tcttcctcca tccgccccgt ctctccccct 8160
tgaacctcct cgttcgaccc cgcctcgatc ctccctttat ccagccctca ctccttctct 8220
aggcgccccc atatggccat atgagatctt atatggggca cccccgcccc ttgtaaactt 8280
ccctgaccct gacatgacaa gagttactaa cagcccctct ctccaagctc acttacaggc 8340
tctctactta gtccagcacg aagtctggag acctctggcg gcagcctacc aagaacaact 8400
ggaccgaccg gtggtacctc acccttaccg agtcggcgac acagtgtggg tccgccgaca 8460
ccagactaag aacctagaac ctcgctggaa aggaccttac acagtcctgc tgaccacccc 8520
caccgccctc aaagtagacg gcatcgcagc ttggatacac gccgcccacg tgaaggctgc 8580
cgaccccggg ggtggaccat cctctagact gcc 8613
<210> 124
<211> 8604
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 124
atggccctgc cagtaacggc tctgctgctg ccacttgctc tgctcctcca tgcagccagg 60
cctcaggttc agcttcagga gagtggccca ggcctggtga agccaagtga gactctcagc 120
ttgacttgca cagtttctgg aggcagtgtc tcctcaggca gctattattg gtcctggatt 180
cggcagcccc ctgggaaagg cctggagtgg attgggtaca tatattacag tggcagcaca 240
aattacaatc catccctgaa gtctcgagta actatcagtg tggacacaag caagaatcag 300
ttttcactca aactgtcttc tgtgactgct gctgacactg ctgtttatta ttgtgccagg 360
gaggggaaaa atggggcatt tgatatttgg ggtcagggca caatggtgac agtcagctct 420
ggaggtggag gctcaggagg aggaggcagt ggaggtggtg ggtcacgcca tcagatgact 480
cagtccccct ccagtctttc tgcctcagtt ggggatagag tgaccatcac atgcagagca 540
agtcagagca tatcatccta tctgaactgg taccagcaga agccagggaa agcccccaaa 600
ttgctgattt atgcagcctc aagtctccag agtggggtgc caagcaggtt ctcaggcagt 660
ggcagtggga cagatttcac attgacaatc agctccctcc aacctgaaga ttttgccacc 720
tactattgcc agcaatccta cagcacgccc ctgacttttg gaggtggcac aaaggtagag 780
atcaagagga ctgcggccgc aattgaagtt atgtatcctc ctccttacct agacaatgag 840
aagagcaatg gaaccattat ccatgtgaaa gggaaacacc tttgtccaag tcccctattt 900
cccggacctt ctaagccctt ttgggtgctg gtggtggttg gtggagtcct ggcttgctat 960
agcttgctag taacagtggc ctttattatt ttctgggtga ggagtaagag gagcaggctc 1020
ctgcacagtg actacatgaa catgactccc cgccgccccg ggcccacccg caagcattac 1080
cagccctatg ccccaccacg cgacttcgca gcctatcgct ccagagtgaa gttcagcagg 1140
agcgcagacg cccccgcgta ccagcagggc cagaaccagc tctataacga gctcaatcta 1200
ggacgaagag aggagtacga tgttttggac aagagacgtg gccgggaccc tgagatgggg 1260
ggaaagccga gaaggaagaa ccctcaggaa ggcctgttca atgaactgca gaaagataag 1320
atggcggagg ccttcagtga gattgggatg aaaggcgagc gccggagggg caaggggcac 1380
gatggccttt tccaggggct cagtacagcc accaaggaca ccttcgacgc ccttcacatg 1440
caggccctgc cccctcgcgg atctggagca acaaacttct cactactcaa acaagcaggt 1500
gacgtggagg agaatcccgg cccaatgcag atcccacagg cgccctggcc agtcgtctgg 1560
gcggtgctac aactgggctg gcggccagga tggttcttag actccccaga caggccctgg 1620
aaccccccca ccttctcccc agccctgctc gtggtgaccg aaggggacaa cgccaccttc 1680
acctgcagct tctccaacac atcggagagc ttcgtgctaa actggtaccg catgagcccc 1740
agcaaccaga cggacaagct ggccgctttc cccgaggacc gcagccagcc cggccaggac 1800
tgccgcttcc gtgtcacaca actgcccaac gggcgtgact tccacatgag cgtggtcagg 1860
gcccggcgca atgacagcgg cacctacctc tgtggggcca tctccctggc ccccaaggcg 1920
cagatcaaag agagcctgcg ggcagagctc agggtgacag agagaagggc agaagtgccc 1980
acagcccacc ccagcccctc acccaggcca gccggccagg cggccgcacc caccacgacg 2040
ccagcgccgc gaccaccaac cccggcgccc acgatcgcgt cgcagcccct gtccctgcgc 2100
ccagaggcgt gccggccagc ggcggggggc gcagtgcaca cgagggggct ggacttcgcc 2160
tgtgatatct acatctgggc gcccctggcc gggacttgtg gggtccttct cctgtcactg 2220
gttatcaccc tttactgcaa ccacaggcgg atccaataac agccactcga ggatccggat 2280
tagtccaatt tgttaaagac aggatatcag tggtccaggc tctagttttg actcaacaat 2340
atcaccagct gaagcctata gagtacgagc catagataaa ataaaagatt ttatttagtc 2400
tccagaaaaa ggggggaatg aaagacccca cctgtaggtt tggcaagcta gcttaagtaa 2460
cgccattttg caaggcatgg aaaaatacat aactgagaat agagaagttc agatcaaggt 2520
caggaacaga tggaacagct gaatatgggc caaacaggat atctgtggta agcagttcct 2580
gccccggctc agggccaaga acagatggaa cagctgaata tgggccaaac aggatatctg 2640
tggtaagcag ttcctgcccc ggctcagggc caagaacaga tggtccccag atgcggtcca 2700
gccctcagca gtttctagag aaccatcaga tgtttccagg gtgccccaag gacctgaaat 2760
gaccctgtgc cttatttgaa ctaaccaatc agttcgcttc tcgcttctgt tcgcgcgctt 2820
ctgctccccg agctcaataa aagagcccac aacccctcac tcggggcgcc agtcctccga 2880
ttgactgagt cgcccgggta cccgtgtatc caataaaccc tcttgcagtt gcatccgact 2940
tgtggtctcg ctgttccttg ggagggtctc ctctgagtga ttgactaccc gtcagcgggg 3000
gtctttcaca tgcagcatgt atcaaaatta atttggtttt ttttcttaag tatttacatt 3060
aaatggccat agtacttaaa gttacattgg cttccttgaa ataaacatgg agtattcaga 3120
atgtgtcata aatatttcta attttaagat agtatctcca ttggctttct actttttctt 3180
ttattttttt ttgtcctctg tcttccattt gttgttgttg ttgtttgttt gtttgtttgt 3240
tggttggttg gttaattttt ttttaaagat cctacactat agttcaagct agactattag 3300
ctactctgta acccagggtg accttgaagt catgggtagc ctgctgtttt agccttccca 3360
catctaagat tacaggtatg agctatcatt tttggtatat tgattgattg attgattgat 3420
gtgtgtgtgt gtgattgtgt ttgtgtgtgt gattgtgtat atgtgtgtat ggttgtgtgt 3480
gattgtgtgt atgtatgttt gtgtgtgatt gtgtgtgtgt gattgtgcat gtgtgtgtgt 3540
gtgattgtgt ttatgtgtat gattgtgtgt gtgtgtgtgt gtgtgtgtgt gtgtgtgtgt 3600
gtgtgtgtgt tgtgtatata tatttatggt agtgagaggc aacgctccgg ctcaggtgtc 3660
aggttggttt ttgagacaga gtctttcact tagcttggaa ttcactggcc gtcgttttac 3720
aacgtcgtga ctgggaaaac cctggcgtta cccaacttaa tcgccttgca gcacatcccc 3780
ctttcgccag ctggcgtaat agcgaagagg cccgcaccga tcgcccttcc caacagttgc 3840
gcagcctgaa tggcgaatgg cgcctgatgc ggtattttct ccttacgcat ctgtgcggta 3900
tttcacaccg catatggtgc actctcagta caatctgctc tgatgccgca tagttaagcc 3960
agccccgaca cccgccaaca cccgctgacg cgccctgacg ggcttgtctg ctcccggcat 4020
ccgcttacag acaagctgtg accgtctccg ggagctgcat gtgtcagagg ttttcaccgt 4080
catcaccgaa acgcgcgaga cgaaagggcc tcgtgatacg cctattttta taggttaatg 4140
tcatgataat aatggtttct tagacgtcag gtggcacttt tcggggaaat gtgcgcggaa 4200
cccctatttg tttatttttc taaatacatt caaatatgta tccgctcatg agacaataac 4260
cctgataaat gcttcaataa tattgaaaaa ggaagagtat gagtattcaa catttccgtg 4320
tcgcccttat tccctttttt gcggcatttt gccttcctgt ttttgctcac ccagaaacgc 4380
tggtgaaagt aaaagatgct gaagatcagt tgggtgcacg agtgggttac atcgaactgg 4440
atctcaacag cggtaagatc cttgagagtt ttcgccccga agaacgtttt ccaatgatga 4500
gcacttttaa agttctgcta tgtggcgcgg tattatcccg tattgacgcc gggcaagagc 4560
aactcggtcg ccgcatacac tattctcaga atgacttggt tgagtactca ccagtcacag 4620
aaaagcatct tacggatggc atgacagtaa gagaattatg cagtgctgcc ataaccatga 4680
gtgataacac tgcggccaac ttacttctga caacgatcgg aggaccgaag gagctaaccg 4740
cttttttgca caacatgggg gatcatgtaa ctcgccttga tcgttgggaa ccggagctga 4800
atgaagccat accaaacgac gagcgtgaca ccacgatgcc tgtagcaatg gcaacaacgt 4860
tgcgcaaact attaactggc gaactactta ctctagcttc ccggcaacaa ttaatagact 4920
ggatggaggc ggataaagtt gcaggaccac ttctgcgctc ggcccttccg gctggctggt 4980
ttattgctga taaatctgga gccggtgagc gtgggtctcg cggtatcatt gcagcactgg 5040
ggccagatgg taagccctcc cgtatcgtag ttatctacac gacggggagt caggcaacta 5100
tggatgaacg aaatagacag atcgctgaga taggtgcctc actgattaag cattggtaac 5160
tgtcagacca agtttactca tatatacttt agattgattt aaaacttcat ttttaattta 5220
aaaggatcta ggtgaagatc ctttttgata atctcatgac caaaatccct taacgtgagt 5280
tttcgttcca ctgagcgtca gaccccgtag aaaagatcaa aggatcttct tgagatcctt 5340
tttttctgcg cgtaatctgc tgcttgcaaa caaaaaaacc accgctacca gcggtggttt 5400
gtttgccgga tcaagagcta ccaactcttt ttccgaaggt aactggcttc agcagagcgc 5460
agataccaaa tactgttctt ctagtgtagc cgtagttagg ccaccacttc aagaactctg 5520
tagcaccgcc tacatacctc gctctgctaa tcctgttacc agtggctgct gccagtggcg 5580
ataagtcgtg tcttaccggg ttggactcaa gacgatagtt accggataag gcgcagcggt 5640
cgggctgaac ggggggttcg tgcacacagc ccagcttgga gcgaacgacc tacaccgaac 5700
tgagatacct acagcgtgag ctatgagaaa gcgccacgct tcccgaaggg agaaaggcgg 5760
acaggtatcc ggtaagcggc agggtcggaa caggagagcg cacgagggag cttccagggg 5820
gaaacgcctg gtatctttat agtcctgtcg ggtttcgcca cctctgactt gagcgtcgat 5880
ttttgtgatg ctcgtcaggg gggcggagcc tatggaaaaa cgccagcaac gcggcctttt 5940
tacggttcct ggccttttgc tggccttttg ctcacatgtt ctttcctgcg ttatcccctg 6000
attctgtgga taaccgtatt accgcctttg agtgagctga taccgctcgc cgcagccgaa 6060
cgaccgagcg cagcgagtca gtgagcgagg aagcggaaga gcgcccaata cgcaaaccgc 6120
ctctccccgc gcgttggccg attcattaat gcagctggca cgacaggttt cccgactgga 6180
aagcgggcag tgagcgcaac gcaattaatg tgagttagct cactcattag gcaccccagg 6240
ctttacactt tatgcttccg gctcgtatgt tgtgtggaat tgtgagcgga taacaatttc 6300
acacaggaaa cagctatgac catgattacg ccaagctttg ctcttaggag tttcctaata 6360
catcccaaac tcaaatatat aaagcatttg acttgttcta tgccctaggg ggcgggggga 6420
agctaagcca gcttttttta acatttaaaa tgttaattcc attttaaatg cacagatgtt 6480
tttatttcat aagggtttca atgtgcatga atgctgcaat attcctgtta ccaaagctag 6540
tataaataaa aatagataaa cgtggaaatt acttagagtt tctgtcatta acgtttcctt 6600
cctcagttga caacataaat gcgctgctga gaagccagtt tgcatctgtc aggatcaatt 6660
tcccattatg ccagtcatat taattactag tcaattagtt gatttttatt tttgacatat 6720
acatgtgaaa gaccccacct gtaggtttgg caagctagct taagtaacgc cattttgcaa 6780
ggcatggaaa aatacataac tgagaataga aaagttcaga tcaaggtcag gaacagatgg 6840
aacagctgaa tatgggccaa acaggatatc tgtggtaagc agttcctgcc ccggctcagg 6900
gccaagaaca gatggaacag ctgaatatgg gccaaacagg atatctgtgg taagcagttc 6960
ctgccccggc tcagggccaa gaacagatgg tccccagatg cggtccagcc ctcagcagtt 7020
tctagagaac catcagatgt ttccagggtg ccccaaggac ctgaaatgac cctgtgcctt 7080
atttgaacta accaatcagt tcgcttctcg cttctgttcg cgcgcttctg ctccccgagc 7140
tcaataaaag agcccacaac ccctcactcg gcgcgccagt cctccgattg actgagtcgc 7200
ccgggtaccc gtgtatccaa taaaccctct tgcagttgca tccgacttgt ggtctcgctg 7260
ttccttggga gggtctcctc tgagtgattg actacccgtc agcgggggtc tttcatttgg 7320
gggctcgtcc gggatcggga gacccctgcc cagggaccac cgacccacca ccgggaggta 7380
agctggccag caacttatct gtgtctgtcc gattgtctag tgtctatgac tgattttatg 7440
cgcctgcgtc ggtactagtt agctaactag ctctgtatct ggcggacccg tggtggaact 7500
gacgagttcg gaacacccgg ccgcaaccct gggagacgtc ccagggactt cgggggccgt 7560
ttttgtggcc cgacctgagt cctaaaatcc cgatcgttta ggactctttg gtgcaccccc 7620
cttagaggag ggatatgtgg ttctggtagg agacgagaac ctaaaacagt tcccgcctcc 7680
gtctgaattt ttgctttcgg tttgggaccg aagccgcgcc gcgcgtcttg tctgctgcag 7740
catcgttctg tgttgtctct gtctgactgt gtttctgtat ttgtctgaaa atatgggccc 7800
gggctagcct gttaccactc ccttaagttt gaccttaggt cactggaaag atgtcgagcg 7860
gatcgctcac aaccagtcgg tagatgtcaa gaagagacgt tgggttacct tctgctctgc 7920
agaatggcca acctttaacg tcggatggcc gcgagacggc acctttaacc gagacctcat 7980
cacccaggtt aagatcaagg tcttttcacc tggcccgcat ggacacccag accaggtccc 8040
ctacatcgtg acctgggaag ccttggcttt tgacccccct ccctgggtca agccctttgt 8100
acaccctaag cctccgcctc ctcttcctcc atccgccccg tctctccccc ttgaacctcc 8160
tcgttcgacc ccgcctcgat cctcccttta tccagccctc actccttctc taggcgcccc 8220
catatggcca tatgagatct tatatggggc acccccgccc cttgtaaact tccctgaccc 8280
tgacatgaca agagttacta acagcccctc tctccaagct cacttacagg ctctctactt 8340
agtccagcac gaagtctgga gacctctggc ggcagcctac caagaacaac tggaccgacc 8400
ggtggtacct cacccttacc gagtcggcga cacagtgtgg gtccgccgac accagactaa 8460
gaacctagaa cctcgctgga aaggacctta cacagtcctg ctgaccaccc ccaccgccct 8520
caaagtagac ggcatcgcag cttggataca cgccgcccac gtgaaggctg ccgaccccgg 8580
gggtggacca tcctctagac tgcc 8604
<210> 125
<211> 63
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 125
atggccctgc cagtaacggc tctgctgctg ccacttgctc tgctcctcca tgcagccagg 60
cct 63
<210> 126
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 126
aggaccttac acagtcctgc tgac 24
<210> 127
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 127
agaacctaga acctcgctgg a 21
<210> 128
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 128
ctgcgatgcc gtctactttg 20
<210> 129
<211> 27
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 129
tgctgaaaca ttcaccttcc atgcaga 27
<210> 130
<211> 25
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 130
tgaaacatac gttcccaaag agttt 25
<210> 131
<211> 26
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 131
ctctccttct cagaaagtgt gcatat 26
<210> 132
<211> 18
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 132
gaaggtgaag gtcggagt 18
<210> 133
<211> 22
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 133
catgggtgga atcatattgg aa 22
<210> 134
<211> 22
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 134
ccaggatggt tcttagactc cc 22
<210> 135
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 135
tttagcacga agctctccga t 21
<210> 136
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 136
acgagggaca ataggagcca 20
<210> 137
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 137
ggcatactcc gtctgctcag 20
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| ВИДЫ КОМБИНИРОВАННОЙ ТЕРАПИИ С ИСПОЛЬЗОВАНИЕМ ХИМЕРНЫХ АНТИГЕННЫХ РЕЦЕПТОРОВ И ИНГИБИТОРОВ PD-1 | 2017 |
|
RU2809160C2 |
| ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ, НАЦЕЛЕННЫЕ НА FLT3 | 2018 |
|
RU2820859C2 |
| СПЕЦИФИЧНЫЕ К MUC16 ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ И ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2795198C2 |
| ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ И СВЯЗЫВАЮЩИЕ АГЕНТЫ, НАЦЕЛЕННЫЕ НА DLL3 | 2020 |
|
RU2822366C2 |
| АНТИТЕЛА К ХИМЕРНЫМ АНТИГЕННЫМ РЕЦЕПТОРАМ, ПОЛУЧЕННЫМ ИЗ 4G7 | 2020 |
|
RU2826051C2 |
| ХИМЕРНЫЙ АНТИГЕННЫЙ РЕЦЕПТОР (CAR) ПРОТИВ CD123 ДЛЯ ИСПОЛЬЗОВАНИЯ В ЛЕЧЕНИИ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ | 2015 |
|
RU2724999C2 |
| Химерные антигенные рецепторы, нацеливающиеся на CD70 | 2019 |
|
RU2801824C2 |
| ЛЕЧЕНИЕ ЗЛОКАЧЕСТВЕННОГО НОВООБРАЗОВАНИЯ С ИСПОЛЬЗОВАНИЕМ ГУМАНИЗИРОВАННОГО ХИМЕРНОГО АНТИГЕННОГО РЕЦЕПТОРА ПРОТИВ ВСМА | 2015 |
|
RU2751660C2 |
| КОМПОЗИЦИИ И СПОСОБЫ СЕЛЕКТИВНОЙ ДЕГРАДАЦИИ БЕЛКА | 2018 |
|
RU2811700C2 |
| ХИМЕРНЫЙ АНТИГЕННЫЙ РЕЦЕПТОР | 2018 |
|
RU2770002C2 |
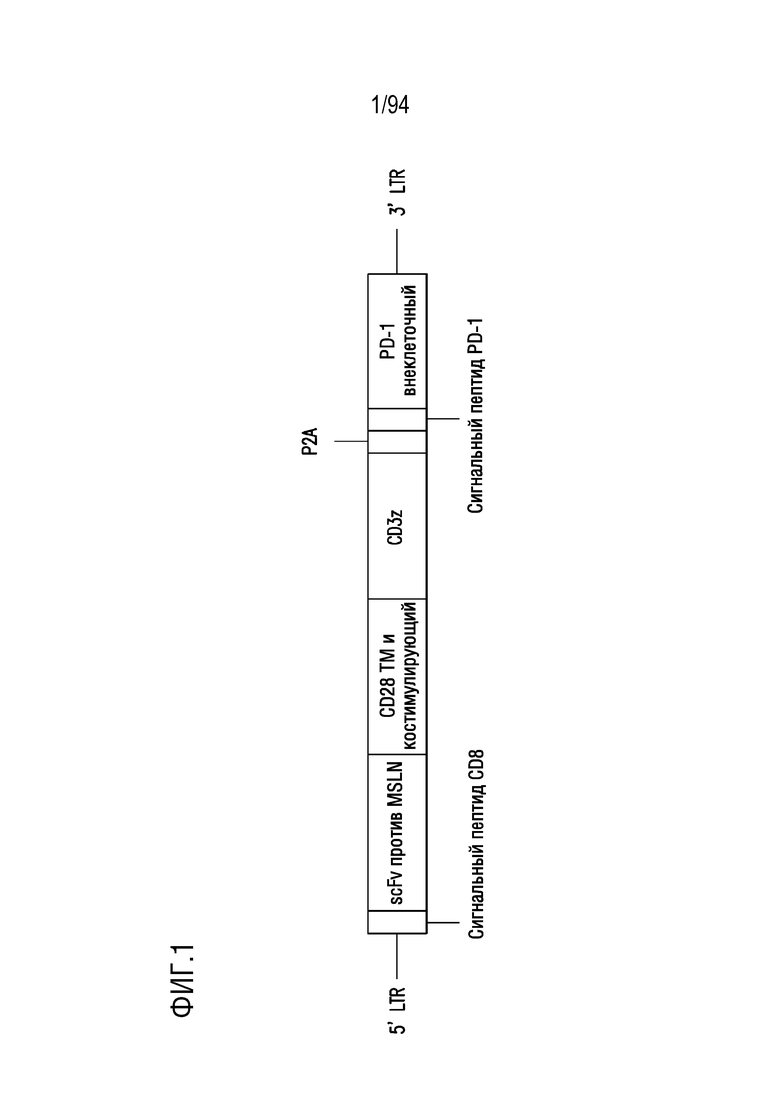
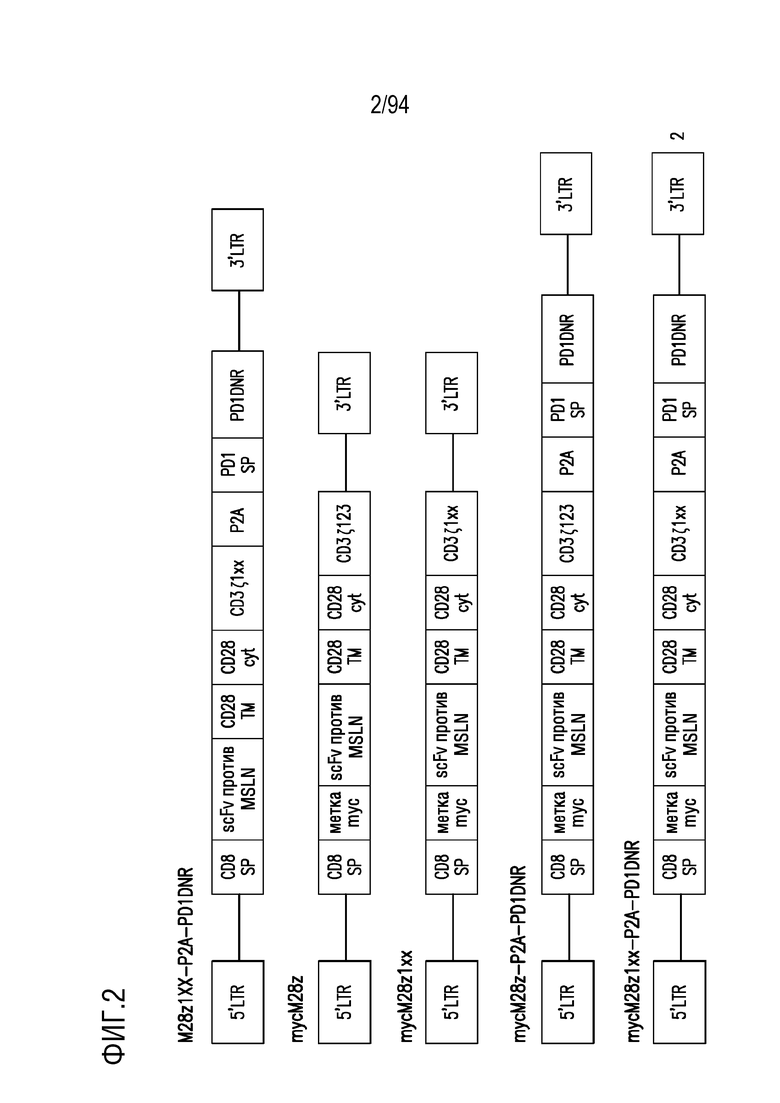
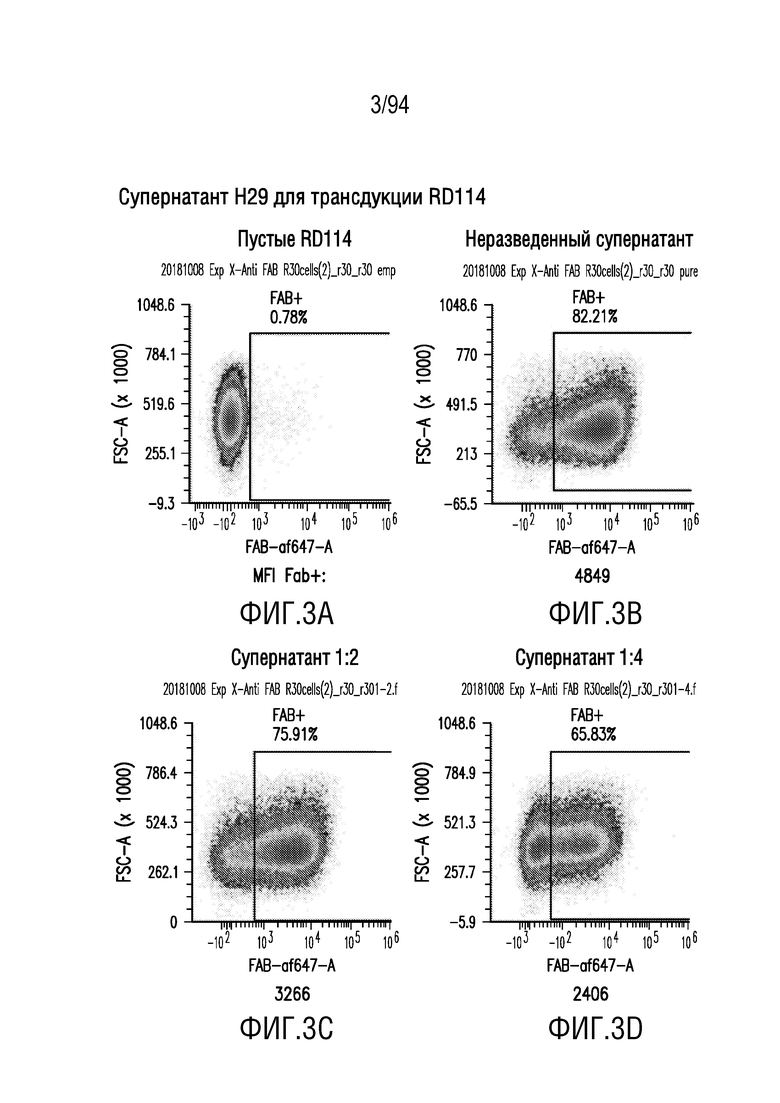
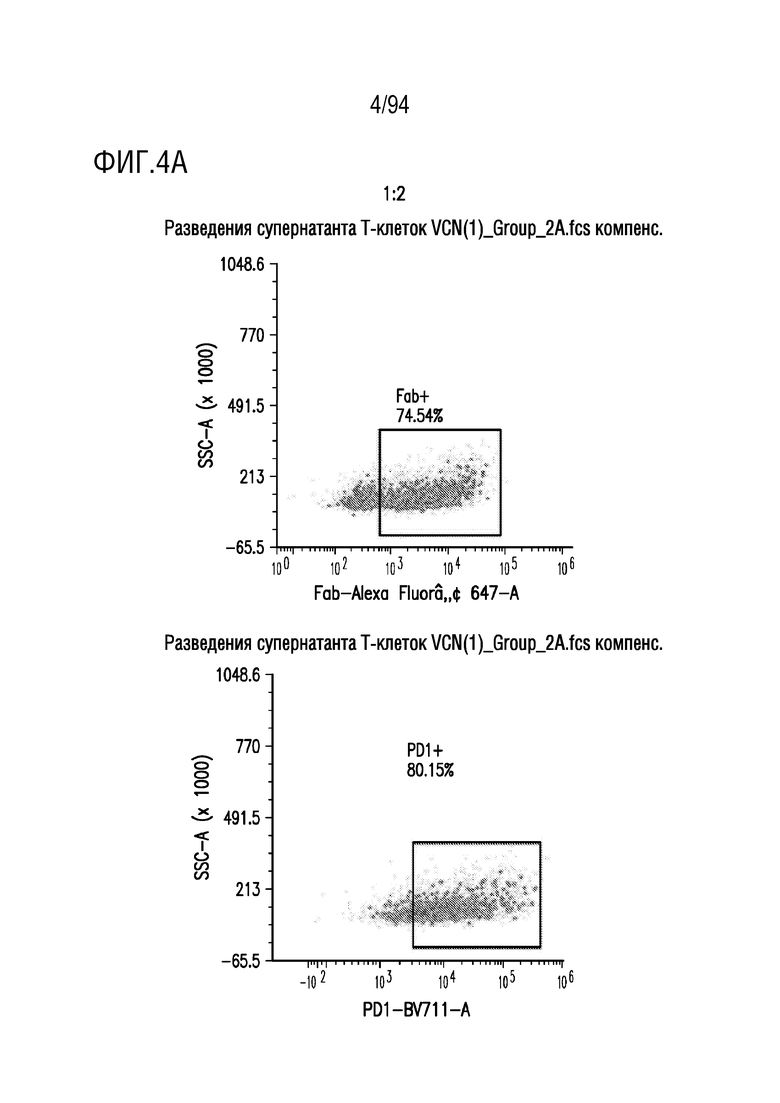
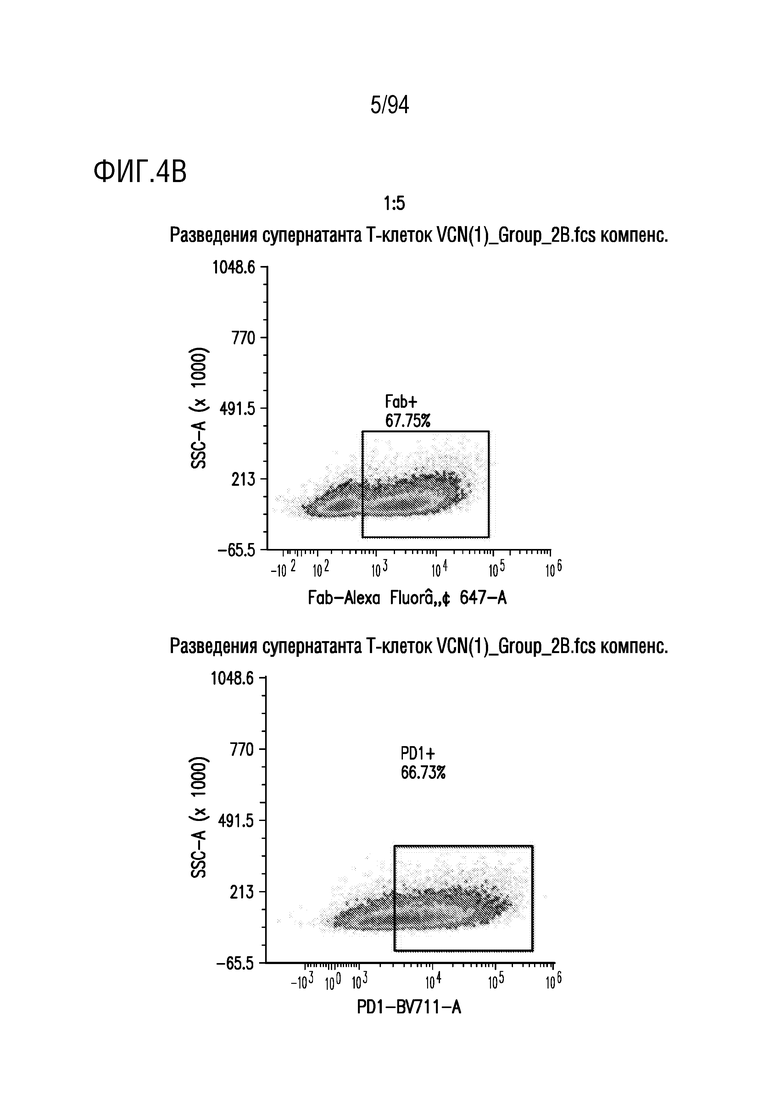
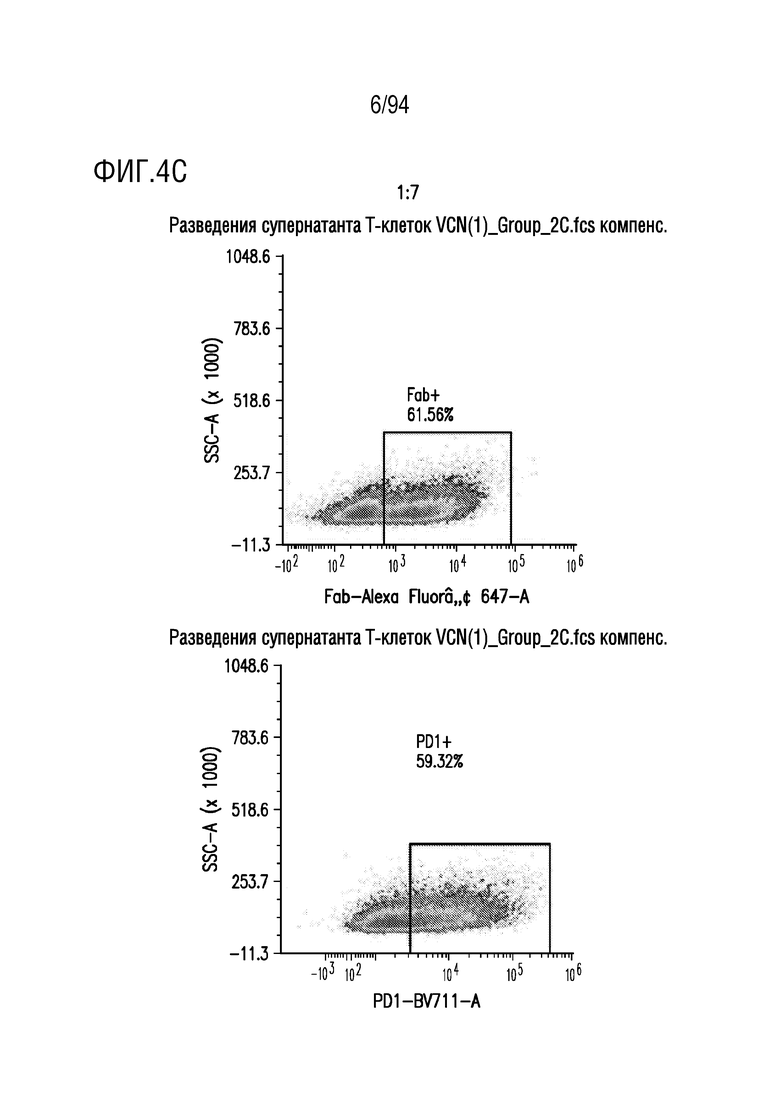
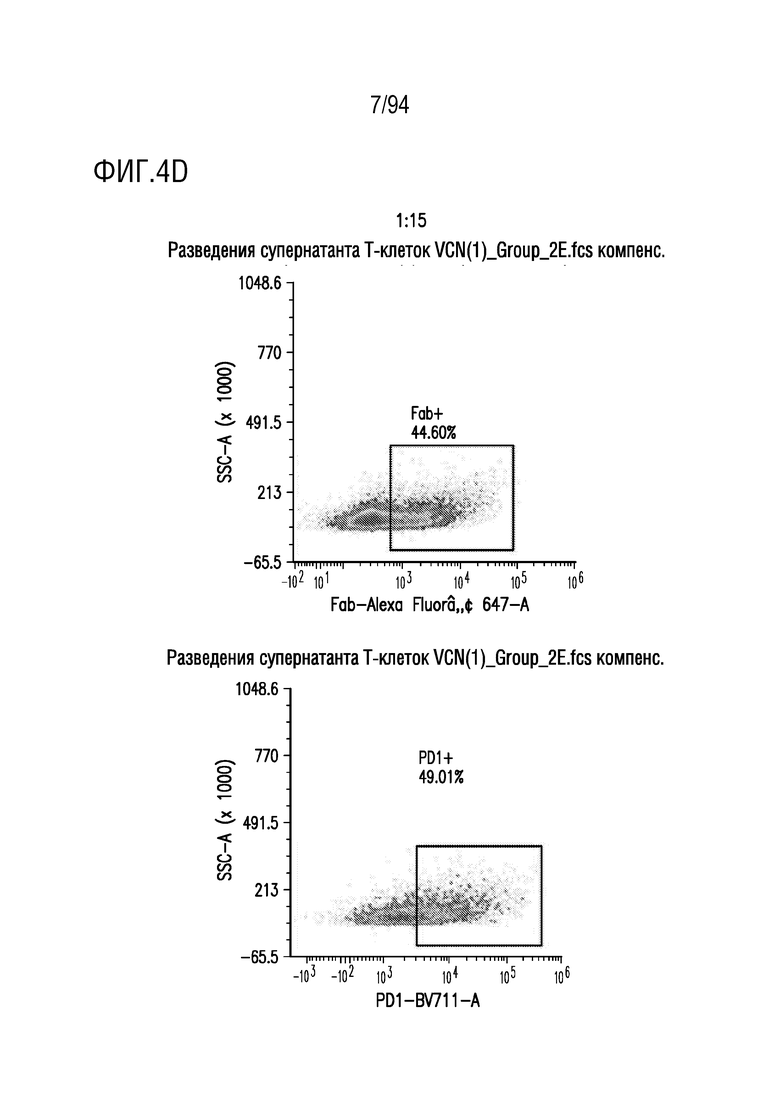
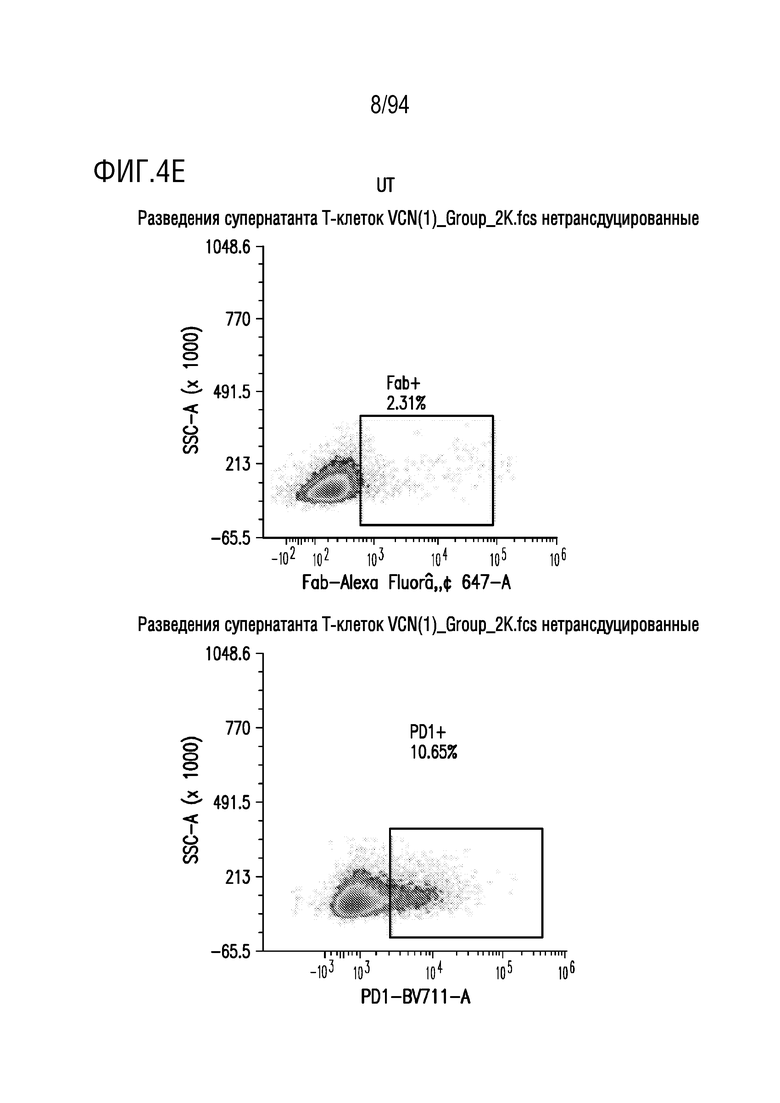
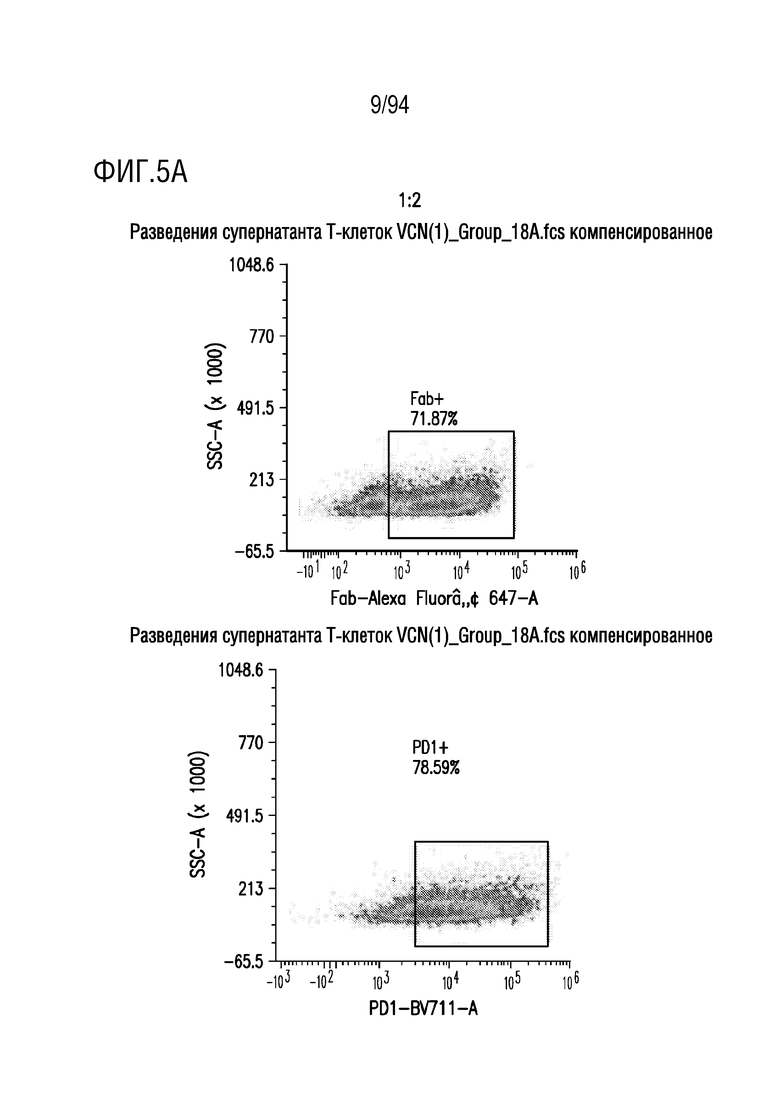
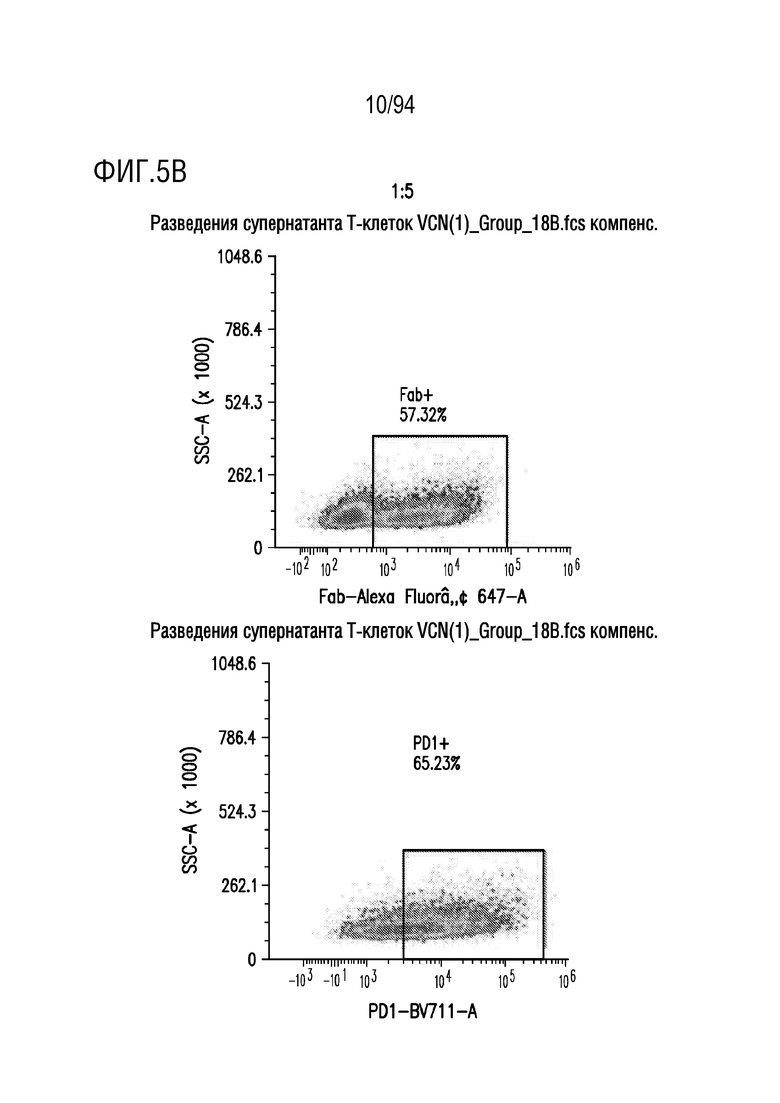
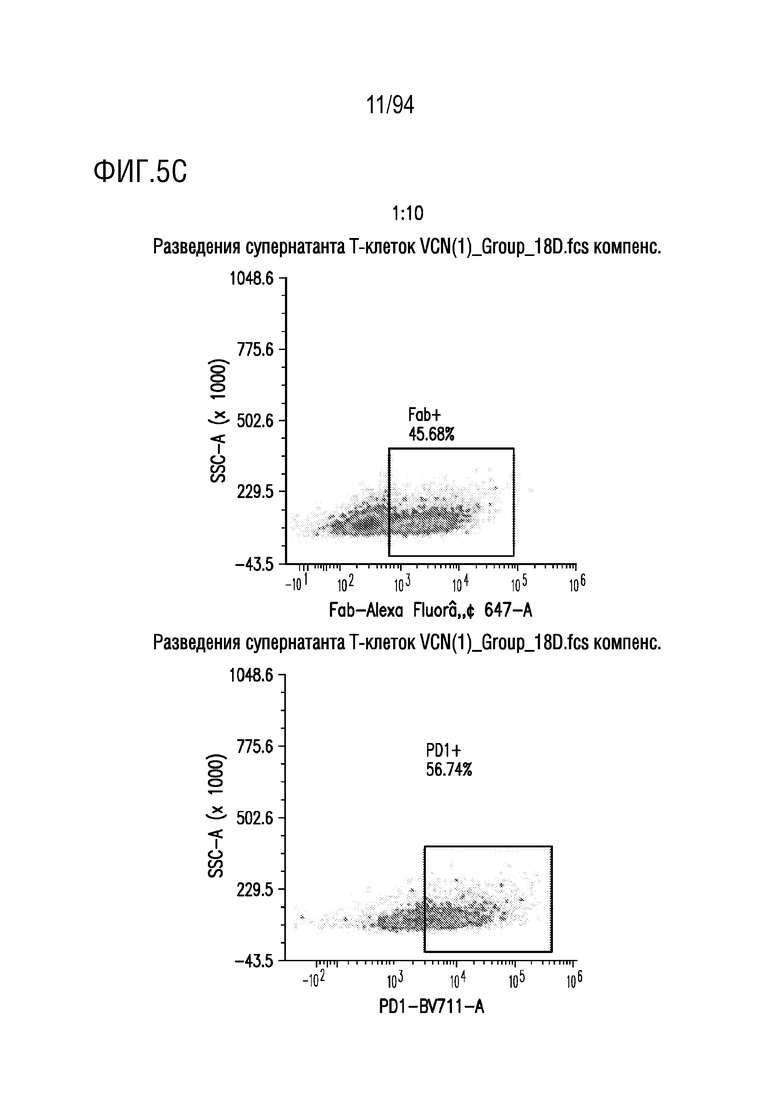
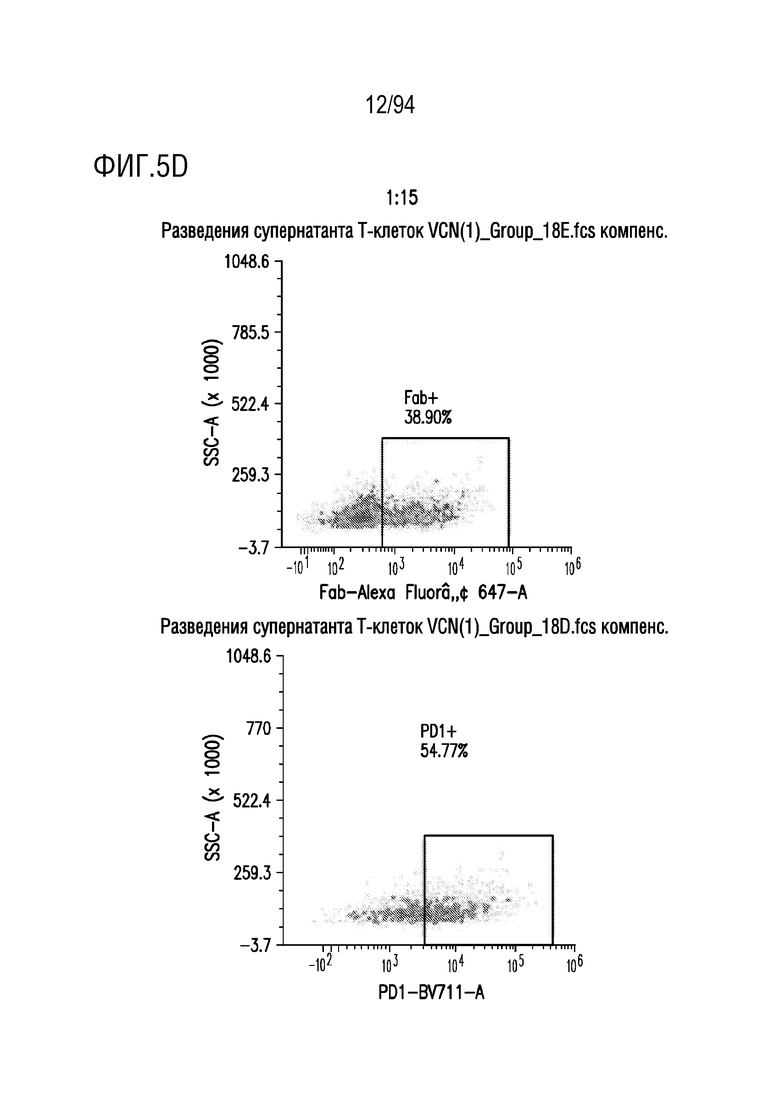
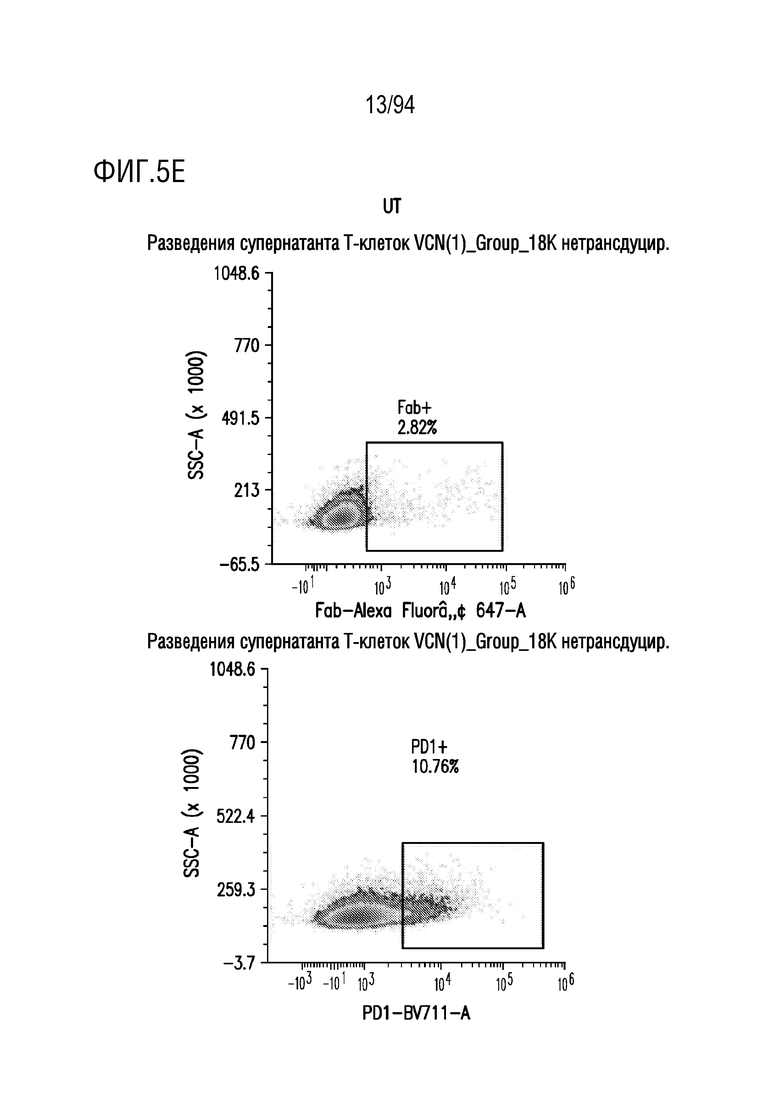
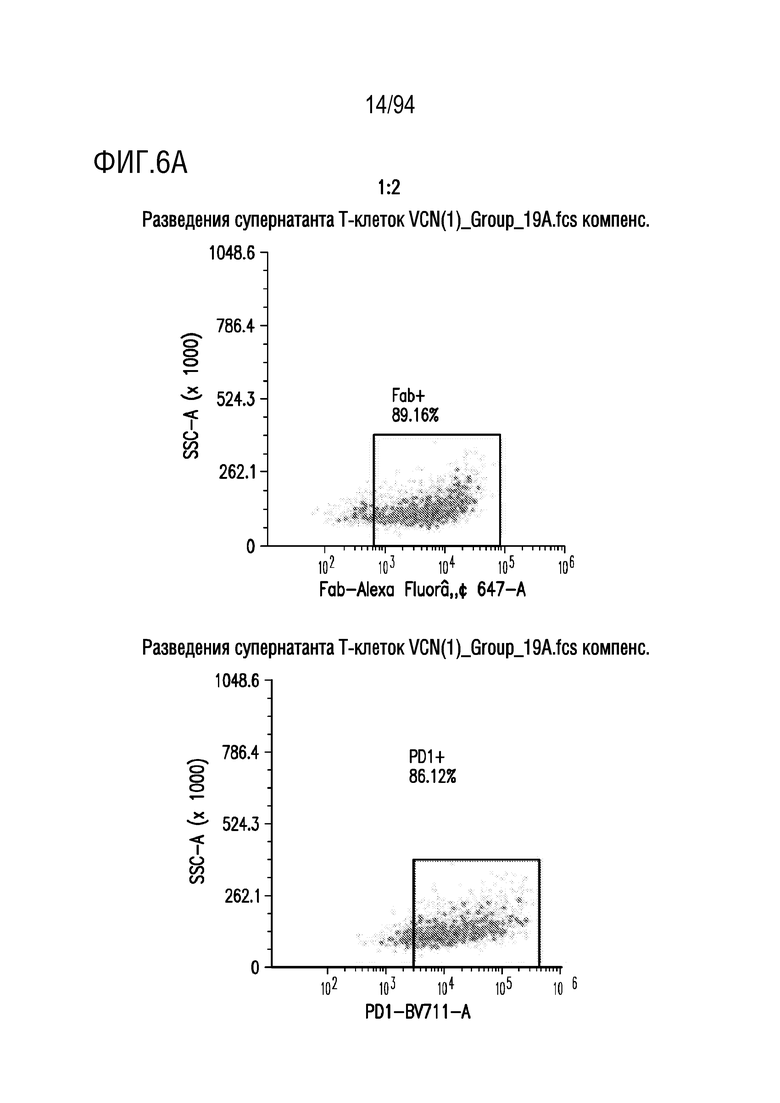
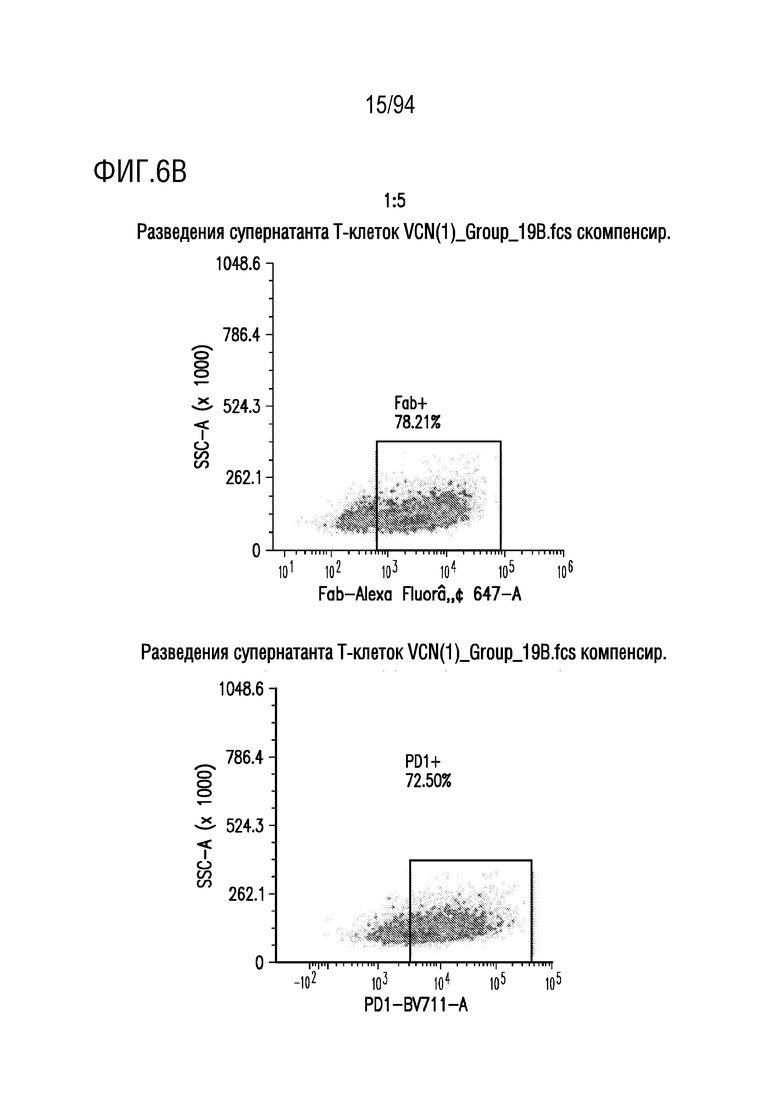
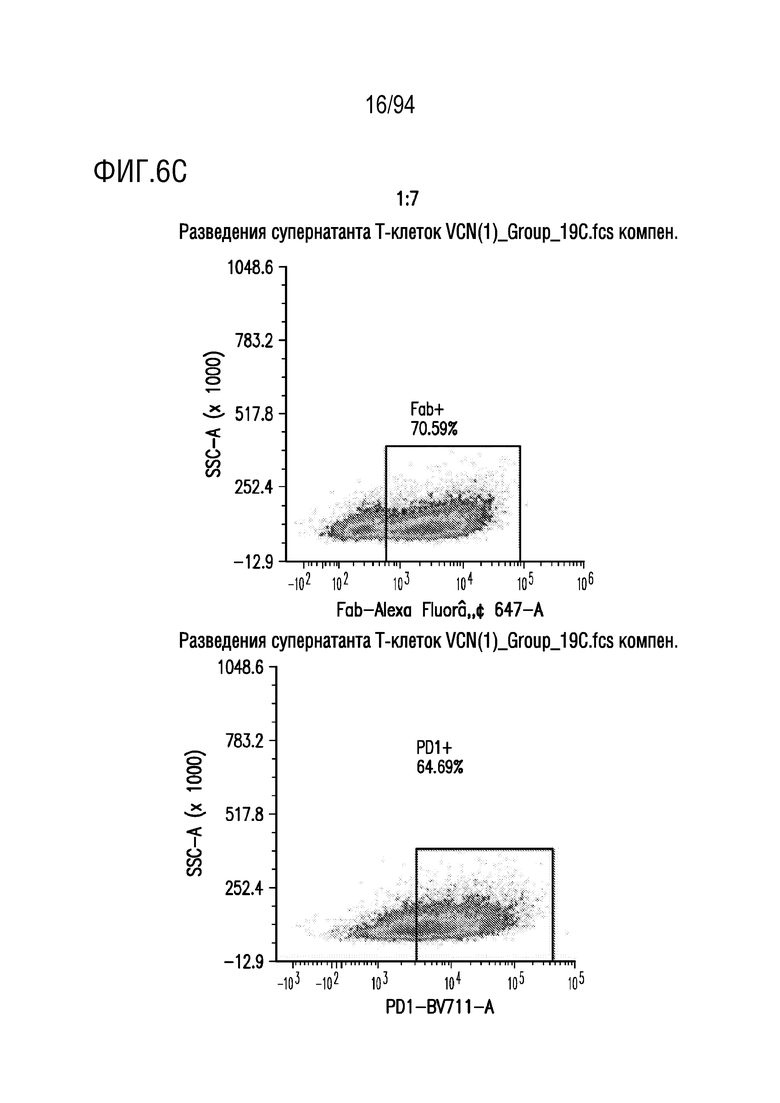
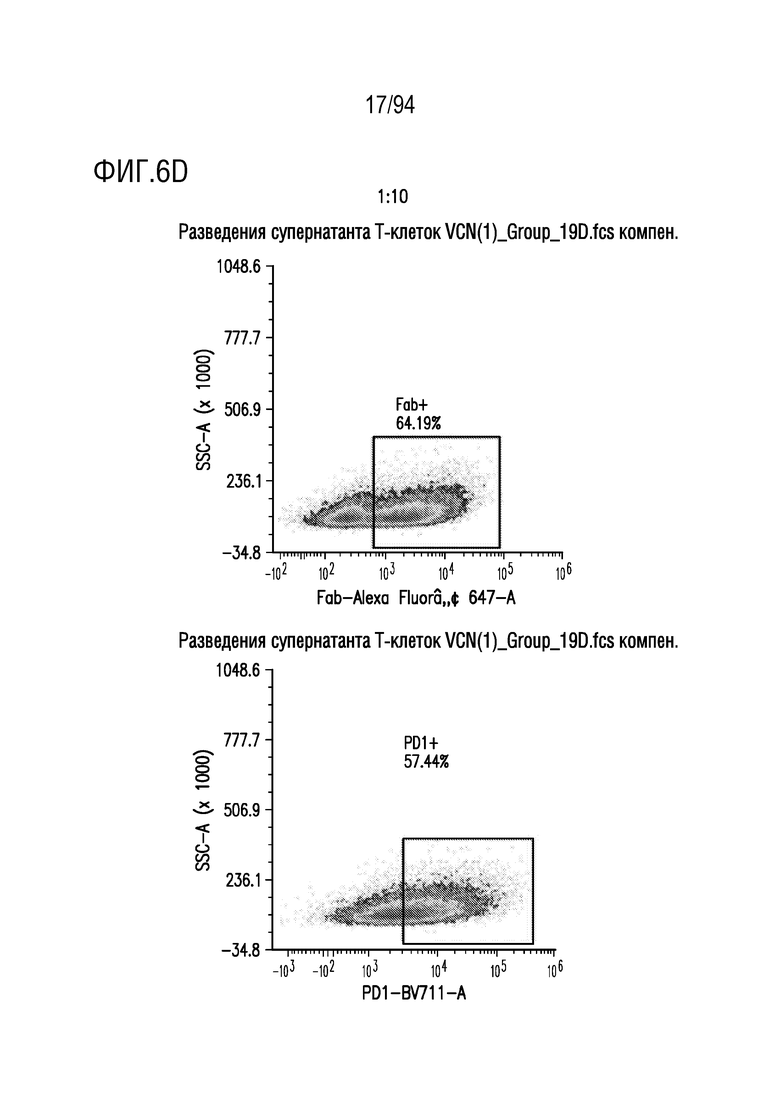
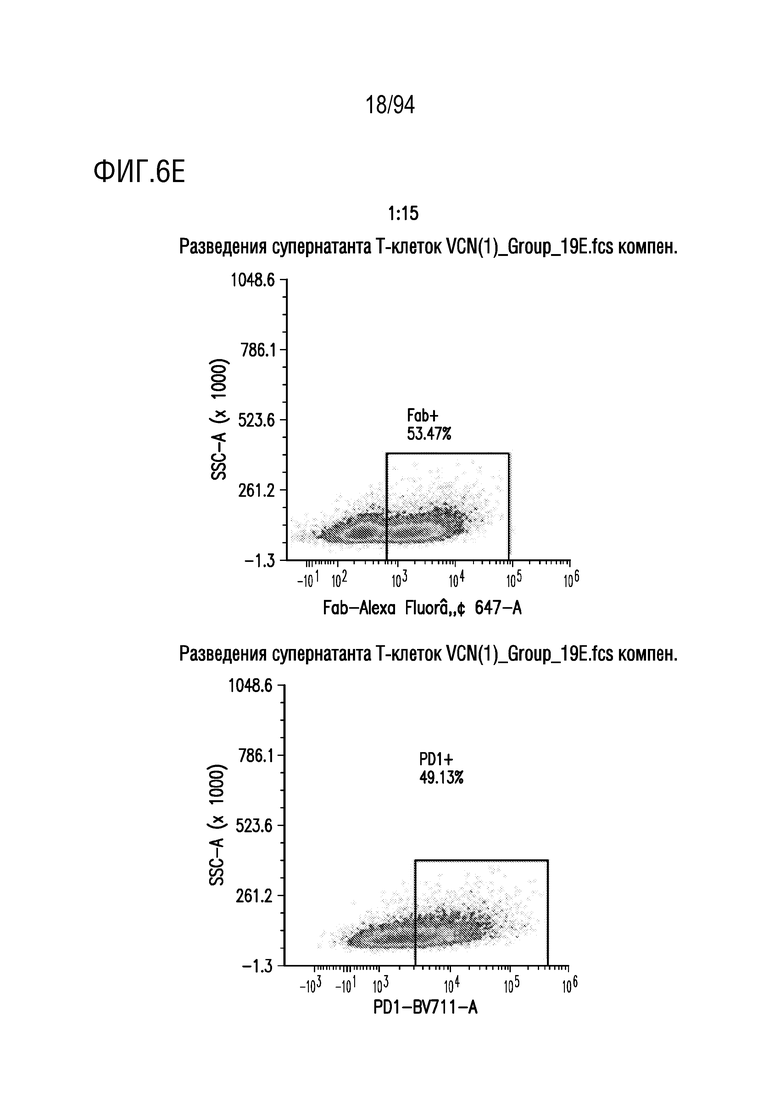
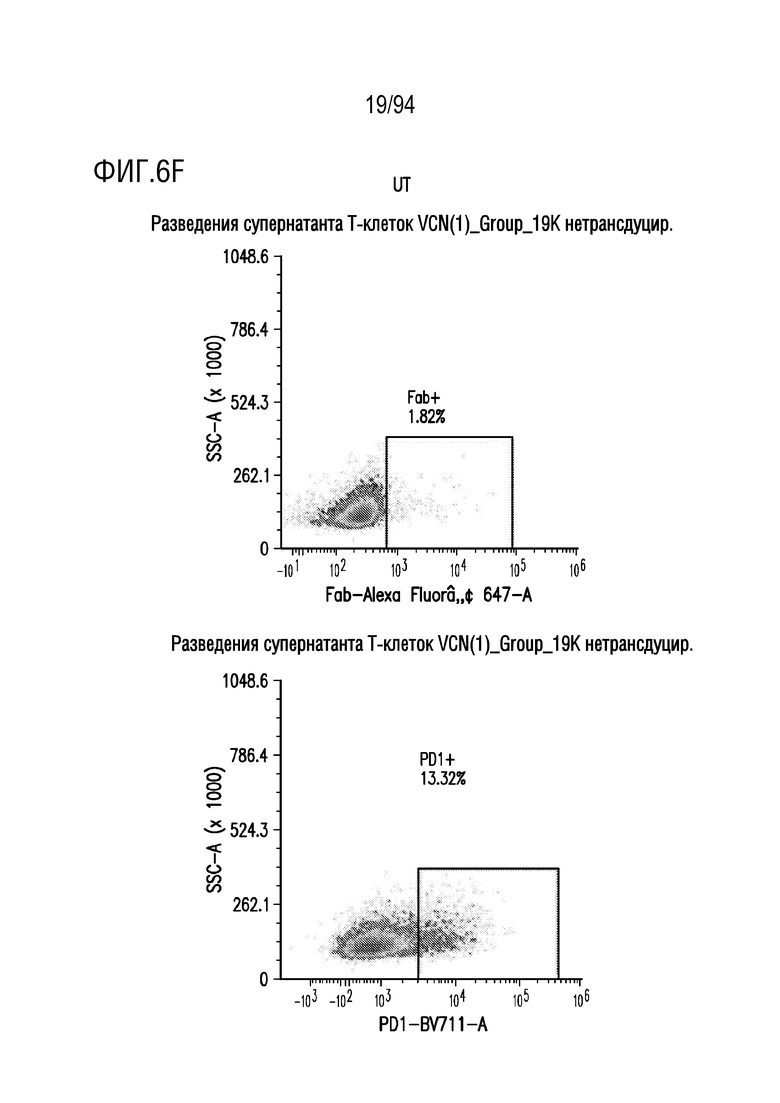
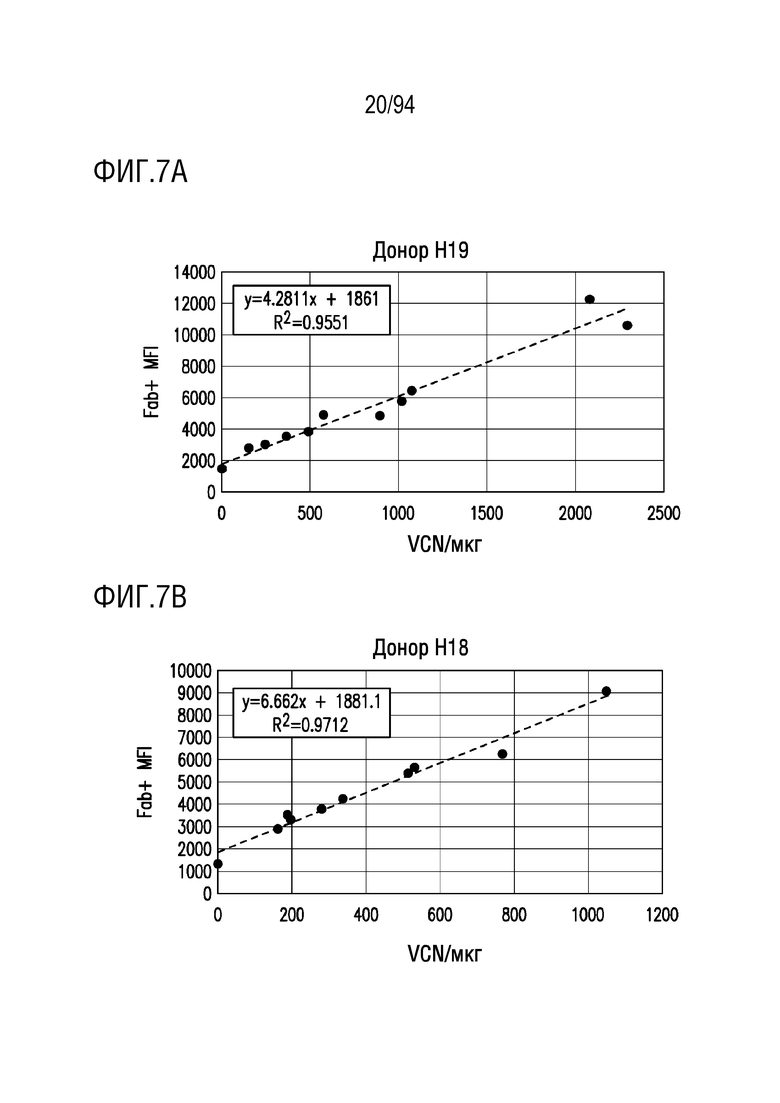
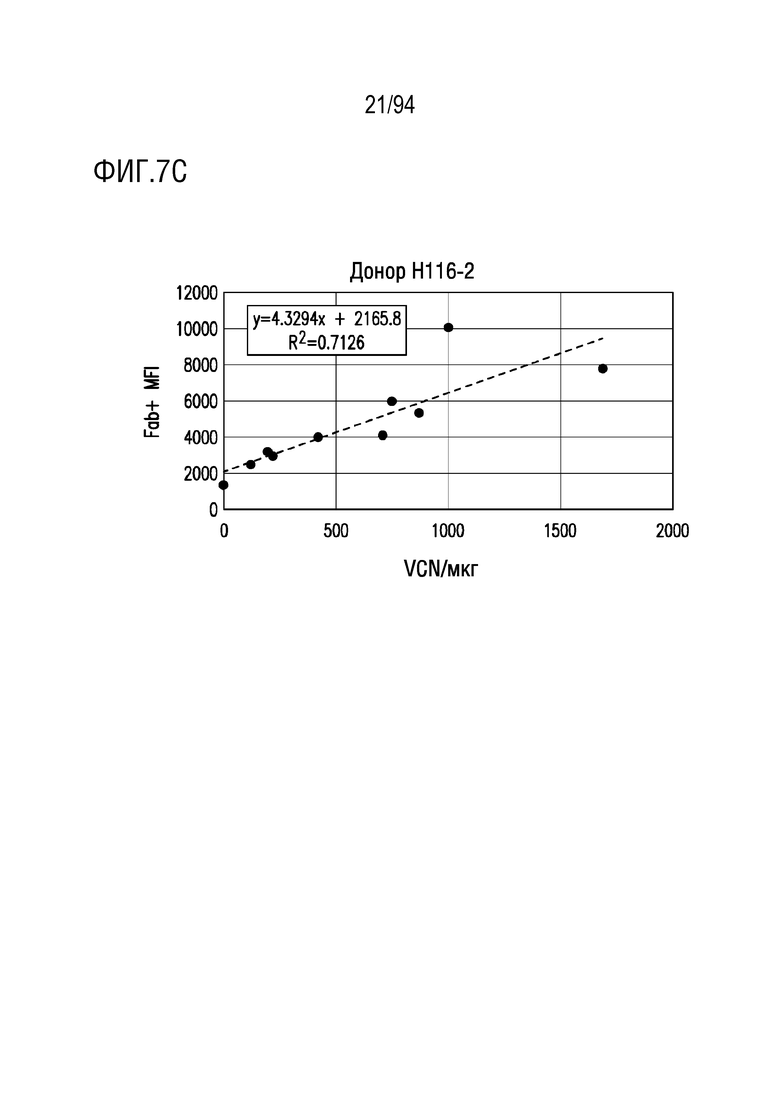
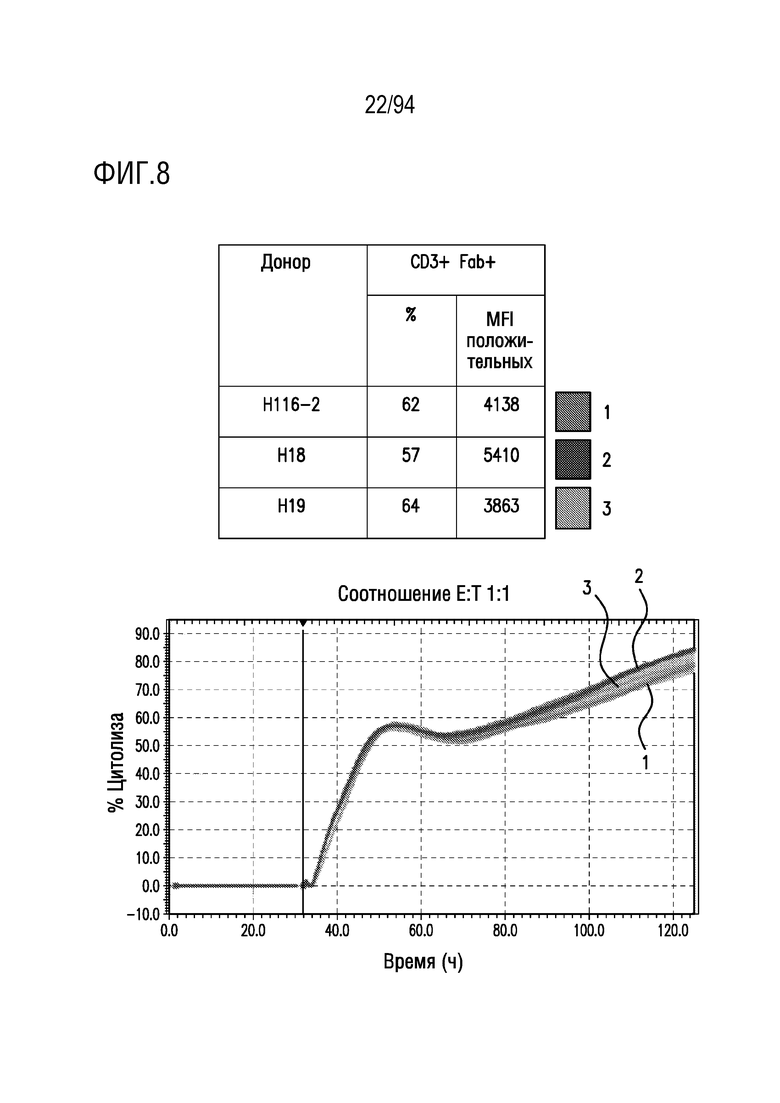
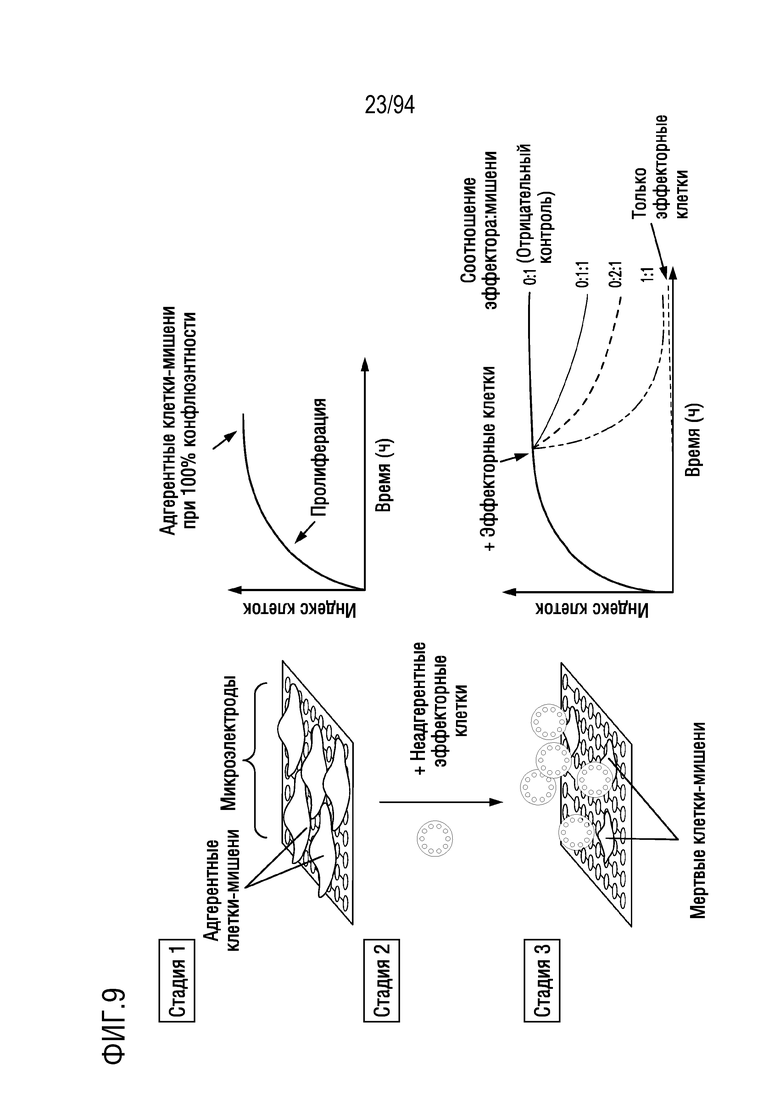

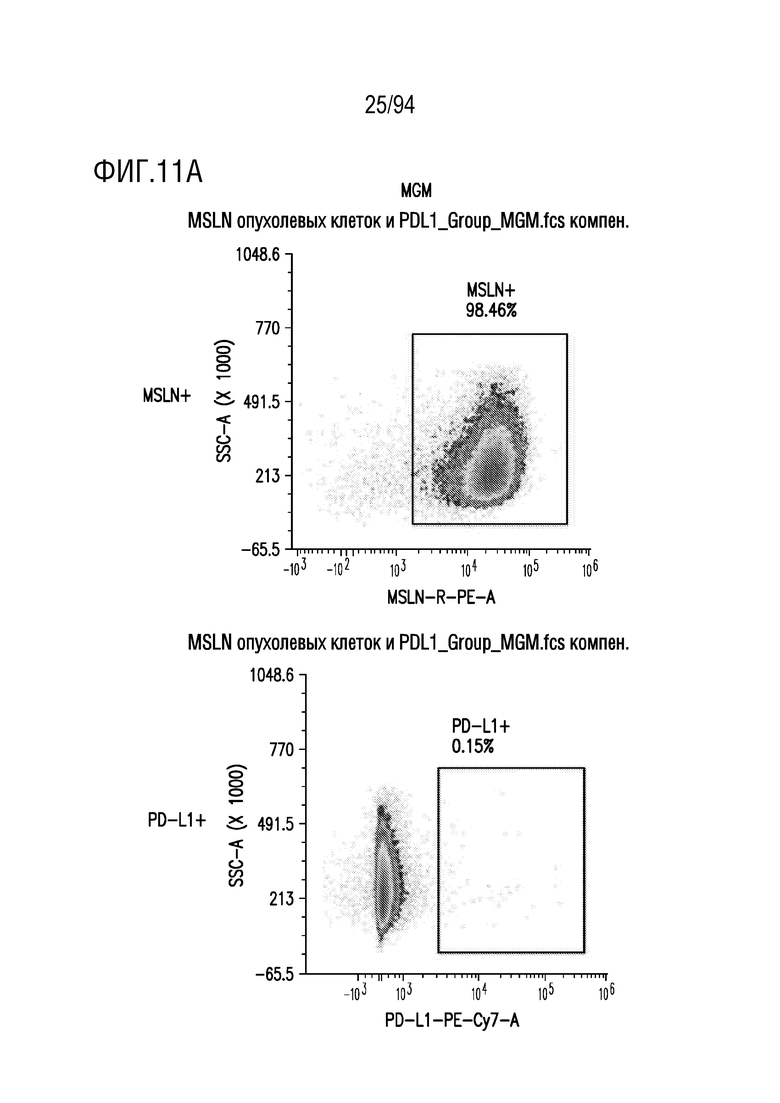
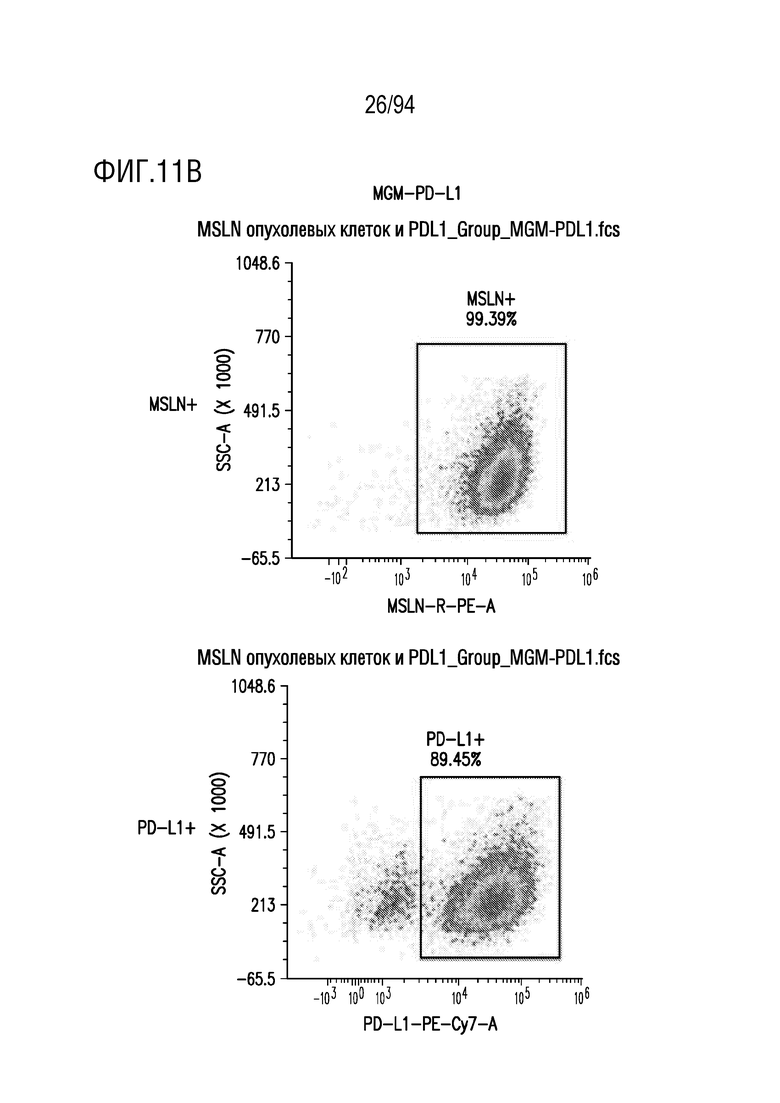
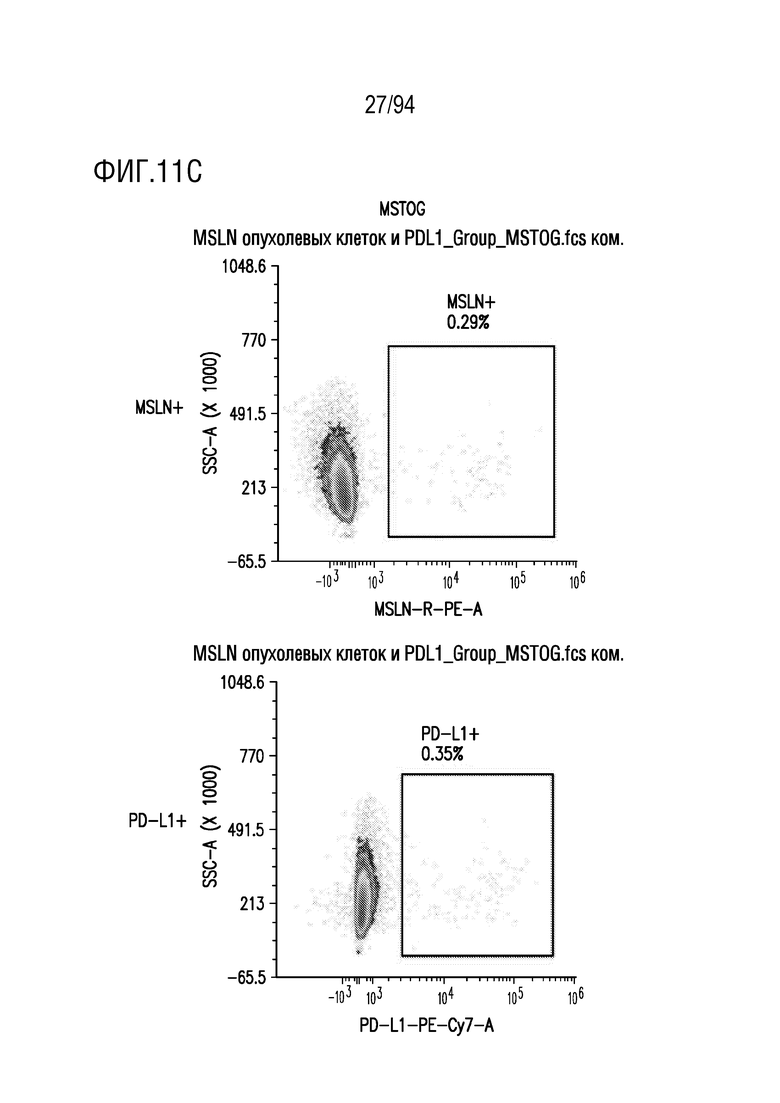
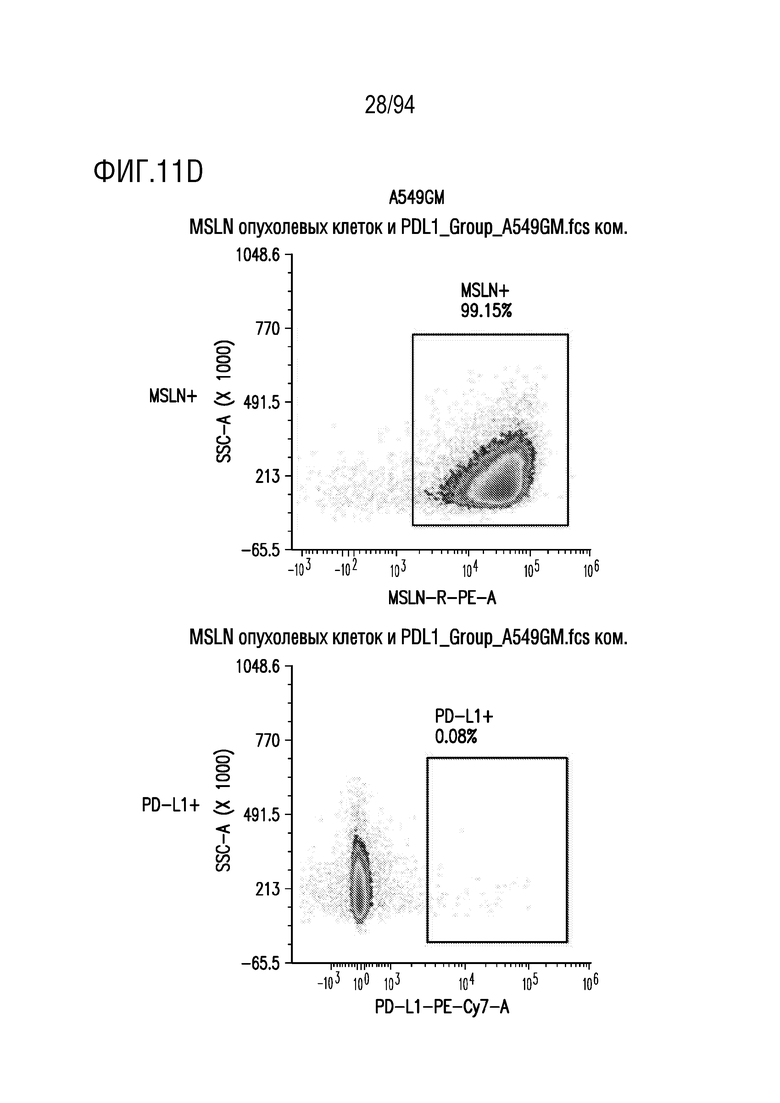
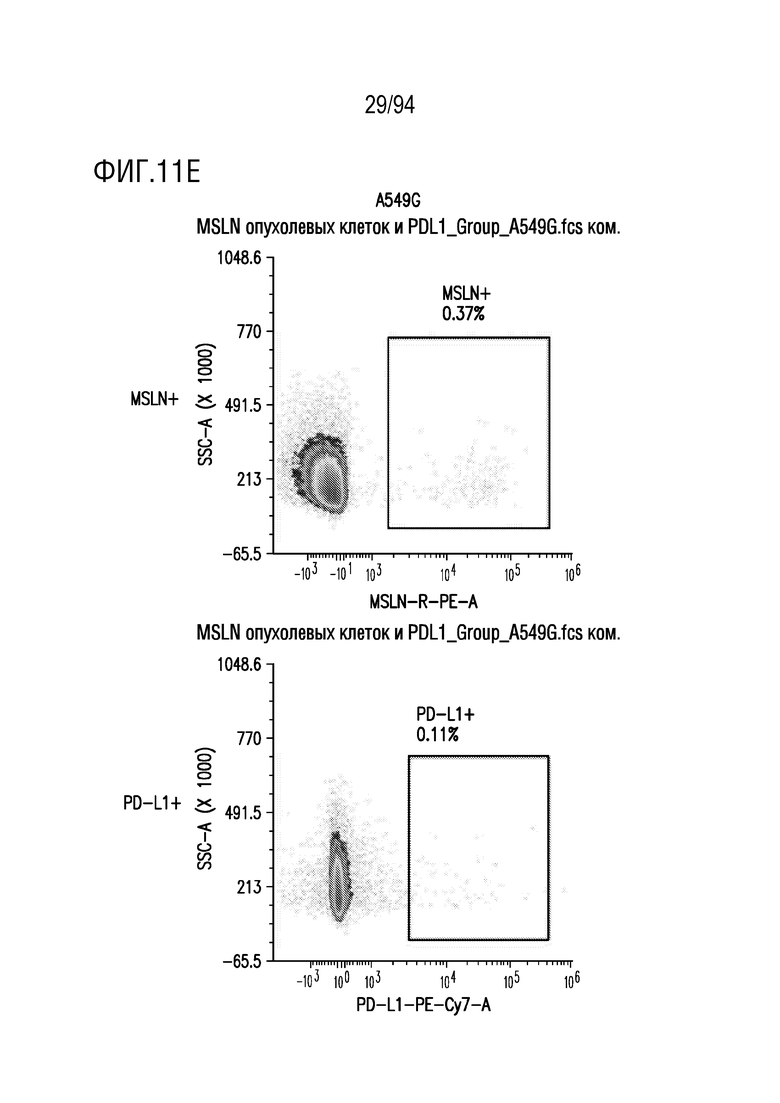
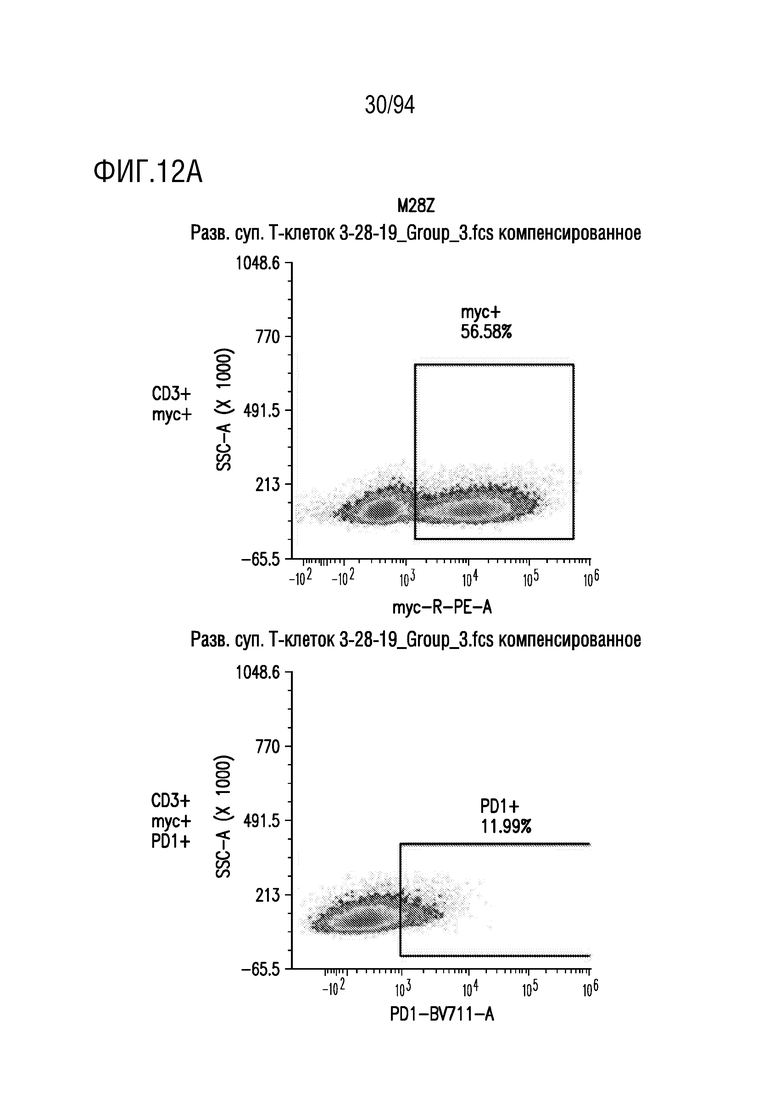
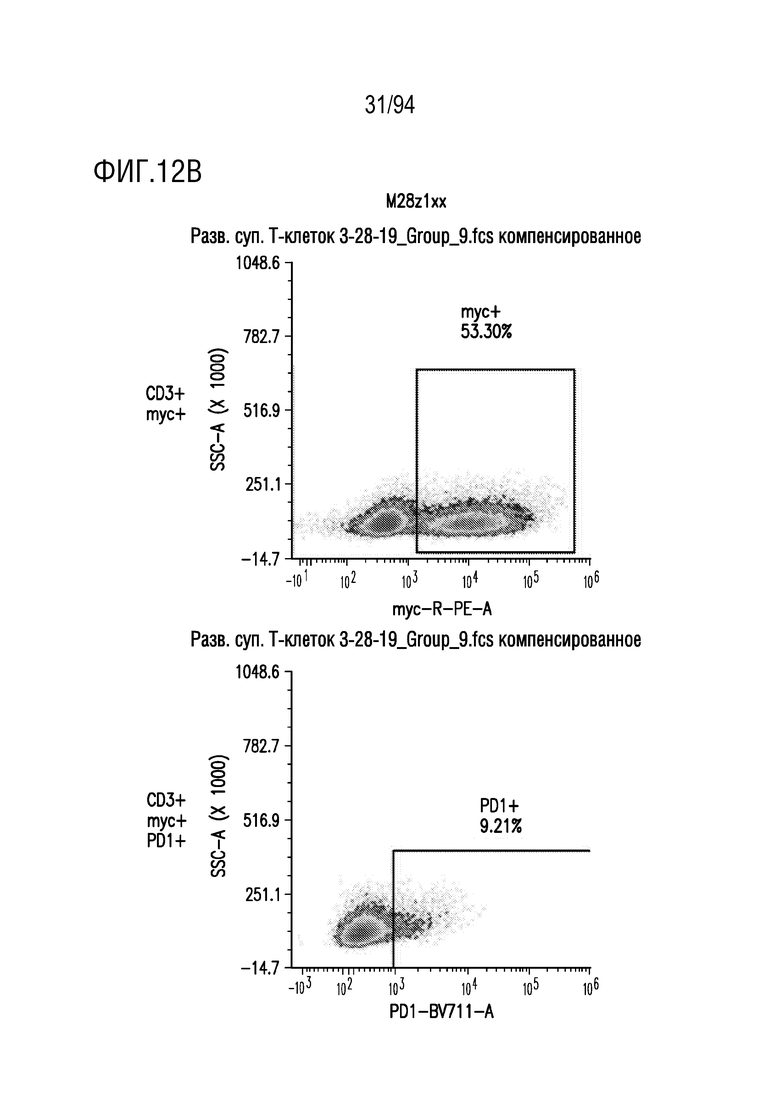
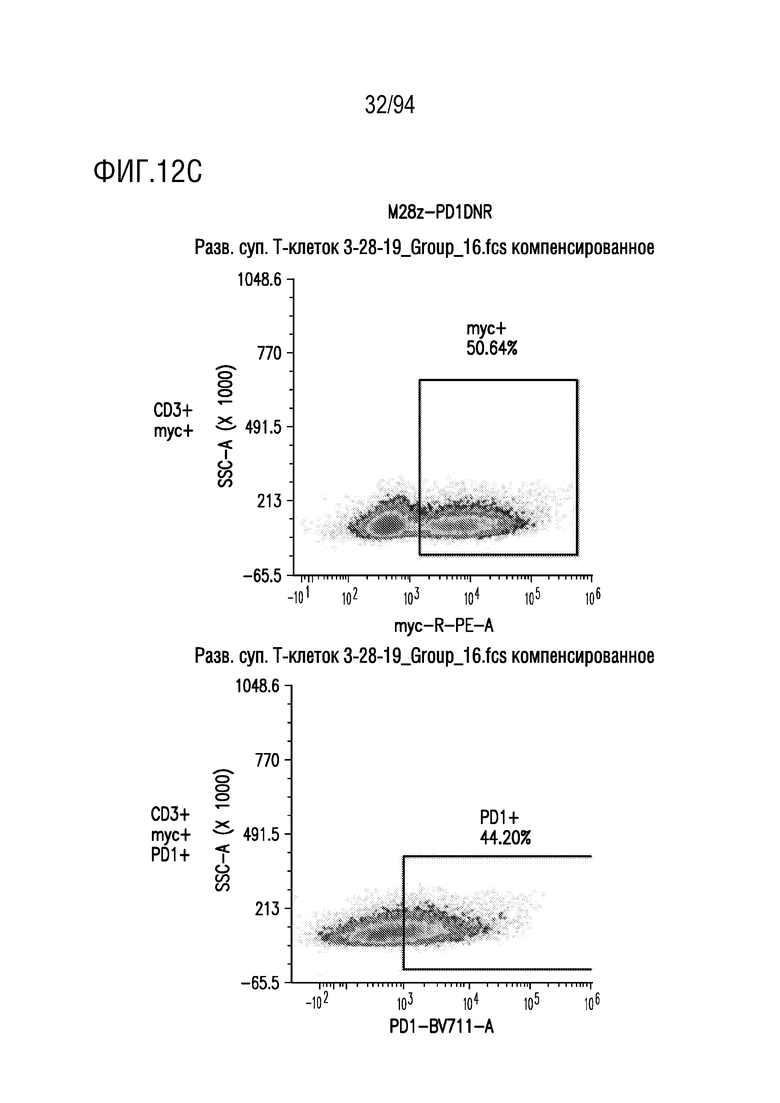
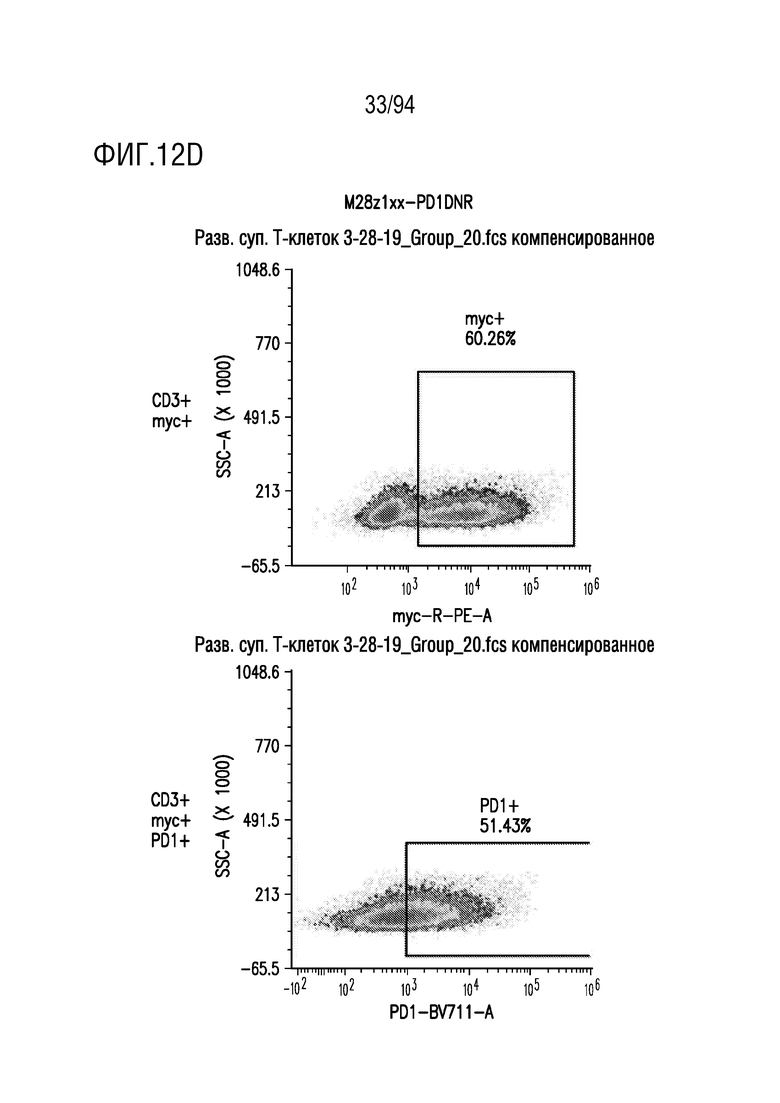
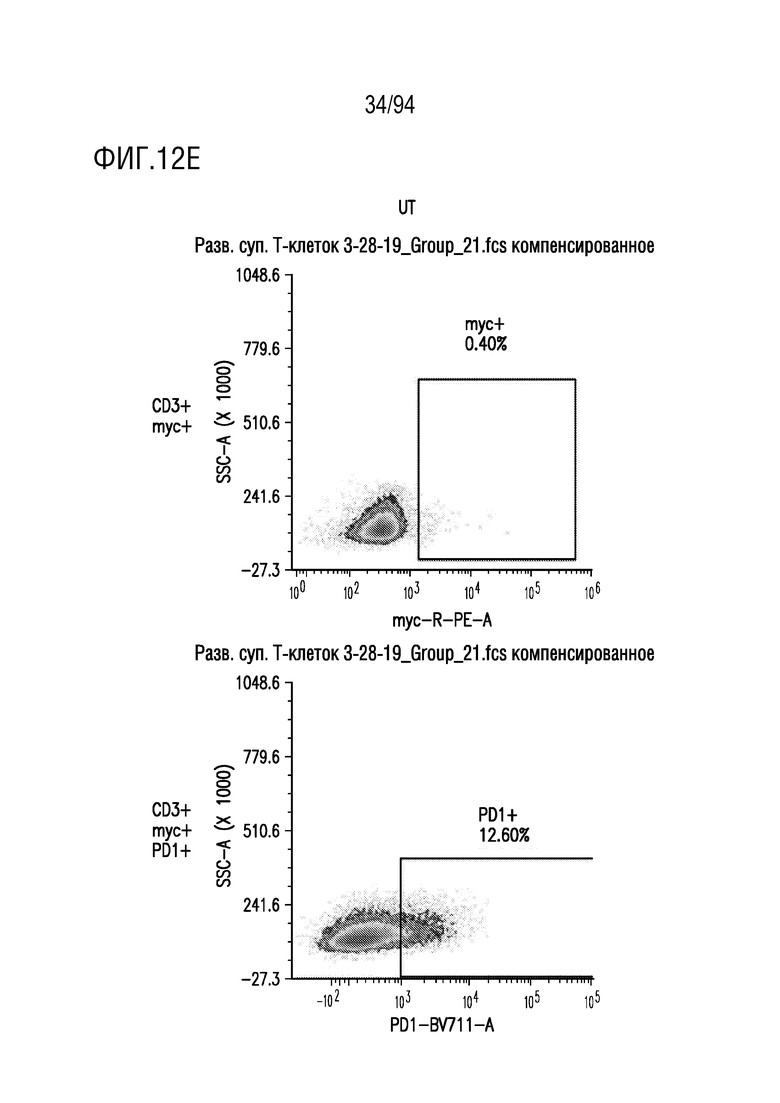
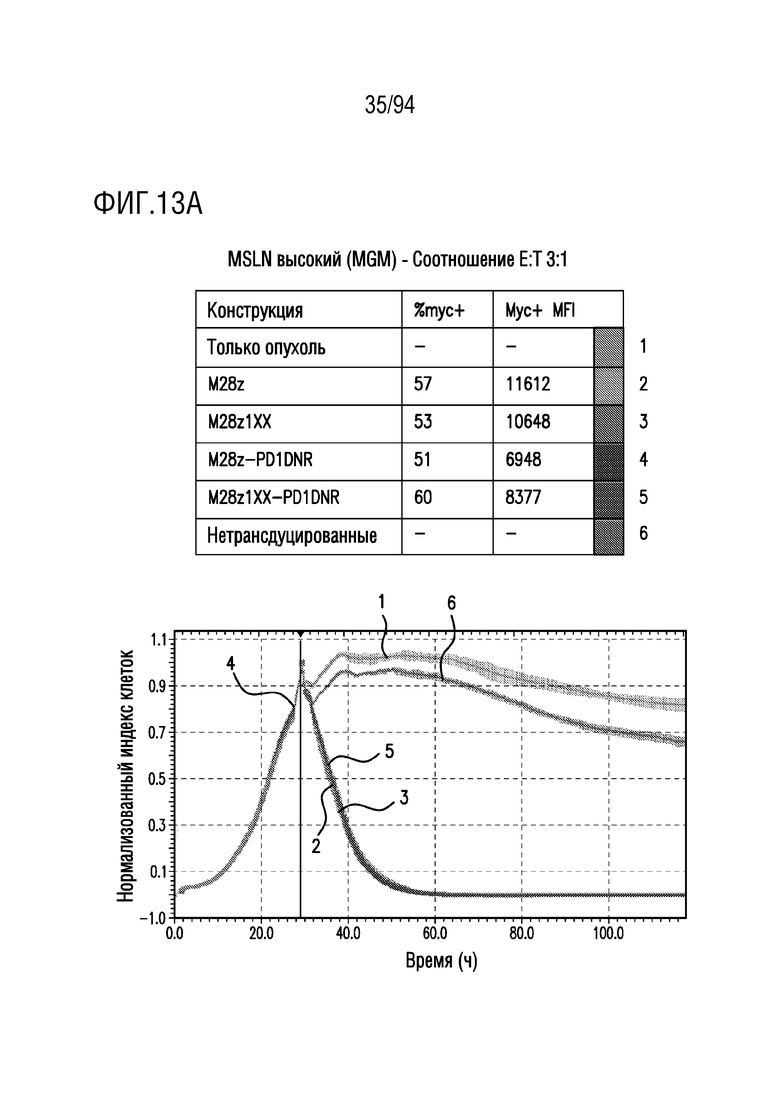
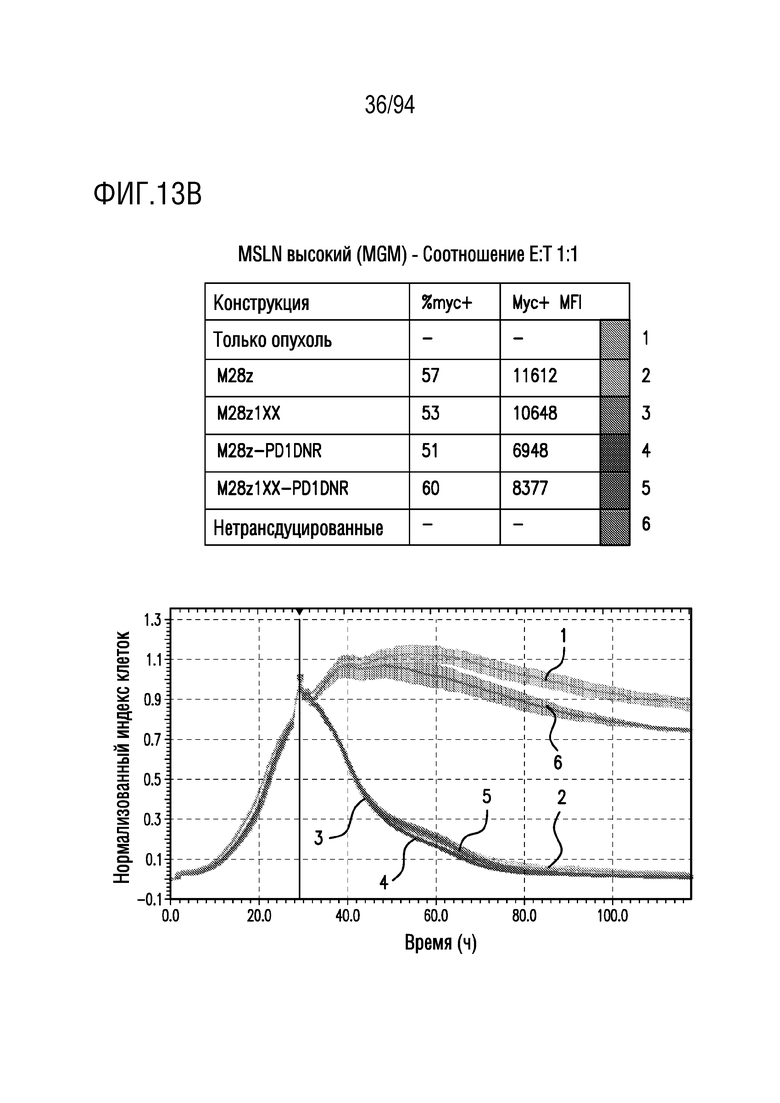
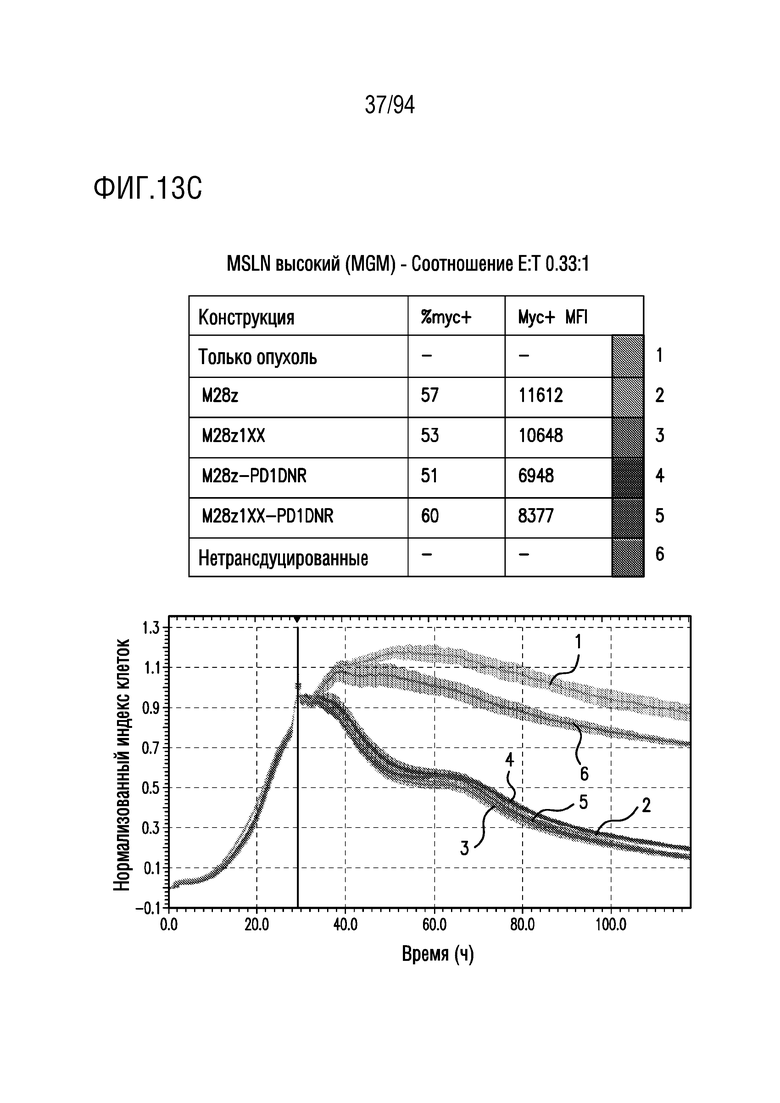
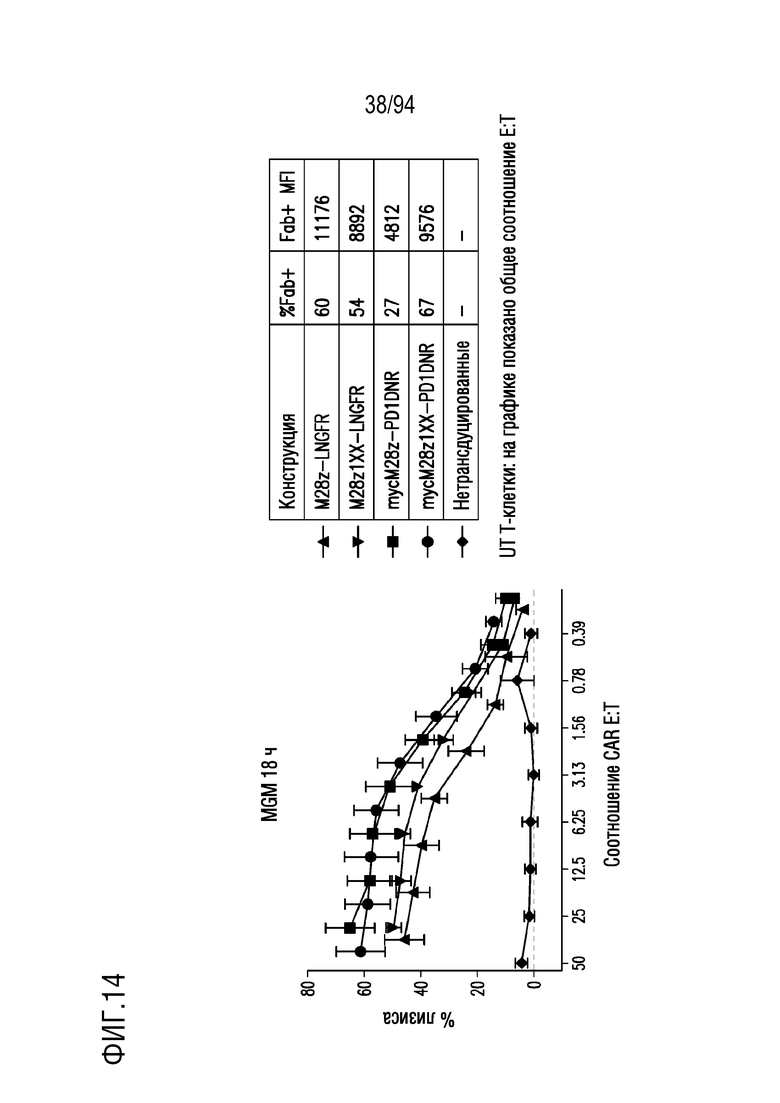
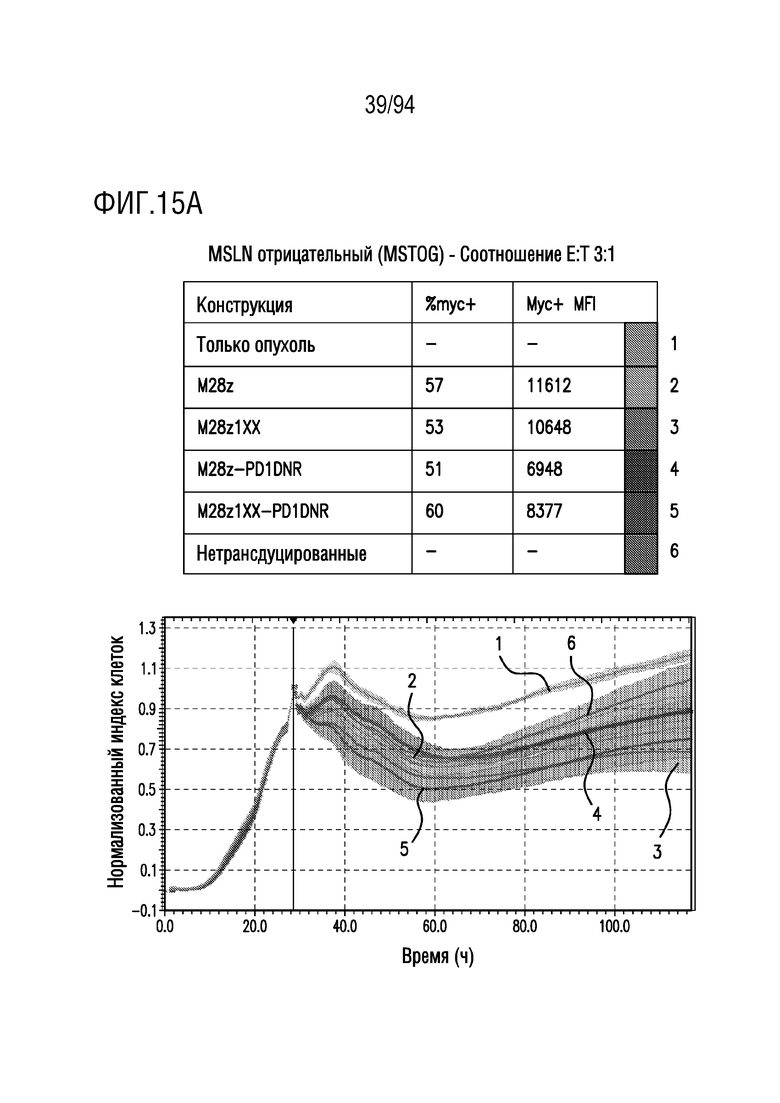
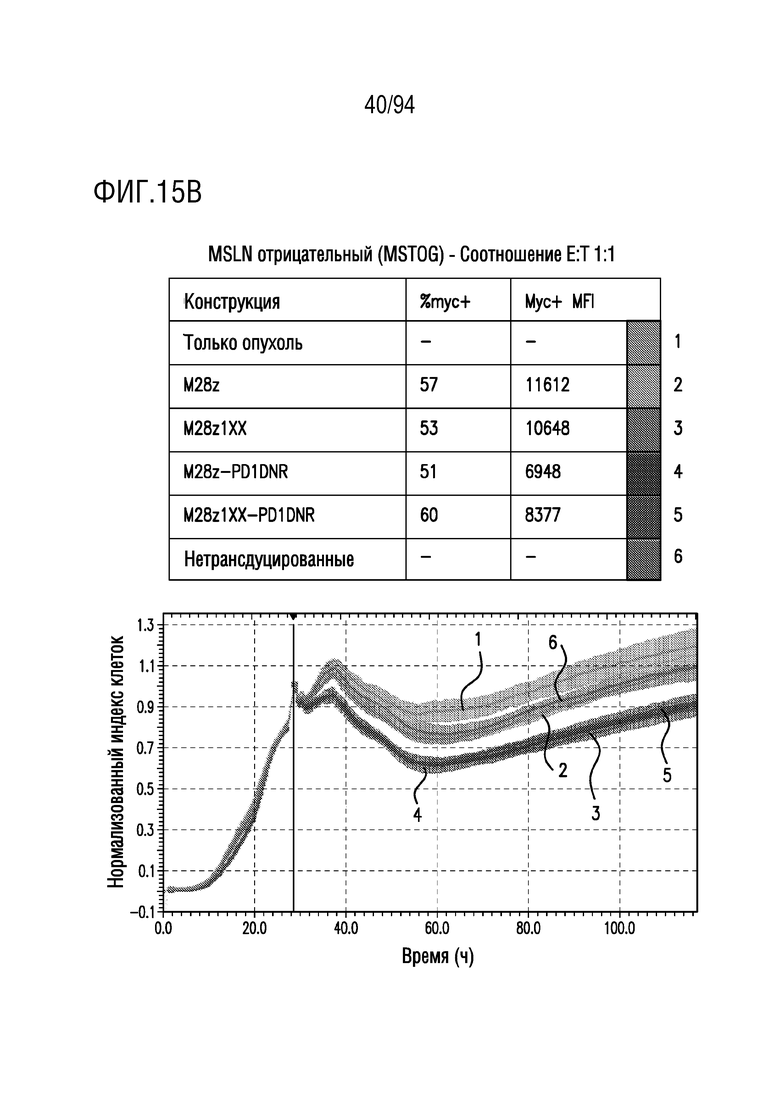
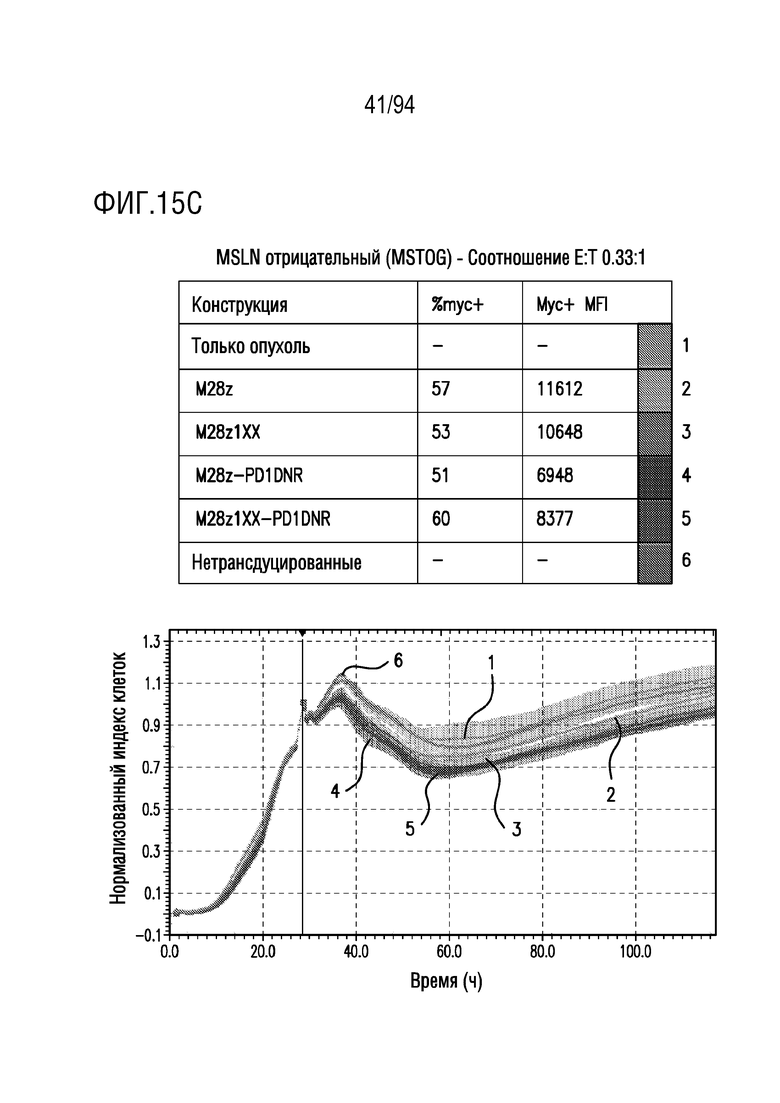
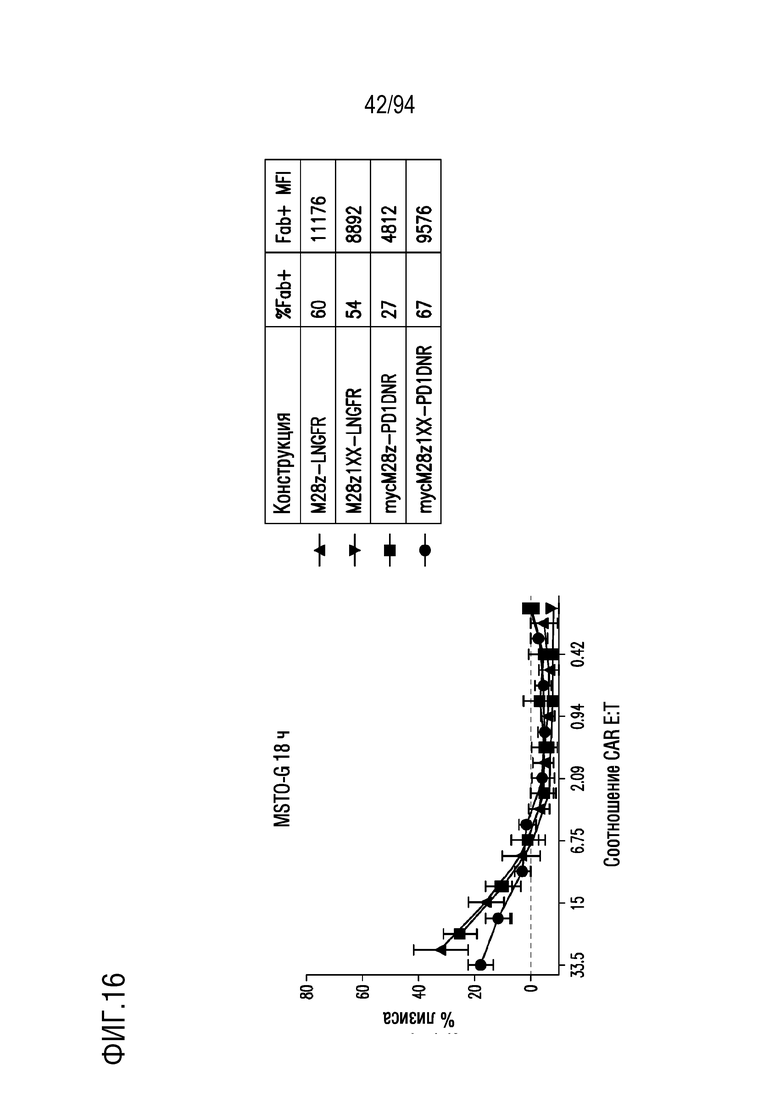
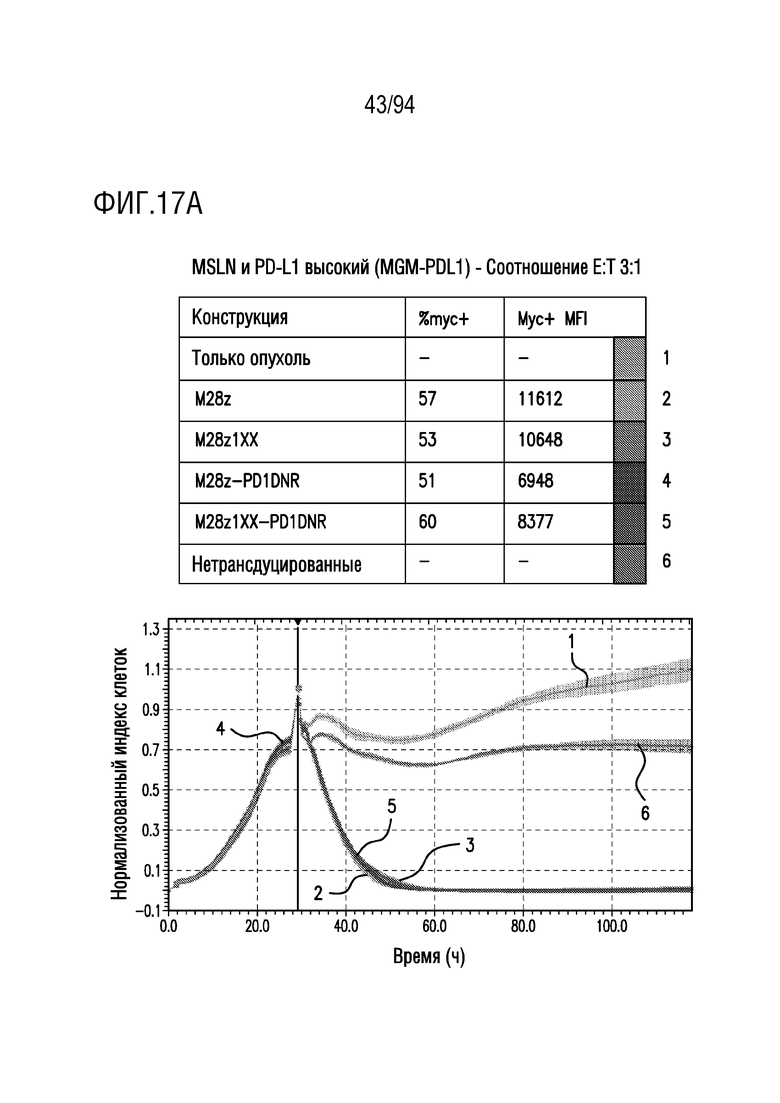
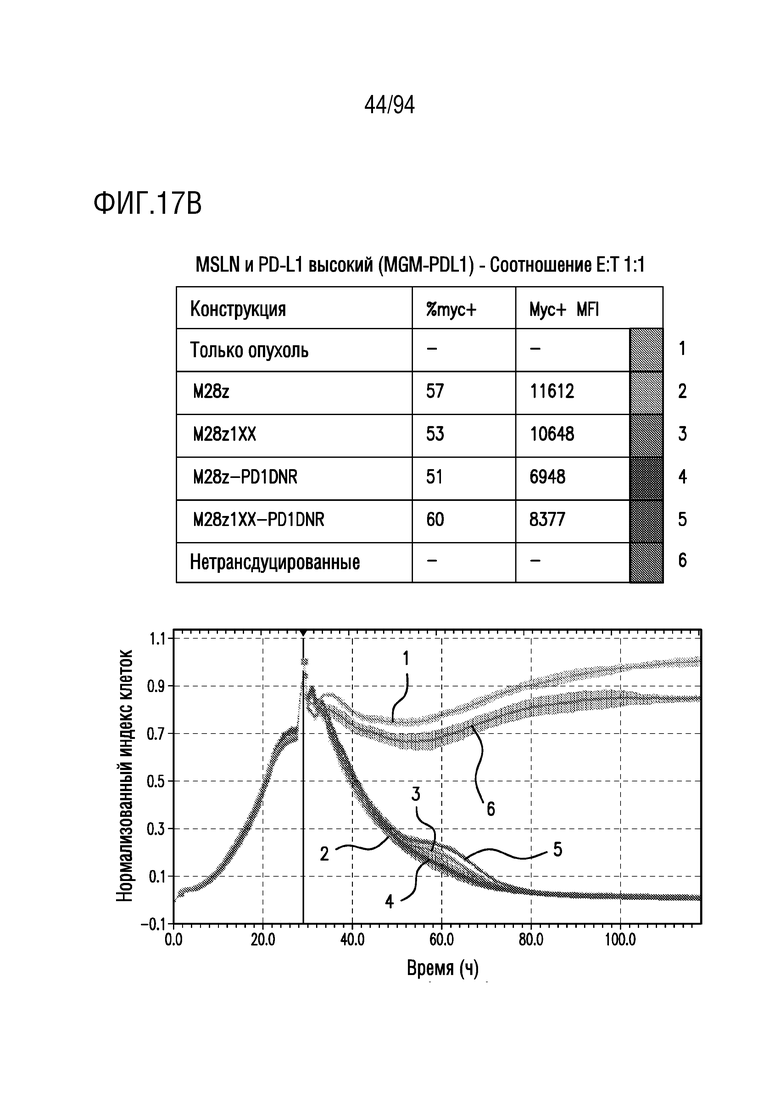
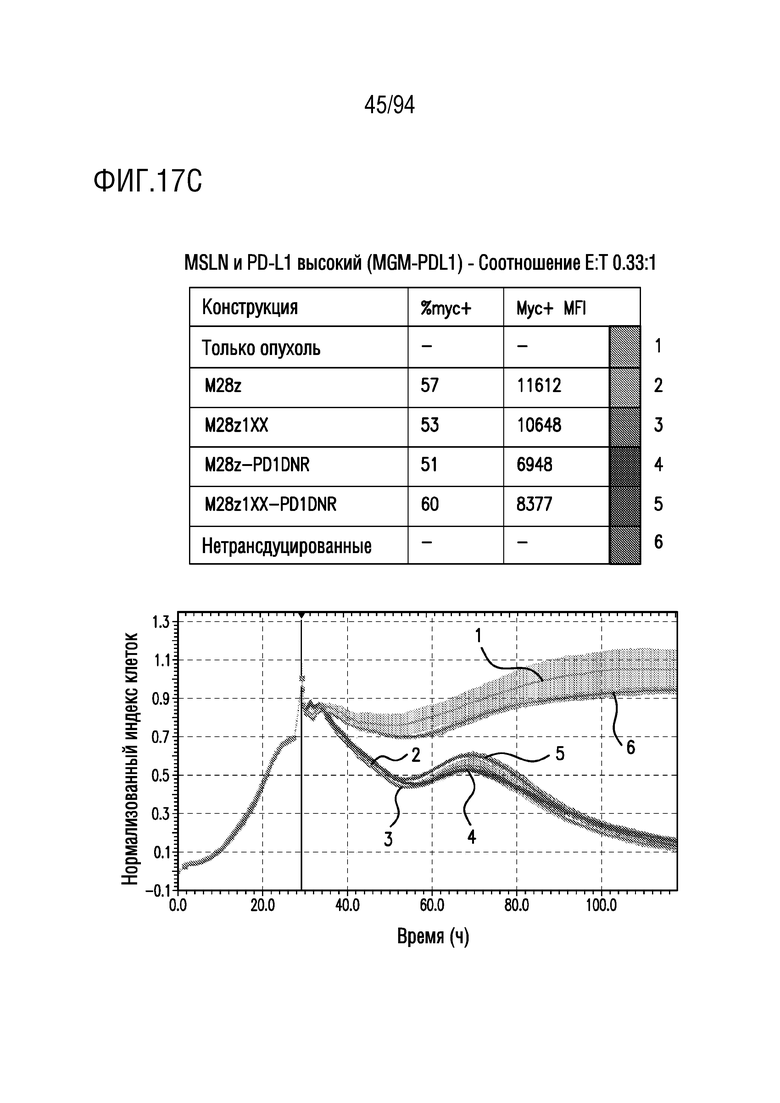
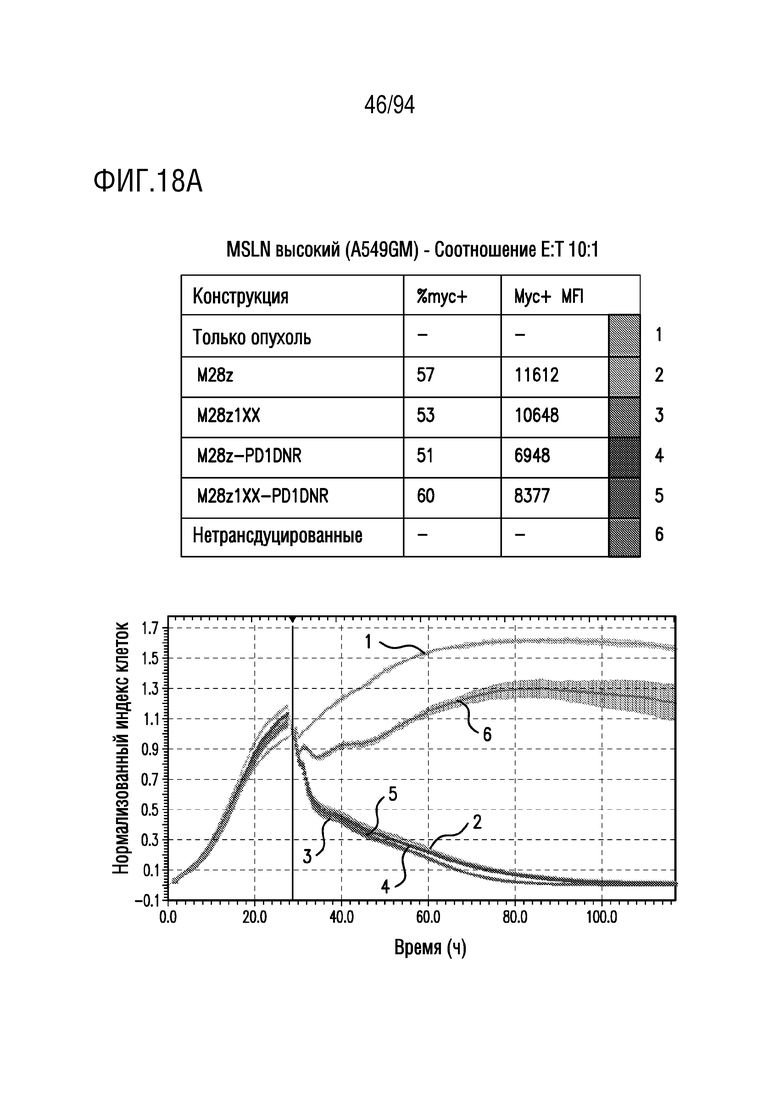
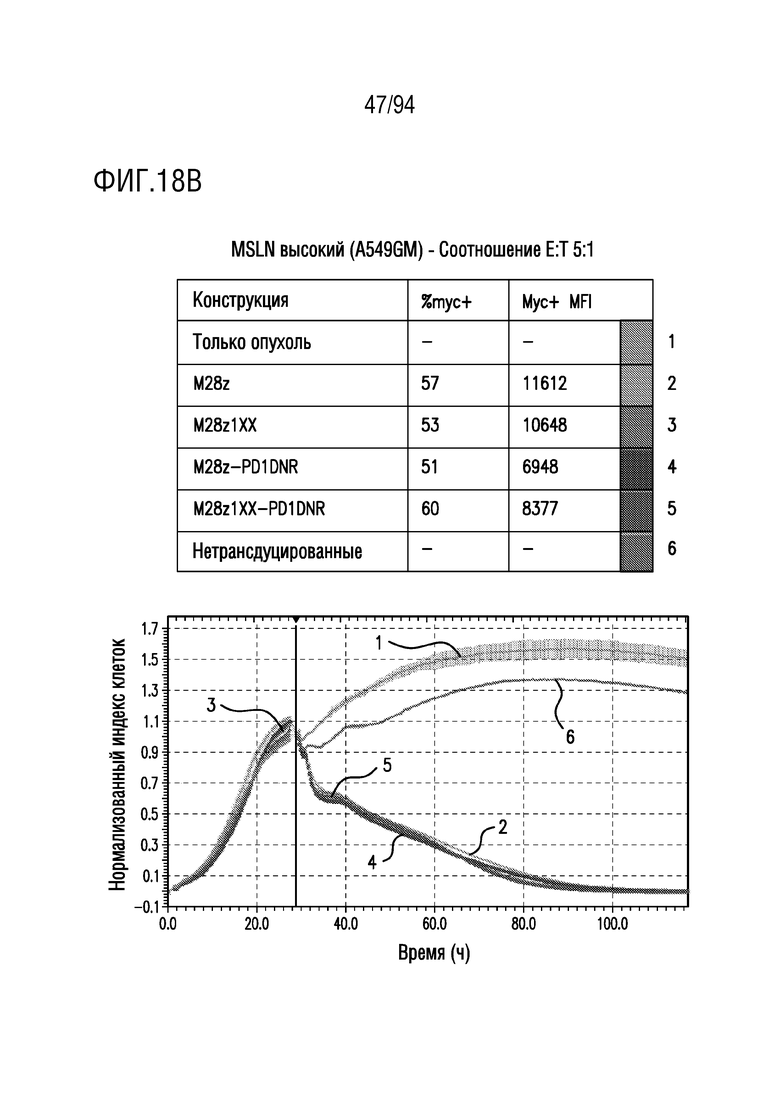
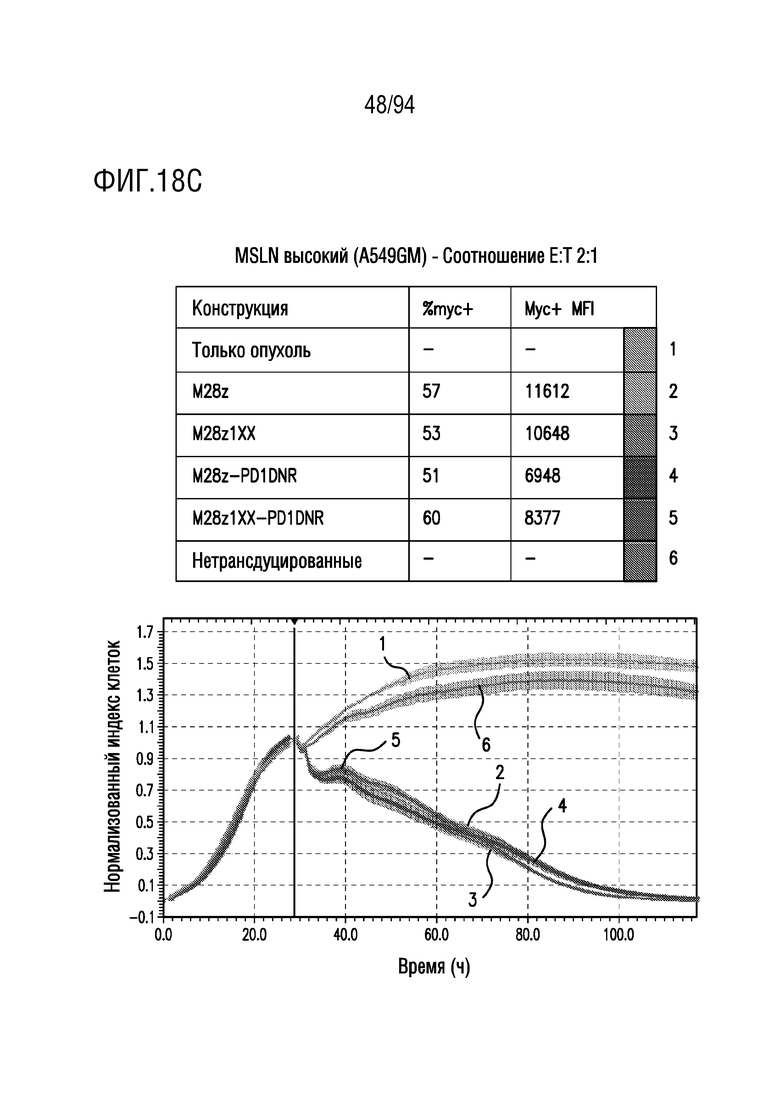
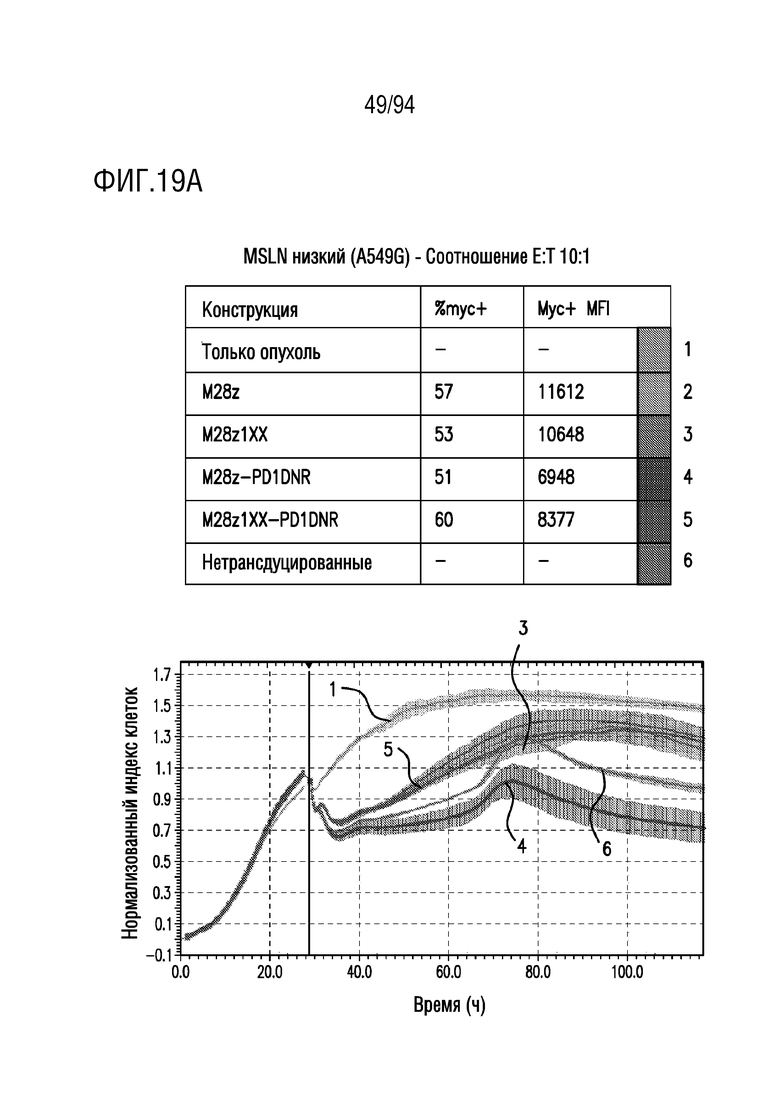
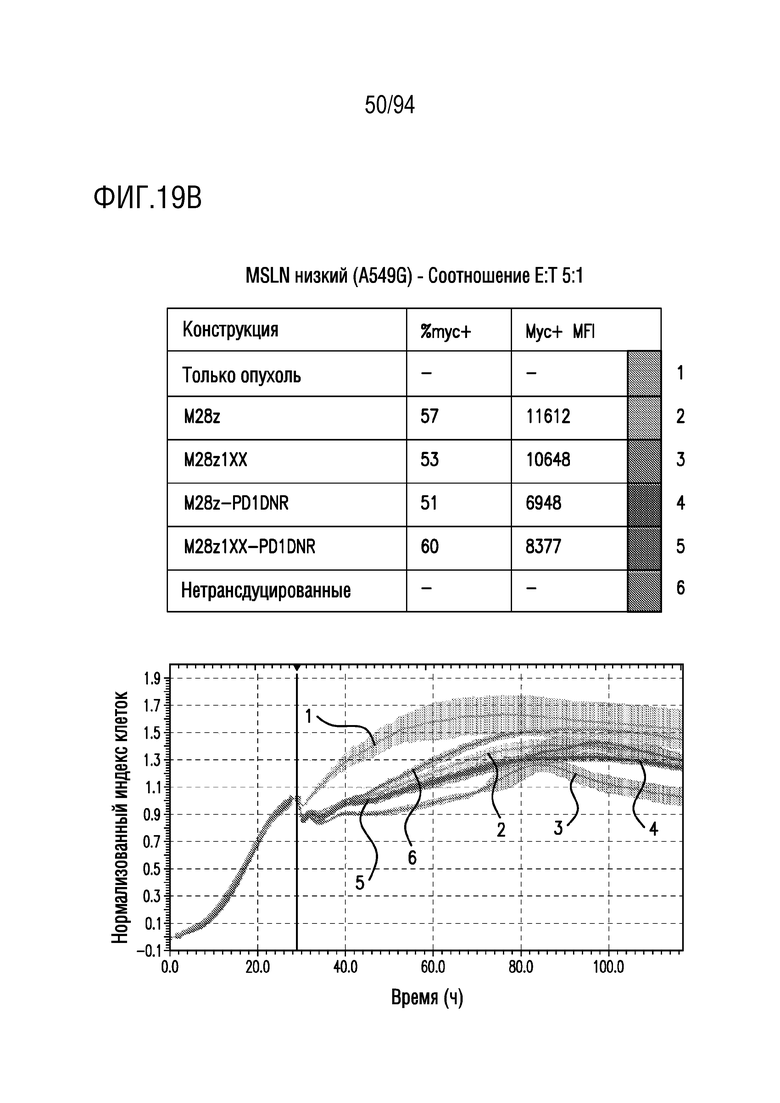
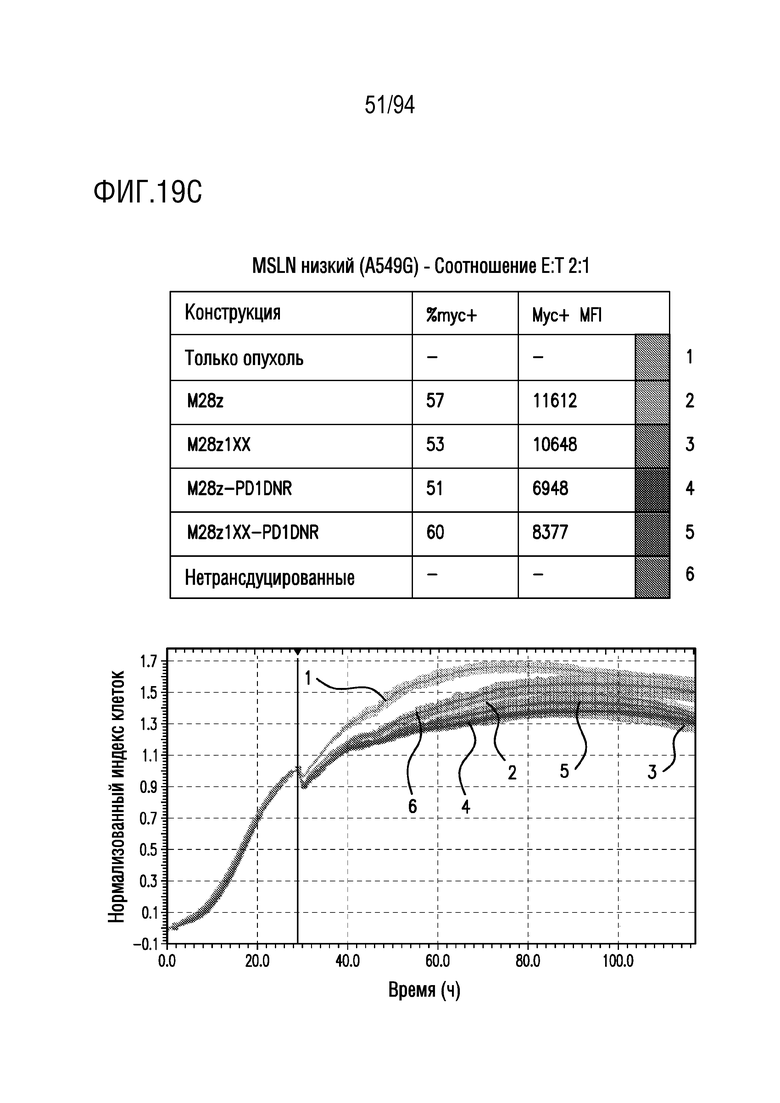
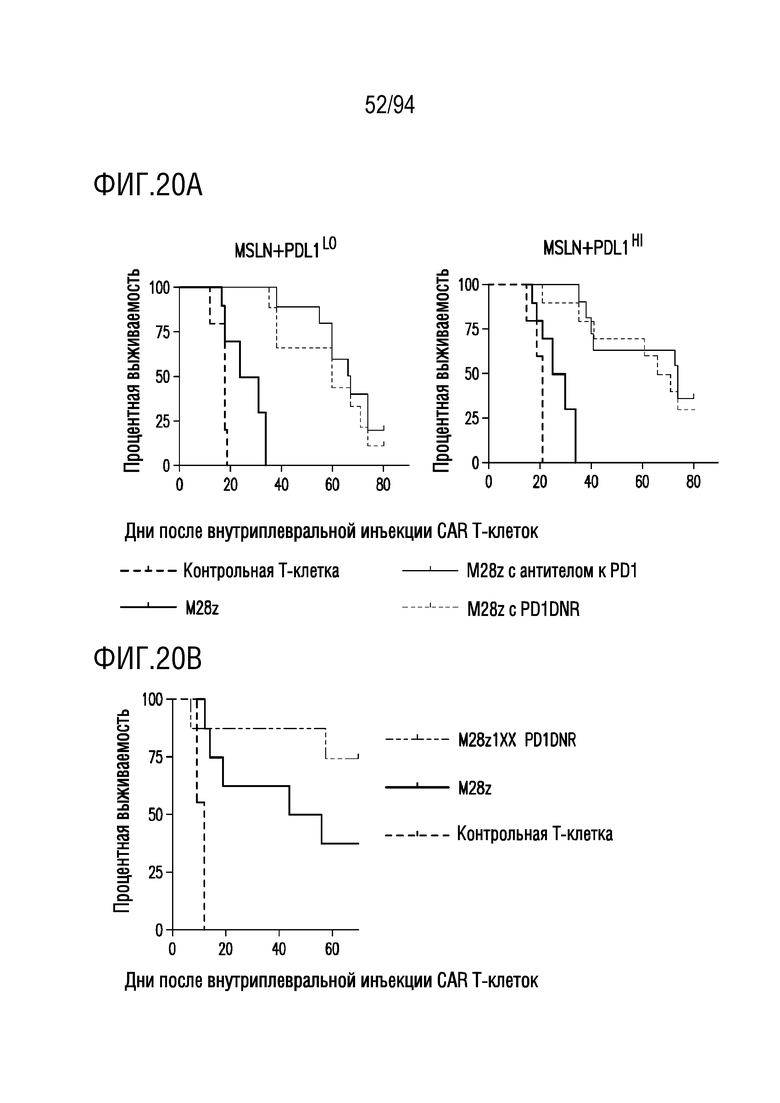
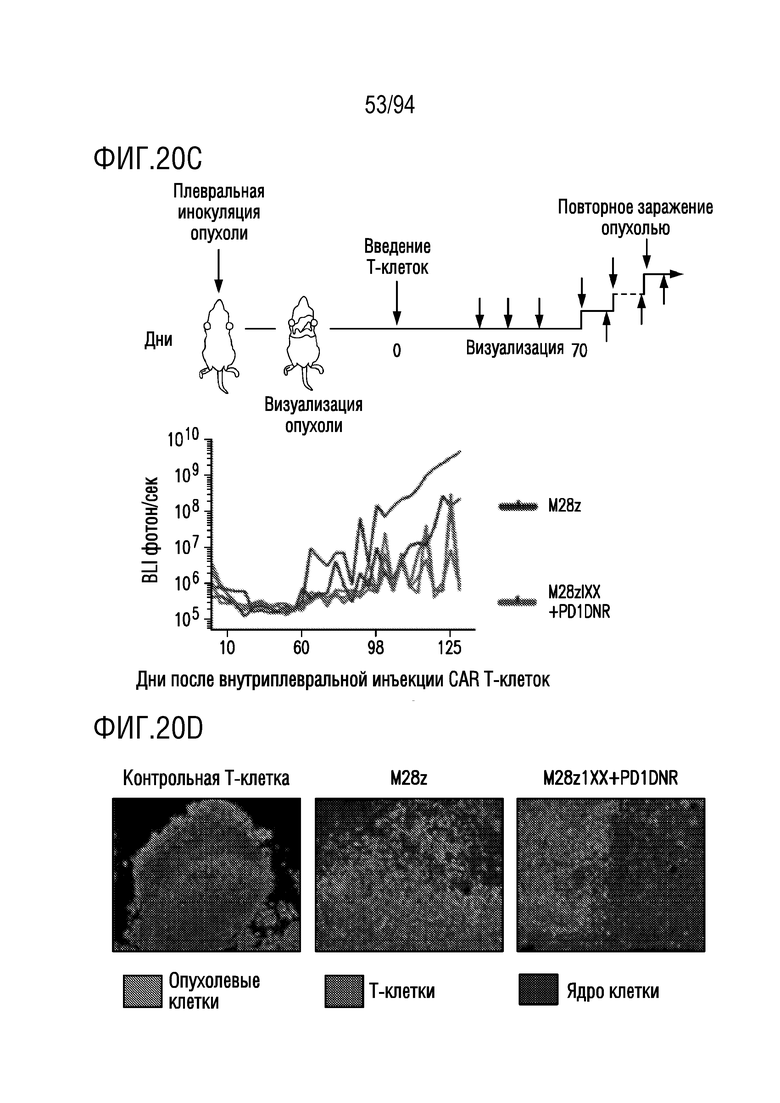
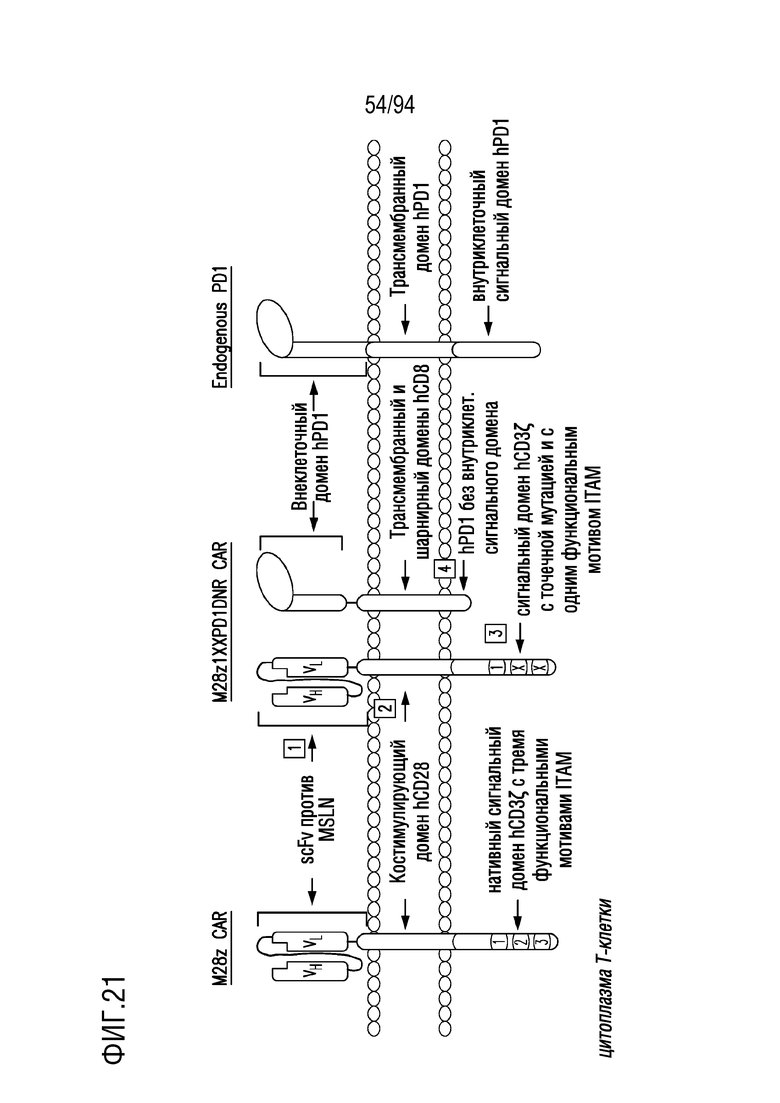
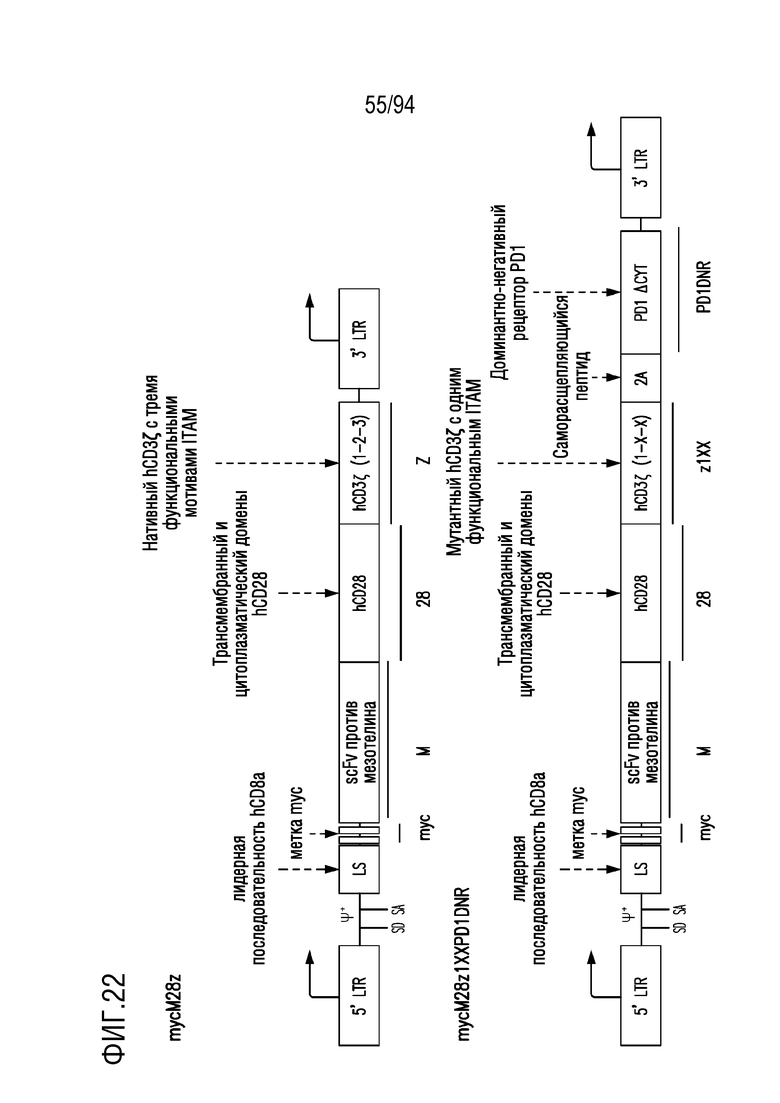
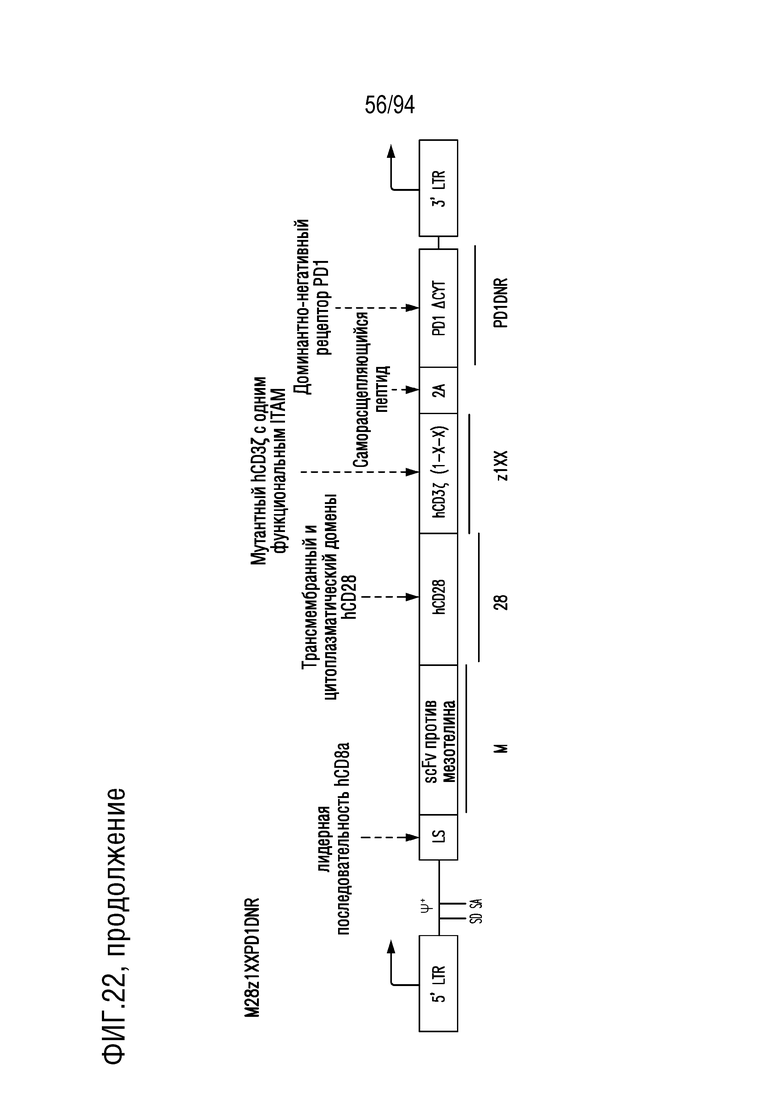
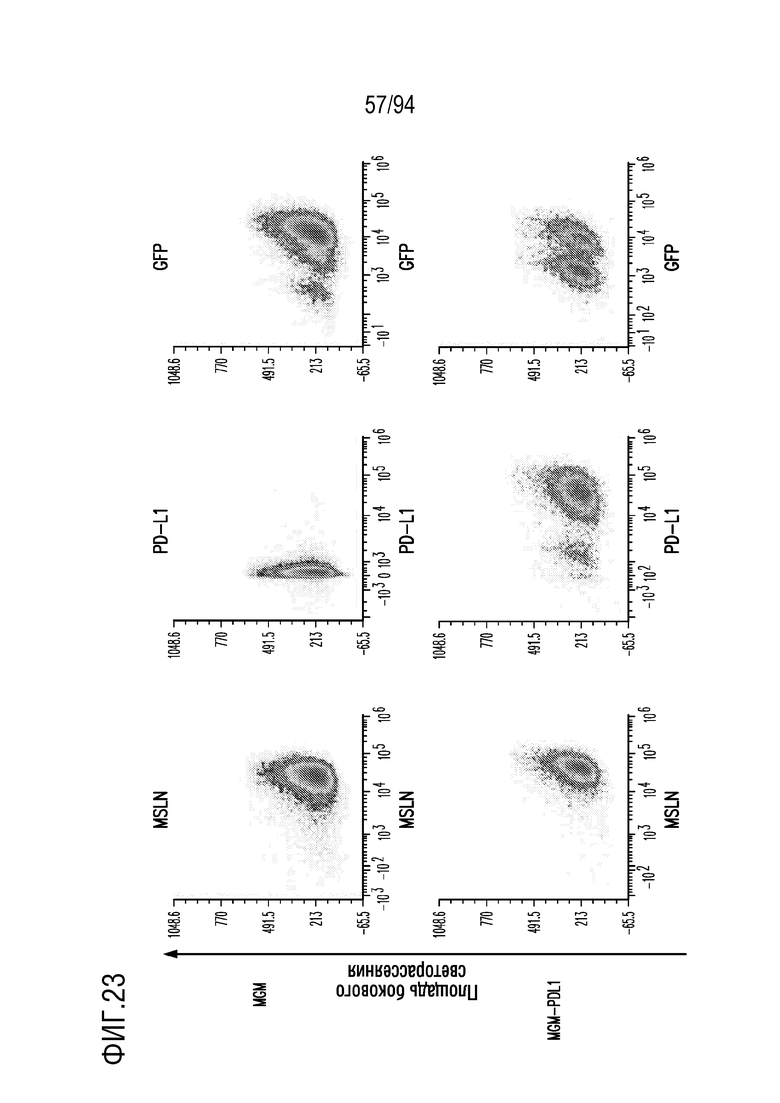
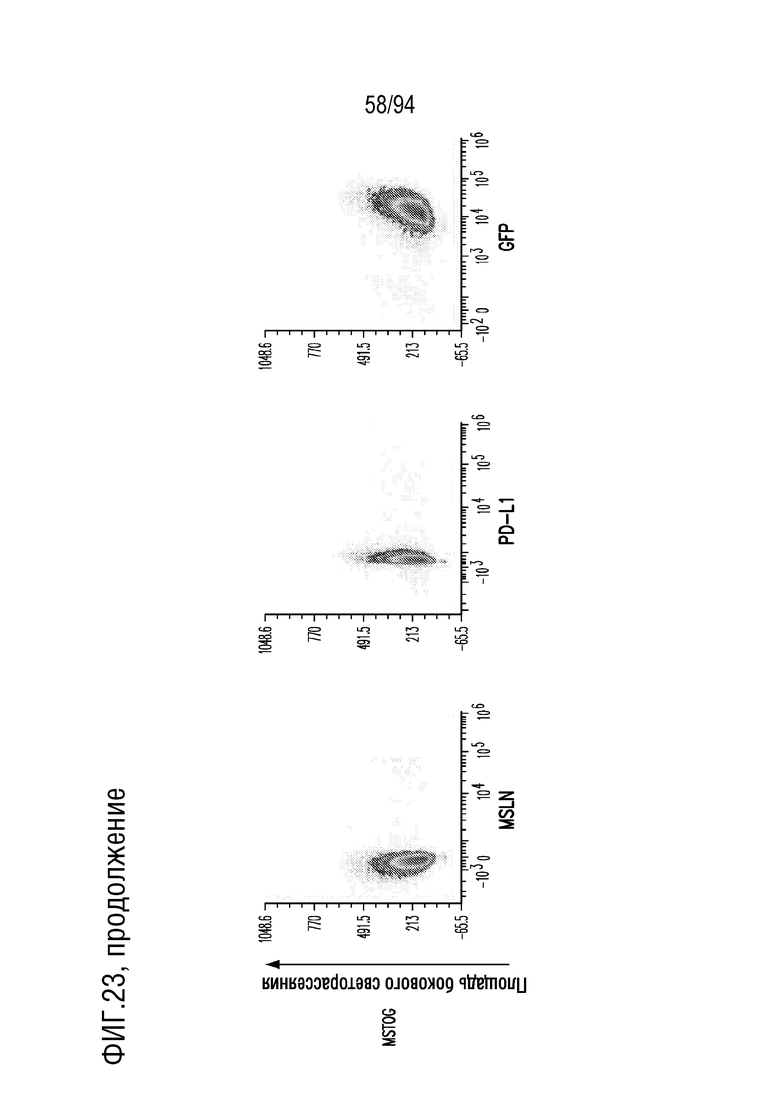
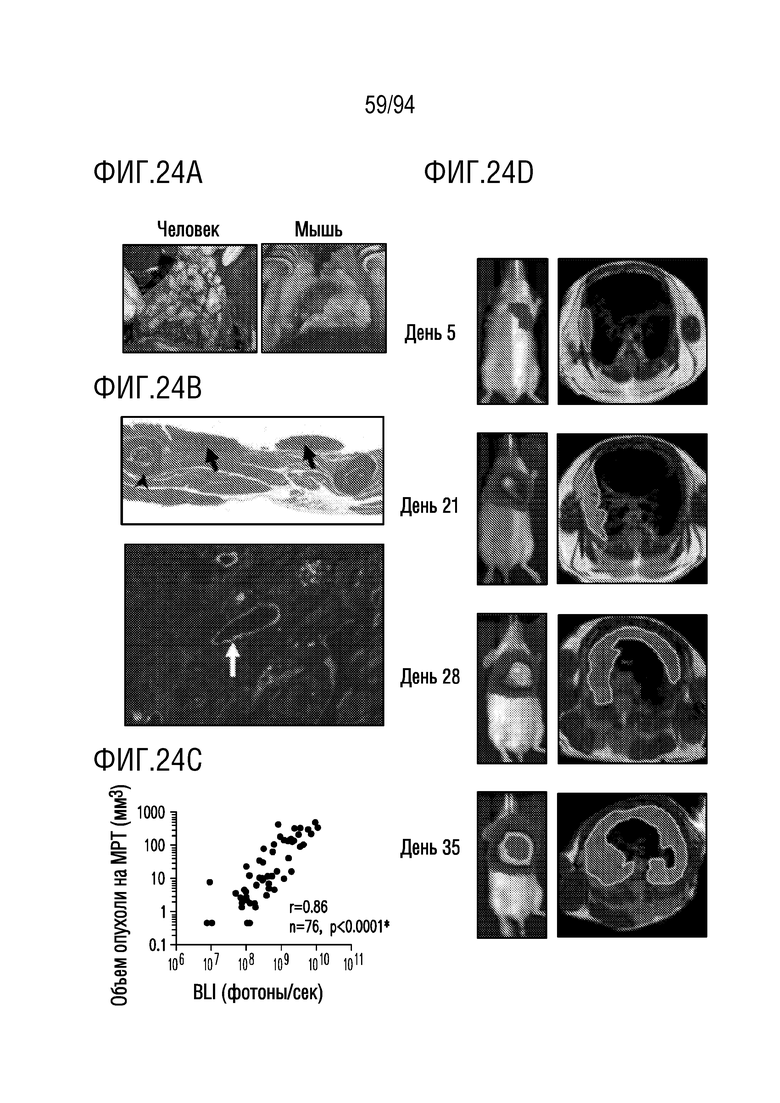
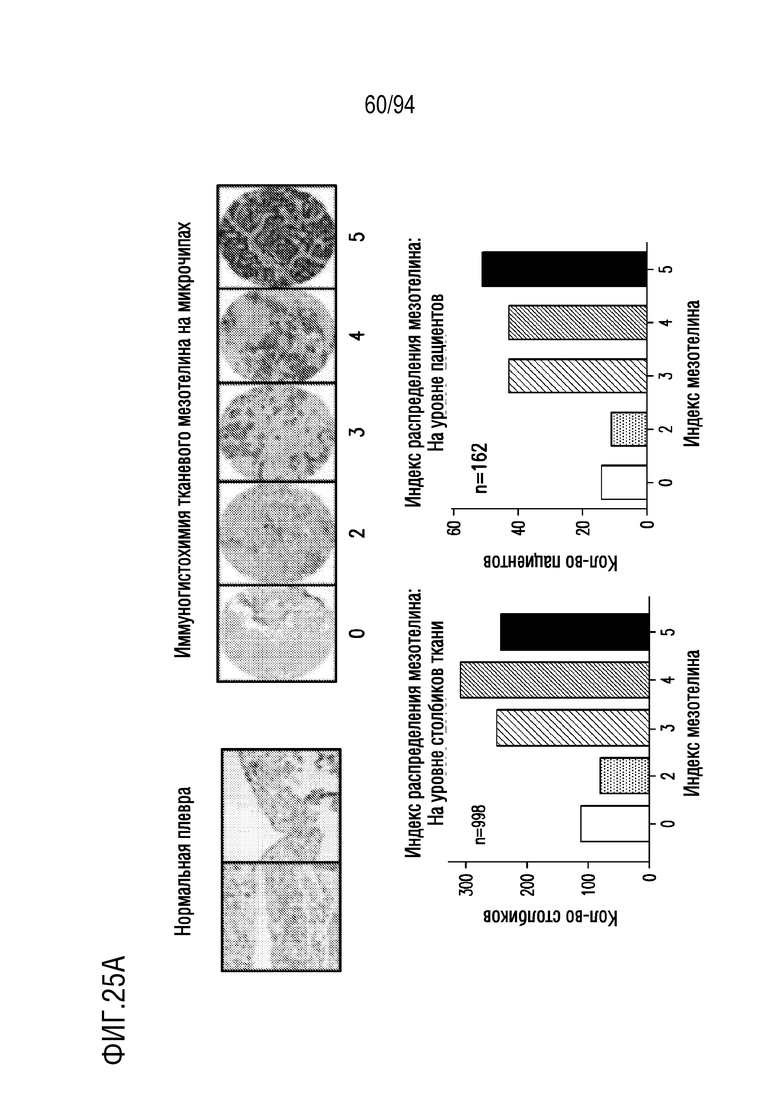
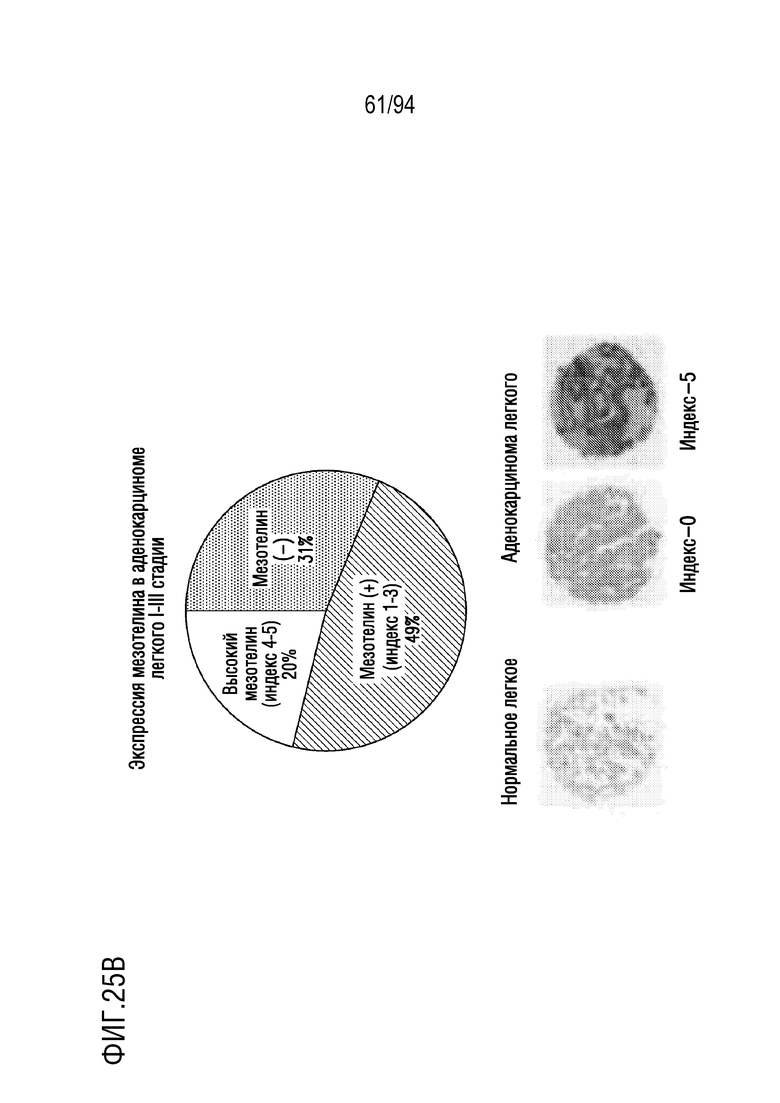
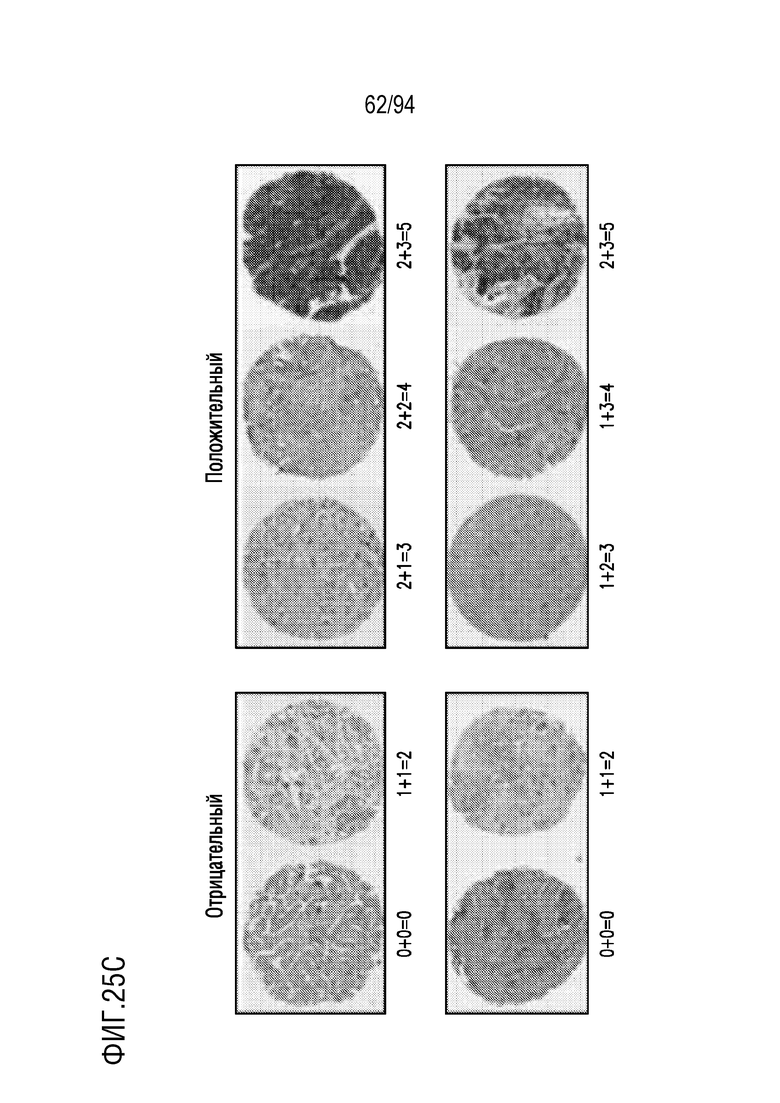
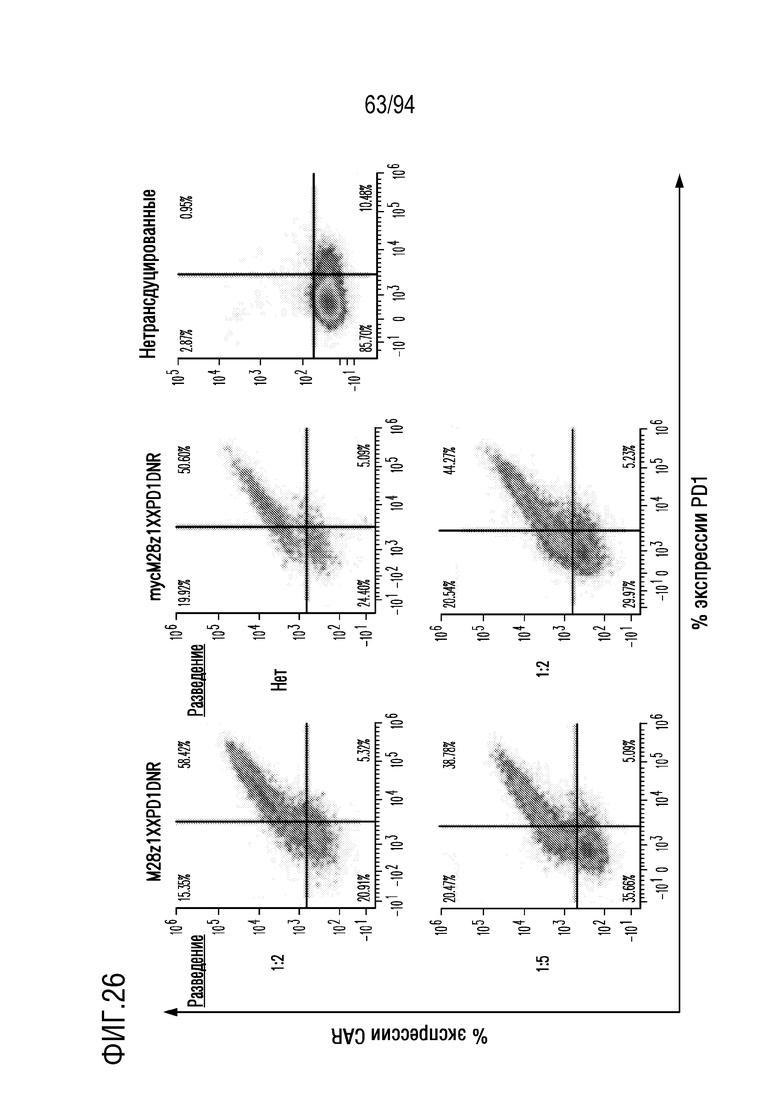
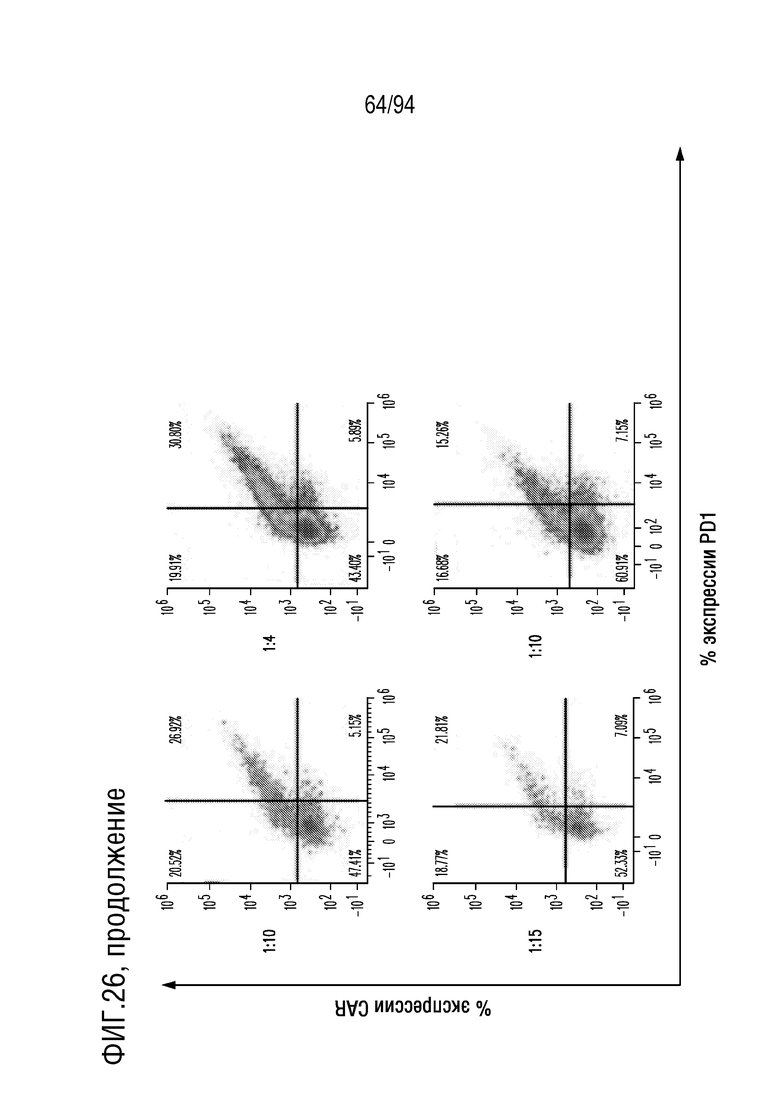
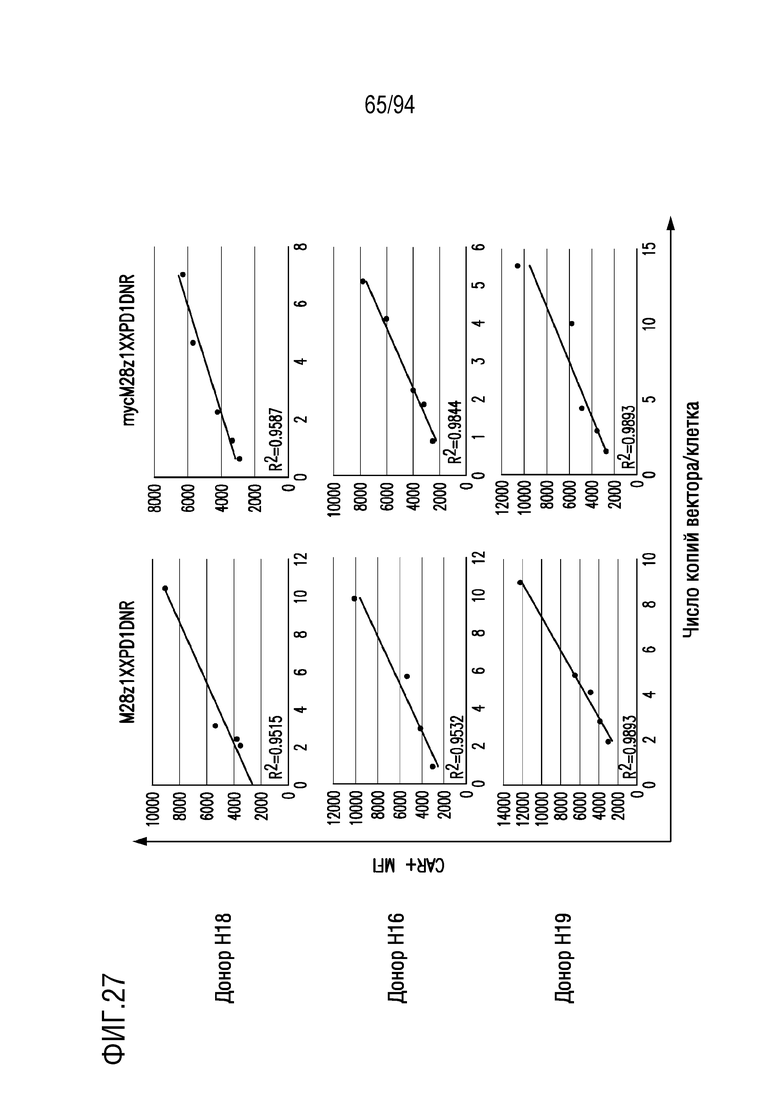
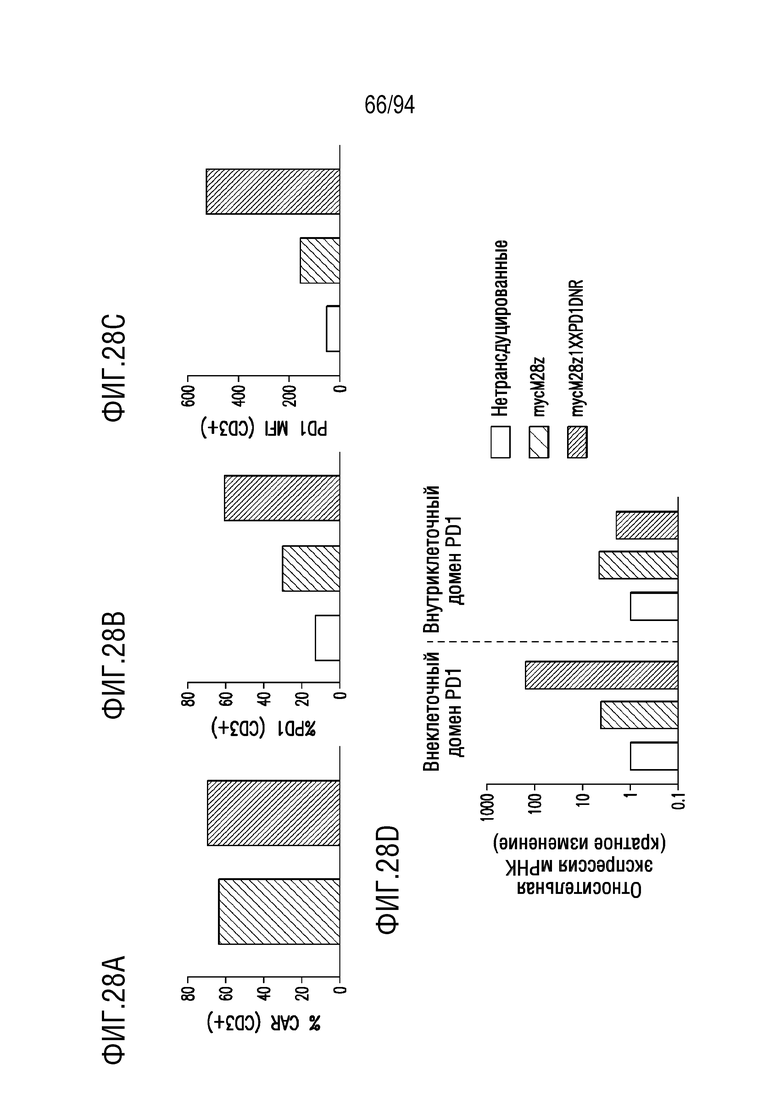
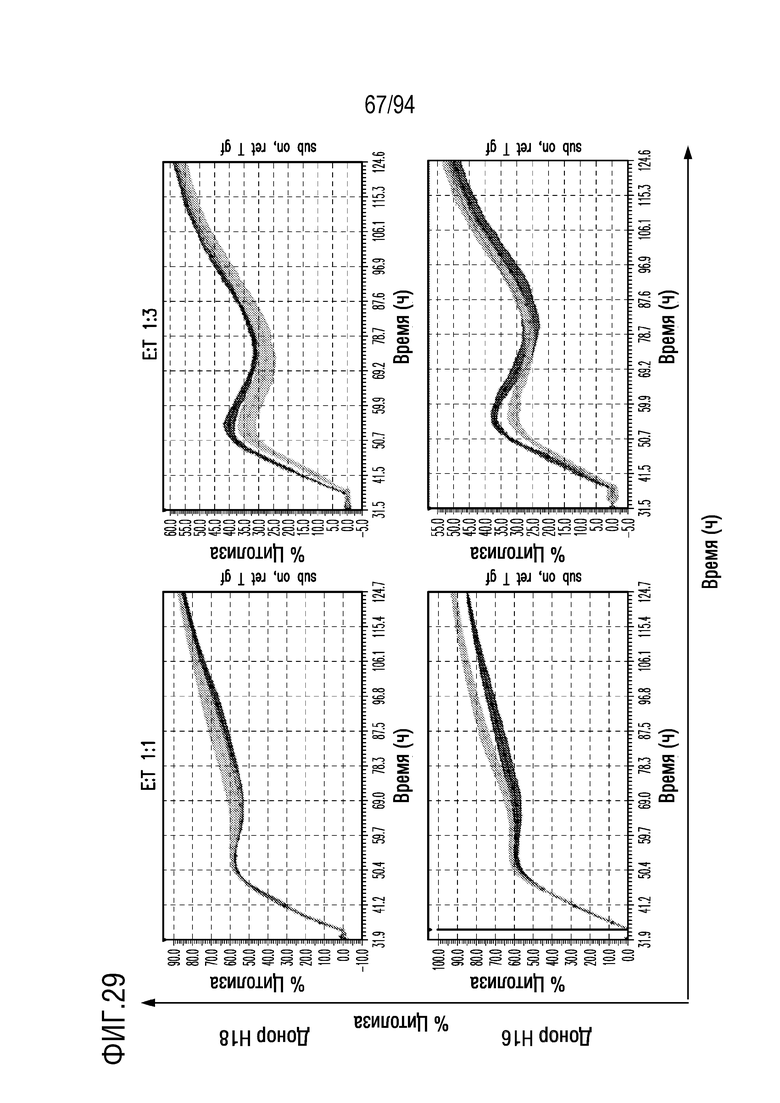
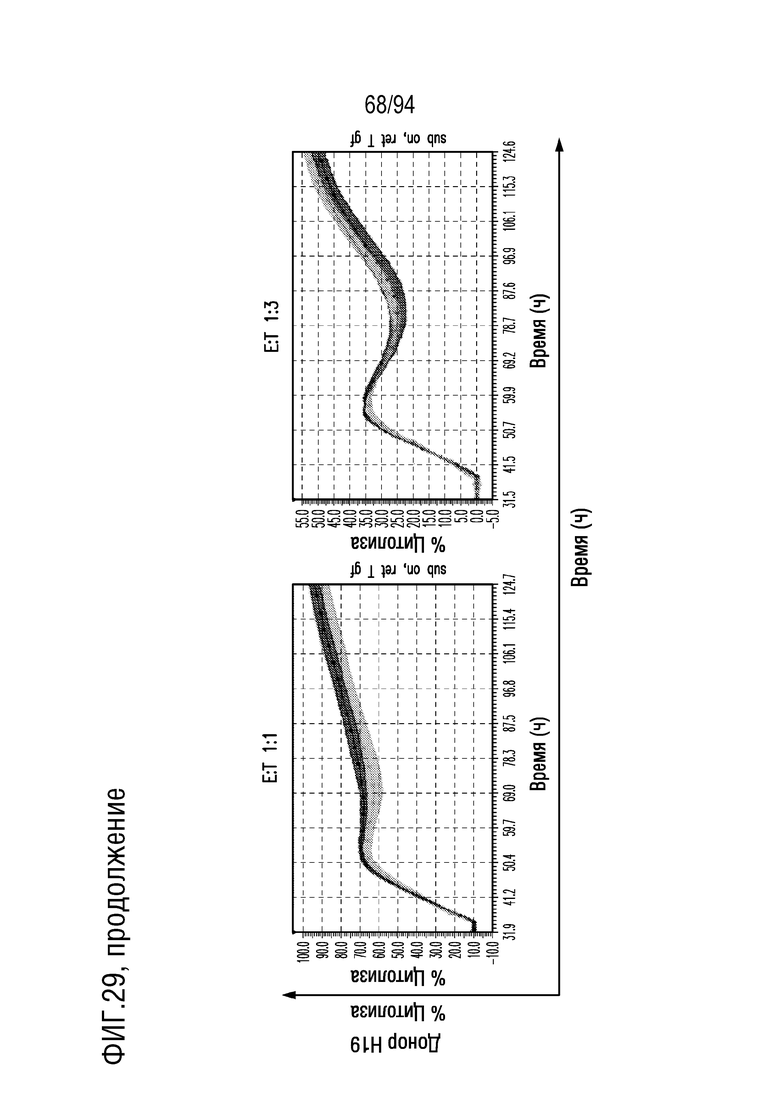
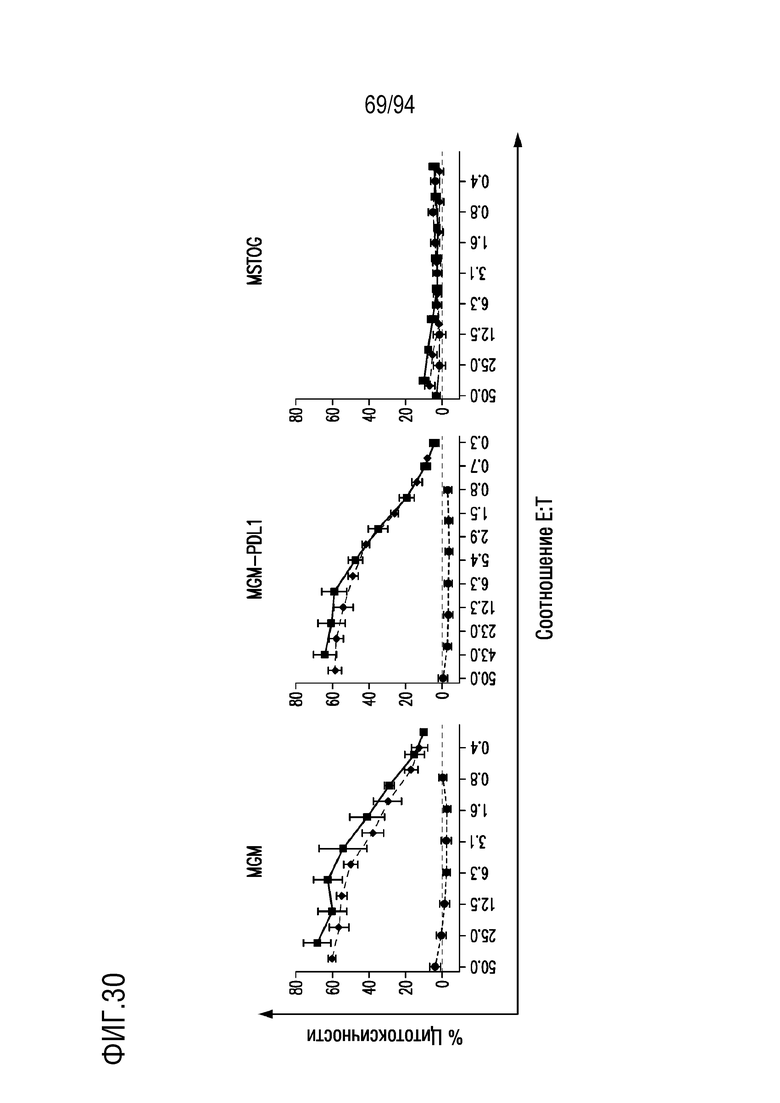
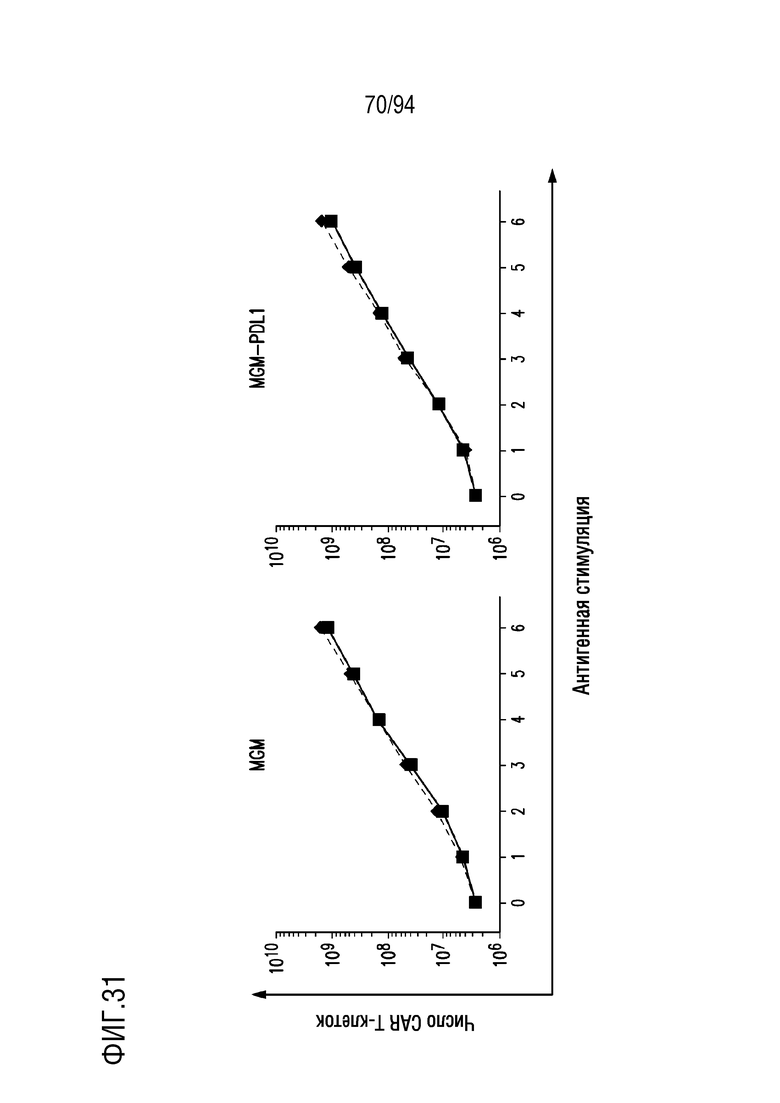
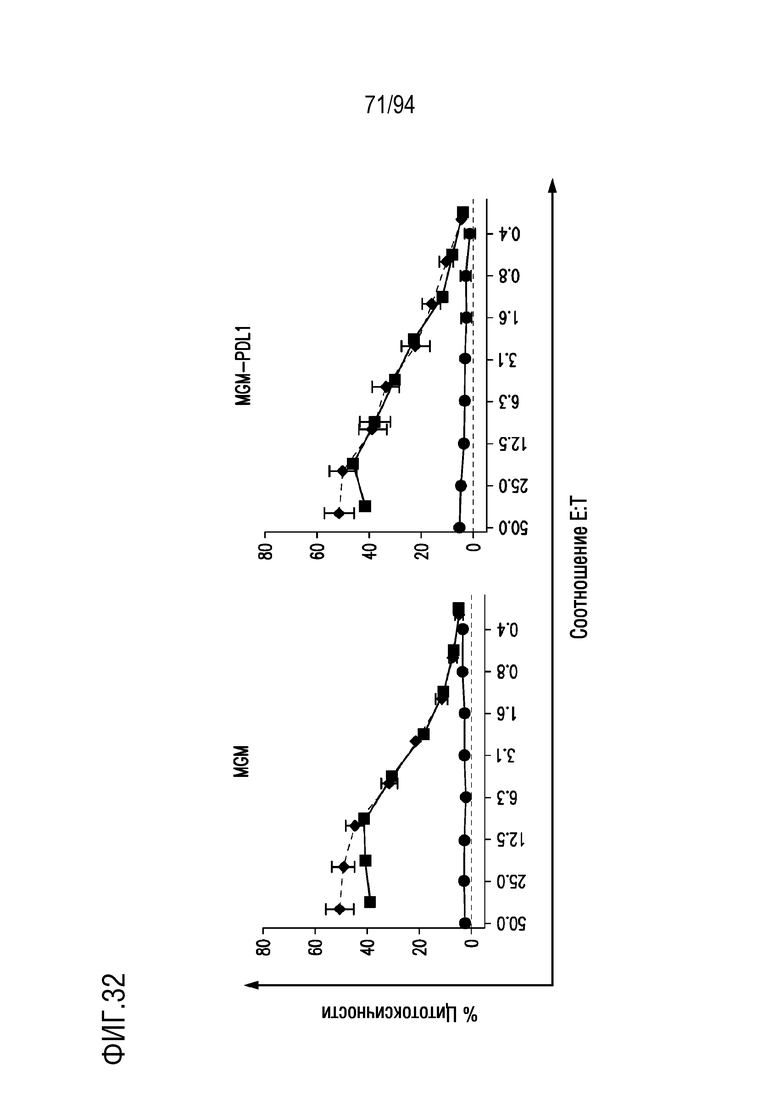
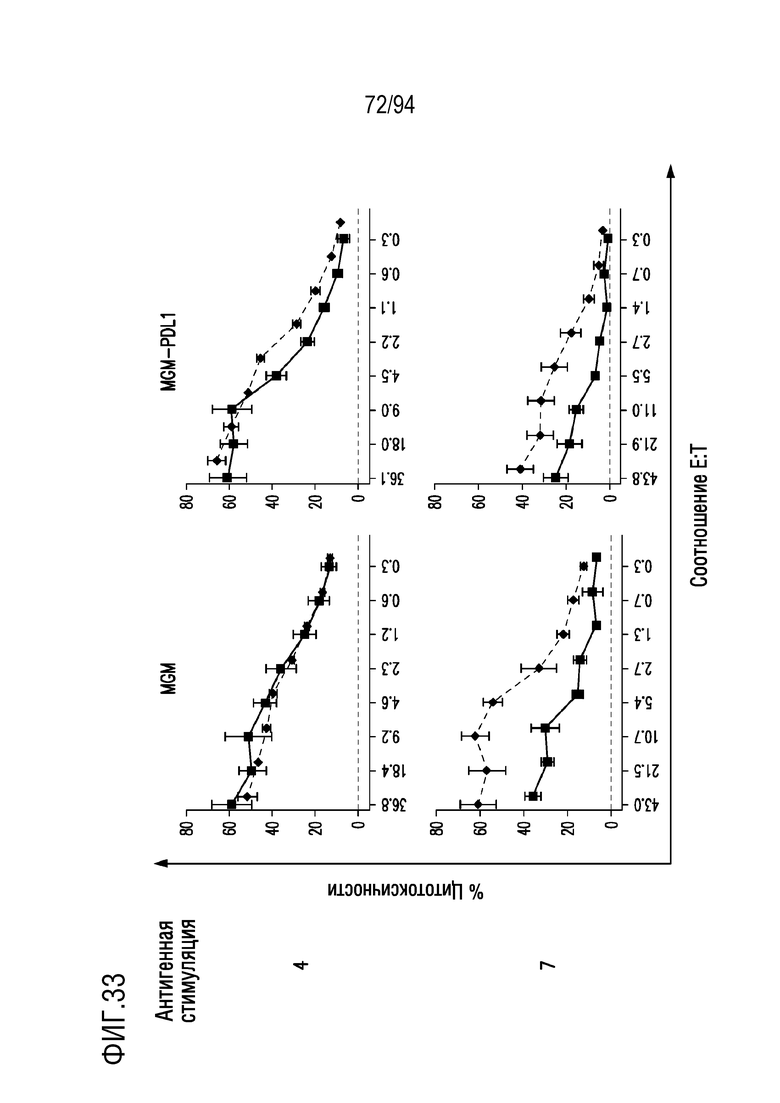
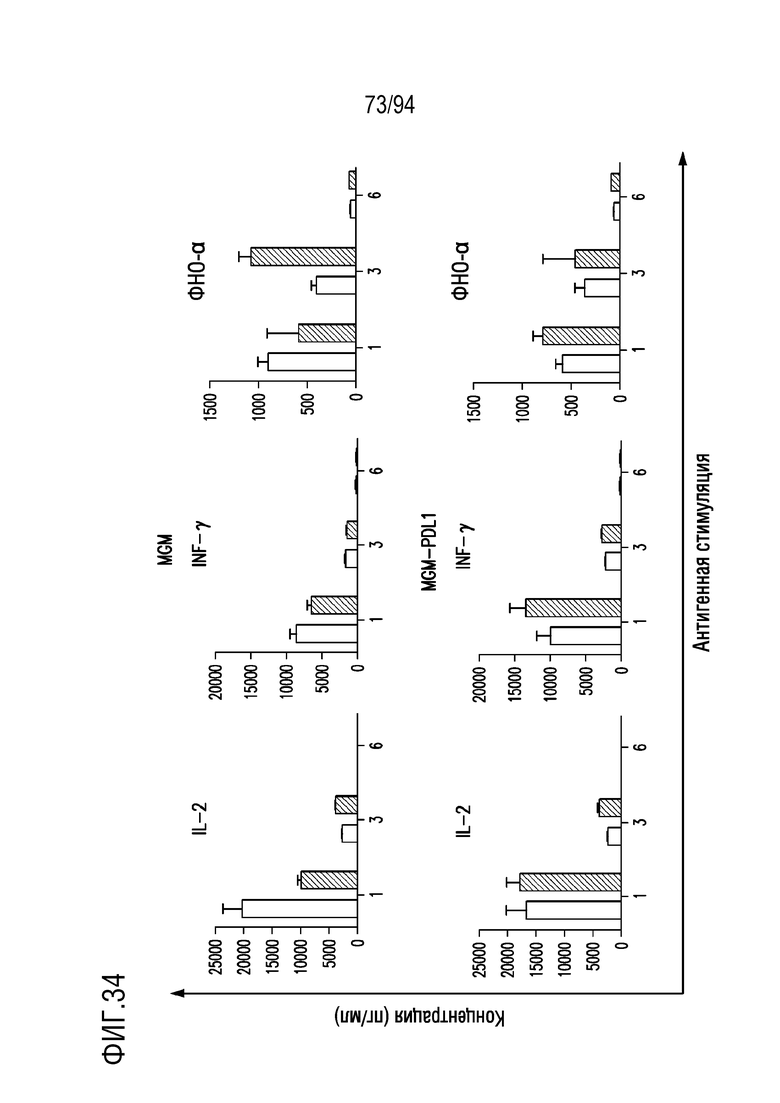
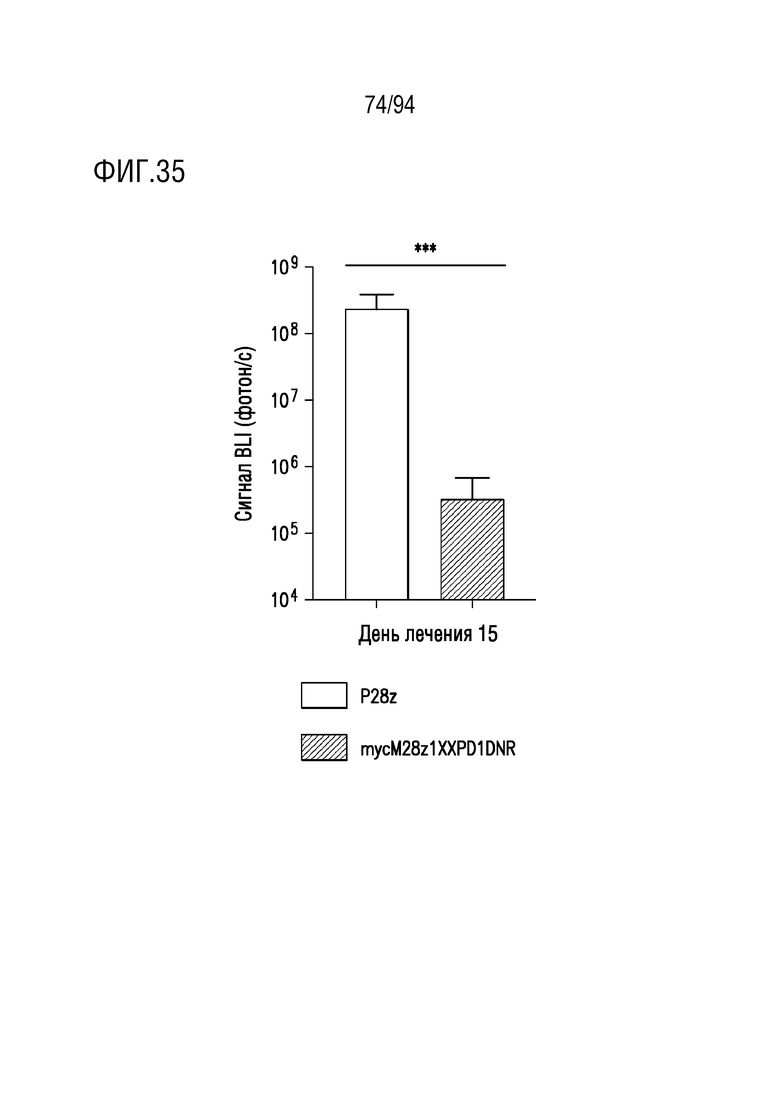
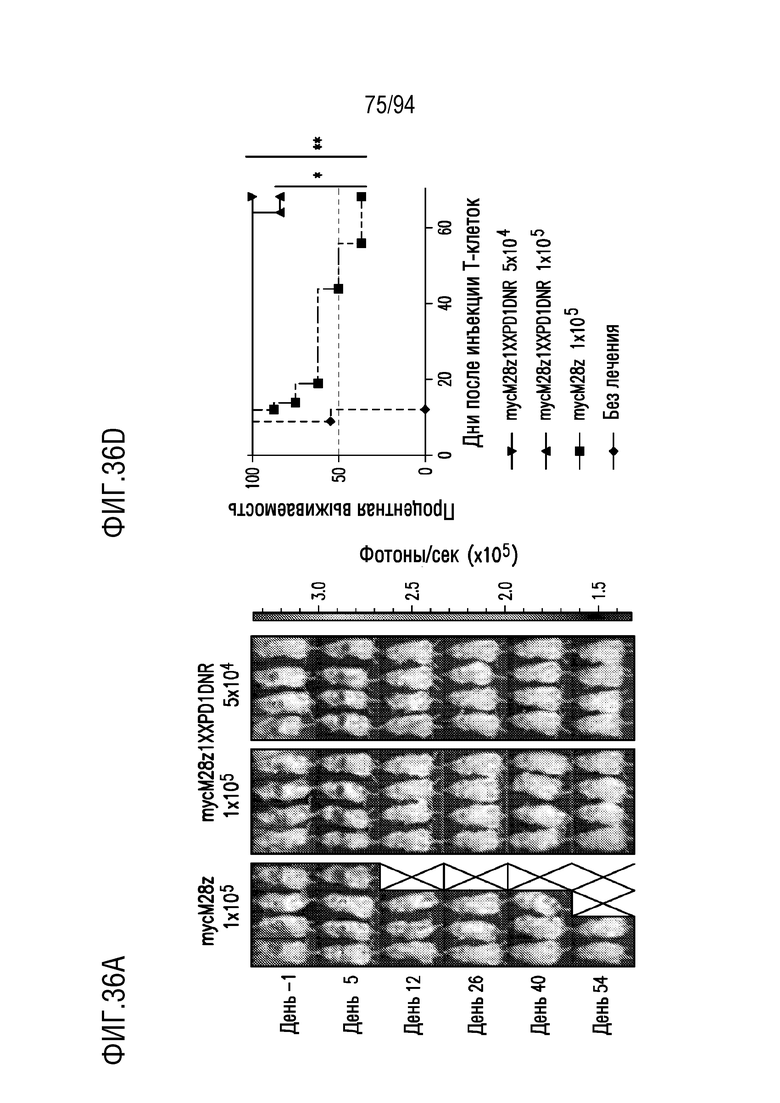
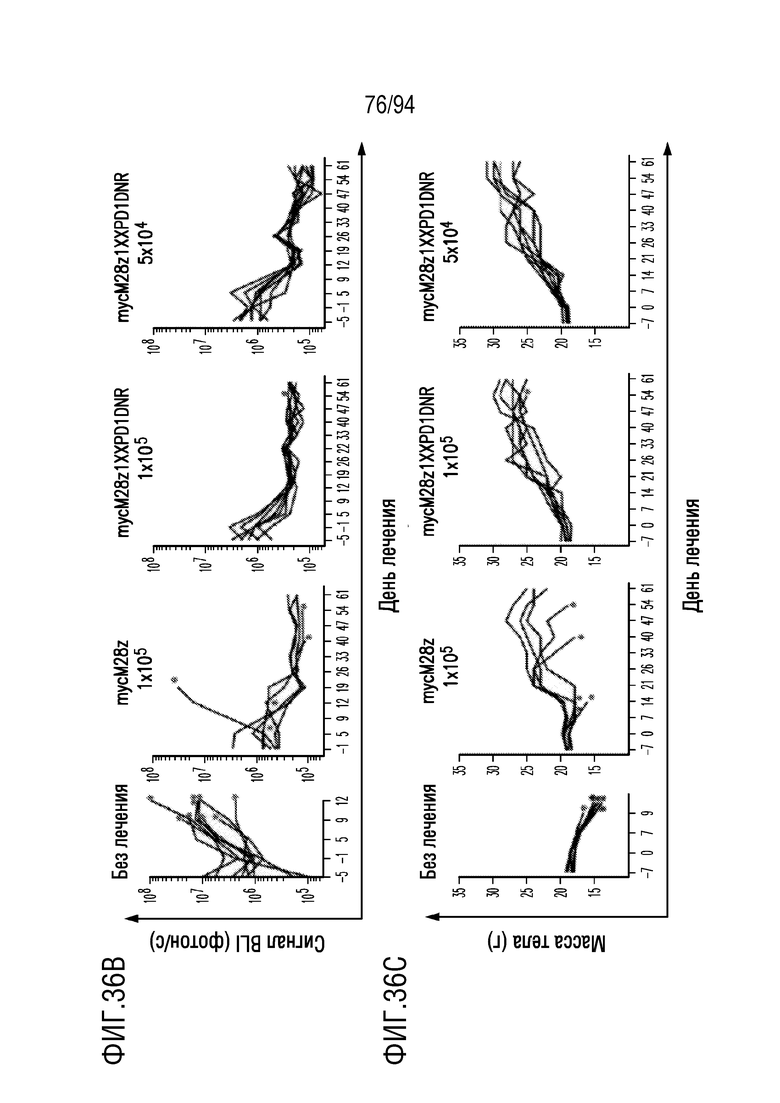
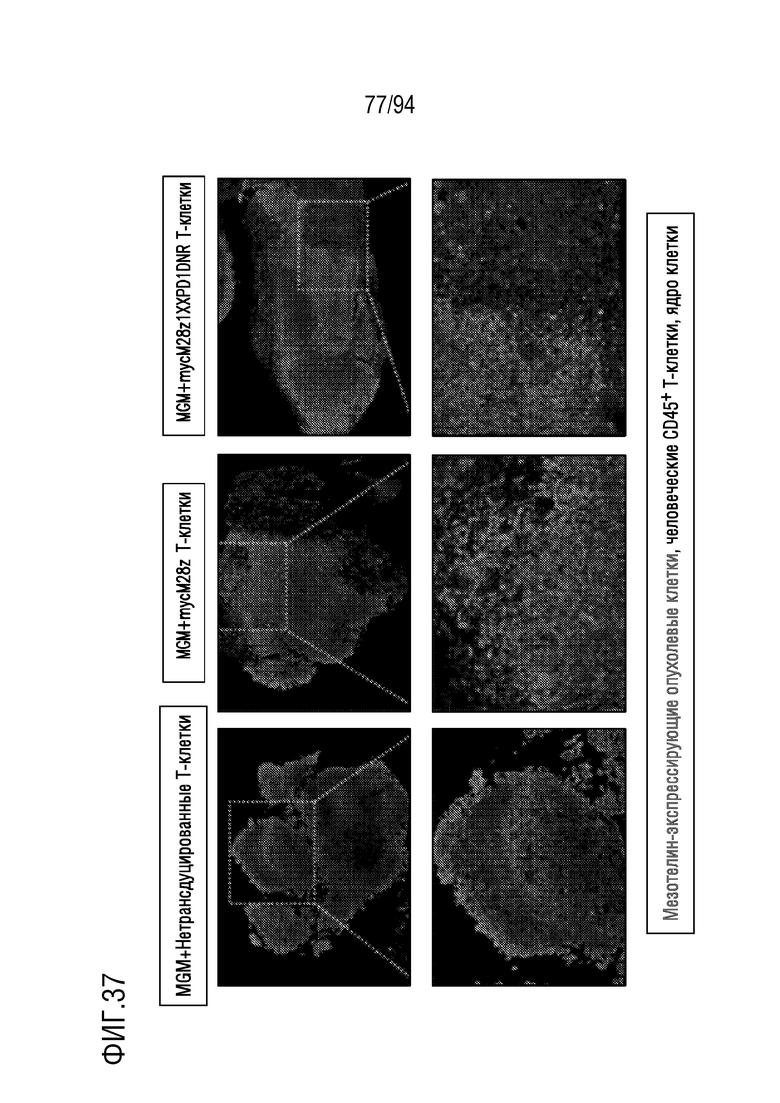
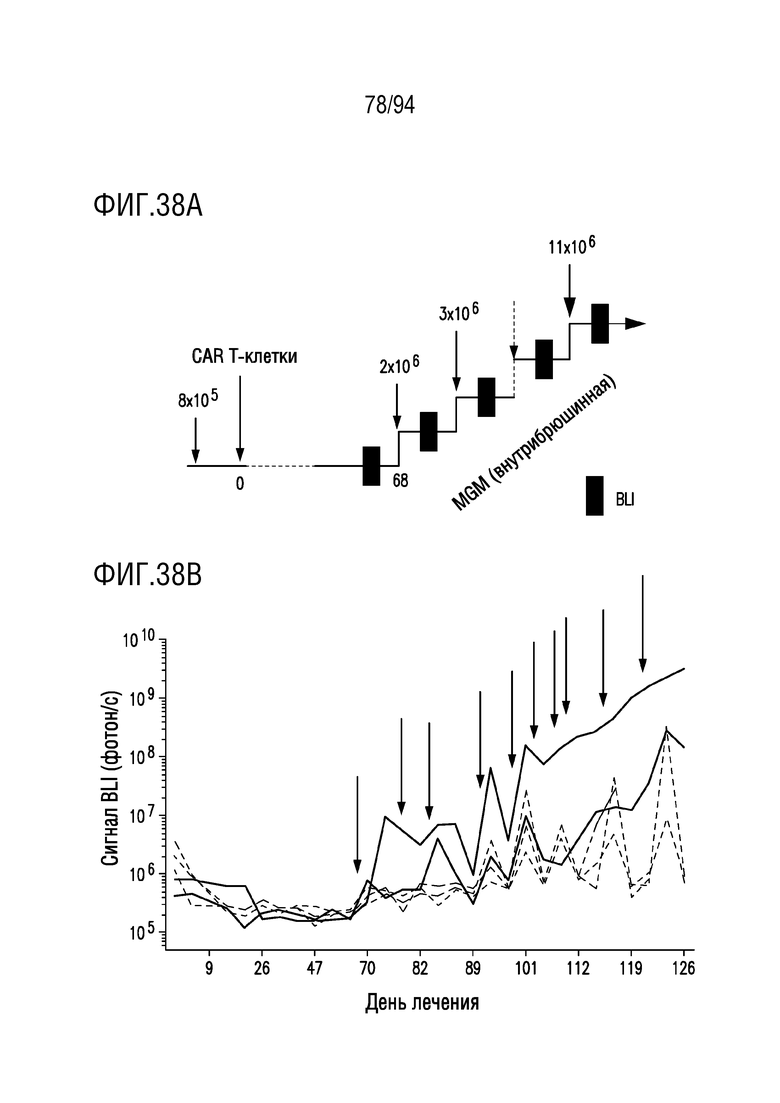
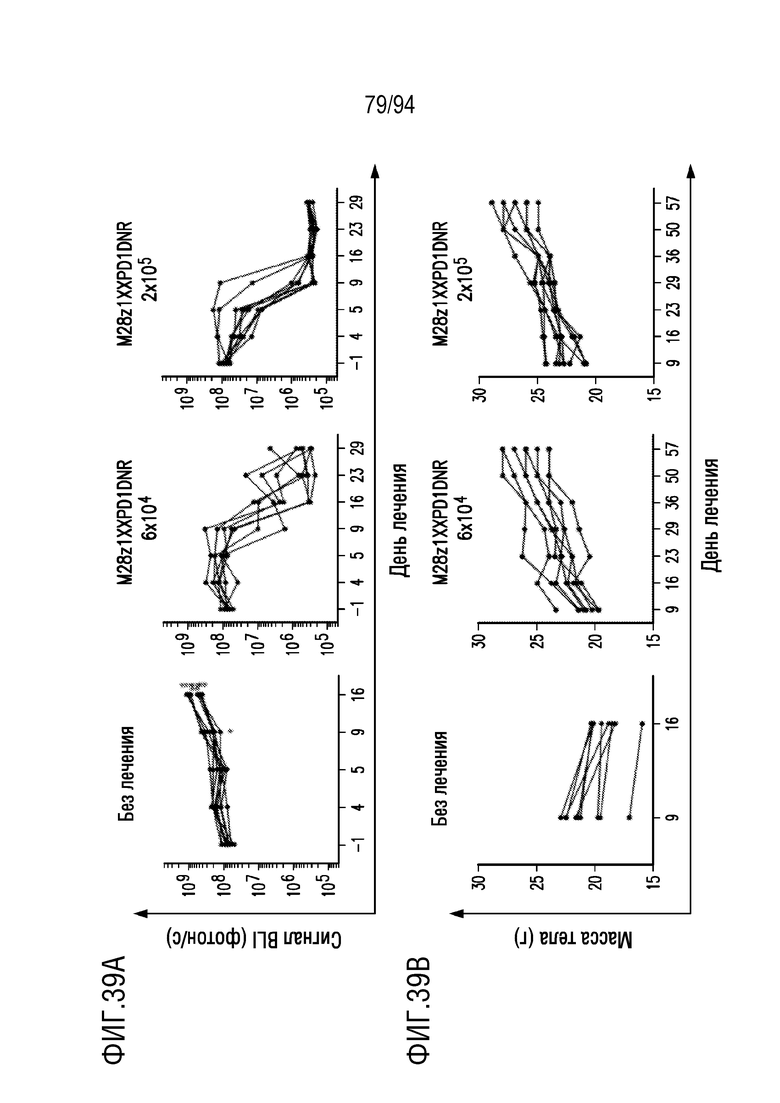
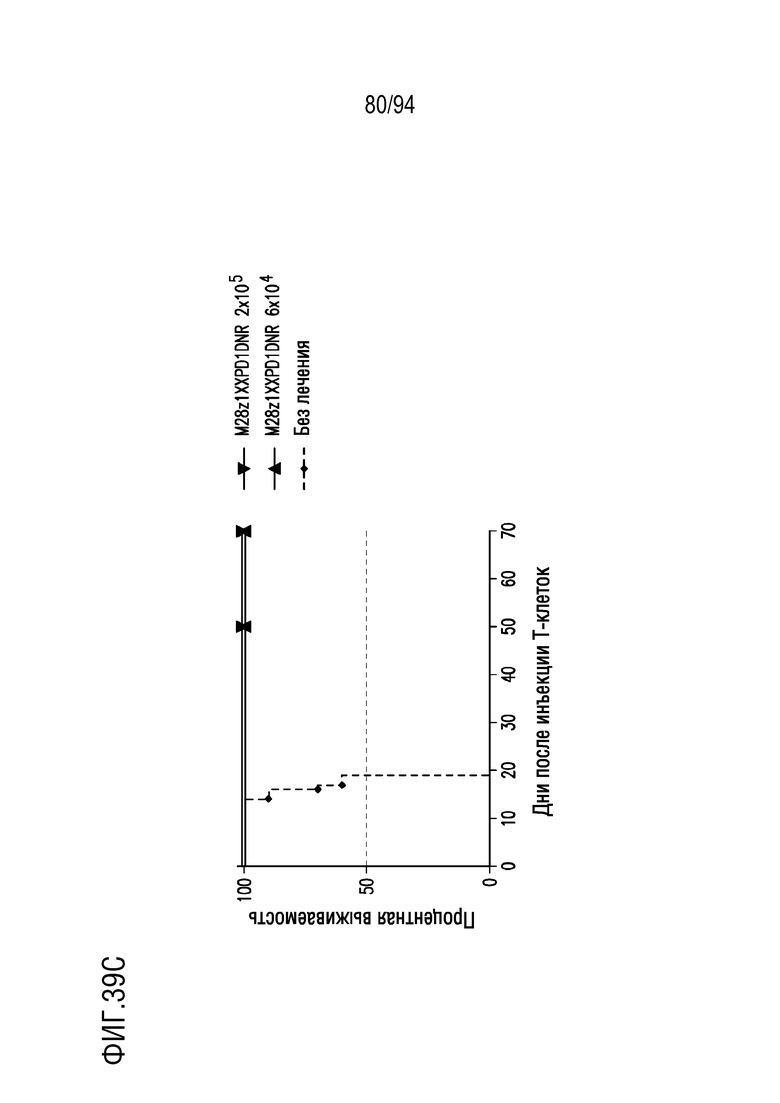
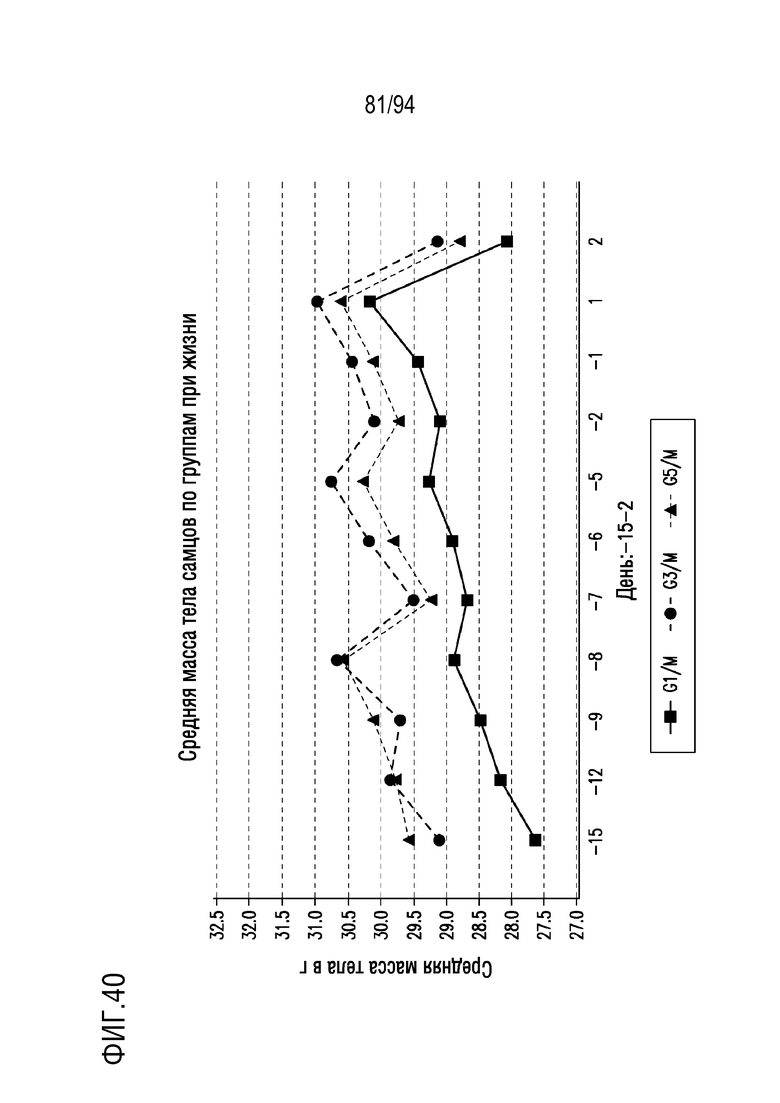
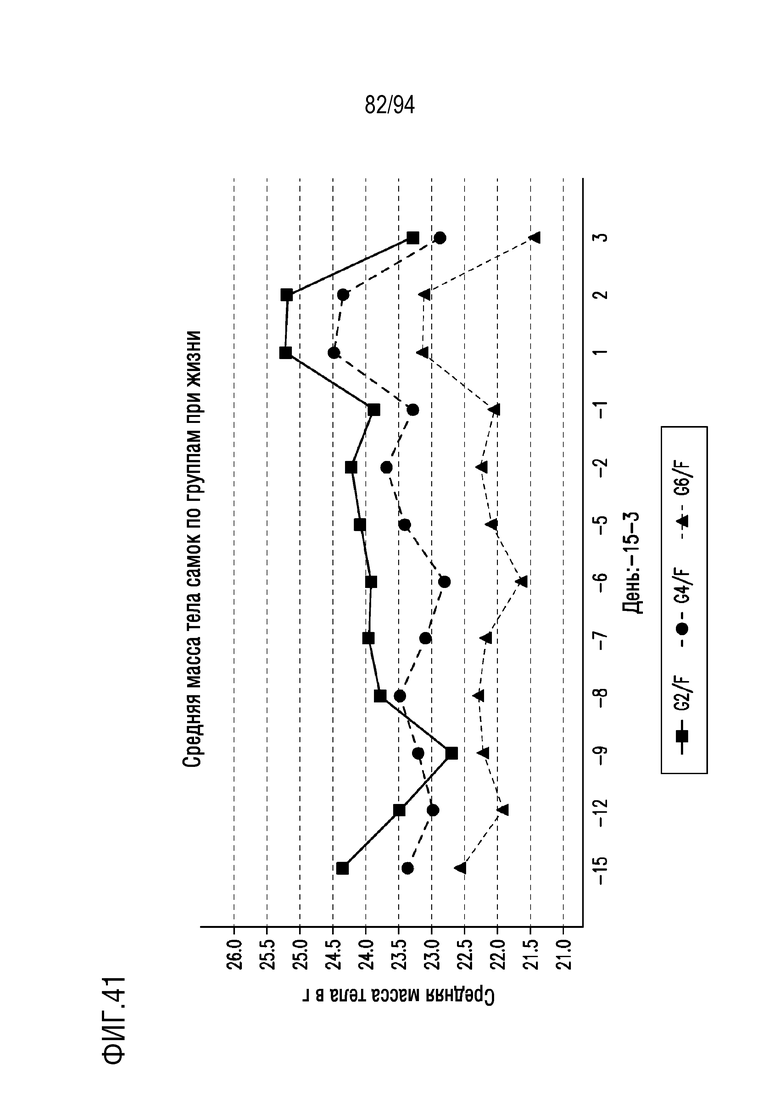
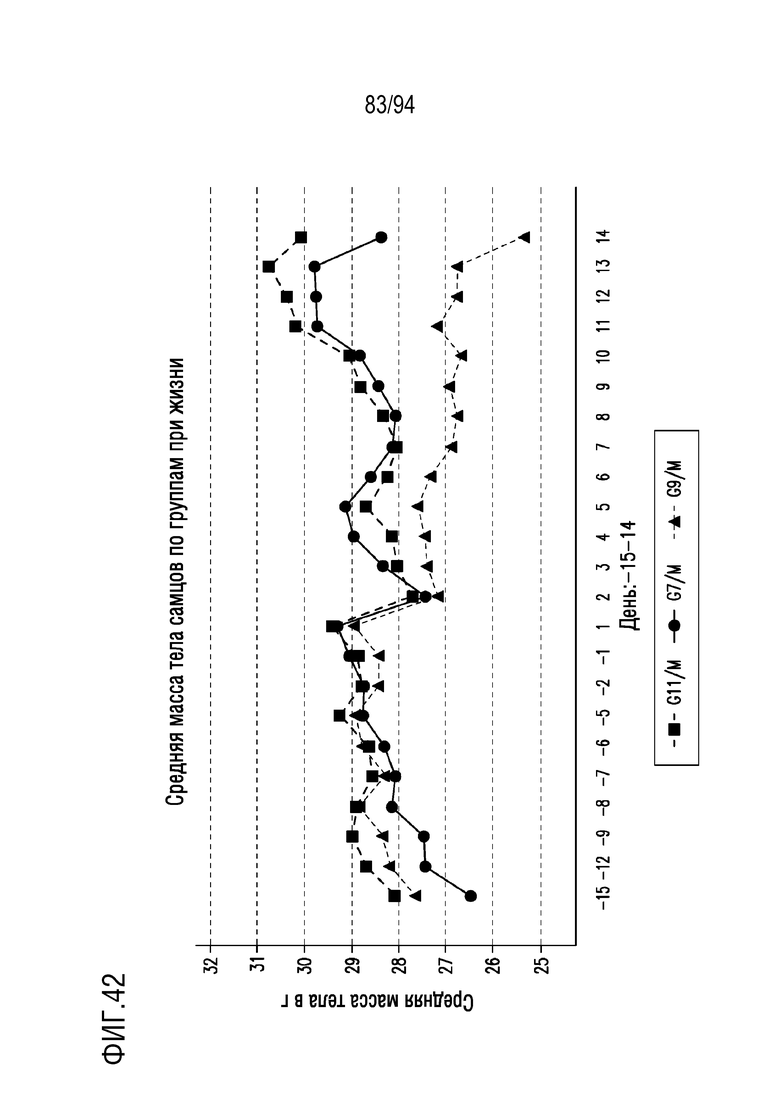
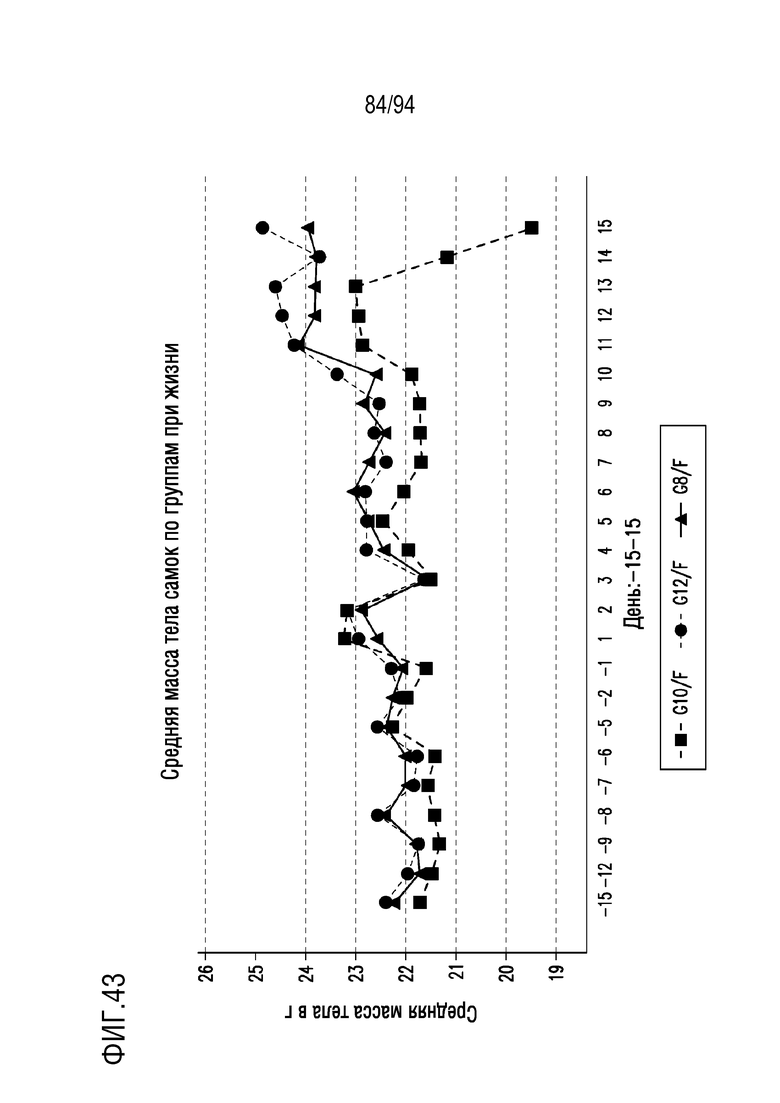
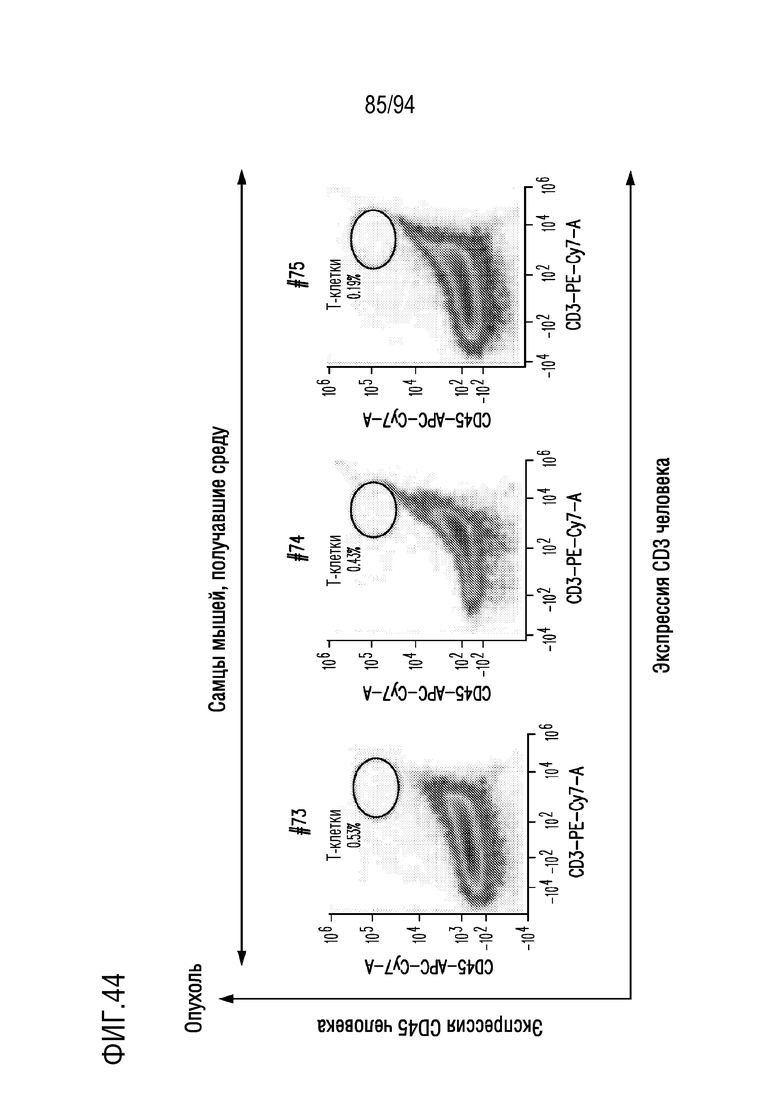
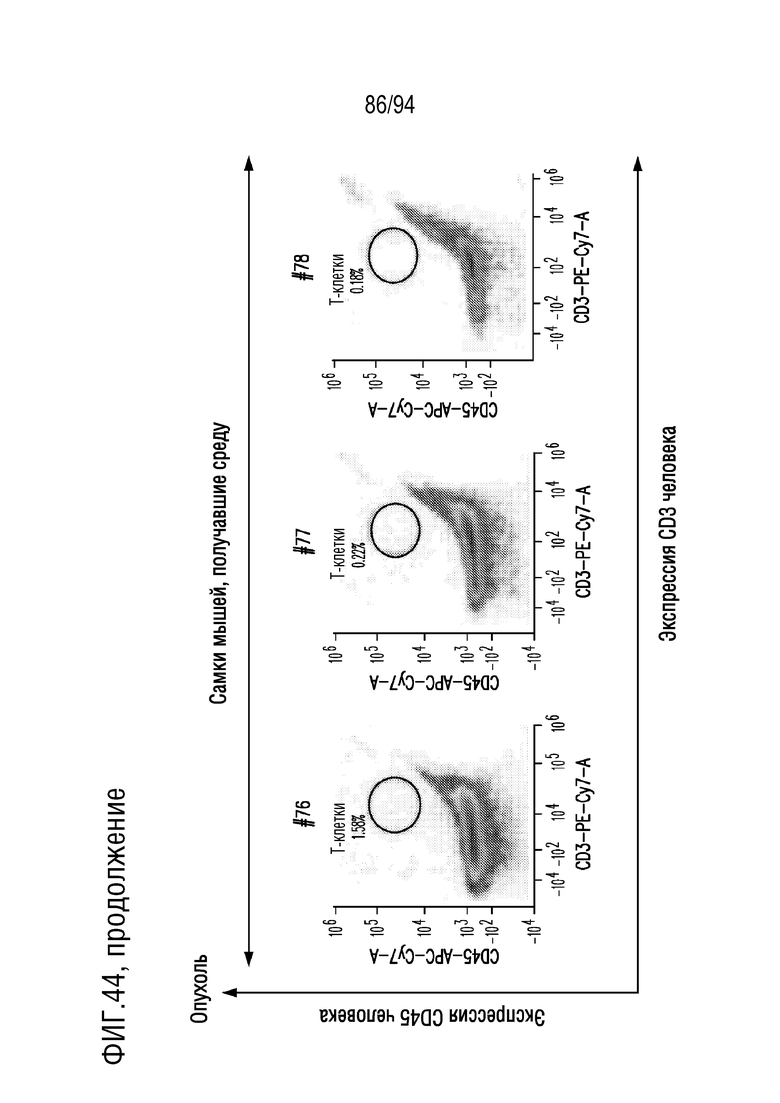
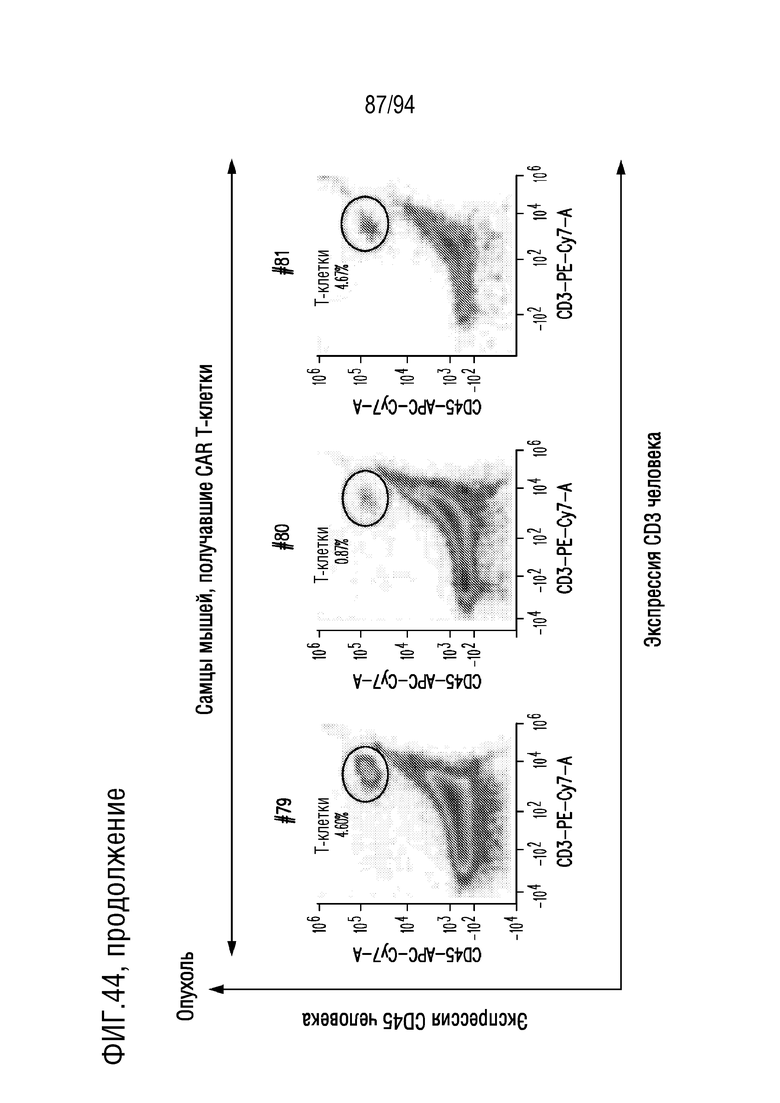
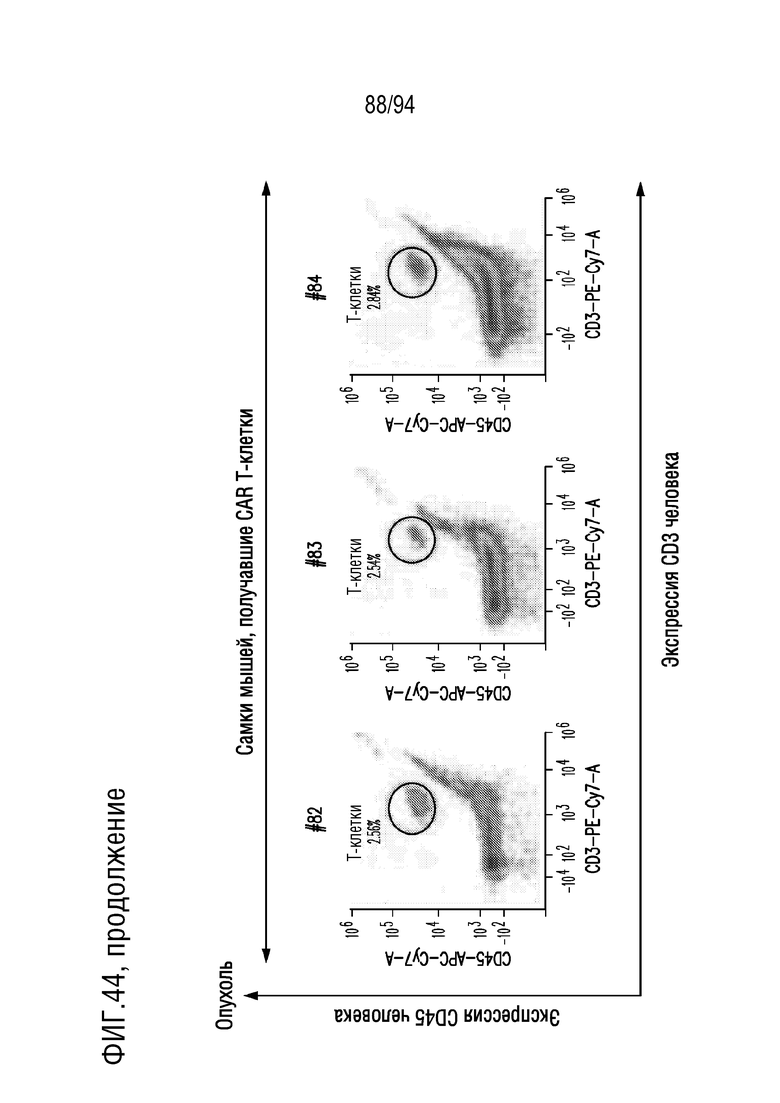

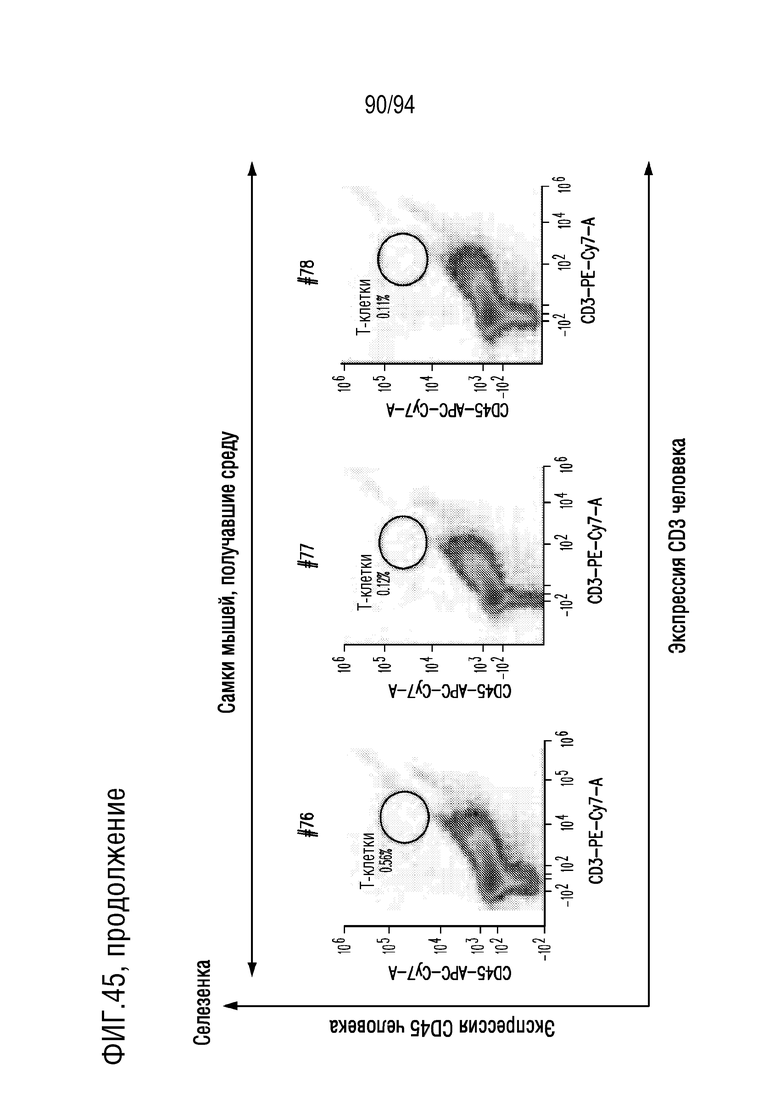
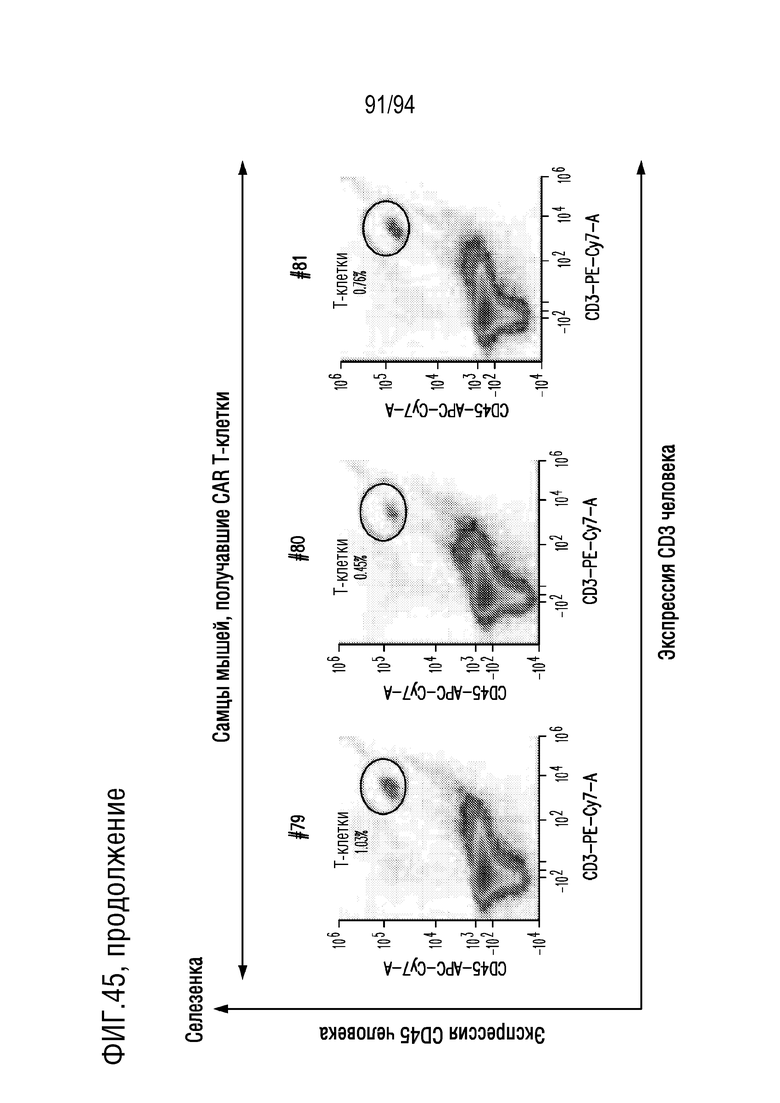
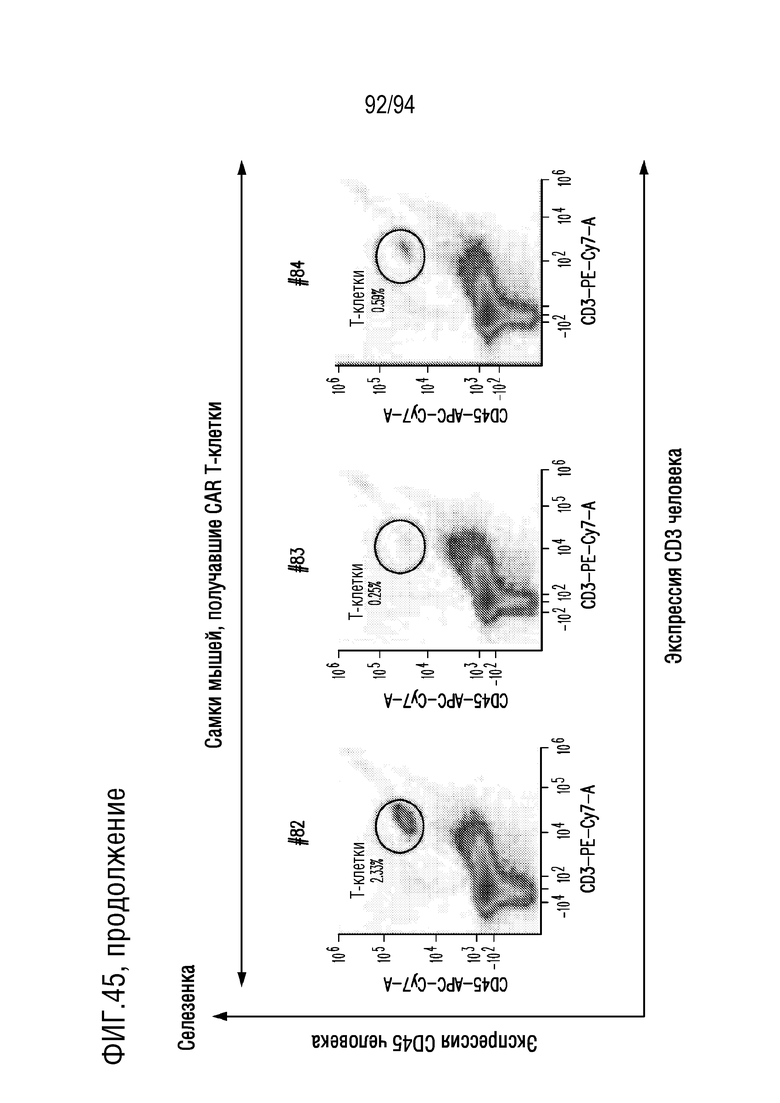
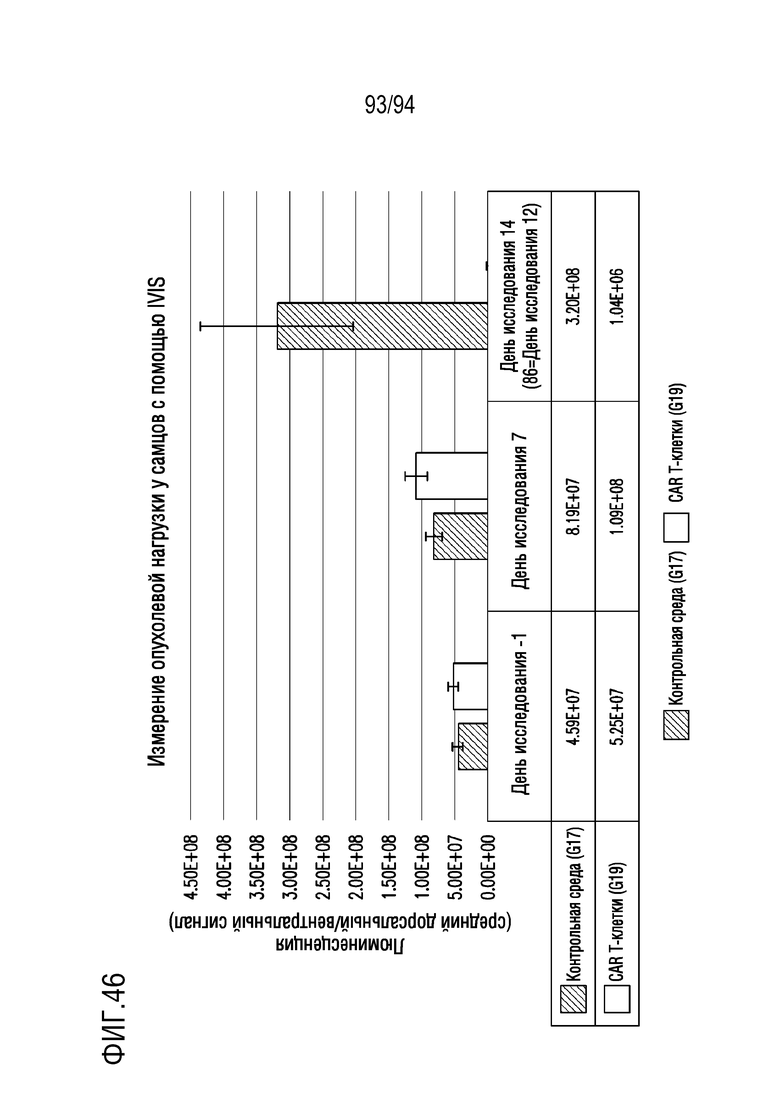
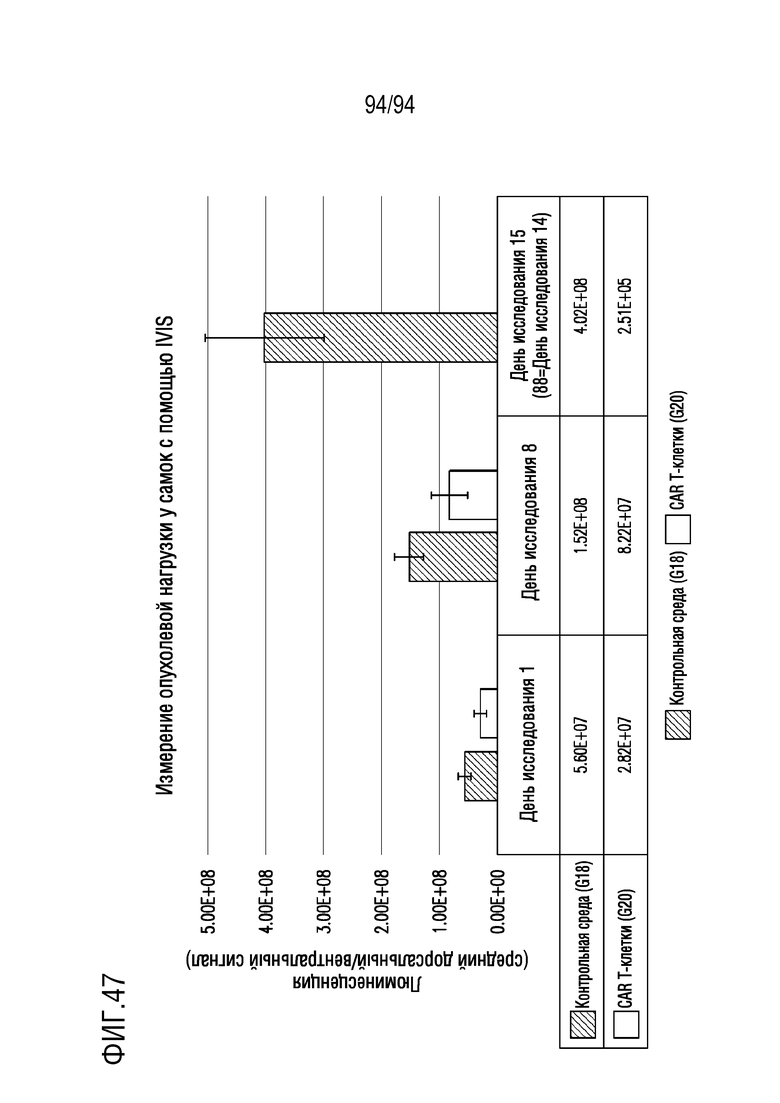
Группа изобретений относится к биотехнологии. Представлены: полипептидная композиция, специфично взаимодействующая с мезотелином человека, иммунореактивная клетка для усиления иммунного ответа в отношении рака и способ ее получения, фармацевтическая композиция для усиления иммунного ответа в отношении рака, композиция нуклеиновой кислоты для получения иммунореактивной клетки и экспрессионный вектор. Также раскрыты набор для усиления иммунного ответа в отношении рака, способ лечения неоплазии у субъекта и лечения субъекта, имеющего рецидив неоплазии, способ увеличения или продления выживаемости субъекта, имеющего неоплазию, способ снижения опухолевой нагрузки у субъекта, способ повышения продукции иммуноактивирующего цитокина в ответ на раковую клетку или патоген у субъекта, способ лечения воспалительного заболевания у субъекта и способ предотвращения отторжения трансплантата у субъекта. Изобретение применяется для усиления иммунного ответа в отношении рака, а также для повышения продукции иммуноактивирующего цитокина в ответ на раковую клетку или патоген у субъекта. 14 н. и 76 з.п. ф-лы, 13 табл., 94 ил., 6 пр.
1. Полипептидная композиция, специфично взаимодействующая с мезотелином человека, включающая:
i) химерный антигенный рецептор (CAR), включающий:
(a) внеклеточный антигенсвязывающий домен, включающий: вариабельную область тяжелой цепи, включающую CDR1, состоящую из аминокислотной последовательности, представленной в SEQ ID NO:76, CDR2, состоящую из аминокислотной последовательности, представленной в SEQ ID NO:77, и CDR3, состоящую из аминокислотной последовательности, представленной в SEQ ID NO:78; и вариабельную область легкой цепи, включающую CDR1, состоящую из аминокислотной последовательности, представленной в SEQ ID NO:79, CDR2, состоящую из аминокислотной последовательности, представленной в SEQ ID NO:80, и CDR3, состоящую из аминокислотной последовательности, представленной в SEQ ID NO:81,
(b) внутриклеточный сигнальный домен, включающий модифицированный полипептид CD3ζ, включающий вариант ITAM2, содержащий аминокислотную последовательность, представленную SEQ ID NO: 29, и вариант ITAM3, содержащий аминокислотную последовательность, представленную SEQ ID NO: 33; и
ii) доминантно-негативную форму белка программируемой смерти 1 (PD-1 DN), включающую:
(a) по меньшей мере часть внеклеточного домена белка программируемой смерти 1 (PD-1), включающую лигандсвязывающую область, и
(b) первый трансмембранный домен.
2. Полипептидная композиция по п.1, где внеклеточный антигенсвязывающий домен CAR специфично связывается с мезотелином человека со значением EC50 от приблизительно 1 нМ до приблизительно 25 нМ.
3. Полипептидная композиция по п.1 или 2, где внеклеточный антигенсвязывающий домен CAR включает одноцепочечный вариабельный фрагмент (scFv), Fab, который необязательно является сшитым, или F(ab)2.
4. Полипептидная композиция по п.3, где внеклеточный антигенсвязывающий домен CAR включает человеческий scFv.
5. Полипептидная композиция по любому из пп.1-4, где внеклеточный антигенсвязывающий домен CAR распознает человеческий мезотелин при уровне экспрессии мезотелина приблизительно 1000 или больше связывающих сайтов мезотелина/клетка.
6. Полипептидная композиция по любому из пп.1-5, где вариабельная область тяжелой цепи включает аминокислотную последовательность, которая по меньшей мере приблизительно на 80% гомологична или идентична аминокислотной последовательности, представленной в SEQ ID NO:82.
7. Полипептидная композиция по любому из пп.1-6, где вариабельная область тяжелой цепи включает аминокислотную последовательность, представленную в SEQ ID NO:82.
8. Полипептидная композиция по любому из пп.1-7, где вариабельная область легкой цепи, включающая аминокислотную последовательность, которая по меньшей мере приблизительно на 80% гомологична или идентична аминокислотной последовательности, представленной в SEQ ID NO:83.
9. Полипептидная композиция по любому из пп.1-8, где вариабельная область легкой цепи включает аминокислотную последовательность, представленную в SEQ ID NO: 83.
10. Полипептидная композиция по любому из пп.1-9, где вариабельная область тяжелой цепи включает аминокислотную последовательность, которая по меньшей мере приблизительно на 80% гомологична или идентична аминокислотной последовательности, представленной в SEQ ID NO:82, и вариабельная область легкой цепи включает аминокислотную последовательность, которая по меньшей мере приблизительно на 80% гомологична или идентична аминокислотной последовательности, представленной в SEQ ID NO: 83.
11. Полипептидная композиция по любому из пп.1-10, где вариабельная область тяжелой цепи включает аминокислотную последовательность, представленную в SEQ ID NO:82, и вариабельная область легкой цепи включает аминокислотную последовательность, представленную в SEQ ID NO: 83.
12. Полипептидная композиция по любому из пп.1-11, где внеклеточный антигенсвязывающий домен CAR включает линкер между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи.
13. Полипептидная композиция по любому из пп.1-12, где лидерная последовательность ковалентно связана с N-концом внеклеточного антигенсвязывающего домена.
14. Полипептидная композиция по п.13, где лидерная последовательность включает полипептид CD8.
15. Полипептидная композиция по п.14, где полипептид CD8 состоит из аминокислотной последовательности, представленной в SEQ ID NO: 71.
16. Полипептидная композиция по любому из пп.1-15, где по меньшей мере часть внеклеточного домена PD-1 включает аминокислоты 21-165 из SEQ ID NO: 48.
17. Полипептидная композиция по любому из пп.1-16, где первый трансмембранный домен PD-1 DN включает полипептид CD8, полипептид CD28, полипептид CD3ζ, полипептид CD4, полипептид 4-1BB, полипептид OX40, полипептид CD166, полипептид CD166, полипептид CD8a, полипептид CD8b, полипептид ICOS, полипептид ICAM-1, полипептид CTLA-4, полипептид CD27, пептид CD40/My88, пептид NKGD2 или их комбинацию.
18. Полипептидная композиция по п.17, где первый трансмембранный домен PD-1 DN включает полипептид CD8.
19. Полипептидная композиция по п.18, где полипептид CD8, содержащийся в первом трансмембранном домене PD-1 DN, включает аминокислоты 137-207 из SEQ ID NO: 86.
20. Полипептидная композиция по любому из пп.1-19, где PD-1 DN включает аминокислоты 21-165 из SEQ ID NO: 48 и аминокислоты 137-207 из SEQ ID NO: 86.
21. Полипептидная композиция по любому из пп.1-20, где каждая из двух мутаций с потерей функции происходит по остатку аминокислоты тирозина.
22. Полипептидная композиция по любому из пп.1-21, где вариант ITAM2 включает или состоит из аминокислотной последовательности, представленной в SEQ ID NO: 29.
23. Полипептидная композиция по любому из пп.1-22, где вариант ITAM3 включает или состоит из аминокислотной последовательности, представленной в SEQ ID NO: 33.
24. Полипептидная композиция по любому из пп.1-23, где модифицированный полипептид CD3ζ включает нативный ITAM1.
25. Полипептидная композиция по п.24, где нативный ITAM1 включает или состоит из аминокислотной последовательности, представленной в SEQ ID NO: 23.
26. Полипептидная композиция по любому из пп.1-25, где модифицированный полипептид CD3ζ включает или состоит из аминокислотной последовательности, представленной в SEQ ID NO: 35.
27. Полипептидная композиция по любому из пп.1-26, где PD-1 DN не содержит внутриклеточный домен.
28. Полипептидная композиция по любому из пп.1-27, где CAR дополнительно включает второй трансмембранный домен.
29. Полипептидная композиция по п.28, где второй трансмембранный домен CAR включает полипептид CD8, полипептид CD28, полипептид CD3ζ, полипептид CD4, полипептид 4-1BB, полипептид OX40, полипептид CD166, полипептид CD166, полипептид CD8a, полипептид CD8b, полипептид ICOS, полипептид ICAM-1, полипептид CTLA-4, полипептид CD27, пептид CD40/My88, пептид NKGD2 или их комбинацию.
30. Полипептидная композиция по п.28 или 29, где второй трансмембранный домен CAR включает полипептид CD28.
31. Полипептидная композиция по любому из пп.1-30, где внутриклеточный сигнальный домен CAR дополнительно включает костимулирующую сигнальную область.
32. Полипептидная композиция по п.31, где костимулирующая сигнальная область включает полипептид CD28, полипептид 4-1BB, полипептид OX40, полипептид ICOS, полипептид DAP-10, полипептид CD27, полипептид CD40/My88, полипептид NKGD2 или их комбинации.
33. Полипептидная композиция по п.31 или 32, где костимулирующая сигнальная область включает полипептид CD28.
34. Полипептидная композиция по любому из пп.1-33, где CAR включает аминокислотную последовательность, представленную в SEQ ID NO: 56.
35. Иммунореактивная клетка для усиления иммунного ответа в отношении рака, включающая полипептидную композицию по любому из пп.1-34, где иммунореактивную клетку выбирают из Т-клетки, естественной киллерной (NK) клетки или плюрипотентной стволовой клетки, из которой может дифференцироваться лимфоидная клетка.
36. Иммунореактивная клетка по п.35, где PD-1 DN и/или CAR экспрессируется рекомбинантно.
37. Иммунореактивная клетка по п.35 или 36, где PD-1 DN и/или CAR экспрессируется с вектора.
38. Иммунореактивная клетка по любому из пп.35-37, где иммунореактивная клетка выбрана из группы, состоящей из T-клетки, естественной киллерной (NK) клетки и плюрипотентной стволовой клетки, из которой могут дифференцироваться лимфоидные клетки.
39. Иммунореактивная клетка по п.38, где иммунореактивная клетка является T-клеткой.
40. Иммунореактивная клетка по п.39, где T-клетка выбрана из группы, состоящей из цитотоксического T-лимфоцита (CTL), регуляторной T-клетки и естественной киллерной Т (NKT) клетки.
41. Иммунореактивная клетка по п.38, где плюрипотентная стволовая клетка является эмбриональной стволовой клеткой или индуцированной плюрипотентной стволовой клеткой.
42. Иммунореактивная клетка по любому из пп.35-41, где иммунореактивная клетка является аутологичной.
43. Иммунореактивная клетка по любому из пп.35-41, где иммунореактивная клетка является аллогенной.
44. Фармацевтическая композиция для усиления иммунного ответа в отношении рака, включающая эффективное количество иммунореактивной клетки по любому из пп.35-43 и фармацевтически приемлемое вспомогательное вещество.
45. Фармацевтическая композиция по п.44, включающая приблизительно от 104 до 106 иммунореактивных клеток.
46. Фармацевтическая композиция по п.44 или 45, включающая по меньшей мере приблизительно 105 иммунореактивных клеток.
47. Фармацевтическая композиция по любому из пп.44-46, включающая приблизительно 105 иммунореактивных клеток.
48. Фармацевтическая композиция по любому из пп.44-47, которая предназначена для лечения неоплазии у субъекта, лечения субъекта, имеющего рецидив неоплазии, снижения опухолевой нагрузки у субъекта, увеличения или продления выживаемости субъекта, имеющего неоплазию, лечения воспалительного заболевания у субъекта, и/или предотвращения отторжения трансплантата у субъекта, который является реципиентом трансплантата органа.
49. Композиция нуклеиновой кислоты для получения иммунореактивной клетки, включающая полинуклеотид, кодирующий полипептид, содержащий
i) химерный антигенный рецептор (CAR), включающий:
a) внеклеточный антигенсвязывающий домен, включающий: вариабельную область тяжелой цепи, включающую CDR1, состоящую из аминокислотной последовательности, представленной в SEQ ID NO:76, CDR2, состоящую из аминокислотной последовательности, представленной в SEQ ID NO:77, и CDR3, состоящую из аминокислотной последовательности, представленной в SEQ ID NO:78; и вариабельную область легкой цепи, включающую CDR1, состоящую из аминокислотной последовательности, представленной в SEQ ID NO:79, CDR2, состоящую из аминокислотной последовательности, представленной в SEQ ID NO:80, и CDR3, состоящую из аминокислотной последовательности, представленной в SEQ ID NO:81,
(b) внутриклеточный сигнальный домен, включающий модифицированный полипептид CD3ζ, включающий вариант ITAM2, содержащий аминокислотную последовательность, представленную SEQ ID NO: 29, и вариант ITAM3, содержащий аминокислотную последовательность, представленную SEQ ID NO: 33; и
ii) доминантно-негативную форму белка программируемой смерти 1 (PD-1 DN), включающую:
(a) по меньшей мере часть внеклеточного домена белка программируемой смерти 1 (PD-1), включающую лигандсвязывающую область, и
(b) первый трансмембранный домен.
50. Композиция нуклеиновой кислоты по п.49, где полинуклеотид включает нуклеотидную последовательность, представленную в SEQ ID NO: 123.
51. Композиция нуклеиновой кислоты по п.49, где полинуклеотид включает нуклеотидную последовательность, представленную в SEQ ID NO: 124.
52. Экспрессионный вектор для получения иммунореактивной клетки, включающий композицию нуклеиновой кислоты по любому из пп.49-51.
53. Вектор по п.52, который является ретровирусным вектором.
54. Вектор по п.53, где ретровирусный вектор является γ-ретровирусным вектором или лентивирусным вектором.
55. Способ получения иммунореактивной клетки, включающий введение в иммунореактивную клетку полипептидной композиции по любому из пп.1-34, композиции нуклеиновой кислоты по любому из пп.49-51 или вектора по любому из пп.52-54, где иммунореактивную клетку выбирают из Т-клетки, естественной киллерной (NK) клетки или плюрипотентной стволовой клетки, из которой может дифференцироваться лимфоидная клетка.
56. Набор для усиления иммунного ответа в отношении рака, включающий полипептидную композицию по любому из пп.1-34, композицию нуклеиновой кислоты по любому из пп.49-51, вектор по любому из пп.52-54, иммунореактивную клетку по любому из пп.35-43 или фармацевтическую композицию по любому из пп.44-48 и письменные инструкции.
57. Набор по п.56, где письменные инструкции включают письменные инструкции по лечению неоплазии у субъекта, лечению субъекта, имеющего рецидив неоплазии, снижению опухолевой нагрузки у субъекта, увеличению или продлению выживаемости субъекта, имеющего неоплазию, лечению воспалительного заболевания у субъекта, и/или предотвращению отторжения трансплантата у субъекта, который является реципиентом трансплантата органа.
58. Способ лечения неоплазии у субъекта, включающий введение субъекту эффективного количества иммунореактивных клеток по любому из пп.35-43 или фармацевтической композиции по любому из пп.44-48.
59. Способ снижения опухолевой нагрузки у субъекта, включающий введение субъекту эффективного количества иммунореактивных клеток по любому из пп.35-43 или фармацевтической композиции по любому из пп.44-48.
60. Способ по п.59, где способ уменьшает количество опухолевых клеток, уменьшает размер опухоли и/или устраняет опухоль у субъекта.
61. Способ по любому из пп.58-60, где неоплазия и/или опухоль является солидной опухолью.
62. Способ по п.61, где солидная опухоль выбрана из группы, состоящей из мезотелиомы, рака легкого, рака поджелудочной железы, рака яичника, рака молочной железы, рака толстой кишки, плевральной опухоли, глиобластомы, рака пищевода, рака желудка, синовиальной саркомы, карциномы тимуса, карциномы эндометрия, рака желудка, холангиокарциномы и их комбинации.
63. Способ лечения субъекта, имеющего рецидив неоплазии, включающий введение субъекту эффективного количества иммунореактивных клеток по любому из пп.35-43 или фармацевтической композиции по любому из пп.44-48.
64. Способ по п.63, где субъект получал иммунотерапию до указанного введения иммунореактивных клеток или композиции.
65. Способ увеличения или продления выживаемости субъекта, имеющего неоплазию, включающий введение субъекту эффективного количества иммунореактивных клеток по любому из пп.35-43 или фармацевтической композиции по любому из пп.44-48.
66. Способ повышения продукции иммуноактивирующего цитокина в ответ на раковую клетку или патоген у субъекта, где способ включает введение субъекту эффективного количества иммунореактивных клеток по любому из пп.35-43 или фармацевтической композиции по любому из пп.44-48.
67. Способ по п.66, где иммуноактивирующий цитокин выбран из группы, состоящей из гранулоцитарно-макрофагального колониестимулирующего фактора (ГМ-КСФ), IFN-α, IFN-β, IFN-γ, ФНО-α, IL-2, IL-3, IL-6, IL-11, IL-7, IL-12, IL-15, IL-21, регуляторного фактора интерферона 7 (IRF7) и их комбинаций.
68. Способ по любому из пп.58-67, дополнительно включающий введение по меньшей мере одного иммуномодулирующего средства.
69. Способ по п.68, где по меньшей мере одно иммуномодулирующее средство выбрано из группы, состоящей из иммуностимулирующих средств, блокаторов иммунных контрольных точек, радиотерапевтических средств, химиотерапевтических средств и их комбинаций.
70. Способ по п.69, где иммуностимулирующее средство выбрано из группы, состоящей из IL-12, агонистического костимулирующего моноклонального антитела и их комбинаций.
71. Способ по п.70, где иммуностимулирующим средством является IL-12.
72. Способ по п.69, где агонистическое костимулирующее моноклональное антитело выбрано из группы, состоящей из антитела против 4-1BB, антитела против OX40, антитела против ICOS и их комбинаций.
73. Способ по п.72, где агонистическое костимулирующее моноклональное антитело является антителом против 4-1BB.
74. Способ по п.69, где блокаторы иммунных контрольных точек выбраны из группы, состоящей из антител против PD-L1, антител против CTLA-4, антител против PD-1, антител против LAG3, антител против B7-H3, антител против TIM3 и их комбинаций.
75. Способ по п.74, где блокатор иммунной контрольной точки является антителом против PD-L1 или антителом против PD-1.
76. Способ по любому из пп.58-75, где субъектом является человек.
77. Способ по любому из пп.58-75, где иммунореактивную клетку плеврально или внутриплеврально вводят субъекту.
78. Способ лечения воспалительного заболевания у субъекта, включающий введение субъекту иммунореактивных клеток по любому из пп.35-43 или фармацевтической композиции по любому из пп.44-48.
79. Способ по п.78, где иммунореактивная клетка является иммуноингибирующей клеткой.
80. Способ по п.79, где иммуноингибирующая клетка является регуляторной T-клеткой.
81. Способ по любому из пп.78-80, где воспалительным заболеванием является панкреатит.
82. Способ по любому из пп.78-81, где субъектом является человек.
83. Способ по любому из пп.78-82, где субъектом является реципиент трансплантата органа.
84. Способ по любому из пп.78-83, где субъектом является реципиент трансплантата поджелудочной железы.
85. Способ предотвращения отторжения трансплантата у субъекта, который является реципиентом трансплантата органа, включающий введение субъекту иммунореактивных клеток по любому из пп.35-43 или фармацевтической композиции по любому из пп.44-48.
86. Способ по п.85, где иммунореактивная клетка является иммуноингибирующей клеткой.
87. Способ по п.86, где иммуноингибирующая клетка является регуляторной T-клеткой.
88. Способ по любому из пп.85-87, где субъектом является человек.
89. Способ по любому из пп.85-88, где субъектом является реципиент трансплантата поджелудочной железы.
90. Иммунореактивные клетки по любому из пп.35-43 или фармацевтическая композиции по любому из пп.44-48 для применения при лечении неоплазии у субъекта, лечении субъекта, имеющего рецидив неоплазии, снижении опухолевой нагрузки у субъекта, увеличении или продлении выживаемости субъекта, имеющего неоплазию, лечении воспалительного заболевания у субъекта и/или предотвращении отторжения трансплантата у субъекта, который является реципиентом трансплантата органа.
| WO 2018044866 A1, 08.03.2018 | |||
| US 20180251546 A1, 06.09.2018 | |||
| WO 2018132506 A1, 19.07.2018 | |||
| WO 2018144535 A1, 09.08.2018 | |||
| Способ получения цианистых соединений | 1924 |
|
SU2018A1 |
| ИММУНОГЕННАЯ КОМПОЗИЦИЯ ПРЕЗЕНТАЦИИ МНОЖЕСТВЕННЫХ АНТИГЕНОВ, ОТНОСЯЩИЕСЯ К НЕЙ СПОСОБЫ И ПРИМЕНЕНИЯ | 2012 |
|
RU2619176C2 |
Авторы
Даты
2024-07-03—Публикация
2020-05-18—Подача