Изобретение относится к области биотехнологии и производству вакцин против парвовирусного энтерита собак, а именно к способу опосредованного определения концентрации вирионов возбудителя парвовирусного энтерита собак в сырье для вакцин с помощью амплификации участка NS1-гена вирусной ДНК и формулы второй производной.
Парвовирус собак является важным высокоопасным патогеном для домашних собак и некоторых видов диких хищников, который у псов вызывает острый энтерит. Возбудитель данного заболевания - Canine parvovirus (CPV), который принадлежит к роду Protoparvovirus семейства Parvoviridae [1].
Геном CPV представлен двуцепочечной молекулой ДНК длиной около 4200-4300 п.н. Участок ДНК в диапазоне 1…2007 п.н. кодирует два неструктурных белка NS1 и NS2. Структурный белок VP1 кодируется участками в диапазонах 2014…2044 и 2117…2514 п.н., а VP2 – 2515…4269 п.н. [2].
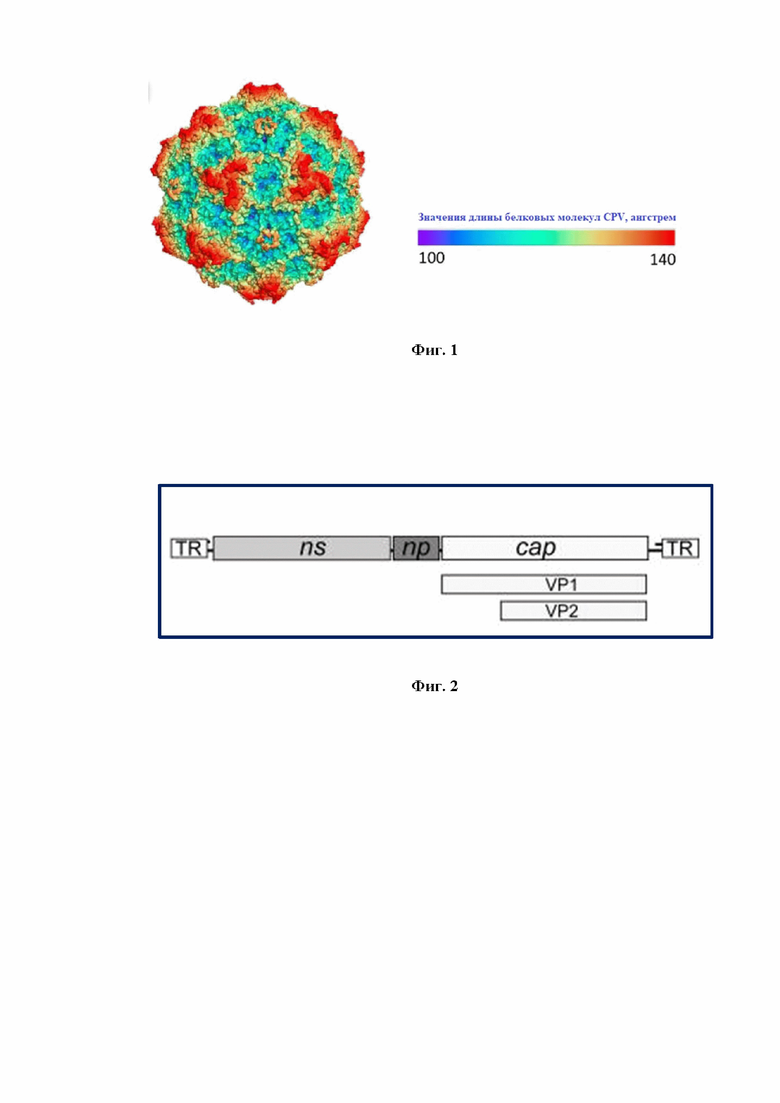
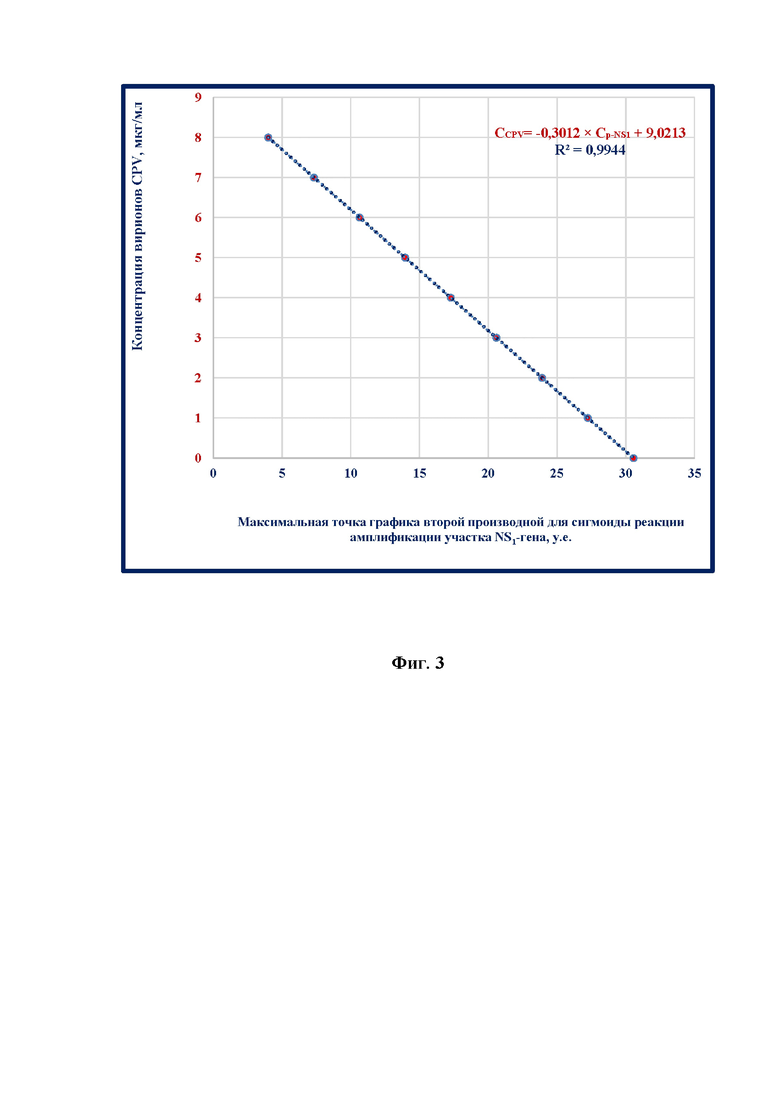
Вирионы парвовируса собак обладают небольшими капсидами без оболочки диаметром от 200 до 280 Å (фиг. 1) [3]. Их икосаэдрические капсиды собраны из 60 вирусных белков, кодируемых с правой стороны открытой рамки считывания (ORF) (фиг. 2). Данный ORF, также известный как cap-участок, кодирует два структурных вирусных белка, указанных выше, которые имеют общую C-концевую область [4]. Размер белка VP1 составляет 675 а.о. с молекулярным весом 77 кДа. Длина белка VP2 – 535 а.о., молекулярный вес – 60 кДа [5, 6].
В целях борьбы с парвовирусным энтеритом собак и его профилактики проводят иммунизацию домашних животных [7]. При изготовлении культуральных вакцин против данного заболевания вируссодержащее сырье до инактивации исследуют на определение концентрации важнейшего иммуногенного компонента вакцины – вирионов CPV (полных собранных вирусных частиц), каждый из которых содержит одну молекулу вирусной ДНК.
Как правило, для определения концентрации вирионов CPV применяют анализ на гемагглютинацию (HA). Данный метод является серологическим, количественным анализом вирусных частиц, основанным на их способности связываться с поверхностным рецептором эритроцитов и приводящий к агглютинации вируса. Тест проводят путем последовательного разбавления вирусной суспензии и титрования постоянным количеством эритроцитов [8]. Основным клеточным рецептором CPV является рецептор трансферрина, но он также обладает способностью гемагглютинировать эритроциты (прототип). Данный метод имеет некоторые недостатки: трудоемкость и продолжительность проводимого анализа (не менее 3 суток), невозможность одновременного исследования большого количества проб, достаточно высокая себестоимость процедуры, недостаточно высокая чувствительность метода.
В связи с этим целесообразно провести поиск альтернативного способа опосредованного определения концентрации вирионов возбудителя парвовирусного энтерита собак в сырье для вакцин.
В настоящее время развиваются методы молекулярной биологии, в частности, модифицированные варианты полимеразной цепной реакции (ПЦР) с использованием формул математического анализа результатов реакции амплификации, в частности, с применением второй производной. Предложенный метод является высокочувствительным и специфичным, объективным и позволяет определять концентрацию вирионов CPV в вируссодержащих суспензиях в течение 2 часов, что в 36 раз быстрее по сравнению с прототипным вариантом, снижает себестоимость процедуры в 7,804 раз (для НА – 2505 руб., для разработанного способа – 321 руб.), не требует отбора крови от барана для получения эритроцитов, качество которых напрямую зависит от состояния здоровья и самочувствия животного.
Задачей настоящего изобретения является разработка высокочувствительного, высокоспецифичного и быстрого способа опосредованного определения концентрации вирионов возбудителя парвовирусного энтерита собак в сырье для вакцин с целью устранения вышеуказанных недостатков.
Данная задача решена благодаря разработке способа опосредованного определения концентрации вирионов возбудителя парвовирусного энтерита собак в сырье для вакцин с помощью амплификации участка VP1-гена вирусной ДНК и формулы второй производной.
Технический результат изобретения заключается в том, что разработанный способ дает возможность: 1) повысить специфичность анализа проб за счет применения высокоспецифичных олигонуклеотидных праймеров, рассчитанных на участок VP1-гена ДНК CPV; 2) увеличить чувствительность анализа за счет применения молекулярного зонда, конъюгированного с красителем Cy5 и гасителем флуоресценции BHQ3;
3) повысить достоверность проводимого анализа благодаря установлению зависимости между концентрацией вирионов CPV (CCPV) и максимальной точки графика второй производной для сигмоиды реакции амплификации участка VP1-гена (Cp-VP1), представленной в виде математической функции:
CCPV = -0,3012 × Cp-NS1 + 9,0213
с высокой достоверностью аппроксимации (R2 = 0,9944) и эффективностью амплификации 99,74% (фиг. 3). Предложенная модель позволит опосредованно определять концентрацию вирионов возбудителя парвовирусного энтерита собак в сырье для вакцин с помощью амплификации участка NS1-гена вирусной ДНК.
Сущность изобретения отражена на графических изображениях:
Фиг. 1 – Модель строения вириона CPV, отражающая белковые молекулы разной длины (в ангстремах).
Фиг. 2 – Модель строения генома CPV, отражающая кодируемые вирусные белки.
Фиг. 3 – Зависимость концентрации вирионов CPV в сырье для вакцин и значений максимальной точки графика второй производной для сигмоиды реакции амплификации участка NS1-гена, представленной в виде логарифмической функции (n=3, p<0,005).
Фиг. 4 – Дизайн оригинальных олигонуклеотидных праймеров и зонда для опосредованного определения концентрации вирионов возбудителя парвовирусного энтерита собак в сырье для вакцин с помощью амплификации участка NS1-гена вирусной ДНК и формулы второй производной. Примечание: А – прямой праймер, Б – молекулярный зонд,
В - обратный праймер, который дан в двух вариантах, а именно, в комплементарном прямом и в формате rev/compl. – обратно-комплементарном; указаны производственные модельные штаммы CPV, с 36 иными изолятами и штаммами данного вируса получены аналогичные результаты.
Сущность изобретения пояснена в перечне последовательностей, в котором:
SEQ ID NO:1 представляет последовательность нуклеотидов гена, кодирующего неструктурные белки CPV;
SEQ ID NO:2 представляет последовательность аминокислот, соответствующих генам, кодирующих неструктурные белки CPV.
Сущность изобретения заключается в новом подходе по опосредованному определению концентрации вирионов CPV в неинактивированном сырье для вакцин с помощью амплификации участка NS1-гена вирусной ДНК и формулы второй производной. Заявляемый способ основан на получении элюата ДНК, проведении реакции амплификации участка NS1-гена вирусной ДНК и определения максимальной точки графика второй производной сигмоиды ПЦР для расчета по регрессионной формуле концентрации вирионов CPV в сырье для культуральных вакцин против парвовирусного энтерита собак.
В настоящее время применяется анализ на гемагглютинацию (прототип), ограничения применения которого в производственном процессе отражены выше. Для решения поставленной задачи способ опосредованного определения концентрации вирионов возбудителя парвовирусного энтерита собак в сырье для вакцин с помощью амплификации участка NS1-гена вирусной ДНК и формулы второй производной ранее не применялся и в литературе не представлен.
В отличие от прототипа разработанный способ включает этапы сорбционного экстрагирования ДНК, реакцию амплификации ДНК с применением оригинальных олигонуклеотидных праймеров и зондов; определение максимальных значений на графике второй производной функции сигмоиды ПЦР для расчета по математической формуле концентрации вирионов CPV в сырье для культуральных вакцин против парвовирусного энтерита собак.
Применение разработанного способа повышает достоверность анализа по определению концентрации вирионов CPV в пробах сырья для культуральных вакцин. Исходя из этого, актуально применять данный способ для опосредованного определения концентрации вирионов возбудителя парвовирусного энтерита собак в сырье для вакцин с помощью амплификации участка NS1-гена вирусной ДНК и формулы второй производной.
Ключевым элементом заявляемого способа является расчет максимальной точки графика второй производной функции сигмоиды по разработанной математической формуле концентрации вирионов CPV в сырье для культуральных вакцин против данного заболевания.
Сопоставительный анализ с прототипом позволяет сделать вывод, что новизна и изобретательский уровень заявляемого изобретения заключается в применении способа опосредованного определения концентрации вирионов возбудителя парвовирусного энтерита собак в сырье для вакцин с помощью амплификации участка NS1-гена вирусной ДНК и формулы второй производной.
На первом этапе исследования составляют контрольную панель готовых разведений стандарта с содержанием вирусной ДНК, эквивалентными следующим концентрациям вирионов CPV (положительные контроли): 0,01; 1,0; 2,0; 3,0; 4,0; 5,0; 6,0; 7,0; 8,0 мкг/мл. В рамках производственного технологического процесса наиболее часто получают суспензии с концентрациями вирионов CPV 1-3 мкг/мл.
На следующем этапе анализа осуществляют выделение ДНК из культуральных проб твердофазным сорбционным методом с применением набора «ДНК-сорб» («Интерлабсервис», РФ) в соответствии с инструкцией производителя.
После получения экстракта ДНК возбудителя парвовирусного энтерита собак проводят ПЦР в режиме реального времени с использованием специфических оригинальных олигонуклеотидных праймеров и зонда для исследования контрольных образцов и проб. Для постановки реакции готовят реакционную смесь, рецептура приготовления которой представлена в табл. 1. В качестве гомологичных NS1-гену возбудителя парвовирусного энтерита собак олигонуклеотидов используют:
CPV-Cvirus-F381-праймер (5'-AATGGAAAGGATGTTCGCTGG-3'),
CPV-Cvirus-R616-праймер (5'-TCCCCATTCATGTTGAATAAACC-3'),
CPV-Cvirus-P491-Cy5/BHQ3-зонд
(5'-Cy5- AATGGACTGGGAATCGGAAGTT-BHQ3-3')
в диапазоне 381…638 п.н. (фиг. 4) в концентрации 8 пМ на реакцию. Для формирования нуклеотидных цепей продуктов реакции применяют дезоксирибонуклеозидтрифосфаты с концентрацией каждого в реакционной смеси по 3,0 мМ. В реакционную смесь добавляют 3,0 мМ хлорида магния и диметилсульфооксид в количестве 2% от общего объема без элюата ДНК. В качестве катализатора реакции амплификации применяют Taq ДНК-полимеразу (2 е.а.).
Объем реакционной смеси компонентов для проведения одной реакции составляет 20 мкл. Элюаты ДНК каждого образца добавляют к смеси по 5 мкл. Общий объем смеси составляет 25 мкл.
Постановку реакции осуществляют при температурных и временных параметрах, сведения о которых представлены в табл. 2. Предварительную денатурацию комплементарной ДНК проводят при температуре 95°С за 2 мин в течение 1 цикла. Реакцию амплификации в режиме реального времени осуществляют в течение 40 циклов, каждый из которых складывается из 3 подэтапов: «денатурации», проводимой при температуре 98°С в течение 8 с, а также подэтапов «отжига праймеров и зонда» и «элонгации и аккумулирования флуоресцентного сигнала», осуществляемых при температуре 60°С за 30 с.
Результаты реакции анализируют, оценивая и сравнивая графики накопления флуоресцентного сигнала с помощью определения максимальной точки графика второй производной функции сигмоиды реакции амплификации участка NS1-гена CPV (Cp-NS1), определенных с помощью построения графика второй производной функции Fl = f х (Cp-NS1). Величина Cp является важной характеристикой реакции, она прямо пропорциональна количеству копий исходной вирусной ДНК и соответственно вирионов CPV в сырье для вакцин. Учитывая, что функция от двойного дифференциала f (Cp) (f ''(Cp)) непрерывна в некоторой окрестности точки Cp = Cp1 и задана на отрезке циклов амплификации от 0 до 40, существует определенный участок около точки Cp, для которого во всех координатах на оси О-Cp двойной математический дифференциал функции f (Cp) будет отрицательным. Поскольку f ''(Cp) является первым дифференциалом от функции f '(Cp), то из условия (f '(Cp))'<0, следует, что f '(Cp) на некотором малом отрезке, содержащем точку Cp = Cp1, будет убывающей. Учитывая, что f '(Cp)=0, на участке при Cp < Cp1 первый дифференциал функции f (Cp) >0, а при Cp > Cp1 получаем, что f '(Cp)<0. Иными словами, первый дифференциал функции f (Cp) при переходе через точку Cp = Cp1 изменяет знак с «+» на «-», следовательно, в точке Cp1 функция, отражающая процесс накопления флуоресцентного сигнала, имеет наибольшее значение [8-11]. Таким образом, если график реакции амплификации представлен функцией Fl = f х (Cp), f '(Cp) = 0 и f ''(Cp)<0, то при условии, что Cp = Cp1 полученная функция имеет наибольшее значение в точке с аргументом Cp1, значение которого учитывают для установления зависимости между концентрацией вирионов CPV в сырье для вакцин и значением Cp функции после проведения расчета максимального значения графика второй производной функции сигмоиды при амплификации участка NS1-гена ДНК возбудителя данного инфекционного заболевания.
Используемый в данном случае метод имеет преимущество в связи с тем, что при умножении кривой на любые множители положение наибольших значений функции не изменяется. Максимум на графике второй производной при его исследовании на максимумы располагается внутри экспоненциального участка сигмоиды, где эффективность реакции амплификации является константой. Наибольшие значения первого дифференциала находятся, чаще всего, в зоне искажения значений эффективности амплификации, поэтому их не рекомендуется использовать для анализа. Графики третьей производной дают менее точные результаты, поскольку их координаты во многом сопряжены с шумовыми значениями [11].
Вычислив значения Cp-NS1 для кривых, отражающих накопление флуоресцентного сигнала образцов с разными концентрациями вирионов возбудителя парвовирусного энтерита, устанавливают зависимость между концентрацией вирионов CPV в неинактивированном сырье для культуральных вакцин и значением точки Cp-NS1 после получения графика второй производной. На основе разработанной модели рассчитывают значение концентрации вирионов CPV в неинактивированном сырье для культуральных вакцин.
Сущность предлагаемого изобретения пояснена примерами его использования, которые не ограничивают объем изобретения.
Пример 1. Выявление существования зависимости между концентрацией вирионов возбудителя парвовирусного энтерита собак в неинактивированном сырье для вакцины и значением точки Cp-NS1
На первом этапе исследования применяли панель готовых разведений стандарта, в качестве которого использовали не инактивированную культуральную суспензию возбудителя парвовирусного энтерита собак с количествами вирусной ДНК, эквивалентными следующим концентрациям вирионов CPV (положительные контроли): 0,01; 1,0; 2,0; 3,0; 4,0; 5,0; 6,0; 7,0; 8,0 мкг/мл.
Проводили выделение ДНК из культуральных суспензий CPV твердофазным сорбционным методом в соответствии с процедурой, представленной выше.
Осуществляли постановку ПЦР в режиме реального времени с использованием разработанных специфичных оригинальных олигонуклеотидных праймеров и зонда для исследования контрольных образцов и проб (фиг. 4). Для проведения реакции составляли реакционную смесь, рецептура которой представлена выше.
Постановку реакции амплификации осуществляли, как описано выше. Результаты реакции анализировали, оценивая и сравнивая графики накопления флуоресцентного сигнала после определения значений точек Cp-NS1 на графиках второй производной функции сигмоиды реакции амплификации целевого участка NS1-гена.
Полученные данные анализировали с помощью программного обеспечения «Rotor-Gene FRT-Manager», которое позволяет строить графики накопления флуоресцентного сигнала в режиме реального времени на протяжении заданного количества циклов амплификации (С). Применяя технологии компьютерной программы «Maxima» (или аналога), проводили построение графиков после вычисления математического дифференциала второй степени для полученных элюатов ДНК CPV каждого разведения стандарта с определенными значениями концентрации вирионов CPV и рассчитывали средние значения Cp-NS1 с проекцией на ось абсцисс O-C (n=3). При исследовании отрицательного контроля накопления флуоресцентного сигнала не наблюдалось, что подтверждает отсутствие возбудителя парвовирусного энтерита собак в данном образце. В представленных исследованиях p-уровень значимости меньше 0,005, что подтверждает достоверность проводимых количественных исследований. Зависимость концентрации вирионов CPV и значений точек Cp-NS1 представлена на фиг. 3 и отражена в виде математической функции:
CCPV = -0,3012 × Cp-NS1 + 9,0213
с высокой достоверностью аппроксимации (R2 = 0,9944) и эффективностью амплификации 99,74%. Предложенная модель позволит опосредованно определять концентрацию вирионов возбудителя парвовирусного энтерита собак в сырье для вакцин с помощью амплификации участка NS1-гена вирусной ДНК.
Пример 2. Апробация способа опосредованного определения концентрации вирионов возбудителя парвовирусного энтерита собак в сырье для вакцины с помощью амплификации участка NS1-гена вирусной ДНК и формулы второй производной
В исследовании использовали 6 культуральных суспензий вируса CPV со следующими концентрациями вирионов: 1,05; 2,02; 1,89; 3,05; 0,89; 4,55 мкг/мл, соответственно (пробы № 1-6). В качестве положительного контроля применяли культуральную суспензию CPV с концентрацией вирионов 2,00 мкг/мл. В качестве отрицательных контролей применяли суспензию клеток CRFK, не контаминированную микроорганизмами. Испытуемые пробы и контрольные образцы исследовали в пяти повторностях. Этапы выделения ДНК, и постановку ПЦР в режиме реального времени проводили, как описано в примере 1.
Средние значения Cp-NS1 для проб № 1-6 составляли 24,90±0,01, 23,24±0,02, 23,68±0,02, 19,83±0,01, 27,00±0,01, 14,84±0,01 соответственно. Пользуясь разработанной регрессионной функцией, представленной выше, рассчитали средние значения концентрации вирионов CPV для проб № 1-6, которые составили 1,05; 2,02; 1,89; 3,05; 0,89; 4,55 мкг/мл, соответственно. Полученные значения соответствовали референтным данным. Для положительного контроля значение порогового цикла амплификации составило 23,31±0,01, что соответствовало концентрации вирионов CPV, равной 2,00 мкг/мл. Для отрицательных контролей экспоненциальные графики не были сформированы, что означало отсутствие возбудителя CPV в данных образцах. Таким образом, разработанный способ позволяет определять концентрацию вирионов CPV в неинактивированном сырье для культуральных вакцин.
Пример 3. Выявление степени достоверности опосредованного определения концентрации вирионов возбудителя парвовирусного энтерита собак в сырье для вакцин с помощью амплификации участка NS1-гена вирусной ДНК и формулы второй производной
Для анализа использовали 600 культуральных суспензий вируса возбудителя парвовирусного энтерита собак с концентрациями вирионов CPV от 0,01 до 8,00 мкг/мл. В качестве положительных и отрицательных контролей использовали те же образцы, которые представлены в примерах 1 и 2. Испытуемые пробы и контрольные образцы исследовали в трех повторностях. Этапы экстрагирования нуклеиновых кислот и проведение реакции амплификации в режиме реального времени осуществляли, как отражено в примере 1. Результаты анализа представлены в табл. 3.
Интерпретацию результатов проводили, пользуясь разработанной регрессионной функцией, с получением значений CCPV для каждой из 600 проб. Для положительного контроля значение порогового цикла амплификации составило 23,31±0,01, что соответствовало концентрации вирионов CPV, равной 2,00 мкг/мл. Для отрицательных контролей экспоненциальные графики не были сформированы, что означало отсутствие CPV в данных образцах.
Выявили, что данные, полученные с помощью разработанного способа, коррелировали с анализом на гемагглютинацию (HA) на 99,87-100,00% для 3,01-8,00 мкг/мл (n=120), на 99,15-100,00% для 1,01-3,00 мкг/мл (n=120), на 98,79-99,89% для 0,51-1,00 (n=120), на 98,02-99,15% для 0,11-0,50 мкг/мл (n=120), на 96,02-98,56% для 0,01-0,10 (n=120). Каждый из 600 образцов исследовали в 13 повторностях. Полученные результаты свидетельствовали о высокой степени точности разработанного способа. Аналитическая чувствительность разработанного способа составила не менее 0,10 мкг/мл с достоверностью не менее 98,02% (n=120, p<0,005). Таким образом, разработанный способ опосредованного определения концентрации вирионов возбудителя парвовирусного энтерита собак в сырье для вакцин с помощью амплификации участка NS1-гена вирусной ДНК и формулы второй производной является достоверным.
Пример 4. Исследование специфичности способа опосредованного определения концентрации вирионов возбудителя парвовирусного энтерита собак в сырье для вакцин с помощью амплификации участка NS1-гена вирусной ДНК и формулы второй производной
При оценке специфичности способа (предлагаемое изобретение) исследовали суспензии вирусов ящура, бешенства, коронавируса кошек, калицивируса кошек и чумы плотоядных животных. Количество инфекционных доз вирусов в суспензиях составлял не менее 6,0 lg ТЦД50/см3 и 6,0 lg ККИД50/см3. Исследования проводили в 5 повторностях.
Этапы элюирования нуклеиновых кислот и постановку ПЦР в режиме реального времени проводили, как описано в примере 1. Для проб, содержащих другие вирусы, не наблюдалось формирования графиков экспоненты, и они не выходили за пороговый уровень флуоресцентного сигнала (0,005 у.е.). Таким образом, разработанный способ является специфичным по отношению к возбудителю парвовирусного энтерита собак и может быть использован для определения концентрации вирионов CPV в неинактивированном сырье для культуральных вакцин.
Основным преимуществом предлагаемого изобретения является возможность опосредованно определить концентрацию вирионов CPV в неинактивированном сырье для культуральных вакцин. Предлагаемое изобретение предлагает сочетание молекулярно-биологического исследования неинактивированной вирусной суспензии возбудителя парвовирусного энтерита собак с методами математического анализа данных, что повышает точность, специфичность и чувствительность способа. В предлагаемом изобретении зависимость концентрации вирионов CPV и значений точек Cp-NS1 представлена в виде математической функции:
CCPV = -0,3012 × Cp-NS1 + 9,0213
с высокой достоверностью аппроксимации (R2 = 0,9944) и эффективностью амплификации 99,74%. Предложенная модель позволит опосредованно определять концентрацию вирионов возбудителя парвовирусного энтерита собак в сырье для вакцин с помощью амплификации участка NS1-гена вирусной ДНК.
Источники информации
1. Cotmore S.F., Agbandje-McKenna M., Canuti M., Chiorini J.A., Eis-Hubinger A.M., Hughes J., Mietzsch M., Modha S., Ogliastro M., Penzes J.J., et al. ICTV virus taxonomy profile: Parvoviridae. J. Gen. Virol. 2019; 100: 367–368.
2. Kang B.K., Song D.S., Lee C.S., Jung K.I., Park S.J., Kim E.M., Park B.K. Prevalence and genetic characterization of canine parvoviruses in Korea. Virus Genes. 2008; 36: 127–33.
3. Camacho C., Coulouris G., Avagyan V., Ma N., Papadopoulos J., Bealer K., Madden T.L. BLAST+: Architecture and applications. BMC Bioinform. 2009; 10: 421.
4. Kailasan S., Halder S., Gurda B., Bladek H., Chipman P.R., McKenna R., Brown K., Agbandje-McKenna M. Structure of an enteric pathogen, bovine parvovirus. J. Virol. 2015; 89: 2603–2614.
5. Meng G., Zhang X., Plevka P., Yu Q., Tijssen P., Rossmann M.G. The structure and host entry of an invertebrate parvovirus. J. Virol. 2013; 87: 12523–12530.
6. Decaro N., Buonavoglia C., Barrs V.R. Canine parvovirus vaccination and immunisation failures: Are we far from disease eradication? Vet Microbiol. 2020 Aug; 247: 108760.
7. Tuteja D., Banu K., Mondal B. Canine parvovirology - A brief updated review on structural biology, occurrence, pathogenesis, clinical diagnosis, treatment and prevention. Comp Immunol Microbiol Infect Dis. 2022 Feb 11; 82: 101765.
8. Sooknanan R., van Gemen B., Malek L. Nucleis acid sequence-based amplification // Molecular methods for virus deteCqion-London: Academic press, 1995. – P. 261-285.
9. Rutledge R.G. Mathematics of quantitative kinetic PCR and the application of standard curves / R.G. Rutledge, C. Cote // Nucleic Acide Res. – 2004. – V. 31, N. 16. – e. 93. P. 1-6.
10. Liu W., Saint D.A. Validation of a quantitative method for real-time PCR kinetics // Biochem. Biophys. Res. Commun. – 2002. – V. 294. – P. 347-353.
11. Peirson S.N., Butler J.M., Foster R.G. Experimantal validation of novel and conventional approaches to quantitative real-time PCR data analysis // Nucleic Acids Res. – 2003. – V. 31:e.73.
Таблица 1
Качественный и количественный состав реакционной смеси для определения концентрации вирионов CPV в сырье для вакцин (разработанный способ)
Milli Q
Примечание: объем реакционной смеси – 20 мкл,
объем вносимого элюата ДНК – 5 мкл,
общий объем mix – 25 мкл.
Таблица 2
Параметры режимов термоциклирования для проведения молекулярно-биологического анализа при определении концентрации вирионов CPV в сырье для вакцин (разработанный способ)
элонгация и аккумулирование флуоресцентного сигнала
Таблица 3
Достоверность способа опосредованного определения концентрации вирионов возбудителя парвовирусного энтерита собак в сырье для вакцин с помощью амплификации участка NS1-гена вирусной ДНК и формулы второй производной (разработанный способ)
(n=13)
--->
<?xml version="1.0" encoding="UTF-8"?>
<!DOCTYPE ST26SequenceListing PUBLIC "-//WIPO//DTD Sequence Listing
1.3//EN" "ST26SequenceListing_V1_3.dtd">
<ST26SequenceListing dtdVersion="V1_3" fileName="CPV-Cvirus.xml"
softwareName="WIPO Sequence" softwareVersion="2.1.2"
productionDate="2023-10-12">
<ApplicationIdentification>
<IPOfficeCode>RU</IPOfficeCode>
<ApplicationNumberText>0</ApplicationNumberText>
<FilingDate>2023-10-12</FilingDate>
</ApplicationIdentification>
<ApplicantFileReference>546</ApplicantFileReference>
<EarliestPriorityApplicationIdentification>
<IPOfficeCode>RU</IPOfficeCode>
<ApplicationNumberText>0</ApplicationNumberText>
<FilingDate>2023-10-12</FilingDate>
</EarliestPriorityApplicationIdentification>
<ApplicantName languageCode="ru">ФГБУ
"Федеральный центр охраны ЕдороРIСЊСЏ
жиРIотных" (ФГБУ
"Р’РќРРР—Р–")</ApplicantName>
<ApplicantNameLatin>FGBI "ARRIAH"</ApplicantNameLatin>
<InventorName languageCode="ru">Доронин Максим
РРіРѕСЂРµРIРёС‡</InventorName>
<InventorNameLatin>Doronin Maksim Igorevich </InventorNameLatin>
<InventionTitle languageCode="ru">РЎРїРѕСЃРѕР±
опосредоРIанного определения
концентрации РIРёСЂРёРѕРЅРѕРI РIоЕбудителя
парРIРѕРIРёСЂСѓСЃРЅРѕРіРѕ энтерита собак РI
сырье для РIакцин СЃ помощью
амплификации участка NS1-гена РIРёСЂСѓСЃРЅРѕР№
ДНК Рё формулы РIторой
РїСЂРѕРёР•РIРѕРґРЅРѕР№</InventionTitle>
<SequenceTotalQuantity>2</SequenceTotalQuantity>
<SequenceData sequenceIDNumber="1">
<INSDSeq>
<INSDSeq_length>2004</INSDSeq_length>
<INSDSeq_moltype>DNA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..2004</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>genomic DNA</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q1">
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>CPV </INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>atgtctggcaaccagtatactgaggaagttatggagggagtaaattggt
tgaagaaacatgcagaaaatgaagcattttcgtttgtttttaaatgtgacaacgtccaactaaatggaaa
ggatgttcgctggaacaactataccaaaccaattcaaaatgaagagctaacatctttagttagaggagca
caaacagcaatggatcaaaccgaagaagaagaaatggactgggaatcggaagttgatagtctcgccaaaa
agcaagtacaaacttttgatgcattaattaaaaaatgtctttttgaagtttttgtttctaaaaatataga
accaaatgaatgtgtttggtttattcaacatgaatggggaaaagatcaaggctggcattgtcatgtttta
cttcatagtaaaaacttacaacaagcaactggtaaatggctacgcagacaaatgaatatgtattggagta
gatggttggtgactctttgttcggtaaacttaacaccaactgaaaagattaagctcagagaaattgcaga
agatagtgaatgggtgactatattaacatacagacataagcaaacaaaaaaagactatgttaaaatggtt
cattttggaaatatgatagcatattactttttaacaaagaaaaaaattgtccacatgacaaaagaaagtg
gctattttttaagtactgattctggttggaaatttaactttatgaaatatcaagacagacaaattgtcag
cacactttacactgaacaaatgaaaccagaaaccgttgaaaccacagtgacgacagcacaggaaacaaag
cgcgggagaattcaaactaaaaaggaagtgtcaatcaaatgtactttgcgggacttggttagtaaaagag
taacatcacctgaagactggatgatgttacagccagatagttatattgaaatgatggcacaaccaggagg
tgaaaatcttttaaaaaatacacttgaaatttgtactttgactttagcaagaacaaaaacagcatttgaa
ttaatacttgaaaaagcagataatactaagctaactaactttgatcttgcaaattctagaacatgtcaaa
tttttagaatgcacggatggaattggattaaagtttgtcacgctatagcatgtgttttaaatagacaagg
tggtaaaagaaatacagttctttttcatggaccagcaagtacaggaaaatctatcattgctcaagccata
gcacaagctgtgggtaatgttggttgttataatgcagcaaatgtaaattttccatttaatgactgtacca
ataaaaatttaatttggattgaagaagctggtaactttggtcaacaagttaaccaatttaaagcaatctg
ttctggacaaacaattagaattgatcaaaaaggtaaaggaagtaagcaaattgaaccaactccagtaatt
atgacaactaatgaaaatataacaattgtgagaattggatgtgaagaaagacctgaacatacacaaccaa
taagagacagaatgttgaacattaagttagtatgtaagcttccaggagactttggtttggttgataaaga
agaatggcctttaatatgtgcatggttagttaagcatggttttgtatcaaccatggctaactatacacat
cactggggaaaagtaccagaatgggatgaaaactgggcggagcctaaaatacaagaaggtataaattcac
caggttgcaaagacttagagacacaagcggcaagcaatcctcagagtcaagaccaagttctaactcctct
gactccggacgtagtggaccttgcactggaaccgtggagtactccagatacgcctattgcagaaactgca
aatcaacaatcaaaccaacctggcgttactcacaaagacgtgcaagcgagtccaacgtggtccgaaatag
aggcagacctgagagccatctttacttctgaacaattggaagaagattttcgagacgacttggat</INS
DSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="2">
<INSDSeq>
<INSDSeq_length>668</INSDSeq_length>
<INSDSeq_moltype>AA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..668</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>protein</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q2">
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>CPV</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>MSGNQYTEEVMEGVNWLKKHAENEAFSFVFKCDNVQLNGKDVRWNNYTK
PIQNEELTSLVRGAQTAMDQTEEEEMDWESEVDSLAKKQVQTFDALIKKCLFEVFVSKNIEPNECVWFIQ
HEWGKDQGWHCHVLLHSKNLQQATGKWLRRQMNMYWSRWLVTLCSVNLTPTEKIKLREIAEDSEWVTILT
YRHKQTKKDYVKMVHFGNMIAYYFLTKKKIVHMTKESGYFLSTDSGWKFNFMKYQDRQIVSTLYTEQMKP
ETVETTVTTAQETKRGRIQTKKEVSIKCTLRDLVSKRVTSPEDWMMLQPDSYIEMMAQPGGENLLKNTLE
ICTLTLARTKTAFELILEKADNTKLTNFDLANSRTCQIFRMHGWNWIKVCHAIACVLNRQGGKRNTVLFH
GPASTGKSIIAQAIAQAVGNVGCYNAANVNFPFNDCTNKNLIWIEEAGNFGQQVNQFKAICSGQTIRIDQ
KGKGSKQIEPTPVIMTTNENITIVRIGCEERPEHTQPIRDRMLNIKLVCKLPGDFGLVDKEEWPLICAWL
VKHGFVSTMANYTHHWGKVPEWDENWAEPKIQEGINSPGCKDLETQAASNPQSQDQVLTPLTPDVVDLAL
EPWSTPDTPIAETANQQSNQPGVTHKDVQASPTWSEIEADLRAIFTSEQLEEDFRDDLD</INSDSeq_s
equence>
</INSDSeq>
</SequenceData>
</ST26SequenceListing>
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ опосредованного определения титра инфекционной активности вобудителя парвовирусного энтерита собак в сырье для вакцин методом ПЦР в режиме реального времени | 2023 |
|
RU2812858C1 |
| Способ опосредованного определения концентрации вирионов возбудителя чумы плотоядных животных в сырье для вакцин с помощью двойного математического дифференциала для точки crossing point сигмоиды при амплификации участка гена CDVgp1 | 2024 |
|
RU2840386C1 |
| Способ опосредованного определения титра инфекционной активности калицивируса кошек в неинактивированном сырье для культуральных вакцин с помощью количественного учета реакции амплификации участка ORF1-гена вирусной РНК | 2023 |
|
RU2821027C1 |
| Способ определения концентрации вирионов калицивируса кошек в сырье для цельновирионных вакцин | 2024 |
|
RU2838181C1 |
| Способ определения концентрации вирионов производственных штаммов возбудителя коронавирусной инфекции животных | 2024 |
|
RU2839298C1 |
| Способ дифференциации вакцинного штамма "Арчи" возбудителя парвовирусного энтерита собак от других штаммов и полевых изолятов ПВЭ собак с помощью высокочувствительного HRM-анализа с применением тандемного флуоресцирующего красителя SN v428 | 2024 |
|
RU2835907C1 |
| Способ опосредованного определения концентрации А-антигена производственного штамма «ВГНКИ» возбудителя инфекционного гепатита собак в сырье для культуральных вакцин по данным цикла количественной оценки при амплификации целевого участка orf25-гена | 2023 |
|
RU2823930C1 |
| Способ определения титра инфекционной активности возбудителя чумы плотоядных животных в сырье для изготовления культуральных инактивированных вакцин | 2024 |
|
RU2831062C1 |
| Способ генотипирования изолятов и штаммов возбудителя парвовирусного энтерита собак на основе филогенетического анализа с применением оригинальных олигонуклеотидных праймеров для высоковариабельного участка гена VP2 | 2023 |
|
RU2822036C1 |
| Способ опосредованного определения титра инфекционной активности возбудителя инфекционного ринотрахеита кошек в сырье для вакцины с помощью дифференциала второго порядка точки пересечения логистической кривой реакции амплификации участка UL35-гена | 2023 |
|
RU2823781C1 |


Изобретение относится к области биотехнологии. Описан способ опосредованного определения концентрации вирионов возбудителя парвовирусного энтерита собак в сырье для вакцин. Способ включает: выделение ДНК возбудителя парвовирусного энтерита собак твердофазным методом; проведение реакции амплификации в режиме реального времени с детекцией флуоресцентного сигнала сигмоид для исследуемых образцов c использованием олигонуклеотидов, рассчитанных на целевой участок NS1-гена возбудителя парвовирусного энтерита собак в диапазоне 381…638 п.н.; расчет максимума на графике второй производной функции сигмоиды для продуктов реакции амплификации; определение титра инфекционной активности возбудителя парвовирусного энтерита собак в сырье для вакцины на основе разработанной математической функции CCPV = -0,3012 × Cp-NS1 + 9,0213 с высокой достоверностью аппроксимации R2 = 0,9944 и эффективностью амплификации 99,74%. В изобретении установлена зависимость концентрации вирионов CPV и значений точек Cp-NS1 с высокой достоверностью аппроксимации (R2 = 0,9944) и эффективностью амплификации 99,74%, что позволяет опосредованно определять концентрацию вирионов возбудителя парвовирусного энтерита собак в сырье для вакцин с помощью амплификации участка NS1-гена вирусной ДНК. Основными преимуществами изобретения является возможность исключить вероятность контаминации в ходе реакции и субъективность при учете результатов анализа; возможность снизить время проведения анализа вируссодержащего сырья для вакцин до 2,0 ч; возможность увеличить специфичность и чувствительность анализа. 1 з.п. ф-лы, 4 ил., 3 табл., 4 пр.
1. Способ опосредованного определения концентрации вирионов возбудителя парвовирусного энтерита собак в сырье для вакцин, включающий следующие этапы:
- выделение ДНК возбудителя парвовирусного энтерита собак твердофазным методом;
- проведение реакции амплификации в режиме реального времени с детекцией флуоресцентного сигнала сигмоид для исследуемых образцов c использованием олигонуклеотидов, рассчитанных на целевой участок NS1-гена возбудителя парвовирусного энтерита собак в диапазоне 381…638 п.н.:
- CPV-Cvirus-F381-праймер
с дизайном 5'-AATGGAAAGGATGTTCGCTGG-3',
- CPV-Cvirus-R616-праймер
с дизайном 5'-TCCCCATTCATGTTGAATAAACC-3',
- CPV-Cvirus-P491-Cy5/BHQ3-зонд с дизайном
5'-Cy5- AATGGACTGGGAATCGGAAGTT-BHQ3-3';
- расчет максимума на графике второй производной функции сигмоиды для продуктов реакции амплификации;
- определение титра инфекционной активности возбудителя парвовирусного энтерита собак в сырье для вакцины на основе разработанной математической функции CCPV = -0,3012 × Cp-NS1 + 9,0213 с высокой достоверностью аппроксимации R2 = 0,9944 и эффективностью амплификации 99,74%.
2. Способ по п. 1, отличающийся тем, что время проведения анализа сокращается до 2,0 ч, аналитическая чувствительность составляет не менее 0,1 мкг/мл.
| Способ опосредованного определения концентрации рибонуклеопротеина вируса бешенства в сырье для вакцины при исследовании на максимальные экстремумы графиков второй производной для логических кривых реакции амплификации в режиме реального времени | 2021 |
|
RU2775745C1 |
| Способ опосредованного определения титра инфекционной активности вируса ящура в неинактивированном сырье для вакцин с помощью математического двойного дифференциала данных точки crossing point при амплификации вирусной кДНК | 2022 |
|
RU2793900C1 |
| WO 2022148755 A9, 14.07.2022. | |||
Авторы
Даты
2024-09-23—Публикация
2023-12-14—Подача