Изобретение относится к аналитической химии, в частности к способам определения, и может быть использовано при определении микроколичеств теллура в природных (речных, морских, минеральных), промьанленных и сточных водах, реактивах. Известен способ электрохимического определения теллура на твердых электродах. Теллур накапливают в результате катодного восстановления его до элементного состояния на золотом, платиновом или графитовом электродах в растворе хлористоводородной кислоты. Обязательным условием использования графитового электрода в известных методах является введение в анализируемый раствор ионов меди, золота, платины, палладия. В качестве источника информации используют анодные поляризационные кривые окисления осадка, образованного на электроде П. . Недостатком этого способа опреде ления теллура является использование дорогостоящего материала для электрода золото, платина . Если ж применяют графитовый электрод, то чувствительность теллура значительно уменьшается. Кроме того, такой способ требует отделения теллура от многих .элементов , В.ТОМ числе от ртути (11), так как ток окисления теллура находится в области потенциалов электрораство рения ртути. Наиболее близким техническим решением к предлагаемому является способ вольтамперометрического опре деления теллура, включающий концент рирование теллура (IV) на поверхности электрода в присутствии реаге та комплексообразователя в электролите с последующим превращением кон центрата С 2. Известный способ включает следую щие операции: создание рабочей поверхности электрода (ртутной каплиJ продувание анализируемого раствора током аргона или водорода (для удаления кислорода из раствора )) концентрирование теллура в элементном электроде из раствора 3 М нее или 2 М H2S04+ 1 М КЗ при разомкнутой цепи; промывание электрода с осажденным на его поверхнос ти теллуром (0); перенос электрода в другой раствор (1 М NaOHj, в кото ром производят электрохимическое определение теллура; электрохимическое определение теллура согласно реакции Те + 2 е, - Те Недостатком этого способа являет ся низкая чувствительность минимально определяемая концентрация составляет лишь t110 M Te(iy), так как степень концентрирования определяется равновесием окислительно-восстановительной реакции взаимодействия теллура (iv) со ртутью (О). Цель изобретения - повышение чувствительности определения. Поставленная цель достигается . тем, что согласно способу вольтамперометрического определения теллура, включающему концентрирование теллура (iv) на поверхности электрода в присутствии реагента комплексообразователя в электролите с последующим превращением концентрата, электролиз проводят в две стадии соответственно при потенциалах (-0,5 )- (-0,6) В и (-0,33) -(-0,35)В в электролите, содержащем (0,6-2,5)-10-Зм Hg(N03)2 (0,4-0,8)М КЛ , а электрохимическое превращение концентрата ведут при катодной поляризации электрода от (-0,33 ) -(-0,35) В, Предварительная обработка электрода при потенциале (-0,5 ) -(-0,6 ) В приводит к тому, что на поверхности графита осаждаются атомы ртути, необходимые для концентрирования теллура. Уменьшение концентрации иодида калия с 1 М до (0,4-0,8 ) М и кислотности раствора с 3 М до 1,5 М, введение дополнительно азотнокислой ртути (II) в количестве (0,62,5 ) 10 М, а также проведение электролиза два раза позволяет увеличить чувствительность определения теллура до- . Для выбора оптимальных концентраций выбранного состава раствора в данном способе проведены следующие исследования. Графитовый электрод поляризуют при потенциале предэлектролиза Ч в течение 1,5-2 мин в перемешиваемом растворе с целью осаждения атомов ртути на поверхности электрода. Затем, не прекращая перемешивание, проводят электролиз этого раствора при потенциале 2 течение определенного времени в зависимости от концентрации теллура (IV) в анализируемм растворе. Перемешивание выключают и регистрируют катодную поляризационную кривую с потенциала Ч до (-0,9 ) В со скоростью развертки 80 мВ/с. Используют среднее из 3-5 измерений значение аналитического сигнала. Необходимым условием получения сигнала теллура является наличие в растворе следующих компонентов: азотнокислой ртути (11J, иодида калия, хлористоводородной кислоты. Оптимальными условиями концентрирования и электрохимического определения теллура (IV) согласно полученным экспериментальным данным являются потенциал предэлектролиэа V;, (-0,5 Ь (-0,6 В, потенциал
электролиза 2 (-0,33 -(0,35) В, концентрация .хлористоводородной кислоты 1,5 М, кс нцентрация азотнокислой ртути (li; (0,б-2,5МОЗм, концентрация иодида калия (0,40,8 ) М. Аналитический сигнал эави- 5 сит от времени предэлектролиза при потенциале . (Ч . В дальнейшем для разных диапазонов концентраций теллура (ly) в анализируемом растворе используют время предэлектролиза Ю при потенциале Ч/, 2-5 мин.
Прямопропорциональная зависимость аналитического сигнала от концентрации теллура (IV) в растворе наблюается в диапазоне концентраций от 15 до 10 М.
Определению теллура (IV ) предлага-емым способом не мешает присутствие :ч растворе Со (II), Сг (VIJ, Сг (111), Se Ul-, Fe (Ш/, Fe (ll), jQ Zn (II), Ag {I ;, V (Y), Mg (11), Mn (II), Mo (VI), Ni (ll) , (1000:1), РЪ (II) , Cd Ul), (500:1 ).
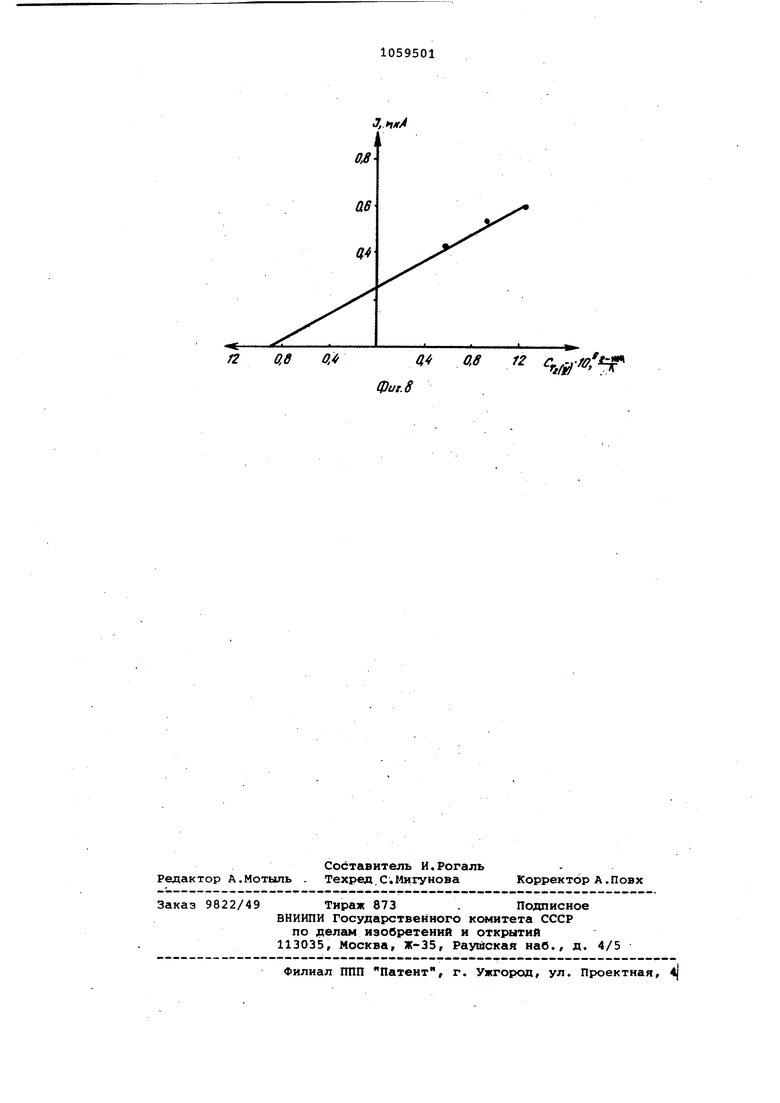
Предлагаемый способ концентрирования и электрохимического определе- jc ния теллура (IV) .благодаря низкому ределу обнаружения и высокой избирательности может быть полезен для анализа приводных вод. Возможности его проверены на примере определения концентрации теллура (IV) в питье- вых водах БАМа, нормируемых по санитарно-токсикологическому признаку вредности, а также в питьевой водопроводной воде г. Свердловска.
Пример. В лабораторных ус- 35 овиях приводят концентрирование и электрохимическое определ.ение телмура при исследовании воды г. Свердловска.
Для этого 5 мл исследуемой воды 40 омещают в электролизер. Добавляют 2,5 мл б М раствора хлористоводородной кислоты, в качестве реагента комплексообразователя берут 0,5 мл раствора Hg( концентрацией jc 10 г/л и 0,8мл8МКЗ, общий бъем пробы доводят до 10 мл водой, то соответствует концентрациям 1,2 10 М ртути (11) и 0,5 М K.J.
Электрод предварительно поляри- зуют при потенциале (-0,6 )В в теение 2 мин в анализируемом растворе/ а затем проводят концентрирование теллура при потенциаде (-0,33) (0,35 ) В в течение 10 мин в том же астворе при перемешивании. Выключа- 55 т перемешиватель и через 15 с регистрируют катодную поляризационную кривую при линейно изменяющемся во времени потенциале в интервале (-0,33 ) -(0,35 ) В, измеряя величину 60 аксимальному катодного тока, которая прямопропорциональна концентрации теллура в растворе.
Содержание теллура определяют етоде добавок или по градуировоч; 5
ному графику с учетом содержания теллура в реактивах. Концентрация теллура в анализируемой питьевой воде равна 9, г-ион/л.
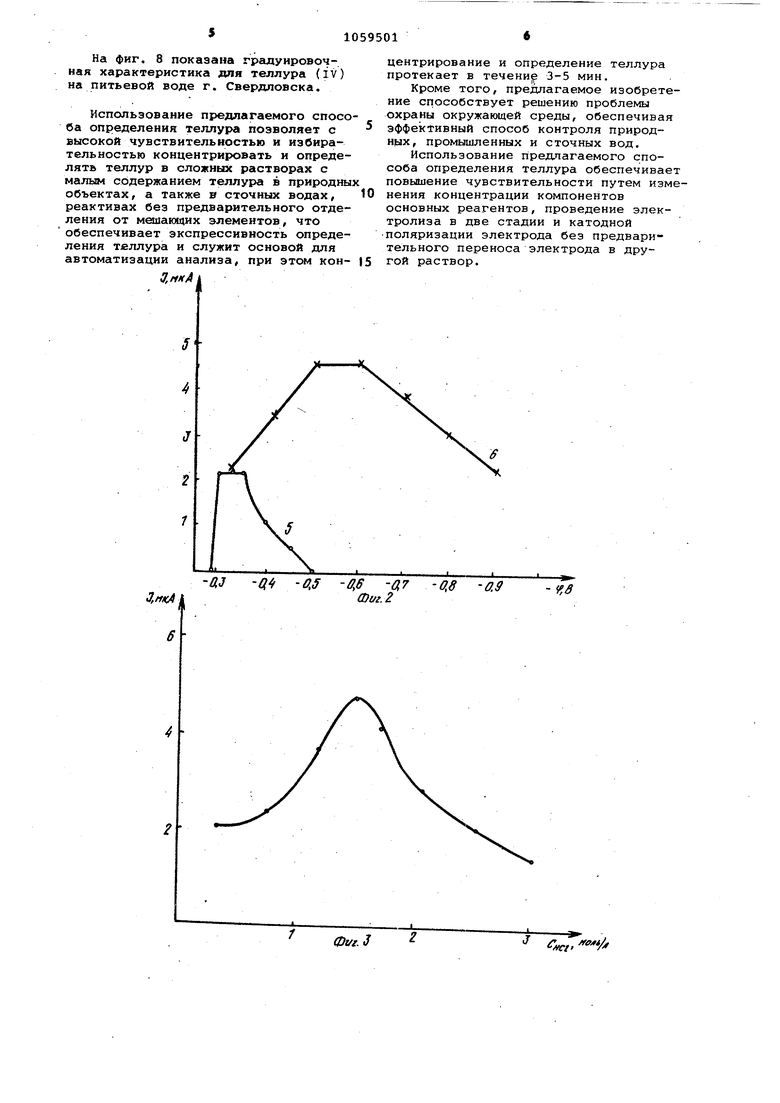
На фиг. 1 показаны поляризационные кривые, полученные в растворах.
Кривая 1 1,5 М НС1 +210вг-ио Те (rv), кривая 2 1,5 М НС1 + 2.-ю-вг-ион/л Те (IV) + 0,4 М КЗ ; кривая 3 1,5 М НС1 + 1,25-10 М Hg(N03)2 210 г-ион/л Те; кривая 4 1,5 М НС1 + 1,25-10 Зм Hg{N0,52+ 0,4 М K:J + 210 г-ион/л Те (IV).
Потенциал предэлектролиза f - 0,9 в; время предэлектролиза (И} 3 мин; потенциал концентрирования (2) - 0,35 BJ время электролиза (t) 3 мин.
На фиг. 2 показана зависимость вличины тока электровосстановления теллура от потенциала 2 %. растворе, содержащем 1,5 М Нс1 + 0,4 М. К D + 1,25«10М Hg(N03)2 + н- 2-10®г-ион/л Те (IV); 3 мин, Л 3 мий.
Кривая 5 Ч, -0,9; у X,
Кривая б Ч X, Ч, -О ,5 В.
Ra фиг. 3 показана зависимость величины тока электровосстановления теллура от концентрации хлористоводородной кислоты в растворе, содержщем 0,4 М К J + 1,25-10- М. Hg(NO-a) + 2-10 г-ион/л Те (IV):
% -0,5 в; % -0,35 в;
3 мин, 3 мин.
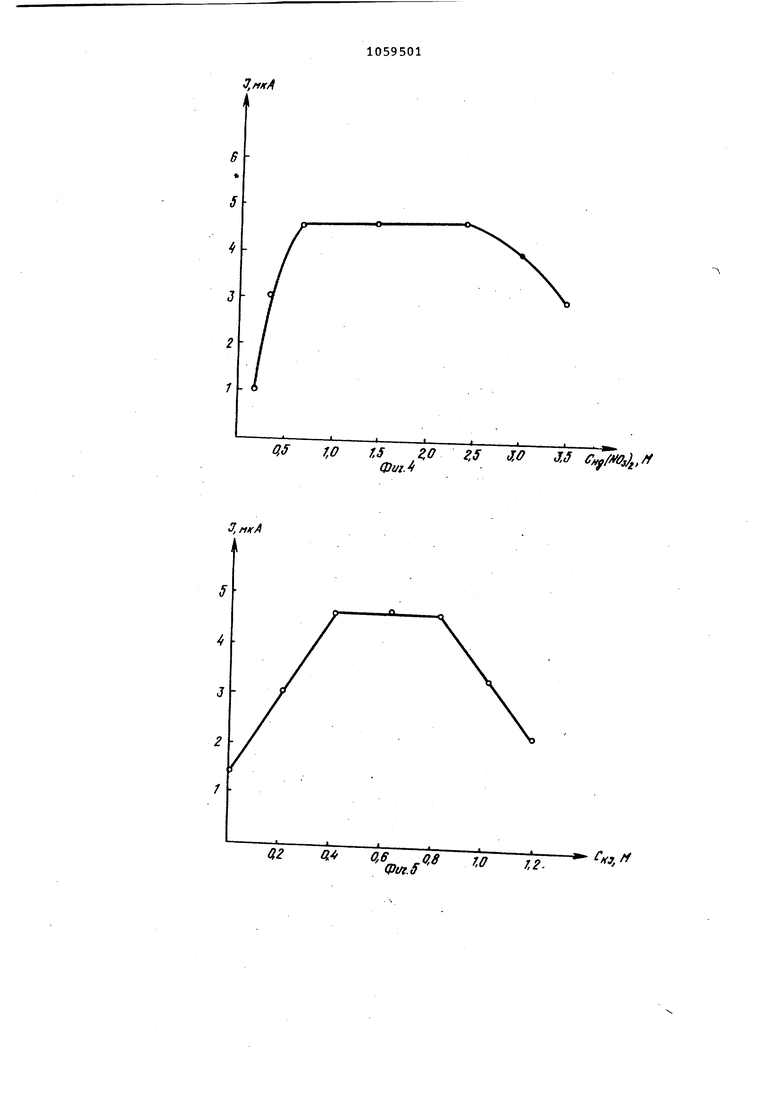
На фиг. 4 дана зависимость величины тока э.лек гровосстановления теллура от концентрации азотнокисло ртути (П ) в растворе, содержащем 1,5 М НС1 + 0,4 КЗ + 210 г-ион/л Т
. % -0,5 в; ч -0,35 в;
t 3 мин; t 3 мин.
. На фиг. 5 показана зависимость величины тока электровосстановления теллура от концентрации иодида калия в растворе, содержащем 1,5 М НС1 + 1,2510Зм HgCNO), + 2-10- г-ион/л Те (IV).
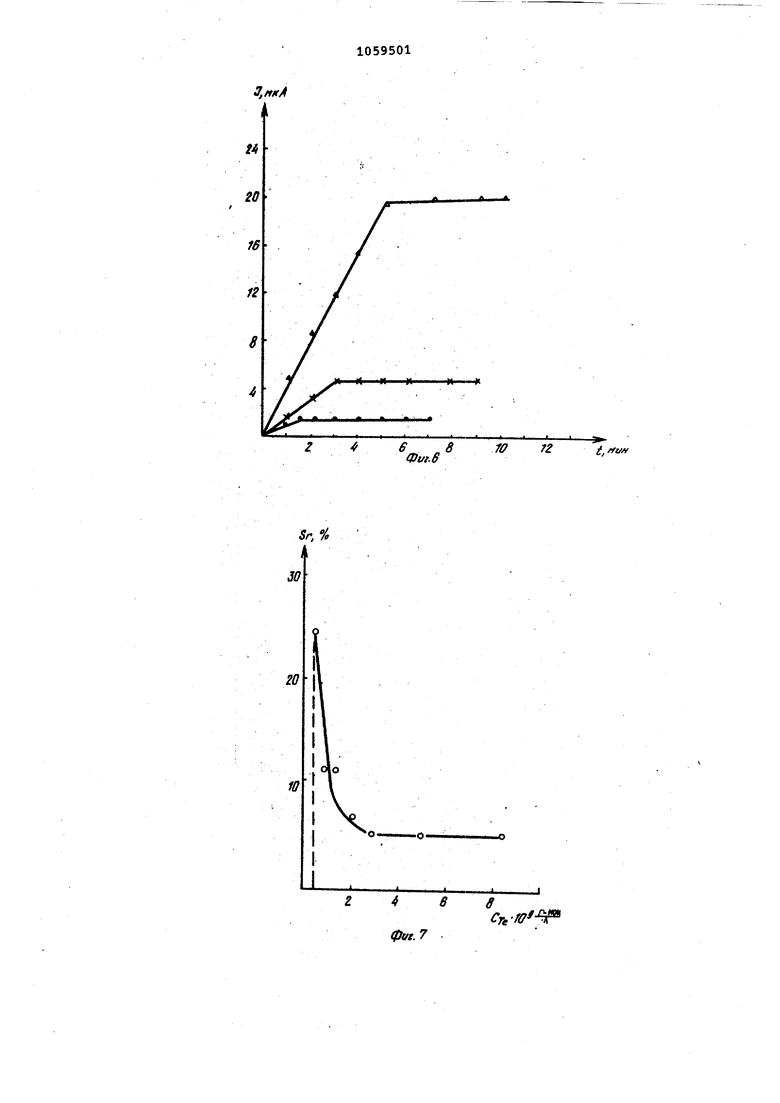
. ч; 0,5 в; Ч -0,35 В,Т 3 мин; t .3 мин. На фиг. б показана зависимость величины тока электровосстановления теллура от времени предэлектролиза (f) при потенциале Ч-, в растворах следующего состава: 1,5 М НС1 + 1,2510 М Hg(NOi)2 + 0,6 М К7 + + 2 - Ю- гтион/л Те (IV ); (f
2,-10 г-ион/л Те {IV ) ,Ч 2 )
210 г-ион/л Те (IV), (3)
На фиг. 7 изображена зависимость относительного стандартного отклонения от концентрации теллура в растворе, содержащем 1,5 НС1 + 0,6 М KJ + 1,25-10-Зм Hg(NO,),,% -0,5 В; 4-2 -0,3 в;
1 3 мин; t 10 мин. На фиг, 8 показана градуировочная характеристика для теллура (iV) на питьевой воде г. Свердловска. Использование предлагаемого спосо ба определения теллура позволяет с высокой чувствительностью и избирательностью концентрировать и определять теллур в сложных растворах с малым содержанием теллура в природны объектах, а также в сточных водах, реактивах без предварительного отделения от мешающих элементов, что обеспечивает экспрессивность определения теллура и служит основой для автоматизации анализа, при этом кон-0,3 -Q -0,5 центрирование и определение теллура протекает в течение 3-5 мин. Кроме того, предлагаемое изобретение способствует решению проблемы охраны окружающей среды, обеспечивая эффективный способ контроля природных, промышленных и сточных вод. Использование предлагаемого способа определения теллура обеспечивает повышение чувствительности путем изменения концентрации компонентов основных реагентов, проведение электролиза в две стадии и катодной поляризации электрода без предварительного переноса электрода в другой раствор. -а7 -0,8 -0.9 

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ инверсионного электрохимического определения вольфрамат-ионов | 1983 |
|
SU1120233A1 |
| Способ определения родия(III) в водных растворах методом инверсионной вольтамперометрии по пикам селективного электроокисления свинца(II) из интерметаллических соединений с родием RhPbи RhPb | 2016 |
|
RU2624789C1 |
| СПОСОБ ВОЛЬТАМПЕРОМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ ЦИСТЕИНА | 2003 |
|
RU2238552C1 |
| Способ вольтамперометрического определения ионов тербия в водных растворах | 1990 |
|
SU1818580A1 |
| Способ инверсионного определения ртути и теллура в теллуриде ртути | 1988 |
|
SU1608561A1 |
| Вольтамперометрический способ определения празеодима в водных растворах | 1989 |
|
SU1728773A1 |
| Способ определения молибдена (у1) | 1983 |
|
SU1150533A1 |
| ВОЛЬТАМПЕРОМЕТРИЧЕСКИЙ СПОСОБ ОПРЕДЕЛЕНИЯ СУММАРНОЙ АКТИВНОСТИ АНТИОКСИДАНТОВ | 2002 |
|
RU2224997C1 |
| Способ инверсионно-вольтамперометрического определения мышьяка | 1983 |
|
SU1187065A1 |
| Способ инверсионного вольтамперометрического анализа теллурида свинца | 1990 |
|
SU1746290A1 |


Фиг.З
У,мнА
Qf 1,0 r.5 2.0 2.5 J,ff .5 ),/ фиг. 4
З.ннА
1
W 20 16 12
л
Фиг.в
20
10
г 4 в 8
Ст -ГОфуг. 7
f2 0,8 0. 0.8 12 e./fff
фиг8
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Нейман Е.Я | |||
| и др | |||
| Некоторые особенности определения мышьяка, селена и теллура методом инверсионной вольтамперометрии на графитовых электродах | |||
| Журнал аналитической химии, 1975, т | |||
| Способ обработки медных солей нафтеновых кислот | 1923 |
|
SU30A1 |
| НИВЕЛЛИР | 1923 |
|
SU1132A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Торопова В.Ф | |||
| и др | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| вительных и катгшитнческих процессов на стационарнсм ртутном микроэлектроде | |||
| Журнгт аналитической химии, 1980, т | |||
| Скоропечатный станок для печатания со стеклянных пластинок | 1922 |
|
SU35A1 |
| ДЖИНО-ПРЯДИЛЬНАЯ МАШИНА | 1920 |
|
SU296A1 |
Авторы
Даты
1983-12-07—Публикация
1982-04-05—Подача