Изобретение относится к клиничес кой биохимии, а именно к способам получения ферментных мембран, которые могут найти применение в измери тельных приборах на основе ферментов (ферментных анализаторах)для определения физиологически важных соединений и ферментативной активно ти. Наиболее близким к изобретению является способ получения ферментны мембран путем связывания ферментов нерастворимыми пленочными носителям .{на основе целлюлозы, пирролидона и к др. полимеров)в присутствии глутарового альдегида ij . иднако полученные таким образом ферментные мембраны обладают низкой механической прочностью и малой активностью. Это связано с тем, что целлюлозные, пирролидоновые и другие полимерные, носители не обладают макропорами, следовательно, непроницаемы ддя белковых молекул, которые лишь адсорбируются на поверхности пленки. Их количество мало, поэтому полученные мембраны не обладают высокой каталитической активностью. Кроме того, используемые пленочные материалы не обеспечи вают механической прочности, поскол ку они. набухают в воде. Целью изобретения является повышение ферментативной активности и механической прочности ферментных мембран. Поставленная цель достигается тем, что согласно способу получения ферментных мембран, включающему связьшание ферментов с нерастворимым пленочным носителем в присутствии глутарового альдегида, процесс связьшания ведут в присутствии сыво роточного альбумина, а в качестве носителя использзпот макропористую лавсановую или поликарбонатную мембрану. Причем используют макропористую .мембрану с проницаемостью 4,7-11,4% диаметром пор 0,051-0,18 мкм и толщиной 9,5-10 мкм. Повышение ферментативной активно ти и механической прочности, в перв очередь, обусловлено применением макропористых пленочных носителей, обеспечивающих проницаемость мембра а также использованием сывороточног альбумина, способствующего связываHfno фермента с носителем. Оптимальные параметры используемых мембран обеспечивают необходимый комплекс свойств получаемого в результате изделия(см. табл. 1 и 2) . Увеличение проницаемости(проницаемость мембран, выражена в процентах, показывает соотношение площади пор к общей площади мембраны и, следовательно, зависит от количества и диаметра пор)приводит к увеличению активности однако при этом падает механическая прочность. Таким образом, указанные параметры мембран являются оптимальными . Пример. 1600 ед. глюкозооксидазы растворяют в 0,6 мл 0,1 М фосфатного буфера рН 6,8, добавляют 0,4 мл 4,5%-ного сьшороточного альбумина и 0,04 мл 25%гного глутарового альдегида. Смесь тщательно перемешивают и выливают на макропористую лавсановую или поликарбонатную мембрану см (проницаемость 9,5%, диаметр пор 0,12 мкм)и покрывают cBejjxy гидратцеллюлозной мембраной, толщиной 10 мкм. Мембрану помещают в холодильник в течение 24 ч. Разрезают на Куски диаметром 2 см и накладьшают на Р4 электрод (с Ft электродом контактирует гидратцеллюлозная мембрана)для определения ферментативной активности. Толщина полученной мембраны 45 мкм. П р и м е р 2. Готовят смесь аналогично примеру 1 и наносят на лавсановую мембрану диаметром 6 мм, которая предварительно прикреплена к резиновому кольцу. Прикосновением микропипеткой наносят 1 мкл смеси и накладьгаают гидратцеллюлозную мембрану толщиной 10 мкм. Оставляют в течение 2 ч при комнатной температуре, наливают на Pt электрод и определяют ферментативную активность. Приме р 3. Мембрану готовят аналогично примеру 2, однако используют макропористую мембрану, толщина которой 9,5 мкм, проницаемость 11:,4% и диаметр пор 0,18 мкм. П р и м е р 4. Мембрану готовят аналогично примеру 2, используя макропористую мембрану, толщина которой 10 мкм, проницаемость 4,7 % и диаметр пор 0,051 мкм. П р и м е р 5. Мембрану готовят аналогично примеру 2, в качестве полупроницаемой мембраны применяют целлофановую толщиной 55 мкм. ft р им е р 6. Мембрану готовят аналогично примеру 2, в качестве полупроницаемой мембраны используют триацетатцеллюлозную мембрану, полученную путем выливания 1 мл . 1,5%-ного раствора триацета.тцеллюлозы в стакан воды, диаметром 10 см толщина мембраны 2 мкм. Пример. Готовят смесь по примеру 1 и в количестве 1 мкл ее наносят на лавсановую макропористую мембрану толщиной 10 мкм, проницае мостью 9,5% и диаметром пор 0,12 мк которая прикреплена к резиновому кольцу, как в примере 2. Наносят ацетатцеллюлозную мембрану толщиной 10 мкм (ацетатцеллюлозную мембрану готовят путем обработки 10 мкм толщины гидратцеллюлозной мембраны (ЮО см)150 мл смеси абсолютного пиридина и уксусного ангидрида (1 :l) при в течение 13ч. Толщина мембраны 25 мкм. При м е р 8. Аналогично примеру 2, но в качестве полупроницаемой 1мембраны используют -полипропилен толщиной 1О мкм. П р и м е р 9. Готовят смесь из .5 мг глюкозооксидазы и .15 мг пероксидазы по примеру 1. Ферментную мембрану готовят по примеру 2 . Ферментная активность глюкозооксидазной и глюкозооксидазной-перок дазной мембран(глюкозооксидазная .активность определена на Pt электро де при 0,6 В (1-7) или -0,бВ(. Ag/AgCl электрода в 0,1 М фосфатном буфере рН 7,2; ферментативная актив ность глюкозооксидазной-пероксдаазн мембраны определена в О,1 М фосфатн буфере рН 7,2 в присутствии 1 мМ ферро.цианида калия на стеклоуглерод ном электроде при О В OTH.Ag/AgCl электроду)приведена в табл. 1. Ферментативную активность биокат литических мембран рассчитывают на основе величины тока ферментных электродов по формуле, приведенной в . . 1 -.d 15 - плотность тока ферментного электрода; П - число переносимых электронов (2) ; F - число Фарадея, Ymax активность, ед/см- ; 3 - толщина ферментных мембран; 5Т - Концентрация субстрата (1 мМ); константа Михаэлиса(для глюкозооксидазы 5,87 мМ З); ,А - коэффициент, отражающий электрохимически активную площадь электрода ( W Полученные по предлагаемому способу мембраны в 10 раз прочнее механически, причем значительно вьппе их ферментативная активность(расчитывается на основе величины тока ферментного электрода). Используются мембраны проницаемостью 4,7-11,4%, диаметрок пор 0,051-0,18 мкм. Увеличение проницаемости приводит к увеличению активности примеры 2-4) . Однако нет необходимости и даже нецелесообразно выходить за верхний предел проницаемости, так как примеры 4, 1,2, 9 и 3 показьшают, что с увеличением проницаемости(увеличением диаметра пор)уменьшается механическая проч-. ность(хотя и за пределами она была бы выще таковой). Наименьшей механической прочностью обладает мембрана по примеру 3. Таким образом, приведенные параметры являются оптимальными, обеспечивающими и достаточно высокую активность и высокую механическую прочность. Сравнительные свойства глюкозо- ; оксида зной (l) и биферментной глюкозооксидазной-пероксидазной(2) мембранj полученных по известному ( целлюлозная мембрана толщиной 55 мкм)и по предлагаемому способам (проницаемость макропористой мембраны 9,5%, диаметр пор 0,12 мкм, толщина 10 мкм)приведены в табл. 2. Технико-экономическая эффективость изобретения заключается в поьшении ферментативной активности механической прочности ферментных ембран, которые могут быть применеы в ферментных анализаторах.
Таблица 


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ иммобилизации алкогольоксидазы | 1988 |
|
SU1615179A1 |
| Способ получения ферментных мембран | 1988 |
|
SU1535892A1 |
| СПОСОБ ИММОБИЛИЗАЦИИ АЛКОГОЛЬОКСИДАЗЫ | 1991 |
|
RU2010858C1 |
| Способ определения активности ферментов,синтезирующих или разлагающих аденозинтрифосфат | 1982 |
|
SU1070166A1 |
| СПОСОБ ПОЛУЧЕНИЯ ИММОБИЛИЗОВАННОЙ ХОЛИНЭСТЕРАЗЫ | 1991 |
|
RU2005785C1 |
| Способ получения покрытия | 1984 |
|
SU1165484A1 |
| СПОСОБ ПОЛУЧЕНИЯ ФЕРМЕНТАТИВНОГО КОМПЛЕКСНОГО ПРЕПАРАТА, ОБЛАДАЮЩЕГО КОЛЛАГЕНАЗНОЙ АКТИВНОСТЬЮ | 2008 |
|
RU2412997C2 |
| БИОКАТАЛИЗАТОР И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2002 |
|
RU2233327C2 |
| Способ изготовления ферментного электрода | 1983 |
|
SU1176250A1 |
| Способ получения сахаристых крахмалопродуктов | 2023 |
|
RU2833702C1 |
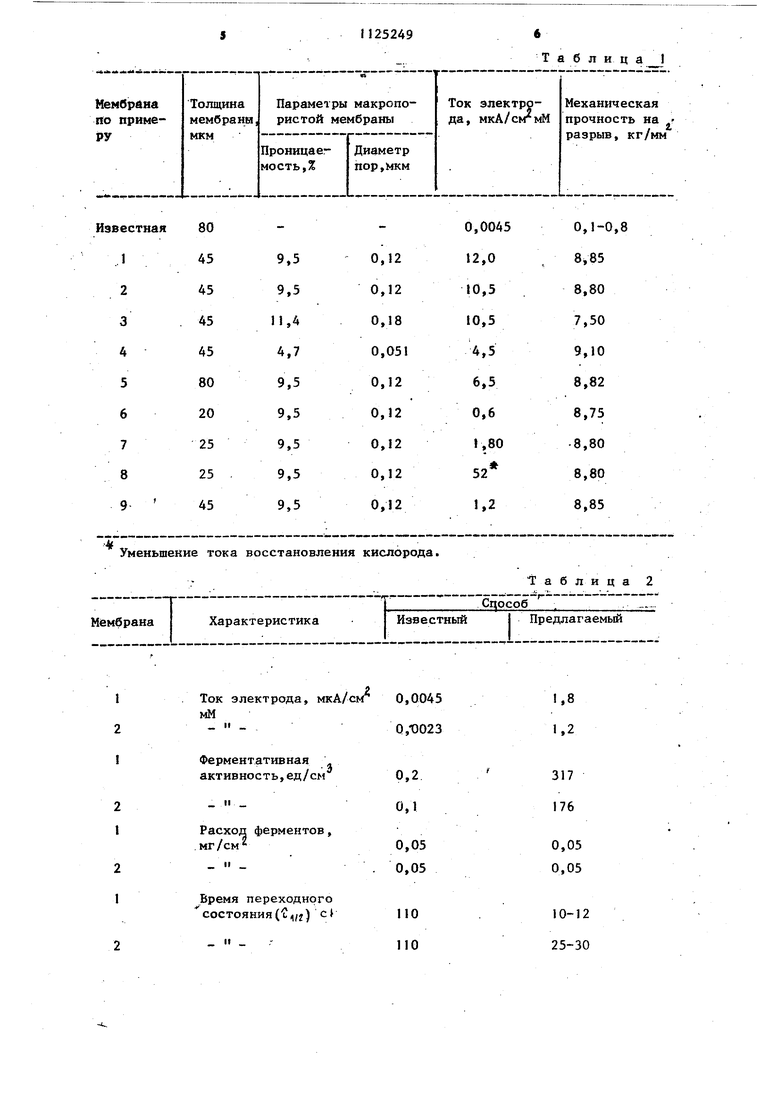
I. СПОСОБ ПОЛУЧЕНИЯ ФЕРМЕНТНЫХ ЖМБРАН, включающий связывание ферментов с нерастворимым пленочным носителем в присутствии глутарового альдегида, о т л и ч a ю щ и и с я тем, что, с целью повышения ферментативной активности и механической прочности мембраны, процесс связывания ведут в присутствии сьгоороточногр альбуминаf а в качестве носителя используют макропористую лавсановую или поликарбонатную мембрану. 2. Способ по п. 1, о т л и ч аю щ и и с я тем, что исяользуют 3 макропористую мембрану с проницаемостью 4,7-11,4%, диаметром пор 0,051-0,18 мкм и толщиной 9, мкм.
80 45 45 45 45 80 20 25 25 45
звестная
9,5
1 2 3 4 5 6 7 8 9 9,5 11,4 4,7 9,5 9,5 9,5 9,5 9,5
Уменьшение тока восстановления кислорода.
Ток электрода, мкА/см
мМ и
Ферментативная активность,ед/см
I
Расход ферментов, мг/см
Бремя переходного состояния () с Г
0,0045
0,1-0,8 8,85 12,0 10,5 8,80 10,5 7,50
4,5 9,10
0,6 8,75
1,80 -8,80
52 8,80
1,2 8,85
Таблица 2
1,8 1,2
317 176
0,05 0,05
10-12 25-30 П25 Мвмв1 айа Характеристика Стерилизуемость 1 Прочность на разрыв, кг/мм II 8 .Продолжение табл.2 Способ Предлагаемый Известный Не стерилизуется- Стерилизуется (инактивация) ркисью зтилейр - ., . ;. 0,1-0,8 0,1-0,8
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Biraun G., Thomas D., at.al | |||
| New inethod, binding enzyme molecuFes in to a water-insoluble raiatric; properties affer insolubilisation Biochem | |||
| Bioeng, VV 15, 1973, p | |||
| Способ получения гидроцеллюлозы | 1920 |
|
SU359A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Аналитические системы на основе иммобилизованных ферментов, Вильнюс, Мокслас, 1981, с | |||
| Термосно-паровая кухня | 1921 |
|
SU72A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| и другие | |||
| Кинетика и стабильность глюкозооксидазы из Penicilliumlvitale.- Прикладная биохт ия и микробиология, 1978, т | |||
| Паровоз для отопления неспекающейся каменноугольной мелочью | 1916 |
|
SU14A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Устройство для получения водяного пара и подведения его в толщу горящего топлива | 1921 |
|
SU377A1 |
| Amperometrio response enhance - ment of the iinmobilized glucose oxidase enzyme.electrode..chem., 1976, V | |||
| Приспособление для автоматической односторонней разгрузки железнодорожных платформ | 1921 |
|
SU48A1 |
Авторы
Даты
1984-11-23—Публикация
1982-10-29—Подача