Изобретение относится к органи- че скому синтезу,; конкретно к способу Получения производного 4-амине- масляной кислоты, проявляющего биологическую активность.
Цель изобретения заключается в разработке способа получения производного А -аминомасляной кислоты, проявляющего повышенную биологическую активность, заключающуюся в улучшении церебрального метаболизма головного мозга при расстройстве его функций.
Пример 1-. 1. Бензиловый эфир (2,4-диокси- 3,3- ДИме- тил-н-бутирил)амино -н-масляной кислоты (5 г) растворили в тетра- гидрофуране (50 мл) и прибавили к нему пиридин (3 г). В смесь по каплям при перемешивании добавили раствор изобутирилхлорида (1,8 г) в тетрагидроЛуране (5 мл) при температуре . Смесь перемешивали при комнатной температуре в течение ночи и затем сконцентрировали при пониженном давлении. Полученный остаток растворили в этилацетате и раствор промыли разбавленной соляной кислотой, водой, водным раствором бикарбоната натрия и насьщен- ным соляным раствором в указанной последовательности. Раствор в этил- ацетате высушили и сконцентрировали при пониженном давлении для удаления растворителя. Остаток очистили при помощи хроматографии на сили- кагеле (растворитель - хлороформ : этилацетат 4:1) и получили бензило- вый эфир (4-изoбyтиpилoкcи- -3 ,3-диметил-2-окси-н-бутирил) ами- ноТ-н-масляной кислоты (3,6 г, 59,2% в виде бесцветного вязкого масла.
ИК (пленка) ,-5
мсякс
3350, 1730
1650. Масс-спектрометрия,1п/е: 393 (М
2. Бензиловый эфир ( изо- бутирилокси-3,З-диметил-2-окси-н-бу- тирил) аминoJ H-масляной кислоты (3,4 г) растворили в метаноле (34 мл и добавили к нему палладиевую чернь (30 мг). Смесь подвергали каталитическому восстановлению при комнатной температуре при атмосферном давлении. После завершения реакции реакционную смесь профильтровали для удаления нерасТворившихся частиц и фильтрат сконцентрировали при пониженном давлении. Остаток рекрис- таллизовали из смеси этилацетата и п -гексана и получили (4-изо
924
бутирилокси-3,З-диметил-2-окси-н-бу- тирил)амино Н-масляную кислоту (2,0 г, 76,3%) в виде бесцветных призм, т.пл. 73-75 с. ИК (нуйол) ,
«же
см
,я.
3320, 1715, 1610. Масс- спржтрпметрия, т/е: 303 (), ы + 37,2° (С 1, этанол).
Повторяют перекристаллизацию указанного продукта из смеси этилаце0 тат и изопропиловый эфир, .получая бесцветные призматические кристаллы с т.пл. 82-83,, ,4° (с 1, этянол).
3. (4-Изобутирилокси-З,35 -диметил-2-окси-н-бутирил)амино1-н- -масляную кислоту (1,0 г) раств о- рили в этаноле (20 мл) и к ней прибавили гидроокись кальция (0,15 г) и воду (2 мл) месь перемешивали при ком0 натной температуре в течение 40 мин. Реакционную смесь профильтровали для удаления не:растворившихся частиц и фильтрат сконцентрировали при пониженном давлении. Остаток обработали н-гексаном
5 и получили 1)(4-изобутирилокси- -3,3 ДИметил-2-окси-н-бутирил)ами- но -н-бутират кальция (0,85 г, 80.0%) в виде бесцветного порошка. + 28,3° (С 1, этанол). Пример 2. 1. Аналогично примеру 1.1, используя бензиловый эфир (2,4-диокси-З,3-диме- тил-н-бутирил)амино -н-масляной кислоты (5,0 г), тетрагидрофуран (55 мл) пиридин (3 г) и изовалерилхлорид
5 (2,1), получили бензиловый эфир (4-изовалерилокси-3,3-диме- тил-2-окси-н-бутирил)амино -н-масляной кислоты (4,0 г, 63,5%) в виде бесцветного вязкого масла. ИК (нуй-
° ол),, „д, 3350, 1730, 1650. Масс-спектрометрия, т/е: 407.
2. Аналогично примеру 1.2, ис пользуя бензиловый эфир (4- -изовалерилокси-3,З-диметил-2-ок си-н-бутирил)амино Н-масляной кислоты (3,8 г), метанол (38 мл) и паллядиевую чернь (30 мг), получили (4-изовалерилокси-З,3-диме- тил-2-окси-н-бутирил)амино -н-бути0 рат (2,1 г, 70,9%) в виде бесцветных призм, т.пл. 84-86 0. ИК (нуй-)
ол),
Макс
-1
см- : 3300, 1720, 1610.
IMU КС .
Масс-спектронетрия, т/е: 317 (М ), Ыд + 34,1° (С 1, этанол). 5 3. Аналогично примеру 1.3, используя (4-изовалерилокси- -3,З-диметил-2-окси-н-бутирил)ами- но -н-масляную кислоту (1,0 г).
этанол (20 мл), гидроокись кальция (0,13 г) и иоду (2 мл), получили (Д-изовалерилокси-З,3-ди- метиЛ 2 ОксИ Н бутирил) амино Н бу- тират кальция (0,84 г, 79,2%) в виде бесцпетного порошка.
+ 26,1° (С 1, этанол).
Пример 3. 1. Аналогично примеру 1.1, используя бензиловый эфир D-4- N( 2,4-диокси-3,3-диме- тил-н-бутирил) aминoJ H-мacлянoй кислоты (5,0 г), тетрагидрофуран (55мл пиридин (3 г) и изогексаноилхлорид (2,3 г), получили бензиловый эфир D-4 N--( 4- Изогексаноилокси 3,3-диме- тил 2-окси-н- бутирил) амино -н-т асля- ной кислоты (4,8 г, 73,1%) в виде бесцветного вязкого масла. ИК (нуй-
ол),, cм 3350, 1730, 1650. Масс-спектрометрия, т/е: 421 (М ). 2. Аналогично примеру 1.2. используя бензиловый эфир (4- -изогексаноилокси-3,3-диметил-2-ок- си-н-бутирил) амино1-н-масляной кислоты (4,0 г), метанол (40 мл) и пал- ладиевую чернь (40 мг), получили (4-изогексаноилокси-3,3-ди- метил- 2-окси-н-бутирил) амино -н-мае-
ляную кислоту (2,9 г, 92,2%) в виде бесцветного вязкого масла. ИК (плен- ка),мо,, 3330, 1720, 1610. Масс-спектромр.трия, т/е: 331 (), с + 31,6° (С 1, этанол).
Пример 4. 1. Аналогично примеру 1.1, используя бензиловый эфир (2,4-диокси-З,3-диметил-н-бутирил )амино -н-масляной кислоты (4,0 г), тетрагидрофуран (45 мл), пиридин (2,4 г) и пивалоил- хлорид, получают бензиловый эфир (4-пивалоилокси-3,3-диметил- -2-окси-н-бутирил)aMHHoJ-H-масляной кислоты (3,0 г, 47,6%) в виде бесцветного вязкого масла. ИК (пленка),
макс 3350, 1730, 1650. Масс- спектрометрия, т/е: 407 ().
2. Аналогично примеру 1.2, используя бензиловый эфир (4-пива- лоилокси-3,3-диметил-2-окси-н-бy- тиpил)aминo H-масляной кислоты (2,8 г), метанол (28 мл) и паллади- евую чернь (30 мг), получили D-4- (4-пивалоилокси-З,3-диметил- -2-окси-н-бутирил)амино2 -н-масляную кислоту (1,1 г, 50,4%) в виде бес- цветньгх кристаллов, после перекристаллизации из смеси этилацетата с н-гексаном, т.пл. 79-82°С. ИК (нуй
5
.rt.
10
,°- мси;с 3350, 1730, 1710, 1610. Масс-спектрометрия, т/е: 317 (М).
П р и м е р 5. 1. Аналогично примеру 1.1, используя бензиловьй эфир (2,4-диокси-3,3-диметил-н- -бутирил) амине н-масляной кислоты (4,0 г), тетрагидрофуран (45 мл), пиридин (2,4 г) и 3,3-диметил-н-бу- тирилхлорид (2,0 г), получили беп- зиловый эфир Г)-4- к-Г4-(3,3-диме- тил-н-бутирил)-окси-3,3-диметил- -2-окси-н-бутирил амино -н-масляной кислоты (3,7 г, 71%) в виде бесцветного вязкого маслянистого вещества. ИК (пленка) ,1 , 3350, 1730, 1650. Масс-спектромет- рия, т/е: 421 (М ).
2. Аналогично примеру 1.2, используя бензиловый эфир -4-Гн-«- -(3,3-диметил-н-бутирил)-окси-3,3-дй- метил-2-окси-н-бутирил амино -н-масляной кислоты (3,5 г), метанол (35 мл) и палладиевуго чернь (40 мг), 5 получили D-4-| N- 4-(3,3-димeтил-н-бy- тирил)-окси-3,3-диметил-2-окси-н-бу- тирил аминов -н-масляную кислоту
0
(2,2 г, 79,7%) в кристаллов,
0 |0л), ,
виде бесцветных 102-104°С. ИК (нуй- 1735, 1715,
т. пл.
Макс, 3340, 1610. Масс-спектрометрия, т/е: 331 (M), + - - -° и м е
32,0 (С 1, этанол). II р и м е р 6. 1. Аналогично примеру 1.1, используя бензиловый 5 эфир (-2,4-диокси-З, 3-диметил-н-бутирил ) амино | -н-масляной кислоты (4,0 г), тетрагидрофурак (45 мл), пиридин (2,4 г) и 2-этилг -н-бутирилхлорид (2,0 г), получили 0 бензиловый эфир 1)(2-этил- -н-бутирил)-окси-3,3-димеТИЛ-2-ОК- си-н-бутирил } аминоЧ-н-масляной
(2,5 г, 47,9%) в виде бес- масла. ИК (пленка).
5
кислоты
цветного вязкого
MqKc
3350, 1730, 1650. Массспектрометрия, т/е: 421 (М).
2, Аналогично примеру 1.2, используя бензиловый эфир -(2-этил-н-бутирил)-окси-3,3-диме-
тил-2-окси-н-бутирил амино)-н-масляной кислоты .(2,4 г), метанол (24 мл) и палладиевзто чернь (30 мг), получили D-4-{N- 4-( 2-зтил- Н-бути- рил)-окси-н-бутирил амино -н-масля-
ную кислоту (1,7 г, 90,1%) в виде бесцветного вязкого масла. ИК (плен- ка), „g.j., см- : 3350, 1730, 1710, 1645. Масс-спектрометрия, т/е: 331
(M ),MC - 25,9 (C .1, этаНОЛ ) .
3. Аналогично примеру 1.3, используя (2 этил Н-бути рил)-окси-3.3-диметил-2-окси-н-бу- тирил амино|-н-масляную кислоту (1,0 г), этанол (20 мл), гидроокись кальция (130 мг) и воду (2 мл), получили (2-этил H бyти- pил)-окси З, 3-диметил-2-окси-н- бу- тирил амино -н- бутират кальция (0,81 г, 76,6%) в виде бесцветного порошка. о(.1 о + 24,7° (С 1, этанол).
Пример 7.1. Бензиловый эфир D-4 ll- l 2,4-диок си-3,3-диме- тил-н-бутирил)амино1 Н-масляной кислоты (4,0 г) растворили В тетрагид- рофуране (30 мл) и добавили к нему пиридин (2 мл). В смесь по каплям при охлаждении льдом добавили раствор ацетилхлорида (1,2 г) в тетра- гидрофуране (5 мл). Смесь перемешивали при комнатной температуре в течение ночи и затем сконцентрировали при пониженном давлении. Остаток растворили в этилацетате и раствор промыли разбавленной соляной кислотой, водой, водным раствором бикарбоната натрия и соляным раствором в указанной последовательности. Этил ацетатный слой .высушили и сконцентрировали при пониженном давлении. Остаток очистили при помощи хроматографии на силикагеле (растворитель - хлороформ: этилацетат 4:1) и получили бензиловый эфир - (4-я.цетокси-3,3-диметил-2-окси-н-бу тирил)аминоЗ-н-масляной кислоты (2,3 г, 50,9% в виде бесцветного вязкого масла. ИК (пленка),5,,,,..,.,см
.
3350, 1730, 1650. Йасс-спектро метрия т/е: 365 (М).
2. Бензиловый эфир (4- -ацетокси-3,3-диметил-2-окси-н-бу- тирил)амиио -н-масляной кислоты (2,0 г) растворили в метаноле-(20 мл и в смесь добавили палладиевую чернь (20 мг), Смесь подвергали каталитическому восстановлению при комнатной температуре при атмосферном давлении. После завершения реакции реакционную смесь профильтровали для удаления нерастворившихся частиц и фильтрат сконцентрировали при пониженном давлении. Получили -(4-ацетокси-3j З-диметил-2-окси-н-
0
10
-бутирил)амино -н-масляную кислоту (1,38 г, 91,6%) в виде бесцветного вязкого масла. ИК (пленка), ,tt 3350, 1720, 1640. Масс- спектрометрия, т/е: 275 (М), ос в + 33,1° (С 1, этанол).
Пример 8. 1. Аналогично примеру 7.1, используя бензиловый эфир (2,4-диокси-З,-3-диме- тил-н-бутирил)амино -н-масляной кислоты (4,0 г), тетрагидрофуран (35 мл), пиридин (2 мл) и пропио- нилхлорид (1,4 г), получили бен- зиловый эфир (4-пропионил- окси-3,З-диметил-2-окси-н-бути- рил)амино |-н-масляной кислоты (2,2 г, 46,9%) в виде бесцветного вязкого масла. ИК (пленка) ,,аке , 20 см : 3350, 1730, 1650. Масс-спект- рометрия, т/е: 379 (М).
2. Аналогично примеру 7.2, используя беизиловый эфир (4- -пропионилоксигЗ, 3- диметш1-2-ок- 2 си-н-бутирил)амино -н-масляной кислоты (2,0 г), метанол (20 мл) и палладиевую чернь (20 мг), получили D-4- N-(4-пропионилокси-3,3-ди- метил-2-окси-н-бутирил)амино1 -н-масляную кислоту (1,46 г, 96,7%; в виде бесцветного вязкого масла. ИК (пленка), макс , 3350, 1720, 1640. Масс-спектрометрия, т/е: 289 (М),о(,л + 30,0 (С 1, этанол).
Пример 9.1. Аналогично примеру 7.1, используя бензиловый эфир (2,4-диокси-З,3-диме- тил-н-бутирил)амино -н-масляной кислоты (4,0 г), тетрагидрофуран (35 мл), пиридин (2 мл) и н-бутирил- хлорид (1,6 г), получили бензиловый эфир (4-н-бутирш1ок си-3,3-ди- метш1-2-окси-н-бутирил)амино -н-мае/ fH XX- .« ..
30
5
ляной кислоты (2,9 г, 59,6%) в виде бесцветного вязкого масла. ИК (пленка),, 3370, 1730, 1650. Масс-спектрометрия, т/е: 393 (М),
Ы / °
+ 27,6 (С 1, этанол). 2. Аналогично примеру 7.2, ис- 0 пользуя бензиловый эфир (4-н- -бутирилокси-3,3-диметш1-2-окси-н- -бутирил) амино -н-масляной кислоты (2,0 г), метанол (20 мл) и паллади- евуп чернь (20 мг), получили.D-4- -fN-(4-н-бутирдлркси-3,3-диметил- -2-ок си-н-бутирил)амино -н-масляную кислоту (1,48 г, 96,0%) в виде бесцветного вязкого масла. ИК (пленка).
м,.с - 1720, 164П. Масс- спектрометрия, п/е: 303 (М), IB - 30,2° (с I, этанол).
П р и м е р 10. 1. Аналогично примеру 7.1, используя бензиловый эфир ( 2, A-flHt-iKCH-B, 3 диме- тил-н-бутирил)амино -н-масляной кислоты (А,О г), тетрагидроЛуран (35 мл), пиридин (2 мл) и. н-вале- рилхлорид (1,8 г), получили бензиловый эфир ( 4-н-валерилокси- -3,3 диметил-2 окси- н- бутирил) ами- но Н-масляной кислоты (3,0 г, 59,5%) в виде бесцветных кристаллов т.п. 34-35°С. ИК (нуйол),,, см 3370, 1730, 1650. Масс-спектромет- рия, т/е: 407 (М).
2.Аналогично примеру 7,2, используя бензиловый эфир (4- H-валерилокси-3 ,3 диметил-2-ок- си-н-бутирил)амино -н-масляной кислоты ( 2,6 г), метанол (30 мл) и палладиевзпо чернь (30 мг), получили D-4- N(4-н-валерилокси-3,3-диме- тил-2-окси-н-бутирил) амино --н-масляную кислоту (1,9 г, 93,8%) в виде бесцветного вязкого масла. ИК (плен Ь мам 3350, 1720, 1640. М;)сс спектрометрия, т/е: 317 (М), Ы 1 + 31,8° (С 1, этанол).
3.1)(4-Валерилокси-3,3-ди- мeтил-2-окси-н-бутирил) амино -н-масляную кислоту (0,9 г) растворили в метаноле (10 мл) и прибавили к ней L-лизин (0,41 г). Смесь перемепшва- ли при комнатной температуре в те-, чение 30 мин. Реакционную смесь сконцентрировали при пониженном давлении для удаления растворителя. Остаток обработали н-гексаном
и полученный порошок собрали фильтрованием. Получили L-лизиновую соль (4-валерилокси-З,3-диметил- -2-окси-н-бутирил)амино -н-масляной кислоты (1,13 г, 86,3%) в виде бесцветного порошка, т.п. ПО-ПЗ с + 25,5° (С 1, этанол).
4.(4-н-Валерилокси-З,3-дметил-2-йк си-н-бутирил)амино -н-масляную кислоту (1,0 г) растворили в метаноле (10 мл) и прибавили к ней гидроокись кальция (0,12 г) и воду
(5 мл). Смесь перемешивали при комнатной температуре и затем скон- центрировали при пониженном давлении. К остатку прибавили этанол, и смесь сконцентрировали до сухости при пониженном давлении. Получили
fO
15
0
5
0
5
(4-н-валерилокси-3,3-диме- ТИЛ-2-ОКси-н-бутирил) амино -н-бути- рат кальция (1,0 г, 94,3%) в виде бесцветного порошка.
Пример 11. 1. Аналогично примеру 7.1, используя бензиловый эфир (2,4-диокси-З,3-диме- тил-н-бутирил)амино -н-масляной кислоты (4,0 г), тетрагидрофу эан (35 мл), пиридин (2 мл) и н-гекса- ноилхлорид (2,0 г), получили бен- зиловый эфир (4-н-гeкcaнoил- oкcи-3 , 3-диметил-2- Окси-н-бути- рил)амино -н-масляной кислоты (3,2 г, 61,4%) в виде бесцветного вязкого масла. ИК (пленка) , |,д , 3370, 1730, 1650. Масс-спектромет- рия, т/е: 421 (М).
2.Аналогично примеру 7.2, используя бензиловый эфир (4- , -гексаноилокси-З.З-диметил-2-окси- -н-бутирил)амино -н-масляной кислоты (2,0 г), метанол (20 мл) и палладиевую чернь (20 мг), получили (4-гексаноил-3,3-диметил-2-окси-н-бутирил)амино Н-масляную кислоту (1,35 г, 85,9%) в виде бесцветного вязкого масла. ИК (nneti- ка),мо.кс 3350, 1720, 1640. Масс-спектрометрия, т/е: 33 (М), Ce lp + 27,6° (С I, этанол).
3.Аналогично примеру 10,3, используя D-4-FN-(4-н-гексаноилокси- -3,З-диметил-2-окси-н-бутирил)ами- но -н-масляную кислоту (1,0 г), L-лизин (0,44 г) и метанол (10 мл), получили L-лизиновую соль
-(4-н-гексаноилокси-3,3-диметил-2- -окси-н-бутирил)амин о -н-масляной кислоты (1,3 т, 90,2%) в виде бесцветного
порошка, о
т.п, 131-134 с.
Ys 25,1 (С 0,5, этанол). Пример 12, 1, Аналогично примеру 7.1, используя бензиловый эфир (2,4-диокси-З,3-диме- тил-н-бутил)амино -н-масляной кислоты (4,0 г), тетрагидрофуран (35 мл), пиридин (2 мл) и н-гепта- ноилхлорид (2,2 г), получили бензиловый эфир (4-н-гептане илокси-3,3-диметил-2-окси-н-бути- рил)амино -н-масляной кислоты (2,5 г, 46,4%) в виде бесцветного вязкого масла. ИК (ппенка} - , 3370, 1730, 1650, Масс-спектрометрия, т/е:.
435 (К), - -
2, Аналогично примеру 7,2; используя бензкловый эфир lr-4- N-(4 Н-тептаноилокси-3,3 диметил- -ок-- . си-н- бутирил) aMHHoJ -н-масляной кис лоты (l , 8 г) , метанол (20 мл) и пал- ладиевую чернь (20 мг) , получили - (4-н- гептаноилокси 3,3-ди метил 2 окси Н бутирнл) аминп -н--мас- лянук) кислоту (1,3 г, 91,1%) в виде бесцветного вяякого масла. ИК (плен-
К -1),макс . 3330, 1720, 1640 Масс-спектрометрия, т/е: 345 (М), W + 30,2° (С , этанол). Пример 13, 1 . Аналогично прмеру 7.1, используя бензиловый эфир D-4- N- (2,4-диокси-З, З-диметил -н-буг тирил)амино Н масляной кислоты (4,0 г), тетрагидрофуран (35 мл), пиридин (2 мл) и н-октаноилхлорид (2,4 г), получили бензиловый эфир ig- (4-н-октаноилокси-З, З-диме- тил-2 окси-н-бутирил)aMHHoJ - н-масляной кислоты (2,2 г, 39,6%) в виде бецветного вяякого масла. ИК (пленка),
мо.кс спектрометрия, т/е: 449 (М ).
2. Аналогично примеру 7.2. используя бензиловый эфир (4-H- -октаноилокси-3,З-диметил-2-окси-н- -бутирил)амино Н-масляиой кислоты (1,4 г),, метанол (20 мл) и паллади- евук) чернь (15 мг), получили D-4-
( 4-н-октаноилокси-3,3-диметил- 2--окси-н-бутирил)амино -1Н-масляную кислоту (1,05 г, 93,8%) в виде бесцветного вязкого масла. ИК (пленка),
«dicc ° спектрометрия, п/е: 359 (М ),
М +27,4° (с 1, этанол).
Пример 14. 1. Аналогично прмеру 7.1, используя бензиловый эфир (2,4-диокси-З,3-диметил-н-бу- тирил)амино Н-масляной кислоты (4,0 г), тетрагидрофуран (35 мл), пиридин (2 мл) и н-нонаноилхлорид (2,6 г),. получили бензиловый эфир (4-н-нонаноилокси-З,3-диме- тил-2 -ок си-н-бу тирил) амино -н-масляной кислоты (3,9 г; 68,0%) в виде бесцветного вязкого масла. ИК (пленка)-.«с . « 3370 1735, 1650. Масс-спектрометрия, т/е: 463 (М ).
2. Аналогично примеру 7.2, используя бензиловый эфир (4-н-но- наноилокси-3,З-диметил-2-оксй-н-бу- тирил)амино -н-масляной кислоты (2,0 г), метанол (20 мл) и паллади- евую чернь (20 мг), получили D-4- N-(4-н-нонаноилокси-З,3-диметил- -2-окси-н-бутирил)амино -н-масляную
кислоту (1,4 г, 86,9%) в виде бесцветного вязкого масла. ИК (пленка) мпхс см : 3330,1720,1640.Масс-спектметрия, т/е: 373 (М-), + 26,2 (с 1, этанол).
3. Аналогично примеру 10.3, используя D -4- N- 4-н-нонаноилокси- -3,3-диметил- 2-окси-н-бутирил) ами- HoJ-н-масляную кислоту (о,9 г), метанол (Ю мл) и t -лизин (о,35 г), получили лизиновую соль О--4- N.- -(4-н-нонаноилокси-З,З-диметил-2-ок- си-н-бутирил)амино -н-масляной кислоты (l,l5 г, 91,8%) в виде бесцветного порошка, т.п. .
TC 22,9° (с 0,5, этанол)/.
Биологическая активность.
Эксперимент 1.
Использовали крыс SD мужских особей весом 200 г в возрасте 7 недель голодавших в течение ночи (одна группа 4 крысы). Каждой крысе перорально ввели суспензию (2 мл) испытываемого соединения в растворе (0,5%) карбоксиметилцеллюлозы при помощи желудочного зОнда (доза испытываемого соединения: 389 ш моль/кг соответствует 100 мг/кг гопантената каль ция). Через один или два часа после введения препарата крыс умертвили, прорезав сонные артерии, и собрали кровь. Кровь каждой крысы центрифугировали (2800 об/мин, 15 мин) для определения плазмы крови. Концентрацию гопаитеновой кислоты в плазме крови (0,1 мл) определили при помощи газовой хроматографии и масс- спектрометрии.
Результаты представлены в табл.1.
Эксперимент 2.
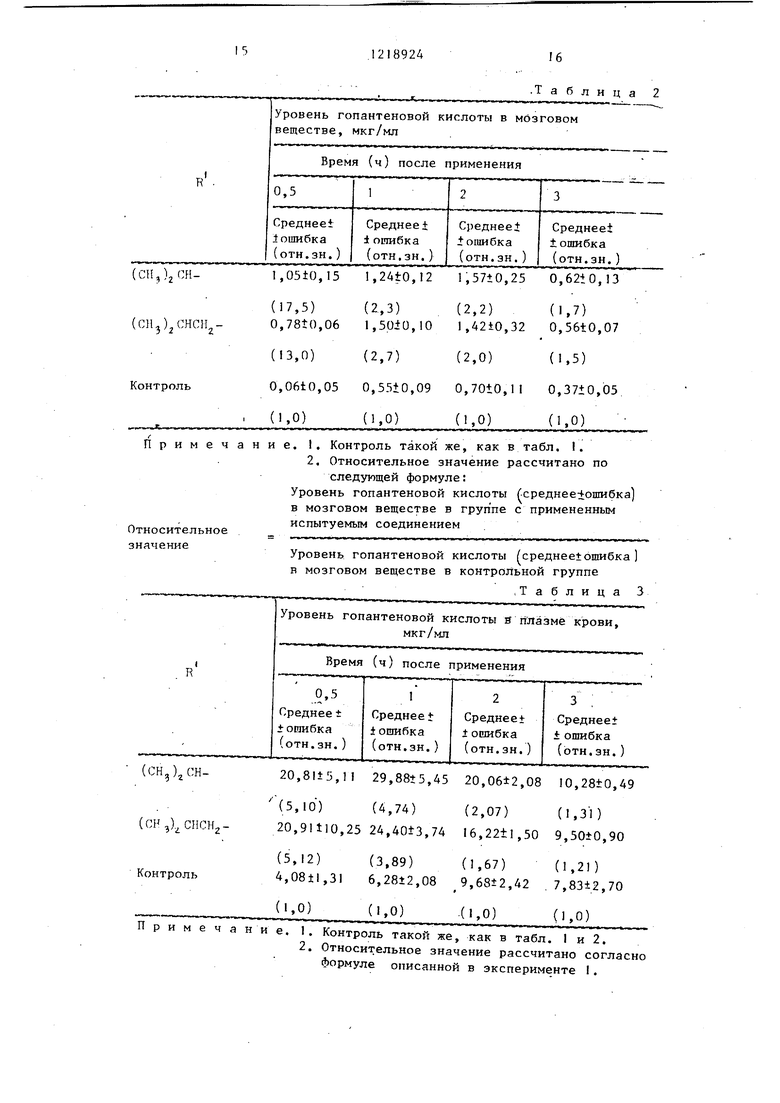
Испытывали крыс SD мужских особей весом 200 г в возрасте 7 недель голодавших в течение ночи (одна группа 4 крысы), Каждой крысе при помогщ желудочного зонда перораль- но ввели суспензию (2 мл/ испытываемого соединения в 0,5%-ном растворе карбоксиметилцеллюлозы (доза испытываемого соединения 389,4 шмоль/ /кг соответствует 100 мг/кг гопантената кальция . Через два или три часа после введения соединения головной мозг был извлечен и промыт физиологическим раствором. К мозгу прибавили в 9 раз больший объем воды, смесь подвергли гомогенизации в гомогенизаторе в течение 1 мин при охлаждении льдом и затем центрифугировали со скоростью 10000 об/мин при температуре в течение I ч. Концентрацию гопан- теновой кислоты во всплывшем слое (1 мл соответствует 0,1 г мозга) определили при помощи газовой хроматографии и масс-спектрометрии. Результаты представлены в табл. 2. Испытывались те же соединения, что в эксперименте 1.
Эксперимент 3.
Использованы три самца гончих, возраст 10 мес, выдержанных без пищи в течение ночи. Каждому догу применили орально суспензию (15 мл) испытуемого соединения (доза туемого соединения 194,7 шмоль/кг соответствует 50 мг/кг гопантената кальция. Образцы крови (2 мл) ото- брали из головной вены и поместили в гепариназные пробирки через 0,5, 1,2 и 3 ч после применения. Кровь .каждого дога центрифугировали (2800 об/мин, 10 мин) для отделения плазмы крови. Концентрацию гопанте- новой кислоты в плазме крови (0,1 мл) измеряли с помощью газовой хроматографии и масс-спектрометрии. Результаты представлены в табл. 3. Испытуемые соединения такие же, как в эксперименте 1.
Соединения (1) предлагаемого изобретения имеют низкую токсичность и, следовательно, высокую безопасность. Например, предлагаемые соединения (4-изoбyтиpилoкcи-3,3- -димeтип-2-oкcи-н-бyтиpил ) амино -н- -масляная .кислота и (4-изо- валерилокси-3,З-диметил-2-окси-н-бу тирил)амино - Н-масляная кислота показывают максимальную толерантность 2000 мг/кг при испытании на мышах (указанную максимальную толерант- 5 ность определяли путем введения испытываемого соединения мьппам, определяя затем количество погибших мышей через 48 ч после обработки; максимальная толерантность представляет
10 собой дозу, чуть меньшую, чем доза, вызвавшая смерть мышей).
Таким образом, предлагаемые соединения превращаются в гопанте- новую кислоту in vivo после введе-
15 ния их животным и обе.спечивают высокую концентрацию гопа нтеновой кислоты в крови и мозге по сравнению с гопантенатом кальция при высокой безопасности и, следовательно, яв-
20 ляются полезными в качестве лекарственных препаратов для улучшения ме- , таболизма головного мозга при расстройстве его функций. Сравнительные данные.
5 Используя методику, описаиную в экспериментах 1 и 2, измерили содержание грпантеновой кислоты в плазме крови и головном мозге после орального введения предлагаемого
0 и известного (контроль) соединений. Измерение осуществляли спустя 30 мин после введения. Результаты измерений показаны в табл. 4 и 5.
Испытуемое соединение 5
СНо
I
ВСООСНгг с- СН-СОКНШг зСООН 0СНзОН
Примечание. 1. Соединение 1 : Изoбyтиpилoкcи -3,3 ДИметил- 2-окси - Н- бу- тирил амино -н-масляная
- . .,кислота.
2.Соединение 2: (4-Изовалерилокси 3,3 Диметил-2- окси-Н(-бу тирил)амино Н-масляная кислота.
3.Контроль: кальций (2,4-дигидрок- .;- ,, ;: си-3,3-Диметил -н-бутирил) амино Н-бутират.
4.Относительное значение рассчитано с помощью следующей формулы:
Уровень гопантеновой кислоты (среднее + ошибка) в. плазме крови в группе с примененным испытуемым соединением
Относительное значение
Уровень гопантеновой кислоты среднее ошибка) в плазме крови у контрольной группы.
Таблица I
Примечание. I. Контроль такой же, как в табл. I.
2. Относительное значение рассчитано по
следующей формуле:
Уровень гопантеновой кислоты (среднее1ошибка) в мозговом веществе в группе с примененным испытуемым соединением
Относительное значение
Уровень гопантеновой кислоты (среднее±ошибка 1 в мозговом веществе в контрольной группе
,Таблица 3
Уровень гопантеновой кислоты s плазме крови, мкг/мп
(СН,)2СН(СН,).СНСИ2Контроль
20,81±5,П 29,8815,45 20,06±2,08 10,28tO,49
(5,10) (4,74) (2,07) (1,31) 20,91tlO,25 24,40t3,74 I6,22±,50 9,50±0,90
(5,12) (3,89) (1,67) (1,2J) 4,08±l,31 6,2812,08 9,68±2,42 .7,83±2,70
(1,0)
(1,0)
(1,0)
(1,0)
Примечание. 1. Контроль такой же, как в табл. I и 2.
2. Относительное значение рассчитано согласно формуле описанной в эксперименте I.
.Таблица 2
(1,0)
(1,0)
(1,0)
Таблица А
Таблица 5









| Y | |||
| Neshizava, etc | |||
| Топка с несколькими решетками для твердого топлива | 1918 |
|
SU8A1 |
| - J | |||
| of vitaminology | |||
| v | |||
| Паровоз для отопления неспекающейся каменноугольной мелочью | 1916 |
|
SU14A1 |
Авторы
Даты
1986-03-15—Публикация
1983-03-04—Подача