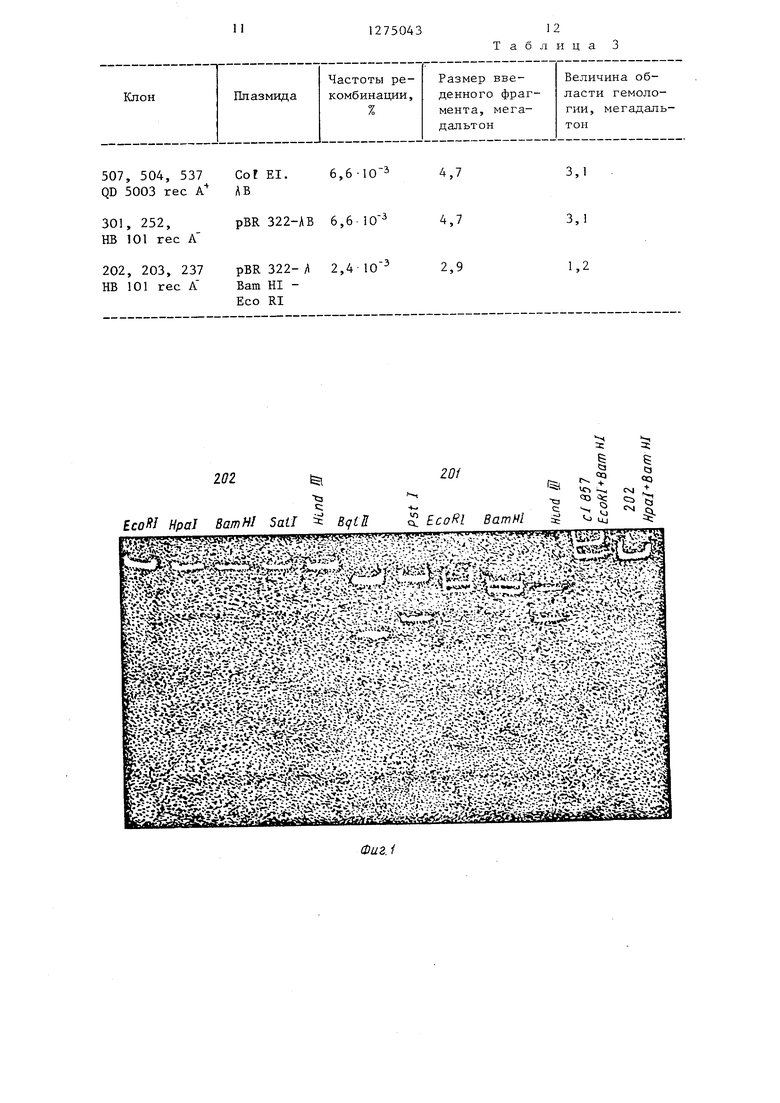
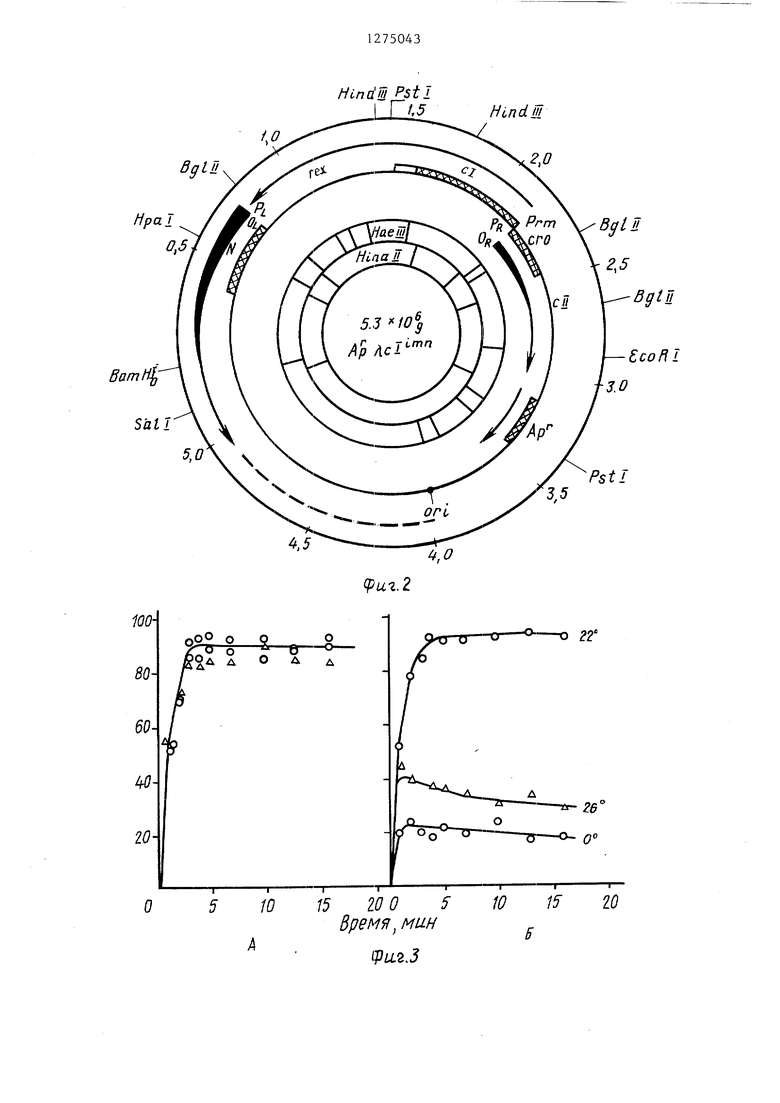
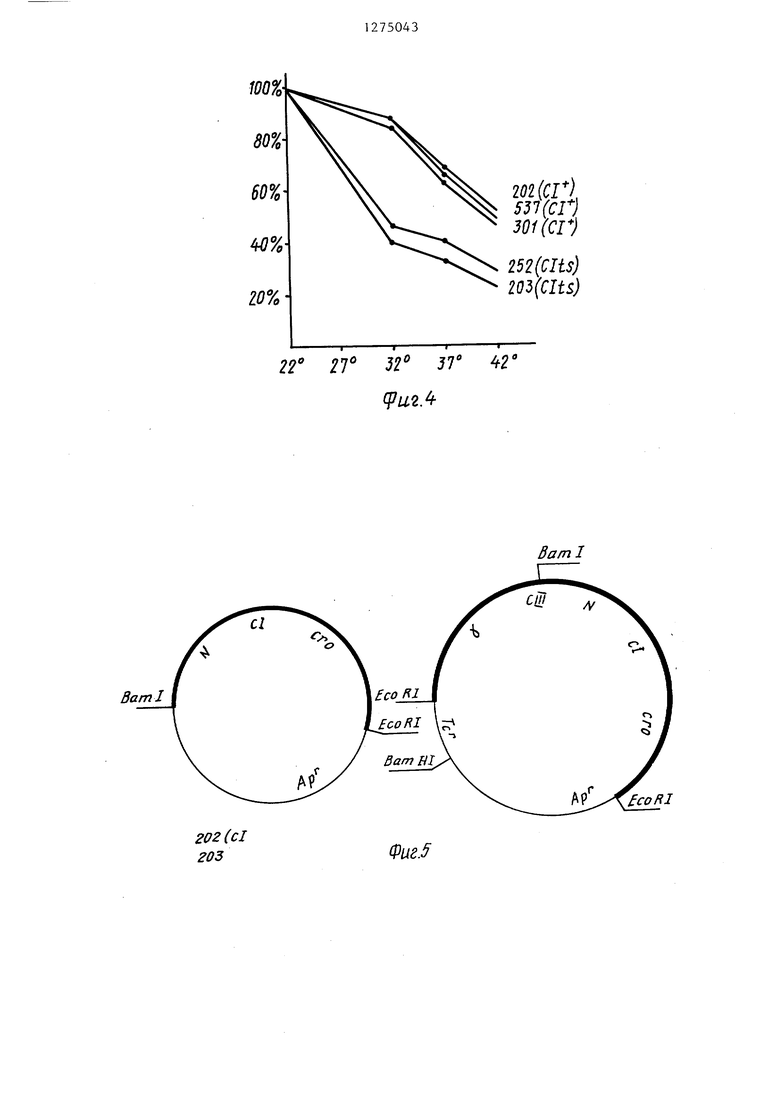
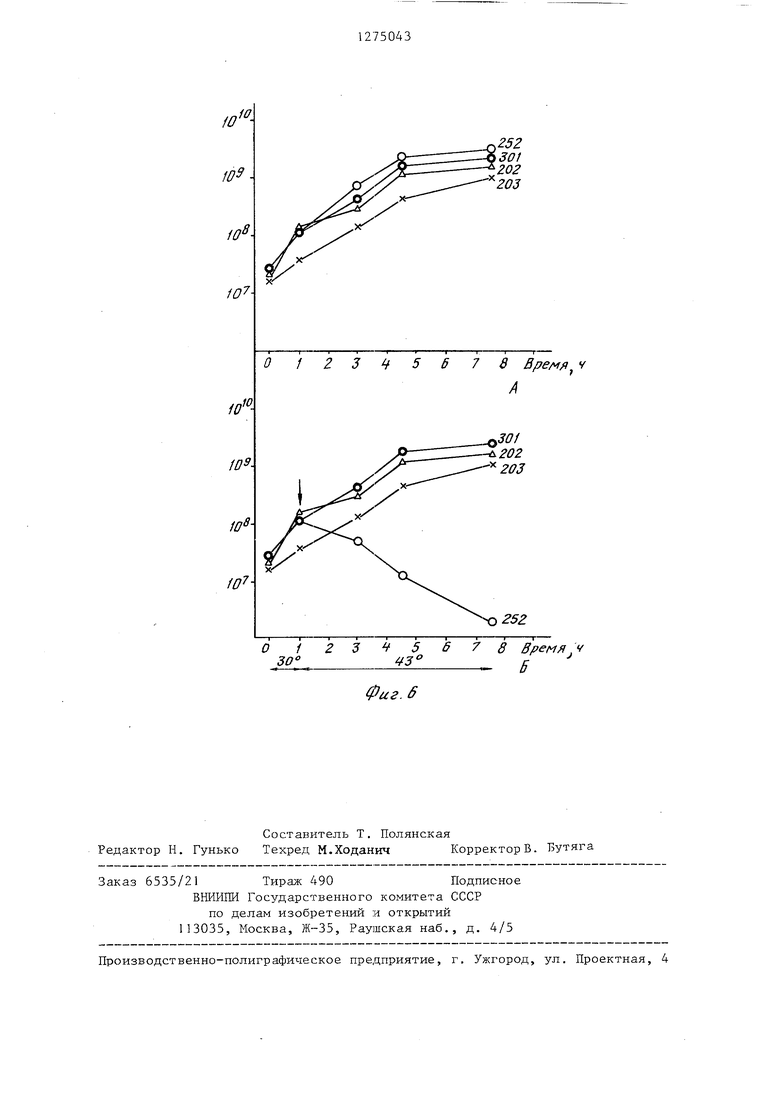
Изобретение относится к молекулярной биологии, а именно к вектору для клонирования генов, обеспечивающему регулируемую, транскрипцию чужеродных генов, и способу его конструирования . Целью изобретения является получение вектора с небольшой молекулярной массой, обеспечивающего регулируемую транскрипцию чужеродных генов На фиг. 1 представлено электрофоретическое разделение фрагментов ДНК при гидролизе различными эндонуклеазами рестрикции; на фиг. 2 - схема плазмид 202 (сГ его ) и 203 (с1 857 его 6) с точкой рестрикции и генетической картой; на фиг. 3 - кинетиъчсвязьшания репрессора с Р ДНК фа ка с1 при различных температурах; на фиг. 4 - связывание репрессора с Р ДНК фага / с1 при различных тем пературах; на фиг. 5 - схема гибридных плазмид; на фиг. 6 - кривая роста культур, содержащих различные плазмиды при 30°С и при перенесении культур на 43°С. Вектор Дочя клонирования, обеспечивающий регулируемую транскрипцию чужеродных генов, состоит из Ват HIECO RI-фрагмента плазмидной ДНК pBR 322 и Ват HI - Есо RI-фрагмента ДНК регуляторной области фага / и имеет мол. массу 5,3 мегадальтона, по одному сайту рестрикции эндонуклеаз рестрикции Ват HI, Есо RI, SaP I, Ира I, по два сайта эндонуклеаз рест рикции Pst I и Hind III, два промотора Р и Р| , сайты Ват HI и Sat I удалены от Р -промотора на 0,7 и 0,9 мегадальтона соответственно, сай Есо RI отстоит на 0,7 мегадальтон от Р -промотора и на 3,1 мегадальтона от Р -промотора, ori - репликон плаз СоЕ EI, мнды Cot hi, термочувствительный ре прессор с1 857, гены фага А cll, его (am 6), cl, rex, N, селективные маркерына расстоянии 2 мегадальтоот Ват Н1-сайта и Ар на расстоя на НИИ 3,5 мегадальтона от Ваш Н1-сайта хозяин вектора - Escherichia . Пример. Получение плазмидной ДНК Р BR 322. Клетки, содержшцие плазмиду pBR 322, выращивают в 500 мл бульона до плотности 0,6 (510 клеток на 1 мл), добавляют в культуральную среду хлорамфеникол до конечной концентрации 200 мкг/1 мл и продолжают 43i культивирование в течение 12 ч. Затем клетки собирают центрифугированием (5000 об/мин, 20 мин), промывают равным объемом буфера (50 мМ трис -НС, рН 8,0), суспендируют в 4 мл 20%-ной сахарозы в 50 мМ , рН 8,0, добавляют 1,2 мл лизоцима (5 мг/мл) и инкубируют 10 мин во льду при аккуратном помешивании. К смеси добавляют 2,4 мл 0,25 М ЭДТА рИ 8,0, оставляют во льду на 10 мин, а затем добавляют последовательно 2.6мл 5М NaCt и 1,2 мл 10%-ного додецилсу Ь(Ззата натрия, инкубируют во льду в течение 5-7 ч. Осветленные лизаты получают центрифугированием при 16000 об/мин в течение 1 ч. К экстрактам добавляют CsCt из расчета 1.7г/мл и бромид этидия до конечной концентрации 200 мкг/мл. Полученную смесь центрифугируют при 44000 об/ /мин в течение 24-48 ч. Нижнюю, прокрашенную бромистым этидием, зону собирают по каплям, нрокалывая пробирку под зоной. Полученную ДНК диализуют против 10 мМ трис -НС, рН 8,0 I мМ ЭДТА, 10 мМ NaCP. Получение ДНК фага ri . Культуру Е. coEi С600 (Д с 1857 его 6) выращивают до плотности 0,4 при 30°С, резко прогревают на газовой горелке до 42°С и инкубируют при этой температуре в течение 15 мин, затем инкубируют при 37°С в течение 2 ч при интенсивной аэрации, добавляют 0,01 обьема хлороформа и через 10 мин лизаты освобождают от клеточных обломков центрифугированием. Фаг очищают тремя циклами дифференциального центрифугирования (20000 об/мин 3 ч, 6000 об/мин) и депротеинизируют водонасыщенным фенолом при рН 8,0 (50 мМ тРис -HCf) дважды. Полученную ДНК фага А диализуют против 10 мМ ТРИС -НСР, 1 мМ ЭДТА, 1М NaCP трижды и окончательно тремя сменами 10 мМ ТРИС -НС, рН 8,0, 1 мМ ЭДТА при 20кратном разведении. Рестрикция ДНК. Ппазмидную (pBR 322) и фаговую (А с1 857 его 6) ДНК для рестрикции смешивают в соотношении 1:5 и одновременно добавляют эндонуклеазы рестрикции Есо RI и Вот HI по 0,2 мкл на каждьш мкг смешенной ДНК. Инкубацию проводят в 50 мМтрис НС г, рН 7,5, 10 мМ MgC Е, 1 мМ ЭДТА и 10 мМ дитиотреитоле (буфер А) в течение 1 ч при 37с, а затем смесь
прогревают до 70°С в течение 10 мин. Анализ полноты гидролиза проводят с помощью электрофореза в 0,8%-ной агарозе в трис -боратном буфере, рН 8,3.
Лигирование ДНК. Смешивают 225 мкл растворов фрагментов ДНК, полученных при гидролизе эндонуклеазами рестрикции (10 мкг), с 25 мкл 5 мМ АТФ и 2 мкл полинуклеотидлигазы (3000 ед/ /мл). Смесь инкубируют при 10°С в те чение 6ч, при 10-кратном разведении добавляют инкубационньй буфер А, АТФ (конечная концентрация 0,5 мМ) и полинуклеотидлигазу из расчета 1 мкл фермента на 10 мгк ДНК. Продолжают и инкубацию при 0°С в течение 2 суток.
Полученную смесь используют для трансформации.
Трансформация рекомбинантной плазмидной ДНК бактериальных клеток. 25 мл бульона заражают 0,1 мл ночной культуры Е. coti и выращивают до плотности 0,6. После 10 мин охлаждения клетки собирают центрифугированием и суспендируют в равном объеме 0,1 М MgSO . Полученную суспензию охлаждают 20 мин, клетки собирают центрифугированием и суспендируют в 0,5 объема 0,1 М CaCl. Суспензию клеток охлаждают в течение 20 мин, клетки осаждают центрифугированием и суспендируют в 1/50 исходного объема 0,1 М CaCt . После дополнительного охлаждения (30 мин) клетки используют для трансформации.
ДНК, предназначенную для трансформации, диализуют против 0,05 М СаСЕ с 10 мМ трис-НС, рН 7,5, смешивают с равным объемом СаС1,-клеток и охлаждают в течение 20 мин. Затем смес подвергают 1 мин термической обработке при 42°С, выдерживают в течение 15 мин при 20°С и охлаждают в течение 20 мин. Эту смесь после десятикратного разбавления бульоном и подращивания клеток при 30°С в течение 30 мин, наносят на чашки Петри с ампициллином (20 мкг/мл) и с фагами
N и Л h 434 imm (1-10 каждого
чзо фага на чашку).
Анализ функционирования генов в гибридной штазмиде. Вьфосшие на твердой среде с ампициллином и в присутствии фагов колонии культивируют с 1 мл бульона в течение 5 ч при 30°С, 0,1 мл культуры высевают в мягком агаре на чашки с МПА, содержащим 20 мкг/мл ампициллина. На мягкий
агар накапывают различные суспензии фагов от 1-10 до 1-10 фаговых частиц в капле.
Результаты анализа представлены в табл. 1, знаком + отмечены фаги, способные размножаться на анализируемой культуре.
Резистентность отобранных клонов к антибиотикам aIiaпизиpyют на агаризованной среде с антибиотиками ампициллиног (20 мкг/мл) и тетрациклином (20 мкг/мл). При введении фрагмента ДНК фага в плазмзду мелоду сайтами Есо R и Ват HI структурньй ген, отвечающий за устойчивость клеток к тетрациклину, нарушается (табл. 1, резистентные к антибиотикам клоны отмечены знаком +). Отбирают пять клонов, резистентных к аьмпициллину, к фагу Л с1 и не увствительные к rll мутантам фага Т4.
Выделение плазмид ускоренным методом. В связи с необходимостью одновременного анализа физической структуры плазмидных ДНК, выделенных из различных клонов, выделяют плазмиды ускоренным методом, который состоит в следующем.
Культуру выращивают в 10 мл бульона, осаждают центрифугированием при 6000 об/мин в течение 20 мин, суспендируют в 1 мл 25%-ной сахарозы в 20 мМ ТРИС -НС1 рН 8,0, добавляют 0,2 мл лизоцима (5 мг/мл) и 50 мк ЭДТА (0,25 М) . После инкубации при осторожном перемешивании в течение 10 мин во льду добавляют 50 мкл панкреатической РНКазы (1 мг/мл), предварительно прогретой при 100°С в течение 5 мин, и 0,5 мл лизирующей смеси (0,3 мл 10% тритон-Х-100, 7,5м М ЭДТА рН 8,0, 1 ,5 мл 1 М ТРИС -НС i рН 8,0, 0,7 мл НО). После инкубации при постоянном помешивании стеклянной палочкой во льду в течение 10 ми получают осветленньм лизат центрифугированием пробы в течение ч при 17000 об/мин (К-24 Janetski). Полученный лизат разбавляют водой вдвое, обрабатьшают равным объемом фенола, насыщенного 50 мМ ТРие-НС1, рН 8,0, при комнатной температуре в течение 10 мин, водную фазу собирают центрифугированием при 6000 об/мин. Оставшийся в пробе фенол удаляют эфирной экстракцией, а ДНК переосаждают 70%ным спиртом. Рестрикционный анализ рекомбинант ных гшазмидных ДНК. Для изучения физической структуры ДНК и идентификации введенного фрагмента регуляторной области фага Л плазмидную ДНК об рабатывают эндонуклвазами рестрикции Есо Rli Bam HI, Sal I, Pst I, Hind III, Pha I и Bgt II. К 0,5 МКГ ДНК в буфере, содержащем 50 мМ трис-HCl, рН 7,5, 10 мМ MgCE, 10 мМ ДТТ, 1 мМ ЭДТА, добавля ют 0,1-5 мкл зндонуклеазы рестрикции Общий объем реакционной смеси колеблется между 10 и 40 мкл при обработках различными рестриктазами. При совместном гидролизе оба фермента до бавляют к реакционной смеси и инкуби руют одновременно. Продолжительность инкубации изменяется в зависимости от активности эндонуклеаз от 30 мин до 3 ч. Для всех эндонуклеаз рестрик ции инкубацию проводят при 37°С, кро ме гидролиза плазмидной ДНК Pst I, который ведут при 30°С. Гидролизаты анализируют с помощью электрофореза реакционной смеси в 0,8%-ном агарозном пластинчатом геле в трис -боратном буфере рН 8,3. Результаты рестрикционного анализа представлены на фиг. 1 и 2. Основьшаясь на известном расположении промоторов фага и данных рестрикционного анализа, можно заключить, что сайты Ват HI и Saf I удале ны от Р -промотора на 0,7 и 0,9 мегадальтона соответственно. Сайт эндонуклеазы рестрикции Есо RI отстоит на 0,7 и 3,1 мегадальтона соответ ственно от Pj и Р . Эти расстояния можно считать достаточно небольшими, так как транскрипция, начинаясь в об ласти иммунности, продолжается влево до поздних генов фага (30% фаговой ДНК или около 10 мегадальтон) и впра во до гена О (около 5 мегадальтон). Анализ синтеза репрессора в клетках, содержащих плазмиды. Количество репрессора в клеточных экстрактах оп ределяют по методу Эхолса и Грин, ко торьп основан на анализе количества меченой фаговой ДНК, связываемой с репрессором и не задерживаемой на нитроцеллюлозных фильтрах. Этот метод использован для изучения кинетики связывания репрессора, выделенно го из различных клонов, а также для изучения уровня его связывания с ДНК при различных температурах. На фиг. 3 показано, что кинетика связьшания репрессора, вьщеленного из клеток с гибридными плазмидами, содержащими с1 дикого типа, существенно не зависит от температуры, тогда как связывание термочувствительного репрессора, синтезированного в клетках с плазмидами, несущими мутантную регуляторную область фага, заметно ухудшается при незначительном изменении температуры инкубации. Уровень связьшания репрессора при 22°С не зависит от наличия мутации и принят за 100%. На фиг. 4 показано, что степень связывания термочувствительного репрессора с ДНК быстрее уменьшается при увеличении температуры, чем репрессора дикого типа. Генетический анализ регуляторной области фага введенной в рекомбинантную плазмидную ДНК. Для доказательства одновременного присутствия мутаций в генах с1 и его проводят рекомбинацию in vivo между плазмидами и фагом А i 434 с, который дает на бактериальном газоне бляшки с мутным центром за счет эффективной лизогенизации. Штаммы, содержащие плазмидную ДНК, выращивают в 10 мл бульона до плотности 0,2 (1,6-10 клеток/мл) при 30°С, инфицируют фагом Д. 434 с множественностью 0,1, инкубируют при 30°С в течение 4 ч, добавляют 1/100 объема хлороформа и оттитровьшают на бактериальном газоне, содержащем и не содержащем профаг 434. Наличие рекомбинантов дополнительно указьшает на присутствие регуляторной области фага с1 в гибридных плазмидах. Частоту рекомбинации анализируют сравнением титра фагов на этих двух культурах при 37°С. Результаты опытов сведены в табл.3. Частоты рекомбинации соответствуют теоретически рассчитанному значению и строго зависят от величины введенного в плазмиду фагового фрагмента. Кроме того, показано, что частота рекомбинации не зависит от гена гее А Е. . Гибридный фаг, полученный при рекомбинации с плазмидами клонов 203, 237, 252, образует на газоне клеток Е. coEi С 600 при 37°С прозрачные бляшки, а при 30° - мутные, что указывает на наличие термочувствительной мутации в гене с1, тогда как рекомбинанты с плазмидами
ные бляшки. Анализ наличия в гибридных фагах супрессируемой мутации в гене его проводят сравнением эффективности титрования этих фагов на штаммах Е. coti с различными супрессорными т-РНК при 30, 38 и 43°С.
Результаты анализа, сведенные в табл. 2, указьшают на одновременное присутствие мутаций в генах его и с1, ю а также на различную степень супрессии в зависимости от типа присутствующего в штамме супрессора. По данным этой таблицы можно заключить, что гибридная плазмида содержит фрагмент is ДНК фага Л с генами с1 857, его 6. Доказательство наличия термоиндуцированной транскрипции с левого фагового промотора в плазмиде, содержащей регуляторную область фага. При о боре клонов, содержащих гибридные плазмиды, наряду с плазмидами типа 202, .203, 237, отбирают плазмиды с мол. массой 7,3 мегадальтон, описанные в данном примере 301 и 252 (фиг. 5). Рестрикционным анализом ус тановлено, что эти гибридные плазмиды содержат Есо RI - фрагмент фага Л с регуляторными генами. Кроме описанных генов этой области плазмиды содержат гены cIII, ki, j,pH EalO. Обнаружено, что клоны, содержащие эти плазмиды, очень плохо растут при 37 С. Изучают эффективность титрования этих клонов при различных температурах. Титр клеток при выращивании этих культур при 43°С понижается приблизительно на четыре порядка (фиг. 6В). При сравнении кривых роста штаммов (фиг. 6), содержащих различные гибридные плазмиды, показано, что эффект понижения титра клеток за йисит от наличия дополнительных гено и присутствия термочувствительной му тации в гене с1, которая позволяет дерепрессировать транскрипцию с левого фагового промотора (Р ). Подобньй эффект описан для лизогенных кул тур с 600 (А с1 875 ашР), и картировано местоположение гена, отвечающего за убийство клеток. Этот ген расположен в N-опероне между cIII и на зван kil. Присутствие этого гена в плазмидах оказьшает аналогичное действие. При непермиссивной температуре наблюдается накопление сильно удлиненных клеток и отсутствие прямого лизиса. Отмечено сохранение характетих повьшенную температуру в течение 6 ч. Полученные данные указывают на наличие в Есо RI-фрагменте функциопирующего гена kiI, подчеркивают его негативное влияние на рост клеток при 37-42°С, содержащих соответствующие плазмиды,. и доказьшают зависимость интенсивности транскрипции с фагового промотора Р от температуры для генов, расположенных слева от этого промотора. Таким образом, предлагаемый способ конструировггния плазмиды позволяет получить мультикопийную плазмиду, содержащую сильные промоторы с регулируемои транскрипцией. Небольшую молекулярную массу, наличие четырех уникальных сайтов (Ват HI, Sat I, Есо RI, Ира I) рестрикции И их малая удаленность от соответствуюш х фаговых промоторов позволяет широко использовать эту плазмиду для клонирования чужеродных генов. Необходимо отметить присутствие близкорасположенных сайтов эндонуклеаз рестрикции Ват HI и Saf I, которые позволяют клонировать фрагменть ДНК, пропродуцируемые такими эндонуклеазами, как Ват HI, BgE II, Bcf I, Mbo I, Sat (Xho) за счет идентичности липких концов при различной специфичности узнавания, а таклсе фрагменты, получаемые при совместном гидролизе соответствующей парой эндонуклеаз . При использовании пары Xlio I Bgl II или Xho 1 - Bel I наблюдается исчезновение сайтов рестрикции, что позволяет проводить соединение фрагментов в присутствии эндонуклеаз, не удаляя мелкий фрагмент (фиг.1). Полученные синтетические линкеы обеспечивают возможность клониования также с помощью других эндоуклеаз рестрикции. Использование репликона мультиопийной плазмиды значительно увеичивает дозу клонируемых генов, в присутствии мутаций в гене с1 и его обеспечивает возможность регуляции транскрипции в широких пределах. В присутствии хлорамфеникола количество копий плазмиды в клетке может увеличиваться на два порядка и теоретически достигать 45% тотальной клеточной ДНК, Присутствие в плазмиде гена N, продукт которого является антитерминатором, обеспечивает в ряде случаев интенсивную транскрипцию на зна чительном протяжении, даже когда кло нируемый фрагмент ДНК содержит определенные терминирующие кодоны. По приблизительной оценке подобные векторы позволяют увеличить синтез белкового продукта в сотни раз.
Наличие регулируемой транскрипции позволяет при необходимости клонировать гены, вызывающие гибель бак териальных клеток, и получать значительные количества продуктов этих ге нов при повышении температуры.
Известны примеры, когда введение эукариотных генов в векторную ДНК
7504310
фага А в отличие от тех же генов в составе плазмиды дает транскрипцию этих генов под контролем левого промотора фага 1 . Это позволяет пред5 положить, что описанная в примере плазмида должна обеспечить эффективную транскрипцию, по крайней мере, некоторых генов эукариотного происхождения . 10
Предлагаемая плазмида является специализированным вектором, с помощью которого возможно создание штаммовсуперпродуцентов различных белков, а 15 также некоторых других веществ биологического происхождения.
Таблица 1




| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения плазмидной рекомбинантнойдНК, СОдЕРжАщЕй гЕНы РЕСТРиКТАзыи МЕТилАзы | 1979 |
|
SU852939A1 |
| Рекомбинантная плазмидная ДНК @ ,способ конструирования плазмидной ДНК и штамм-продуцент эндонуклеазы рестрикции @ | 1983 |
|
SU1130602A1 |
| Рекомбинантная плазмидная ДНК @ 435,кодирующая синтез ДНК-лигазы фага Т 4.способ ее конструирования и штамм @ . @ ВКМ в-1449-продуцент ДНК-лигазыфага Т4 | 1981 |
|
SU1122003A1 |
| Способ конструирования рекомбинатной плазмидной ДНК и штамм продуцент эндонуклеазы рестрикции | 1982 |
|
SU1074139A1 |
| Векторная плазмидная ДНК рТК 1285, предназначенная для интеграции чужеродного фрагмента в геном вируса осповакцины, и способ ее конструирования | 1988 |
|
SU1640164A1 |
| Фагово-плазмидный вектор @ 131 и способ его конструирования | 1985 |
|
SU1280009A1 |
| Рекомбинатная плазмидная ДНК pGp 120 - 428, кодирующая гибридный белок с антигенными свойствами белка @ р 120 ВИЧ-1 | 1991 |
|
SU1789562A1 |
| РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК РДТИ 23, СПОСОБ ПОЛУЧЕНИЯ РЕКОМБИНАНТНОЙ ПЛАЗМИДНОЙ ДНК РДТИ 23 И ШТАММ БАКТЕРИЙ ESCHERICHIA COLI, СОДЕРЖАЩИЙ РЕКОМБИНАНТНУЮ ПЛАЗМИДНУЮ ДНК РДТИ 23 - ПРОДУЦЕНТ СЛИТОГО БЕЛКА ДТИЛ 2 | 1993 |
|
RU2077585C1 |
| Рекомбинантная плазмидная ДНК рСЕК 10,кодирующая синтез фрагмента Кленова ДНК-Полимеразы 1 Е.coLI,и способ ее конструирования | 1986 |
|
SU1392094A1 |
| Способ конструирования вектора pVM061 | 1983 |
|
SU1479004A3 |

1. Вектор для клонирования генов, обеспечивающий регулируемую транскрипцию чужеродных генов, состоит из Ват HI - Есо RI-фрагмента плазмидной ДНК pBR 322 и Ват Hi Есо RI-фрагмента ДНК регуляторной области фага/ , имеет мол. массу 5,3мегадальтона, по одному сайту рестрикции эндонуклеаз рестрикции Ват HI, Есо RI, SaE I, Нра I, по два сайта эндонуклеаз рестрикции Pst I и Hind III, два промотора Р « Р , сайты Ваш HI и Sa I удалены от Р -промотора на 0,7 и 0,9 мегадальтона соответственно, сайт Есо RI отстоит на 0,7 мегадальтона от Р -промотора и на 3,1 мегадальтона от Р -промотора, ori - репликон плазмиды Со EI, термочувствительный репрессор с I 857, гены фага Д с II, его (атб), с I, rex, N, селективные маркеры расстоянии 2 мегадальтона от Ват HIсайта и АР на расстоянии 3,5 мегадальтона от Ват Н1-сайта, хозяин вектора - Escherichia coEi. 2. Способ конструирования вектора для клонирования генов, включающий гидролиз донорной и реципиентной ДНК эндонуклеазами рестрикции, соединение образовавщихся фрагментов ДНК с помощью полинуклеотидлигазы, трансформацию клеток Escherichia смесью полученных гибридных ДНК, отбор клонов. Содержащих гибридные плазмиды, выделение вектора для клонироваi ния, отличающийся тем, что, с целью получения вектора с меньсл шей молекулярной массой, обеспечивающего peгyлиpye гyю транскрипцию чужеродных генов, в качестве реципиентной ДНК используют ДНК плазмиды pBR 322, в качестве донорной ДНК - ДНК фагаД с1 857 его 6, а гидролизу подвергают ND СЛ смесь донорной и реципиентной ДНК, из эндонуклеаз рестрикции используют эндонуклеазы Ват HI и Есо RI, О при этом последние вносят в реакциNU онную смесь одновременно, отбор клооо нов, содержащих гидридные гшазмиды, проводят на среде с ампициллином в присутствии фагов / с1 и h 434 imm/ cl, причем из клеток вьщеляют вектор для клонироваш-ш, содерх ащ1сй ДНК регуляторной области фага А , включающей ранние промоторы фага , и гены репрессоров с мутациями с1 857 и его am 6.
201с1
202с
203с1 252 cl 301 cl
301 cl
304 cl
- + Примечание. В нижней части табл. 2 данные.
+ +
+ + -I- +
+ +
+ +
+ ++
+ +
Таблица 2 представлены известные 507, 504, 537 Co El. QD 5003 rec A 301, 252, pBR 322-AB HB 101 rec Л 6,6 -10 6,6 10 HindinPstl 7.5 PstI
100%
80%
60%
%
10%
т(сГ
(СГ) 301 (СГ)
252(CIts) 20ЦСШ)
22° 2Г 32° 37 42 BamI (pu2. .5
10
8
10
i07
0 1 2 3 ч 5 6 7 8 BpCMfl ч
A
w 810
fl}70 Врем V 30° ,
Фиг. 6
| НАТЯЖИТЕЛЬ ЦЕПИ РАСПРЕДЕЛИТЕЛЬНОГО ВАЛА ДВИГАТЕЛЯ ВНУТРЕННЕГО СГОРАНИЯ | 2004 |
|
RU2281426C2 |
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
| Планшайба для точной расточки лекал и выработок | 1922 |
|
SU1976A1 |
| HeEinski D.R | |||
| et а in | |||
| Recombinant Molecules | |||
| - Raven | |||
| Press, New York, 1977, p | |||
| Двухколейная подвесная дорога | 1919 |
|
SU151A1 |
Авторы
Даты
1986-12-07—Публикация
1978-09-13—Подача