Изобретение касается способа получения новых производных бензоатных эфиров 3-оксиморфинанов общей формулы
I /
(I)
где Y - водород или 4-, или 5-алкокси группа с числом атомов углерода от 1 до 4, X - OR , где R - СО-алкил Ст-С
или С-,-С4-алкш1, R - циклопропилметил или циклобутилметил,
R, - ОН
R - ОН или 0,
которые могут использоваться в качестве болеутоляющих средств или антагонистов наркотиков.
Цель изобретения - биоусвояемости 3-оксиморфинанов при оральном введении.
Используемые обозначения представляют собой следующие соединения:
налбуфин: (-)-17-(циклобутилме- тил) -4, Зв -эпоксиморфинан-3, 6о, 14-три ол или его соль,
налтрек сон: (-)-17-(циклопрошш- .метид)-4 , 5 /-эпокси-3,14-диоксиморфи- нан-6-он или. его соль,
налоксон: (-)-17-аплш1-4,5о(-эпок- си-3,14-диоксиморфинан-6-он или его
соль,
бупренорфин; (-)-17-(цшслопропил- метил)-а-(1,1-диметилэтил)-4,5-эпок- си-18,19-дигидро-3-окси-6-метокси- -(/-метилгб, 14-этеноморфинан-7-метано или его соль.П р и мер 1. Налбуфин-3-(аце- тилсагшцилат)
О
п
( -СНзСО, Y Н).
В круглодонную колбу заливают 35 мл хлористого метилена и раство ряют в нем 3,57 г (0,01 моль) налбу- фина. Затем добавляют 1,11 г (0,011 моль) триэтиламина и охлаждают раствор до 0-5°С. После этого к содержимому колбы добавляют по каплям при интенсивном перемешивании раствор 2,18 г (0,011 моль) ацетилса- i лицилоилхлорида if 25 мл хлористого метилена в атмосфере азота при 0-5 С
0
5
0
5
30
о
После окончания добавления ледяную баню удаляют и реакционную смесь пе- ремешивают в течение 5 ч при температуре окружающей среды. По данным тонкослойной хроматографии (сили- кагель, смесь этилацетата и гег.сана в соотношении 3:1) образуется целевой продукт со следами налбуфина. Реакционную смесь промывают 10%-ньм раствором карбоната натрия и затем в одой, высушивают над сульфатом натрия, фильтруют и упаривают. Твердый остаток растирают с эфиром, фильтруют и высушивают на воздухе. В результате получают 4,6 г налбуфин-3- -(ацетилсалидилата) с т.пл. 165- 68°С, По данным тонкослойной хроматографии образуется целевой продукт с R 0,22, содержащий примеси с E.f 0,01 и 0,09.
Полученный продукт подвергают очистке с помощью жидкостной хроматографии под давлением в колонке диаметром 50 мм и длиной 300 мм, заполненной силикагелем с размером зерна 15-25 мкм. Продукт растворяют в хлористом метилене и заливают в колонку. Элюирование осуществляют, смесью гексана и ацетона в соотношении 70:30. Б результате получают 3,6 г очищенного продукта с т. пл. 172-173°С. На тонкослойной хромато- грамме имеется одно пятно, R 0,22. .. По данным высокопроизводительной жид- 35 костной хроматографии полученный продукт имеет чистоту выше 99%.
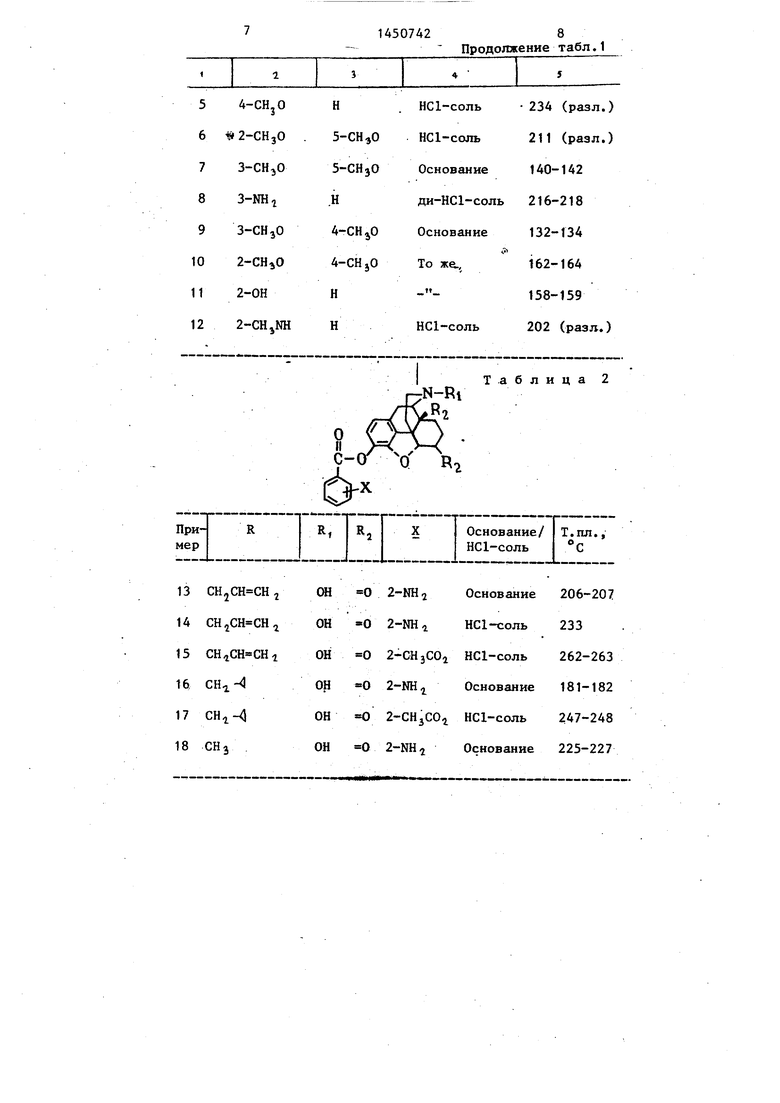
Аналогичным образом, но с.применением других исходных, могут быть получены следующие соединения (табл. 1).
Пример 15. Налоксон-3-(аце- тилсалицилат)-гидрохлорид (формула I, где R CHiCH CH, R, ОН, R О, 45 X 2-СН5СО. Y Н). .
Проводя процесс по примеру 1, из 10 ммоль налрксона получают 4,1 г налоксон-3-(ацетилсалицилат)-гйдро- хлорида с т.пл. 262-263 С.
П р. и м е р 17. Налтрексон-З- -(ацетш1салицилат)-гидрохлорид (формула I, где R , RI ОН, R О, X Y Н).
Проводя процесс по примеру 1, из 10 ммоль налтрексона получают 3,9 г налтрексон-3-ацетилсалицилат-гидрО7 хлорид с т.пл. 247-248 С.
В табл. -2 приведены характеристики соединений согласно примерам 15
50
55
и -16, а также других соединений, кторые могут быть получены предлагамым способом.
Предлекарства 3-оксиморфинанов формулы (I) в соответствии с изобретением могут вводиться в целях болеутоления различными способами,обес- печиваю1дими контактирование активного компонента с чувствительными центрами в организме млекопитающего. Они могут вводиться любыми существующими известными способами введения фармацевтических препаратов как в виде индивидуальных анальгетиков, так и в композиции с другими терапевтическими агентами. Они могут вводиться сами по себе, однак целесообразно вводить юс вместе с фармацевтически приемлемым носителем. Выбор того или иного носителя определяется исходя из способа введения и стандартной фармацевтическо практики.
Предлекарства по предлагаемому способу могут вводиться орально в виде твердых форм, например в виде таблеток, капсул, или порошка, или в жидкой форме, например в виде элисиров, сиропов и суспензий.
Целевые соединения представляют собой Предлекарства лекарств налок- сон, налтрексон и налбуфин, находящиеся в продаже. Поскольку первые два из этих лекарств представляют собой антагонисты наркотиков, а налбуфин - одновременно агонист и антагонист наркотиков, который не зарегистрирован в качестве наркотика, как , например, морфин и другие чистые агонисты наркотиков, токсичность этих лекарств, исходя из коммерческих лекарств, является .низкой. Биологические испытания. Результаты проведенных испытаний свидетельствуют о том, что новые соединения формулы (I) по предлагаемому способу повьплают биоусвояемость 3-оксиморфинанов при оральном введении композиции. Методы.
Для оценки эффективности предле карств 3-оксиморфинанов по предлагаемому способу проводят опыты по определению скорости их гидролиза в человеческой плазме и плазме крыс, а также биоусвояемости 3-оксиморфинанов у собак и крыс при оральном введении им Предлекарства. KoHueHT-
ое1450742
10
5
рацию 3-окси-морфинана определяют с помощью аналитической высокоразрешающей хроматографии. Детектирование осуществляют с помощью электрохимического датчика, реагирующего на фенольную гидроксильную группу (в 3-положении) и, следовательно, не реагирующего на Предлекарства с защищенной группой в этом положении. Концентрацию плазмы определяют после экстракции растворителем. Гидролиз плазмы.
Предлекарство добавляют в свежей плазме (не поЗже, чем через 24 ч после изъятия) в таком количестве чтобы концентрация его составляла 0,28 мкмоль, выдерживают плазму при 37 С и определяют скорость появления в ней лекарства.
Биоусвояемость 3-оксиморфинанов при оральном введении.
Крысам и собакам вводят внутривенно и орально З-оксшюрфинаны и 5 орально предлекарство формулы (I). Как правило, Предлекарства вводят в виде водных растворов, приготовленных непосредственно перед введением. Отдельные собаки получают ле- Q карства или Предлекарства в твердой форме. Отбирают плазму и замораживают ее до определения концентрации 3-оксиморфинана. Для 1 аждого животного определяют площадь под кривой зависимости концентрации 3-оксифор- S минана в плазме от времени (AUC). Биоусвояемость 3-оксиморфинана (F) рассчитывают по формуле
0
F
AUC
Ро
Do Se
AUC w « DoSe Pt
100/0.
F означает количество (%) лекарства, перешедшего в плазму. Относительную биоусвояемость (RB) определяют путем сравнения биоусвояе- мости 3-оксиморфинана при оральном введении Предлекарства () с биоусвояемостью орально введенного лекарства ()
Ь pro
RE
e -i)0
Результаты опытов с налбуфином.
Как показали опыты по биоусвояемости налбуфина при оральном введе- НИИ и скорости гидролиза предлекар- ства в плазме in vitro, собаки оказались ближе к человеку, чем крысы и обезьяны.
5
В табл. 3 приведены результаты по биоусвояемости (%) налбуфина при оральном введении у различных млекопитающих. По биоусвояемости налбуфина при оральном введении собаки . (5,4%) ближе всех других подопытных животных к человеку (14%).
В табл 4 приведены периоды полураспада при гидролизе налбуфин-аце- тилсапицилата в качестве преДлекарст ва налбуфииа в плазме t 1/2 (ч) различных млекопитающих.Период полураспада в плазме собак ближе по величине к периоду полураспада в плазме человека.
С учетом результатов, приведенных в табл. 3 и 4,- МО5КНО сделать вывод, что наиболее характерным критерием при доклинической оценке предлекарст является биоусвояемость их при ораль ном введении у собак.
В табл. 5 приведены значения относительной бкоусвояемости (RB) у собак различных предлекарств 3-ок- симорфинанов по предлагаемому способу. Формула изобретения
Способ получения производных бен- зоатных эфиров 3-окс1- морфйнана общей формулы
0
о т
5
0742
где
Y
X R R, - Ro водород, с числом 1 до 4, OR , где
6
4- или атомов
5-алкокси углерода от
К - СО-алкил
или С,-С4-алкил,
циклопропилметил, циклобутилметил,
ОН,
ОН или 0,
чающийся тем, что срответствующий 3-оксиморфинан в ап- ротонном растворителе подвергают взаимодействию с ацилирукяцим агентом общей формулы
и
где Y и X имеют указанные значения, в присутствии основания, такого как триэтиламин, N-метилморфолин, пиридин, карбонат натрия при температуре от 0°С до комнатной.
Приоритет по признакам: от 05.07.84 R - циклобутилметил, R.J - ОН;
от 14.05.85 - все остальные значения радикалов.
Таблица 1



Изобретение касается гетероциклических соединений, в частности : способа получения производных бен- зоатньсс эфиров 3-оксиморфинана общей формулыjj.p г-0 . где Z - группа формулы -С(0) .jXY, Y-H, 4- или 5-С f-4 Злкоксигруппа, X - OR , R С(0)-С,- -алкил или С .-алкил, К-циклопропилметил, цик- лобутилметил, ОН, R - ОН или 0, которые могут быть использованы в медицине в качестве болеутоляющих средств или антагонистов наркотиков. Цель - повышение биоусвояемости 3- -оксиморфинанов при оральном введении. Процесс ведут реакцией 3-оксиморфинана и ацилирующего агента - ZC1 в присутствии основания (три- этиламин, N-метилморфолин, пиридин, 3) в среде апротонного растворителя при . Новые соединения позволяют повысить биоусвояемость ,3-оксиморфинанов у собак при оральном введении в 1,7-70,34 раза. 5 табл. СО
Г.он
СНг
СНз
ОН 0 2-Ш Основание 181-182 ОН 0 2-СНзСОг НС1-соль 247-248 ОН 0 2-Ш-г Основание 225-227
Млекопитающие
Крысы2,7+0,4
Собаки . 5,4 ± 0,9
Обезьяны . 0,9,±1,6
1/ Человек1 ч
20 мг налбуфина/кг, 4 мг налбуфина/кг, мг в виде таблетки или раствора.
Таблиц
Млекопитающие
лат
0,2
2,8
.0,6
6,2
Пример
RB у собак (биоусвояемость 3-оксиморфинана при оральном введен ш 1)
13,929,5 42,7
71,9.
81,7
115,9
J670,34 (+30,1)
Заказ 6981/58 Тираж 370 Подписное -полигр. пр-тяе, г. Ужгород, ул. Проектная, 4
Биоусвояемость нал- буфина, % от введенной дозы + SE
Налбуф 1Н- аце тил салициТаблица 5
| Патент США № 3254088, - | |||
| .кл | |||
| Прибор для периодического прерывания электрической цепи в случае ее перегрузки | 1921 |
|
SU260A1 |
| СЛОИСТАЯ СТРУКТУРА ИЗ ПЛАСТИЧНОГО МАТЕРИАЛА ДЛЯ ПОЛУЧЕНИЯ КЕРАМИЧЕСКОЙ ОБЛИЦОВОЧНОЙ ПЛИТКИ | 2006 |
|
RU2323192C1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1989-01-07—Публикация
1985-07-04—Подача