1
Изобретение относится к способу получения новых,2Н-хроменов, которые являются аналогаьда вьщeляe ыx из природных веществ прекосена-1 (PI) и прекосена 2 (Р2), обладают биологи- ческой активностью по отношению к насекомым, и могут найти применение в качестве нового средства дня борьбы с вредителями в сельском хозяйстве.
Цель изобретения - получение ног вых 2Н-хроменов, обладаюишх ценными ;биологически активными свойствами.
Чистоту получения соединений контролируют методом тонкослойной и газовой хроматографии, а их структуру с помощью ИК-, ЯМР-спектров и масс- спектрометрии,
Пример. 7-н-Пропокси-8-мет- окси-2,2-диметил-2Н-хромен.
Суспензию 5,5 г (30 ммоль) 2-мет- окси-3-н-пропоксифенола, 6,5 г
(60 ммоль) З-хлор-З-метилбут-1-ина, 5 г карбоната калия и 8 г йодистого калия в 50. мл абсолютного ацетона кипятят при перемешивании в течение 20 ч. Неорганическую соль отсасывают а-остаток после упаривания фильтрата кипятят в течение 8 ч в 100 мл К,Ы-диметиланилинао После этого ре- акционьтую смесь оставляют стоять на ночь и затем разлагают 200 мл 5%-но- го раствора хлористого аммония. После обычной обработки и очистки с помощью колоночной хроматографии (силикагель-60-; элюент смесь гексана и эфира в соотношении 9:1) получают бесцветную маслянистую жидкость. Выход 5,8 г (80%).
Получаемый промежуточньй продукт j( - -диметилпропаргил)окси-2- метокси-ЗН-пропилоксибензол (бесцвет кое масло) хдоактеризуется следующими данными ЯМР и МС.
Н-ЯМР (CDCl.j)s 1,02 (ЗН, t, j 7 Hj,); 1,65 (6Н, S); 1,8 (ЗН, m); 2,6 (Ш, S); 3,8 (ЗН, S); 3,85 (2Н, q, He); 6,7-7,4 (ЗН, m).
MC (Ei/M)E: 248 (67%); 233 (100% Аналогичным образом получают соединения, представленные в табл. 1.
Поскольку соединения формулы (I) обладают биологической активностью по отношению к насекомым, они могут найти применение в качестве нового средства для борьбы с вредителями. Биологическая активность прекосенов механизм их действия и метаболизм описаны в многочисленных публикациях, согласно которым действие этих активных eeDiecTB выражается в нару- шении деятельности органа Corpora allata, вырабатывающего ювенильные Г ормоны в организме насеко1 ых. В результате исследований природных соединений установлено, что биоло- гическая активность их зависит от 2 хроменового кольца.
В результате исследований устанолено, что известные 2Н-хромены, такие как 6-метокси-7-этокси-2,2-ди- метил-2Н-хромен (РЗ Zr 3623) и 6- метокси-7-изопропокси-2,2-диметил-2Н- хромен (Р4), обладают значительно высокой активностью.
Определение тормозящего действия на развитие насеком)1х и нематоцид- ного действия.
Жук картофельный.
Круглые черви Caenorhabditis ele- gans; Meloidogyne marioni.
50%-ные эмульгируемые концентраты предлагаемых активных веществ имеют следующий состав ;
Активное вещество,г 500 Арилан С.А., г64,2
Луброл N13, г40,0
Аромасол, млДо объема
1000,0
На отдельных насекомых и ,червях i испытания проводят следующим образом.
Хлопковые клещи.
Из испытуемых активга 1Х веществ готовят ацетонные растворители различных концентраций. По 0,2 мкл раствора с помощью шприца Гамильтона наносят на спину 50 личинок, находящихся на второй стадии развития. Актив- ное вещество абсорбируется кутикулой Личинки выдерживают в чашке Петри с семенами хлопчатника и водой. После линьки определяют степень развития оставшихся в живых насеко№ х, а также количество выведшихся из отложенных яиц насеко1 1х (личинки капустницы, картофельный жук).
Из 50%-ного эмульсионного концентрата готовят водные растворы различной концентрации и опрыскивают ими капусту. После высыхания жидкости на растения (в том числе и на контрольные, необработанные растения помещают по 20 личинок, находящихся на второй стадии развития и освещают- кх в течение длительного времени (18 ч при освещении, 6 ч в темноте). Изъеденные растения при необходимости заменяют отработанными таким же образом свежими растениями. После окончания испытаний определяют число погибщих особей, степень развития личинок, а также морфологические изменения куколок и взрослых на- секомзк.
Colaphellus Sophiae. Двухнедельные растения горчины опрыскивают препаратом, состоящим из
5
0,1 г активного ве1чества, 0,5 мл диметилсульфоксида, 10 мкл 50 ЕС-добавок и 10 мл воды. После высыхания жидкости на растения (в том числе и на контрольные, необработанные рас- тения) помещают по 20 личинок Cola phellus Sophiae, находящихся на вто- рой стадии развития. Каждые два дня изъединенные растения заменяют свежими, обработанными таким же образом растегшями. После окончания испытаний определяют .количество вылупившихся из куколок взрослых насекомых. Мухи .комнатные.
Личинки мух выдерживают в стеклянных сосудах 30 X 100 мл с питательной средой, состоящей из 2 мл молока, 2 мл воды, 2 г отрубей пшеницы и О, г насып1.енного спиртового- раствора нипагкна. Активные вещества растворяют 3 молоке, готовя 0,1%-ные растворы, что соответствует 0505%-но концентрации их в питательной среде. После добавки к питательной среде активного вещества в сосуды, помещают по 25 личинок (в контрольный сосуд активное вещество не вводится), находящихся на первой стадии развития, и сосуд) закрывают пробкой с воным затвором. После развития из .личинок куколок их извлекают из сосудов и выдерживают в чашках Петри диаметром 25 мм до вылуппения мух. По- спе окончания испытаний определяют количество вьшупивщих.ся мух.
Caenorhabditis elegans.
На несодержавще бактерий NGM-ara- ровые пластинки наносят 0,5 мл раствора активного вещества в ацетоне и после высыханш раствора помещают на них 25-30 молодых червей. Через 24 ч определяют количество живых и мертвых червей.
Meloidogyne inarioni.
Собирают яйца червей с корешков томатов и выдерживают их на фильтре в стерилизованной воде при 25°С до ин2 убации. Вылупившиеся личинки выдерживают в течение 24 ч в питательной среде. На несодержащие бактерий NGM-агаровые пластинки в чашках Петри с питательной средой наносят 0,5 мл раствора активного вещества в ацетоне и после удаления растворителя наносят на них 5 мкп суспензии личинок, приготовленной из зараженных личинок, находящихся на вто684186
рой стадии развит : я. Через 72 ч опре- делякгг число живых к мертвых особей. Результаты действия на хлопкового g клып.а, лнчин ш калустнииьг, Coldpbt; - lus sophiaes кo G:aтньix картофельного и Caenoihabditis elegans приведень: в табл. 2.
Испытания на токсичность проведе10 нкя на мышах (СГЬР-род, ве с 20-26 г). Соединения суспенд. фуют в Тх-гееп, вводят per, OS. Животные наблюдаются в течегшп 7 дкан. Значение LD ыг/кг рассчитывают по L.i( 5 Uilooxon, Получентле значения ток- сичко сти дня соединений (I) мей:ду 200-1200. Данные по токсичности LD, дл.я R., R.J и Кд рлвкы 200., 250 и 310 мг/кг соответственно.
20
Формула изобрятення
25
1. Способ получеш я 211-хроменов общей ф ормулы
где R и R.J низший аякил; водород, низшн катоксигруппа;
тi..
Rj - водород, низши -5 алкнл гп;/
R - водород; 355 с ЭТОКСИ-, н-пропокси-, кзобутокси-, изопропокск-, втор,бутскси, проларгг лок- сигруппа;
Rg - водород Ш1Н метокскгруппа.
D
о т л и чающийся тем, что
фенол общей формулы
% HivY
Нб
Bjs RE,- и 6 имсю-т указанные
значения,
подвергают взаимодействию с производ- ныьш ацетилена общей формулы
UR2
х5RI
где R и R имеют указанные значения;
X - галоген, в присутствии основания и галогенида
щелочного металла в качестве катализатора в среде биполярного апротон- ного растворителя при кипячении, полученные соединения общей формулы
R.
R
где R,,R,,R,,R4, указанные значения,
подвергают циклизации с Ы,Ы диметил или К,Н-диэтиланилином при 190-210 С.
2, Способ по п. , отличающийся тем, что в качестве биполярного органического растворителя используют ацетон или Н,М-диметил- формамид, в качестве основания используют карбонат калия и в качестве га- логенил,а щелочного металла - иодид калия.





| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных пирролидина или их солей с неорганической кислотой | 1984 |
|
SU1416056A3 |
| Способ получения производных хлорметилхинолина | 1983 |
|
SU1516010A3 |
| Способ получения производных N-деметил-морфинов | 1985 |
|
SU1398776A3 |
| Способ получения производных 1,4-дигидропиридина | 1987 |
|
SU1607687A3 |
| Способ получения производных 2-бензимидазол или 2-имидазопиридинсульфонамида | 1987 |
|
SU1813087A3 |
| Способ получения производных хлорметилхинолина | 1987 |
|
SU1748645A3 |
| Способ получения производных 3,7,11-триметил-2,4-додекадиеновой кислоты | 1981 |
|
SU1069621A3 |
| Способ получения пептидов | 1987 |
|
SU1560058A3 |
| Способ получения производных цефалоспорина или их солей с щелочными металлами или их сложных эфиров (его вариант) | 1981 |
|
SU1077572A3 |
| Способ получения производных цефалоспорина или их фармацевтически приемлемых солей с основаниями или кислотами | 1981 |
|
SU1077573A3 |
Изобретение касается замещенных гетероциклических веществ, в частно cT H jnony4e2№ H 2H;;;2cpoMeHoB общей ф-лы: CR CR GB CRb-C-C-CH CH-CR, где RJ и RJ - низший алкил; К - водород, низший алкил или кетоксигруппа; R - водород; R - этокси-, н- пропокси-, изобутокси-, изопропокси-, втор.бутокси-, пропаргилоксигруппа; Rg - водород или метоксигруппа, которые могут быть использовань; в сель- , ском хозяйстве для борьбы с вредителями различных культур. Цель изобретения - создание новых веществ активностью, не характерной для указанного класса. Их синтез ведут кипячением соответствующе замещенного фенола с производным ацетилена: СНеС - где R, и R - см. вьппе; X - галоген, в присутствии основания и катализатора - галогенида щелочного металла (KJ) в среде биполярного апротонного растворителя. В качестве последнего целесообразно использовать ацетон или К,Ы-диметш1формамид. Затем проводят циклизацию полученного вещества с помощью N,N-димeтил- или N,N-диэтиланилина при 190-210 С. Новые вещества практически до 100% уормозят развитие насекомых - хлопковых клещей, личинок капустницы, картофельных жуков, комнатных мух. Токсичность для животных LDj;o 200- 1200 мг/кг. 1 з.п. ф-лы, 7 табл.. § С Voa I
Маткл И
Н в-Пропоксн Н
72
iSaran МЕТИЛ Н ИэоЗутокси Н
73
Метил.Н
НетияВ
HcrsranВ
HenmН
НетяяН
йствя8 йетвпН
МетйЛВ
МетилН
Н Зтоксн Метил 50
Н н-Пропокси Метил 69
Н Изсхпропок- Menm 78 си
R втор.Бут- Метин 82 окси
Н Изовуток- Метил 80 ся
Н ЭтоксяМеток- 49
си
Я и-Пропок- Меток- 80 сиси
Н втор.Бут- Меток- 59 окся Си
Н Изопропок- Наток- 50 сиси
15 R.
0.94 (); 1,36 (6Н; S); 1,7 С2Н; т); 3,8 (2Я; t;
); 5,34(1Н; d; ): 6,1&(1Н; d; ); 6,3 (2Н; m);
6,76 (Ш; d; ).
1,24(6Н; d; J-6); 1,36(6H; S); 4,4 (Ш; m); 5,34 (IH; d;
); 6,16 (IH; d; ); 6,3 (2H; m); 6,76 (IH; d; ).
0,96, (6H; d; ); ,34 (6H; S); 2,0 (IH; ra); 3,6 (2H; d;
J-3); 5,34 (IH; d; J -iO); 6,i6 (18; d; J-IC); 6,3 (2B; m);
6,76 (IH; d; ).
1,32 (3H; t; ); 1,36 (бН; S); 2,2 (3H; S); 3,9 (2H; q;
J-6); 5,4 (IH; d; ); 6,6 (2H; m); 6,36 (IB; d; J-lO).
0,96 (3H; t; J-6); 1.36. (6H; S); 1.7 (2B; m); 2,16 (3H; S);
1,24 (6H; d; ); 1,36 (6H; S); 2,16 (3H; S); 4,4 (tH; m)5 5,38 (Ш; d; J°10); 6,16 (2H; m); 6,34 (IH; d; ). 0,92 (3H; t; J-); ,22 (3H; d; J-i); 1,34 (6H; S); ,6 (2Я; ш); 2,18 (3H; S); 4,2 (IH; m); 5,4 (IH; d; J-IO); 6,16 (2H; m); 6,36 (IH; d; J-10).
0,96 (6Hi d; J«7); 1,35 (6H; S; ,0); IH; S; 2,18 (3H; S); 3,6 (2H; d; ); 5,4 (IH; d; ); 6,2 (2H; m); 6,36 (iH; d; ).
1,42 (6H; S;+3H; t; ); 2,1 (3H; S); 4,0 (2H; q; 5,47 (IH; d; ); 6,27 )H; d; 6,35 (IH; d; J- S); 6,75 (Ш; d; J-8).
1,05 (3H; t; J«8); I,42(6H; S); 1,57 (2H; ra); 2, (3H; S); 3,9 (2H; t; J-6); 5,47 (IH; d; ); 6,25 (IH; d; J-IO); 6,35 (Ш; d; ); 6,75 (IH, d; ).
1,35 (6K; d; J-6); 1,42 (6H; S); 2,1 (3H; S); 4,47 (H; ш); . 5„45 (Н; d; ); 6,25 (IH; d; ); 6,35(IH; d; J-S); 6,75 (H; d; ). 0,97 (3H; t; J-8); 1,3 (3H; d; ); 1,42 (6H; S); 1,68 (2H; m); 2,1 (3KJ S); 4,25 (IH; m); 5,45 (IH; d; ); 6,25 (H; d; ); 6,35 (IH; d; J-S); 6,72 (H; d; ). 1,05 (6H; d; ); 1,46 (6H; S); 2,1 (4H; S-nu); 3,7 (2H; d; J); 5,47 (Ш; d; ); 6,27 (IH; d; J-IO); 6,35 (IH; d; J«-8); 6,75 (IH; d; J).
1,38 (3H; c; J 8); 1,42 (6H; S); 3,8 (3H; S); 4,0 (2H; 4) ); 5,44 (Ш; d; ); 6,2 (IH; d; J-10); 6,32 (IH; d; J S; 6,56 (IH; d; J«8).
1,02 (3H; t; ); ,40 (6H; S); 1,8 (2H; m); 3,8 (3H; S); 3,83 (2H; q; ); 5,42 (1н; d; ); 6,19 (IH; d; ); 6.32 (IH; d, ); 6,56 (IH; d; ).
0,96 (3H; t; ); 1,24 (3H; d; ); 1,41 (6Я; S); 1,7 (2H; ш); 3,76 (3H; S); 4,2 (IH; m); 5,4 (IH; d; ); 6,18 (IH; d; ); 6,32 (IK; d; ); 6,56 (IH; d; ). 1,28 (6H; d; ); 1,42 {6H; S); 3,76 C3H; S); 4,44 (IH; m);
Прамечанне; ЯМР-спектры характериэукгтся следуотсим образом: химический сдвиг (число протог.ов; итльтиплетность; константа связи, Гц).
Таблица2
6-Метокси-7-втор. бутокси-2,2-диме- тил-2Н-хромен
6,7-Дифенипокси- 2,2-диметил-2Н- хромен
6-Метокси-7-изобу- тилокси-2,2-диме- тил-2Н-хромен
Контроль При обработке ацетоном 90-95% насеко 1х остаются живыми.
Продолжение табл.
OJ
м
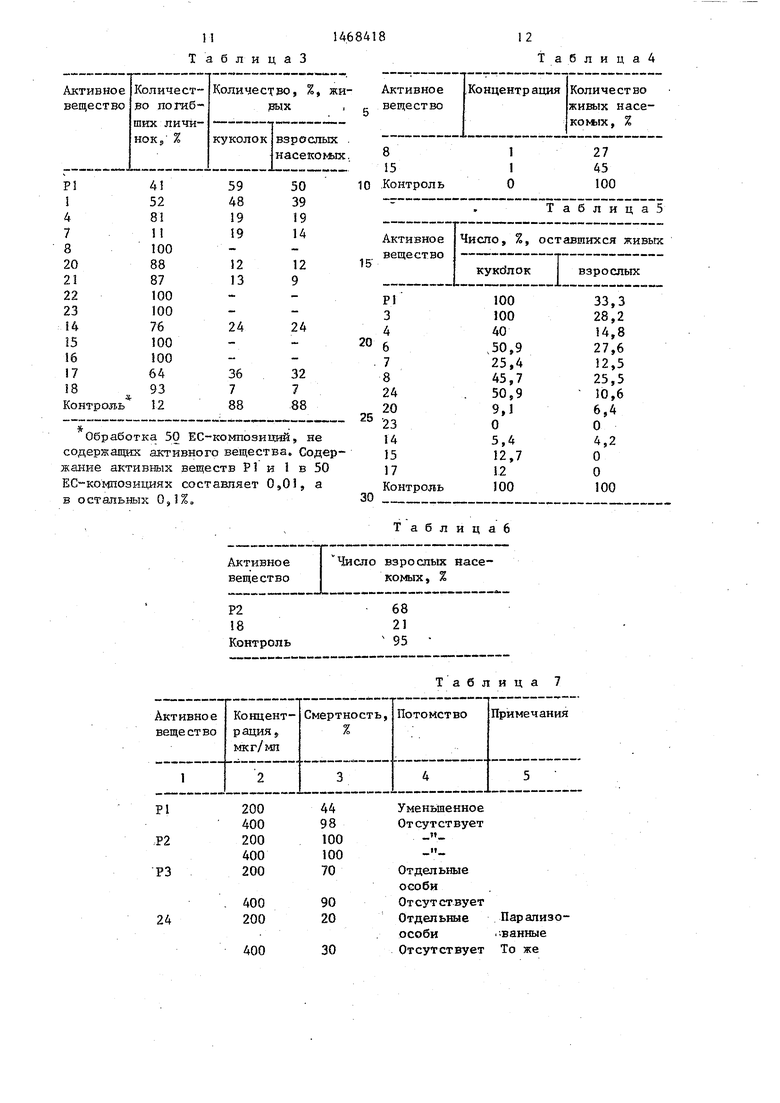
т а б л и ц а 3
1468418
Обработка 50 ЕС-композиций, не
содержащих активного вещества. Содержание активных веществ Р1 и 1 в 50 EC кo шosицияx составляет 0,01, а в остальных 0,1%,
200 400 200 400 200
400 200
400
44
98
100
100
70
90 20
30
12
Т аблица4
Таблица 5
Таблицаб
Таблица 7
Уменьшенное Отсутствует
|Т
Отдельные
особи
Отсутствует
Отдельные особи
Отсутствует
13
ь
200 400 200 400 200 400
АО
100
60
73
25
85
О
О
468418 4
фзодолжение табл.7
Уменьшенное Отсутствует Уменьшенное
11
II
Нормальное
| Гетероциклические соединения./ | |||
| Под ред | |||
| Р.Эрдельфильда | |||
| М., 1954, т | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Прибор для исправления снимков рельефа местности | 1921 |
|
SU301A1 |
| at al | |||
| - Science, 1976, 193, с | |||
| Кладка стен из фасонного кирпича | 1922 |
|
SU542A1 |
| Elle ed, Td | |||
| Wiley and Soar | |||
| London, 1877, c | |||
| Зубчатое колесо со сменным зубчатым ободом | 1922 |
|
SU43A1 |
| Hlufucek I, et al | |||
| Aust | |||
| - I | |||
| Chem., 1971, c | |||
| Досчатая пустотелая стена | 1925 |
|
SU2347A1 |
Авторы
Даты
1989-03-23—Публикация
1984-02-14—Подача