Цель изобретения - разработка на основе известных методов способа получения новых производных пиррола, обладающих фармакологическими преиму ществами перед их ближайшими структурными аналогами подобного действия
Пример 1. К раствору 12 г 3-окси-2-(7-бром-1,8-нафтиридин-2- ил)-1-изоиндолинона в 300 см без- водного диметилформамида, поддерживаемому в атмосфере аргона, добавляют при температуре около маленькими порциями 2,4 г масляной суспензии (50 вес.%) гидрида натрия и кую суспензию перемешивают в течение 30 мин при температуре около 0°С. Затем, поддерживая температуру при 0°С, прибавляют 6,9 г N-пропил-хлор- ацетамида и продолжают перемешивать еще в течение. 1 ч при 0°С, затем в :течение 4 ч при температуре, близкой |к 20 С. Реакционную смесь после это- 1го выливают в смесь 150 г льда и 350 см воды, нейтрализуют водным
1 н. раствором соляной кислоты и экстрагируют 3 раза 250 см дихлормета- на. Органические фазы объединяют, промывают 4 раза 75 см воды, сушат над сульфатом магния, отфильтровыва- ют, затем концентрируют досуха при пониженном давлений (2,7 кПа) при 40°С. Полученный остаток обрабатывают 25 см этилацетата и нерастворимый продукт отфильтровывают, промывают последовательно 10 см этилацетата, 10 см диизопропилового эфира, затем его удаляют, фильтрат концентрируют досуха при пониженном давлении
(2,7 кПа) при 40°С. Полученный оста-
ТОК очищают путем хроматографии на 120 г диоксида кремния, содержащихся в колонке диаметром 3 см (элюирующее средство: дихлорметан-метанол 98,5- 1,5 по объему). Элюируют сначала с по мощью 170 см растворителя: соответствующий элюат удаляют; затем элюиру- ют -С помощью 800 см растворителя и соответствующий элюат концентрируют досуха при пониженном давлении (2,-7 кПа) , После перекристаллизации остатка из этилацетата получают 2,1 г 2-(7-бром-158-нафтиридин-2- ил)-З-оксо-1-изоиндолинил |-Ы-пропш1- гликольамида, плавящегося при 174°С.
Пример 2. По примеру 1 полу- чают 2-(7-хлор-1,8-нафтиридин-2-ил)- 3-(4-метил-пентилокси)-1-изоиндоли-, нон, плавящийся при 104 С,
5
0 5. 0 5
0
и
с
5
0
Пример 3, По примеру 1 полу- |чают 2- (7-хлор -1,8-нафтиридин-2-ил) - 3-(5-метил-гексилокси)-1-изоиндоли- i нон, плавящийся при .
Пример4. По примеру 1 получают 2-(7-хлор-1,8-нафтиридин-2-ил)- 3-оксо-1-изоиндолинил)-Н-Ы-пентамети- леноксиацетамид, плавящийся при 185 с.
Пример 5. По примеру 1 получают 2-(7-хлор-1,8-нафтиридин-2-ил)- (4-метилпиперидино)-2-оксо-эток- си -1-изоиндолинон, плавящийся при 170 С.
Пример 6, По примеру 1 получают 2-(7-хлор-1 ,8-нафтиридин-2- ил)-3-oкco-1-изoиндoлиншr -N-изoпpoпил- оксиацетамид, плавящийся при 188°С.
Пример 7. По примеру 1 получают 2-(7-хлор-1,8-нафтиридин-2- ил)-3-оксо-1-изоиндолиншЛ-М-пропил- оксиацетамид, плавящийся при .
Пример8. По примеру 1 получают (7-хлор-1 ,8-нафтиридин-2-ил)- 3-oкco-1-изoиндoлил -N-(2-мeтил-пpo- пил)-оксиацетамид, плавящийся при 146°С.
Пример 9. По примеру 1 получают 3-бутокси-2-(7-хлор-1,8-нафти- ридин-2-ил)-1-изоиндолинон, плавящийся при 128°С.
Соединения общей формулы обладают интересными фармакологическими свойствами, проявляющимися в анксполити-1 ческой, гипнотической, антиконвульсивной, антиэпилептической и миоре- лаксантной активности.
Кроме того, предлагаемое соединение и его соли обладают слабой токсичностью. LDj-p обычно выше 300 мг/кг перорально у мьши.
Описание используемых тестов.
Тест на сродство к центральным ре- цепторным участкам бензодиазепинов.
Методика разработана на основе способа, описанного Nature 266, 732- 743 (1977) и заключается в измерении в присутствии изучаемого продукта специфической фиксации лиганда рецепторов бензодиазепинов, третированного флунитразепама.
Если продукт обладает сродством к рецепторным участкам бензодиазепинов, то специфическая фиксация лиганда будет уменьшена, .
Эксперимент заключается в следующем.
Промытый гомогенат (2 центрифугирования при 50000) всей коры голов516
ного мозга самцы крысы в буфере трис- НС1, 50 мМ, рН 7,4 (конечная концентрация. 0,1 мг протеина на 1 мл) смешивают с изучаемым продуктом в различ-. ных концентрациях и с тритироваыным флунитразепамом (концентрация конечная 1,5 нМ) . Неспецифическзто фиксацию определяют в присутствии диазепа- ма (10 мМ). После инкубации в течение 120 мин при 0°С каждый образец. фильтруют через фильтр из стекловолокон и удержанную на фильтре радиоактивность измеряют в сцинтиллирующей
жидкости.
Таким образом определяют CIg-Q, т.е. концентрацию изз аемого продукта, которая ингибирует 50% специфической фиксации/диганда.
Тест на химические конвульсии, вызванные пентетразолом.
Используют мышей весом по 18-22 г. Все мьшш получают подкожно фиксированную дозу 150 мг/кг пентетразола (единичная дозы, содержащаяся в 25 мл раствора на 1 кг мыши). Изучаемые продукты вводят перорально за 45 мин или за 1,5 ч до пентетразола, причем единичные дозы содержатся в объема 25 мл на 1 кг веса мыши.
Используют по 5 мьш1ей на дозу и по 3 дозы на продукт.
После инъекции пентетразола мьш1ей помещают в ящик, разделенный на 15 отдалений со стороной 13 см так, чтобы каждая мьш1Ь оставалась изолированной в течение всего эксперимента. Эти накрывают прозрачной пластиной. Все контрольные мьшш, получившие дозу 150 мг/кг подкожно пентетразола, по истечении менее 15 мин проявляют более или менее сильные конвульсии, которые быстро заканчиваются смертью животного. Мышей наблкщают в течение 30 мин после инъекции пентат- разола. Считают защищенной от конвульсий любую мьш1ь, которая в этот интервал - 30 мин не проявляет никакой : конвульсии. EDjo продукта - это доза, которая в кульминацию своего эф- фекта, ликвцдирует конвульсии, вызванные пентетразолом, у 50% животных Тест на прицепление. Этот способ заключается в подвешивании мьши передними лапами к металлической проволоке, натянутой горизонтально: считают, что животное подвергалось депрессивному нервно-мыг шечному воздействию, если оно -после
9976
3 попыток не сумело прицепиться или,., если оно зацепилось за проволоку, нсЗГ упало за время 5 с или менее 5 с; все контрольные животные легко прицепляются к проволоке и держатся на ней прицепленными, и даже за время 5 с или менее 5 с осуществляют подтягивание, которое приводит одну из их
Q задних лап к соприкасанию с проволокой .
Используют по 6 мьш1ей на дозу и по 4-5 доз на продукт. EDg-Q продукта - это доза, которая в кульминацию эф5 фекта, развивает депрессивную нервно- мьшечную активность у 50% животных.
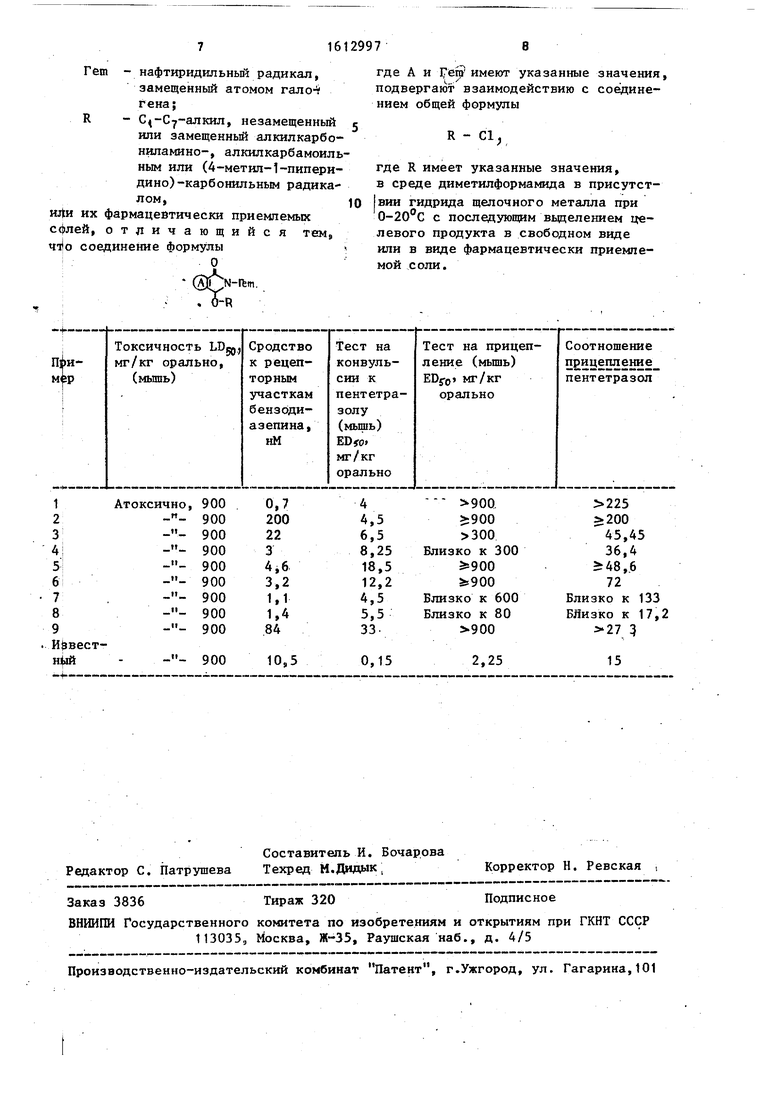
Результаты сравнительных испытаний предлагаемых соеЬ;инений с двуш наиболее активными известными соединениями
20 приведены в таблице.
Как следует из полученных результатов, соединейия согласно изобрете- . нию в тесте на-сродство к рецептор- .
25 ным участкам бензодиазепинов и в тесте на конвульсии, вызванные пентетразолом, проявляют активность, близкую к активности известных продуктов (иногда большую, иногда мень30 ШУЮ). Однако существенное отличие
новых соединений от известных заклю- чается в их слабой седативной актив- ности. Эта активность проявляется в тесте на прицепление. Так чем вьш1е EDtro прицепления
35 соотношение
менее продукт седативен. Таким образом, предлагаемые соединения более интересны, чем известные, так как, 40 будучи транквилизаторами, они практически не оказывают депрессивного нервно-мьш1ечного действия, которое нежелательно для такого рода соединений.
45
Формула изобретения.
Способ получения производных пиррола общей формулы
50
5
А вместе с пиррольным циклом образует изоиндолиг новое ядро;
Гет - нафтиридильньй радикал, замещенньй атомом галот гена;
С -С у-алкил, незамещенный с или замещенньй алкилкарбо- ниламино-, алкилкарбамоиль- ным или (4-метил-1 пипери- дино)-карбонильным радикалом, их фармацевтически приемлемых й, отличающийся тем, соединение формулы
О ,-Jk.
(MjN-lbm.
7o-R
где А и I7ew имеют указанные значения, подвергают взаимодействию с соединением общей формулы
R - С1
),
где R имеет указанные значения, в среде диметилформамида в присутствии гидрида щелочного металла при 0-20 с с последующим вццелением целевого продукта в свободном виде или в виде фармацевтически приемлемой соли.


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных пиррола или их оптических изомеров либо фармацевтически приемлемых солей | 1987 |
|
SU1616515A3 |
| Способ получения производных пиррола | 1988 |
|
SU1678202A3 |
| Способ получения производных пиррола | 1988 |
|
SU1685264A3 |
| Способ получения производных изоиндолинона или их фармацевтически приемлемых солей | 1988 |
|
SU1657056A3 |
| Способ получения производных пиррола | 1989 |
|
SU1630612A3 |
| Способ получения конденсированных производных пиррола | 1987 |
|
SU1577698A3 |
| Способ получения производных нафтиридинов | 1977 |
|
SU638258A3 |
| Способ получения производных нафтиридинов или их солей | 1976 |
|
SU648102A3 |
| Способ получения амидных производных хинолина или их солей с кислотами | 1986 |
|
SU1508957A3 |
| Способ получения производного замещенного амида | 1985 |
|
SU1417797A3 |
Изобретение относится к гетероциклическим соединениям, в частности к получению производных пиррола ф-лы I @ где А - вместе с пиррольным циклом образует изоиндолиновое ядро
Гет - нафтиридильный радикал, замещенный атомом галогена
R -C1-C7-алкил, незамещенный или замещенный алкилкарбониламино-,алкилкарбамоильным или (4-метил-1-пиперидино)-карбонильным радикалом, или их фармацевтически приемлемых солей, обладающих фармакологическими свойствами. Цель - разработка способа получения указанных соединений. Получение ведут реакцией соединения ф-лы I, где R - H, а А и Гет - указаны выше, с соединением ф-лы R -CL, где R указано выше, в среде диметилформамида в присутствии гидрида щелочного металла при 0 - 20°С с последующим выделением целевого продукта в свободном виде или в виде фармацевтически приемлемой соли. 1 табл.
Редактор С. Патрушева
Составитель И. Бочарова Техред М.Дидык,
Заказ 3836
Тираж 320
ВНИИПИ Государственного комитета по изобретениям и открытиям при ГКНТ СССР 113035э Москва, Ж-35, Раушская наб., д. 4/5
Корректор Н. Ревская ,
Подписное
| Способ получения гетероциклических соединений | 1975 |
|
SU673173A3 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1990-12-07—Публикация
1988-12-15—Подача