Изобретение относится к способам получения гетероциклов, в частности новых производных пироола общей формулы О
-А
(А}| N-ГетI
OCO-R
где А с пиррольным циклом образует изоиндолиновое ядро;
Гет-нафтипиридинильный радикал, замещенный атомом галогена или С1-С4-ал- кильным, С1 С4-алкоксирадикалом;
R - незамещенный Сз Се-алкил, или низший алкил, замещенный низшей алкоксигруппой или 4-пиперидил, замещенный в положении I радикалом бутироил, которые обладают анксиолитической, гипнотической, антиконвульсивной, антизпилеп- тической и миорелаксантной активностью, с также хорошим средством (In vinto) к рецеп- торным участкам к бензодиазепину в концентрациях 0,4-200 нМ.
У животного (мыши) они обычно активны в дозах 0,3-200 мк/кг перорально по
СП
ю
о
4
отношению к конвульсиям, вызванным пен- татрозолом.
Новые продукты общей формулы (I) обладают незначительной токсичностью. Их ЛДво составляет 300-900 мг/кг перорально у мыши, или S 1510 мг/кг.
Целью изобретения является разработка способа получения новых соединений, обладающих более высокой биологической активностью.
Сущность изобретения иллюстрируется следующими примерами.
Пример1.В раствор 12,3 г 2-(7-меток- си-1,8-нафтиридин-2-ил)-3-оксм-1-изоиндо линона э 200 см3 метиленхлорида, поддерживаемый при температуре, близкой к 20°С, добавляют 27 см3 триэтмламина. Затем в течение 20 мин прикапывают 10,8 мг 4-ме- тилпентаноил-хлорида и 50 мг 4-диметилэ- минопиридина, после чего реакционную смесь кипятят в течении 19 ч с обратныг з холодильником, Полученную суспензию выливают в 800 см3 воды, полученное твердое вещество отфильтровывают и удаляют. Органическую фазу декантиоуют, промывают водой, высушивают и концентрируют досуха при пониженном давлении (2,7 кПа). Полученный маслянистый остатозсочищзют путем хроматографии на 150 г силмкагеля (0,063-0,2 мм), содержащихся в колонке диаметром 2,7 см (элюирующее средство: мети- ленхлорид), элюируя фракции по 50 см . Фракции 6-18 объединяют и концентрируют досуха при пониженном давлении {2,7 кПа)при 40°С. После перекристаллизации ацетонигрила получают 4,9 г твердого вещества (2-{7-метокси-1,8-нафтирмдин-2- ил)-3-оксо-1-изоиндолинмл) -4-метил-пен- таноата, плавящегося при 133°С.
П р и м е р 2. Работают по примеру 1, но исходят из 6,8 г 2-(7-метокси-1,8-чафти- ридин-2-ил)-3 окси-1-изоиндолинона в 100см метилечхлорида, 10,1 гтриэтилами- на, 6,4 г 5-метил-гексаноил-хлорида и 50 мг 4-диметиламинопиридина. Полученный после обработки остаток очищают хроматографией на 100 г силикагеля (0,063-0,2 мм) Б колонке диаметром 2,8 см (элюирующее средство: метиленхлорид), собирая фракции по 30 см3. Фракции 19-94 объединяют и концентрируют досуха при пониженном давлении (2,7 кПа). После перекристаллизации полученного остатка из 75 см° гептана получают 3,6 г (2-7-метокси-1,8-нафтири- дин-2-ил/-3-оксо-1-изоиндолинил) -5-ме- тил-гексаноата, плавящегося при 105°С.
Пример 3.8 раствор 9,2 г 2-{7-меток- си-1,8-нафтиридин-2-мл}-3-окси-1-изоиндо- линона и 20 см3 триэтилзмина в 150 см3 1,2-дих/юр§тан8, поддерживаемый при тем0
Ь
0
0
5
пературе около 20°С, в течение 20 мин добавляют раствор 9 г 2-метил-пропокси-аце- тилхлорида в 20 см3 1,1-дихлорэтана, затем 50 мг4-диметил-аминопиридина и кипятят с
обратным холодильником в течение 16 ч. Реакционную смесь выливают в 250 см воды, затем экстрагируют 100 см3 метиленхлорида. После промывки водой, высушивания и концентрирования досуха при пониженном давлении (3 кПа) полученный остаток очищают путем двух последовательных перекристаллизации из этанола, Получают 7,9 г 2-{7-метокси-1,8-нафтиридин-2-ил}-3-ок- со-1-изоиндолинил-2-метил -пропоксиацета- та, плавящегося при 114°С.
2-Метил-пропоксиацетил-хлорид может быть получен следующим образом: в течение 15 мин 5 см тионилхлорида добавляют к раствору 8,3 г 2-метил-пропоксиуксусной кислоты в 50 см хлороформа. Смесь в течение 5 ч кипятят с обратным холодильником, затем выпаривают досуха при пониженном добавлении (2,7 Пз). Получают таким образом 7,5 г 2-метил-пропоксиацетилхлорида в виде масла, используемого сырым в последующих синтезах.
2-Метил-пропоксиуксусная кислота может быть получена следующим образом.
К 200 см узобутилового спирта, поддерживаемого при температуре около 100°С, добавляют 12,7 г натрия и нагревают до его полного исчезновения. Затем в течение часа добавляют 23.6 г хлоруксусной кислоты и продолжают нагревать в течение 2 ч. После охлаждения реакционную смесь выливают а 250 см воды. Водную фазу промывают 200 см3 диэтилового эфира, концентрируют до половины объема при пониженном давлении (3 кПа), затем подкис0 ляют до значения рН, близкого к 1, с помощью водного 1 н.раствора соляной кислоты. Образовавшееся масло экстрагируют 3 раза 150 см3 диэтилового эфира. Органическую фазу промывают водой, су5 шат и концентрируют досуха при пониженном давлении (3 кПа). После перегонки при пониженном давлении полученного остатка получают 21,8 г 2-метил-пропоксиуксусной кислоты, кипящей при 92-96°С при 0,93 кПа.
0П р и м 6 р 4.
К суспензии 12,5 г 2-(7-хлор-1,8-наф- тмридин-2-ил)-3-окси-1-изоиндолинона в 600 см° метиленхлорида добавляют 12,2 г триэтиламина, 90 см пиридина, затем 9,7 г
6 3-метил-бутирмл-хлорида, поддерживая температуру около 25°С. После 4 ч переме- ишвэкия при температуре, близкой к 25°С, снова добавляют 9,7 г 3-метил-бутироилхло- рида и перемешивают еще в течение 16ч при этой температуре. Затем реакционную
смесь концентрируют досуха при пониженном давлении (3 кПа) и остаток обрабатывают 500 см3 воды. Образовавшийся нерастворимый продукт отфильтровывают, промывают, высушивают, затем перекристаллизовывают из смеси диизопропилового эфира с этила- цетатом (50:50 по объему). Таким образом получают 7,9 г 2-{7-хлор-1,8-нафтиридин-2- ил)-3-оксо-1-изоиндолинил -Зметил-бутира- та, плавящегося при 154°С.
Пример 5. К раствору 6,4 г 2-{7-хлор- 1,8-нафтиридин-2-ил)-3-окси-1-изоиндоли- нона в 320 см метиленхлооида последовательно добавляют 48лсм3 пиридина, затем в течение30 ммн 12,8-г.бутирил-хлорида, поддерживая температуру около 25°С. Смесь перемешивают в течение 3 ч при этой температуре, затем добавляют 100 см3 воды. Органическую фазу декантируют, промывают водой, высушивают и концентрируют досуха при пониженном давлении {2,7 кПа). Полученный остаток кристаллизуют из диизопропилового эфира, затем дважды перекристаллизовывают из ацетонитрила. Таким образом получают 1 г 2-{7-хлор-1,8- нафтиридин-2-ил)-3-оксо-Т-изоиндолинил- , плавящегося при 140°С.
П р и м е р 6. Работают по примеру 1, но исходят из 8,55 г 2-(7-бром-1,8-нафтиридин- 2-ил)-3-окси-1-изоиндолинона в 110 см ме- тиленхлорида, 11,1 г триэтиламина, 7 г 5-метил-гексаноилхлорида и 50 мг 4-диме- тиламинопиридина. После кристаллизации из гексана, а затем перекристаллизации из этанола полученного остатка получают 7,5 г 2-{7-бром-1,8-нафтиридин-2-ил)-3-оксо-1-и- зоиндолинил-5-метил-гексаноата, плавящегося при 136°С.
Пример 7. Работают по примеру 1, но исходят из 3,7 г 2-(7-метил-1,7-нафтиридин-2- ил)-3-окси-1-изоиндолинона, 7,8 г 5-метил- гексаноил-хлорида, 12 см3 триэтиламина и 50 мг 4-диметиламино-пиридина. После перекристаллизации из метилциклогексана, полученного после обработки твердого вещества, получают 3,8 г 2-{7-метил-1,8-нафти- ридин-2-ил)-3-оксо-1 -изоиндол и н и л-5-мет- ил-гексаноата, плавящегося при 144°С.
Пример 8, Работают по примеру 1, но исходят из 5 г 2-{7-фтор-1,8-нафтиридин- 2-ил}-3-окси-1-изоиндолинона в 60 см мети- ленхлорида, 6,5 г триэтиламина, 3,66 г 4-метил-гсентаноил-хлорида и 10 мг 4-диме- тилзминогшридина. После перекристаллизации дез этанола получают 1,2-г 2-{7-фтор-1,8-кафтмридин-2-ил)-3-оксо -1-изоикдолинил-4-метил-пентаноата, плавящегося при 154°С.
2-{7-Фтор-1,8-нафтиридин-2-ил}-3-окси -1-иэоиндолинон может быть получен следующим образом.
К суспензии 16.1 г 2-{7-фтор-1,8-нафти- ридин-2-ил)-изоиндолин-1,3-диона в смеси 90 см 3 безводного метанола и 30 см3 ди- оксана при температуре около 20°С маленькими порциями добавляют 2,3 г тетрагидробората калия. Полученную сус0 пензию перемешивают в течение 3 ч при температуре около 20°С Затем реакционную смесь выливают в смесь 120 г льда с 240 см3 воды. Нерастворимый продукт отфильтровывают, промывают 3 раза 50 см
5 воды, сушат на воздухе и перекристаллизовывают из ацетонитрила. Такик) образом получают 10,3 г2-(7-фтор-1,8 нафтиридин-2- ил}-3-окси-1-изоиндолинона, плавящегося при246°С.
02-(7-Фтор-1,8-нафтиридин-2-ил)-изоин
долин-1,3-дион может быть получен следующим образом,
К суспензии 20,6 г 2-{7-хлор-1,8-нафти- рмдин-2-ил)-изоиндолин-1,3-диона в
5 270 см3 безводного нитробензола, поддерживаемой в атмосфере аргона, добавляют 15 г фторида калия. Реакционную смесь кипятят с обратным холодильником при перемешивании в течение 22 ч. После ох0 лаждения до температуры, близкой к 80°С, реакционную смесь концентрируют досуха при пониженном давлении (0,13 кПа) при 80°С. Полученный остаток обрабатывают 170 см3 этилацетата. Нерастворимый про5 дукт отфильтровывают, промывают последовательно 30 см3 этилацетата, 6 раз 30 см3 воды и высушивают на воздухе. Таким образом получают 16,9 г2-(7-фтор-1,8-нафтиридин- 2-ил}-изоиндолин-1,3-диона, плавящегося при
0 264°С.
Работая по примеру 1, из соответствующих исходных веществ получают
(7-Хлор-1,8-нафтиридин-2-ил)-3-оксо-1 -изоиндолинил-4-метил-пентаноат, плавя5 щийся при 147°С (пример 9)
2-(7-Хлор-1,8-нафтиридин-2-ил}-3-оксо -2-изоиндолинил-5-метил-гексаноат, плавящийся при 132°С (пример 10)
2-(7-Хлор-1,8-нафтиридин-2-ил)-3-оксо
0 -1-изоиндолинил-(1-бутирил-4 -пиперидин)- карбоксилат, плавящийся при 165°С (пример 11).
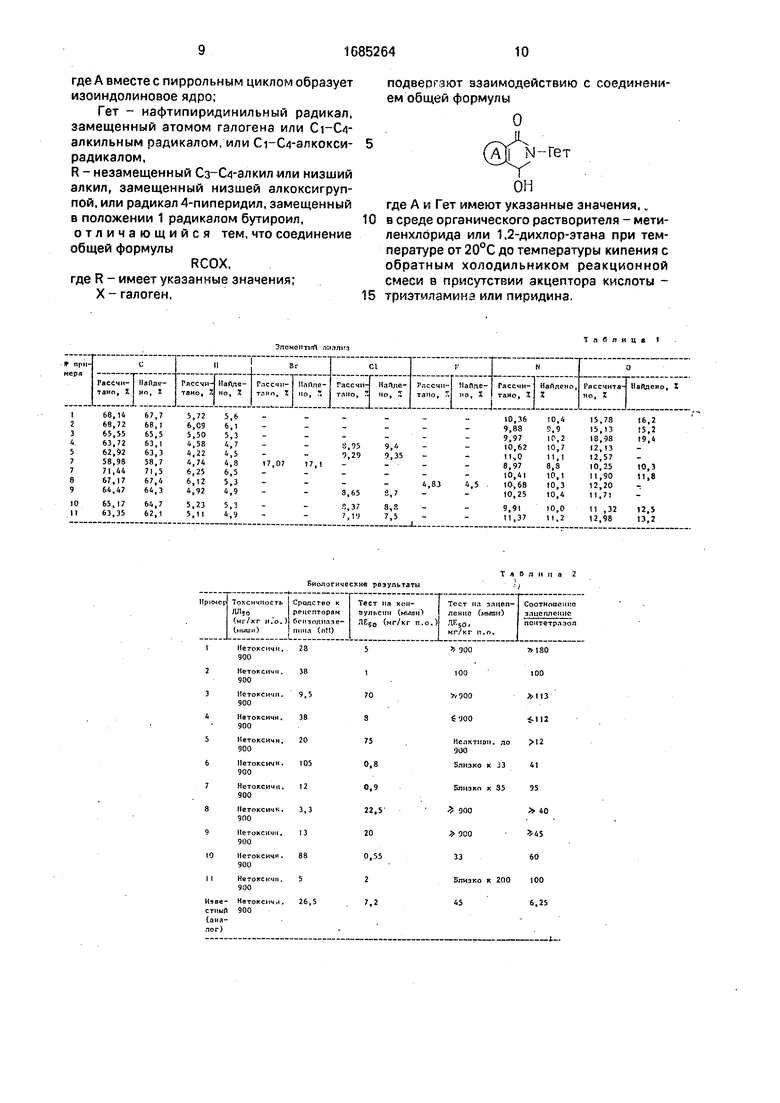
Данные элементарного анализа приведены в табл.1.
5 Тест на токсичность.
Определяют максимальную дозу продукта (ЛДю). которая при введении мышам перорально вызывает смерть 50% из них.
Тест на сродство к центральным рецеп- тормым участкам бензодмазепинов.
Метод заключается в определении в присутствии изучаемого продукта специфической фиксации лиганда бензодиазепино- вых рецепторов, меченого тритием флунитразепама.
Если продукт обладает сродством к ре- цепторным участкам бензодиазепинов, специфическая фиксация лиганда будет уменьшена.
Смешивают промывочный гомогенат (2 центрифугирования при 50 000) всей коры головного мозги самца крысы (СД, COBS, Charles RIVER France) в 50 мМ буфере Трис- НС и рН 7,4 (конечная концентрация 0,1 мг протеина на мл) с изучаемым продуктом в различных концентрациях и меченым тритием фяунитразепамом (конечная концентрация 1,5 нМ). Неспецифическая фиксация определяется в присутствии диазепамз (10 нМ). После инкубации в течение 120 мин при 0°С каждый образец фильтруют на фильтре из стекловолокна (фильтр WHATMAN GF/B), удержанную фильтром радиоактивность измеряют в сцинтмллиру- ющей жидкости.
Таким образом определяют Ciso, т.е. концентрацию изучаемого продукта, которая ингибирует 50% специфической фиксации лиганда.
Тест на химические конвульсии, наведенные пентетразолом
Используют мышей весом по 18-22 г,
Все мыши получают подкожно фиксированную дозу 150 мг/кг пентетразола (единичная доза, содержащаяся в 25 мл раствора на кг веса мыши). Изучаемые продукты вводят перорально за 45 мин и за 1,5 ч до пентетразола, причем единичные дозы содержатся в 25 мл на кг веса мыши.
Используют по 5 мышей на дозу и по 3 дозы на продукт.
После инъекции пентетразола мышей помещают в камеру, разделенную на 15 секций со стороной 13 см так, чтобы каждая мышь оставалась изолированной на протяжении всего времени наблюдения. Камеры покрывают прозрачной пластинк.ой Rhodoid. Все контрольные мыши, получившие дозу 150 мг/кг пентетразола подкожно меньше чем в 15 мин, имеют более или менее сильные конвульсии, которые скоро становятся смертельными. Мышей наблюдают в течение 30 мин после инъекции пентетразола. Защищенной от конвульсий считают любую мышь, которая в этот интервал i (30 мин) не имеет конвульсий. ЭДю продукта представляет собой дозу, которая при максимальном эффекте уничтожает конвульсии, вызванные пентетразолом (50% животных).
Тест на зацепление.
Этог метод состоит в подвешивании мыши передними лапами на горизонтально на- тянутой металлической проволоке; депрессивное мышечно-нервное действие рассматривают на всяком животном, которое не старается зацепиться после трех попыток или которое, если оно и прицепилось к проволоке, падает за 5 или менее чем за 5 0 с. Все контрольные животные легко прицепляются к проволоке, остаются прицепленными и даже совершают за 5 или менее чем за 5 с подтягивание, которое приводит по крайней мере одну из их задних лап в сопри- 5 косновениес проволокой.
Используют по 6 мышей на дозу и 4-5 доз на продукт.
ЭД50 продукта равно дозе, которая при максимальном эффекте развивает депрес- 0 сивную нервно-мышечную активность у 50% животных.
Полученные результаты сведены в табл, 2 и сравниваются с известным продуктом формулыО
oWv
V ci ocoNQN-сНз
Сравнение показало, что соединение 0 формулы I в тесте на сродство к рецептор- ным участкам бензодиазепина и оба соединения в тесте на консульсмю, наведенную пентетразолом, проявляют схожую активность, в некоторых случаях большую, а в 5 некоторых случаях меньшую.
Существенное отличие соединений формулы известного продукта заключается в невысокой седативности. Эта активность определяется в тесте на зацепление. Так, чем
больше соотношение
ДЕю зацепления
ДЕзо пентетразола тем меньше седативность соединений. С этой точки зрения соединения формулы I более интересны, чем известный продукт,
так как будучи транквилизаторами они не проявляют депрессивного нервно-мышечного эффекта, который для такого рода соединений представляет собой нежелательное побочное действие.
Таким образом, предложенный способ позволяет получить соединения с более высокой биологической активностью по сравнению с известным.
Формула изобретения
Способ получения производных пиррола общей формулы О
(А N-Ife-г
V OCO-R
гдеАвместеспиррольным циклом образует изоиндолиновое ядро;
Гет - нафтипиридинильный радикал, замещенный атомом галогена или алкильным радикалом, или С1-С4-алкокси- радикалом,
R - незамещенный Сз-С -алкил или низший алкил, замещенный низшей алкоксигруп- пой, или радикал 4-пиперидил, замещенный в положении 1 радикалом бутироил, отличающийся тем, что соединение общей формулы
RCOX, где R - имеет указанные значения;
X - галоген,
подвергают взаимодействию с соединением общей формулы
О
N-Гет
где А и Гет имеют указанные значения, „ в среде органического растворителя - мети- ленхлорида или 1,2-дихлор-этана при температуре от 20°С до температуры кипения с обратным холодильником реакционной смеси в присутствии акцептора кислоты - триэтияамина или пиридина.



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных пиррола | 1988 |
|
SU1678202A3 |
| Способ получения производных пиррола или их фармацевтически приемлемых солей | 1988 |
|
SU1612997A3 |
| Способ получения производных пиррола или их оптических изомеров либо фармацевтически приемлемых солей | 1987 |
|
SU1616515A3 |
| Способ получения конденсированных производных пиррола | 1987 |
|
SU1577698A3 |
| Способ получения производных изоиндолинона или их фармацевтически приемлемых солей | 1988 |
|
SU1657056A3 |
| Способ получения производных пиррола | 1989 |
|
SU1630612A3 |
| Способ получения производных изоиндолинона или их солей | 1989 |
|
SU1739845A3 |
| Способ получения производных 2,3,6,7-тетрагидротиазоло /3,2- @ / пиримидин-5-она | 1982 |
|
SU1145932A3 |
| Способ получения производных нафтиридинов | 1977 |
|
SU638258A3 |
| ПРАВОВРАЩАЮЩИЙ ИЗОМЕР 6-(5-ХЛОР-2-ПИРИДИЛ)-(4-МЕТИЛ-1-ПИПЕРАЗИНИЛ)-5-КАРБОНИЛОКСИ-7-ОКСО-6,7-ДИГИДРО-5Н-ПИРРОЛО-(3,4-B)ПИРАЗИНА И ЕГО ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМАЯ КИСЛОТНО-АДДИТИВНАЯ СОЛЬ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 1992 |
|
RU2110519C1 |
Изобретение касается производных пиррола, в частности получения соединений О общей ф-лы1: 61 0-C(0)-R где Гет- нафтиридинил, замещенный галогеном, ИЛИ С1-С4-9ЛКИЛ, ИЛИ С1-С4-ЗЯКОКсигруппа; А вместе с пиррольным циклом образует изоиндолиновое кольцо; R - Сз Сб-алкил или низший алкил, замещенный низшей алкоксигруппой, 4-пиперидил, замещенный 1-бутироилом, обладающих анксиолитической, гипнотической, антиконвульсивной, антиэпилептической и миорелаксантной активностями что может быть использовано в медицине. Цель - создание новых более активных веществ указанного класса. Синтез ведут реакцией соединения ф-лы II Р-С(0)Х,где Х- галоген, и соединения формулы III Гет-М-С(0)-С С-С(О) в среде органического растворителя - или 1,2-дихлорэтана при температуре от 20°С до температуры кипения (с обратным холодильником) реакционной смеси в присутствии акцептора кислоты - триэтиламина или пиридина. Новые вещества имеют невысокую седативность, т.е будучи транквилизаторами они не проявляют депрессивного нервно-мышечного эффекта, который сопровождает применение известных веществ. 2 табл. ел
Тпблнцв t
| Способ получения гетероциклических соединений | 1975 |
|
SU673173A3 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Способ получения производных изоиндолина или их солей | 1971 |
|
SU455535A3 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1991-10-15—Публикация
1988-11-04—Подача