Изобретение относится к способам получения гипоглицеридально-активных полисахаридов, т.е. полисахаридов, снижающих содержание триглицерида в крови млекопитающих.
Вещества подобного типа действия могут быть применены в качестве терапевтических препаратов против атеросклероза или гиперлипидемии, которые являются наибо-. лее типичными заболеваниями людей среднего и пожилого возраста.
Известен способ получения физиологически активного полисахарида путем культивирования штаммов-продуцентов из рода Pseudomonas на соответствующей питательной среде и выделения из ферментационного бульона посредством фракционирования биополимеров 1.
Недостатком способа является недостаточно высокая физиологическая активность полисахарида.
Целью изобретения является повышение активности целевого продукта.
На фиг. 1-4 приведены хроматограммы. поясняющие предлагаемый способ.
Сущность способа получения гипотриг- лицеридально-активных полисахаридов состоит в том, что на питательной среде - бульоне Рогозы - а аэробных условиях выращивают штаммы-продуценты Streptococcus faecium PERM BP-296 или Streptococcus faecalis PERM BP-297, или Streptococcus savlum BP-298, или Streptococcus salivalls
XI
CJ ГО 00
д
ел
OJ
PERM BP-299, или Streptococcus durans PERM BP-300, или Streptococcus mltls PERM BP-301, или Streptococcus equlnus PERM BP-302 до максимального наполнения целевого продукта, отделяют биомассу от культуральной жидкости и осуществляют выделение целевого продукта из культуральной жидкости или из биомассы после ее депротеинизации и дезынтеграции.
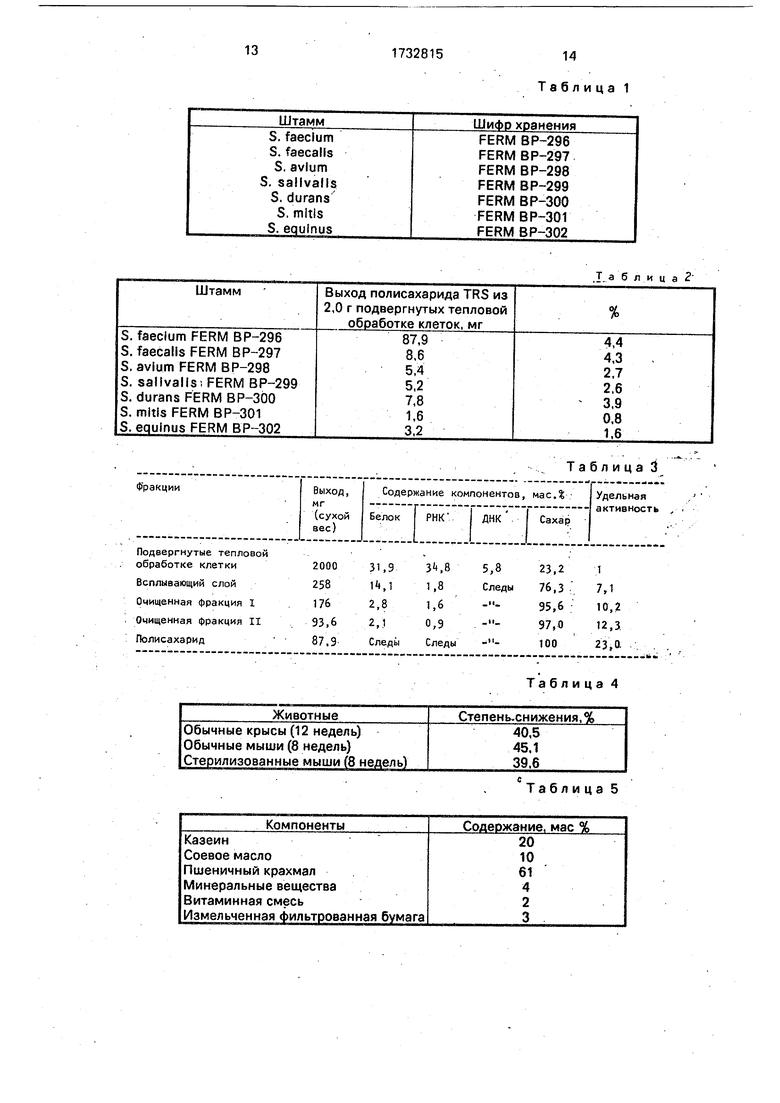
Наиболее общие примеры таких микроорганизмов сданы на хранение в Исследовательский институт ферментации (ИИФ, т.е. Международный центр хранения в соответствии с Будапештским соглашением) в Японии, а шифры хранения перечислены в табл.1.
Микробиологические характеристики микроорганизмов, используемых в предлагаемом способе, являются такими же, что и микробиологические характеристики известных микроорганизмов, принадлежащих тому же классу, т.е. общие микробиологические характеристики, методы культивирование и другие свойства соответствуют характеристикам, описанным в Руководстве Бергея по определительной бактериологии, 8-е изд.
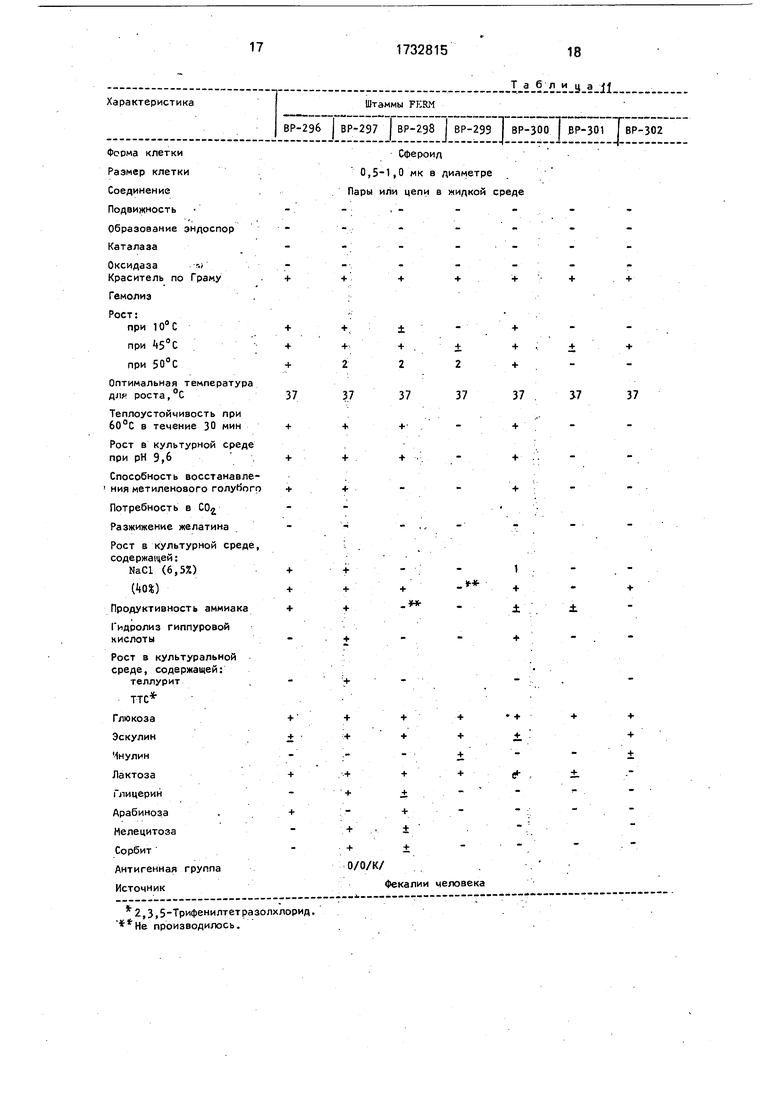
Наиболее общие микробиологические свойства указанных штаммов приведены в табл.2 и 11.
Указанные микроорганизмы можно - культивировать известным методом. Например, бактериальные клетки могут быть получены при помощи стационарного культивирования в среде бульона Рогоза при аэробных условиях, затем бактериальные клетки отделяются при помощи центрифугирования культуры.
Состав среды бульона Рогоза следующий, г: триптиказа 10; экстракт дрожжей 5; триптоза 3; К2НР043; КН2Р043; триаммоний цитрат 2; твин-80 1; глюкоза 20; хлоргидрат цистеина 0,2, кроме того, раствор соли (1 MgS,04 7H20 11,5; FeSCV7H20 0,68; MnS04 2H20 2,4; дистиллированная вода 100 мл) 1-5 мл и дистиллированная вода - до объема 1 л, (рН 7, стерилизация нагреванием до температуры 121 °С, которая поддерживается в течение 15 мин).
Получение полисахарида ПССТ.
Выращивание микроорганизмов. Каждый из указанных микробных штаммов, засевают на среду бульона Рогоза и инкубируют без перемешивания при 37°С в течение 5-10 ч при аэробных условиях, в результате чего получают культуральный бульон с некоторой концентрацией живых бактериальных клеток.
Культуральный бульон непрерывно подвергают центрифугированию со скоростью 12000 об/мин, а собранные бактериальные клетки затем промывают в соляном растворе (0,85% NaCI) 2 или 3 раза.
Разрушение бактериальных клеток. Промытые клетки суспендируют в физиологический соляной раствор и обрабатывают термическим способом при 115°С в течение
0 10 мин с целью их разрушения.
Бактериальные клетки, промытые и суспендированные в физиологический соляной раствор, разрушают при помощи обработки ультразвуком (15 кГц, 60 мин) французским
5 прессом или другими известными способами.
Удаление жира из клеток. Суспензию разрушенных клеток смешивают со смесью хлороформ-метанол (2:1 об/об). Компонен0 ты, экстрагируемые органическим растворителем, затем полностью удаляются.при помощи центрифугирования со скоростью 300 об/мин в течение 10 мин, а слой хлороформа сливают.
5 Обработка протеолйтическими ферментами. Обезжиренные пробы обрабатывают протеолйтическими ферментами, такими как проназа, трипсин и пепсин при помощи известных процедур. Из этих протеолитиче0 ских ферментов проназа является наиболее предпочтительной для этой цели. Условия обработки этим ферментом являются известными.
Очистка. В верхний слой после центри5 фугирования протеолитической реакционной смеси добавляют такие осаждающие агенты, как трихлоруксусная кислота или сульфат аммония с тем, чтобы протеиновая фракция выпала в осадок и ее можно было
0 удалить. Фракцию верхнего слоя затем обрабатывают соответствующей нуклеазой или протеолйтическими ферментами с тем, чтобы удалить составляющие нуклеиновых кислот, таких как ДНК и РНК или протеины
5 фракции. После такой ферментной обработки несколько раз осуществляют диализ.
Частично очищенную фракцию затем снова подвергают другим процедурам очистки, таким как гелевая фильтрация и очист0 ка с использованием хроматографической колонны. Чистая препарация полисахарида, обозначаемого как полисахарид ПССТ, получается в конце последней стадии.
В общем случае этот полисахарид ПССТ
5 может быть получен в соответствии с его физико-химическими характеристиками при помощи многочисленных процедур изоляции и очистки, которые уже давно широко используются в это области техники, таких как осаждение-растворение и экстракция, экстрагирование растворителем, диализ, применение хроматографической колонны, электрофорез, гелевая фильтрация или любая комбинация этих процедур. Таким образом, изобретение никоим образом не ограничивается какой-либо конкретной из упомянутых процедур.
Т.е. препарация изобретения относится к способам получения активных продуктов, снижающих содержащие триглицеридов в крови, которые состоят из полисахарида, и их получают из микроорганизмов, принадлежащих семейству Streptococcus, так как фармакологическая активность была обнаружена во фракции полисахарида,
Отметим, что активность по снижению содержания триглицерида в верхнем слое культурального бульона составляет примерно 1/5 от активности в бактериальной клетке.
Физико-химические и физиологические характеристики полисахарида ПССТ состоят в следующем.
Химическая природа и свойства растворимости. Тонко измельченная проба, полученная после обессоливания и сушки вымораживанием, является негигроскопичным белым порошком, обладающим высокой растворимостью (100 мг/мл) в воде, но она только частично растворяется в этаноле, метаноле и ацетоне и совсем не растворяется в простом эфире и хлороформе.
Молекулярный вес. Молекулярный вес полисахарида ПССТ оценивается в примерно 14000±3000 и устанавливается при помощи гелевой фильтрации с использованием нескольких правовращающих материалов различного молекулярного веса в качестве индексов, и колонны Тойопеарл HW/55 (фирма Тойосоде Ко., Лтд), уравно- вешенной при помощи 25 мМ трис-НС буфера, содержащего 0,ЗМ NaC (pH 7,5).
Удельный показатель вращения. Удельный показатель вращения упомянутого полисахарида ПССТ в 1,8%-ном растворе, , равен + 190,1 (правое вращение). Этот показатель определяется при помощи поляриметра (модель ДИП-4, фирма Джапан Спектроскопик, Ко. Лтд.).
Сахарный состав. 4мг пробы обрабаты- вают 0,2 М раствором ТФК (трифторуксус- ной кислоты) при 100°С в течение 7 ч, а триметилсилилирование осуществляют следующим образом: пробу смешивают с 0,2 мл гексаметилдисилазана (20% в пиридине) и 0,02 мл триметилхлорсилана, смесь перемешивают в течение 15 мин и после отстаивания в течение 5 мин подвергают газовой хроматографии q целью определения содержания глюкозы, рамнозы и т.д. Температура колонны разделения составляет 179 С. Содержание уроновой кислоты определяют с использованием метода карбазол-НаЗСм (модифицированный метод Биттера-Муира).
Состав Сахаров полисахарида ПССТ следующий, %: глюкоза 70,3; рамноза 13,7; уроновая кислота 16,0.
Кислотно-основные характеристики. рН 0,1 и 0,5%-ного раствора полисахарида ПССТ составил 6,71.
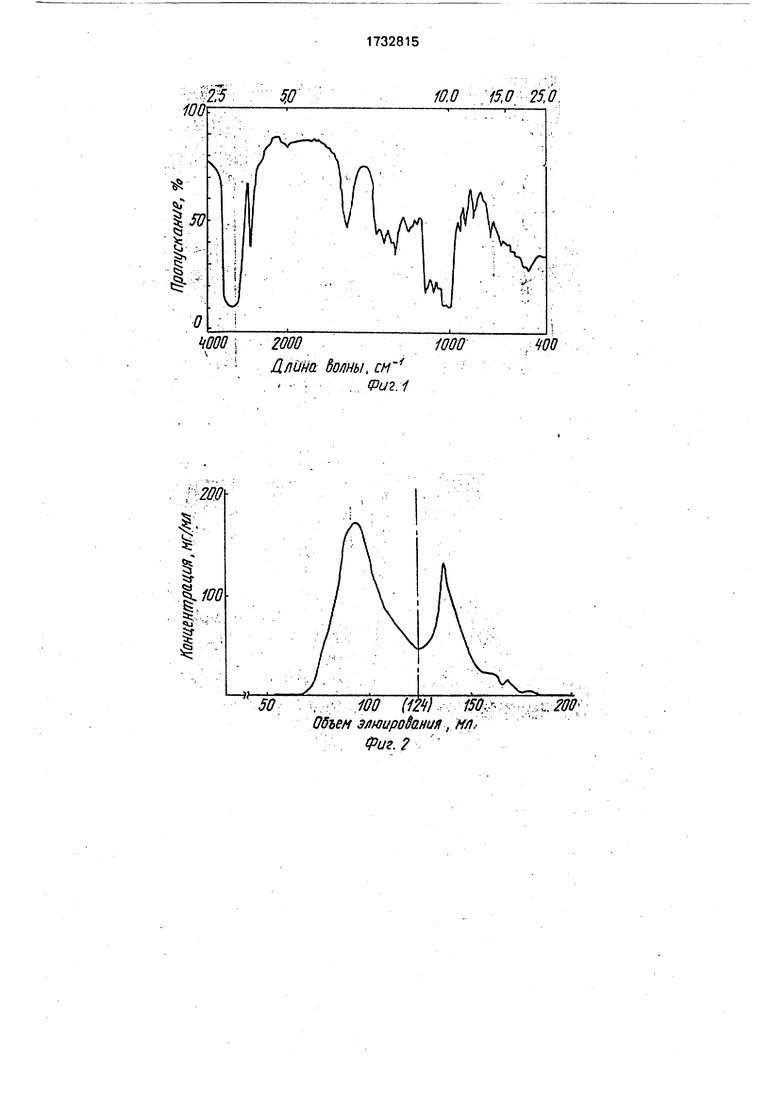
Спектр инфракрасного поглощения. Инфракрасный спектр поглощения полисахарида ПССТ, полученный с использованием инфракрасного спектрометра (модуль IASLO А 302, Джапан Спектроскопик Ко, Лтд), приведен на фиг. 1,где по осям абсцисс и ординат отложены длина волны и пропускание соответственно.
Элементарный анализ. Элементарный анализ при помощи элементарного анализатора (модель 240 В, Перкин-Элмер) дал следующий результат: С 37,2%, Н 6,4% и О 56,4%, для полисахарида ПССТ. Упрощенная формула имеет следующий вид
С31Н64Н35.
Температура точки плавления. Точка плавления полисахарида ПССТ составила 235-241 °С, ее измеряют при помощи установки для измерения температуры точки плавления (модель Яанако МР-3, фирма Яанагимото Сейсакушо, Япония).
Физиологические характеристики. Полисахарид ПССТ является активным при применении с целью снижения содержания триглицерида в крови млекопитающего при стоматическом применении.
Эта активность является стабильной в области температур от -80°С до 115°С и при рН в области от 4,1 до 11, если даже полисахарид перед применением хранился.
Фармакологическое действие полисахарида ПССТ.
Фармакологические эффекты. Предлагаемый антиатеросклеротический препарат, содержащий предлагаемый полисахарид ПССТ, является в высшей степени эффективным при снижении содержания триглицерида в крови млекопитающих. В соответствии с этим предлагаемый препарат используется в качестве терапевтического или профилактического препарата при заболеваниях, связанных с атеросклерозом, гиперлипи- демией, гиперлипопротеиномией, ксанто- матозом, холецистолитизом, гипертонией, диабетом и другими заболеваниями.
Предлагаемая композиция может быть применена к млекопитающим стоматическим, внутрибрюшинным внутривенным или любым другим способам. Количество
препарата в одной дозе должно составлять от примерно 1 мг до 0,5 г/кг веса тела. При стоматическом применении в предпочтительном варианте это количество в одной дозе составляет от примерно 0,01 мг до 100 мг/кг веса тела. Для применения лекарственного препарата может быть выбрана любая его форма: его можно применять в виде раствора в физиологическом соляном растворе или в других носителях, в виде инъекций, изготовленных при помощи лио- филизации и т.д., в виде суппозиториев, таблеток с покрытием, гранул, таблеток, капсул и т.д. с соответствующими носителями и разбавителями.
Острая токсичность. Указанная величина для предлагаемого полисахарида ПССТ составляет более 1200 мг/кг веса тела при внутрибрюшинном применении мышам. Предлагаемый материал является по существу нетоксичным при стоматическом применении.
Пример Получение и очистка полисахарида ПССТ. Streptococcus faectum ФЕРМ БП-296 прививают в 2 л среды бульона Рогоза с конечной концентрацией клеток 1x106 бактерий/мл. Среду после прививки культивируют в течение 10 ч при 37°С без перемешивания в аэробных условиях с тем, чтобы в результате получить культуральный бульон с концентрацией клеток 10 бактерий/мл. Бактериальные клетки собирают при помощи непрерывного центрифугирования со скоростью 12000 об/мин, промывают физиологическим соляным раствором (0,85% NaCI) и суспендируют в такой раствор с тем, чтобы получить 100 мл суспензии клеток с концентрацией 2х1010 бактерий/мл.
Упомянутую суспензию бактериальных клеток обрабатывают при 115°С в течение 10 мин и обрабатывают 3 раза смесью хлороформ-метанол (2:1 в/в) с целью удаления жиров.
Обезжиренную суспензию бактерий подвергают центрифугированию со скоростью 3000 об/мин в течение 10 мин, а нижний слой, т.е. слой хлороформа, удаляют. Водный слой используют в качестве исходного материала на следующих стадиях очистки.
Исходный материал затем обрабатывают 20 мг проназы (сигма протеаза типа X1Y) в 100 мл фосфатного буфера (рН 7,8), содержащего 0,0015 мг СаС12, при 47°С в течение 24 ч, а затем обрабатывают при помощи 10 мг проназы при тех же условиях.
Материал, обработанный проназой, разделяют на осажденную фракцию и фракцию верхнего слоя после отстаивания при
помощи центрифугирования-со скоростью 3000 об/мин в течение 10 мин.
Во фракцию верхнего слоя добавляют 1/9 объема 100%-ного (в/о) раствора трихлоруксусной кислоты (ТХК), выдерживают при 4°С в течение 3 ч при перемешивании, а затем полученный материал подвергают центрифугированию при скорости 3000 об/мин в течение 10 мин, в результате чего
0 получают осадок и верхний слой. В осажденную фракцию добавляют такой же объем 10%-ного раствора ТХК и повторяют описанную процедуру. Полученный верхний слой промывают 3 раза этиловым простым
5 эфиром с целью удаления ТХК, растворяют в 50 мл дистиллированной воды, нейтрализуют 1 н. раствором NaOH, диализируют с целью полного удаления ТХК и, наконец, подвергают его лиофилизации с тем, чтобы
0 получить 258 мг (сухой вес) фракции верхнего слоя.
Полученную фракцию верхнего слоя обрабатывают проназой, подвергают диализу, в результате чего получаю т 176 мг
5 (сухой вес) диализированной фракции (MB 3500). Диализированную фракцию в дальнейшем будем называть очищенной фракцией I.
Очищенную фракцию I подвергают
0 фракционированию при помощи хроматог- рафической колонны СефадексТ-100 (фирма Фармациа), урвновешенной буфером 0,05 М трис-HCI. Полученная в результате хроматограмма очищенной фракции I при
5 скорости элюирования 1 мл/мин, приведена на фиг.2, где по абсциссе откладывают объем элюирования, а по оси ординат - концентрацию элюированного материала. Фракцию после 124 мл собирают и в даль0 нейшем будем ее называть очищенной фракцией II (сухой вес 93,6 мг).
На фиг.З - приведена хроматограмма очищенной фракции II, которая была получена при помощи колонны Тойопеарал HW 5 55F, уравновешенной 25 мМ буфера трис- HCI, содержащего 0,3 М NaCI.
Скорость элюирования составила 1 мл/мин. На фиг.З кривые 1-3 представляют собой профили элюирования сахара, проте0 ина и нуклеиновой кислоты соответственно.
Очищенный полисахарид ПССТ (87,9 мг
сухой вес) выделяют при помощи отбора
порции, элюированной в области фракций
80 100мл.
5 На фиг.4 приведена хроматограмма полисахарида ПССТ при тех же эсперимен- тальных условиях, которые были использованы для фиг.З.
В табл.З приведен количественный выход протеина, который определялся мегодом Лоури, РНК, который определялся методом орсинола, ДНК, который определялся методом дифениламина, и сахара, который определялся методом фенола-НаЗСМ в каждом способе получения.
Удельная активность, приведенная в табл.3, указывает на относительную активность по снижению содержаний триглице- рида каждой фракции при испытании на крысах на единицу веса, причем активность термически обработанных бактериальных клеток равна 1. Методы анализа по определению активности снижения содержания триглицерида у животных описаны в примере 2.
Установлено, что полисахарид ПССТ может быть выделен и очищен из других бактериальных штаммов, перечисленных в табл.1, по аналогии с настоящим примером, но с меньшим выходом.
П р и м е р 2. Фармакологический эффект полисахарида ПССТ.
Активность по снижению содержания триглицерида.
1.Пробы физиологического раствора, содержащие эквивалент 16 мг/кг веса тела лиофилизованного полисахарида ПССТ, получают аналогичным образом. Эти пробы применяют стоматическим способом в ежедневной дозе 1 мл в крысам (возраст 18 недель, самцы, средний вес 246 г, 10 крыс в группе) и стерильным мышам (возраст 18 недель, самцы, средний вес тела 30 г, 10 мышей в группе). Крысы и мыши вскармливаются в течение 8-12 недель. Затем собирают артериальную кровь из абдоминальной аорты этих животных, а пробы сыворотки отделяют при помощи центрифугирования всей крови. Определяют содержание триглицерид ТГ ВАКО (фирма Вако Юниаке Ко, Лтд. Ацетил-ацетоновый метод).
Полученные рузультаты собраны в табл,4 (степень снижения-no сравнению со значениями в контрольных группах, к которым описанная обработка не применялась),
Состав диеты, которая применялась на период вскармливания, приведен в табл.5.
2.Упомянутые пробы применяют орально стоматическим способом в ежедневной дозе 1 мл к обычным крысам (возраст 18 недель, самцы, средний вес животного 238 г, 15 крыс в группе) и к обычным стерилизованным мышам (возраст 18 недель, самцы, средний вес животного 31 г, 10 мышей в группе) в течение 4 недель. Содержание триглицерида в крови определяют в точности так же, как это было описано. Полученные результаты собраны в табл.6 (степень снижения по сравнению со значениями.
полученными для необработанной контрольной группы).
3. Физиологические соляные пробы, содержащие 4 мг/мл полисахарида ПССТ, 5 применяют стоматическим способом в ежедневной дозе 1 мл на крысу в течение 2 недель к крысам, больным гиперлипиде- мией (возраст 18 недель, самцы, средний вес животного 250 г, 5 крыс в группе), кото0 рых вскармливают кормом, богатым холестерином. Содержание триглицерида в крови определяется в соответствии с приведенным описанием. Результаты собраны в табл.7.
5 Реакция на различные дозы. Физиологические соляные пробы, содержащие от 0,1 до 20 мг/мл полисахарида ПССТ, применяют стоматическим способом в ежедневной дозе 1 мл на обычную крысу (возраст 6 не0 дель, самцы, средний вес животного 216 г, 5 крыс в группе) в течение 4 недель. Содержание триглицерида в крови определяют указанными методами (в качестве контрольной группы использовалась группа необра5 ботанных крыс). Полученные результаты собраны в табл.8.
Острая токсичность. Физиологические соляные пробы (0,5 мл/мышь), содержащие 1,10 и 100 мг полисахарида ПССТ, применя0 ют внутрибрюшинным способом к мышам 1C (возраст 6 недель, средний вес 31,6±0,6 г, 10 животных в группе). Тана- тобиологические наблюдения за мышами осуществляют в течение 14 дней. Контроль5 ным материалом был физиологический соляной раствор.
Величина LDso, рассчитанная в соответствии с методом Беренса-Кербера, составила более 1200 мг/кг веса животного. При
0 стоматическом применении предлагаемый материал является по существу нетоксичным.
Фармацевтические композиции.
1.25 мг очищенного полисахарида 5 ПССТ тщательно перемешивают с 275 мг
порошка очищенного крахмала, а затем из полученной смеси изготавливают таблетки для стоматического применения. Каждая полученная таким образом таблетка соот- 0 ветствует дозе в 101 термически обработанных клеток/кг веса тела для взрослого пациента, имеющего вес в 50 кг.
2.Полисахарид ПССТ тщательно перемешивают с разбавителями, такими как
5 карбонат кальция, лактоза и т.д., смазывающими материалами, такими как стеариновая кислота, тальк и т.д, и другими добавками, а затем из полученной смеси получают таблетки для стоматического применения. Ежедневная доза полисахарида
ПССТ в общем случае составляет от 01, до 100 мг/кг веса тела.
3. Полисахарид ПССТ (900 мг) суспендируют и растворяют в дистиллированной воде (30 мл), добавляют ароматизирующий сироп, а затем приготавливают композиции в виде сиропа.
ПримерЗ. Получение и очистка ТР5- полисахарида.
S.faecalis PERM BP-297, S avlum PERM ВР-298, S. sallvarlus PERM BP-299, S.durans PERM BP-300, S.mltis PERM BP- 301, S.equlnus PERM BP-302 инокулируют в бубьон Рогоза {2 л) при конечной концентрации 1x10 бактерий/мл. Засеянную среду инкубируют в течение 10 ч при 37°С без перемешивания при аэробных условиях до получения 109 бактерий/мл культурального . бульона. Затем бактериальные клетки собирают при помощи непрерывного центрифугирования при 12000 об/мин, промывают физиологическим раствором (0,85% NaCI) и суспендируют в том же растворе до получения 100 мл суспензии клеток при концентрации 2х1010 мл.
Указанную бактериальную клеточную суспензию подвергают тепловой обработке при 115°С в течение 10 мин и трехкратной обработке смесью хлороформа и метанола (2:1 об/об) в целях удаления жиров.
Обезжиренную бактериальную суспензию центрифугируют при 3000 об/мин в течение 10 мин и нижний слой, т.е. слой хлороформа, отбрасывают. Водный слой используют в качестве исходного материала в последующей стадии очистки. Затем исходный материал обрабатывают 20 мг проназы (сигма проназа типа XIV) в 100 мл фосфатного буфера (рН 7,8), содержащего 0,0015 мг CaCl2, в течение 24 ч при 47°С, а затем при тех же условиях обрабатывают 10 мг проназы.
Обработанный проназой материал разделяют на фракции преципитации и супернатанта путем центрифугирования при 3000 об/мин в течение 10 мин. Во фракцию супернатанта добавляют 1/9 объема 100 мас.%-ной трихлоруксусной кислоты (ТСА), оставляют с перемешиванием на 3 ч при 4°С, а затем центрифугируют при 300 об/мин в течение 10 мин для получения фракции преципитации и супернатанта. Фракцию преципитации дополняют тем же объемом 10% ТСА и повторяют указанную процедуру. Полученный супернатант 3 раза промывают этиловым эфиром для удаления
ТСА, растворяют в 50 мл дистиллированной воды, нейтрализуют 1н. NaOH, диализуютс целью полного удаления ТСА и, наконец, лиофилизуют для получения фракции супернатанта.
Полученную фракцию супернатанта обрабатывают проназой описанным способом и диализуют для получения диализирован- ной фракции (MW 3500).
Указанную очищенную фракцию фракционируют при помощи хроматографии на колонках с Сефадексом С-100, уравновешенным 0,05 М трис-HCI буфером.
Очищенный TPS полисахарид выделяют
путем сбора элюированной части в 80- 100 мл фракций.
Выход полисахаридов приведен в табл.9.
Физико-химические свойства TPS полисахарида являются такими же, как описанные.
П р и м е р 4. Фармакологический эффект TPS полисахарида.
Указанные образцы были введены пероральнопри дневной дозе 10 мг/день/крыса стандартным крысам (самцам в возрасте 18 недель со средним весом 238 г, каждая группа содержала 15 крыс). Кровь животных анализировали на уровень триглицерида.
Степень снижения триглицерида приведена в табл.10.
Формула изобретения Способ получения гипотриглицеридаль- но-активных полисахаридов предусматривающий выращивание штамма-продуцента на питательной среде, содержащей источники углерода, азота, фосфора, минеральные соли, биостимуляторы роста и воду, в аэробных условиях до максимального накопления целевого продукта, отделение биомассы продуцента с образованием потока культуральной жидкости и последующее выделение и очистку целевого продукта с его депротеинизацией, отличающийся
тем, что, с целью повышения активности целевого продукта, в качестве штамма-продуцента используют штамм S.faecium PERM ВР-296 или S.faecails PERM BP-297, или S.savium PERM ВР-298, или S.sallvalls
PERM BP-299, или S.durans PERM BP-300, или S.mltis PERM BP-301, или S.equinus PERM BP-302, в качестве питательной среды - бульон Рогозы, а выделение целевого продукта проводят из культуральной жидкости или из биомассы после ее депротеини- зации и дезинтеграции.
13
1732815
14 Таблица 1







Изобретение относится к способу получения физиологически активных полисахаридов, которые могут найти применение в медицине. Целью изобретения является повышение активности целевого продукта. Способ заключается в том, что на бульоне Рогозы в аэробных условиях культивируют штамм Streptococcus faecium PERM BP-296 или Streptococcus faecalls PERM BP-297, или Streptococcus savlum PERM BP-298, или Streptococcus salivalls PERM BP-299, или Streptococcus olurans PERM BP-300, или Streptococcus mitis PERM BP-301, или SheptoccoccuS equinus PERM BP-302, отделяют биомассу от культуральной жидкости с последующим выделением целевого прс- дукт. Получаемые полисахариды обладают способностью снижать уровень триглицери- да в крови от 45 до 50%. 11 табл., 4ил. w Ё
.Т. а блица 2
Таблица 3
Таблица 4
Таблица 5
15
1732815
Диета, обогащенная холестерином (добавление 1 % холестерина в указанную диету)
Диета, обогащенная фруктозой (замена фруктозой всего количества пшеничного крахмала в указанной диете)
Таблица 7
Таблица 6
Таблица 8
Таблица 9
Табл и ца 10
+
+
+
2
37
+
+
+
+
+
+
+
+
Сфероид
0,5-1,0 мк в диаметре Пары или цепи в жидкой среде
± + 2
37
+ 2
37
+ +
37
+ .
1 +
±
2,3,5-Трифенилтетра золхлорид. производилось.
+ 2
37
+ +
37
3-7
37
+ .
1 +
±
Концентрация ,нг/м - .
%
Пропускание, % fe
I
N,
0,4
|1 Г
s
со го
00
ел
1
i
И
200
50100
05ын элншрованця, мл (Риг.5
О
100- 0&ъем эшироёания, мл
Фиг.4
f5ff
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Способ получения полисахарида | 1978 |
|
SU929015A3 |
| кл | |||
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
| Устройство для видения на расстоянии | 1915 |
|
SU1982A1 |
Авторы
Даты
1992-05-07—Публикация
1984-07-26—Подача