Изобретение относится к микробиологии и генной инженерии и касается способа получения рестриктирующей эндонуклеазы Sso II, которая может быть использована для определения первичной структуры ДН К. рестрикционного анализа, создания гибридных молекул.
Целью изобретения является повышение степени очистки целевого продукта.
Поставленная цель достигается тем, что в качестве продуцирующего микроорганизма используют штамм Е. coli B834/d24 несущий рекомбинантную плазмиду d 24, ответственную за синтез R Ssoll (4). Активные фракции с фосфоцеллюлозы Р II подвергают диализу против 5-30 мМ К-фосфатного буфера и проводят дополнительную аффинную хроматографию на денатурированной ДНК-целлюлозе.
За единицу активности рестриктазы принимают минимальное количество фермента, необходимое для полного расщеплеа
N К
а
ния 1 мкг ДНК фага в течение 1 ч при 37°С Активность фермента определяется в инкубационной смеси объемом 50 ml, содержащей 1-2 ml ферментного препарата, 1 мкг ДН К фага Я и буферный раствор следующего состава 0,1 М трис-HCI, 0,01 М MgClz О 001 М меркаптоэтанола, 50 мМ NaCI рН- 7 4 Время инкубации 1 час при 37°С
Фрагментацию ДНК тестируют в 0,8% агарозном геле Гель окрашивают раствором этидия бромида в концентрации 3 мкг/мл в течение 15 мин и фотографируют в ультрафиолетовом свете при 254 нм с красным светофильтром
Примеры конкретного осуществления способа
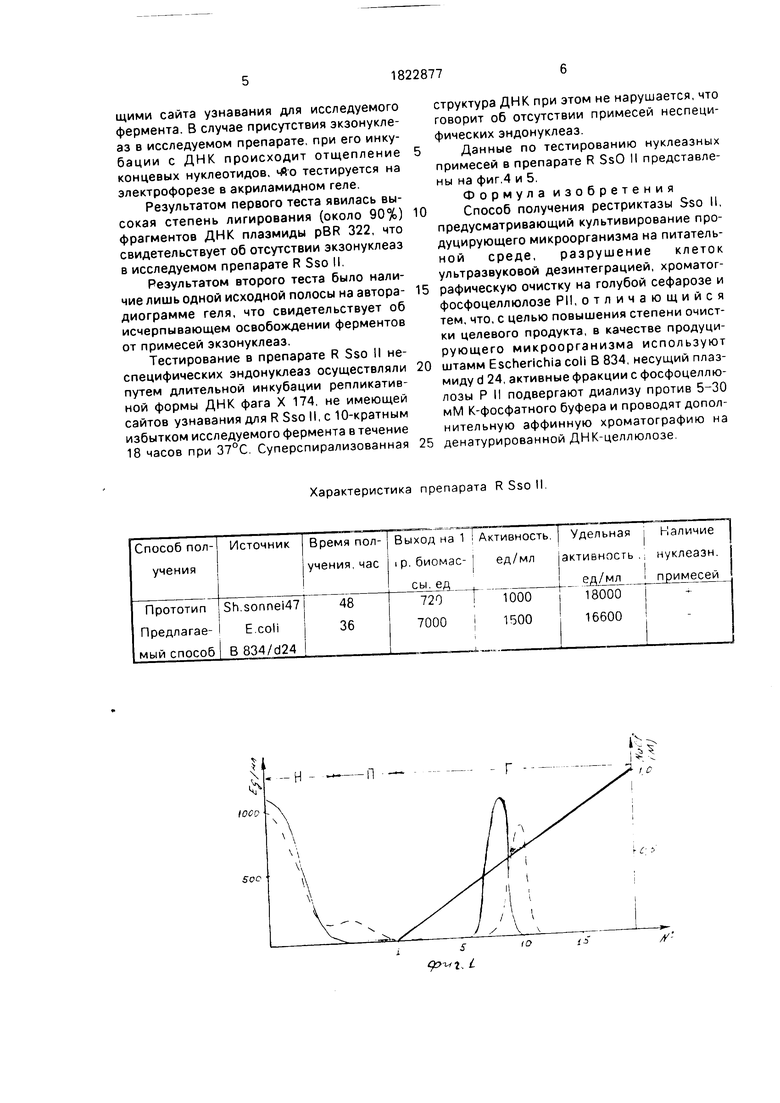
Пример 1 Клетки Е coli выращивают в ферментере АНКУМ-2 на среде Лурия до конца экспоненциальной фазы роста Разрушение клеток проводят методом ультразвуковой дезинтег рации при +4°С в течение 5 мин в режиме 12 кГц Обломки клеток удаляют центрифугированием при 40000 об/мин Хроматографическую очистку фер мента на ГС и ФЦ РП проводят аналогично способу прототипу Фракции после ФЦ РП содержащие рестриктазную активность, ди- ализуют против рабочего буфера (РБ) рН 7 4 содержащего 5 мМ фосфата калия 7 мМ меркаптоэтанола и 10 мМ ЭДТА наносят на колонку с денатурированной ДНК-целлюлозой размером 1 2 х 36 см уравновешенную тем же буфером Белок элюируют градиентом концентрации NaCI отО 0до 1 ОМ Фермент обнаруживается во фракциях с оответствующих 0 3-0 4 М NaCI неспецифическая нуклеазная активность - в области О 35-0 45 М NaCI частично перекрываясь с пиком ресктриктазной активности Колонку уравновешивали РБ содержащим 5 мМ фосфата калия Элюирующая система представлена линейным градиентом концентрации NaCI от 0 0 до 1 О М Скорость фракционирования 1 5 мл/ч Объем промывочного буфера 12 мл объем градиента 60 мл объем одной фракции 1 мл (см фиг 1)
На фиг 1 обозначены Н - оттекающая жидкость П - промывочный буфер, Г - гра диент По оси абсцисс номера фракций по оси ординат слева активность фермента (ед/мл) справа - молярность элюирующего раствора NaCI (M)
Облучен препарат R Sso II за 36 ч с удельной активностью 10 тыс ед/мг белка однако целевой продукт содержит нуклеаз- ные примеси Потери активности ферментного препарата составляют 25%
Пример 2 Фракции градиента с ФЦ PII содержащие рестриктазную актив ность диализуют против РБ содержащего
10 мМ фосфата калия, и проводят аффинную хроматографию на денатурированной ДЕК- целлюлозе, также используя 10 мМ К-фос- фатный буфер. Остальные параметры
фракционирования аналогичным примеру 1 R Sso II обнаруживается в первых фракциях промывочного буфера, т.е. элюируется 0,0 М NaCI пик неспецифических нуклеаз - в области 0 35-0,45 М NaCI. Колонку уравновешивали РБ, содержащим 10 мМ фосфата калия Элюирующая система и обозначения аналогичны примеру 1 (см.фиг 2) Фракции, обладающие рестриктазной активностью диализуют против РБ, содержащего 50%
глицерина, с целью концентрирования и стабилизации фермента
За 30 часов получен препарат R Sso II с удельной активностью 16 тыс ед/мг белка, полностью свободный от неспецифических
эндонуклеазных и экзонуклеазных примесей и пригодный для любых видов структурных исследований Потери активности фермента в процессе очистки составляют 20%
5ПримерЗ Способ получения R SsO
II включает все названные стадии При хроматографии на денатурированной ДНК-целлюлозе используют буфер, содержащий 30 мМ фосфата калия R Sso II и неспецифиче0 ские нуклеазы обнаруживаются в оттекающей жидкости в виде двух перекрывающихся пиков Колонку уравновешивали РБ содержащим 30 мМ фосфата калия Обозначения те же (см фиг 3). За 26 ч
5 получен препарат R SsoII с удельной активностью 8 тыс ед/мг белка Целевой продукт содержит нуклеазные примеси Потери активности Е SsOII составляет 25%
Для стандартной процедуры выделения
0 рестриктазы Sso II выбран пример 2
Преимущества предлагаемого способа получения R Ssoll по сравнению с прототипом заключаются в том, что фермент полностью свободен от примесей экзонуклеаз и
5 пригоден для всех видов молекулярно-био- логических работ включая структурные исследования например картирование генома
Препарат R Ssoll хранится при -20°С в
0 течение 12 месяцев (срок наблюдения) без потери активности
Сравнительные данные пи прототипу и предлагаемому способу представлены в таблице
5 Для доказательства отсутствия примесей экзонуклеаз в полученном ферментном препарате были использованы два теста 1) на эффективность лигирования фрагментов ДНК 2) тест короткими синтетическими мечеными Р олигонуклеотидами не имеющими сайта узнавания для исследуемого фермента. В случае присутствия экзонукле- аз в исследуемом препарате, при его инкубации с ДНК происходит отщепление концевых нуклеотидов, чЗо тестируется на электрофорезе в акриламидном геле.
Результатом первого теста явилась высокая степень лигирования (около 90%) фрагментов ДНК плазмиды pBR 322, что свидетельствует об отсутствии экзонуклеаз в исследуемом препарате R Sso II.
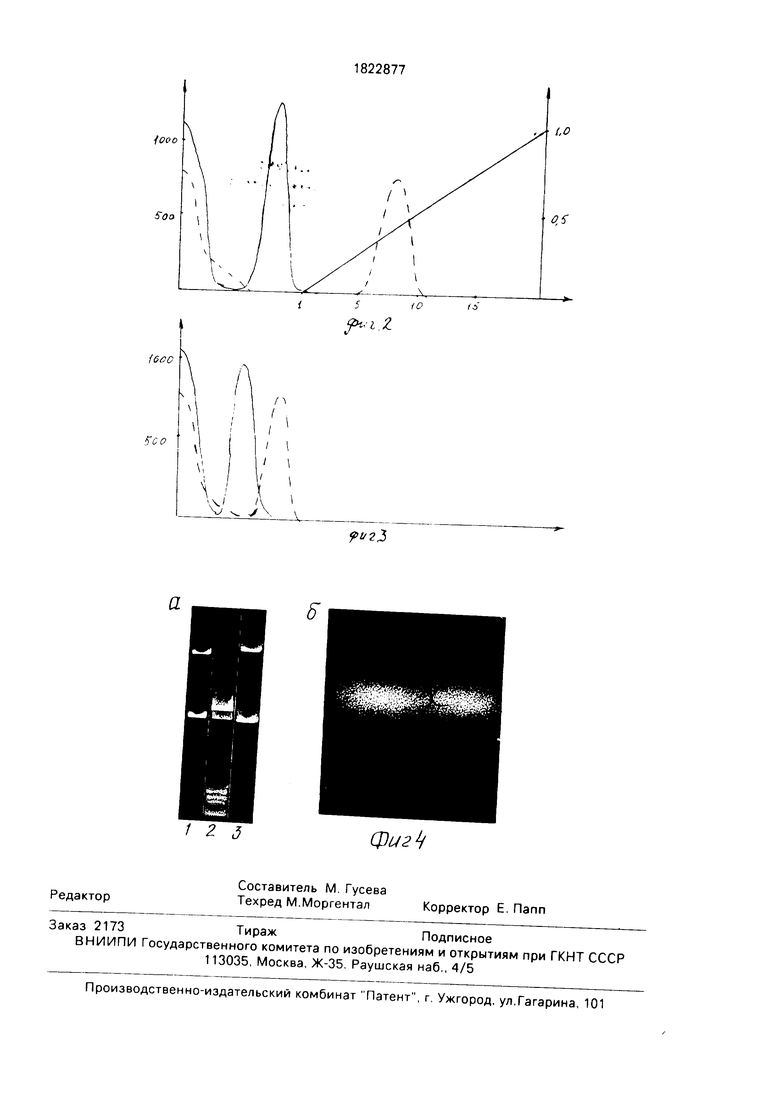
Результатом второго теста было наличие лишь одной исходной полосы на автора- диограмме геля, что свидетельствует об исчерпывающем освобождении ферментов от примесей экзонуклеаз.
Тестирование в препарате R Sso II неспецифических эндонуклеаз осуществляли путем длительной инкубации релликатив- ной формы ДНК фага X 174, не имеющей сайтов узнавания для R Sso II, с 10-кратным избытком исследуемого фермента в течение 18 часов при 37°С. Суперспирализованная
структура ДНК при этом не нарушается, что говорит об отсутствии примесей неспецифических эндонуклеаз.
Данные по тестированию нуклеазных примесей в препарате R SsO II представлены на фиг.4 и 5.
Формула изобретения Способ получения рестриктазы Sso II, предусматривающий культивирование продуцирующего микроорганизма на питательной среде, разрушение клеток ультразвуковой дезинтеграцией, хроматог- рафическую очистку на голубой сефарозе и фосфоцеллюлозе РИ, отличающийся тем, что, с целью повышения степени очистки целевого продукта, в качестве продуцирующего микроорганизма используют штамм Escherichia coli В 834, несущий плаз- миду d 24, активные фракции с фосфоцеллю- лозы Р II подвергают диализу против 5-30 мМ К-фосфатного буфера и проводят дополнительную аффинную хроматографию на денатурированной ДНК-целлюлозе

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения рестриктирующей эндонуклеазы SaU 6782 | 1991 |
|
SU1796676A1 |
| Способ получения ферментов из биомассы BacILLUS амYLоLIQUеFасIеNS штамм ВКПМ В-3188 | 1989 |
|
SU1661211A1 |
| Способ выделения эндонуклеазы рестрикции Ара 1 | 1989 |
|
SU1655986A1 |
| Способ получения рестриктазы | 1982 |
|
SU1067041A1 |
| Способ выделения рестриктаз II класса | 1989 |
|
SU1698289A1 |
| Способ получения сайт-специфической эндонуклеазы @ @ | 1983 |
|
SU1120019A1 |
| Способ получения рестриктазы, способной узнавать и расщеплять последовательность нуклеотидов GTCGAC | 1989 |
|
SU1752769A1 |
| Штамм бактерий ТнеRмUS RUвеR-продуцент рестриктазы TRU 9 1 | 1989 |
|
SU1687614A1 |
| Способ получения эндонуклеаз-рестриктаз, обладающих способностью узнавать и расщеплять последовательности нуклеотидов 5 @ -GPUCGPYC-3 @ и 5 @ -CATG-3 @ | 1987 |
|
SU1458388A1 |
| Штамм бактерий BacILLUS coaGULaNS - продуцент рестриктазы Всо AI | 1990 |
|
SU1761804A1 |

Использование:биотехнология и генная инженерия. Сущность изобретения: способ выделения рекстриктазы Sso II из клеток E.coli В 834 d 24, несущих плазмиду d 24, предусматривает трехстадийную схему хро- матографической очистки: голубая сефаро- за. фосфоцеллюлоза Р II, аффинная хроматография на денатурированной ДНК- целлюлозе, причем активные фракции с фосфоцеллюлозы подвергают диализу против 5-30 мМ К-фосфатного буфера. Получают рестриктазу с высокой степенью чистоты, полностью свободную от неспецифических нуклеазных примесей Фермент как и аналогичные препараты коммерческих фирм, обладает высокой удельной активностью и стабилен в течение 12 месяцев. Фермент Sso II узнает последовательность СС N GG, в которой центральный нуклеотид вырожден по всем четырем основаниям. Фермент может быть использован в генной инженерии для клонирования индивидуальных генов, создания гибридных молекул и в тонких структурных исследованиях, при картировании генома 1 табл. 5 ил (/ С
Характеристика препарата R Sso II
ЮОО 500
.. L
fee о
1 2 5
1,0
рыЈ
фМ2
| Roberts R.J | |||
| Restriction and modification enzymes and their recognition sequence Nucl | |||
| Acids | |||
| Res,1983, 11 | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Способ обделки поверхностей приборов отопления с целью увеличения теплоотдачи | 1919 |
|
SU135A1 |
| Косых A.M., Пунтежис М.А | |||
| Выделение рестриктирующей эндонуклеазы Есо R II Биохимия, № 47, с.619-624 | |||
| Упорова Т.М., Карташева И.М., Скрип- кин Е.А. | |||
| Лопарева Е.Н., Никольская И.И., Дебов С.С | |||
| Способ очищения сернокислого глинозема от железа | 1920 |
|
SU47A1 |
| мед | |||
| химии | |||
| Приспособление для установки двигателя в топках с получающими возвратно-поступательное перемещение колосниками | 1917 |
|
SU1985A1 |
| Способ очистки нефти и нефтяных продуктов и уничтожения их флюоресценции | 1921 |
|
SU31A1 |
| Способ получения продукта конденсации бетанафтола с формальдегидом | 1923 |
|
SU131A1 |
Авторы
Даты
1993-06-23—Публикация
1991-03-20—Подача