зптб. Изобретение относится к новому способу получения не описанных ра-. нее пиридо (3,2-Ь) индолов или их солей, которые являются потенциальными биологически активными соединениями. Известны способы получения производных пиридо (2,3-t) индолов (rf карболинов) методом Гребе-Ульмана и Гулланда (1-2), заключающиеся в том, что (Ь -бромпиридйн конденсируют с.фенилендиамином, диазотированием полученного пиридил-фениленди амина и полученный при этом ft -гтридштбензотриазол сплавляют с хлористы цинком при 320 С. При этом получают смесь карболинов Ci:,i:2:. Эти методы имеют ограниченное при .менение вследствие многостадийности, малой доступности исходных веществ и низкого выхода целевых продуктов (720%). Кроме того, указанные методы н позволяют получить сГ-карболины без примесей изомеров. С целью разработки нового способа получения не описанных ранее гПроизвод ных пирнцо (3,2-Ь) индолов, содержащ различные заместители, которые являю ся потенциальными биологически актив ными соединениями, предлагают способ получения производных пиридо (3,2-Ь) индолов общей формулы где R - водород, низший алкил; водород, низший алкил, галоид алкоксигруппа; Я,, R - метип или их соли путем обработки хлоргидратов 3-амино-2-индолкарбоновых кислот общей формулыгде R и R имеют указанные выше значения, при кипячении с ацетилацетоном. Целевые продукты выделяют в вяде основания или солей. Отличительными признаками способа является использование в качестве исходных соединений хлоргидратов производных З-амино-2-индолкарбоновой кислоты и обработка поспедней ацетилацетоном при кипячении реакционной массы. Схема процесса NH2HCl 0 С Особенность реакции состоит в одновременном протекании трех процессов: образования азометина, неожиданно легкого декарбоксилирования и циклизации с образованием производных (-карболинов без вьделения промежуточных соединений, т.е. в одну стадию. Соединения общей формулы I и их хлоргидраты получены с выходом 34,065,0%. Структура производных пиридо (3,2-t) индолов подтверждена данными масс, ИК- и УФ-спектров. Пример 1. 2,4-Диметил-5Нпиридо (3,2-Ь) индол. К раствору 4,6 г (0,023 моль) 2-карбэтокси-З-аминоиндола в 30 мл спирта прибавляют 6 мл 50%-ного раствора едкого кали и кипятят в колбе с обратным холодильником 20 мин. После охлаждения реакционной массы выпавший осадок калиевой соли З-амина-2-индолкарбоновой кислоты отфильтровывают, промывают спиртом и растворяют в 30 мл воды. Из охлажденного до 10 С раствора вьщеляют З-амино-2-индолкарбоновую кислоту при действии концентрированной соляной кислоты. Выпавший осадок З-амино-2-индолкарбоновой кислоты отфильтровывают, промывают водой, тщательно отжимают, а затем суспендируют в 30 мл диоксана, насыщенного хлористым водородом. Образовавшийся хлоргидрат 3-амино-2-индолкарбоновой кислоты отфильтровывают и промывают диоксаном насыщенным хлористым водородом. К полученной таким образом пасте хлор гидрата З-амино-2-индолкарбоновой кислоты прибавляют 25 мл ацетклацет на и медленно нагревают до образова ния прозрачного раствора, который затем кипятят 10-15 мин. В результа те образуется густая кристаллическа масса. От нее после охлаждения отфильтровывают кристаллы, промывают их диметилформамидом и сушат. Выход хлоргидрата 2,4-диметил-5Н-пиридо (3,2-Ъ) индола 2,0 г (38,0%), т.раз .выше 300°С {из диметилформамида). Найдено, %: N 12,4; С1 15,12%. C H jNjCl., Вычислено, %: N 12,04; СГ 15,23% ИК-спектр, см : 3060 (VNH индольн.) 2620 (). К раствору 2,0 г (0,009 моль) хлоргидрата 2,4-диметил-5Н-пиридо (3,2-Ь) индола в 30 мл воды прибавляют при размешивании 25%-ный водны раствор аммиака до щелочной среды. Выпавший при этом осадок отфильтровывают, промывают водой и сушат. Вы ход 2,4-диметил-5Н-пиридо (3,2-Ъ) индола-1,5 г (34,6% , считая на 2карбэтокси-3-аминсиндол), т.пл. 236 (из бензола). %: С 79,34; Н 6,25; Найдено, 14,44. Вычислено,%: С 79,56; Н 6,16; N 14,28. Мол. вес. 196. 4 jn р и м е р 2. 2,4,8-Трйметил-5Н-ПЙРИДО (3,2-Ь) индол получают в условиях примера 1 из 2,0 г (0,009 моль) 2-карбоэтокси-З-амино-5-метилиндола. Выход 2,4,8-триметш1-5Н-пиридо (3,2-) индола 0,8 г (41,7%), т.пл. 227-228°С (из бензола). Найдено, %: С 79,90; Н 6,56; 13,36. ., Вычислено,%: С 79,97; Н 6,71; N 13,32. Пример 3. 2,4-Диметил-8-хлор-5Н-пиридо (3,2-Ъ) индол получают в условиях примера 1 из 1,19 г (0,005 моль) 2-карбоэтокси-З-амино-5-хлориндола. Выход 2,4-диметил-8-хлор-5Н-пиридо (3,2-Ь) индола о,4 г (34,2%), т.пл. 228-229°С (из изопропанола). Найдено, %: С 67,90; Н 4,77; N 11,97; се 15,31%. C,jH,,NjCl. Вычислено, %: С 67,68; Н 4,81; 12,14; се 15,37%. Пример 4. Хлоргидрат 2,4,5-триметилпиридо (3,2-Ь) индола получают в условиях примера 1 из 2,7 г (0,012 моль) 1-метил-3-амино-2-карбоэтоксииндола. Выход хлоргидрата 2,4,5-триметилпиридо (3,2-Ь) индола2,0 г /65,0%), т.пл. 324-325°С (из спирта). Найде«о, %: N 11,76; С 14,36. iC H sNjCb. Вычислено,%: N 11,36; С1 14,37.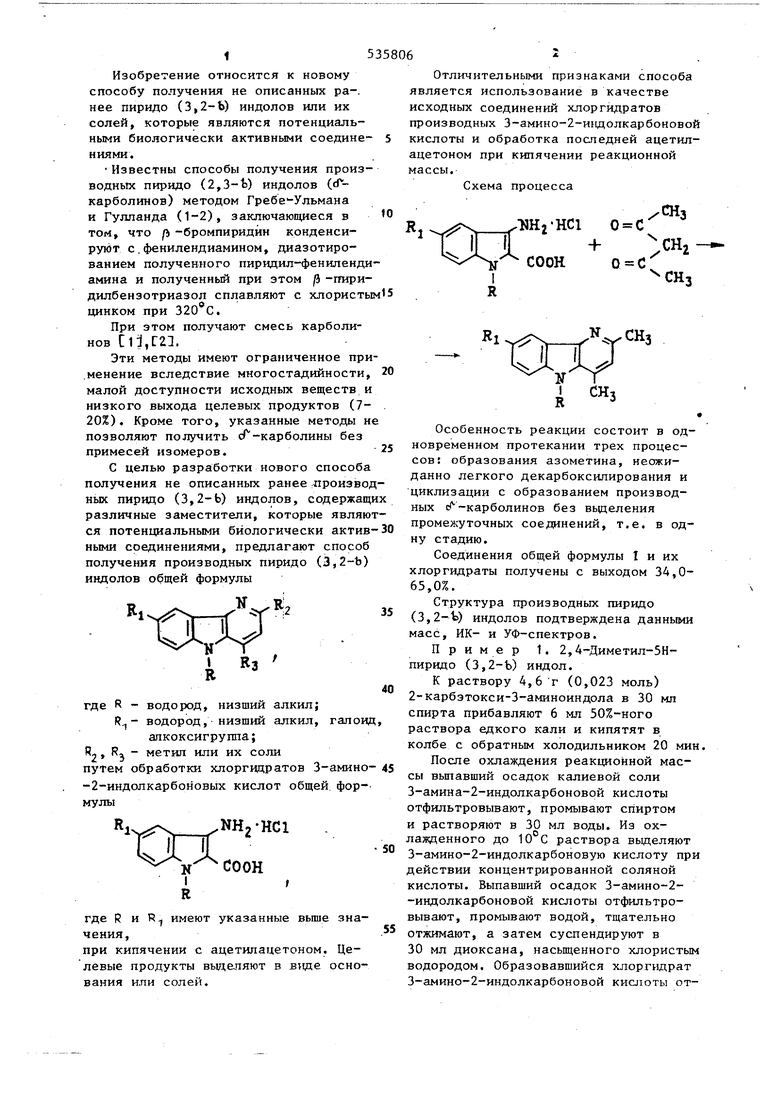

1. Способ получения пиридо 
| Spath Е., Eiter К | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Ber | |||
| Способ подготовки рафинадного сахара к высушиванию | 0 |
|
SU73A1 |
| и др | |||
| CCCXCV | |||
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| J | |||
| Chetn | |||
| Soc., 1929, 2926 (прототип). | |||
Авторы
Даты
1984-06-23—Публикация
1975-07-18—Подача