I
Изобретение относится к производным новой гетероциклической системы THeHuLz , 3 :5,6 пиримидо 3,4-а индола, которые могут найти применени в синтезе биологически активных веществ.
Известий производные тиено 2, 3ejпиримидина (1) и производные индоло С1,2-сЗх1 - азолина (и)
п
- I
Цель изобретения - производные новой гетероциклической системы.
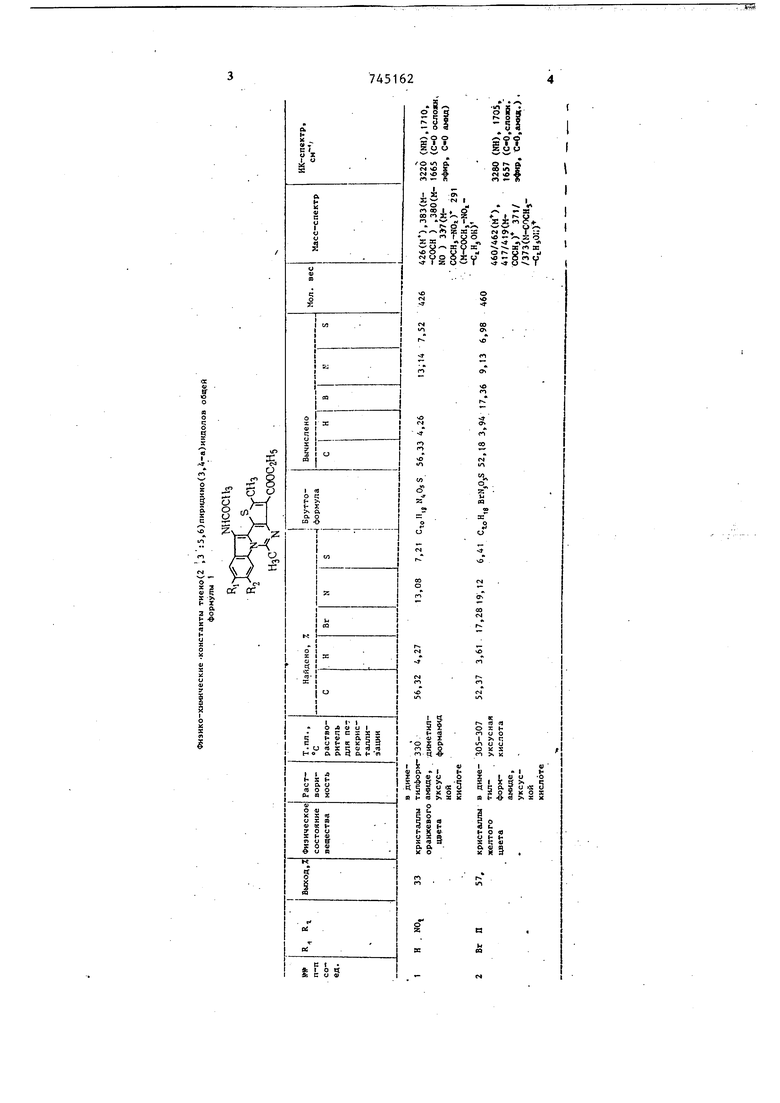
Цель достигается производными 2,5-диметш1-3-карбэтокси-11-апетиламинотиено 2 ,3 :5,б1пйримидо 3,4-а индола формулы
JIHCOCHj
л
R,
СНз
где R RI - водород или R, - водород, а RZ - нитрогруппа, или R,, бром, а RZ - йодород.
Способ получения соединений по изобретению основан на реакции N,0-диацетилиндоксила с арилгидразинами и аналогичен известному.
Нижеследуклцие примеры иллюстрируют получение целевых соединений.
Пример 1.
2,5-Диметш1-3-карбэтокси-11-ацетиламинотиено 2 ,3. :5,6jItиpимидo- 3,4-aЗиндoл.
К суспензии 0,54 г (0,0025 моль) N,0-диацетилиндоксила в 5 мл ледяной уксусной кислоты добавляют при пере451622.
мешивании 1 г (0,005 моль) М-(2-метил-3-карбэтокситиенш1-4) гидразина и дойодят до кипения. Затем добавляют 1,52 г (0,015 моль) уксусного ангйд5 .рида и кипятят 5 мин. Смесь охлаждают, вьщелившийся осадок отфильтровывают, промывают метанолом.
Получают 0,3 г (31,5%) 2,5-диметил-З-карбэтокси-11-ацетиламинотие10 ,3 :5,6 пиримидоСЗ,4-а индола в виде кристаллов желтого цвета трудно растворимых в спирте, растворимых при нагревании в диметилфюрмамиде и уксусной кислоте, т.пл. 286-287 С (из 15 уксусной кислоты). М.в. 381.
Найдено, %: С 62,82; Н 4,97;N 11,10; S 8,60. CioH jNjOjS
Вычислено, %: С 62,97; Н 5,02; 20N 11,02; S 8,41.
ИК-спектр, (V, ): 3300 (Ш), 1675 (, ел.эф., амид). УФ-спектр, СЛмАкс нм. (IgE) : 25 246 (4,46), 276 (4,59), 3,10 (3,85), плечо, 350 (3,92).
Масс-спектр: 331 (М), 338 (МСОСНз), 292 (М-СОСНл-CiHsOH)
ПМР-спектр, 8 , М.Д.: 2,31-с.СНз(«; , 302,75-С.СН,(„ , 3,15-с.
СНз(5), 4,42-СгН5сз, KB.CHi 1,4 -С Н5Смтр.СНз, 7,35-8,2 (ароматические протоцы),
9,58 - с. NH(1) . 5 t
Аналогично получают 2,5-диметил-З-карбзтокси-8-нитро-11-ацетиламинотиено 2 , 3 :5,6 пиримидо 3,4-а индол (соедин. 2) и 2,5-диметил-З-карбэток40 си-9-бром-11-ацетиламинотиеноС2 , 3 : 5,6 пиримидо Е3,4-а индол (соедин. 3), характеристика которых приведена в таблице.
| название | год | авторы | номер документа |
|---|---|---|---|
| Гидрохлориды производных 1(3) @ -2 метил-8 @ -индоло-(3,2- @ ) (1,3) бензодиазепина и способ их получения | 1979 |
|
SU803386A1 |
| Способ получения 4-окси-3-нитрокарбостирилов | 1974 |
|
SU578869A3 |
| Способ получения производных 1,2-диоксо-3-хлорнафталина или 4,5-диоксоиндола | 1981 |
|
SU1068417A1 |
| Способ получения 1н-2-оксопиридо /3,2-в/индолов | 1975 |
|
SU546616A1 |
| Способ получения производных бензиламина или их солей | 1975 |
|
SU640657A3 |
| Тиазолопиримидопиримидины, способ их получения и соли 3-амино-5-метилтиазоло[3,2- @ ]пиримидиния в качестве исходных | 1989 |
|
SU1647003A1 |
| Способ получения производных бензиламина или их солей | 1975 |
|
SU543341A3 |
| Способ получения производных карбоксамида оксобензотиазин-1,1-диоксида | 1975 |
|
SU664563A3 |
| Прлизводные 3- ( -бензохинонилимино) -4-оксо-3,4-дигидротиено (2,3- ) пиримидина, обладающие противовирусным дествием | 1977 |
|
SU677345A1 |
| Способ получения замещенных 3-(2-4фенил-1-пиперазинил-этил)-индолинов или их солей, или их четвертичных аммониевых солей | 1972 |
|
SU488408A3 |
Производные 2,5-диметил;-3-карбг этокси-11 -ацетиламинотиено 2 , : 5, 6 пиримидо 3,4-аЗ индола формулы ШСОСНз /H-j СООС2Н5 i где - водород юш R - водород, а Кг -нитрогруппа, или R, бром, а RI - водород.
| Способ сбора нерастворимых жидкостей с поверхности воды | 1981 |
|
SU1057612A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Двухтактный двигатель внутреннего горения | 1924 |
|
SU1966A1 |
| Шведов В.И | |||
| и др | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| ХГС, 1977, № 3, с.377 | |||
| СПОСОБ ПОЛУЧЕНИЯ КАТАЛИЗАТОРОВ НА ЦЕОЛИТНОЙ ОСНОВЕ ДЛЯ ПРЕОБРАЗОВАНИЯ ОКСИГЕНАТОВ В НИЗШИЕ ОЛЕФИНЫ | 2011 |
|
RU2548916C2 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1985-12-30—Публикация
1978-12-27—Подача