Изобретения относятся к ветеринарной вирусологии и биотехнологии и могут быть использованы при разработке и изготовлении средств специфической профилактики болезни Марека.
Болезнь Марека (БМ) - высококонтагиозное, лимфопролиферативное, злокачественное, вирусное заболевание птиц. БМ регистрируется во всех странах мира, где развито промышленное птицеводство, в том числе и в нашей стране, вызывая большие экономические потери. БМ характеризуется образованием единичных (в начальной стадии) и множественных опухолей во внутренних органах, коже, мышцах, а также изменениями центральной и периферической нервной системы. Вирус болезни Марека (ВБМ) повреждает иммунокомпетентные органы (селезенку, тимус, клоакальную сумку) и обладает таким образом иммунодепрессивной активностью, что приводит к снижению общей резистентности птиц и повышению их чувствительности к другим болезням. В связи с этим БМ довольно часто протекает в ассоциации с другими заболеваниями. Важным средством предупреждения БМ и снижения потерь от заболевания является вакцинопрофилактика. Для специфической профилактики используют вакцины трех типов: из аттенуированных штаммов ВБМ (серотип 1), из природноослабленного непатогенного ВБМ (серотип 2) и из штаммов вируса герпеса индеек (серотип 3).
Известна вирусвакцина против БМ, содержащая суспензию клеток фибробластов СПФ-эмбрионов кур (ФЭК), инфицированных штаммом CV1988 ВБМ 1 серотипа, сыворотку крови КРС и диметилсульфоксид (ДМСО) в качестве криопротектора (1).
Недостаток данной вакцины состоит в том, что она не устраняет носительства вирулентного вируса и сохраняет умеренную вирулентность для высокочувствительных линий цыплят.
Известна вирусвакцина против БМ, содержащая суспензию клеток ФЭК, инфицированных штаммом SB-1 вируса герпеса кур (ВГК) 2 серотипа, сыворотку крови КРС и ДМСО (2).
Недостаток данной вакцины состоит в том, что она также не устраняет носительства вирулентного вируса и опасность поражения лимфатических органов птиц высоковирулентными онкогенными штаммами ВБМ.
Известна вирусвакцина против БМ, содержащая суспензию клеток ФЭК, инфицированных штаммом "ВНИВИП" ВБМ, сыворотку крови КРС и ДМСО (3).
Недостаток данной вакцины состоит в том, что она не обладает достаточно высокой иммуногенной активностью в хозяйствах с высоким уровнем заболеваемости БМ.
Наиболее широкое распространение во всем мире получила вакцина на основе ВГИ (штамм FC-126), поскольку вирус не требовал аттенуации, не опасен в плане риверсии и подвергается стабилизации во внеклеточном состоянии. На основе ВГИ готовят 2 типа вакцин: свободную от клеток (сухую) и клеточно-ассоциированную (нативную).
Наиболее близким предлагаемому изобретению по совокупности существенных признаков является вирусвакцина против БМ, содержащая суспензию клеток ФЭК, инфицированных штаммом FC-126 ВГИ 3 серотипа, сыворотку крови КРС и ДМСО в следующем соотношении, мас.%:
суспензия инфицированных клеток - 80,0- 90,0
сыворотка КРС - 5,0-10,0
ДМСО - 5,0-10,0 (4).
Недостаток вакцины-прототипа состоит в ее низкой иммуногенной активности.
Известен способ изготовления вирусвакцины против БМ, включающий инфицирование культуры клеток ФЭК штаммом CV1988 ВБМ 1 серотипа, инкубирование зараженной культуры, сбор вируссодержащей клеточной массы, добавление криопротектора и получение целевого продукта (1).
Известен способ изготовления вирусвакцины против БМ, включающий инфицирование культуры клеток ФЭК штаммом SB-1 ВГК 2 серотипа, инкубирование зараженной культуры, сбор вируссодержащей клеточной массы, добавление криопротектора и получение целевого продукта (2).
Известен способ изготовления вирусвакцины против БМ, включающий инфицирование культуры клеток ФЭК штаммом "ВНИВИП" ВБМ, инкубирование зараженной культуры, сбор вируссодержащей клеточной массы, добавление криопротектора и получение целевого продукта (3).
Недостатком известных способов изготовления вирусвакцин против БМ состоит в том, что полученные вакцины не обладают достаточно высокой иммуногенной активностью в хозяйствах с высоким уровнем заболеваемости БМ.
Наиболее близким предлагаемому изобретению по совокупности существенных признаков является способ изготовления вирусвакцины против БМ, включающий инфицирование культуры клеток ФЭК штаммом FC-126 ВГИ 3 серотипа, сбор вируссодержащей клеточной массы, добавление криопротектора и получение целевого продукта (4)
Недостаток способа-прототипа состоит в том, что полученная вакцина также не обладает высокой иммуногенной активностью в хозяйствах с высоким уровнем заболеваемости БМ.
В задачу создания группы настоящих изобретений входила разработка вирусвакцины против БМ на основе нового штамма ВГИ 3 серотипа, обладающей более высокой иммуногенной активностью по сравнению с вакциной-прототипом, и способа ее изготовления.
Технический результат от использования группы предлагаемых изобретений заключается в повышении иммуногенной активности целевого продукта.
Указанный технический результат достигнут созданием группы изобретений, образующих единый изобретательский замысел. В группу включены изобретения, одно из которых предназначено для получения другого.
Указанный технический результат достигнут созданием вирусвакцины против БМ, охарактеризованной следующей совокупностью признаков:
1) вирусвакцина против БМ;
2) суспензия клеток, инфицированных штаммом ВГИ 3 серотипа;
3) из штаммов 3 серотипа вакцина содержит штамм "ВНИИЗЖ/N110" ВГИ;
4) штамм "ВНИИЗЖ/N110" взят в эффективном количестве;
5) вирусвакцина содержит штамм "ВНИИЗЖ/N110" ВГИ с биологической активностью не ниже 1•105 ФОЕ/см3;
6) в качестве клеточного субстрата вирусвакцина содержит культуру клеток ФЭК:
7) сыворотка крови КРС;
8) ДМСО в качестве криопротектора;
9) вирусвакцина содержит суспензию клеток ФЭК, инфицированных штаммом "ВНИИЗЖ/N110" ВГИ, сыворотку крови КРС и ДМСО в следующем соотношении, мас. %:
суспензия инфицированных клеток - 60,0-80,0
сыворотка крови КРС - 15,0-25,0
ДМСО - 5,0-15,0
Предлагаемое изобретение включает следующую совокупность существенных признаков, обеспечивающих получение технического результата во всех случаях, на которые испрашивается правовая охрана:
1) вирусвакцина против БМ;
2) суспензия клеток, инфицированных штаммом ВГИ 3 серотипа;
3) из штаммов 3 серотипа вирусвакцина содержит штамм "ВНИИЗЖ/N110" ВГИ;
4) штамм "ВНИИЗЖ/N110" ВГИ взят в эффективном количестве;
5) сыворотка крови КРС.
6) ДМСО.
Предлагаемое изобретение характеризуется также другими признаками, выражающими конкретные формы его выполнения или особые условия использования:
1) в качестве клеточного субстрата вирусвакцина содержит культуру клеток ФЭК;
2) вирусвакцина содержит штамм "ВНИИЗЖ/N110" ВГИ с биологической активностью не менее 1•105 ФОЕ/см3;
3) вирусвакцина содержит суспензию клеток ФЭК, инфицированных штаммом "ВНИИЗЖ/N110" ВГИ, сыворотку крови КРС и ДМСО в следующем соотношении, мас. %:
суспензия инфицированных клеток - 60,0-80,0
сыворотка крови КРС - 15,0-25,0
ДМСО - 5,0-15,0
Признаками изобретения, характеризующими предлагаемую вирусвакцину и совпадающими с признаками прототипа, в том числе родовое понятие, отражающее назначение, являются:
1) вирусвакцина против БМ;
2) суспензия клеток, инфицированных штаммом ВГИ 3 серотипа;
3) сыворотка крови КРС;
4) ДМСО.
По сравнению с вирусвакциной-прототипом существенным отличительным признаком является то, что из штаммов 3 серотипа предлагаемая вирусвакцина содержит штамм "ВНИИЗЖ/N110" ВГИ, взятый в эффективном количестве.
Предлагаемое изобретение характеризуется также другими отличительными признаками, выражающими конкретные формы его выполнения или особые условия использования:
1) в качестве клеточного субстрата вирусвакцина содержит культуру клеток ФЭК;
2) вирусвакцина содержит штамм "ВНИИЗЖ/N110" ВГИ с биологической активностью не ниже 1•105 ФОЕ/см3;
3) вирусвакцина содержит суспензию клеток ФЭК, инфицированных штаммом "ВНИИЗЖ/N110" ВГИ, сыворотку крови КРС и ДМСО в следующем соотношении, мас. %:
суспензия инфицированных клеток - 60,0-80,0
сыворотка крови КРС - 15,0-25,0
ДМСО - 5,0-15,0
Предлагаемая вирусвакцина обладает более высокой иммуногенной активностью по сравнению с вирусвакциной - прототипом.
Штамм "ВНИИЗЖ/N110" является новым, ранее неизвестным вариантом ВГИ.
Указанный технический результат достигнут также созданием способа изготовления вирусвакцины против БМ, охарактеризованного следующей совокупностью признаков:
1) способ изготовления вирусвакцины против БМ;
2) инфицирование культуры клеток штаммом ВГИ 3 серотипа;
3) в качестве клеточного субстрата используют культуру клеток ФЭК;
4) из штаммов 3 серотипа используют штамм "ВНИИЗЖ/N110" ВГИ в эффективном количестве;
5) штамм "ВНИИЗЖ/N110" ВГИ используют с биологической активностью не ниже 1•105 ФОЕ/см3;
6) инкубирование зараженной культуры;
7) сбор вируссодержащей клеточной массы;
8) добавление криопротектора;
9) суспензию клеток ФЭК, инфицированных штаммом "ВНИИЗЖ/N110" ВГИ, сыворотку крови КРС и ДМСО берут в соотношении 12:16 - 3:5 - 1:3 соответственно;
10) получение целевого продукта.
Предлагаемое изобретение включает следующую совокупность существенных признаков, обеспечивающих получение технического результата во всех случаях, на которые испрашивается правовая охрана:
1) способ изготовления вирусвакцины против БМ;
2) инфицирование культуры клеток штаммом "ВНИИЗЖ/N110" ВГИ 3 серотипа;
3) инкубирование зараженной культуры;
4) сбор вируссодержащей клеточной массы;
5) добавление криопротектора;
6) получение целевого продукта.
Предлагаемое изобретение характеризуется также другими признаками, выражающими конкретные формы использования:
1) в качестве клеточного субстрата используют культуру клеток ФЭК;
2) штамм "ВНИИЗЖ/N110" ВГИ используют с биологической активностью не ниже 1•105 ФОЕ/см3;
3) суспензию клеток ФЭК, инфицированных штаммом "ВНИИЗЖ/N110" ВГИ, сыворотку крови КРС и ДМСО берут в соотношении 12:16 - 3:5 - 1:3 соответственно.
Признаками изобретения, характеризующими предлагаемый способ и совпадающими с признаками прототипа, в том числе родовое понятие, отражающее назначение, являются:
1) способ изготовления вирусвакцины против БМ;
2) инфицирование культуры клеток штаммом ВГИ 3 серотипа;
3) инкубирование зараженной культуры;
4) сбор вируссодержащей клеточной массы;
5) добавление криопротектора;
6) получение целевого продукта.
По сравнению со способом-прототипом существенным отличительным признаком изобретения является использование в составе вирусвакцины нового штамма "ВНИИЗЖ/N110" ВГИ в эффективном количестве.
Предлагаемое изобретение характеризуется также другими отличительными признаками, выражающими конкретные формы его выполнения или особые условия использования:
1) в качестве клеточного субстрата используют культуру клеток ФЭК;
2) штамм "ВНИИЗЖ/N110" ВГИ используют с биологической активностью не ниже 1•105 ФОЕ/см3;
3) суспензию клеток ФЭК, инфицированных штаммом "ВНИИЗЖ/N110" ВГИ, сыворотку крови КРС и ДМСО берут в соотношении 12:16 - 3:5 - 1:3 соответственно.
Вирусвакцина, полученная предлагаемым способом, обладает более высокой иммуногенной активностью по сравнению с аналогичным препаратом, полученным способом-прототипом.
Достижение технического результата от использования предлагаемого способа объясняется тем, что при изготовлении вирусвакцины используют новый штамм "ВНИИЗЖ/N110" ВГИ, обладающий по сравнению со штаммом FC-126 ВГИ более высокой иммуногенной активностью.
Исходный вирус для получения штамма "ВНИИЗЖ/N110" был выделен в 1998 году из эпителия перьевых фолликулов СПФ-цыплят, иммунизированных вируссодержащим материалом из штамма FC-126 ВГИ. Производственный штамм "ВНИИЗЖ/N110" ВГИ получен методом перемежающихся пассажей через организм СПФ-цыплят и культуру клеток фибробластов СПФ-эмбрионов кур. Штамм "ВНИИЗЖ/N110" ВГИ представляет собой апатогенный генетически однородный вирусный материал, легко культивируемый в культуре куриных эмбриональных фибробластов с высокой биологической активностью (титр вируса 2,0-3,0•106 ФОЕ/см3) и вызывающий напряженный иммунитет по сравнению со штаммом FC-126 у привитой птицы.
Штамм "ВНИИЗЖ/N110" ВГИ депонирован в коллекции микроорганизмов Всероссийского государственного научно-исследовательского института контроля, стандартизации и сертификации ветеринарных препаратов (ВГНКИ) 18.12.98 г. под регистрационным номером "ВНИИЗЖ/N 110-ДЕП".
По сравнению со штаммом FC-126 штамм "ВНИИЗЖ/N 110" обладает более высокой биологической, антигенной и иммуногенной активностью в нативном виде. Экспериментально подтверждена его возможность использования для приготовления вакцины против БМ. Штамм "ВНИИЗЖ/N 110" ВГИ обеспечивает получение живой вакцины против БМ, создающей защиту птиц против указанного возбудителя заболевания.
Сущность изобретения пояснена на графическом материале (см. чертеж), на котором представлена нуклеотидная последовательность фрагмента гена gB 966-1296 штамма "ВНИИЗЖ/N 110" ВГИ (жирным шрифтом отмечены его нуклеотидные отличия от штамма FC-126).
Штамм "ВНИИЗЖ/N 110" ВГИ характеризуется следующими признаками и свойствами.
Морфологические признаки
Штамм "ВНИИЗЖ/N 110" ВГИ относится к семейству Herpesviridae, роду Herpesvirus, серотипу 3. На основании сравнительного электронно-микроскопического изучения производственного штамма FC-126 ВГИ и штамма "ВНИИЗЖ/N 110" при репродукции их в культурах клеток установлена идентичность характеристик обоих штаммов. Эти вирусы проходили онтогенетический цикл развития в нуклеоплазме, а в цитоплазме - завершающие стадии морфогенеза. Внутриядерный цикл развития включает стадии виропласта, нуклеотида, сборку нуклеокапсида, формирование наружной суперкапсидной мембраны. Наиболее частой формой, присутствующей на всех стадиях культивирования, является нуклеокапсид с нуклеотидом, представленным плотным образованием, заключенным в капсидную белковую оболочку. При электронно-микроскопическом исследовании штамм "ВНИИЗЖ/N 110" представлен типичными для вирусов герпеса группами В вирионами, имеющими икосаэдрическую форму, нуклеокапсид содержит 2-нитевую ДНК. В ядре пораженной клетки вирион имеет величину 90-100 нм, в цитоплазме размер его увеличивается за счет белковой оболочки до 180-200 нм. Оболочка состоит из 162 капсомеров, расположенных в кубической симметрии.
Антигенные свойства
По своим антигенным свойствам штамм "ВНИИЗЖ/N 110" ВГИ относится к серотипу 3. При введении в организм вызывает латентно протекающую вирусемию. Антитела к данному вирусу обнаруживают в крови цыплят к 14-21-дневному сроку с дальнейшим нарастанием к 40-60 дню. При вакцинации вирус индуцирует образование специфических антител, выявляемых в РДП и ИФА. Активность в РСК не установлена. Концентрированный антиген "ВНИИЗЖ/N 110" реагирует в РДП со специфическими сыворотками ВГИ и ВБМ. Выявляются общие антигены с ВБМ в прямой и непрямой РИФ. При разрушении клетки вступает в реакцию с антителами к ВГИ и ВБМ в РН. В ИФА вступает в реакцию с антителами к ВГИ и ВБМ.
Биотехнологические характеристики
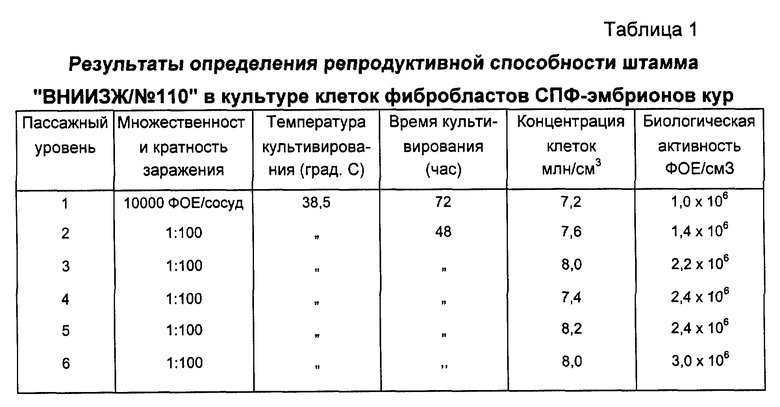
Штамм "ВНИИЗЖ/N 110" активно размножается в СПФ-эмбрионах кур и в первично-трипсинизированной культуре фибробластов СПФ-эмбрионов кур. Трипсинизацию эмбрионов и культивирование фибробластов проводят по общепринятым методикам с использованием смеси сред на основе ГЛА, Игла и 199, взятых в равных частях, с добавлением 10% эмбриональной сыворотки КРС. Клетки фибробластов выращивают во флаконах емкостью 50 см3 и 100 см3 (Повицкого), в матрасах емкостью 1,5 дм3 и в роллерных 3-литровых сосудах. Посевная концентрация для флаконов и матрасов составляет 400-500 кл/см3, для роллерных сосудов от 1,2 до 1,5 млн. кл/см3. При размножении в культуре фибробластов вирус проявляет ярко выраженный цитопатический эффект - образование характерных фокусов, состоящих из рефрактильных округлых клеток (поликариоцитов). Размеры фокуса достигают 0,1-0,2 мм. При проведении последовательных пассажей в культуре фибробластов СПФ-эмбрионов кур инфекционный титр вируса увеличивался и достигал 2,0-3,0•106 ФОЕ/см3 (фокусообразующих единиц).
При заражении 6-суточных СПФ-эмбрионов кур в желточный мешок штамм "ВНИИЗЖ/N 110" вызывает их гибель до 20% на 3-5 сутки инкубации. У павших эмбрионов отмечают отставание в росте, гепатиты, увеличение селезенки и почек. На хориоаллантоисной оболочке образуются мелкие бляшки серовато-белого цвета звездчатой формы размером до 1 мм в небольших количествах. У эмбрионов развивается гепатит. Штамм "ВНИИЗЖ/N 110" ВГИ предназначен для использования в качестве сырья для изготовления живой вакцины против БМ.
Результаты определения репродуктивной способности штамма "ВНИИЗЖ/N 110" в культуре клеток фибробластов СПФ-эмбрионов кур представлены в таблице 1.
Хемо- и генотаксономическая характеристика
Штамм "ВНИИЗЖ/N 110" является ДНК-содержащим вирусом с молекулярной массой 108-120•106 Д. Нуклеиновая кислота представлена двуцепочечной линейной молекулой. Содержание G+C - 46%. Вирион состоит из нуклеотида, икосаэдрического капсида, асимметрично расположенного вокруг капсида электронноплотного материала, обозначаемого как тегумент, и липопротеидной оболочки. Вирионная ДНК участвует в образовании белков-предшественников в инфицированных клетках. Предшественники в свою очередь расщепляются с образованием более стабильных структурных и неструктурных полипептидов вируса. Основными антигенными белками являются гликопротеины А (gA) и В (gB). Гликопротеин В играет важную роль в индукции защитного иммунитета и является высококонсервативным среди герпесвирусов. Он представляет собой комплекс трех гликопротеинов: gp 49, gp 60 и gp 100.
Проведено определение первичной структуры фрагмента гена gB вируса с помощью полимеразно-цепной реакции (ПЦР) и секвенирования амплифицированного фрагмента. Изучение нуклеотидной последовательности генома штамма "ВНИИЗЖ/N 110" методом секвенирования по Сенсеру показало, что фрагмент гена gB 966-1296H имеет 2 нуклеотидные замены в позициях 1038Н "С" на "Т", 1200Н "А" на "G" и одну замену в позиции 1175Н с "Т" на "C" в отличие от штамма FC-126, представленного в международном ген-банке. Таким образом, штамм "ВНИИЗЖ/N 110" отличается от штамма FC-126 по трем нуклеотидным основаниям, однако все три мутации не приводят к заменам соответствующих аминокислот. Гомология нуклеотидной структуры исследованного фрагмента штаммов FC-126 и "ВНИИЗЖ/N 110" составляет 99,1%. Результаты исследований представлены на прилагаемом графическом материале.
Устойчивость к внешним факторам
Устойчивость штамма "ВНИИЗЖ/N 110" ВГИ к физическим и химическим факторам характеризуется следующими данными. Центрифугирование при 50000 g осаждает вирус в течение 1 час. В пределах pH 4-10 вирус чувствителен к эфиру.
Вирус выдерживает неоднократное замораживание - оттаивание и воздействие ультразвуком в течение 10 мин. Полная термоинактивация вируса происходит при 4oC через 2 недели хранения, при 20-25oC - через 4 дня, при 37oC - через 18 часов и при 60oC - за 10 мин.
Хранение и консервирование
Вирус сохраняется в клеточно-ассоциированном виде в смеси из равных объемов сред на основе гидролизата лактальбумина (ГЛА), Игла и 199 с 20% сыворотки КРС и 10% диметилсульфоксида в герметически запаянных ампулах в жидком азоте при - 196oС в течение 24 месяцев.
Патогенные свойства
Не вызывает инфекции у птиц, контагиозность не установлена. Лабораторные и домашние животные к вирусу не чувствительны.
Иммуногенность штамма
Штамм вызывает иммунитет в дозе 1000 ФОЕ у 90-98% цыплят в производственных условиях. Иммуногенность не меняется в течение 5 последовательных пассажей.
Дополнительные признаки и свойства
Штамм "ВНИИЗЖ/N 110" ВГИ свободен от контаминации бактериальной и грибковой флорой, чужеродными вирусами и микоплазмами, безвреден в 10-кратной дозе для суточных цыплят.
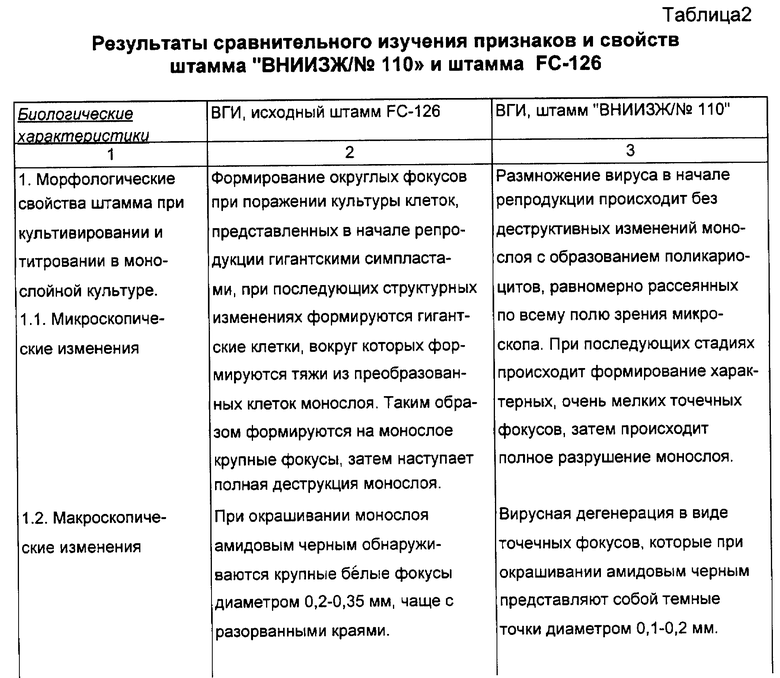
На основании полученных данных можно утверждать, что штамм "ВНИИЗЖ/N 110" ВГИ является оригинальным, в таксономическом отношении новым, ранее неизвестным изолятом ВГИ.
В таблице 2 приведены результаты сравнительного изучения признаков и свойств штамма "ВНИИЗЖ/N 110" и штамма FC-126.
Проведенный заявителем анализ уровня техники, включающий поиск по патентным и научно-техническим источникам информации, и выявление источников, содержащих сведения об аналогах предлагаемых изобретений, позволил установить, что заявитель не обнаружил источники, характеризующиеся признаками, тождественными (идентичными) всем существенным признакам предлагаемых изобретений. Определение из перечня выявленных аналогов прототипов, как наиболее близких по совокупности признаков, позволило установить совокупность существенных по отношению к усматриваемому заявителем техническому результату отличительных признаков предлагаемой вирусвакцины и способа ее изготовления, изложенных в независимых пунктах формулы.
Следовательно, заявляемые изобретения соответствуют условию патентоспособности "новизна".
Для проверки соответствия предлагаемых решений условию патентоспособности "изобретательский уровень" проведен дополнительный поиск известных решений для выявления признаков, включенных в отличительные части независимых пунктов формулы. Результаты поиска показали, что предлагаемые решения не вытекают для специалиста явным образом из известного уровня техники, изложенного в соответствующем разделе описания (не выявлены решения, имеющие признаки, совпадающие с отличительными признаками предлагаемых изобретений), а также не выявлено влияние предусматриваемых существенными признаками предлагаемых изобретений преобразований для достижения технического результата.
Следовательно, предлагаемая вакцина и способ ее изготовления соответствуют условию патентоспособности "изобретательский уровень".
Сущность предлагаемых изобретений пояснена примерами их исполнения.
Пример 1.
Вакцину готовят следующим образом. Вакцинный штамм "ВНИИЗЖ/N110" хранят в сосудах Дьюара с жидким азотом (- 196oC). При изготовлении вакцины производят рассев расплодки в культуре куриных эмбриональных фибробластов. Для этого берут 3-7 ампул с вакцинным штаммом вируса, титр которого должен быть не менее 1•105 ФОЕ/см3. После извлечения из азота ампулы немедленно помещают в воду с температурой 35-37oC до полного оттаивания. После оттаивания содержимого ампул горлышки ампул тщательно обтирают спиртом, обжигают и отбивают запаянные концы стерильным корнцангом. Пипеткой аккуратно берут содержимое ампул, объединяют и разводят (или используют без разведения) питательной средой, содержащей смесь сред на основе ГЛА, Игла и 199, взятых в равном соотношении, из расчета, чтобы в каждом 1 см3 содержалось 10000 ФОЕ. Затем сливают из роллерных флаконов с 24-48-часовой культурой клеток ростовую среду и заменяют ее поддерживающей с 2% сыворотки КРС. В поддерживающую среду вносят вируссодержащую суспензию в количестве 100-150 ФОЕ/см3 площади флакона. Флаконы с зараженной культурой помещают в роллерную установку со скоростью вращения 8-10 об/час в термальной комнате (термостате) при температуре 39-40oC на 3 суток. К моменту съема клеток типичные фокусные поражения на культуре клеток должны быть отчетливо видны под микроскопом.
Поддерживающую среду удаляют осторожно, не допуская смывания клеток со стекла, в сосуды вносят подогретый до 30-37oC 0,125-0,25% раствор трипсина из расчета 0,07-0,1 см3/см2 площади флакона. Монослой смачивают раствором трипсина 2-3 мин, затем раствор трипсина сливают, флаконы вращают со скоростью до 20 об/мин при комнатной температуре 5-7 мин, после чего в сосуды в тех же объемах вносят поддерживающую питательную среду без сыворотки. Энергичным покачиванием клетки отслаивают от стекла и суспендируют в среде, после чего проводят 2 пассаж. С этой целью инфицированными клетками, собранными с одного роллерного флакона, заражают свежий монослой из расчета 1:5-1: 10, т.е. 5-10 роллерных флаконов, и культивируют монослой до съема вируса и проведения 3 пассажа 48 часов. Сосуды с клеточными культурами, зараженными вирусом первого пассажа, помещают в роллерные установки в термальной комнате при 39-40oC. Характер специфического вирусного поражения монослоя, зараженного вирусом первого пассажа, несколько отличается от поражений, вызываемых вирусом второго пассажа. При культивировании вируса первого пассажа отмечают очаговое (фокусное) поражение монослоя. Вирус второго пассажа поражает гораздо большую часть клеток: в культуре клеток на 50-70% монослоя образуются симпласты и поликариоциты (крупные многоядерные клетки), которые легко можно увидеть под микроскопом. Сбор клеток, инфицированных вирусом второго пассажа, осуществляется методом, описанным для вируса первого пассажа. Клеточносвязанным вирусом второго пассажа заражают монослойные культуры клеток (3 пассаж вируса) из расчета 1:50-1:100 и затем их инкубируют 48-72 часа. По окончании периода инкубации в термальной комнате при 39-40oC проводят сбор инфицированных клеток. Для этого инфицированные монослои обрабатывают 0,125-0,25% раствором трипсина, т.е. так же, как и при съеме вируса первого и второго пассажей. После удаления трипсина во флаконы вносят поддерживающую среду с 20% сыворотки крови КРС и 10% ДМСО. Объем среды для сбора и суспендирования клеток составляет 0,02-0,04 см3/см2 площади флакона. Собранные суспензии инфицированных клеток объединяют в общем объеме. Концентрация клеток в суспензии должна быть 5-10 млн/см3. Собранную суспензию инфицированных клеток разливают по 1-2 см3 в предварительно маркированные ампулы, которые закрывают стерильной ватой, запаивают в пламени газовой горелки и помещают в холодильник (2-4oC) на 40-60 мин. Затем ампулы выдерживают 40-60 мин при -40oC, после этого ампулы с вакциной немедленно погружают в жидкий азот.
Полученную таким образом вакцину контролируют на стерильность и инфекционную активность. Титр вируса в вакцине должен быть не ниже 1•105 ФОЕ/см3. По титру устанавливают количество иммунизирующих доз в 1 см3. За одну прививную дозу принимают 1000 ФОЕ. Срок годности вакцины при условии хранения ее в жидком азоте 12 месяцев. Вирусвакцина жидкая культуральная применяется с профилактической целью. Вакцинируют цыплят в первые часы после выборки из выводных шкафов непосредственно в инкубатории. Вакцину в дозе 1000 ФОЕ/0,2 см3 вводят цыплятам внутримышечно в верхнюю треть бедра.
Полученная вирусвакцина против БМ имеет оптимальный компонентный состав, мас.%:
Суспензия клеток ФЭК, инфицированных штаммом "ВНИИЗЖ/N110" ВГИ - 60,0 - 80,0
Сыворотка крови КРС - 15,0 - 25,0
ДМСО - 5,0-15,0
Пример 2
Проведены испытания предлагаемой вирусвакцины против БМ, содержащей, мас.%:
Суспензия клеток ФЭК, инфицированных штаммом "ВНИИЗЖ/N110" ВГИ - 70,0
Сыворотка крови КРС - 20,0
ДМСО - 10,0
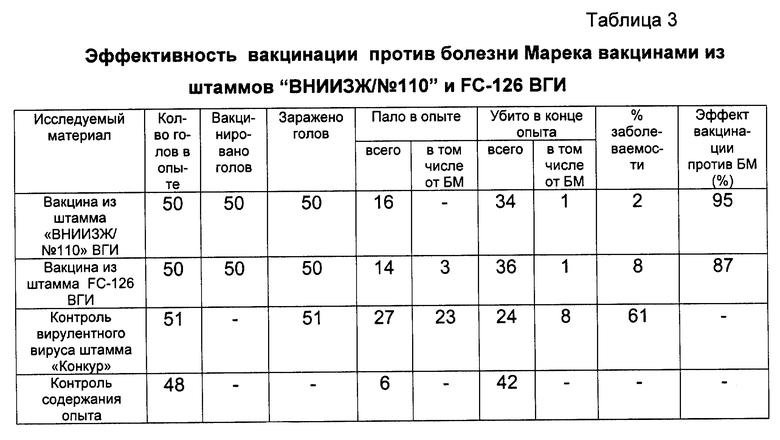
Сравнительная оценка эффективности вирусвакцины из штамма "ВНИИЗЖ/N110" и вирусвакцины из штамма FC-126 проведена на суточных цыплятах. Для этого было сформировано 4 группы цыплят. Цыплят 1 группы в количестве 50 голов вакцинировали вакциной из штамма "ВНИИЗЖ/N110" в дозе 1000 ФОЕ/0,2 см3. Цыплят 2 группы в количестве 50 голов вакцинировали вакциной из штамма-прототипа FC-126 в дозе 1000 ФОЕ/0,2 см3. Цыплят в 3 группе в количестве 51 головы заражали вирулентным штаммом "Конкур". Цыплят 4 группы в количестве 48 голов использовали в качестве контроля содержания опыта. Через 14 дней цыплят в 1 и 2 группах заражали вирулентным штаммом "Конкур". Результаты опыта приведены в таблице 3.
Приведенные в таблице 3 данные свидетельствуют о возможности изготовления вакцины против БМ из штамма "ВНИИЗЖ/N110" для специфической профилактики БМ.
Таким образом, приведенная выше информация свидетельствует о выполнении при использовании предлагаемых изобретений следующей совокупности условий:
- вирусвакцина против БМ и способ ее изготовления, воплощающие предлагаемые изобретения, предназначены для использования в сельском хозяйстве, а именно, в ветеринарной вирусологии и биотехнологии;
- для группы предлагаемых изобретений в том виде, как они охарактеризованы в независимых пунктах формулы изобретения, подтверждена возможность их осуществления с помощью описанных в заявке или известных до даты приоритета средств и методов;
- при использовании предлагаемых вирусвакцины против БМ на основе штамма "ВНИИЗЖ/N110" и способа ее изготовления достигается технический результат, предусмотренный задачей создания изобретения.
Следовательно, предлагаемая группа изобретений соответствует условию патентоспособности "промышленная применимость".
Литература:
1. Ветеринарные препараты. Справочник. Сост. Осидзе Д.Ф.-М.- Колос.- 1981. - С. 140-144.
2. Сюрин В.Н. и др. Вирусные болезни животных / М. - ВНИТИБП. - 1988. - С. 689-721.
3. Пат. России N 2059404, А 61 К 39/255, 10.05.96 г.
4. Временная инструкция по изготовлению и контролю клеточной культуральной вирусвакцины против БМ из штамма FC-126 ВГИ. Утверждена ГУВ МСХ СССР 04.06.84 г. (прототип).
5. Коровин P. Н., Зеленский В.М. Опухолевые болезни птиц/ М. - Колос.- 1984. - 223 с.
6. Пат. ЕПВ N 0496135, А 61 К 39/255, 27.07.94 г.
7. Пат. ЕПВ N 0703294; А 61 К 39/255; C 12 N 7/00, 27.03.96 г.
| название | год | авторы | номер документа |
|---|---|---|---|
| БИВАЛЕНТНАЯ ВАКЦИНА ПРОТИВ БОЛЕЗНИ МАРЕКА И СПОСОБ ЕЕ ИЗГОТОВЛЕНИЯ | 1999 |
|
RU2144377C1 |
| СУХАЯ ВИРУСВАКЦИНА ПРОТИВ БОЛЕЗНИ МАРЕКА И СПОСОБ ЕЕ ИЗГОТОВЛЕНИЯ | 1999 |
|
RU2144376C1 |
| ВИРУСВАКЦИНА ПРОТИВ БОЛЕЗНИ МАРЕКА | 2001 |
|
RU2205660C2 |
| ШТАММ № 3004/№ 109 ВИРУСА БОЛЕЗНИ МАРЕКА ДЛЯ ИЗГОТОВЛЕНИЯ ВАКЦИННЫХ ПРЕПАРАТОВ | 2001 |
|
RU2199583C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ВИРУСВАКЦИНЫ ПРОТИВ БОЛЕЗНИ МАРЕКА | 2001 |
|
RU2209635C2 |
| ШТАММ "ВНИИЗЖ/№ 110" ВИРУСА ГЕРПЕСА ИНДЕЕК ДЛЯ ИЗГОТОВЛЕНИЯ ВАКЦИНЫ ПРОТИВ БОЛЕЗНИ МАРЕКА | 1999 |
|
RU2144562C1 |
| ВИРУСВАКЦИНА ПРОТИВ БОЛЕЗНИ МАРЕКА | 2009 |
|
RU2410117C1 |
| ПРОИЗВОДСТВЕННЫЙ ШТАММ "ВЛАДИМИР" ВИРУСА ГЕРПЕСА ИНДЕЕК ДЛЯ ИЗГОТОВЛЕНИЯ ВИРУСВАКЦИНЫ ПРОТИВ БОЛЕЗНИ МАРЕКА | 2007 |
|
RU2336303C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИВАЛЕНТНОЙ ВАКЦИНЫ ПРОТИВ БОЛЕЗНИ МАРЕКА | 2000 |
|
RU2203681C2 |
| СПОСОБ ИЗГОТОВЛЕНИЯ СУХОЙ ПОЛИВАЛЕНТНОЙ ВИРУСВАКЦИНЫ ДЛЯ ПРОФИЛАКТИКИ БОЛЕЗНИ МАРЕКА И СУХАЯ ПОЛИВАЛЕНТНАЯ ВИРУСВАКЦИНА ДЛЯ ПРОФИЛАКТИКИ БОЛЕЗНИ МАРЕКА | 2005 |
|
RU2327488C2 |

Изобретение предназначено для профилактики болезни Марека (БМ). Вирусвакцина содержит суспензию клеток фибробластов СПФ-эмбрионов кур, инфицированную штаммом "ВНИИЗЖ/ 110-ДЕП" (коллекция ВГНКИ) вируса герпеса индеек (ВГИ), сыворотку крови КРС и диметилсульфоксид (ДМСО). Компоненты берут в соотношении, мас. %: суспензия инфицированных клеток 60,0-80,0; сыворотка крови КРС 15,0-25,0; ДМСО 5,0-15,0. Штамм "ВНИИЗЖ/ 110" ВГИ используют с биологической активностью не ниже 1•105 ФОЕ/см3. Изобретение повышает иммуногенную активность вакцины. 2 с. и 7 з.п. ф-лы, 3 табл., 1 ил.
Суспензия клеток, инфицированных штаммом ВГНКИ "ВНИИЗЖ/ 110-ДЕП" - 60 - 80
Сыворотка крови крупного рогатого скота - 15 - 25
Диметилсульфоксид - 5 - 15
5. Способ изготовления вирусвакцины против болезни Марека, включающий инфицирование культур штаммом вируса герпеса индеек 3 серотипа, инкубирование зараженной культуры, сбор вируссодержащей суспензии клеток, добавление криопротектора и получение целевого продукта, отличающийся тем, что из штаммов 3 серотипа используют штамм вируса герпеса индеек, сем.Herpesviridae, род Herpesvirus ВГНКИ "ВНИИЗЖ/ 110-ДЕП" в эффективном количестве.
| Разбавитель для сухой вирусвакцины против болезней марека | 1974 |
|
SU563175A1 |
| RU 96111000 A, 10.10.98 | |||
| RU 2059404 C, 10.05.96 | |||
| ШТАММ ВИРУСА ГЕРПЕСА КУР КАК КОМПОНЕНТ ДЛЯ ИЗГОТОВЛЕНИЯ БИВАЛЕНТНОЙ ВАКЦИНЫ ПРОТИВ БОЛЕЗНИ МАРЕКА | 1995 |
|
RU2085582C1 |
| ШТАММ ВИРУСА ГЕРПЕСА КУР КАК КОМПОНЕНТ ДЛЯ ИЗГОТОВЛЕНИЯ БИВАЛЕНТНОЙ ВАКЦИНЫ ПРОТИВ БОЛЕЗНИ МАРЕКА | 1995 |
|
RU2085583C1 |
| US 5565202 A, 15.10.96 | |||
| US 5686287 A, 11.10.97 | |||
| GB 1452344 A, 13.10.76 | |||
| СПОСОБ ВИБРАЦИОННОЙ ОБРАБОТКИ И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 1991 |
|
RU2023537C1 |
| ВЫСАЖИВАЮЩИЙ КОНУС К ВЫСАДКОПОСАДОЧНОМУАППАРАТУ | 0 |
|
SU244760A1 |
| Состав сварочной проволоки | 1974 |
|
SU496135A1 |
| Электролит для электрохимической обработки титановых сплавов | 1978 |
|
SU703294A1 |
| Домовый номерной фонарь, служащий одновременно для указания названия улицы и номера дома и для освещения прилежащего участка улицы | 1917 |
|
SU93A1 |
Авторы
Даты
2000-01-20—Публикация
1999-06-28—Подача