Изобретение относится к биотехнологии и микробиологии и представляет собой способ получения биомасс рекомбинантных штаммов E.coli, содержащих плазмидные ДНК, кодирующие биосинтез цитокинов со свойствами факторов некроза опухолей α и β (ФНО-альфа и ФНО-бета), гранулоцитарного колониестимулирующего фактора (Г-КСФ) и гранулоцит-макрофаг колониестимулирующего фактора (ГМ-КСФ) человека и несущие в качестве селективного маркера ген bla (устойчивость к ампициллину). Полученные биомассы могут быть использованы для выделения и очистки из них рекомбинантных цитокинов: ФHO-α, ФHO-β, Г-КСФ и ГМ-КСФ, с целью их детального исследования и применения в медицинской практике.
Цитокины - это белки, вырабатываемые преимущественно активированными клетками иммунной системы и являющиеся медиаторами межклеточных взаимодействий при иммунном ответе, гемопоэзе, воспалении, а также межсистемных взаимодействиях. Традиционно цитокины разделяют на несколько групп: интерлейкины, интерфероны, факторы некроза опухолей (ФНО), колониестимулирующие факторы (КСФ) и др. В организме они действуют взаимосвязанно, образуя единую цельную цитокиновую сеть [1,2]. Все это делает перспективным детальное исследование этих белков и применение в медицине [3-7] и, как следствие, актуальна разработка способов их получения.
Известны способы получения цитокинов, основанные на использовании культуральной жидкости продуцирующих их клеточных линий [8-13]. Однако эти способы трудоемки, трудно масштабируемы, не позволяют получать белки в больших количествах; и только техника рекомбинантных ДНК позволила нарабатывать цитокины в количествах, доступных для широкомасштабного исследования и применения в медицинской практике. Способы получения рекомбинантных цитокинов микробиологическим синтезом с использованием рекомбинантных плазмид известны [14-24] и бурно развиваются [25-32].
Одной из первых основополагающих стадий технологии получения белков является стадия получения биомассы клеток рекомбинантного штамма-продуцента. Обычно, компетентные клетки штамма-реципиента (чаще всего клетки Escherichia coli) трансформируют плазмидой, несущей ген целевого белка и селективный генетический маркер (обычно ген устойчивости к антибиотику). Трансформанты выращивают на среде с антибиотиком и далее размножают трансформированные клетки в ферментере с целью получения биомассы. При этом часто при выращивании клеток необходимо проводить индукцию промотора для экспрессии гена целевого белка с помощью специальных индукторов или повышением температуры [15,19-22] , что приводит к усложнению и удорожанию технологии производства. Наиболее технологично, когда целевой белок экспрессируется в ходе выращивания клеток постоянно, без индукции [16,17, 24-32]. Тем не менее практика показывает, что процесс получения качественной биомассы рекомбинантных штаммов-продуцентов крайне нестабилен, содержание целевых белков в ней невелико (от 3% до 10% от суммы клеточных белков), а также сильно варьирует от опыта к опыту [10,22,24,30,32] . Основной причиной нестабильности биомассы по продуктивности является сегрегация плазмид и селективное преимущество в скорости размножения клеток, не содержащих плазмиду [33-37]. Для повышения качества биомассы рекомбинантных штаммов авторы работ [33-36] рекомендуют тестировать отдельные клоны трансформантов на содержание целевого белка и использовать для получения инокулята наиболее продуктивные из них, в качестве посевного материала использовать культуру в первой трети - середине логарифмической фазы роста, усилить селективное давление на клетки в ходе ферментации путем повышения в среде концентрации антибиотика, подбором в ходе роста культуры оптимальной температуры для синтеза нужного метаболита. Первые две рекомендации авторов являются бесспорными и применимы для всех исследованных рекомбинантных штаммов E.coli, продуцирующих ФHO-α, ФHO-β, α2- интерферон. Однако увеличение в среде концентрации антибиотика для усиления селективного давления, используемого успешно в работе [35] для культивирования штамма E. coli SG20050/pIFN16 - продуцента лейкоцитарного интерферона α2, не всегда резонно, т. к. может привести к резкому снижению скорости роста культуры и снижению выхода биомассы [34] . Изменение температуры при выращивании рекомбинантного штамма может привести не только к изменению уровня синтеза целевого белка, но и изменить его конформационное состояние [37,38]. Этот параметр в каждом случае требует специального исследования.
Наиболее близким (прототипом) к заявляемому способу является способ получения биомассы рекомбинантного штамма бактерий E.coli, обогащенной полипептидом со свойствами лимфотоксина человека [39, прототип]. Стабилизация процесса биосинтеза лимфотоксина и повышение его процентного содержания в биомассе в 2,0-2,5 раза достигается путем отбора высокопродуктивных клонов клеток-трансформантов для получения посевного материала, получения посевного материала на плотной среде с добавлением в среду второго антибиотика - хлорамфеникола с целью увеличения амплификации плазмиды и сбором биомассы клеток в конце логарифмической фазы роста культуры. Совокупность указанных приемов позволяет получать биомассу с содержанием целевого белка 10-16% от суммы клеточных белков. К недостаткам способа следует отнести низкую технологичность на стадии получения посевного материала (инокулята), т.к. получение его на твердой питательной среде трудно масштабируется, и узкий специализированный прием увеличения плазмидной ДНК в штамме-продуценте, подходящий только для улучшения рекомбинантных штаммов, содержащих в плазмиде ген устойчивости к хлорамфениколу.
Технической задачей предлагаемого изобретения является стабилизация процессов биосинтеза группы человеческих цитокинов (ФHO-α, ФHO-β, Г-КСФ и ГМ-КСФ) и повышение их процентного содержания в биомассе рекомбинантных штаммов, содержащих в качестве селективного маркера ген β-лактамазы (устойчивость к ампициллину, Apr).
Задача решается путем обработки посевного материала ампициллином в повышенной концентрации (400-500 мкг/мл) с целью разрушения накопившихся бесплазмидных клеток и последующим дробным добавлением антибиотика в процессе ферментации.
Сущность предлагаемого способа получения биомассы рекомбинантных штаммов E.coli заключается в следующем:
Плазмидой, содержащей целевой ген цитокина (pTNF311 Δ либо pLT21, либо pGG8, либо 280GM), трансформируют компетентные клетки Escherichia coli SG20050, трансформанты подращивают на плотной селективной среде (Ap, 50-150 мкг/мл) в течение 16-18 ч при температуре 30-32oC. Колонии трансформантов анализируют на содержание целевого белка. Наиболее продуктивные засевают в жидкую селективную питательную среду (Ap, 50-150 мкг/мл) и выращивают до одной трети - середины логарифмической фазы роста. Затем в культуру добавляют ампициллин до концентрации 400-500 мкг/мл и инкубируют в течение 2-3 ч. Полученной культурой засевают ферментер с селективной питательной средой (Ap, 100 мкг/мл), и клетки выращивают до конца логарифмической фазы роста. При этом в ходе ферментации периодически через 1-2 ч добавляют ампициллин в концентрации 100 мкг/мл среды. В конце логарифмической фазы роста клетки собирают центрифугированием и используют для выделения цитокина сразу или после хранения при температуре -70oC.
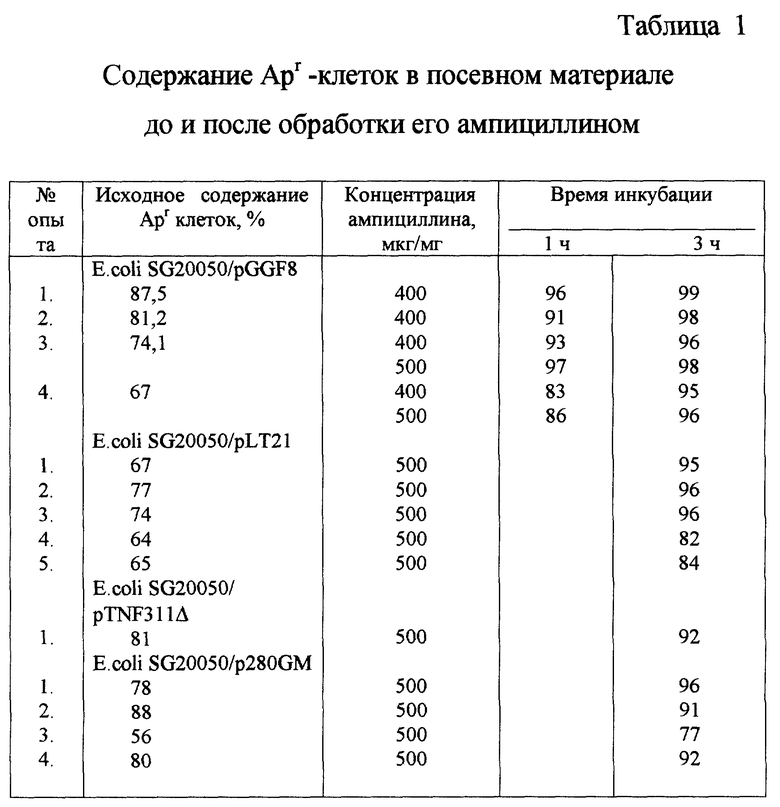
Анализ посевного материала (инокулята) на содержание плазмидсодержащих клеток (Apr) показал, что их количество колеблется от опыта к опыту от 60 до 80% (табл. 1), т.е. около 20- 40% популяции клеток уже на стадии получения посевного материала даже из высокопродуктивных колоний трансформантов могут потерять плазмиду и далее, быстро размножаясь в процессе ферментации, вытеснят плазмидсодержащие клетки, что приведет к низкому качеству биомассы.
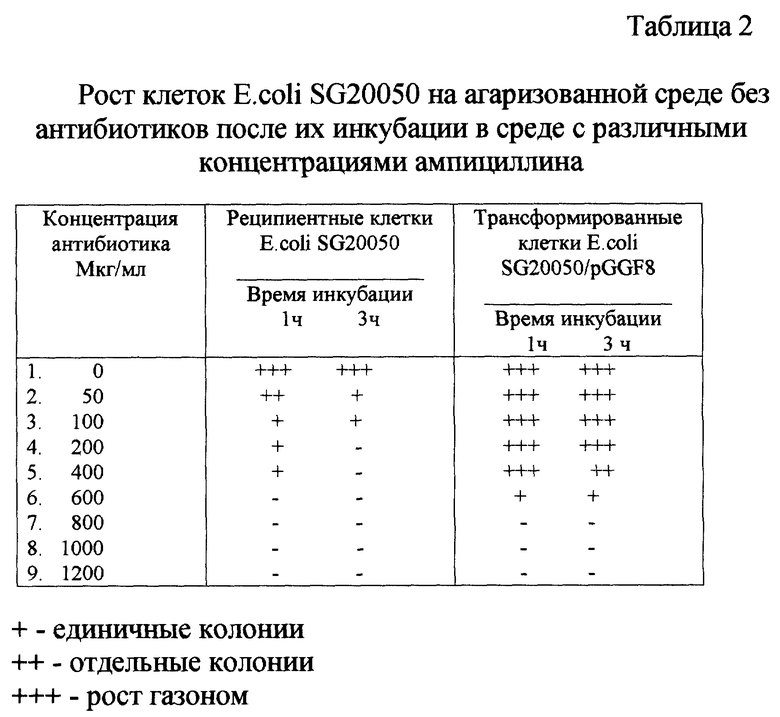
Для удаления бесплазмидных клеток из инокулята используют обработку его ампициллином в повышенной концентрации 400-500 мкг/мл в течение 2-3 ч. При этом показано (табл.2), что после такой обработки бесплазмидные клетки E.coli SG20050 (Aps) практически полностью теряют жизнеспособность. Анализ культуральной жидкости на белок методом электрофореза показывает, что клетки лизируются (белки выходят в культуральную жидкость) (фиг. 1). Способность к росту трансформированных клеток E. coli после такой обработки полностью сохраняется (табл.2).
Анализ популяции клеток посевного материала (инокулята) на содержание плазмидсодержащих клеток после обработки его высокими концентрациями (400-500 мкг/мл) ампициллина показал, что их количество увеличивается и составляет не менее 90% (данные табл. 1).
В связи с тем, что селекция по ампициллин резистентности не является эффективной, поскольку плазмидные клетки синтезируют β- лактамазу, которая, являясь секретируемым белком, разрушает ампициллин в среде, то с целью усиления селективного давления в ходе ферментации и подавления роста Aps клеток, появляющихся в ходе роста культуры в результате сегрегации плазмиды, необходимо периодически добавлять в среду ампициллин. Экспериментально показано, что целесообразно это делать при вступлении культуры в логарифмическую фазу роста, через каждые 1-2 ч.
Новыми по сравнению со способом-прототипом признаками являются: обработка посевного материала рекомбинантных штаммов ампициллином в концентрации 400-500 мкг/мл в течение 2-3 ч для удаления бесплазмидных клеток и дробное добавление в среду ампициллина в концентрации 100 мкг/мл при ферментации культуры в экспериментально подобранное время для снижения сегрегации плазмиды и накопления бесплазмидных клеток.
Совокупность указанных признаков позволяет повысить выход целевых белков в биомассе, стабилизировать процесс их биосинтеза и постоянно получать качественную биомассу рекомбинантных штаммов: E. coli SG200-50/pTNF311 Δ (продуцент ФHO-α), E.coli SG20050/pLT21 (продуцент ФHO-β), E.coli SG20050/pGGF8 (продуцент Г-КСФ) и E.coli SG20050/p280GM (продуцент ГМ-КСФ), содержащую целевые белки в количестве не менее 10% от суммы клеточных белков. Содержание ФHO-α в биомассе в среднем повысилось в 1,5 раза, ФHO-β - в 4 раза, Г-КСФ - в 2-3 раза и ГМ-КСФ - в 8 раз.
Графические материалы:
Фиг. 1. Анализ культуральной жидкости (без клеток) на наличие клеточных белков после инкубации клеток E.coli SG20050 с различными концентрациями ампициллина (мкг/мл): 1-0; 2-50; 3-100; 4-200; 5-400; 6-600; 7-800; 8-1000.
Ниже следуют примеры конкретного получения обогащенных цитокинами (ФHO-α, ФHO-β Г-КСФ и ГМ-КСФ) биомасс рекомбинантных штаммов E.coli SG20050, содержащих плазмиды с генами вышеперечисленных цитокинов и геном β-лактамазы (ген bla) в качестве селективного маркера.
Пример 1. Получение трансформированных клеток, отбор высокопродуктивных клонов и выращивание их в жидкой селективной среде
Трансформацию компетентных клеток E.coli SG20050 плазмидной ДНК pTNF311 Δ [40], или pLT21 [24], или pGGF8 [30], или p280GM [32] проводят кальциевым методом, как описано ранее [41]. Отбор высокопродуктивных клонов проводят, как описано в способе-прототипе [39]. Клоны с наибольшим содержанием целевого белка используют для получения инокулята. Их подращивают в L-бульоне, содержащем 100 мкг/мл ампициллина при 32oC до середины логарифмической фазы роста (Д550 = 0,5-0,6).
Анализ полученных клеток на содержание плазмидсодержащих клеток проводят методом, описанным в [42]. Полученные данные представлены в табл. 1 (графа 2).
Как видно из таблицы, процентное содержание Apr клеток в посевном материале колеблется от 60 до 85%.
Пример 2. Влияние ампициллина на жизнеспособность реципиента E.coli SG20050 и рекомбинантного штамма E.coli SG20050/pGGF8.
Исследован процесс влияния различных концентраций ампициллина на жизнеспособность штамма-реципиента E. coli SG20050 и рекомбинантного штамма-продуцента Г-КСФ, данные представлены в табл.2 и фиг. 1.
Как видно из табл.2, после инкубации реципиента клеток (Aps) в среде с антибиотиком (до 400 мкг/мл) в течение 1 ч, отдельные колонии сохраняют способность к росту при высеве на среду без селективного давления, тогда как после 3-часовой инкубации их роста не наблюдается. В то же время после инкубации трансформированных клеток (Apr) в тех же условиях их способность к росту практически не изменяется.
Из фиг. 1 видно, что при обработке реципиентных клеток антибиотиком в культуральной жидкости начинают обнаруживаться в значительных количествах клеточные белки E. coli при концентрациях ампициллина выше 400 мкг/мл, что указывает на лизис клеток. Полученные данные свидетельствуют о том, что до этих концентраций антибиотика происходит подавление роста бесплазмидных клеток, но они могут сохраняться в нативном состоянии, и при инактивации ампициллина β-лактамазой способны к интенсивному росту. После обработки клеточной популяции ампициллином в концентрации 400-500 мкг/мл в течение 2-3 ч можно ожидать гибель бесплазмидных клеток.
Пример 3. Получение посевного материала с повышенным содержанием Apr клеток.
Отобранный высокопродуктивный клон, выращенный на чашке отдельно растущими колониями, смывают в жидкую среду в качалочные колбы с объемом L-бульона 200 мл и дозой ампициллина 100 мкг/мл. Подращивают культуру при температуре 32oC и скорости вращения качалки 150-160 об/мин до первой трети - середины логарифмической фазы роста (Д550=0,5-0,6). Далее проводят инкубацию с ампициллином в концентрации 400-500 мкг/мл в течение 2-3 ч.
В табл. 1 (графа 4) представлены результаты анализа полученной популяции клеток. Как видно из табл. 1, обработка инокулята антибиотиком в концентрации 400-500 мкг/мл в течение 3 ч способствует повышению уровня Apr клеток, и их содержание достигает 90%.
Пример 4. Ферментация без дробного добавления ампициллина.
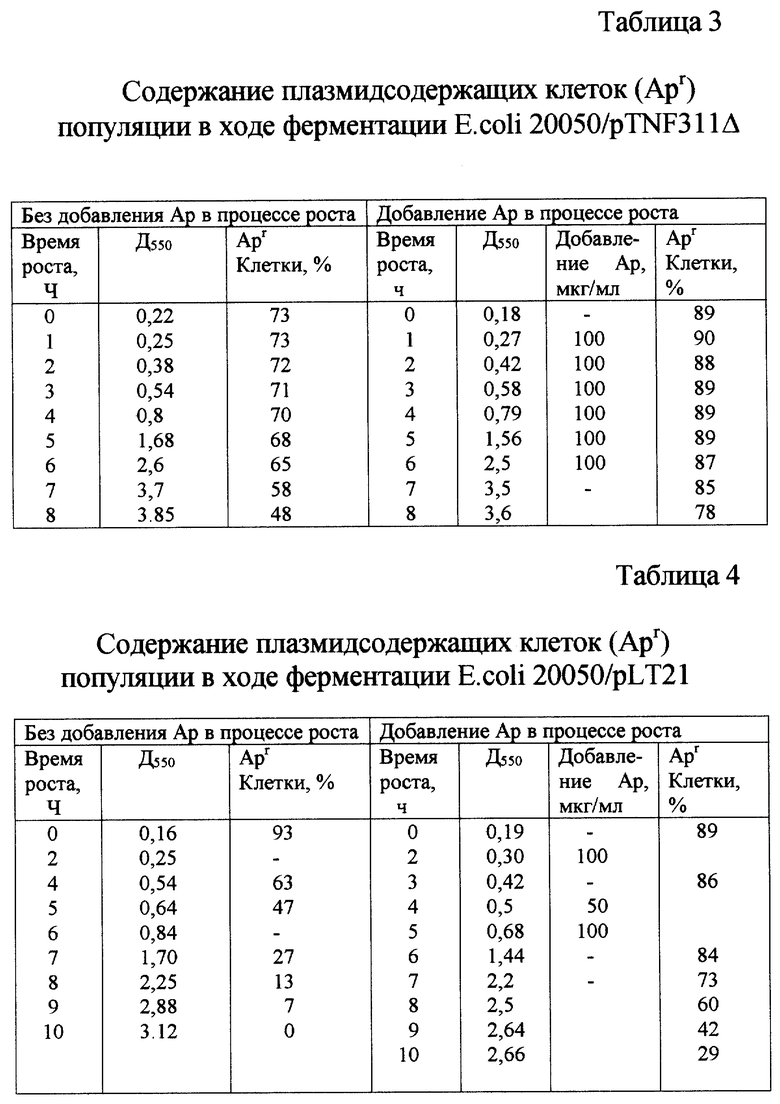
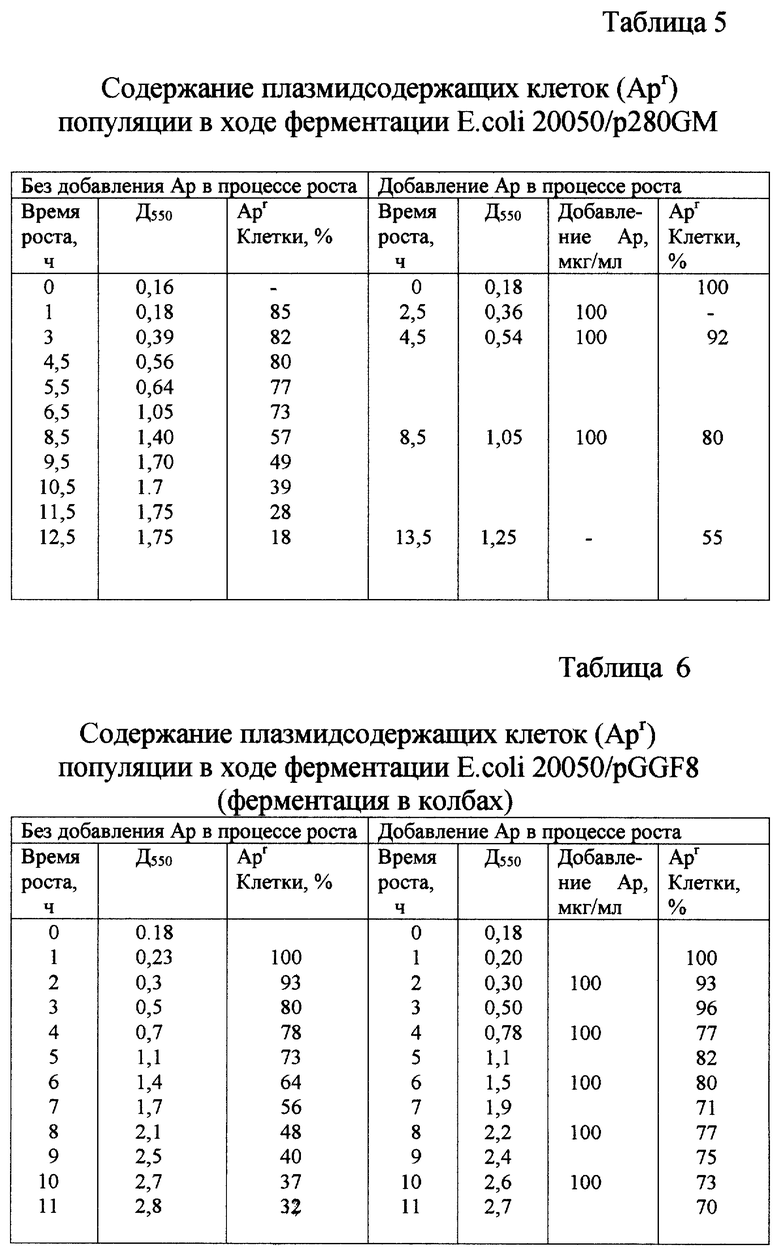
Ферментацию проводят в качалочных колбах с объемом среды 250 мл или в ферментере "Ультраферм" с рабочим объемом 4 л при температуре 31-32oC. Питательная среда - L-бульон, содержащий Ap в концентрации 100 мкг/мл. Скорость вращения качалки 150-160 об/мин. Скорость вращения мешалки в ферментере от 100 до 200 об/мин, подача воздуха 0,5-1,0 л/мин на 1 л среды. Для засева используют посевной материал, полученный, как описано в примере 3. Объем посевного материала 1% (об/об) от объема среды для ферментации. Время ферментации 9-10 ч. Заканчивают ферментацию в конце логарифмической фазы роста. Культуральную жидкость охлаждают до 5-10oC, клетки собирают центрифугированием и хранят при температуре минус 70oC. Данные по содержанию плазмидсодержащих клеток в ходе ферментации представлены в табл. 3-6 (графы 1-3).
Содержание целевого белка в биомассах колеблется от опыта к опыту и составляет от суммы клеточных белков в %: ФHO-α - 10-15%, ФHO-β - 1-3%, Г-КСФ - 1,0-4,0%, ГМ-КСФ - 1-4%.
Пример 5. Ферментация с дробным добавлением ампициллина.
Ферментацию проводят, как описано в примере 4, за исключением того, что в процессе ферментации через каждые 1-2 ч роста добавляют в среду ампициллин до концентрации 100 мкг/мл. Данные по содержанию плазмидсодержащих клеток в процессе ферментации представлены в табл. 3-6 (графы 4-7). Целевые белки в биомассах всегда присутствуют в количестве не ниже 10% от суммы клеточных белков: ФHO-α - 15 -25%, ФHO-β - 10-16%, Г-КСФ - 10-12%, ГМ-КСФ - 10%.
Таким образом, предлагаемый способ получения биомасс рекомбинантных штаммов E.coli SG20050, содержащих ген bla в качестве селективного маркера, позволяет стабилизировать процесс биосинтеза 4-х целевых белков-цитокинов, исключить "холостые" производственные ферментации и повысить их содержание в биомассе: ФHO-α в 1,5 раза, Г-КСФ и ГМ-КСФ в 2-3 раза. Содержание ФHO-β в биомассе не ниже, чем в способе-прототипе, но процесс получения инокулята универсален и легко масштабируется.
ЛИТЕРАТУРА
1. Кетлинский С.А., Симбирцев А. С., Воробьев А.А. // Эндогенные иммуно-модуляторы.- СПб: Гиппократ.- 1992.- С.256.
2. ЯрилинА.А.//Иммунология.- 1997.-N 5.-С.7-14.
3. Варпаховская И. //Remedium. 1998.- N 2.- Р.45-49.
4. Моисеенко В.М. //Вопросы онкологии.- 1998.- Т.44.- N1.-С. 120-125.
5. Нейпоген. Информационные материалы фирмы Ф.Хоффманн-Ля Рощ АГ, Базель, Швейцария.- 1993.
6. Смирнова Н.Б. // Клиническая фармакология и терапия.- 1995.-N 4.-С. 49-51.
7. Лейкомакс. Информационные материалы фирмы "Sandoz".- Базель.- Швейцария.- 1993-1994.
8. Патент США N 48333127, кл. A 61 K 37/02, 1989.
9. Nomura Н., Imazeki I., Oheda M., Kubota N et al.// EMBO J.-1986.- N 5.-P.871-876.
10. Европ. патент N 215126, кл. C 12 N 15/00. - 1987.
11. Патент США N 4604284, кл. A 61 K 37/02; C 07 K 13/00; C 12 P 21/00, опубл. 05.08.1986.
12. Aggarwal B.B., Moffat В. and Harkins R.N. //J. Biol. Chem.- 1984.- V.259.- N 1.- P.686-691.
13. Lee F., Yokota Т., Otsuka T. et al. // Proc. Natl. Acad. Sci. USA.- 1985.- V.82.- P.4360-4364.
14. Заявка WO 86/03751, кл. A 61 K 37/02, 45/02, опубл. 03.10.1986.
15. А.С. СССР 1614765, кл. C 12 N 15/28, опубл. 15.12.1990.
16. Shirai Т. , Yamaguch H., ltoH. et al. //Nature, 1985.- V.313.- P. 803-806.
17. Тихонов Р. В., Якимов С.А., Коробко В.Г., Вульфсон А.Н. // Биоорг. Химия.- 1996.- Т.22.- N3.- C.163- 167.
18. Патент США 4617378, кл. C 07 K 15/26, опубл. 14.10.1986.
19. Heng-Fong Seow, Cynthia R.Coh, Kristman L., Porter A. // Biotechnology.-1989.- V.7.-N 4.- P.363-368.
20. Schoenfeld H. J. , Poesche D., Frey J.R. et al. // J. Biol. Chem.- 1991.- V.266.-N 6.- P.3863-3869.
21. Европ. патент N215126, кл. C 12 N 15/00, 1987.
22. Патент США N 4810643, кл. C 12 N 15/00, 1989.
23. Европ. патент N 0299782, кл. C 07 K 13/00, опубл. 18.01.1989. Б. 89/03.
24. Патент РФ N2048521, кл. C 12 P 21/00, 1992.
25. Патент РФ 2101292, кл. C 07 K 1/36, C 12 P 21/00, опубл. 10.01.1989, Б N1.
26. Патент РФ 2102988, кл. A 61 K 35/00, 35/26, 35/76, 39/00, опубл. 27.01.1998, Б N3.
27. Патент РФ N2082430, кл. A 61 K 38/21, опубл. БМ N 8, 1997.
28. Заявка на патент РФ N 97110634 от 20.06.97.
29. Заявка на патент РФ N97105785 от 10.04.1997.
30. Заявка на патент РФ N96113021. От 21.06. 1996. Положительное решение от 26.09.1997.
31. Заявка на патент РФ N 97106895 от 23.04.1997.
32. Патент РФ N2091488, кл. C 12 N 1/21, опубл. БИ N27, 1997.
33. Лебедев Л.Р., Зернов Ю.П., Пустошилова Н.М. и др. // Биотехнология.- 1995.- N 12.- С. 19-24.
34. Андреева И. С., Лебедев Л.Р., Пустошилова Н.М. // Биотехнология.-1996.- N1.- С.9-12.
35. Андреева И.С., Закабунин А.И., Пучкова Л.И. и др. // Биотехнология.- 1996.- N10.- С.18-23.
36. Лебедев Л. Р. , Пустошилова Н.М., Синичкина С.А., Андрева И.С. // Прикладная биохимия и микробиология.- 1998.- Т.34.- N1.- С.120-126.
37. Шмелев В.А., Бунина З.Ф., Кудрявцева Т.Ю. и др. // Мол. генет. микробиол. и вирусол.- 1995.- N1.- С.9-14.
38. A.C. 1712416, кл. C 12 N 15/00.
39. Способ получения биомассы рекомбинантного штамма бактерий E.coli, обогащенной полипептидом со свойствами лимфотоксина человека.//Заявка N 97103807, положительное решение от 23.04.1998.
40. Патент РФ N 1445193, кл. 6 C 12 N 15/28. Опубл. 20.03.96, Б. N8.
41. Маниатис Т., Фрич Э., Сэмбрук Дж. // Молекулярное клонирование.- М.: Мир.- 1984. С.
42. Луста К.А., Фихте Б.А. // Методы определения жизнеспособности микроорганизмов.- Пущино.: ОНТИ НЦБИ СССР. 1990.- С. 186.
Изобретение предназначено для биосинтеза цитокинов человека (факторов некроза опухолей альфа и бета, гранулоцит и гранулоцит-макрофаг колониестимулирующих факторов) рекомбинантными штаммами Е. соli SG20050/pTNF322Δ, Е. coli SG20050pLT21, E. coli SG20050/pGGF8 и E.coli SG20050/p280GM. Для получения посевного материала с высоким содержанием плазмидсодержащих клеток инокулят обрабатывают ампициллином в концентрации 400 - 500 мкг/мл в течение 2-3 ч. В процессе ферментации в среду добавляют ампициллин до концентрации 100 мкг/мл. Ампициллин добавляют через каждые 1-2 ч роста культуры. Изобретение понижает сегрегационную нестабильность рекомбинантных штаммов и повышает содержание целевых белков в биомассах. 5 з.п.ф-лы, 1 ил., 6 табл.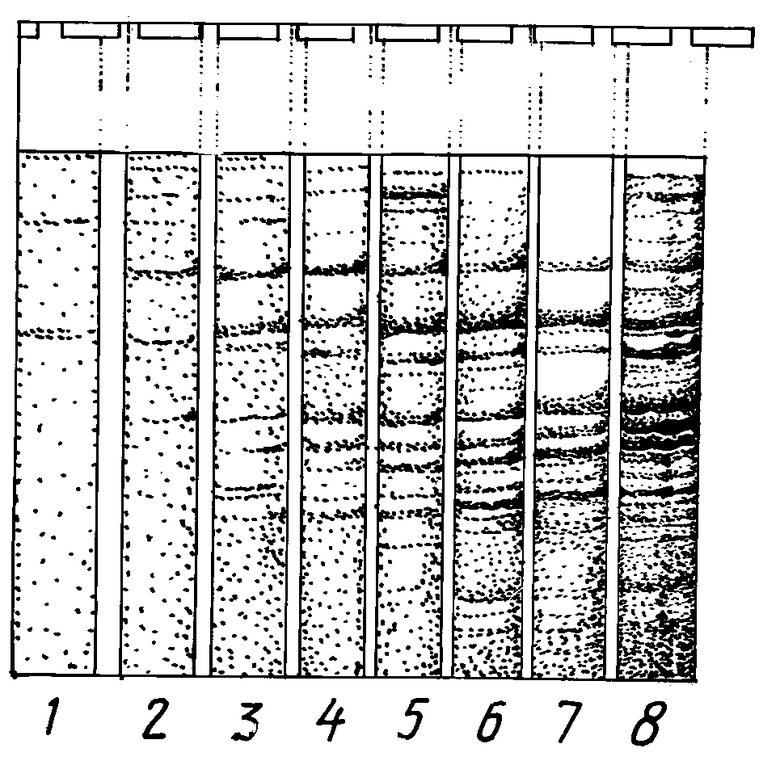
Авторы
Даты
2000-10-27—Публикация
1998-10-19—Подача