Изобретение относится к способам окислительной очистки нефти и газоконденсата от сероводорода и меркаптанов и может быть использовано в газонефтедобывающей и нефтеперерабатывающей промышленности для дезодарации нефти и газоконденсата.
Для очистки нефтепродуктов от меркаптанов широко применяют способы, основанные на переводе меркаптанов водными растворами щелочей в меркаптиды с последующим окислением меркаптидов кислородом воздуха в дисульфиды в присутствии катализаторов (см. Сигеру Оаэ. Химия органических соединений серы. -М. , Химия. 1975. -с. 98-101). Недостатком этих способов является сложность их реализации, требующих создания специальных многостадийных промышленных установок (заводов).
Известны способы демеркаптанизации нефтепродуктов путем обработки их растворами гипохлорита натрия, перекисью водорода, органическими перекисями, надкислотами и диметилсульфоксидом (см. Сигэру Оаэ. Химия органических соединений серы. -М., Химия. - 512 с; c. 101-103).
Известны также способы очистки нефти и газоконденсата от сероводорода и меркаптанов с использованием водно-спиртовых растворов щелочей, содержащих органические кислородсодержащие реагенты (кетоны, альдегиды) (см. а.с. N 1567598, 1579927, 1583435. Кл. С 10 19/04, 1990 г.). Недостатком этих способов является низкая эффективность очистки и большой расход реагентов.
Описан опыт обессеривания керосинового дистиллата обработкой равным объемом разбавленной (32 мас.%) азотной кислотой при комнатной температуре и энергичном перемешивании в течение 3 часов. При этом общее содержание серы снижается с 2,18 до 0,24%. После обработки азотной кислотой масляный слой отделяют от кислотной, промывают водой и щелочью. (см. Наметкин С.С., Сборник трудов, т.III. изд-е АНСССР. -М.: 1955. С.622-626).
Недостатком описанного способа является большой расход азотной кислоты, многостадийность процесса и необходимость обезвреживания отработанной кислоты и промывных вод.
По технической сущности и достигаемому результату наиболее близким к предлагаемому изобретению является способ очистки нефти и газоконденсата от сероводорода, описанный в заявке на изобретение N 98104888/04 от 16.03.98. кл. С 10 G 27/00.
По этому изобретению для очистки от сероводорода нефть и газоконденсат обрабатывают 20-50%-ным водным раствором пероксида водорода в присутствии азотсодержащего основания и/или щелочного реагента. Используют аммиак или органический амин, карбонаты или гидроксиды натрия и калия в количестве 0,5-5 молей на 1 моль сероводорода. В качестве органического амина применяют этаноламины, алкиламины C1-C4, этилендиамин, полиэтиленполиамин, циклогексиламин, изопропаноламины и их смеси. Водный раствор пероксида водорода берут из расчета 1-5 молей H2O2 на 1 моль H2S.
В патенте N 2121491, 6 C 10 G 27/04, 29/02 от 02.12.96 окисление сероводорода и меркаптанов в нефти и газоконденсате пероксидом водорода в присутствии органического амина проводят при 15-65oC и давлении 0,14-2,1 МПа и сырье дополнительно обрабатывают элементной серой, взятой в количестве 0,15-0,5 молей на 1 моль меркаптановой серы.
Недостатком описанных способов является низкая эффективность их при очистке сырья от меркаптанов и большой расход реагентов (пероксида водорода и оснований).
Задачей настоящего изобретения является повышение степени очистки сырья и снижение расхода реагентов.
Согласно изобретению решение поставленной задачи достигается путем обработки исходного сырья 10-50%-ным водным раствором пероксида водорода, взятого в количестве 0,5-3,0 моля H2O2 на 1 моль сероводородной и меркаптановой серы, в присутствии азотсодержащего основания и/или щелочного реагента, взятых в количестве 0,2-3,0 моля на 1 моль сероводородной и меркаптановой серы, и катализаторов при температуре 0-70oC и давлении до 1,0 МПа. Катализаторы берут из расчета 0,1-50 граммов на 1 т сырья. Катализаторы предварительно смешивают с водным раствором щелочного реагента или азотсодержащего основания. В качестве катализаторов применяют соединения металлов VI, VII и VIII группы периодической системы элементов: гидроксиды и соли Fe, Ni, Со, Cd, Mo, Cr, Mn. Из металлоорганических соединений используют дисульфо-, тетрасульфо-, диоксидисульфодихлор- и полифталоцианины кобальта. Можно использовать также перманганаты и бихроматы натрия, калия и аммония. Соли вышеперечисленных металлов при действии сильных щелочей образуют гидроксиды.
В качестве щелочного реагента используют, как и в известном способе по заявке N 98104888/04, водные растворы карбонатов и гидроксидов натрия, калия, аммония и органические амины (этаноламины, алкиламины C2-C4, алкилэтаноламины, этилендиамин, полиэтиленполиамин и их смеси).
В нефть и/или газоконденсат сначала вводят щелочные реагенты и/или азотсодержащие основания с растворенными и/или эмульгированными в них катализаторами, перемешивают до получения однородной эмульсии, затем в эмульсию при перемешивании вводят водный раствор пероксида водорода.
Отличительными признаками предложенного способа являются проведение процесса окисления сероводорода и меркаптанов пероксидом водорода в щелочной среде в присутствии катализаторов процесса окисления в вышеуказанном оптимальном количестве.
Указанный отличительный признак предлагаемого технического решения определяет его новизну и изобретательский уровень в сравнении с известным уровнем техники, так как о применении катализаторов (каких катализаторов и в каком количестве) для ускорения реакции H2O2 с H2S и RSH в патентной и научной литературе не описано. Дополнительное введение катализаторов в процессе обработки нефти и газоконденсата пероксидом водорода в присутствии основных (щелочных) реагентов существенно повышает степень очистки сырья от H2S и RSH и позволяет снижать расход реагентов (H2O2 и оснований).
Процесс очистки сырья от H2S и RSH основан на реакциях
H2S + H2O2 ---> S + H2O (1)
2 RSH + H2O2 ---> RSSR + H2O (2)
В присутствии щелочей, например NaOH, образуются Na2S, NaHS и RSNa, которые окисляются легче, чем исходные H2S, RSH.
При низких температурах (0-20oC) реакции типа 1 и 2 идут медленно. С повышением температуры эти реакции ускоряются. Однако с повышением температуры ускоряется также реакция разложения:
2H2O2 ---> 2H2O + O2 (3)
В присутствии щелочных агентов и аминов процесс разложения пероксида водорода также ускоряется. Соответственно, для проведения процесса требуется большой избыток H2O2, т.е. щелочная среда и температура, с одной стороны, действуют положительно (ускоряют реакции 1 и 2), с другой стороны, воздействуют на процесс отрицательно - разлагают окислитель H2O2.
Введение фталоцианиновых катализаторов, во-первых, ускоряет реакции 1 и 2, во-вторых, кислород, выделяющийся при разложении H2O2 в присутствии фталоцианинов кобальта, сам легко окисляет H2S и RSH по реакциям
NaHS + О 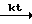 NaOH + S
NaOH + S
2RSNa + О + H2O 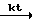 RSSR + 2NaOH
RSSR + 2NaOH
В присутствии фталоцианинов кобальта и при проведении процесса под давлением потери кислорода можно избежать, т.е. в этом случае кислород H2O2 можно использовать полностью на окисление H2S и RSH.
Наряду с реакциями 1-3 имеют место также реакции дальнейшего окисления сероводорода и дисульфидов до тиосульфатов и сульфоксидов, поэтому требуется избыток H2O2 от стехиометрии. Чем больше количество щелочных реагентов, тем в большей степени идут реакции дальнейшего окисления H2S и RSH и тем больше требуется расход H2O2. Максимальный расход H2O2 при необходимости ускоренного проведения процесса окисления составляет 3 моля H2O2 на 1 моль серы H2S и RSH. Минимально необходимый расход H2O2 по реакции 2 равен 0,5 молям H2O2 на 1 моль RSH, поэтому за минимальное количество взято 0,5 молей H2O2 на 1 моль RSH.
При расходе щелочных реагентов ниже 0,2 молей на 1 моль RSH процесс окисления идет очень медленно (более 24 часов), в повышении расхода щелочных реагентов более трех молей на 1 моль серы H2S и RSH нет необходимости.
При расходе фталоцианинового катализатора ниже 0,1 г на 1 т сырья его действие становится незаметным. Повышение расхода катализаторов, содержащих соединения Fe, Cr, Mn, Ni, Mo, более 50 г/т неоправданно с точки зрения экономики и низкой растворимости дешевых соединений типа Fe(ОН)3 в щелочных растворах. При максимальных расходах реагентов процесс очистки сырья от сероводорода можно проводить и при низкой температуре 0-10oC. Более экономично (для экономии реагентов) проведение процесса при 50-70oC.
В случае предварительного смешения катализатора, щелочного агента и раствора H2O2 происходит разложение H2O2 в щелочной среде и необратимое окисление катализатора и случае использования фталоцианинов. Поэтому оптимально двухступенчатое введение реагентов в сырье. Для получения устойчивой эмульсии сначала в сырье вводят щелочной реагент и катализатор, потом раствор Н2O2. Порошкообразный катализатор удобнее вводить в виде раствора или суспензии в щелочном растворе.
Предлагаемый способ очистки нефти и газоконденсата может быть реализован непосредственно на промыслах, внедрение способа не требует больших капиталовложений.
Предлагаемый способ апробирован в лабораторных условиях, ниже приведены примеры и результаты проведенных экспериментов
Пример 1
Круглодонную колбу, вместимостью 100 мл, заполняют инертным газом аргоном. В колбу вводят расчетное количество предварительно приготовленной смеси катализаторов в водном растворе щелочного реагента или азотсодержащего основания (амина). Затем в колбу вводят расчетное количество (30-70 мл) исходного сырья, охлажденного до ± 10oC. Колбу закрывают пробкой и содержимое ее перемешивают встряхиванием в течение 5-10 секунд. После в колбу вводят расчетное количество концентрированного раствора пероксида водорода. Колбу плотно закрывают резиновой пробкой, перемешивают резким встряхиванием, нагревают до заданной температуры и дают выдержку при перемешивании в течение 5-60 мин при заданной температуре в водяной бане. После дают выдержку в течение 1-20 часов без перемешивания при температуре 0-25oC. В течение этого времени из верхней зоны колбы берут несколько раз пробы сырья на анализ. Общее содержание меркаптановой и сероводородной серы определяют потенциометрическим титрованием, содержание индивидуальных меркаптанов определяют хроматографическим методом.
При проведении реакции при 50-70oC процессы окисления заканчиваются в течение 3-5 мин. После этого при выдержке без перемешивания содержание H2S и RSH не изменяются. При 20-30oC снижение содержания H2S и RSH при выдержке наблюдается еще 20-120 мин. При 0-10oC реакция может продолжаться в течение до 20 часов.
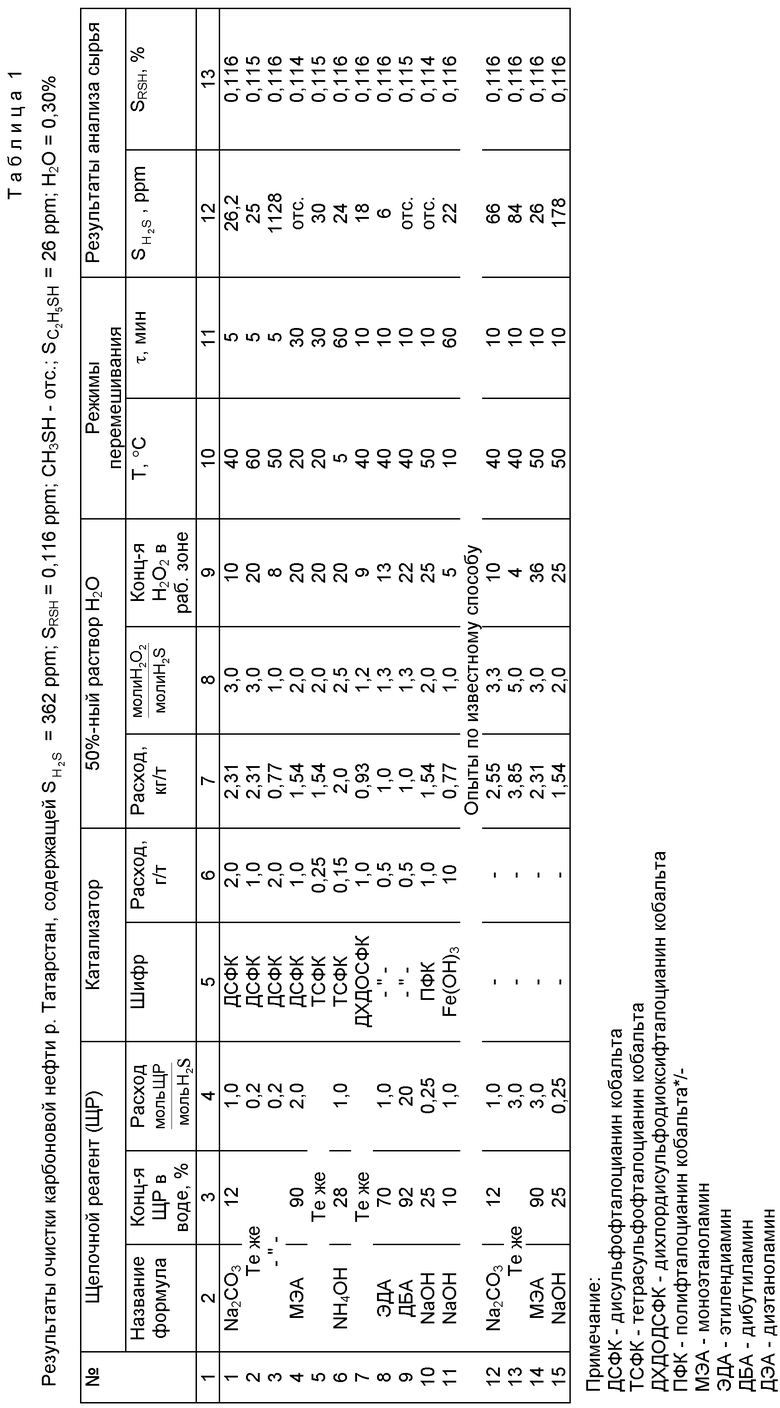
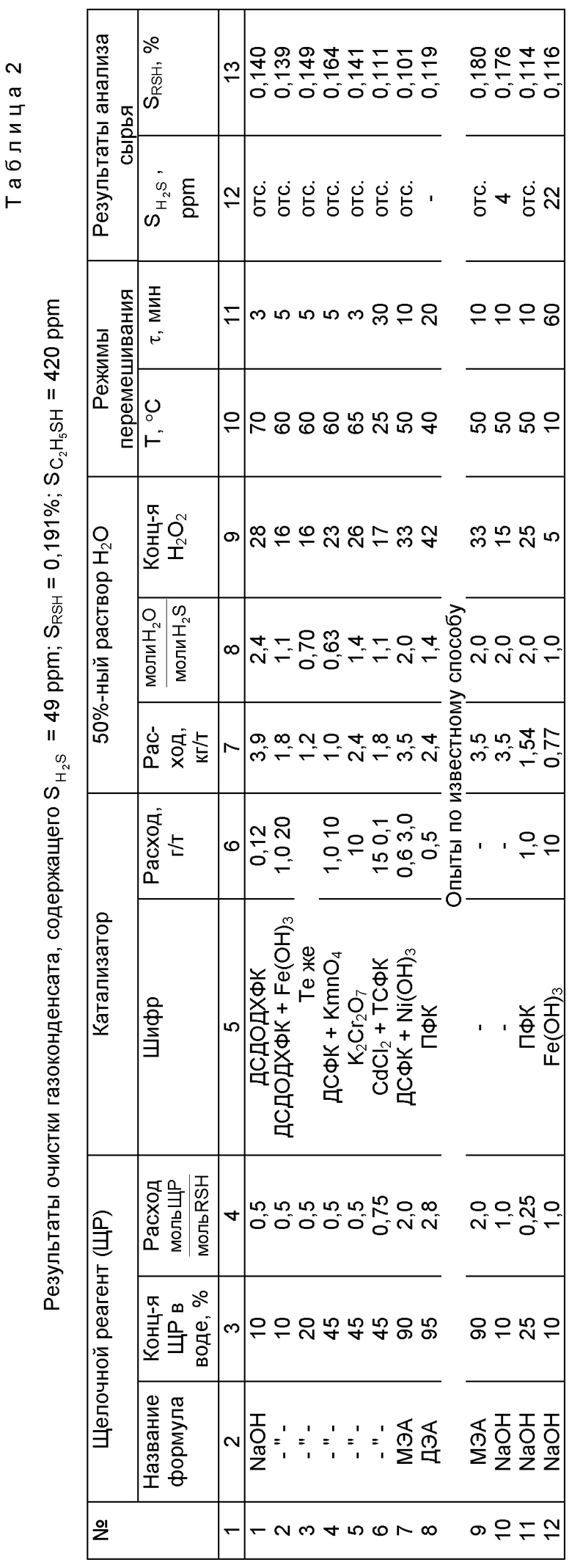
В табл. 1-3 приведены величины содержания сероводородной серы, общей меркаптановой серы и серы меркаптанов C1-C3 после окончания процесса окисления.
Контрольные опыты по известному способу (табл.1 опыты N 12- 15: табл.2 опыты N 9, 10) проводят так же, но без введения катализаторов.
В качестве сырья использовали различные образцы нефтей и газоконденсатов, а также модельные растворы меркаптанов C2-C3 в толуоле и гептане.
Результаты опытов приведены в табл. 1 - 3.
Как следует из табл. 1 и 2, дополнительное введение катализаторов существенно улучшает степень очистки сырья от H2S и RSH (см: табл. 1 опыты N 1 и 12, 4 и 14, 10 и 15, а также табл. 2 опыты N 7 и 9, и 1, 2 и 10). Введение катализаторов дает возможность снизить расход реагентов (см. табл. 1 опыты N 2 и 12, 13; 4 и 14, а также табл. 2 опыты N 2 и 10).
Из исследованных катализаторов наиболее активными являются фталоцианины кобальта. Каталитический эффект фталоцианинов проявляется уже при добавлении 0,1-0,15% (табл. 1 опыт N 6 и табл. 2 опыт N 6). Соли металлов [Cd(Cl)2 в щелочной среде образуют гидроксиды [Cd(OH)2] , а KмnO4 и K2Cr2O7 в присутствии восстановителей типа H2S и RSH быстро переходят в формы Mn+2, Mn+4, Cr+2 и Cr+3, т.е. в реакционной зоне присутствуют также в виде гидроксидов и оксидов. Каталитический эффект их гораздо ниже, чем фталоцианинов. Однако ввиду дешевизны (например, Fe(OH)3) они могут найти практическое применение, но их надо вводить в количестве 10-50 г/т.
Более активный щелочной агент NaOH достаточно вводить 0,2-0,5 молей на моль H2S или RSH. Менее активных щелочных агентов- аминов необходимо вводить 2-3 моля на 1 моль RSH. Поскольку водные растворы NaOH, Na2CO3, КОН, K2CO3 не растворяются в нефтях и слабо эмульгируются в газоконденсатах, применение нефтерастворимых аминов C2-C6 может стать необходимостью при дезодорации некоторых видов газоконденсатов.
Как видно из табл. 3, предлагаемый процесс является селективным по отношению к низкомолекулярным меркаптанам, т.е. этилмеркаптан окисляется гораздо легче, чем изопропилмеркаптан. Такое явление очень полезно для дезодорирующей очистки сырья, так как неприятный (токсичный) запах нефтей в основном определяется содержанием H2S и меркаптанов C1-C2. Опыты табл. 3 также показывают, что в опытах табл. 1 и 2 снижение содержания меркаптановой серы происходит в основном (на ~ 80%) за счет окисления меркаптанов С1-С2.

Изобретение относится к способам окислительной очистки нефти и газоконденсата от сероводорода и меркаптанов и может быть использовано в газонефтедобывающей и нефтеперерабатывающей промышленности. Содержащиеся в нефти и газоконденсате сероводород и низкомолекулярные меркаптаны окисляют 10-50%-ным раствором пероксида водорода до элементной серы, тиосульфатов и дисульфидов в присутствии щелочных агентов и катализаторов при температуре 0-70oС и давлении до 1,0 МПа. Сначала в сырье вводят при перемешивании смесь катализаторов в растворе щелочного агента, потом пероксид водорода. На 1 моль сероводородной и меркаптановой серы берут 0,2-3,0 моля щелочного агента (NaOH, КОН, Nа2СО3, К2СО3, NH4OH) или азотсодержащего органического основания (аминов C2-C6) и 0,5-3,0 моля пероксида водорода. На 1 т сырья берут 0,1-50 г катализаторов - соединений металлов VI-VIII группы периодической системы переменной валентности. Данный способ повышает степень очистки, особенно от низкомолекулярных меркаптанов и снижает расход реагентов. 3 з.п. ф-лы, 3 табл.
| СПОСОБ ОЧИСТКИ НЕФТИ И/ИЛИ ГАЗОКОНДЕНСАТА ОТ СЕРОВОДОРОДА | 1998 |
|
RU2146693C1 |
| СПОСОБ ОЧИСТКИ НЕФТИ, ГАЗОКОНДЕНСАТА ОТ СЕРОВОДОРОДА И МЕРКАПТАНОВ | 1996 |
|
RU2121491C1 |
| СПОСОБ ДЕЗОДОРИРУЮЩЕЙ ОЧИСТКИ НЕФТИ И ГАЗОКОНДЕНСАТА ОТ СЕРОВОДОРОДА И НИЗКОМОЛЕКУЛЯРНЫХ МЕРКАПТАНОВ И УСТАНОВКА ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 1997 |
|
RU2120464C1 |
| DE 3151133 А1, 30.06.1983. | |||
Авторы
Даты
2001-12-27—Публикация
2000-09-19—Подача