Изобретение относится к способу получения лекарственного препарата индапамида, обладающего гипотензивным и диуретическим действием, применяемого при артериальной гипертензии и хронической сердечной недостаточности:
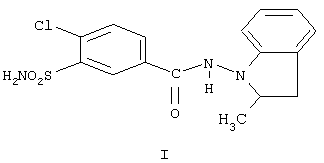
Известен способ получения 1-(3-сульфамоил-4-хлорбензоил)амино-2-метилиндолина (I) реакцией ацилирования гидрохлорида 1-амино-2-метил-индолина (II) 4-хлор-3-сульфамоилбензоилхлоридом (IV) в тетрагидрофуране (ТГФ) в присутствии триэтиламина (ТЭА) (ЕР №0462017 кл. С 07 D 209/08, 1991).
В этом способе триэтиламин вносят сразу 2.11 моля на 1 моль гидрохлорида 1-амино-2-метилиндолина (II). При этом 1 моль триэтиламина расходуется на перевод гидрохлорида амина (II) в основание (III). Оставшийся 1.11 моль триэтиламина способствует реакции ацилирования амина (III) 4-хлор-3-сульфамоилбензоилхлоридом (IV):
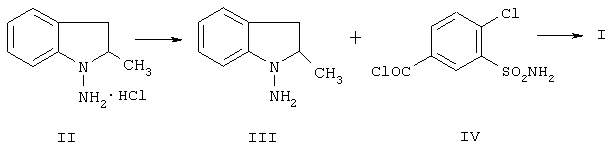
Введение бензоилхлорида (IV) в сильнощелочную среду, создаваемую 1.11 моля триэтиламина, приводит к частичному гидролизу такого непростого бензоилхлорида, каким является бензоилхлорид (IV), и, следовательно, приводит к недостаче его как реагента. К тому же ведение реакции в тетрагидрофуране, который, как известно, очень легко образует гидроперекиси, делает процесс далеко не безопасным. Присутствие в ТГФ даже следов гидроперекисей недопустимо, т.к. последние инициируют процесс окисления и без того легко окисляющегося амина (III), до образования интенсивно синего соединения. Образующийся в таких условиях индапамид может при многократной очистке сохранять голубоватый оттенок. Выход - 80.5%.
Задачей изобретения является упрощение процесса получения, а также увеличения выхода индапамида.
Эта задача решается заменой легковоспламеняющегося и взрывоопасного ТГФ на диоксан, а также первоначальным введением в реакцию 1 моля ТЭА на 1 моль гидрохлорида амина (II) при 18-20°С для перевода его в основание (III) и затем параллельным внесением ацилирующего агента (IV) и 1.11 моля ТЭА, растворенных в диоксане, поддерживая рН 7.5-8.0, внесением 0.25 г активированного угля, удалением шлама гидрохлорида триэтиламина, удалением растворителя и кристаллизацией осадка из водного изопропанола в соотношении 7.5:6.0.
Предлагаемый способ иллюстрируется примерами, приведенными ниже.
Пример 1
В пятитигорлую колбу емкостью 500 мл с мешалкой, термометром, двумя капельными воронками и форштосом с хлоркальциевой трубкой пропускают в течение 5 мин инертный газ, загружают 160 мл диоксана, 7.39 г (0.040 моль) гидрохлорида амина (II), размешивают, охлаждают до 15-17°С и из капельной воронки вносят 4.04 г (0.040 моль) ТЭА в 4 мл диоксана. Размешивают 30 мин при 18-20°С. После чего из двух капельных воронок параллельно вносят 10,2 г (0,0401 моль) бензоилхлорида (IV) в 84 мл диоксана и 4.52 г (0.0446 моль) ТЭА в 16 мл диоксана, поддерживая температуру 27-30°С и рН 7.5-8.0. По окончании выдержки в реакционнуую массу вносят 0.25 г активированного угля, фильтруют от шлама, фильтрат упаривают. Остаток кристаллизуют из водного изопропанола. Получают 12.87 г (88%) бесцветного кристаллического порошка с содержанием основного вещества 100%. Температура плавления 166-167°С. Литературная Т. пл. 160-162° /US 3565911 кл. 260-326.11 1968/.
Пример 2 (сравнительный по прототипу)
В реакционную колбу, продутую азотом в течение 10 мин, вносят 80 мл ТГФ, 3.76 г (0.02045 моль) 1-амино-2-метилиндолина гидрохлорида. Размешивают и в течение 10 мин из капельной воронки вносят 4.37 г (0.0433 моль) ТЭА при температуре 18-20°С. Полученную суспензию выдерживают при работающей мешалке 30 мин при 18-20°С, после чего из капельной воронки в течение 1 ч 45 мин вносят 5.2 г (0.0205 моль) 4-хлор-3-сульфамоилбензоилхлорида в 40 мл ТГФ. Реакционную массу размешивают 3 ч при 24-30°С, вносят 0.5 г активированного угля, фильтруют, фильтрат упаривают. Остаток кристаллизуют из изопропилового спирта. Получают белый осадок с выходом 80.5% с содержанием основного вещества 99.98%.
Таким образом, как видно из приведенных примеров, заявляемый способ получения 1-(3-сульфамоил-4-хлорбензоил)амино-2-метилиндолина позволяет упростить процесс получения благодаря замене легковоспламеняющегося и взрывоопасного ТГФ на диоксан, а также увеличить выход целевого продукта до 88%.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения бензамидов | 1980 |
|
SU1039440A3 |
| ПРОИЗВОДНЫЕ 5-АРИЛ-1Н-1,2,4-ТРИАЗОЛА И СОДЕРЖАЩАЯ ИХ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2000 |
|
RU2249588C2 |
| ПРОИЗВОДНЫЕ АРИЛИДЕН- ИЛИ АРИЛАЛКИЛ-1-АЗАЦИКЛОАЛКАНА, СМЕСИ ИХ ИЗОМЕРОВ ИЛИ ОТДЕЛЬНЫЕ ИЗОМЕРЫ ИЛИ СОЛИ | 1993 |
|
RU2126400C1 |
| Способ получения гетероциклических бензамидов или их солей | 1979 |
|
SU1158040A3 |
| СПОСОБ ПОЛУЧЕНИЯ ВЫСОКОЧИСТОГО ПРАЗУГРЕЛЬ ГИДРОХЛОРИДА | 2008 |
|
RU2435776C2 |
| ДИНАТРИЕВЫЕ СОЛИ 4-СУЛЬФОКСИЭТИЛСУЛЬФОНИЛ- 2-X-2' -Y-4' -АМИНО-N-МЕТИЛСУЛЬФО-N- N-2" -( 4" -ХЛОР- 6" -АМИНО-ДИ-( β -ГИДРОКСИЭТИЛ)- 1", 3", 5" -ТРИАЗИНИЛ)-АЗОБЕНЗОЛА ДЛЯ КРАШЕНИЯ ИЛИ ПЕЧАТИ МАТЕРИАЛОВ ИЗ НАТУРАЛЬНЫХ И/ИЛИ СИНТЕТИЧЕСКИХ ВОЛОКОН | 1993 |
|
RU2064949C1 |
| Способ получения производных 2,4,-бис/азиридинил-1/-6-амино-симмтризина | 1974 |
|
SU521272A1 |
| Способ получения 7- -амино-7 метокси-цефалоспориновых эфиров | 1974 |
|
SU546282A3 |
| Способ получения 4-хлор-3-сульфамоилбензойной кислоты | 1988 |
|
SU1736339A3 |
| НОВЫЕ ИНГИБИТОРЫ BRAF КАК «РАЗРУШИТЕЛИ ПАРАДОКСА» | 2020 |
|
RU2825870C1 |
Изобретение относится к улучшенному способу получения 1-(3-сульфамоил-4-хлорбензоил)амино-2-метилиндолина ацилированием гидрохлорида 1-амино-2-метилиндолина 4-хлор-3-сульфамоилбензоилхлоридом в среде диоксана, причем первоначально вносят 1 моль триэтиламина, затем параллельно вносят 4-хлор-3-сульфамоилбензоилхлорид в диоксане и оставшиеся 1,11 моля триэтиламина в диоксане, поддерживая рН 7,5-8. Способ обеспечивает повышение выхода целевого продукта до 88% против 80,5%, замену использования тетрагидрофурана на диоксан.
Способ получения 1-(3-сульфамоил-4-хлорбензоил)амино-2-метилиндолина реакцией ацилирования гидрохлорида 1-амино-2-метилиндолина 4-хлор-3-сульфамоилбензоилхлоридом в присутствии 2,11 молей триэтиламина с последующим выделением целевого продукта, отличающийся тем, что реакцию проводят в среде диоксана с первоначальным внесением 1 моля триэтиламина и последующим параллельным внесением 4-хлор-3-сульфамоилбензоилхлорида и оставшейся части триэтиламина, растворенных в диоксане, поддерживая рН 7,5-8.
| Устройство для предупреждения попадания посторонних предметов в скважину | 1971 |
|
SU462017A1 |
| J | |||
| Med | |||
| Chem | |||
| Приспособление для изготовления в грунте бетонных свай с употреблением обсадных труб | 1915 |
|
SU1981A1 |
| J | |||
| of Medicinal Chemistry | |||
| Дверной замок, автоматически запирающийся на ригель, удерживаемый в крайних своих положениях помощью серии парных, симметрично расположенных цугальт | 1914 |
|
SU1979A1 |
| Машина для добывания торфа и т.п. | 1922 |
|
SU22A1 |
| J | |||
| of Heterocyclic Chemistry | |||
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ АНТИГИПЕРТЕНЗИВНЫМ И ДИУРЕТИЧЕСКИМ ДЕЙСТВИЕМ, И СПОСОБ ЕЁ ПОЛУЧЕНИЯ | 2002 |
|
RU2201751C1 |
Авторы
Даты
2005-10-10—Публикация
2004-07-26—Подача