Изобретение относится к области медицинской диагностики, может быть использовано для прогнозирования риска развития диабетической дистальной полинейропатии у жителей Центральной России с сахарным диабетом 2 типа.
Сахарный диабет является одним из четырех главных неинфекционных заболеваний, требующих пристального внимания и новых эффективных методов диагностики и лечения в целях борьбы с его распространенностью и связанными с ним осложнениями [Oguntibeju OO. Type 2 diabetes mellitus, oxidative stress and inflammation: examining the links. Int J Physiol Pathophysiol Pharmacol. 2019 Jun 15;11(3):45-63]. СД2 также считается самым распространенным в мире заболеванием, связанным с нарушением обмена веществ; в основе прогрессирования СД2 лежит снижение функционирующей массы β-клеток поджелудочной железы, связанное в том числе с развитием хронического стресса эндоплазматического ретикулума из-за нарушений фолдинга белков, в том числе препроинсулина, проинсулина и самого инсулина. [Roden M, Shulman GI. The integrative biology of type 2 diabetes. Nature. 2019 Dec;576(7785):51-60. doi: 10.1038/s41586-019-1797-8]. Обозначенные патологические изменения провоцируют развитие осложнений СД2, к их числу относятся патологии нервной системы, включая диабетическую дистальную полинейропатию, которая является самым частым осложнением у пациентов с СД2 и наблюдается у 75% больных [Charlton A, Garzarella J, Jandeleit-Dahm KAM, Jha JC. Oxidative Stress and Inflammation in Renal and Cardiovascular Complications of Diabetes. Biology (Basel). 2020 Dec 30;10(1):18]. Исследования последних лет указывают на то, что нарушения процесса фолдинга белков и стресс эндоплазматического ретикулума способствуют развитию окислительного повреждения и митохондриальной дисфункции, которые, в свою очередь, могут повреждать периферические нервы [Ansari, P., Hannan, J. M. A., Azam, S., & Jakaria, M. Challenges in Diabetic Micro-Complication Management: Focus on Diabetic Neuropathy. International Journal of Translational Medicine. 2021 1(3), 175-186.]. Одним из основных классов шаперонов, которые принимают непосредственное участие в фолдинге белков, является семейство Hsp70, главным представителем которого является белок HSP72. Данные белок кодируется геном HSPA1A и отвечает за контроль качества процесса упаковки белков, а также за цитопротекцию в стрессовых условиях метаболизма клетки [Henstridge DC, Whitham M, Febbraio MA. Chaperoning to the metabolic party: The emerging therapeutic role of heat-shock proteins in obesity and type 2 diabetes. Mol Metab. 2014 Aug 30;3(8):781-93]. По данным транскриптомного анализа GTex Portal полиморфный вариант rs1043618 ассоциирован со снижением экспрессии гена HSPA1A в нервной ткани [https://www.gtexportal.org].
Известен способ диагностики стадии нейропатии у больных с сахарным диабетом 2 типа (RU 2501517 С2, дата публикации 20.12.2013), включающий исследование температурной чувствительности, при этом проводят температурное исследование стопы сенсорным путем последовательно, определяя сначала температуру адаптации, затем, подавая измененный температурный стимул, измеряют пороговые значения как минимум в трех зонах. Результаты измерений записывают и определяют температурный коэффициент стопы по формуле: Тк=(Тч1-Хч1)×(Тч2-Хч2)×…×(Тчn-Хчn), где Тк - температурный коэффициент стопы, Тч1, 2, n - тепловая чувствительность в выбранных зонах , Хч1, 2, n - холодовая чувствительность в выбранных, Тчз - среднее значение тепловой чувствительности у здоровых людей без нейропатии, Хчз - среднее значение холодовой чувствительности у здоровых людей без нейропатии. Далее по значению температурного коэффициента стопы оценивают стадию нейропатии: отсутствие нейропатии - Тк≤2; субклиническая нейропатия: А - Тк от 2 до 50; Б - Тк от 51 до 100; клиническая нейропатия - Тк от 101 до 200; выраженная (осложненная) нейропатия - Тк более 200.
Существенным преимуществом данного метода является достаточно точная диагностика стадии нейропатии у больных с СД2, однако метод не позволяет спрогнозировать риск развития диабетической дистальной полинейропатии.
Известен способ диагностики субклинической стадии диабетической нейропатии по патенту на изобретение RU 2671630 C1 (дата публикации 06.11.2018), включающий исследование сывороточного уровня мозгового нейротрофического фактора (BDNF) с помощью иммуноферментного анализа. Дополнительно определяют уровни высокоспецифичного тропомиозинового рецептора киназы (Trk-B), васкулоэндотелиального фактора роста (VEGF) и уровень гликемии натощак (Glu). В последующем высчитывают коэффициент по формуле регрессионной модели K=0,2*Glu+0,55*TrkB+0,3*(BDNFA/VEGF), где К - коэффициент, 0,2 - константа регрессии, Glu - уровень глюкозы крови, 0,55 - константа регрессии, Trk-B - сывороточный уровень тропомиозинового рецептора киназы типа В, 0,3 - константа регрессии, BDNF - сывороточный уровень мозгового нейротрофического фактора, VEGF - сывороточный уровень васкулоэндотелиального фактора роста, и при значении коэффициента K>4,5 диагностируют субклиническую стадию диабетической нейропатии.
Однако данный способ не рассчитан на выявление предрасположенности к развитию диабетической дистальной полинейропатии у пациентов с СД2, и способен диагностировать только субклиническую стадию диабетической нейропатии.
Наиболее близок по результату и методу исследования способ прогнозирования риска развития диабетической дистальной полинейропатии у женщин с сахарным диабетом 2 типа (RU 2787273, дата публикации 09.01.2023). В данном методе осуществляют забор образца периферической венозной крови. После экстракции ДНК проводят анализ полиморфного варианта гена малой ГТФ-азы RAC1 rs7784465 (T>C). В случае выявления аллеля rs7784465-C прогнозируют повышенный риск формирования диабетической дистальной полинейропатии у женщин с сахарным диабетом 2 типа. При обнаружении генотипа rs7784465-Т/Т прогнозируют низкий риск развития диабетической дистальной полинейропатии у женщин с сахарным диабетом 2 типа.
Недостатком метода является то, что прогнозирование риска развития диабетической дистальной полинейропатии возможно только для женщин и не может быть использован для всех пациентов с сахарным диабетом 2 типа.
Технический результат заключается в получении критериев оценки риска формирования диабетической дистальной полинейропатии у жителей Центральной России с сахарным диабетом 2 типа по данным о генетическом полиморфизме rs1043618 (G>С).
Технический результат достигается тем, что после экстракции ДНК проводят анализ полиморфного варианта гена HSPA1A rs1043618 (G>С) и прогнозируют повышенный риск формирования диабетической дистальной полинейропатии у жителей Центральной России с сахарным диабетом 2 типа при выявления генотипа rs1043618-С/С, а при обнаружении генотипов rs1043618 G/G или G/C - низкий риск развития диабетической дистальной полинейропатии у пациентов с сахарным диабетом 2 типа в популяции Центральной России.
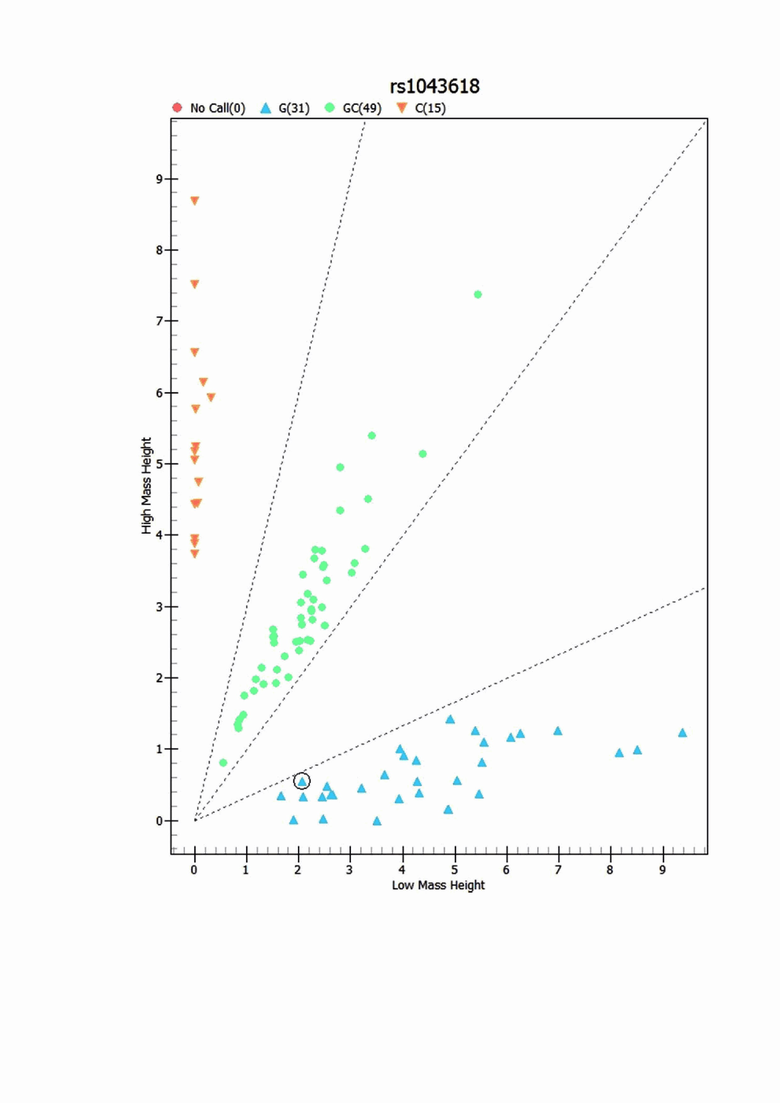
Изобретение поясняется следующим чертежом: дискриминация генотипов по локусу rs1043618 гена HSPA1A при генотипировании на основе масс-спектрометрии: генотипы rs1043618 -G/G показаны голубым цветом, генотипы rs1043618-G/C показаны зеленым цветом, генотипы rs1043618 -С/С показаны оранжевым цветом.
Способ осуществляют следующим образом:
1. Выделение ДНК из периферической венозной крови. На первом этапе к 0,5 мл крови добавляли 0,5 мл PBS и центрифугировали 10 мин при 12 тыс. об/мин. Надосадочную жидкость сливали, добавляли 1 мл PBS и вновь центрифугировали при тех же условиях. Надосадочную жидкость сливали, добавляли 200 мкл ТЕ-буфера, пипетировали до растворения осадка и затем последовательно добавляли 10 мкл 1% раствора додецилсульфата натрия SDS и 5 мкл протеиназы К. Пробирки инкубировали в термостате при t=37°C 12 ч. В ходе второго этапа проводили четыре последовательных центрифугирования с фенолом и хлороформом согласно протоколу методики (10 мин, 8 тыс. об/мин), после чего ДНК осаждали ледяным раствором 95% этилового спирта и центрифугировали 10 мин при 14,3 тыс. об/мин. По испарении спирта ДНК растворяли в 100 мкл деионизированной дистиллированной воды. Получаемый раствор ДНК в воде имел чистоту в диапазоне А260/280=1,5-2,0 и среднюю концентрацию около 180-200 нг/мкл.
Экстракция геномной ДНК из цельной крови колоночным методом проводилась с помощью набора QIAamp DNA blood mini kit (QIAGEN, Германия) на автоматической станции QiaCube (QIAGEN, Германия). Роботизированный протокол продолжительностью 58 минут включал этап лизиса клеток 0,2 мл цельной крови с помощью лизирующего буфера и протеиназы к QIAGEN, инкубирование, перенос лизата в колонку, связывание ДНК с мембраной колонки, центрифугирование, двукратное промывание колонки буфером AW1 и AW2, центрифугирование колонки и, наконец, элюирование очищенной ДНК. Получаемый раствор ДНК в воде имел идеальную чистоту А260/280=1,7-1,9 и среднюю концентрацию около 40-50 нг/мкл. Экстрагированные из крови образцы ДНК хранились в морозильниках Thermo Fisher Scientific (США) при -20°С.
2. Подготовка образцов ДНК к масс-спектрометрическому анализу. Качество выделенной ДНК оценивали по степени чистоты и концентрации раствора на спектрофотометре NanoDrop (Thermo Fisher Scientific, США). Все анализируемые образцы ДНК были разведены деионизированной водой до концентрации 10 нг/мкл при А260/280=1,5-2,0.
3. Анализ полиморфизма гена HSPA1A - генотипирование методом матрично-активированной лазерной десорбционно-ионизационной масс-спектрометрии MALDI-TOF. Использовали следующие последовательности праймеров: прямой F: 5`- ACGTTGGATGTTCCGTTTCCAGCCCCCAAT -3`, обратный R: 5`- ACGTTGGATGTAGGTGGTGCCCAGGTCGAT -3`, праймер удлинения E: 5`- GCTCTCTGTCGGCTC -3`. Для приготовления ПЦР-микса (в расчете на один спектральный чип) в центрифужную микропробирку вносили 80,6 мкл ddH2O, 50,4 мкл 10x буфера, 40,3 мкл MgCl2 (концентрация 25 ммоль/л), 10,1 мкл смеси дНТФ (концентрация 25 ммоль/л), 100,8 мкл смеси ПЦР-праймеров (концентрация 0,5 мкмоль/л) и 20,16 мкл HotStartTaq полимеразы (концентрация 5 ЕД/мкл). Смесь вортексировали и раскапывали в 96-луночный ПЦР-планшет по 3 мкл в лунку, после чего с помощью восьмиканального дозатора вносили по 2 мкл ДНК (концентрация 10 нг/мкл). Планшет заклеивали, центрифугировали 20 сек при 1000 об/мин и загружали в термоциклер CFX96 Bio-Rad на 125 мин при следующем режиме: денатурация 2 мин при 95°С, амплификация 44 цикла, состоящая из денатурации 30 сек при 95°С, отжига 30 сек при 56°С и элонгации 60 сек при 72°С. После чего пробы инкубировали 5 мин при 72°С. Не прореагировавшие в ходе ПЦР дНТФ удаляли с помощью реакции SAP (shrimp alkaline phosphatase), в ходе которой щелочная фосфатаза креветки гидролизовала дНТФ до нуклеозидов и фосфатов. Для приготовления SAP-микса в микропробирке смешивали 161,6 мкл ddH2O, 18 мкл 10хTS буфера и 31,7 мкл SAP фермента. Далее вносили по 2 мкл SAP-смеси в каждую лунку, планшет заклеивали, центрифугировали 20 сек при 1000 об/мин и загружали в термоциклер CFX96 Bio-Rad на 55 мин при следующем режиме: 45 мин при 37°С и 10 мин при 85°С. Для проведения третьей реакции iPLEX готовили Е-праймер-микс из расчета 8,8 мкл праймеров Е1-Е9, 11,7 мкл праймеров Е10-Е18, 14,6 мкл праймеров Е19-Е27, 17,5 мкл праймеров Е28-Е35 и 45,1 мкл ddH2O. После масс-спектрометрической оценки интенсивности пиков Е-праймеров в полученной смеси, в микс добавляли Е-праймеры в количествах, необходимых для достижения одинаковой интенсивности сигнала. Для приготовления iPLEX-микса в микропробирке смешивали 65,4 мкл ddH2O, 21,2 мкл iPLEX буфера, 21,2 мкл терминирующей смеси, 99,3 мкл Е-праймер-микса и 4,33 мкл iPLEX-фермента, вортексировали и раскапывали в лунки по 2 мкл. Планшет заклеивали, центрифугировали 20 секунд при 1000 об/мин и загружали в термоциклер CFX96 Bio-Rad на 135 мин при следующем режиме: денатурация 30 сек при 94°С, затем 40 циклов, состоящие из денатурации 5 сек при 94°С, отжига 5 сек при 52°С, элонгации 5 сек при 80°С, с последующим инкубированием в течение 3 мин при 72°С. По завершении реакции iPLEX, планшет охлаждали до +4°С, добавляли по 30 мкл воды во все лунки, центрифугировали 1 мин при 1000 об/мин и загружали в масс-спектрометр. Ввиду того, что небольшие полярные молекулы и положительно заряженные катионы натрия и калия могут образовывать аддукты с олигонуклеотидами и создавать серию контаминантных пиков, ампликоны были подвергнуты роботизированному обессоливанию путем их обработки смолой SpectroCLEAN (Agena Bioscience). Перенос образцов на спектральный чип с матрицей для ионизации осуществлялся в автоматическом режиме на рабочей станции Nanodispenser. Пример кластерного распределения генотипов по SNP rs1043618 в результате масс-спектрометрического анализа на геномном масс-спектрометре MassArray analyzer 4 (Agena Bioscience) показан на чертеже.
Статистические расчеты проводили с помощью программы SNPStats (Solé, X., Guinó, E., Valls, J., Iniesta, R., & Moreno, V. (2006). SNPStats: a web tool for the analysis of association studies. Bioinformatics, 22(15), 1928-1929).
4. Прогнозирование повышенного риска формирования диабетической периферической полинейропатии в случае выявления генотипа rs1043618 -С/С и пониженного риска развития этого осложнения сахарного диабета 2 типа при выявлении генотипов rs1043618 G/G или G/C.
Возможность использования предложенного способа для определения риска развития диабетической дистальной полинейропатии у жителей Центральной России подтверждает анализ результатов наблюдений 1408 пациентов с СД2, у 1301 из которых установлена диабетическая дистальная полинейропатия. В исследование включались лица славянской национальности Центральной России. Диагноз СД2 был установлен врачами-эндокринологами ОБУЗ ГК БСМП на основе клинического и лабораторно-инструментального обследования. Установлено, что генотипы rs1043618-G/G и rs1043618-G/С значимо чаще встречался у пациентов без диабетической дистальной полинейропатии (92%) по сравнению с больными СД2, имеющими данное осложнение основного заболевания (73%). Носительство генотипа rs1043618-С/С HSPA1A ассоциировалось с повышенным риском развития диабетической дистальной полинейропатии: OR=2,85, 95% CI 1,28-6,37, P=0,0038 (таблица 1).
Ассоциация полиморфного варианта rs1043618 гена HSPA1A с диабетической дистальной полинейропатией у пациентов с сахарным диабетом 2 типа
(SNP ID)
тип, аллель
(95% CI)2
(n=115)
(n=1239)
2Отношения шансов и 95% доверительный интервал с поправками на ковариаты - возраст и индекс массы тела,
В качестве примеров конкретного применения разработанного способа приведено генетическое обследование пациентов Центральной России, не являющихся родственниками между собой: проведено генетическое обследование по локусу rs1043618 (G>С) гена HSPA1A.
Пациент М., 49 лет, находился на стационарном лечении в ОБУЗ КГКБ СМП г. Курска с 31.12.2019 по 14.01.2020. Диагноз: сахарный диабет, 2 тип, фаза декомпенсации от 31.12.2019, фаза компенсации от 14.01.2020. Индивидуальный целевой уровень HbA1c<6,2%. Целевой уровень гликемии плазмы натощак <7,5 ммоль/л, через 2 ч после еды <8,7 ммоль/л. У пациента была взята венозная кровь, при генотипировании полиморфного локуса rs1043618 (G>С) был выявлен генотип G/G HSPA1A, что позволило отнести пациента в группу больных с низким риском развития диабетической дистальной полинейропатии. Дальнейшее наблюдение не подтвердило диагноз диабетической дистальной полинейропатии.
Пациентка Ж., 74 года, находилась на стационарном лечении в ОБУЗ КГКБ СМП г. Курска с 30.11.2015 по 15.12.2015. Диагноз: сахарный диабет, 2 тип, фаза декомпенсации от 30.11.2015, фаза компенсации от 15.12.2015. Индивидуальный целевой уровень HbA1c<8.0%. Целевой уровень гликемии плазмы натощак <8,0 ммоль/л, через 2 ч после еды <10,5 ммоль/л. У пациентки была взята венозная кровь, при генотипировании полиморфного локуса rs1043618 (G>С) был выявлен генотип rs1043618 С/С HSPA1A, что позволило отнести пациентку в группу больных с высоким риском развития диабетической дистальной полинейропатии. Углубленное неврологическое исследование подтвердило наличие у женщины данного заболевания.
Пациент К., 66 лет, находился на стационарном лечении в ОБУЗ КГКБ СМП г. Курска с 1.12.2017 по 11.12.2017. Диагноз: сахарный диабет, 2 тип, впервые выявленный, фаза декомпенсации от 1.12.2017, фаза компенсации от 11.12.2017. Индивидуальный целевой уровень HbA1c<6,5%. Целевой уровень гликемии плазмы натощак <7,5 ммоль/л, через 2 ч после еды <9,0 ммоль/л. У пациента К. была взята венозная кровь, при генотипировании полиморфного локуса rs1043618 (G>С) был выявлен аллель С в составе генотипа rs1043618 С/С HSPA1A, что позволило отнести пациента в группу больных с высоким риском развития диабетической дистальной полинейропатии. Углубленное неврологическое исследование подтвердило наличие у пациента диабетической дистальной полинейропатии.
Применение данного способа позволит на доклиническом этапе формировать среди больных диабетом 2 типа группы риска и своевременно реализовывать в этих группах необходимые лечебно-профилактические мероприятия по предупреждению развития диабетической дистальной полинейропатии.
Таким образом, полученные данные свидетельствуют о том, что генготип rs1043618-С/С гена HSPA1A является генетическим фактором риска развития диабетической дистальной полинейропатии у пациентов с сахарным диабетом 2 типа (OR=2,85).
Таким образом, использование предложенного способа позволит прогнозировать развитие диабетической дистальной полинейропатии у пациентов с сахарным диабетом 2 типа, что даст возможность осуществлять мероприятия по профилактике дистальной полинейропатии: диспансерное наблюдение, регулярный контроль уровня глюкозы в крови, нормализацию массы тела, достаточную физическую активность, правильное питание с ежедневным включением в рацион свежих овощей и фруктов и ограничением рафинированных углеводов и жиров.
Изобретение относится к медицине, а именно к медицинской диагностике, и может быть использовано для прогнозирования риска развития диабетической дистальной полинейропатии у жителей Центральной России с сахарным диабетом 2 типа. Осуществляют забор образца периферической венозной крови. После экстракции ДНК проводят анализ полиморфного варианта гена из семейства белков теплового шока HSPA1A rs1043618 (G>C). В случае выявления генотипа rs1043618 C/С прогнозируют повышенный риск формирования диабетической дистальной полинейропатии. При обнаружении генотипа rs1043618 G/C и G/G прогнозируют низкий риск. Способ обеспечивает получение новых критериев оценки риска формирования диабетической дистальной полинейропатии у жителей Центральной России с сахарным диабетом 2 типа по данным о генетическом полиморфизме rs1043618 (G>С). 1 ил., 1 табл., 3 пр.
Способ прогнозирования риска развития диабетической дистальной полинейропатии у жителей Центральной России с сахарным диабетом 2 типа, включающий забор образца периферической венозной крови, отличающийся тем, что после экстракции ДНК проводят анализ полиморфного варианта гена из семейства белков теплового шока HSPA1A rs1043618 (G>C) и прогнозируют повышенный риск формирования диабетической дистальной полинейропатии у жителей Центральной России с сахарным диабетом 2 типа в случае выявления генотипа rs1043618 C/С, а при обнаружении генотипа rs1043618 G/C и G/G – низкий риск развития диабетической дистальной полинейропатии у жителей Центральной России с сахарным диабетом 2 типа.
| Способ прогнозирования риска развития диабетической дистальной полинейропатии у женщин с сахарным диабетом 2 типа на основе генотипирования полиморфизма rs7784465 гена RAC1 | 2022 |
|
RU2787273C1 |
| КЛЁСОВА Е.Ю | |||
| и др | |||
| Устройство для вывода информации | 1982 |
|
SU1043618A1 |
| Генофонд и репродуктивное здоровье человека: сборник тезисов всероссийской конференции молодых ученых (Санкт-Петербург, 22-23 июня 2022 г.) | |||
| - Санкт-Петербург, 2022 | |||
| Прибор для нагревания перетягиваемых бандажей подвижного состава | 1917 |
|
SU15A1 |
| КЛЁСОВА Е.Ю | |||
| и др | |||
Авторы
Даты
2023-12-19—Публикация
2023-07-14—Подача