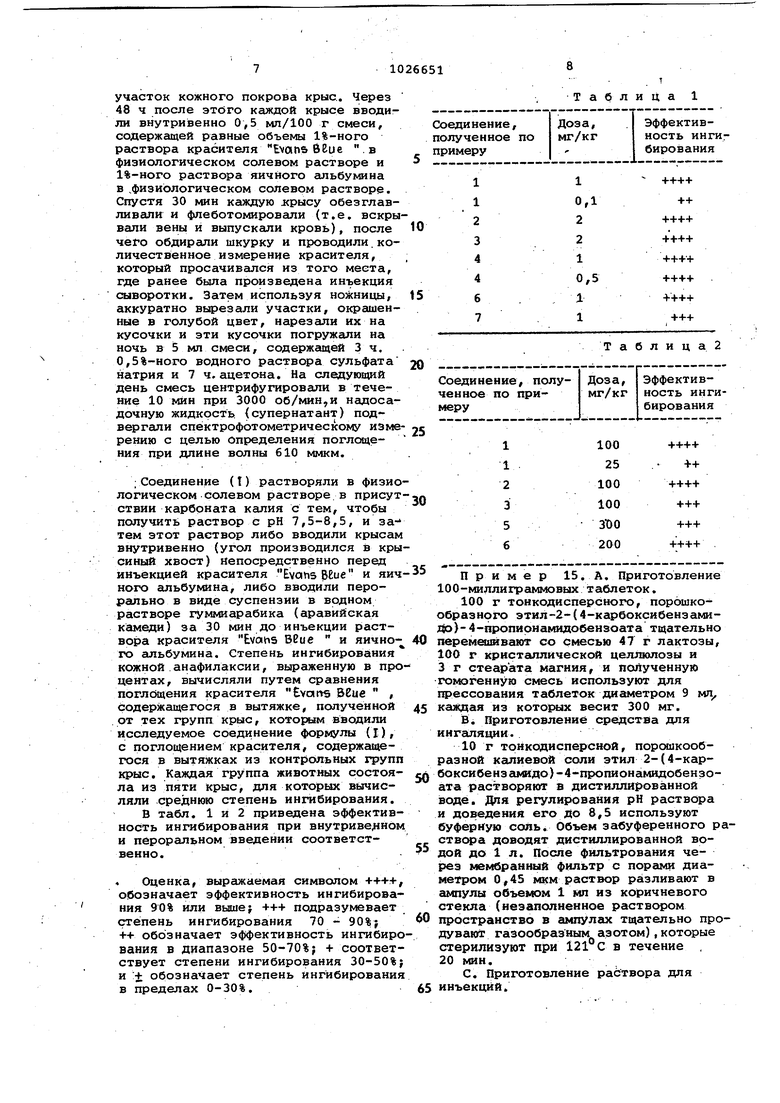
Изобретение относится к способу получения новых моноамидных произв ных терефталевой кислоты общей фор лы NHCOH - , -алкил -f - С или С;|-С - лкил; R - С или нормальный С2-С4 л и их фармацевтически приемлемых солей. Указанные соединения могут найт применение в качестве фармацевтиче кого средства для профилактики и/и лечения аллергической бронхиальной астмы, аллергических дерматитов и других аллергических заболеваний. Известны М-замещенные амиды 2,4 -бис-(бензамидо)бензойной кислоты формулы.. где А - {СН2)2-, - ( одинаковы или различны и представляют собой С -Сдкил;Y - одинаковы или различны и представляют собой метил и метоксигруппу, которые обл дают противоаллергической активностью l . Цель изобретения - разработка сп срба получения моноамиДных производ ных терефталевой кислоты общей формулы (I), обладающих более высокой прбфивоаллергической активностью. Поставленная цель достигается те что согласно способу получения моно амидных производных.терефталевой кислоты общей формулы (1), который основан на методе получения амидов из дигидробёнзоксазинонов путем раскрытия оксазинового цикла L23 f соединение общей формулы где R , и R имеют указанные значения подвергают взаимодействию с соедине нием общей формулы (III) , (ИГ) где R--имеет указанные значения, при 50-10О с в органическом растворителе в присутствии третичного амина. Обычно взаимодействие осуществляют при 80-100с, в качестве органичес.кОго растворителя используют этиловый спирт, тетрагидрофуран, диоксан или диметилформамид, а -в качестве третичного амина - триэтиламин, трибутиламин или N-метилМОрфолин. Соединение формулы (II) легко получсиот восстановлением соответствующего нитросоединения, в результате чего получается соединение формулы COOTl (W) где R имеет значение, охарактеризованноекоторое затем подвергают взаимодействию с соединением формулы (RCOCJ) где R имеет значение, охс1рактеризованное выше, в пиридине. Пример 1. Смесь 12 г 7-(пропионамудо)-2-(4-карбоксифенил)-4Н-3,1-бензоксазин-4-она, 120 мл абсолютного этанола и 9 мл триэтиламина нагревают в режиме кипяченая с обратным холодильником в течение 8 ч. После этого смесь охлаждают до комнатной температура и затем прибавляют к ней 9 мл уксусной кислоты и 500 мл воды Выпавшее при этом в осадок кристаллическое вещество отфильтровывают и перекристаллизовывают из смеси этилового спирта и воды. В итоге получают. 10 г целевого этил 2-{4-карбоксибензамидо)-4-пропионамидобенг зоата, имеющего т.пл, 246-248с. Вычислено, %;С62,5;Н5,2; N 7,3. Найдено, %: С 62,2; Н 5,2j, N 7,2. Пр им е р 2. Процедуру примера 1 повторяют, подвергая взаимсяействию 7-(пропионамидо)-2-(4-карбоксифеиил)-4Н-3,1-бензоксазин-4-он с н-пропанолом, и реакционный продукт обрабатывают аналогично примеру 1 за исключением того, то в качестве растворителя для перекристаллизации используют смесь диоксана и воды. Полученный с 80%-ным выходом продукт представляет собой пропил 2-(4-карбоксибензамидо)-4-пропионамидобензоат, имеющий т.пл. 233-235 с. Вычислено, %:С63,3;Н5,6; N 7,0. С 21 Н 22 Найдено, %: С 63,1; Н 5,9; N 7,0. Пример 3. Процедуру примера 2 повторяют, подвергая взаимодействию 7-(пропионамидо)-2-(4-карбоксифенил)-4Н-3,1-бензоксазин-4-он с н-бутанолом, и реакционную смесь обрабатывают аналогично примеру 2, в итоге с 75%-ным выходом получают н-бутил 2-(4-карбоксибензамидо -4- -пропионамидобензоат, имеющий т.пл. 243-245°С. Вычислено, %:С64,1;Н5,9; N 6,8. Найдено, %: С 64,0; Н 6,2; N 6,7. Пример 4. Смесь 5 г 7-(про пионамидо)-2-(4-карбоксифенил)-4Н-3,1-бензоксазин-4-она, 50 мл димети формамида, 10 мл воды и 8 мп триэтил амина нагревают при 80-90°С в течение. 10 ч. После того, как смесь охладилась до комнатной температуры, ее подкисляют разбавленной соляной кислотоИ с целью доведения рН до 2-3 Выпавший при этом кристаллический осадок отфильтровывают, промывают водой и после перекристаллизации из изопропилового спирта получают 4,1 г 2-(4-карбоксибензамидо)-4-пропионамидобензойной кислоты, имекяцей т.пл 284-28бс. {с разложением). Пример 5 Смесь 4 г 7-(пропионамидо)-2-(4-этоксикарбонилфенил) -4Н-3,1-бензоксазин-4-она, 3.00 мп абсолютного этилового спирта и 10 мл триэтиламина нагревают в режиме кипя чения с обратным холодильником в течение 24 ч. После завершения реакции смесь концентрируют в вакууме и остаток после удаления растворителя перекристаллизовывают из смеси этилового спирта и воды, в результате чегополучгиот . 3,8 г эгил 2-(4-этоксикарбонилбензамидо)-4-пропионамидобензоата, имеющего т.пл. 172-173°С. П р и lit е р 6. Смесь 3,7 г 7-{пропионамидо)-2-(4-этоксикарбонилфенил-4Н-3,1-бензоксазин-4-она, 50 МП диметилформамида, 3 мд триэтил амина и 0,2 мл воды перемешивают, при 70-90 с в течение 24 ч. После завершения реакции к смеси прибавляют 300 МП воды и подкисляют разбавленной соляной кислотой, чтобы довести рН системы до 1-2, алпавший при этом кристаллический осадок отделяют филь рованием, промывают на фильтре водои и перекристаллизовывают из ацето нитрила, в результате чего получают 3,0 г 2-(4-этоксикарбонилбензамидо) -4-пропионамидобензоата, имеющего т.пл. 240-243 С. Пример 7. Смесь, состоящую из 3,7 г 7-(изокапронамидо)-2-(4-карбонилфенил)-4Н-3,1-бензоксаэин-4-она, 50 МП тетрагидрофурана, 3 мп трибутиламина и 0,2 мп воды, подвергают реакции при 50-60°С в течение 35 ч. Реакционную смесь обрабатывают согласно методике примера 4 с образованием 2-(4- -карбоксибензамидо)-4-изокапронамидобензойяой кислоты; т.пл. 296-ЗОО С (с разложением), выход 49%. Вычислено, %: С63,3; Н5,6; N7,0. HjiNjOfe Найдено, %:С 63,5; Н 5,5; N 7,3. Примере. Смесь, состоящую из 3,5 г 7-{изобутиламидо)-2- 4-метоксикарбонилфенил)-4Н-3,1-бензоксазин-4-она, 50 мл диоксана, 2,5 мл N-метилморфолина и 0,2 мп вода, перемешивают при/ 90-95с в течение 2 ч. Реакционную смесь обрабатывают аналогично примеру 4 с образованием 2-(4-метоксикарбонилбензамидо)-4-изобутиламидобензойной кислоты; т.пл. 244-247С (с разложением), выход 57%. Вычислено, %: С 62,5; Н 5,2;N7,3. 10 го Найдено, %i С 62,4; Н 5,5; N 7,1. П р и м е р 9, Смесь, состоящую из 4,0 г 7-{пропианамидо)-2-{4-бутоксикарбонилфенил)-4Н-3,1-бензоксадин-4-она, 50 МП диметилформаи ида, 3 мл триэтиламина и 0,2 мп воды, перемешивают при 70-80 С в течение 20 ч. Реакционную смесь обрабатывают согласно примеру 4 с образованием 2-(4-бутоксикарбонилбензамидо)-4-пропионамидобек- зоййой кислоты,т.пл.183-1 57,выход 55%, Вычислено, %: С 64,1; Н 5,9; N 6,8. CZlH24N206 Найдено, %; С 64,5; Н 5,7; М 6,6, П р и м е р. 10, Смесь, состоящую из 3,8 г 7-(пpoпиoнaмндo)-2-(4-изoщx)пил6кcикapбoнилфeнил ) -4Н-3 , 1-бензоксазин-4-она, 50 мп димeтилфopмa в да, 3 МП триэтиламин:а и 0, воды, перемешивааот при 80-90 С в течение 24 ч. Реакционную смесь обрабатывают аналогично примеру 4 с образованием 2-(4-изопропилоксийарбонил6ензамидо)-4-пропионамидобензойной кислотму . 219-221°С, выход 46%. Вычислено, %:С63,3;Н5,6; N 7,0. C HrtjNjOi Найдено, %: С 63,5; Н 5,4; N 7,3. При м е р 11. Получение соли. Образец, состоящий из 7,1 кг ,этил 2-{4-карбоксибенза№{До)-4-пропионамидобензоата суспендируют в 25 л воды и 7 л ацетона. К суспензии постепенно добавляют 970 г карбоната натрия при 30-40с. После растворения карбоната натрия к расзтвору добавляют смесь, состоящую из 20 л ацетона и 700 г обесцвечивающего угля, и полученную смесь перемешивают в течение 1 ч при 40-50 0. После отфильтровывания обесцвечивающего угля добавляют к раствору ацетон,и раствор выетаивают в течение ночи при комнатно температуре. После фильтрации осажденного кристаллического вещества и промывания ацетоном получают 6,3 натриевой соли этил 2-(4-карбоксибензамидо-4-пропионамидобензоата;т.пл. 218-240С (с разложением). Пример 12. 3,5 г 7-ацетами -2-(4-карбокси6ензамидо}-4Н-3 1-бен оксазин-2-она и 0,2 мл веды обрабатывают согласно способу, описанному в примере 4, получая 2-(4-карбоксибензамидо}-4-ацетамидобензойную кис лоту, т.пл. 302-304°с (с разложением), выход 47%. Шлчислено, %: С 59,7 Н 4,1; N 8,2. C,f Найдено, %; С 59,9; Н 3,9; N 8,1 Пример 13. 3,7 г 7-н-бутил амидо-2-{4-карбоксибензамидо}-4Н-3, -бензоксазин-2-она и 0,2 мл воды обрабатывают согласно способу, описанному, в примере 4, получая 2-(4-карбоксибензамидо)-4-н-бутйламидоб зойную кислоту, т.пл. 297-299 0 (с разложением), выход 54%. Вычислено, %:С61,6;Н4,9; N 7,6. С,9 Найдено, %: С 61,3; Н 4,8; N 7,7 П р и м е р 14. 3,9 г 7-пропион амид-2-(4-пропоксибензилбензамидо)-4Н-3,1-бензоксазин-4-она и 0,2 мл воды обрабатывают согласно способу, описанному в примере 6, получая 2-(4-пропокгсикарбонилбензамидо)-4-пропионакидобензойную кислоту, т.п 199-200°С, выход 45%. Вычислено, %: С 63,3; Н5,6; N 7,0. . C iHojNnO Найдено, %: С 63,1;.Н 5,7; Н 7,2 Соединения формулы (I), в которы аминогруппа во втором положении 2,4 -диалшнобензойной кислоты ацилирована терефталевой кислотой или ее моноалкиловым эфиром, а аминогруппа в четвертом положении превращена в амид низшей алифатической кислоты, обладают значительно более высокой противоаллергической активностью, чем известные производные 2 ,4-диамин бензойной кислоты, такие соединения способны ингибировать различные аллергические реакции, включая различные виды и разновидности животных и типы антител. Аналогичные производные, в которых аминогруппа во втором положении 2,4-диамимобензойной кислоты ацилирована фталевой кислотой или изофталевой кислотой, обладают лишь слабой противоаллергической активностью. Соединения (I) являются эффективными противоаллергическими агентами Будучи введены животным перорально или внутривенно, они требуют лишь очень малой дозы для ингибирования пассивной кожной анафилаксии (повышенной кожной чувствительности) , которая используется в качестве традиционного или общепринятого индикатора при оценке противоаллергического эффекта того или иного исследуемого вещества. Соединения формулы (I) можно вводить пациентам в виде любой дозировочной форлы (таблетки, порошки, капсулы Или жидкие рецептуЕдд). Их готовят путем использования обычных мет-рдов для введения соединения (1) в композиции,включающие воспринимающее или растворяющее средство (эксципиент) ,с,вязу1ощее, растворитель или другие разбавители, обычно при.меняемые для фармацевтических целей, такие как лактоза, крахмал, кристаллическая целлюлоза, тальк, карбонат кальция, стеарат магния, маннит, сорбит, бензиловый спирт и вода. Дозировка и способ введения сое-, динения (I) зависят от состояния пациента, тяжести заболевания и других факторовj причем, как правило, дозировка варьируется в диапазоне от 10 до 2000 мг/день (от 100 до 1000 мг/день). Для перорального введения ввиде таблеток от 50 до 200 мл соединения (I), смешанного с подходящим фармацевтическим разбавителем, его прессуют в таблетки, причем пациенту, нуущакщемуся в лечении вводят одну или две таких таблетки один или несколько раз в день. Другие подходящие фармацевтические форма, содержшцие в качестве активного HHipeдиента соедийение формулы (I), также могут быть получены путем использования обычных методов формования лекарственных препаратов и введены пациентам в соответствующей курсу их лечения дозировке. Вместе с тем средство для ингаляции , позвояЯ1вщее осуществлять местjioe. (топическое) вйедение препарата, имеет то преимущество перед другими формами и спЬсобами введения, что в этом случае для проявления противо«аллергического эффекта достаточна дозировка 1-200 мг/день. Методика проведения медико-биоло- « гических экспериментов. . Крысиные антитела к яичному альбумину были приготовлены путем гомоло гичной сенсибилизации. 1 мг яичного альбумина и 10 кле- ток НаЁтоphi Bus pertu.ssf вводили крысам путем внутримышечных и внутрибркшинных ; инъекций (соответственно) и спустя 14 дней после инъекции у подопытных животных извлекали сыворотку. 0,1 мм этой сыворотки, разбавленной в 16 раз, инъектировали в дорсальный (спинной) участок кожного покрова крыс.. Через 48 ч после этбго каждой крысе вводили внутривенио 0,5 мл/100 г смеси, содержащей равные объемы 1%-ного раствора красителя Ехапв бВие .в физиологическом солевом растворе и 1%-ного раствора яичного альбумина в .физиологическом солевом растворе. Спустя 30 мии каждую крысу обезглавливали и флеботомировали (т.е. вскры вали вены и выпускали кровь), после чего обдирали шкурку и проводили.количественное измерение красителя, который просачивался из того места, где ранее была произведена инъекция сыворотки. Затем используя ножницы, аккуратно вырезали участки, окрашенные в голубой цвет, нарезали их на кусочки и зти кусочки погружали на ночь в 15 мл смеси, содержащей 3ч. 0,5%-ного водного раствора сульфата натрия и 7 ч. ацетона. На следующий день смесь центрифугировали в течение 10 мин при 3000 об/мин,и надосадочную жидкость {супернатант) подвергали спектрофотометрическому изме рению с целью Определения поглощения при длине волны 610 ммкм. ;Соединение (t) растворяли в физио логическом-солевом растворе.в присут ствии карбоната калия с тем, чтобы получить раствор с рН 7,5-8,5, и за- тем этот раствор либо вводили крысам внутривенно (угол производился в кры синый хвост) непосредственно перед инъекцией красителя Evans и яич ного альбумина, либо вводили перорал ьно в виде суспензии в водном растворе гуммиарабика (аравийская камеди) за 30 мин до инъекции раствора красителя Evohs БВие и яичного сшьбумина. Степень ингибирования кожной анафилаксии, выраженную в про центах, вычисляли путем сравнения поглощения красителя Evans ВСае , содержащегося в вытяжке, полученной от тех групп крыс, которым вводили исследуемое соединение формулы (I), с поглощением красителя, содержащегося в вытяжках из контрольных групп крыс. Каждая группа животных состояла из пяти крыс, для которых вычисляли среднюю степень ингибирования. В табл. 1 и 2 приведена эффективность ингибирования при внутривед1ном и пероральном введении соответственно. . Оценка, выражаемая символом ++++, обозначает эффективность ингибирования 90% или вышe +++ подразумевает степень ингибирования 70 - 90%; ++ обозначает эффективность ингибиро вания в диапазоне 50-70%; + соответствует степени ингибирования 30-50%; и + обозначает степень ингибирования в пределах 0-30%. Таблица 1 Таблиц а2 Пример 15. А. Приготовление 100-миллиграммовых таблеток. 100 г тонкодисперсного, порошкообразного этил-2-(4-карбоксибензамиrto)-4-пропирнамидобеизоата тщательно переманивают со смесью 47 г лактозы, 100 г кристаллической целлюлозы и 3 г стеарата магния, и полученную гомогенную смесь используют для прессования таблеток диаметром 9 мл каждая из которых весит 300 мг. B.Приготовление средства для ингаляции. 10 г трнкодисперсной, порсхакообразной кгшиевой соли этил 2-(4-кapбoкcибeнзclMИДo)-4-пpoпиoнaмидoбeнзoaтa растворяют в дистиллированной воде. Для регулирования рН раствора и доведения его до 8,5 используют буферную соль. Объем забуференного раствсчра доводят дистиллированной водой до 1 л. После фильтрования через мембранный фильтр с порами диаметром 0,45 мкм раствор разливают в ампулы объемом 1 мп из коричневого стекла (незаполненное раствором пространство в ампулах тщательно продувают газообразным азотом) , которые стерилизуют при 121 С в течение , 20 мии. C.Приготовление раствора для инъекций.
91026651 10
20 г натриевой соли этил 2-(4-кар-ного 1л. Посхпе фильтрования чере-
бокси6ензамидо)-4-пропионамидобен-мембранный фильтр, имеющий поры
зоата растворяют в дистиллированнойдиаметром 0,45 мкм, раствор разли воде (для инъекций). Для доведения рНвают в 2-миллилитровые ампулы из
раствора до 9г8 и создания осмотичес-коричневого стекла (незаполненное
кого давления 280 миллион/кг в раст-5 раствором пространство в ампулах
вор вводят соответствующие количест-тщательно продувают газообразным
ва уксусной кислоты и хлористого нат-азотом), которые подвергают стерилирия, после чего раствор доводят дис- зации при 121С в течение
тйллированной -водой до объема, рав-120 мин.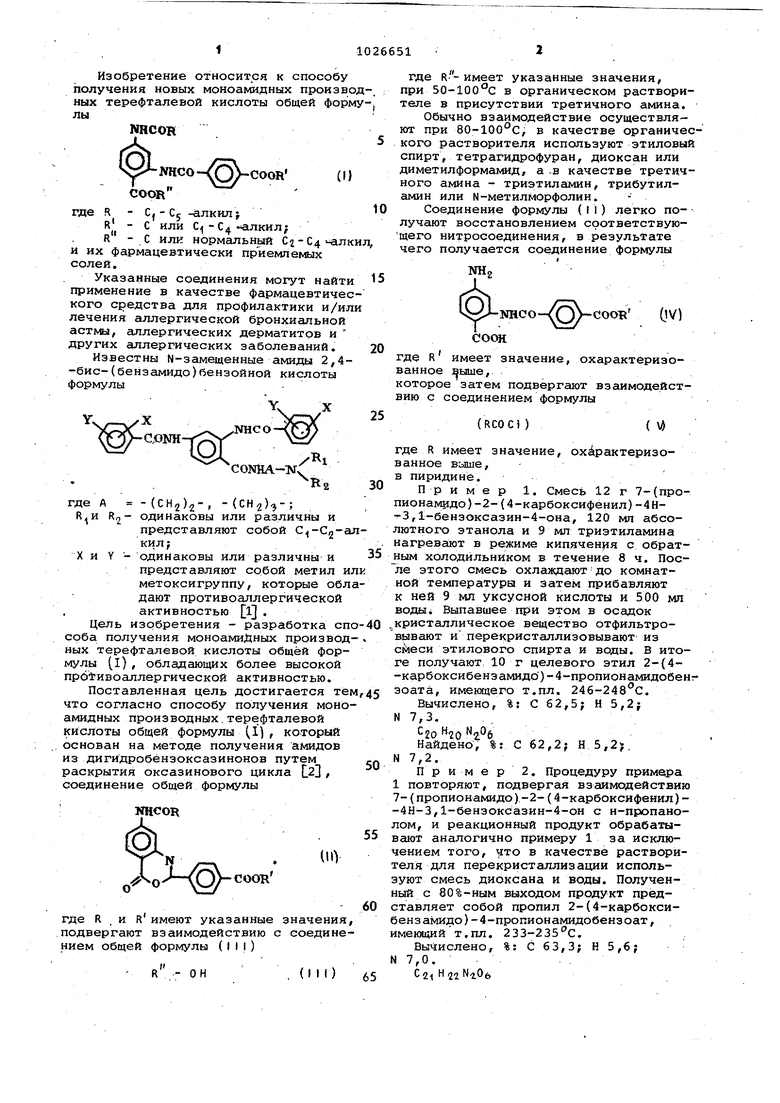



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных диоксолобензизоксазола | 1986 |
|
SU1494868A3 |
| Способ получения производных фуробензоксазола | 1986 |
|
SU1498391A3 |
| Способ получения производных фуробензизоксазола | 1989 |
|
SU1676452A3 |
| Способ получения производных пиридинтрикарбоновых кислот или их кислотно-аддитивных солей | 1986 |
|
SU1419517A3 |
| Способ получения ксантоновых производных | 1986 |
|
SU1470194A3 |
| Способ получения производных диамина | 1986 |
|
SU1500155A3 |
| Способ получения замещенных 1-алкокси- 2,4-биС-бЕНзАМидОбЕНзОлОВ | 1978 |
|
SU820660A3 |
| Способ получения 1,2-бис-(никотинамидо)-пропана или его солей с фармацевтически приемлемой кислотой | 1980 |
|
SU1053749A3 |
| Способ получения производных бис/бензамидо/-бензола или их солей | 1975 |
|
SU691083A3 |
| Способ получения производных хинолина или их солей | 1981 |
|
SU1181544A3 |
1. Способ получения моноамидных производньщ терефталевой кислоты Общей формулы NHCOR где к - -алкил; R - С; или С1-С4«алкял; Ri - С или нормальный -алкил,.. и их ф мацевтически приемлемых солей, о т л и Ч аи Ц и и с я тем, что соег нёние ббщей г 7ЩСОВ 00 COOR где кия имеют указанные значения, подвергают взаимодействшо с соединением общей формулы к - , (Hi) too || где R.имеет указанные значешяя, щ)и 50-100 с в сч)гайическом растворителе в присутствий третичного амина. : 2.Способ по П.1, о т л и чаю щи и с я тем, что взаимодействие осуществляют при 80-100с. 3.способ йо n.l, о тли ч а ю - to щи и с я тем, что в качестве оргаО) нического раство И|теля используют этилош й спирт, тетрагидроф ран, о: диоксан или диметилформгшид. ел 4.Способ ПО П.1, о т л и ч а ю щ и и с я TiaM, в качестве третичного ateiHa используют тризтил aMiH, трибутил/аши или N-мётилмор-, фолин. 
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Способ получения -замещенныхАМидОВ 2,4-биС(бЕНзАМидО)-бЕНзОй-НОй КиСлОТы | 1978 |
|
SU812170A3 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Чугунный экономайзер с вертикально-расположенными трубами с поперечными ребрами | 1911 |
|
SU1978A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Запальная свеча для двигателей | 1924 |
|
SU1967A1 |
Авторы
Даты
1983-06-30—Публикация
1979-12-04—Подача