Изобретение относится к способу получения новых водорастворимых и стабильных формполиеновых антибиотиков, а именно к способу получения комплексов пслиеновый антибиотик-Х - -циклодекстрин (J-ЦЦ).
Цель изобретения - получение новых производных полиеновых антибиотиков, обладающих большей растворимо- стью в воде при сохранении химической и биологической стабильности, по сравнению с исходным антибиотиком.
Способ осуществляют следующим образом.
Пример 1. Получение комплекса флавофунгина . с J-циклодекстри- ном в гомогенной фазе.
22 г f -циклодекстрина (содержание 130ДЫ 1,5%) при 30°С растворяют в 500 мл дистиллированной воды и к раствору добавляют 2,5 г (3,85 ммоль твердого флавофунгина. Раствор в течение 3 ч интенсивно перемешивают, затем отфильтровывают и полученный интенсивно-желтого цвета фильтрат лиофилизуют. Получают 21 г продукта, спектрофотометрически измеренное содержание флавофунгина в котором составляет 9,3%. Это соответству ет примерно 80% используемого количества флавофунгина. Комплекс пред- ставляет собой рыхлый желтый порошок 100 мг комплекса растворяется в 2,5м
дистиллированной воды при 50 С мгно- .
венно с образованием прозрачного раствора. Этот раствор содержит 3,5 мг/мл флавофунгина и при хранении в течение 6 дней при комнатной температуре и на рассеянном свету не претерпе- вает никаких обнаруживаемых химическим или физическим путем изменений. . Максимальная растворимость наступает при содержании равном примерно 4% (концентрация флавофунгина 4 мг/мл), поэтому путем лиофилиза- ции этого раствора получается комплекс самого предпочтительного соста- ва (9-10 вес.% биологически активного вещества).
Термогравиметрические измерения, исследования с помощью дифференциально-сканирующего калориметра (ДСК) и термодеструктивного анализа (ТДА) - (Tmermal Evolution Analyse) показы- вают характерную разницу между флаво- фунгином, комплексом флавофунгина с у-ЦЦ и смесями из флавофунгина -ЦЦ, Флавофунгин при 100 С теряет
Q
5
0 5 о
5
Q З 0
7% своей массы (на основании ТДА-кри- вой выделяются органические вещества), выше 100°С он начинает разлагаться и до 300 С теряет 24% своей массы. Лиофилизированная проба из флавофунгина и у -ЦД получается в виде комплекса вследствии того, что вплоть до не теряет никаких органических веществ и в ДСК-кривой между 100 и не появляется характерное для окисления флавофунгина экзотермическое изменение, однако, при 263°С появляется характерный для экзотермического процесса пик, который указывает на окисление вьделяющегося из комплекса флавофунгина.
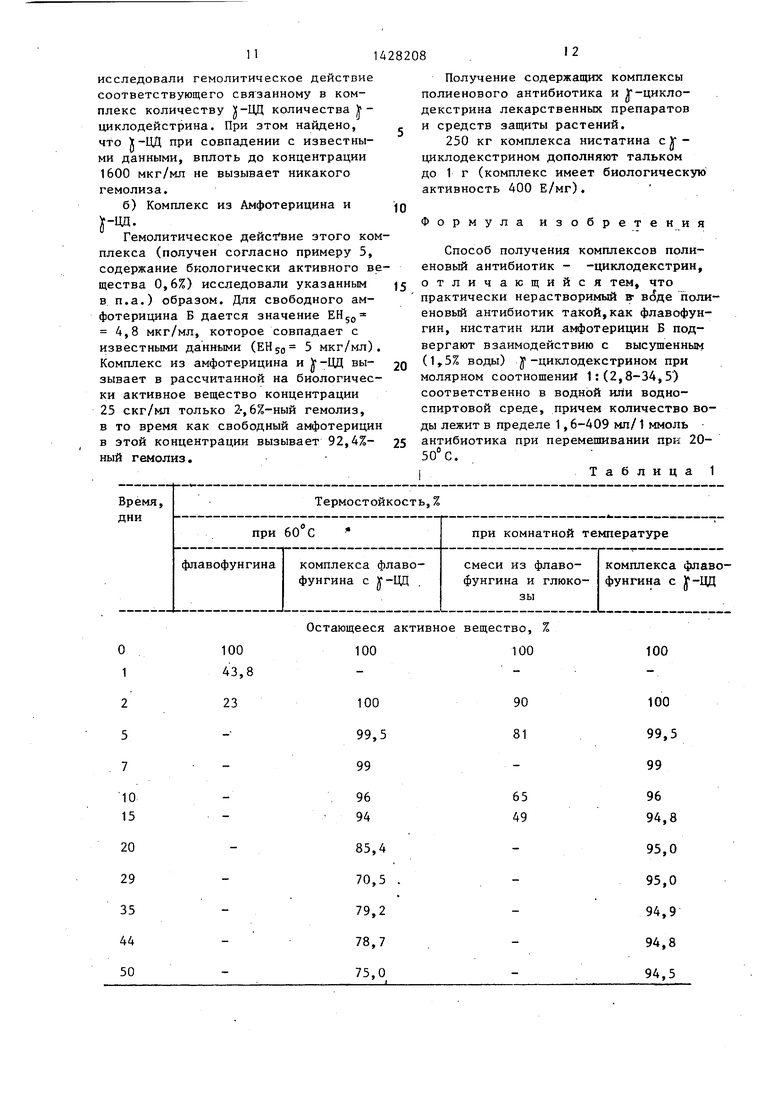
Дпя исследования термостабильности комплекса флавофунгина с J-ЦЦ вещества ТОЛ11ЩНОЙ слоя 1 мм помещали на часовые стекла и,не защищая от света воздуха, хранили при комнатной температуре и при 60°С в сушильном шкафу. Пробы, отобранные в.различные моменты времени, анализировали спектрофотометрически.
На основании химических измерений найдено, что не включенный в комплекс флавофунгин Через 24 ч при 60 С претерпевает сильное разложение (это подтверждено также путем снятия полного УФ-спектра). Содержание биологически активного вещества в комплексе флавофунгина с у-ЦД через 50 дней становится равным примерно 75%. Содержащая 10% флавофунгина, приготовленная с глюкозой физическая смесь теряет при 14-дневном хранении при комнатной температуре 50% биологически активного вещества. Содержание биологически активного вещества в комплексе через 50 дней больше 95%. Хра- нивщаяся в закрытом сосуде при +4 С в течение 7 мес проба не показывала потерь биологически активного вещества.
Результаты измерений представлены в табл. 1 (термостойкость выраженная в процентах первоначального содержания биологически активного вещества),
Микробиологическое оценочное Измерение также подтвердило, что флавофунгин в форме J -ЦЦ-комплекса намного стабильнее. Комплекс флавофунгина с У-ЦД хранили при комнатной температуре и при , Противогрибковое . действие было точно таким,, как и первоначальное (М1С-значение хранившегося в атмосфере азота в холодильнике
пробы флавофунгина мкг/мл исследовались на тест-микроорганизмах. S. cerevLsial, с. albicans, с. pseu- dotropicals и с. orusei.
Пример 2. Получение комплекса флавофунгкна с У-ЦЦ, в гетерогенной фазе.
9г J-циклодекстрина (содержание воды 1,5%) гомогенизируют в фарфоровой ступке с 1 г флавофунгина при комнатной температуре., Смесь суспендируют в 5 мл 50%-ного этанола. Суспензия через несколько минут перемешивания внезапно становится твердой. Пастообразное вещество размазывают по ширине до тонкого слоя и в течение нескольких часов высушивают в вакуумном эксикаторе. Затем твердый комплекс измельчают в порошок. Получают 10 г продукта с 10 вес.% биологически активного вещества.
Продукт изучают на термостойкость При этом находят, что комплекс как лиофилизированный комплекс обладает повышенной термостойкостью и его противогрибковое действие не уменьшается.
На снимках рентгенодифракционного анализа превращенного в порошок комплекса проявляются характерные пики рефлекции при значительно отклоняющейся (20) величине угла в другом месте, чем в случае физической смеси подобного состава, что свидетельствует о другой кристаллической решетке и подтверждает факт комплексо- образования. Рентгенодифракционный снимок лиофилизированного комплекса флавофунгина с J-ЦД указывает на аморфную структуру.
Пример 3. Получение комплекса нистатина с в гомогенной фазе.
10г J-ЦЦ (содержание воды 1,5%) при 50 С растворяют в 90 мл дистиллированной воды. К раствору добавляют
2 г (2,16 ммоль) нистатина (биологическая активность 5033 Е/мг). Раство интенсивно перемешивают в течение 15 мин. После отфильтровывания осадк желтого цвета раствор лиофилизируют. Получают 10 г продукта, спектрофото- метрически определенное .содержание нистатина в котором составляет 8%. Биологическая активность 399 Е/мг. Комплекс нистатина с представляет собой светло-желтый рыхлый порошок, который быстро растворяется в
8
воде при-комнатной температуре с образованием прозрачного раствора.Концентрация нистатина в растворе 8- 9 мг/мл,что соответствует примерно 100 мг комплекса на мл раствора. Биологическое оценочное определение комплекса показывает, что биологическая активность исходного нистатина
сохраняется.
Термогравиметрические измерения, исследования с помощью дифференциально-сканирующего калориметра (ДСК) и термодеструктивного анализа (ТДА)
показывают характерное различие между нистатином, комплексом -нистатина с Х-ЦД и смесью нистатина с V-ЦЦ. Нистатин содержит 3% воды, которую отдает вплоть до (TG-кривая) .
Разложение веЕцества начинается при 150 С с экзотермическим процессом (в ДСК-кривор пик при 165 С, при потере в весе 8% - TG-кривая), затем протекает медленное разложение, и
при 350 С измерима массовая потеря 54%, Хотя разложения нистатина . Х-ЦЦ в отношении температуры совпадают, однако есть некоторые отклонения в термоциклических кривых комплекса в смеси, которые в лиофили- зате делают вероятным наличие комплекса. В ТДА-кривой отсутствует острый пик при ТбО С, который указы- вает на улетучивание органических
ве.ществ. В ДСК-кривой не проявляет- с,ч характерного для разложения нистатина экзотермического пика (лишь при температуре 200 С). В TG-кривой различие проявляется в том, что лиофилизированная проба вьппе 250 С разлагается быстрее, чем физическая смесь. Комплексообразование нистатина с Х-ЦД также подтверждается ЯМР-ис- следованиями.
Стабильность приготовленных из лиофилизированной пробы комплекса нистатина с )f-im растворов иссл.едова- ли следующим образом.
Из содержащего 8% биологически активного вещества готовили водный раствор концентрации 5 мг/мл. Рас твор хранили при комнатной температуре незащищенным от света. В разичные моменты времени спектрофото- метрически контролировали содержание биологически активного вещества в растворах.
, дниКонцентрация нистатина мг/мл
05,0
14,8
24,75
54,70
64,6
74,55 - 84,5
104,5
124,5
214,1
Растворы на второй день начинают опалесцировать. Отбор проб осуществляли после встряхивания раствора. Пробу разбавляли 400-кратным количеством этилового спирта и затем фо- тометрировали. Расчет осуществляли из имеющихся (кажущихся) при Л„д, 304±1 величин экстинкции.Послехра- нения в течение 3-х недель водного раствора еще имеется свыше 80% всего количества биологически активного вещества. Высоким значениям экстик- ции принадлежат высокие значения ак- тивности,
Пример 4. Получение комплекса нистатина с J-циклодёкстри- ном в гетерогенной фазе.
. 9 г J-циклодекстрина (содержание воды 1,5%) и 1 г нистатина (биологическая активность 5033 Н/мг) гомогенизируют друг с другом в фарфоровой ступке при комнатной температуре Полученную смесь суспендируют в 6 мл 50%-ного этанола. Через несколько минут суспензия внезапно становится твердой. Вещество размельчают и для удаления следов воды и растворителя сушат в эксикаторе над пентоксидом фосфора. На следующий день твердый комплекс измельчают в порошок. Получают продукт с содержанием биологически активного вещества 10 вес.% (биологическая активность 45 Е/мг).
Полученный комплекс.при термоаналитических исследованиях по сравнению со смесью показывает такие же отклонения, как и приготовленный по примеру 3 путем лиофилизации комплекса. -Исследовали растворимость соотвествующего количеству биологически активного вещества 10 мг/мл количества комплекса нистатина с у-ЦД .и основ- ного нистатинового материала в 15 мл дистиллированной воды при 37 С. Растворы перемешивали с помощью магнитной мешалки, совершающей 150 оборо
тов в минуту, в различные моменты времени отбирали пробы, отфильтровывали и исследовали спектрофотометри- чески содержание в них биологически активного вещества.
ремя,мин
2
5
15
40
60
90
Комплекс нистатина с Y -ЦЦ, мг/мл
-9,0 7,2 7,8
7.А
7,2 .
6,0
5 0
0 5 5
г
0
0
Спектр отобранных из водной суспензии основного нистатинового материала проб не оценивали. Спектр отобранной в течение первых 5 мин пробы идентичен спектру нистатина, позднее наблюдается прогрессирующее рас- ложение. Сначала деформировался максимум около 290 нм и затем полностью исчез, и в области меньших длин волн появился новый максимум, что позволяет сделать вывод о повреждении конъю- гированной аморфной системы.
Пример. Получение комплекса нистатина с jC-Iffl в гетерсггенной фазе путем лиофилизации.
8 г у-ЦД (содержание воды 1,5%) при 40 С растворяют в 80 мл воды и к раствору добавляют 2 г (1,16 ммоль) нистатина. Суспензию перемешивают в течение 24 ч при 40 С, затем смесь обезвоживают путем лиофилизации. Получают в виде желтого рыхлого порошка 10 г продукта, спектрометрически измеренное содержание биологически активного вещества в котором состав- |Ляет 20%. Биологическая активность 950 Е/мг. .
В продукте мольное соотношение между нистатином и -ЦЦ составляет 1:3. Согласно рентгенодифрактомет- рическим исследованиям комплекс имеет аморфную структуру. Обработанное таким же образом, но без р-ЦД, основное вещество сохраняет свой кристаллический характер, его рентгено- дифрактограмма полностью идентична таковой основного вещества, а биологическая активность значительно хуже. Если получают описанным образом комплекс с более высоким содержанием биологически активного вещества, то рентгеаодифрактограмма показывает характерный для кристаллического нистатина пик.
Для исследования растворимости комплекса 500 мг его перемешивают в течение 5 мин в 10 мл воды при комнатной температуре. В фильтре спе трофотометрически обнаружена концентрация нистатина 4,5 мг/мл.
Пример 6. Получение комплекса амфотерицина Б с у-ЦД.
10 г У-циклодекстрина (содержание воды 1,5%) растворяют в 90 мл дистиллированной воды г1ри 37 С, К раствору добавляют 200 мг амфотерицина Б. Смесь интенсивно перемешивают 2 ч, затем отфильтровьтают оса- док желтого цвета, фильтрат лиофили- зируют.Получают Юг продукта, спек- трофотометрически измеренное содержание амфотерицина Б в котором составляет 0,6-0,8 вес.%. Комплекс представляет собой желтый рыхлый порошок, которьм в воде быстро растворяется с образованием прозрачного раствора. Полученный раствор имеет концентрацию 0,6-0,8 мг/мл амфотерицина Б и может неограниченно разбавляться водой или физиологическим раствором хлорида натрия без выпадения в осадок твердого вещества или помутнения раствора.Раствор хранят при комнатной температуре в течение 6 дней и спектроскопически исследуют: содержание в нем биологически активного вещества неизмененное.
.Пример 7. Определение противогрибкового действия полученных комплексов как тотчас после получения, так и после хранения в условиях, при которых не .защищенное за счет ком- плексообразования биологически активное вещество претерпело уже значительные потери активности.
а) Комплекс флавофунгина с г-цик- лодекстриноМо
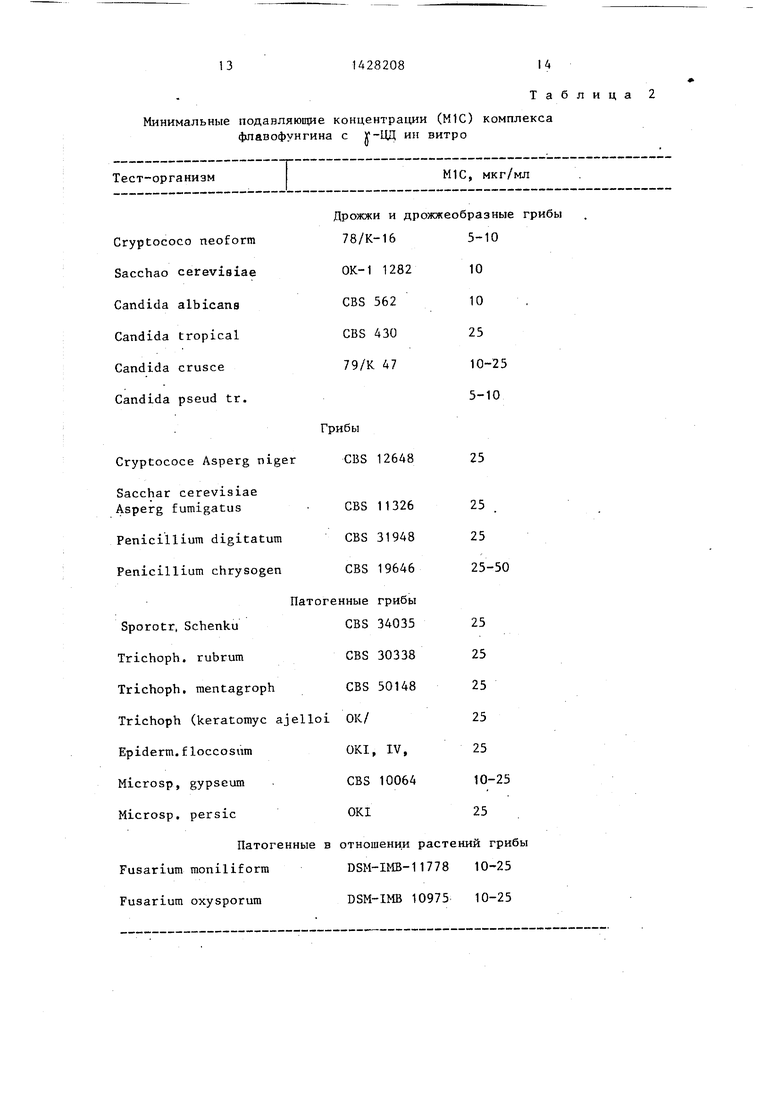
Противогрибковое действие водного раствора этого комплекса исследовались на 6 бактериях и 13 гифоми- цетах.
Результаты представлены в табл. 2
В расчете на флавофунгин минимальная подавляющая концентрация в каждо случае бьша 10-25 скг/мл, что соотвествует активности не связанного комплексно биологически активного вещества. Особенно нужно отметить, что вещество активно также против фито- патогенных грибков, т.е. применение против грибковых поражений растений
0
0
5
5
0
5
0
5
0
5
обосновано. Комплексносвязанное биологически активное вещество действует в такой же концентрации, как к флавофунгин. Исследования осуществляли методом диффузии на агаре. Комплекс имеет то преимущество, что для приготовления растворов не требуется никаких энергетических растворителей (ЛМФ или ШСО) . Эти растворители действуют иманно подавляюще на некоторые грибы, поэтому при измерениях нужно уменьшать концентрацию растворителя путем рабавления водой до значения, не действующего з же подавляющее. На практике, например, допуст14ма концентрация ДМСО ниже 1%. Некоторые полиены, склонны к осаждению при такого рода разбавлении, т.е. при приготов- левии нeoбxoди aк для исследований растворов часто сталкиваются с препятствиями. Рекомендуется вещество превращать в порошок и приготовление раствора, а также его разбавление . водой осуществлять всегда непосрдд- ственно перед измерением.
Концентрация флавофунгина в каждом случае составляет 10-25 мкг/м.п. Появляющиеся при приготовлении раствора из флавофукгина проблемы беспредметны при применении комплекса.
б)Комплекс нистатина с У-ВД. Биологическое оценочное измере™
ние осуществляли с помощью агар-диф- фузионного метода при применении Candida albicans в качестве тест- организма. Комплексы растворяли только в воде, нистатин - в содержащем хлорид кальция метаноле.
Растворы разбавляли водой, Спектрофотометрически измеренное содержание биологически активного вещества и биологическая активность некоторых комплексов показаны э табл. 3. .
Используемое для комппексообразо- вания основное нистатиновое веще™ ство имело биологическую активность . 5033 Е/мг.
в)Комплекс змфотеридина Б с У-ЦД, Противогрибков то активность этого комплекса исследовали с помощью агар-диффузионного метода и Candida albicans в качестве тест-организма. По отношению к амфотерицину Б минимальная подавляющая концентрация бьта меньше 5 мкм/мл, что соответствует активности не связанного ком-
плексно биологически активного вещества.
Пример 8. Изучение поглощения (всасывания) комплексов полиено- ;вых антибиотиков с циклодекстрином.
а) Поглощение (всасываемость) нистатина из применяемого перорально комплекса Нистатина с .
Всасывание биологически активного вещества исследовали на мышах, на модели сепсиса, вызванного путем внутривенного введения суспензии Candida albicans. Сепсис в течение 2-3-х дней :вызывал смертность. Подопытные животные получали перорально приготовленный по примеру 3, содержащий 8% нистатина сомплекс. В параллель- ном опыте нистатин вводили внутривенно. Для обеих групп определяли в расчете на необработанный контроль удлинение продолжительности жизни (см.табл.4).
Если сравнивать применяемые в виде комплекса перорально дозы нистатина с вводимыми внутривенно дозами нистатина , которые вызывают примерно равн ое удлинение продолжительности жизни (табл. 4), последний столбец, то можно сделать вывод, что из комплекса в среднем в кровеносное русло попадает 6,2% биологически активного вещества. В случае более высоких доз (внутривенно 1,56 мг/кг, перорально 25 мг/кг) уменьшение продолжительности жизни сводится к слабой токсичности нистатина.
б) Всасывание нистатина из подкожно вводимого комплекса нистатина с
j-цц.
Самок CFI-крыс со средним весом 180 г обрабатьшают нистатином, комплексом нистатина с )-ЦЦ (содержание биологически активного вещества 8%) и )t -ЦЦ. Для этого из исследуемых веществ с помощью содержащего Твин 8 физиологического раствора хлорида натрия готовят суспе нзию и вводят ее . подкожно. Связь между дозами и смертностью представлена в табл. 5.
Из обработанных комплексом животных при дозе 20 мг/кг 90% погибает в течение 48 ч, из обработанньк свободным нистатином животных при дозе 150 мг/кг в течение недели наблюдения не погибает ни одного. Для контроля 10 животным подкожно вводили столько у-ЦД, чтобы получить погиба0
5
0
5
0
5
0
5
0
5
ющую на 90% группу с помощью комплекса (302 мг/кг). В течение недели наблюдения не погибло ни одного животного.
Из табл. 5 видно, что из комплекса нистатина с J-ЦД при подкожном введении поглощается токсическая доза, в то время как свободный нистатин при подкожном введении вооё- ще не поглощается или всасывается только в допустимой незначительной мере.
Всасываемость исследовали также путем измерения уровня его в крови, так как поглощенный, попавший в кровеносное русло, нистатин обнаруживается в УФ-спектре сыворотки крови. При подкожном введении свободного нистатина дозой 200 мг/кг в крови ничего не обнаружено, в то время как комплекс уже при дозе 20 мг/кг дает.хорошо измеряемый уровень в крови через: 2-4 ч после введения в крови было обнаружено 6-10 мкг/мл.
Пример 9. Снижение гемо- лизирующего действия полиеновых антибиотиков путем комплексвобразова- ния с у-ЦД.
а) Комплекс нистатина с -1Ш,Гемолитическое действие нистатина, комплекса нистатина с у-ЦД (содержание биологически активного вещества 8%) и )р-1Щ исследовали на приготовленных из человеческой крови суспензиях красных кровяных телец по методу Т. Tru и др. (J. Pharm Dyn 6, 408-114, 1983). Результаты указываются в форме относяш 1хся к 50%-ному гемолизу концентраций (). Полученное для свободного нистатина значение (ЕН 57 мкг/мл) показывает совпадение с известным значением EHso 50 мкг/мл (J. Antibiotus, 22, 1080-1081, 1979). Для комплекса нисиатина с . -ЦД, в расчете на биологически активное вещество найдено значение ЕНуд 115 мкг/мл, т.е. комт плекс снижает гемолизирующее действие нистатина наполовину. При исследовании концентрированной зависимости гемолитического действия обнаруживается, что комплекс нистатина с )г-ЦД вплоть до концентрации 70 мкг/мл нистатина практически.не действует гемолитически, в то время как свободный нистатин в этой концентрации вызывает уже 70%-ный гемолиз. Также
исследовали гемолитическое действие соответствующего связанному в комплекс количеству (-ЦЦ количества V- циклодейстрина. При этом найдено, что Х-ЦД при совпадении с известными данными, вплоть до концентрации 1600 мкг/мл не вызывает никакого гемолиза.
б) Комплекс из Амфотерицина и
1-1Щ,
Гемолитическое дейст вие этого комплекса (получен согласно примеру 5, содержание биологически активного вещества 0,6%) исследовали указанным в п.а.) образом. Для свободного ам- фотерицина Б дается значение EHj 4,8 мкг/мл, которое совпадает с известными данными (ЕН5о 5 мкг/мл). Комплекс из амфотерицина и V-ЦД вы- зывает в рассчитанной на биологически активное вещество концентрации 25 скг/мл только 2-,6%-ный гемолиз, в то время как свободный амфотерицин в этой концентрации вызывает 92,4%- ный гемолиз.
Получение содержащих комплексы полиенового антибиотика и )-цикло- декстрина лекарственных препаратов и средств защиты растений.
250 кг комплекса нистатина cY - циклодекстрином дополняют тальком до 1 г (комплекс имеет биологическую активность 400 Е/мг).
Формула изобретения
Способ получения комплексов поли- еновый антибиотик - -циклодекстрин, отличающийся тем, что практически нерастворимый в- воде поли еновый антибиотик такой,как флавофун- гин, нистатин или а1 |1отерицин Б подвергают взаимодействию с высушенным (1,.5% воды) J -циклодекстрином при молярном соотношения 1:(2,8-34,5) соответственно в водной или водно- спиртовой среде, причем количество воды лежит в пределе 1,6-409 мл/1 ммоль антибиотика при перемешивании при 20- 50 С. IТ а б л и ц а 





| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения вещества, обладающего гормональным действием | 1972 |
|
SU624562A3 |
| Способ получения комплексов включения 7-изопропоксиизофлавона | 1986 |
|
SU1757472A3 |
| Способ получения комплексов включения циклодекстринов | 1981 |
|
SU1269738A3 |
| Композиция для получения ароматизатора чая | 1981 |
|
SU1382392A3 |
| Способ получения 2-[(3-метилксантинил-7)метил]-1,3-диоксалана | 1988 |
|
SU1598878A3 |
| Способ получения полиоксиметиленовой композиции | 1978 |
|
SU784758A3 |
| Способ получения @ -замещенных 3-циклоалкилсульфонилпирролидиндионов-2,5 | 1981 |
|
SU1156594A3 |
| Способ получения производных угольной кислоты | 1982 |
|
SU1186085A3 |
| Способ получения 4-тиа-или 4-сульфинил- @ производных | 1981 |
|
SU1053746A3 |
| Способ получения кормовой смеси | 1980 |
|
SU1544171A3 |
Изобретение касается производных Сахаров, в частности способа получения комплексов полиенового антибиотика с у -циклодекстрином, обладающих биологической активностью, что может быть использовано в медицине. Цель изобретения - создание новых веществ указанного класса, обладающих боль- шей растворимостью в воде при сохранении химической и биологической активности. Процесс ведут обработкой практически нерастворимого антибиотика, такого как флавофунгин, нистатин или амфотерицин Б с. помощью высушенного (1,5% воды) у -циклодек- стрина при мольном соотношении 1: :(2,8-34,5) в водной или водно-спир- товой среде при соотношении 1,6- 409 мл на 1 ммоль антибиотика, перемешивании при 20-50 0. Новый комплекс, например, с флавофунгицэдом имеет растворимость в воде до 4%, содержание в нем активного вещества составляет 75% после 50-дневного нагревания до 60° С -при минимальной подавляющей концентрации в отношении различных дрожжей и грибов (5-50) мкг/мл. 5 табл. § СО Ци N5 X) N0 D Х
100
Остающееся активное вещество, 100100
100
Таблица 2
Минимальные подавляющие концентра1Ц€И (М1С) комплекса флавофунгина с витро
Тест-организм
М1С, мкг/мл
co neoform cerevisiae albicans tropical crusce pseud tr.
Дрожжи и дрожжеобразные грибы 5-10
78/К-16 ОК-1 1282 CBS 562 CBS 430 79/К 47
10
10
25
10-25
5-10
Грибы Cryptococe Asperg niger CBS 12648
Sacchar cerevisiae Asperg fumigatus
Penicillium digitatum Penicillium chrysogen
Sporotr, Schenku
Trichoph. rubrum
Trichoph. mentagroph Trichoph (keratomyc a
Epiderm.floccosum
Microsp, gypseum
Microsp. persic
Патогенные в отношении растений грибы Fusarium moniliform DSM-IMB-11778 10-25
Fusarium oxysporum
DSM-IMB 10975 10-25
ожжеобразные 5-10
10
10
25
10-25
5-10
25
25 25 25-50
25
25
25
25
25
10-25
25
15
ВНИИПИ Заказ 4870/59 Тираж 348
Произв.-полигр. пр-тие, г. Ужгород, ул. Проектная, 4
142820816
Таблица 3
Таблица 4
Таблица 5
Подписное
| Hammond S.M | |||
| Biological Activity of Polyene | |||
| - Antibiotics Progress in Medical chemistry, т | |||
| Паровоз для отопления неспекающейся каменноугольной мелочью | 1916 |
|
SU14A1 |
| North - Holland Publishing Company, 1977, p | |||
| Транспортер для перевозки товарных вагонов по трамвайным путям | 1919 |
|
SU105A1 |
Авторы
Даты
1988-09-30—Публикация
1984-12-28—Подача