Изобретение относится к органической химии, конкретно к новому способу получения бензимидазолхалькогенонов-2 общей формулы I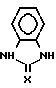
где а) X Se
б) X S
которые могут найти применение в качестве стабилизаторов полимеров, компонентов фотокомпозиций, ускорителей вулканизации каучуков, антиоксидантов, аналитических реагентов.
Известен способ получения бензимидазолтиона-2, 1б заключающийся во взаимодействии о-фенилендиамина (II) с тиомочевиной при повышенных температурах (170 180oC)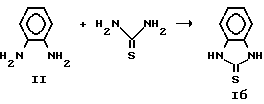
Способ позволяет получать бензимидазолтион-2 1б с выходами 70 80%
Однако, бензимидазолселенон-2 1а исходя из селеномочевины получить таким образом не удается, вследствие окислительного выделения селена при повышенных температурах.
Известен также способ получения бензимидазолтиона-2 1б, состоящий во взаимодействии о-фенилендиамина с роданистым калием в кислой среде, позволяющий получить соединение 1б с выходом 80%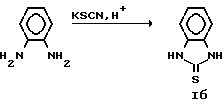
Однако и этим способом исходя из селеноцианата калия не удается получить бензимидазолселенон-2 1а, вследствие выделения селена в ходе реакции в водной среде.
Этот недостаток устраняет промышленный способ получения тиона 1б и единственный продуктивный лабораторный способ получения селенона 1а, включающий взаимодействие халькогеноуглеродов CX2(X Se, S) с о-фенилендиамином II в водной или спиртовой среде
Способ позволяет получать тион 1б с высокими выходами 85 90% при относительно низких температурах (70 80oC). Селенон 1а получается в аналогичных условиях с выходом 85%
Способ наиболее близок по технической сущности и достигаемому результату к заявляемому (принят в качестве прототипа).
Недостатками способа-прототипа являются следующие.
Применение высокотоксичных и огнеопасных халькогеноуглеродов. Сероуглерод способен самопроизвольно воспламеняться на воздухе и в этом отношении весьма опасен. Кроме того, он является кровяным ядом. Еще более токсичен селеноуглерод, который к тому же является одним из самых зловонных из известных органических соединений. Высокие огнеопасность и токсичность селеноуглерода исключают возможность освоения метода в промышленности. Синтез последнего из товарного дихлорметана и селена также осложняется применением высоких температур ( приблизительно 500 600oC), что крайне неэкономично.
Низкие выходы селенона 1а при получении из товарного сырья. По известным методам для получения соединения 1а проводится синтез селеноуглерода из товарных дихлорметана и селена (выход 27%). Общий выход по двум стадиям 23%
Бензимидазолселенон 1б, полученный по известному способу, характеризуется низкой чистотой, так что соединение становится малоустойчивым, подверженным окислению кислородом воздуха.
Целью изобретения является создание нового способа получения бензимидазолхалькогенонов-2, исходя из низкотоксичного и неогнеопасного сырья, что в целом упрощает процесс и улучшает его экологию.
Поставленная цель достигается новым способом получения бензимидазолхалькогенонов-2, 1б, включающем превращение о-фенилендиамина (II) и отличающимся тем, что взаимодействие проводится с халькогенами (серой или селеном) в двухфазной системе хлороформ водная щелочь при температуре 50 - 65oC.
Способ отличается также тем, что для достижения наиболее высоких выходов целевых продуктов применяют катализ реакции не менее 3 мол. четвертичных аммониевых солей.
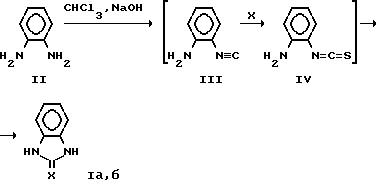
Описанная реакция, в которой генерируется карбен, по-видимому, протекает через промежуточные аминоизонитрилы III и аминоизохалькогеноцианаты IV. Однако, вероятен также путь через халькогенофосгены CXCl2, образующиеся в реакционной среде из соответствующих карбенов и халькогенов с последующей конденсацией с о-фенилендиамином II. Не исключена возможность параллельного протекания обоих потоков, регулируемых условиями синтеза.
В ходе превращения достигаются высокие выходы селенона 1а (95% в расчете на прореагировавший селен и 48% на диамин II) и тиона 1б (75% в расчете на диамин II), причем выход первого значительно выше, чем по способу прототипу, составляющему лишь 23%
Соединения 1а, б идентифицированы по отсутствию депрессии температуры плавления в пробах смешения образцов веществ, полученных новым и известными способами, а также сопоставлением их ИК и ПМР спектров, величин Rf.
Проведение реакции при температурах ниже 50oC, в частности 40oC, технологически нецелесообразно, т. к. приводит к сильному уменьшению выходов халькогенонов (до 6 10%). При температурах выше 65oC требуется применение автоклавов, что нетехнологично. Лучшие результаты по выходам целевых продуктов получены при температуре 65oC (48% для селенона 1а, 75% для тиона 1а).
Применение четвертичных аммониевых солей в качестве катализаторов межфазного переноса позволяет увеличить выход селенона 1а с 18 до 48% При достижении концентраций солей 3 мол. выход халькогенонов-2 1а, б уже не возрастает. Однако увеличивается скорость процесса, так, при содержании тетраэтиламмонийхлорида 10 моль реакция завершается при 65oC за 3 ч. Поэтому содержание катализатора в синтезе строго не ограничено, но реально применяется не более 100 моль солей, что соответствует стехиометрическим отношением реагентов.
Пример 1. Получение бензимидазолселенона-2 1а. В колбу емкостью 1,5 л, снабженную мешалкой и обратным холодильником, загружают 108 г (1 моль) о-фенилендиамина, 80 г (1 моль) селена в виде пудры, 5 г тетраэтиламмоний хлорида, 160 мл хлороформа и нагревают на водяной бане при 70oC до интенсивного кипения хлороформного раствора (внутренняя температура 65oC). К содержимому колбы прикапывали при интенсивном перемешивании 220 г едкого натра в виде 50% водного раствора в течение 5 ч. После этого перемешивают еще 2 ч и,не прекращая перемешивания, обратный холодильник заменяют на прямой и отгоняют остаток хлороформа в течение 1 ч. К содержимому колбы добавляют 700 мл воды и при интенсивном перемешивании медленно доводят pH раствора до 2, концентрированной соляной кислотой, суспензию охлаждают до комнатной температуры, фильтруют, промывают 200 мл 5%-ной соляной кислоты и 400 мл воды. Влажный продукт перемешивают с 40 г едкого натра в 600 мл воды при 70 - 80oC 20 мин, охлаждают, отфильтровывают непрореагировавший селен, подкисляют уксусной кислотой до легкого помутнения и вновь фильтруют. Фильтрат обрабатывали углем (2 г) и нейтрализовали концентрированной соляной кислотой при 90oC. Охлаждают, бензимидазолселенон 1а отфильтровывают, сушат на воздухе. Получают 95 г (48% или 95% на прореагировавший селен) темно-желтого порошка, Т.пл. 235oC (с разлож. из этанола) Rf 0,52, не дает депрессии температуры плавления с образцом соединения, полученным согласно [4]
Пример 2. Проводят аналогично примеру 1, но с 54 г (0,5 моль) о-фенилендиамина и 16 г (0,5 моль) серы. Выход бензимидазолтиона-2 1б 56 г (75%). Т. пл. 298 300oC (из этанола), Rf 0,52. Идентичен с образцом вещества, полученным согласно [3]
Пример 3. Проводят аналогично примеру 1, но при 50oC в течение 10 ч. Выход селенона 1а 70,9 г (36%) в расчете на амин. Т.пл. 234 237o Rf 0,52.
Пример 4. Проводят аналогично примеру 2, но при 50oC в течение 10 ч. Выход тиона 1б 34,5 г (46%). Т.пл. 298 300oC. Rf 0,52.
Пример 5. Проводят аналогично примеру 1, но с 8,27 г (0,05 моль) тетраэтиламмонийхлорида. Выход селенона 1а 94,6 г (48%). Т.пл. 234 - 237oC. Rf 0,52.
Пример 6. Проводят аналогично примеру 1, но с 11,37 г (0,05 моль) бензилтриэтиламмонийхлорида. Выход селенона 1а 86,7 г (44%). Т.пл. 234 - 236oC. Rf 0,52.
Пример 7. Проводят аналогично примеру 1, но без катализатора. Выход селенона 1а 35,5 г (18%). Т.пл. 233 236oC. Rf 0,52.
Заявляемый способ имеет следующие технико-экономические преимущества перед способом-прототипом.
Способ позволяет избежать применения высокотоксичных и огнеопасных халькогеноуглеродов. В заявляемом способе используются хлороформ популярный органический растворитель с относительно низким уровнем токсичности, (который применялся ранее при хирургических операциях в составе средств наркоза), сера и селен малотоксичные и нелетучие вещества, не имеющие запаха.
Значительно (с 23 до 95%) возрастает выход селенона 1а. Непрореагировавший селен может быть направлен в синтез повторно.
Селенон 1а получаемый по предлагаемому способу, отличается повышенной чистотой и, как следствие, стабильностью при хранении (не окисляется под действием кислорода воздуха: срок хранения не менее 1 года).
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения бензо-2,1,3-тиадиазола | 1983 |
|
SU1114677A1 |
| Способ получения 1,1-дигалоген2,6-дигалогенметил-1,4-селен (теллур)оксанов | 1976 |
|
SU685663A1 |
| Способ получения 1-(2,3-эпитиопропил)-3-(2,3-эпоксипропил)-бензимидазолона-2 | 1988 |
|
SU1574600A1 |
| 1,2-БИС-(1-ГЛИЦИДИЛБЕНЗИМИДАЗОЛ-2-ИЛТИО)ЭТАН В КАЧЕСТВЕ СООТВЕРДИТЕЛЯ ЭПОКСИДНЫХ СМОЛ И 1,2-БИС-(БЕНЗИМИДАЗОЛ-2-ИЛТИО)ЭТАН КАК ПРОМЕЖУТОЧНЫЙ ПРОДУКТ В СИНТЕЗЕ 1,2-БИС-(1-ГЛИЦИДИЛБЕНЗИМИДАЗОЛ-2-ИЛТИО)ЭТАНА В КАЧЕСТВЕ СООТВЕРДИТЕЛЯ ЭПОКСИДНЫХ СМОЛ | 1990 |
|
SU1743160A1 |
| Способ получения 4-хлор-5-карбоэтоксиметоксибензо-2,1,3-тиадиазола | 1981 |
|
SU940473A1 |
| ХЛОРАНГИДРИД 3,4-ДИЦИАНО - 4′- -КАРБОКСИДИФЕНИЛОКСИДА В КАЧЕСТВЕ ПОЛУПРОДУКТА ДЛЯ СИНТЕЗА ТЕТРАНИТРИЛОВ АРОМАТИЧЕСКИХ ТЕТРАКАРБОНОВЫХ КИСЛОТ, ТЕТРАНИТРИЛЫ АРОМАТИЧЕСКИХ ТЕТРАКАРБОНОВЫХ КИСЛОТ КАК МОНОМЕРЫ ДЛЯ СИНТЕЗА ПОЛИГЕКСАЗОЦИКЛАНОВ И ПОЛИГЕКСАЗОЦИКЛАНЫ КАК МАТЕРИАЛЫ ДЛЯ ЭЛЕКТРОПРОВОДЯЩИХ ПОКРЫТИЙ | 1981 |
|
SU1045566A1 |
| ПРОИЗВОДНЫЕ ЗАМЕЩЕННОГО 5-БЕНЗИЛОМ БЕНЗИМИДАЗОЛИН-2-ТИОНА, СПОСОБ ИХ ПОЛУЧЕНИЯ И АНТИГИПЕРЛИПОПРОТЕИНЕМИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 1991 |
|
RU2043343C1 |
| Способ получения эфиров @ -(2-аминобензгидрил)- @ -, @ -, @ -аминокислот и дипептидов | 1981 |
|
SU1010057A1 |
| 1-(1,2,4-Триазолил-4-аминометилен)-бензазолтионы-2 в качестве стабилизаторов негативных галогенсеребряных фотографических материалов | 1989 |
|
SU1671663A1 |
| Способ получения аренселеноновых кислот | 1985 |
|
SU1293176A1 |
Использование: бензимидазолхалькогеноны-2 формулы C6H4NH = x-NH (1), x = Se, S могут найти применение в качестве стабилизаторов полимеров, компонентов фотокомпозиций, ускорителей вулканизации каучуков. Сущность изобретения: реагент 1-о-фенилендиамин, реагент 2 - селен или сера. Условия реакции: двухфазная система: хлороформ - водная концентрированная щелочь, 50 - 65oC. Предпочтительно дополнительно можно вводить не менее 3 мол.% четвертичных аммониевых солей. 1a, X = Se, т.пл. 235oC (с разлож. из этанола), порошок желтого цвета, Rf 0,52. Выход 18 - 48%, 1 б.Х = S, т.пл. 298 - 300oC (из этанола) Rf 0,52. Выход 45 - 75%. 1 з.п. ф-лы.

а) Х Se,
б) X S,
путем конденсации о-фенилендиамина с халькогенсодержащим соединением при повышенной температуре, отличающийся тем, что, с целью улучшения экологии и упрощения процесса, в качестве халькогенсодержащих соединений берут селен или серу и процесс ведут в присутствии хлороформа и водной концентрированной щелочи при 50 65oС.
| Kym.J.Prart chem | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Ber | |||
| Аппарат для электролиза воды | 1924 |
|
SU1912A1 |
| Способ образования коричневых окрасок на волокне из кашу кубической и подобных производных кашевого ряда | 1922 |
|
SU32A1 |
| Frerichs, Hup Ka, Archiv pharmacie, 1903, 241,5, 165 | |||
| Способ получения молочной кислоты | 1922 |
|
SU60A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Приспособление для установки двигателя в топках с получающими возвратно-поступательное перемещение колосниками | 1917 |
|
SU1985A1 |
| Warner | |||
| J.S, J | |||
| org | |||
| Chem, 1963, v | |||
| Видоизменение прибора с двумя приемами для рассматривания проекционные увеличенных и удаленных от зрителя стереограмм | 1919 |
|
SU28A1 |
| Тиражная машина | 1924 |
|
SU1642A1 |
Авторы
Даты
1997-06-10—Публикация
1991-04-15—Подача